OBJETIVOS
La lectura de este artículo la capacitará para:
1. Descubrir la fisipatología y las causas de la IRA.
2. Identificar los hallazgos de la valoración de los pacientes con IRA.
3. Conocer los objetivos del tratamiento y las actividades de enfermería para los pacientes con IRA.
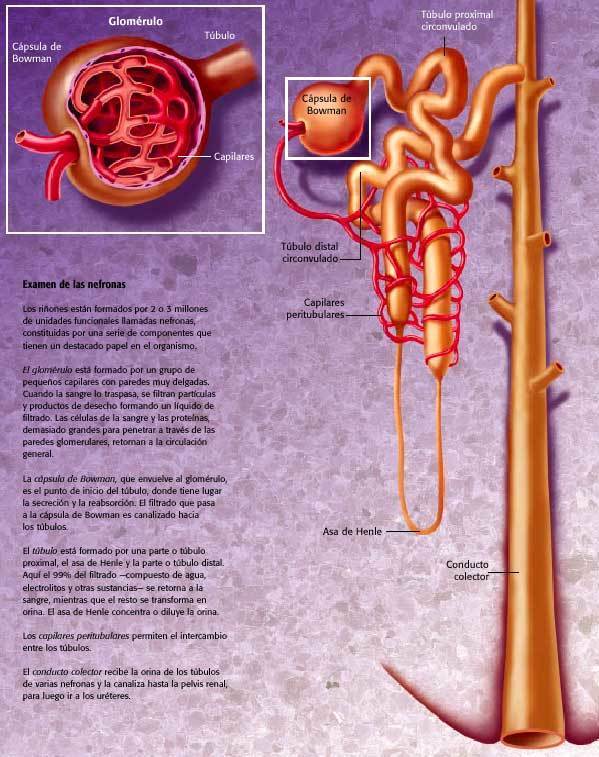
LA INSUFICIENCIA RENAL aguda (IRA) implica una pérdida brusca de la función renal, con liberación de productos de desecho tóxicos, como la urea y la creatinina, a la sangre. A diferencia de la insuficiencia renal crónica, en la que de un 90 a un 95% de nefronas dejan de funcionar de forma permanente paulatinamente, la IRA se produce cuando los riñones se colapsan de forma brusca, provocando la pérdida de la funcionalidad en un 50% o más de nefronas de forma tan rápida que el organismo es incapaz de compensarlo. (Para conocer las funciones más importantes, véase el anexo Explorar las nefronas.)
Si se corrige la causa subyacente, estas nefronas pueden recuperarse, pero en algunos casos la lesión se hace permanente, convirtiéndose en una insuficiencia renal crónica.
Aunque la IRA afecta con mayor frecuencia a las personas ancianas, la evolución y los índices de supervivencia son similares en todas las edades. Afecta a un 5% de pacientes hospitalizados y puede llegar a ocasionar complicaciones graves e incluso la muerte del enfermo, generalmente por una infección sobreañadida o por problemas cardiopulmonares.
Con la lectura de este artículo descubrirá más aspectos de la IRA, su evolución y cómo contribuir a la recuperación del enfermo.
Ratio de filtrado glomerular, la clave de la función renal
El ratio de filtrado glomerular (RFG) es la cantidad de sangre que se filtra a través de los glomérulos de los riñones. Es la fuerza de conducción de la producción de orina. Normalmente de 120 a 125 ml/min, el RFG disminuye cuando ocurre un problema renal. El incremento de las concentraciones de urea nitrogenada en sangre y creatinina son indicadores directos de la reducción del RFG.
Muchas causas, muchos efectos
Aunque la IRA tiene múltiples causas, la isquemia y la toxicidad son las más habituales. Dependiendo de dónde se origine el problema, la IRA puede clasificarse en prerrenal, intrarrenal o posrenal.
IRA prerrenal. También denominada azotemia prerrenal, es la forma más común. Se produce cuando la disminución del aporte de sangre al riñón causa isquemia de las nefronas. Las causas principales son pérdidas de sangre, deshidratación grave, septicemia o shock cardiogénico. Por suerte, el restablecimiento de la circulación sanguínea renal y de la ultrafiltración glomerular pueden revertir rápidamente una IRA prerrenal.
Otra causa importante de IRA prerrenal es el uso de antiinflamatorios no esteroideos, inhibidores de la ciclooxigenasa o inhibidores de la enzima conversiva de la angiotensina). Estos medicamentos pueden alterar las respuestas de autorregulación renal al bloquear la producción de prostaglandinas, necesarias para mantener la perfusión renal. El riesgo de problemas relacionados con el tratamiento con estos fármacos es más elevado en enfermos ancianos con insuficiencia renal, insuficiencia cardíaca o hepatopatía avanzada.
IRA intrarrenal. También denominada IRA intrínseca, se asocia con una lesión del parénquima renal. La IRA prerrenal puede desencadenar este problema, pero la causa principal de esta afección, así como de la IRA en general, es la necrosis tubular aguda (NTA), es decir, la lesión de los túbulos renales por isquemia o toxicidad. Aunque los términos IRA y NTA se utilizan a menudo como sinónimos, no significan lo mismo. Así, entre un 20 y un 30% de los pacientes con IRA por isquemia o nefrotoxicidad no presentan evidencias de necrosis tubular.
Las enfermedades que afectan a los grandes vasos renales, como la estenosis de la arteria renal, y de los pequeños vasos y glomérulos, como en la glomerulonefritis, son las principales causas isquémicas de IRA intrarrenal. Las sustancias nefrotóxicas que pueden desencadenar IRA intrarrenal incluyen los medios de contraste radiológicos, la ciclosporina, los antibióticos (especialmente los aminoglucósidos) y la quimioterapia. Otros agentes nefrotóxicos incluyen los metales pesados como el mercurio o el arsénico.
IRA posrenal. Se produce como resultado de un proceso obstructivo del flujo urinario, provocando su retorno hacia el riñón. La hipertrofia prostática, la obstrucción ureteral (habitualmente bilateral) y la obstrucción del conducto vesical son las causas principales.
Efectos multisistémicos
El cuidado de un enfermo con IRA es un reto. El trastorno renal suele afectar a diferentes sistemas orgánicos, por lo que se deberán abordar signos y síntomas de enfermedad renal, pero también problemas de otros órganos y sistemas. A continuación se expone un resumen de los criterios de valoración organizados por sistemas.
Renal. El efecto renal más importante de la IRA es la disminución de la diuresis que causa retención de líquidos y edema. El signo clásico, la oligiria (menos de 400 ml de diuresis en 24 h), indica que el riñón no está produciendo suficiente orina para excretar los productos de desecho.
De todos modos, algunos pacientes presentan una IRA no oligúrica (generalmente en los casos de azotemia prerrenal y en contadas ocasiones en la IRA intrarenal). En estos casos, las concentraciones de urea nitrogenada (BUN) y creatinina en sangre se incrementan, y la diuresis es variable. El restablecimiento del volumen intravascular, así como el mantenimiento del gasto cardíaco y de la presión arterial suelen detener la progresión de la IRA no oligúrica, por lo que la terapéutica sustituroria renal con hemodiálisis o hemofiltración arteriovenosa continua no es necesaria. (Para conocer más a fondo estas opciones terapéuticas véase el anexo Pros y contras de la terapéutica sustitutiva renal.)
La incapacidad renal para eliminar los productos de desecho de la sangre causa un incremento de las concentraciones de toxinas, como
la urea y la creatinina. Puesto que muchos procesos, como el metabolismo proteico, una hemorragia interna o una infección, aumentan las concentraciones de BUN, se considera que este es un indicador de función renal menos fiable que la creatinina, que es un producto intermedio del metabolismo muscular. De todos modos, hay que recordar que si existe una disminución de la masa muscular, como en el caso de los enfermos delgados o frágiles, la producción y los valores de creatinina pueden mantenerse dentro de la normalidad incluso cuando existe una alteración de la función renal. Por ello, las variaciones de las concentraciones de creatinina son mejores indicadores de la función renal.
Otros valores de laboratorio cuya anormalidad puede sugerir IRA incluyen la acidosis metabólica y los trastornos electrolíticos, como la hiponatremia, la hipercaliemia, la hiperfosfatemia, la hipocalcemia y la hipermagnesemia.
Cardiovascular. La hipertensión, el edema pulmonar, el edema periférico y las arritmias son los principales efectos cardiovasculares de la IRA. Puesto que la disminución de la diuresis causa una retención de líquidos, el paciente desarrolla hipertensión. Si el corazón no puede bombear el volumen adicional, se produce una insuficiencia cardíaca. La sobreproducción de renina también contribuye a la hipertensión.
El edema resultante del exceso de líquidos pasa de los vasos al espacio intersticial o a los tejidos. Puesto que la albúmina sérica es esencial para garantizar el paso de agua y solutos a través de los capilares y prevenir su paso al espacio intersticial, unas concentraciones de albúmina sérica bajas causarían edema.
La hiperpotasemia aparece cuando el riñón es incapaz de excretar el exceso de potasio. Controle atentamente la aparición de signos y síntomas, como debilidad muscular, pérdida de tono muscular e irritabilidad neuromuscular, incluyendo temblor labial o digital. Las alteraciones electrocardiográficas, como una onda P plana, una prolongación del complejo QRS o la presencia de ondas T elevadas, también son signos de hipercaliemia. De todos modos, es bastante habitual que ésta no provoque sintomatología, por lo que es imperativo el control de las concentraciones de potasio en sangre, ya que unas concentraciones superiores a 6 mEq/l podrían desencadenar bradicardia, bloqueo cardíaco, asistolia u otras arritmias.
Respiratorio. Si el exceso de líquidos continúa, el paciente puede empezar a presentar disnea, lo que indica que existe edema pulmonar. Valore la presencia de disnea de reposo o en ejercicio y ausculte los pulmones para descartar estertores.
Neurológico. La acumulación de productos de desecho metabólicos puede afectar el estado mental del paciente. Valore cambios en el nivel de conciencia que pudieran evolucionar hasta el coma. Los cambios sensoriales y la debilidad en las extremidades son indicadores de neuropatía urémica.
Hematológico. La anemia es el principal efecto hematológico de la IRA. Los factores contribuyentes incluyen un trastorno en la producción de hematíes, hemólisis, hemorragia, hemodilución y una disminución de la supervivencia de los hematíes. La vida media normal de los hematíes --alrededor de 120 días en caso de IRA-- se reduce a unos 60. Y puesto que los riñones dañados producen cada vez menos cantidad de eritropoyetina que estimule la producción de hematíes no hay una reposición suficiente de estas células. Controle la disminución de la concentración de hemoglobina y hematocrito, así como la presencia de disnea asociada con una oxigenación insuficiente.
Gastrointestinal (GI). La uremia causa anorexia, náuseas y vómitos, que conducen a desnutrición y a una pérdida de masa muscular. Puesto que la uremia puede desencadenar colitis y úlceras gástricas, el paciente tiene riesgo de hemorragia GI. Además, su aliento puede adquirir un olor de orina insoportable a causa del incremento de la urea.
Para confirmar el diagnóstico de IRA, el médico llevará a cabo una valoración completa y un examen físico, así como pruebas de sangre
y orina, y probablemente una ecografía renal. Si las pruebas confirman la IRA, prepárese para actuar rápidamente con el fin de prevenir una lesión renal permanente.
Eliminar la causa
En la mayoría de casos de IRA, la función renal vuelve a la normalidad en cuestión de semanas. Los objetivos terapéuticos persiguen eliminar la causa de la IRA y proporcionar el soporte necesario a la función renal y al resto de sistemas orgánicos afectados, lo que implica el restablecimiento del aporte de sangre renal en la IRA prerrenal, el tratamiento de la enfermedad renal intrínseca, como la glomerulonefritis aguda, o la eliminación de la obstrucción posrenal. Con independencia del tipo de IRA que afecte al paciente, deberá proporcionarle los siguientes cuidados de soporte:
Mantener el balance hidroelectrolítico. La valoración exacta del balance hídrico es fundamental, por lo que es necesario controlar estrictamente el peso del paciente así como los aportes y pérdidas. Asegúrese de incluir la cantidad de vómito o heces líquidas en la determinación de las pérdidas.
Valore la presencia de edema, generalmente en las piernas y los pies si está sentado y en la región sacra si está en decúbito supino, pero que también puede aparecer alrededor de los ojos. Registre el color y las características de la orina.
El paciente con IRA tiene un mayor riesgo de hipercaliemia, hiponatremia y sobrecarga de líquidos, por lo que debe controlarse estrictamente el equilibrio de líquidos y electrolitos. Una combinación de diuréticos puede contribuir a eliminar su exceso.
Eliminar los productos de metabolismo nitrogenado. Controle las concentraciones de BUN y creatinina. Si la IRA evoluciona hasta tal punto que los productos de desecho se acumulan en el organismo, puede ser necesario iniciar el tratamiento sustitutivo renal con hemodiálisis o hemofiltración arteriovenosa para eliminarlos.
Recuerde que el enfermo precisará una fístula arteriovenosa para la hemodiálisis e intente limitar el acceso venoso periférico a la parte dorsal de las manos para preservar las venas cefálicas. Si ya dispone de un acceso vascular para diálisis resérvelo estrictamente para este propósito; su empleo con otros fines terapéuticos podría amenazar su funcionamiento y su permeabilidad. (Véase, en la sección "Lo que debe y no debe hacer", "Protección de una fístula de hemodiálisis" en el número de mayo de NURSING 2003).
Soporte nutricional. Es vital para combatir la desnutrición y los trastornos hidroelectrolíticos, ya que la desnutrición caloricoproteica es muy prevalente en pacientes con IRA. El catabolismo por el estrés asociado con enfermedad crítica es proporcional a la gravedad de la insuficiencia renal. Cuando un paciente está en un estado hipercatabólico, el organismo destruye la masa muscular en busca de proteínas, causando
un incremento adicional de las concentraciones de BUN y creatinina.
Para evitar una mayor carga proteica a escala renal, el soporte nutricional debería encaminarse a proporcionar la cantidad necesaria de calorías sin aumentar la carga proteica. La dieta recomendada debe ser baja en proteínas y sodio, y rica en grasas e hidratos de carbono. Administre la alimentación por vía oral si el tracto digestivo sigue funcionando; en caso contrario, utilice la vía parenteral.
Generalmente las restricciones dietéticas incluyen de 2 a 4 g/día de sodio para evitar una mayor retención de líquidos, una disminución del aporte de potasio para reducir el riesgo de arritmias cardíacas y una limitación del aporte de fósforo posiblemente mediante el uso de fórmulas de unión durante las comidas para evitar una disminución de las concentraciones del ión calcio en sangre. El volumen de líquidos debe restringirse a la diuresis más 500 a 700 ml.
Proporcione apoyo emocional y eduque al enfermo. Tanto para el paciente como para la familia, la IRA es un acontecimiento brusco, inesperado y traumático. Apóyelos emocionalmente y proporcione la educación sanitaria sobre la medicación, las necesidades nutricionales, la restricción de líquidos y la función de la diálisis.
Si todo va bien, el paciente se recuperará en los siguientes 3 a 12 meses. Pero si la causa de la IRA no puede corregirse y persiste la lesión de la nefrona, éste desarrollará una insuficiencia renal crónica que precisará diálisis de mantenimiento o trasplante renal.
Comprender el proceso
Ahora que ya comprende cómo la IRA afecta a tantos procesos fisiológicos, puede iniciar los pasos necesarios para apoyar la recuperación del paciente y enseñarle lo que necesita saber para afrontar este problema.
Diana Campbell es enfermera especializada en cuidados renales del Vancouver Island Health Authority Renal Program en British Columbia, Canadá.
WEB SELECCIONADAS
American Academy of Family Physicians: Acute Renal Failure
http://www.aafp.org/afp/20000401/2077.html
MedLine Plus Health Information: Acute Renal Failure
http://www.nlm.nih.gov/medlineplus/ency/article/000501.htm
BIBLIOGRAFÍA SELECCIONADA
Agrawal, M., and Swartz, R.: "Acute Renal Failure," American Family Physician. 61(7):2077-2088, April 1, 2000.
Braunwald, E., et al. (eds): Harrison's Principles of Internal Medicine, 15th edition. New York, N.Y., McGraw-Hill, 2001.
Dirkes, S.: "Continuous Renal Replacement Therapy: Dialytic Therapy for Acute Renal Failure in Intensive Care", Nephrology Nursing Journal. 27(6):581-592, December 2000.
Hynes-Gay, P., and Rankin, J.: "Continuous Renal Replacement Therapy: An Overview," Dynamics. 11(3):26-30, Fall 2000.
Kumar, S., and Berl, T.: "NSAID-induced Renal Toxicity: When to Suspect, What to Do", Consultant. 39(1):195-202, January 1999.
Solomon, R.: "Managing Acute Renal Failure: Do Vasodilators and Diuretics Have a Role?" Journal of Critical Illness. 13(11):709-714, November 1998.