El manejo de la información mediante soportes digitales permite abordajes innovadores de la identificación de los casos de demencia mediante búsquedas automatizadas en las bases de datos clínicas con sistemas de codificación de los diagnósticos. El objetivo de este trabajo fue analizar la validez de un registro de demencia en Gipuzkoa basado en los sistemas de registro administrativos y clínicos existentes en el Servicio Vasco de Salud.
MétodosEs un estudio descriptivo basado en la evaluación de las fuentes de datos disponibles. Primero, mediante revisión de historias clínicas se evaluó la validez diagnóstica en 2 muestras de casos identificados y no identificados como demencia. Se midió la sensibilidad, especificidad y valor predictivo positivo y negativo del diagnóstico de demencia. Posteriormente se buscaron los casos de demencia vivos a fecha 31 de diciembre de 2016 en toda la población guipuzcoana y se recogieron variables sociodemográficas y clínicas.
ResultadosLas 2 muestras de validación incluyeron 986 casos y 327 no casos. La sensibilidad calculada fue del 80,2% y la especificidad del 99,9%. El valor predictivo negativo fue del 99,4% y el positivo del 95,1%. Los casos registrados en toda la población guipuzcoana fueron 10.551 que supone un 65% de los casos previstos según la literatura. Un 40% tomaban medicación antisicótica. La población institucionalizada fue del 25%.
ConclusionesUn registro de demencias basado en las bases de datos clínicas y administrativas es válido y factible. Su principal aportación es mostrar la dimensión que tiene la demencia en el ámbito del sistema sanitario.
The handling of information through digital media allows innovative approaches for identifying cases of dementia through computerized searches within the clinical databases that include systems for coding diagnoses. The aim of this study was to analyze the validity of a dementia registry in Gipuzkoa based on the administrative and clinical databases existing in the Basque Health Service.
MethodsThis is a descriptive study based on the evaluation of available data sources. First, through review of medical records, the diagnostic validity was evaluated in 2 samples of cases identified and not identified as dementia. The sensitivity, specificity and positive and negative predictive value of the diagnosis of dementia were measured. Subsequently, the cases of living dementia in December 31, 2016 were searched in the entire Gipuzkoa population to collect sociodemographic and clinical variables.
ResultsThe validation samples included 986 cases and 327 no cases. The calculated sensitivity was 80.2% and the specificity was 99.9%. The negative predictive value was 99.4% and positive value was 95.1%. The cases in Gipuzkoa were 10,551, representing 65% of the cases predicted according to the literature. Antipsychotic medication were taken by a 40% and a 25% of the cases were institutionalized.
ConclusionsA registry of dementias based on clinical and administrative databases is valid and feasible. Its main contribution is to show the dimension of dementia in the health system.
La demencia plantea uno de los mayores retos de salud pública debido al rápido envejecimiento de la población. Es una de las causas principales de discapacidad, pérdida de calidad de vida e institucionalización1,2. La información de la que se dispone sobre esta enfermedad está basada principalmente en estudios transversales y de cohortes que han aportado información sobre su evolución a nivel cognitivo, factores de riesgo o mortalidad y han permitido conocer su prevalencia e incidencia3–5. Sin embargo, los expertos han indicado que la información sobre la demencia está dispersa y poco accesible y que en parte por esta razón se le presta una inadecuada atención6. En otros procesos relacionados con el envejecimiento como el ictus o las fracturas de cadera, las bases de datos asociadas a los ingresos hospitalarios (Conjunto Mínimo Básico de Datos) han permitido conocer su incidencia y el uso de recursos asociado a su atención sanitaria7,8. Por el contrario, dado el manejo clínico ambulatorio de las demencias, la información que aporta el Conjunto Mínimo Básico de Datos es muy limitada y no permite medir el impacto sobre el sistema sanitario en términos de utilización de recursos9,10. En las enfermedades neurológicas causantes de discapacidad se requiere además conocer la prevalencia, ya que representa la frecuencia de una determinada enfermedad en la población estudiada en un momento determinado y determina la carga sanitaria y social de la enfermedad11.
La planificación de los recursos necesarios para responder a las necesidades de los pacientes con demencia a corto, medio y largo plazo requiere de sistemas de información dinámicos que permitan monitorizar el impacto del envejecimiento en términos de incidencia y prevalencia10. Los registros poblacionales de enfermedades constituyen un modelo de sistema de información dinámico ya que permiten obtener datos reales acerca de la incidencia de la enfermedad de interés, realizar estudios epidemiológicos y contribuir eficazmente a la planificación de los recursos necesarios para su atención12. Existen diferentes tipos de registros de demencias a nivel internacional, pero no todos son poblacionales12. Por un lado, existen registros constituidos por la integración de diferentes cohortes para aumentar el tamaño muestral y con fines fundamentalmente de investigación, como el registro CERAD13. Por otro, están los basados en la notificación activa por parte del neurólogo y búsqueda de la información en la historia clínica, como el Registro de Girona14,15. Por último, están los registros de ámbito poblacional basados en la explotación automatizada y exhaustiva de las bases de datos disponibles y su integración en un único registro. Su mayor exponente es el de South Carolina, que contiene 225.938 casos desde 199816. En el contexto español, la experiencia de referencia es el Registro de Girona14,15, pero su generalización se ha visto limitada por la dificultad de disponer de los recursos suficientes para llevar a cabo un registro basado en la búsqueda individual en la historia clínica.
El manejo de la información mediante soportes digitales permite actualmente nuevos abordajes mediante la identificación de los casos de demencia llevando a cabo búsquedas automatizadas en las bases de datos clínicas con sistemas de codificación de los diagnósticos17,18. Uno de los problemas planteados por esa vía de acceso a la información es la validación de los diagnósticos obtenidos19–21. Los resultados han sido diferentes dependiendo de la fuente de los casos y del sistema de validación. Si se documenta que los sistemas automatizados aportan información válida se abrirá la puerta a registros de demencias que no estén limitados por el volumen de pacientes. La falta de procedimientos de codificación de los diagnósticos de las consultas externas hospitalarias ha impedido la aplicación de un diseño automatizado de demencias. En el Servicio Vasco de Salud se puso en marcha en 2013 una nueva versión de la historia clínica electrónica que requería que el médico asignase un diagnóstico codificado para la apertura de los episodios de consultas externas hospitalarias. Su extensión al conjunto de hospitales del País Vasco abre la puerta a la implantación de un registro de demencias automatizado de tipo poblacional que incluya todas las bases de datos sanitarias (Atención Primaria, Atención Hospitalaria y Farmacia).
El objetivo principal de este trabajo fue analizar la validez de un registro de demencia en Gipuzkoa basado en los sistemas de registro administrativos y clínicos existentes en el Servicio Vasco de Salud. Como objetivo secundario se pretendió mostrar la capacidad del registro para describir el perfil clínico y sociodemográfico de los casos identificados.
Pacientes y métodosEs un estudio descriptivo basado en la evaluación de las fuentes de datos disponibles y su validez diagnóstica. El protocolo del estudio fue aprobado por el CEIC de Euskadi con el número de registro EPA2016069.
El estudio se desarrolló en varias fases. En el año 2014 se llevó a cabo una revisión bibliográfica sobre registros de demencias y de enfermedad de Alzheimer en diferentes países. En nuestro país, se identificó el Registro de Girona14,15 como referente y se exploró la posibilidad de implantar dicho modelo en Gipuzkoa. A continuación, se describió el «circuito» que siguen los pacientes con deterioro cognitivo y demencia en Gipuzkoa. Se identificó la consulta externa de neurología como el punto clave del sistema de información puesto que es donde se lleva a cabo el diagnóstico de demencia. Además, se constató que los evolutivos de consultas externas de neurología contenían la información necesaria para poder identificar a los casos, ya que los diagnósticos de demencia y deterioro cognitivo estaban registrados. A pesar de ello, la historia clínica electrónica (Osabide Global) no estaba totalmente desplegada y aún se mantenía la historia clínica en papel en algunos hospitales. En Osabide Global, la apertura de un episodio de consulta externa implica que el especialista tiene que asignar un diagnóstico que se codifica automáticamente en la CIE-9. Esto permite identificar a posteriori los casos de demencia en la base de datos de episodios de consulta externa. Sin embargo, en aquel momento la información de consultas externas no estaba disponible en la base de datos corporativa de Osakidetza Oracle Business Intelligence (OBI). Todo ello dificultaba el desarrollo de un registro basado en un diseño automatizado. Sin embargo, 2 avances en la digitalización de la información modificaron favorablemente la situación. Primero, la implantación completa de Osabide Global con la desaparición de la historia clínica en papel en los años 2014-2015. Segundo, los datos de consultas externas se incorporaron a OBI en 2015. Estos nuevos desarrollos tecnológicos abrían de nuevo la posibilidad de poner en marcha un registro de demencias y de otros trastornos cognitivos. Por último, se evaluó la validez de un registro de demencia mediante el análisis de las bases de datos administrativas y clínicas de Osakidetza.
Validación de los diagnósticosEl estudio de validación de los diagnósticos de demencia y deterioro cognitivo se llevó a cabo en la población atendida por la Organización Sanitaria Integrada Bajo Deba, que incluye un hospital y los centros de salud correspondientes a una población de 72.751 habitantes. El objetivo era medir la fiabilidad diagnóstica de los casos de demencia según la fuente de identificación. Se partió de la población de Bajo Deba con 50 años o más, que contenía 38.952 individuos vivos a 6 de octubre del 2016. En este grupo de edad se hicieron diferentes búsquedas en la base de datos OBI con los códigos de los diagnósticos de demencia en CIE9 (290xx; 331.0, 331.1, 331.2, 331.82) y CIE10 (F03.5x; F03.8x; F03.9x; G30.0x; G30.1x; G30.8x; G30.9x; G31.0x; G31.1x; G31.2x; G31.8x; G31.9x). La CIE 10 se incorporó a las búsquedas porque desde el 1 de enero de 2016 es la CIE oficial. OBI es una base de datos anonimizada en donde cada individuo tiene un identificador específico para esta base de datos que no permite relacionarlo directamente con sus datos personales. Las búsquedas fueron realizadas en las siguientes fuentes de información: atención primaria (AP), consulta externa de neurología, hospitalización y prescripción de medicamentos específicos para enfermedad de Alzheimer o grupo ATC N06D (donepezilo, rivastigmina y galantamina). Todos ellos requieren ser prescritos por un especialista (neurólogo, geriatra o psiquiatra) y que los servicios de inspección médica autoricen su dispensación con cargo al sistema público de salud.
También se identificó si esos pacientes tenían episodio de consulta de neurología. Dado que el criterio de validación fue que el neurólogo hubiese registrado en la historia clínica el diagnóstico, solamente podían ser validados aquellos casos que tenían algún episodio de consulta de neurología. Algunos de los casos con episodio tenían el diagnóstico de demencia pero otros eran anteriores a la implantación de la historia digital de Osabide Global y por ello no tenían posibilidad de codificación automática del episodio. Esto nos permitió validar los casos basados en prescripción de medicamentos y de AP y hospitalización sin diagnóstico de consulta externa. Se acordó con los neurólogos del estudio que el criterio del neurólogo, geriatra o psiquiatra identificando el diagnóstico permitía etiquetar el caso de demencia como confirmado. Si solamente estaba disponible el diagnóstico en AP o en hospitalización se asignaba la categoría de caso probable. Se utilizaron para la validación todos los casos con algún diagnóstico codificado de demencia (AP, hospital o consultas externas) y un episodio en consulta externa de neurología. También se revisó una muestra aleatoria de 327 individuos mayores de 60 años sin diagnóstico en ninguna base de datos.
Se decidió considerar como caso confirmado de demencia cuando en el episodio de consultas externas de neurología se indicaba, bien en el juicio diagnóstico, bien en el evolutivo, la presencia de los siguientes términos: demencia; demencia a estudio, EA, E.A., Alzheimer, cuerpos Lewy, DC Lewy, DFT, demencia frontotemporal, demencia vascular y demencia senil. Se formó a una persona con experiencia previa en revisión de historias clínicas para buscar en la documentación de la historia de consulta externa los términos asociados a los diagnósticos.
Con los resultados de las 2 muestras se calcularon los valores predictivos positivo y negativo. La validación de los casos se realizó en el total de la población. Sin embargo, únicamente se validó una muestra aleatoria de los no casos. Los intervalos de confianza de la muestra de no casos se realizó mediante bootstrapping22. Se simularon 1000 muestras con remplazo y se calcularon los percentiles 2,5 y 97,5. Para el cálculo de la sensibilidad y especificidad del registro en la población mayor de 50 años en la comarca Bajo Deba, se aplicó el valor predictivo negativo al total de la población de no casos con el objetivo de estimar el número de casos no detectados en el total de la población.
Búsqueda de casos en la población guipuzcoanaPosteriormente se llevó a cabo una búsqueda en las bases de datos de toda la población guipuzcoana para identificar todos los casos que cumplían con los criterios de demencia. Estas búsquedas fueron anonimizadas ya que no se utilizó para el registro ningún dato de filiación de los casos sino el identificador de OBI que es específico de esta base de datos.
Como muestra de la capacidad de la base de datos se extrajeron de todos los pacientes identificados las siguientes variables demográficas (edad y género), clínicas (fecha del diagnóstico de demencia, diagnóstico de demencia y enfermedades concomitantes: hipertensión arterial, diabetes, enfermedad de Parkinson, ictus, enfermedad cardiovascular, traumatismo craneoencefálico, trastorno depresivo y síndrome de Down), los medicamentos prescritos (anticolinesterásicos, memantina, antidepresivos, antipsicóticos, ansiolíticos, hipnóticos) y situación de institucionalización. El listado de códigos de la CIE-9 y CIE-10 aplicados para la búsqueda de las comorbilidades se muestra en el apéndice.
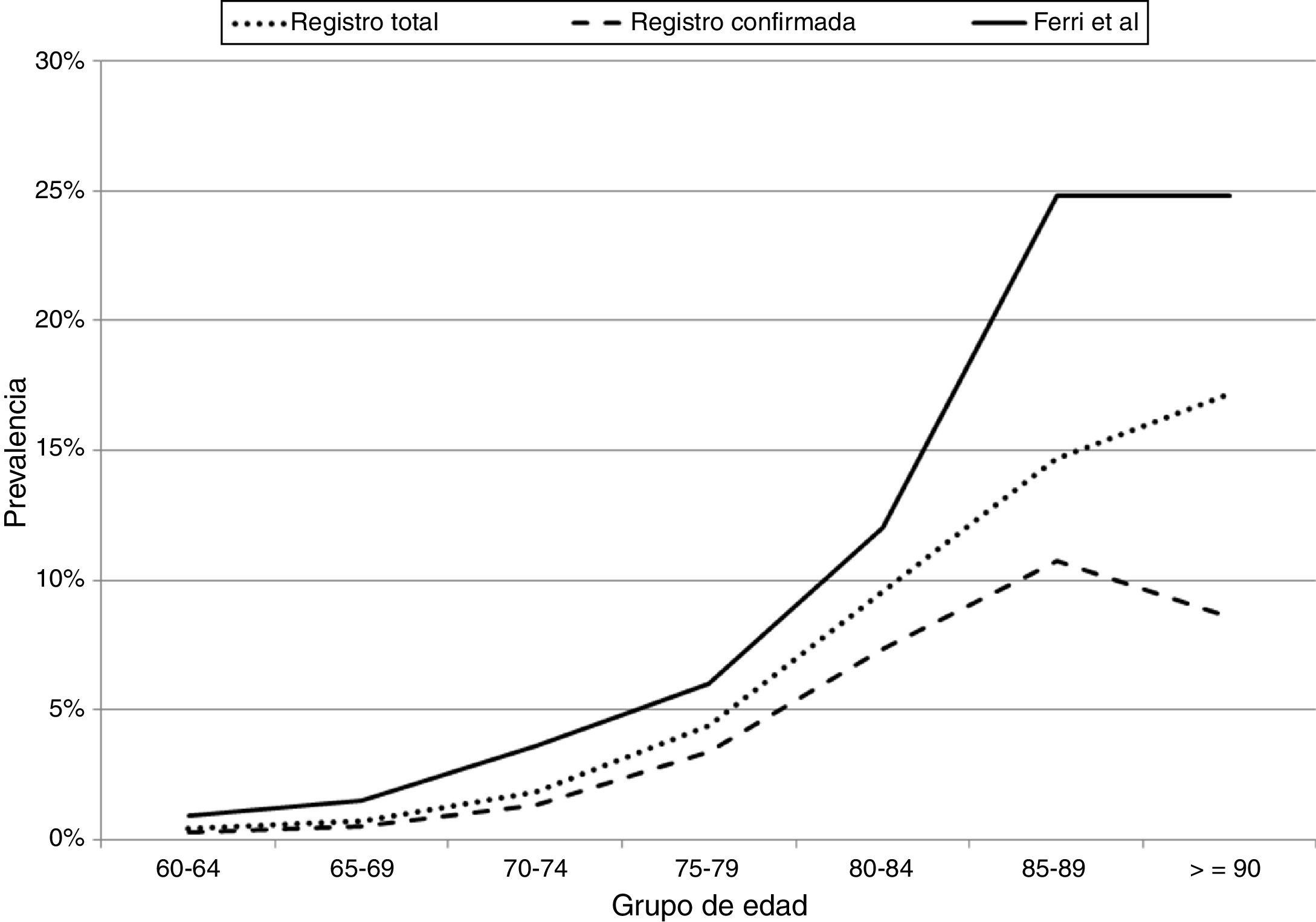
Para valorar el nivel de cobertura diagnóstica del registro se compararon las tasas poblacionales de casos totales y confirmados con las cifras del estudio de Ferri et al.23.
ResultadosLos casos incluidos en el estudio de validación de los diagnósticos de las bases de datos de AP, hospitalización, consulta externa y prescripción de medicamentos específicos se muestran en la tabla 1. El estudio de validación se presenta en la tabla 2 e incluyó 986 casos y 327 no casos. El porcentaje de diagnósticos válidos de demencia (valor predictivo positivo) fue del 95,1% en total y del 96,9% en los casos identificados en consulta externa y en los que tenían prescrita alguna medicación del grupo específico para enfermedad de Alzheimer. Cuando solamente se encontraba el diagnóstico en AP y/u hospitalización los casos confirmados bajaron al 91,7%. En los 327 no casos se encontraron 2 casos de demencia lo que determinó un valor predictivo negativo del 99,4%. El cálculo de los intervalos de confianza mediante bootstrapping dio como resultado un 1,52% y un 0% de error en la muestra de no casos. Al proyectarse al conjunto de la población no identificada como demencia en Bajo Deba supuso 232 casos (intervalos de confianza 95%: 69-396). La sensibilidad calculada fue del 80,2% y la especificidad del 99,9% (tabla 3).
Casos identificados según fuente de información del diagnóstico en Bajo Deba
| Población total mayor de 50 años en Bajo Deba | 38.952 | 100% |
| Sin diagnóstico | 37.771 | 970% |
| Con diagnóstico o medicación | 1.181 | 3% |
| Diagnóstico en CCEE | 317 | 0,8% |
| Diagnóstico en CCEE, hospital o AP | 970 | 2,5% |
| Medicación Grupo ATC N06D | 498 | 1,3% |
| Pacientes con diagnóstico (CCEE, hospital o AP) o medicación y episodio de Neurología | 986 | 2,5% |
AP: atención primaria; ATC: Anatomical, Therapeutic, Chemical classification system; CCEE: consultas externas.
Resultados de la validación de la muestra de casos y no casos y de la extrapolación de la muestra de no casos de demencia
| Casos validados | Casos | No confirmado | Error (%) |
|---|---|---|---|
| Total | 986 | 48 | 4,9 |
| Con diagnóstico en CCEE | 457 | 14 | 3,1 |
| Sin diagnóstico en CCEE | 529 | 34 | 6,4 |
| Con diagnóstico en AP u Hospitalización | 348 | 29 | 8,3 |
| Sin diagnóstico en AP u hospitalización (único diagnóstico en Farmacia) | 181 | 5 | 2,8 |
| No casos validados | No casos | No confirmado | Error |
|---|---|---|---|
| Muestra | 327 | 2 | 0,6 |
| Proyección poblacional media | 37.966 | 232 | 0,6a |
AP: atención primaria; CCEE: consultas externas; IC: intervalo de confianza.
Sensibilidad y especificidad de la búsqueda automatizada de demencia en las bases de datos clínicas
| Clasificación de la población | Caso confirmado | No caso confirmado | Total |
|---|---|---|---|
| No caso en registro | 232 | 37.734 | 37.966 |
| Caso en registro | 938 | 48 | 986 |
| Total | 1.170 | 37.782 | 38.952 |
| Media | IC inferior 95% | IC superior 95% | |
|---|---|---|---|
| Sensibilidad | 80,16% | 61,77% | 100% |
| Especificidad | 99,87% | 99,87% | 99,87% |
| Valor predictivo positivo | 95,13% | 95,13% | 95,13% |
| Valor predictivo negativo | 99,39% | 98,47% | 100% |
IC: intervalo de confianza.
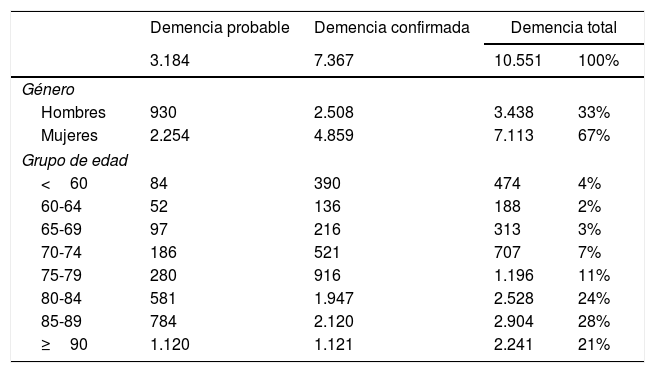
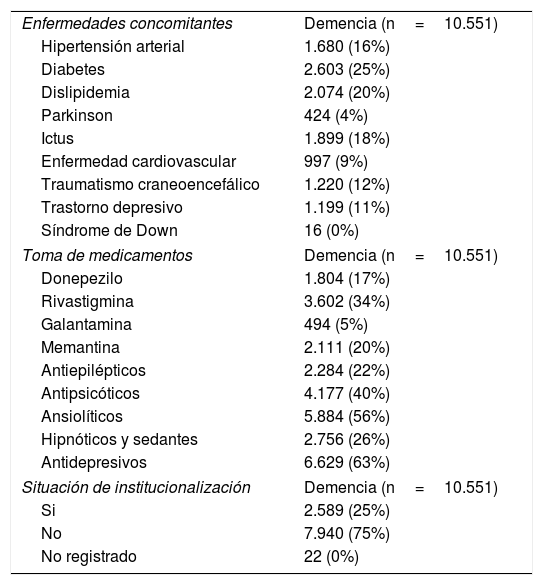
Después de la validación en la OSI Debabarrena se procedió a la extracción de los casos en toda Gipuzkoa. La tabla 4 contiene la distribución de los casos vivos de demencia probables y confirmados en Gipuzkoa según su presencia en las diferentes bases de datos a fecha 31 de diciembre de 2016, que suman un total de 10.551 demencias. Dado que muchos pacientes aparecen en más de una, el número total de casos no es igual a la suma de ambos. En la tabla 5 se muestra la distribución de los casos totales, confirmados y probables por género y edad. La proporción de mujeres es superior a la de hombres. La distribución de los casos totales según enfermedades concomitantes, toma de medicamentos y situación de institucionalización aparece en la tabla 6. La enfermedad concomitante más frecuente fue la dislipidemia. Entre los medicamentos más frecuentemente prescritos figuran los ansiolíticos y los antidepresivos. Están institucionalizados un 25% de los individuos con demencia.
Distribución de los casos vivos de demencia probables y confirmados en Gipuzkoa según su presencia en las diferentes bases de datos
| Demencia (n=10.551) | ||
|---|---|---|
| Probable (n=3.184) | (Confirmado n=7.367) | |
| Atención primaria | 3.053 (96%) | 4.448 (60%) |
| Consultas externas | 0 | 3.464 (47%) |
| Hospitalización | 245 (8%) | 414 (6%) |
| Fármacos específicos | 0 | 5.867 (80%) |
Distribución de los casos totales, confirmados y probables por género y edad
| Demencia probable | Demencia confirmada | Demencia total | ||
|---|---|---|---|---|
| 3.184 | 7.367 | 10.551 | 100% | |
| Género | ||||
| Hombres | 930 | 2.508 | 3.438 | 33% |
| Mujeres | 2.254 | 4.859 | 7.113 | 67% |
| Grupo de edad | ||||
| <60 | 84 | 390 | 474 | 4% |
| 60-64 | 52 | 136 | 188 | 2% |
| 65-69 | 97 | 216 | 313 | 3% |
| 70-74 | 186 | 521 | 707 | 7% |
| 75-79 | 280 | 916 | 1.196 | 11% |
| 80-84 | 581 | 1.947 | 2.528 | 24% |
| 85-89 | 784 | 2.120 | 2.904 | 28% |
| ≥90 | 1.120 | 1.121 | 2.241 | 21% |
Distribución de los casos totales según enfermedades concomitantes, toma de medicamentos y situación de institucionalización
| Enfermedades concomitantes | Demencia (n=10.551) |
| Hipertensión arterial | 1.680 (16%) |
| Diabetes | 2.603 (25%) |
| Dislipidemia | 2.074 (20%) |
| Parkinson | 424 (4%) |
| Ictus | 1.899 (18%) |
| Enfermedad cardiovascular | 997 (9%) |
| Traumatismo craneoencefálico | 1.220 (12%) |
| Trastorno depresivo | 1.199 (11%) |
| Síndrome de Down | 16 (0%) |
| Toma de medicamentos | Demencia (n=10.551) |
| Donepezilo | 1.804 (17%) |
| Rivastigmina | 3.602 (34%) |
| Galantamina | 494 (5%) |
| Memantina | 2.111 (20%) |
| Antiepilépticos | 2.284 (22%) |
| Antipsicóticos | 4.177 (40%) |
| Ansiolíticos | 5.884 (56%) |
| Hipnóticos y sedantes | 2.756 (26%) |
| Antidepresivos | 6.629 (63%) |
| Situación de institucionalización | Demencia (n=10.551) |
| Si | 2.589 (25%) |
| No | 7.940 (75%) |
| No registrado | 22 (0%) |
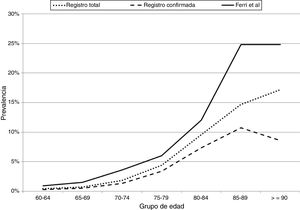
Por último, la figura 1 muestra la comparación de la cobertura de casos totales y confirmados por grupos de edad en Gipuzkoa que en total supone un 65% de los casos previstos según la prevalencia de Ferri et al. a nivel europeo23.
DiscusiónA la luz de los resultados de este estudio valoramos que un registro de demencias basado en las bases de datos clínicas y administrativas es válido y factible. Su principal aportación es mostrar la dimensión que tiene la demencia en el ámbito del sistema sanitario. El enfoque aplicado para establecer la condición de confirmado o probable se basa en dar como criterio fiable el establecido por el neurólogo en su consulta. El sistema de codificación automática a partir de los diagnósticos asignados a los episodios de consulta funciona con suficiente validez como para poder ser usados en el análisis epidemiológico. Un segundo aspecto a resaltar es que este formato permite repetir el proceso cada año y por tanto analizar de forma dinámica la evolución de esta población, ya que estarían disponibles las fechas del primer contacto con el sistema sanitario (probable diagnóstico inicial) y fallecimiento. Su carácter dinámico permite la valoración de las tendencias y las características epidemiológicas que definen una enfermedad como incidencia, prevalencia y mortalidad24.
Existen muy pocos estudios de validación de algoritmos diagnósticos en las bases de datos clínicas24. Un modelo similar se ha planteado en Canadá25. Sin embargo, ante la falta de diagnósticos codificados en consultas externas aplican un tipo de validación diferente basado en una combinación de contactos en hospitalización y AP. Sus resultados en términos de sensibilidad (80,7%) y especificidad (98,7%) son similares a los nuestros. En ambos casos se corrobora que el registro tiene limitaciones en la identificación de los casos (sensibilidad del 80%) pero cuando se diagnostica la demencia su fiabilidad es realmente buena dada la especificidad del 99%. Pensamos que la sensibilidad va a mejorar a medida que los neurólogos se adapten mejor al sistema de codificación automática. El estudio de validación se ha hecho con episodios de la época de transición de la historia en papel a la historia digital. La localización de la información en documentos escaneados ha podido obstaculizar la validación y aumentando los casos no confirmados. En cualquier caso creemos que el nivel de calidad alcanzado en el registro es suficiente para medir la carga de la demencia en el sistema sanitario vasco.
Las definiciones y clasificaciones de los registros suelen incluirse en marcos y modelos más amplios de vigilancia de la salud pública y presentación de informes sobre la calidad de la atención de la salud26. Un reciente trabajo ha revisado el tema de los registros de demencias12 y distingue siguiendo la terminología epidemiológica en inglés entre «register» y «registry»27. En general, en epidemiología, el término «register» se refiere a un «archivo de datos sobre todos los casos de una enfermedad particular u otra condición relevante para la salud en una población definida» y un «registry» es un «sistema de registro continuo»27. En el primer grupo incluiríamos los registros de demencia con vocación poblacional como el de South Carolina16. Por el contrario, registros como el CERAD encajan mejor en el segundo13. Aunque los casos proceden de las bases de datos clínicas, nuestra propuesta de registro de demencia tiene un enfoque poblacional por lo que se podría denominar «register». El motivo es que localiza los diagnósticos de demencia en todos los contactos de los individuos con el sistema sanitario. Su mayor fortaleza es la cobertura alcanzada que supone un 65% de la prevalencia esperada23. Es una buena cifra si tenemos en cuenta que parte de los casos no se ponen en contacto con el sistema sanitario o no se diagnostican. También parece plausible que los casos confirmados bajen enormemente con respecto al total en las edades por encima de 90 años. En estas edades los síntomas cognitivos son valorados de diferente manera y el paciente no se remite a la consulta del especialista. Una comparación de las características clínicas con las del registro de Girona muestra unos porcentajes de comorbilidades similares en enfermedad de Parkinson, ictus y diabetes mellitus28. Por el contrario, la hipertensión arterial y los trastornos tiroideos aparecen con cifras diferentes. Una limitación de nuestro enfoque es la menor profundidad clínica de las variables recogidas si se compara con un registro basado en la búsqueda activa en la historia clínica como el de Girona14. Una consecuencia de esta limitación es la dificultad de separar los diferentes tipos de demencia. Posiblemente este punto mejorará a medida que se estandaricen en las consultas externas la codificación de los episodios de demencia.
En una comunicación personal del Departamento de Servicios Sociales de la Diputación de Gipuzkoa presentado con ocasión del día mundial de la enfermedad de Alzheimer en 2011 se identificaba la demencia como diagnóstico para 4.746 casos que recibían ayuda de acuerdo con los criterios de la ley de Dependencia. De ellos estaban institucionalizados el 34% (1631 individuos). En nuestro estudio la cifra de individuos institucionalizados es de 2.589 lo que sitúa la cobertura de la ley de dependencia en el 63% si se mantuviese en 2016 el número de individuos incluidos en las ayudas sociales.
Este registro ha incluido los casos vivos a 31 de diciembre de 2016 y nuestra propuesta es completarlo cada año con una nueva búsqueda que aporte los datos referidos a los pacientes incluidos en años anteriores (cohortes prevalentes) y los nuevos casos del año terminado (cohorte incidente). De esta manera cada año se actualizaría la información de cada individuo. Hacer análisis poblacionales sería posible ya que cada campo lleva incorporada la fecha de su registro. También hay que resaltar que el mantenimiento de este registro dinámico implica el manejo de una base de datos anonimizada y que no requiere la identificación a los casos.
Como conclusión final queremos resaltar que nuestra propuesta de registro dinámico de demencias de tipo poblacional basado en las bases de datos del Servicio Vasco de Salud es factible y además viable desde el punto de vista económico ya que implica un uso eficiente de los recursos. Aunque este estudio se ha limitado a la población guipuzcoana, por estar basado en búsquedas automatizadas se podrían aplicar al conjunto de Euskadi y requeriría unos recursos de personal pequeños.
Conflicto de interesesDeclaramos que no existe conflicto de intereses que pueda percibirse como un perjuicio a la imparcialidad de la investigación informada.
FinanciaciónEl estudio fue financiado por una ayuda de la Fundación Vasca de Innovación e Investigación Sanitarias (Bioef) número BIO12/AL/005.