El ataque cerebrovascular isquémico es una entidad de alta prevalencia que representa un alto costo y una carga importante de morbimortalidad en la población general. Dentro de las diferentes estrategias para su tratamiento se encuentran el inicio temprano de antiagregación, el ingreso oportuno a una unidad de cuidado crítico neurológico, la trombólisis y la trombectomía mecánica.
ObjetivosEn el presente artículo hacemos una revisión narrativa de la mejor evidencia disponible acerca de los nuevos avances en cuanto a terapias de reperfusión y su impacto en la práctica clínica.
DesarrolloCon los avances en la terapia endovascular, se ha ampliado de forma importante el rango de tiempo para lograr ofrecer una intervención oportuna a un mayor número de pacientes, sin embargo, en los últimos años se ha buscado ampliar aún más esta ventana para realizar trombólisis endovenosa por encima de las 4,5 h clásicamente descritas.
ConclusionesLa nueva evidencia disponible apunta hacia la extensión de las ventanas de tiempo clásicamente descritas a partir del uso de imágenes con técnicas como la perfusión por tomografía o resonancia, con el fin de aumentar el número de pacientes que se benefician de estas intervenciones (trombólisis y trombectomía) y disminuir la morbi mortalidad asociada a la enfermedad.
Ischemic stroke is a highly prevalent disease that represents a high cost and a significant burden of morbidity and mortality in the general population. Among the different strategies for its treatment are the early initiation of anti-aggregation, timely admission to a neurological critical care unit, thrombolysis, and mechanical thrombectomy.
ObjectivesIn this article we present a narrative review of the best available evidence about new advances in reperfusion therapies and their impact on clinical practice.
DevelopmentWith advances in endovascular therapy, the time range has significantly expanded to offer a timely intervention to a greater number of patients, however, in recent years it has been sought to further expand this window to perform intravenous thrombolysis above the classically described 4.5 h.
ConclusionsThe new available evidence points towards the extension of the time windows classically described from the use of images with techniques such as perfusion by tomography or resonance, in order to increase the number of patients who benefit from these interventions (thrombolysis and thrombectomy) and reduce the morbidity and mortality associated with the disease.
El ataque cerebrovascular (ACV) isquémico agudo es un síndrome clínico caracterizado por una alteración en la circulación cerebral, que deriva en un desequilibrio entre el aporte de oxígeno y los requerimientos del mismo, lo que lleva a un déficit focal del tejido encefálico1-4.
El ACV es una urgencia neurológica que tiene una alta carga de enfermedad, siendo la segunda enfermedad más prevalente después de la enfermedad coronaria en el mundo1. Al mismo tiempo representa una carga importante de morbilidad y discapacidad, tratándose de una condición que genera alto costo, por la cual se han buscado diferentes estrategias de tratamiento para mejorar los desenlaces en términos de funcionalidad y calidad de vida5-8.
El tratamiento del infarto cerebral agudo se ha visto influenciado por tres terapias: el uso temprano de aspirina9, el ingreso del paciente a unidades de ACV y la trombólisis intravenosa en las tres primeras horas en ventana estándar y hasta 4,5 h en ventana extendida10,11, siendo estas las intervenciones que han demostrado mayor efectividad.
En los últimos años, con el advenimiento de nuevos dispositivos, se ha instaurado la terapia endovascular como una nueva terapia de reperfusión con excelentes resultados clínicos, logrando extender la ventana de tratamiento inicialmente a seis horas y recientemente hasta 24 h después del evento vascular isquémico12,13.
Posteriormente, se ha tratado de evaluar la eficacia de la combinación de las terapias de reperfusión tanto endovenosa como endovascular, con el fin de establecer el beneficio de realizar las dos cuando el paciente cumple los criterios de selección o, si por el contrario, no existe diferencia en cuánto a brindar una sola opción terapéutica14,15.
El objetivo de esta revisión narrativa es presentar un estado del arte de la mejor evidencia disponible en los últimos años de estudios que evalúan la efectividad de las terapias de reperfusión en ventana extendida y de las propuestas existentes para mejorar la toma de decisiones con el fin de aumentar el número de pacientes beneficiados con el tratamiento para el ACV isquémico agudo.
MetodologíaSe realizó una búsqueda de la literatura en Medline (incluido PubMed), Scopus y Embase con la siguiente estrategia: ((stroke) AND (thrombolysis) OR (mechanical thrombectomy)). Se encontraron 9.958 artículos, de los cuales, se incluyeron 30, no hubo restricción respecto al idioma ni al tamaño de la muestra de los estudios, se tomaron estudios que cumplían con los criterios: estudios que describen el diagnóstico y tratamiento del ACV y, con base en estos textos, se redactó esta revisión narrativa. Se excluyeron estudios si se cumplía alguno de los siguientes criterios: resultados no descritos, artículos de más de 15 años, uso de otras terapias alternativas a la trombólisis y trombectomía, entidades trombóticas en sitios diferentes al sistema nervioso central y trombosis de origen venoso.
Actualidad en las terapias de reperfusiónEn el 2006, el estudio DEFUSE se documentó la utilidad del uso de imágenes avanzadas como la resonancia magnética (RM) para establecer el perfil de los pacientes que podían tener una mejor respuesta clínica al tratamiento con alteplasa y se describieron los patrones imagenológicos que predecían este desenlace16. En ellos se encuentra el patrón de desacople (conocido en inglés como «mismatch») clásico perfusión/difusión (definido como una lesión en la secuencia de perfusión [PWI]) con volumen mayor o igual a 10 mL y 120% del volumen de lesión en la secuencia de difusión magnética (conocido como DWI), con el que se logró una respuesta favorable del 56% (IC 34-75) comparado con pacientes que no cumplían este perfil 19% (OR 5,4; p = 0,039)16. En este estudio se definió respuesta favorable como un puntaje en la escala de Rankin de 0-1 o una reducción de la escala de los National Institutes of Health Stroke Scale (NIHSS) de ocho puntos a los 30 días y reperfusión como la disminución del tamaño mayor o igual al 30% y mayor o igual de 10 mL de volumen en PWI (perfusión) comparado con el estudio basal16.
Inicialmente, las terapias de reperfusión estaban orientadas por el paradigma del tiempo teniendo un punto de corte de 4,5 h para el uso de alteplasa, usando como guía el estudio ECASS III17. En ese trabajo se evidenciaron resultados clínicos favorables para los pacientes con este periodo de tiempo entre el ACV y el inicio del fibrinolítico hasta los 270 min. Por otro lado, cinco estudios (MR CLEAN18, SWIFT-PRIME19, EXTEND-IA20, REVASCAT21, PISTE22) demostraron que en individuos con oclusión de vaso grande con menos de seis horas de síntomas, NIHSS > 6 y Alberta Stroke Programme Early CT Score (ASPECTS) > 6 son candidatos a recibir terapia endovascular, con un OR cercano a tres y un número necesario a tratar (NNT) de dos.
Sin embargo, el paradigma del tiempo ha pasado a un segundo plano y actualmente la elección de las terapias de reperfusión se realiza basado en la viabilidad tisular. Los estudios WAKE-UP23 y el estudio EXTEND24 demostraron que con el uso de imágenes avanzadas de resonancia magnética (RM) o tomografía axial computarizada (TAC) con perfusion, respectivamente, algunos pacientes que tienen tiempo de síntomas desconocido o un tiempo de instauración de la enfermedad mayor a 4,5 h se benefician del tratamiento con alteplasa. Se establecieron dos modelos, uno de un centro de infarto o core pequeño con gran área de alteración de la perfusión para el tratamiento mecánico (EXTEND) y el otro es el de lesión < 4,5 h, el cual precisa el desacople entre las secuencias de imagen de RM en el que lesiones positivas en DWI y negativas en fluid attenuated inversion recovery (FLAIR) (menores a 4,5 h). Establecen la posibilidad de que se trate de un infarto hiperagudo en pacientes con ACV del despertar o aquellos que se desconoce la hora de inicio de síntomas (WAKE-UP). Por otro lado, dos ensayos (DAWN y DEFUSE-3) mostraron que algunos pacientes con síntomas de hasta 24 h de duración o tiempo de ventana desconocido y oclusión de vaso grande se benefician del manejo con trombectomía.
Trombólisis: ACV del despertar, tiempo de síntomas desconocido y ventana extendidaEl estudio EPITHET25 reclutó 101 pacientes con ACV de tres a seis horas de evolución desde el inicio de los síntomas, el objetivo primario fue valorar el crecimiento del infarto teniendo en cuenta la difusión inicial y el control imagenológico a los 90 días en pacientes con desacople. La intervención fue el tratamiento con activador del plasminógeno tisular recombinante (rTPA) vs. placebo en una relación 1:1. Todos los pacientes tuvieron resonancia con perfusión-difusión, y mostró que el grupo de alteplasa aumentó el grado de reperfusión, disminuyó el crecimiento del infarto y mejoró la funcionalidad, teniendo en cuenta que el beneficio de la reperfusión sucedió en aquellos que tenían desacople.
Se sabe que los pacientes con tiempo de síntomas menor a 4,5 h presentan un desacople entre la secuencia de difusión (DWI) y la secuencia FLAIR26. En el estudio WAKE-UP23 se usó RM para determinar si existía desacople entre estas dos secuencias en los sujetos que se presentaban con tiempo de inicio de síntomas desconocido, de esta manera evaluando la posibilidad de que aún exista penumbra potencialmente salvable. El desenlace primario de eficacia en este estudio era un desenlace clínico favorable que precisaron como un puntaje en la escala de Rankin modificada (ERm) de 0 o 1 a los 90 días del evento, el cual se obtuvo en el 53% del grupo intervenido y 42% del grupo placebo23. Para los pacientes con ACV del despertar y lesiones lacunares el beneficio fue del 56 vs. 49% con OR de 1,67 (IC 0,77-3,64)23.
En cuanto a la trombólisis en ventana extendida, el estudio EXTEND24 evaluó la posibilidad de realizarla hasta nueve horas posterior al ACV con la ayuda de imágenes avanzadas. Se incluyeron pacientes con ERm de 0 o 1, con puntaje NIHSS entre 4 y 26 y que tuvieran regiones de hipoperfusión cerebral salvables detectadas por imágenes por perfusión que fueron procesadas por el software RAPID®. Las regiones con hipoperfusión crítica fueron medidas con RM o TAC por perfusión de acuerdo con la demora de llegada de un agente trazador inyectado (tiempo máximo de la función residual > 6 segundos). Definieron el desacople de lesión isquémica (perfusión)/core como una tasa mayor a 1,2 entre el volumen de hipoperfusión y el volumen de core isquémico; una diferencia absoluta de volumen mayor a 10 mL (área de penumbra), con un volumen de core isquémico menor a 70 mL medido con un flujo sanguíneo cerebral relativo (FSCr) menor del 30% comparado con el tejido normal24.
En los datos observados se encontró oclusión de vaso grande en el 69% de los pacientes seleccionados para trombólisis y en el 72% del grupo control24. El desenlace primario de eficacia fue obtener un puntaje de 0 o 1 en ERm a los 90 días del evento y se alcanzó en el 35,4% del grupo intervención y 29,5% del grupo placebo24. En cuanto a hemorragia intracerebral sintomática se mostró que el grupo tratado con alteplasa sangró más (6,2%) que el grupo control (0,9%), sin embargo, el porcentaje de muertes a los 90 días no evidenció diferencias significativas24.
En 2019, con el fin de aclarar el beneficio de realizar trombólisis sistémica en pacientes con ventana extendida de 4,5 a 9 h en casos seleccionados con desacople DWI/PWI positivo, se realizó el estudio ECASS-427 con 119 pacientes en múltiples países europeos, aleatorizado, multicéntrico, doble ciego, fase 3, cuyo objetivo primario fue valorar la funcionalidad a través de la ERm a 90 días con la intervención vs. el placebo. Definieron que el desacople para la penumbra era una relación (ratio) en PWI:DWI mayor de 1,2 y un volumen mínimo de PWI de 20 mL27. Tras realizar el reclutamiento de pacientes entre 2014 y 2017, y con los resultados de los estudios de trombectomía mecánica (DAWN y DEFUSE-3), hubo un importante número de deserción de los pacientes y el reclutamiento no se pudo completar adecuadamente por lo que se finalizó de forma temprana. Dentro de los resultados no encontraron diferencias significativas que soportaran el uso de trombólisis sistémica en ventana extendida y en términos de seguridad, observaron que la tasa de mortalidad a 90 días fue de 11,5% en el grupo de trombólisis vs. el 6,8% en el grupo de placebo27.
Tras los avances mencionados publicados en la literatura mundial para extender la ventana de las terapias de reperfusión, la práctica clínica ha venido evolucionando. En ese sentido, se han incluido algunas recomendaciones nuevas en la guía de práctica clínica de la organización europea de ACV (European Stroke Organization) de 202128 que se mencionan a continuación:
Para pacientes con ACV en ventana de tiempo entre 4,5 y 9 h seleccionados con TAC, ¿la trombólisis con alteplasa lleva a mejores desenlaces funcionales vs. no intervenir?Con un grado de recomendación fuerte y una calidad de la evidencia moderada, no recomiendan la administración de alteplasa en el contexto de solo contar con una imagen de tomografía, dado que los estudios no mostraron beneficio y por el contrario se evidenció un aumento en el riesgo de hemorragia intracraneal, con un OR de 6,8928.
En pacientes con ACV isquémico en ventana de 4,5 a 9 h, con TAC y RM con desacople core/perfusión, ¿la trombólisis lleva a mejores desenlaces funcionales vs. la no intervención?Desde el punto de vista técnico, el desacople entre una TAC simple y una TAC con perfusión o entre un DWI y un PWI puede cuantificar la zona de penumbra isquémica y podría identificar pacientes que se beneficien de alteplasa más allá de 4,5 h. Esto no solo permite que se pueda extender la ventana de tiempo, sino también que los pacientes con ACV del despertar se beneficien de la intervención ya que permite identificar la ventana tisular27.
Como mencionamos previamente el estudio EPITHET25 no demostró beneficio de alteplasa clínicamente, pero con una disminución significativa del tamaño del infarto en aquellos pacientes tratados con el trombolítico dentro de tres a seis horas. Continuando en esa línea, el ECASS-427 tampoco logró tener un mejor desenlace funcional a tres meses con el uso de alteplasa entre 4,5 a 9 h.
Por otro lado, el estudio EXTEND24 sí halló que la trombólisis con alteplasa se asociaba a mejores desenlaces funcionales (por ERm 0-1) a tres meses. En ese sentido, y con un grado de recomendación fuerte y con una baja calidad de la evidencia, la guía recomienda que en pacientes con síntomas de ACV entre 4,5 y 9 h, con TAC/resonancia con desacople core/perfusión y que no tengan indicación de trombectomía o que no tengan la disponibilidad, la administración de alteplasa.
En pacientes con ACV isquémico del despertar o de tiempo desconocido, ¿la trombólisis con alteplasa lleva a mejores desenlaces funcionales vs. la no intervención?En 2020 se llevó a cabo el metaanálisis EOS29, en el cual se incluyeron los estudios WAKE-UP, EXTEND, THAWS30 y ECASS-427, aportando 843 pacientes entre los cuatro ensayos clínicos. Se encontró un desenlace favorable en 199 (47%) de 420 pacientes con alteplasa y en 160 (39%) de 409 casos del grupo control. Documentaron que alteplasa se asoció con una tendencia hacia un curso clínico favorable y a mayor probabilidad de desenlaces adecuados en términos de funcionalidad. En cuanto a la prevalencia de hemorragia intracraneal sintomática, fue mayor en el grupo de alteplasa vs. el control (3 vs. < 1%). Concluyeron que en pacientes con ACV de tiempo desconocido con desacople DWI/FLAIR o con perfusión, alteplasa resultó en mejores desenlaces funcionales a 90 días en comparación con el cuidado clínico estándar.
Existen cinco ensayos clínicos aleatorizados controlados que estudian esta pregunta, dentro de los cuales el estudio WAKE-UP23 y el THAWS30 (ambos terminados de forma temprana), no lograron demostrar diferencia en mejores desenlaces a tres meses en el grupo de alteplasa vs. el control, pero tampoco hubo diferencias significativas para mortalidad.
El estudio EXTEND24 sí demostró asociación con mejores desenlaces a corto plazo en términos de funcionalidad en el grupo de trombólisis endovenosa. En ese sentido, con un grado de recomendación fuerte y alta calidad de la evidencia acuerdan que en pacientes con ACV isquémico del despertar o de tiempo desconocido, que tengan desacople DWI/FLAIR y que no tengan indicación de trombectomía, o no la tengan disponible, sugieren la administración de alteplasa con un grado de evidencia moderado. Adicionalmente, recomiendan que en pacientes que tengan desacople en TAC por perfusión o resonancia con desacople core/perfusión con la misma consideración de no indicación de la trombectomía, se realice trombólisis endovenosa.
Trombectomía mecánica: ventana extendidaComo se mencionó previamente, la trombectomía mecánica es una terapia de reperfusión indicada en pacientes que tuvieran menos de seis horas de síntomas, un puntaje de ASPECTS > 6 y NIHSS > 6 según cinco estudios (MR CLEAN, SWIFT-PRIME, EXTEND-IA, REVASCAT, PISTE). Sin embargo, así como sucedió con la trombólisis, dos estudios (DEFUSE-3 y DAWN) analizaron la posibilidad de realizar terapia mecánica hasta 16 y 24 h desde el inicio de los síntomas en pacientes seleccionados.
En el estudio DEFUSE-313 se evaluó la eficacia y seguridad de la trombectomía mecánica en ventana extendida de seis a 16 h después de transcurrido el ACV en pacientes que tuvieran tejido cerebral isquémico potencialmente salvable identificado por imágenes de perfusión. Se eligieron individuos con oclusión de arteria carótida interna, porción cervical o intracraneal y arteria cerebral media (ACM) M1, que al inicio presentaran un core isquémico menor de 70 mL, una tasa de volumen de tejido isquémico/ volumen de infarto mayor o igual a 1,8 y una penumbra de 15 mL o más13.
El tamaño de la zona de penumbra fue estimado mediante el retraso en el tiempo de llegada del contraste al tejido Tmáx > 6 seg y para calcular el volumen de core isquémico se utilizó FSCr menor del 30% comparado con el tejido normal; para visualizar más fácil y rápidamente las regiones de penumbra en la TAC por perfusión o RM por difusión se usó el software RAPID®13. Los pacientes que fueron incluidos presentaron un NIHSS > 6 y un puntaje ERm entre 0 y 2. Por el contrario, se excluyeron pacientes que recibieron rTPA en una ventana mayor a 4,5 h o que presentaran un ASPECTS < 6 en la TAC. En cuanto al desenlace primario de eficacia, el cual fue el puntaje ordinal de la ERm a los 90 días, se evidenció que el grupo tratado con terapia endovascular y terapia médica estándar presentó una distribución más favorable comparado con el grupo control, OR crudo 2,77 (IC 1,63-4,7, p≤0,001) y OR ajustado 3,36 (IC 1,96-5,77, p≤0,001). Además, el grupo intervenido logró un mayor porcentaje de pacientes con independencia funcional (ERm 0-2) 45 vs. 17%, RR 2,67 (IC 1,6-4,48, p≤0,001). Por otro lado, la mortalidad a los 90 días fue de 14% en el grupo de terapia endovascular y 26% en el grupo de terapia médica (p = 0,05), la tasa de hemorragia intracraneal sintomática no presentó diferencias significativas13.
Finalmente, el estudio DAWN12 también evaluó la eficacia de la trombectomía en ventana extendida de seis a 24 h posterior al ACV en pacientes que presentan disociación entre el déficit clínico y el infarto. Fueron elegidos individuos que presentaran oclusión intracraneal de arteria carótida interna, el segmento M1 de ACM o ambas, además, debían presentar una disociación entre la severidad del déficit clínico y el infarto del volumen. Se seleccionaron tres grupos de pacientes dependiendo la edad, el NIHSS y el volumen del infarto: grupo A eran pacientes mayores de 80 años con puntaje NIHSS > 10 y volumen de infarto < a 21 mL, el grupo B eran pacientes < de 80 años con puntaje NIHSS > 10 y volumen de infarto < a 31 mL y por último el grupo C eran pacientes < de 80 años, con puntaje NIHSS > 20 y volumen de infarto entre 31 mL y menos de 51 mL.
El volumen del infarto fue obtenido con ayuda de RM por difusión o TAC por perfusión y el software RAPID®12. Dentro de los criterios de inclusión se encontraban pacientes que por última vez hubiesen sido vistos bien entre seis a 24 h previos, tener un puntaje en ERm de 0 a 1, que no tuvieran un infarto que comprometa más de 1/3 del territorio de la ACM y que no fueran candidatos a manejo con alteplasa. El desenlace primario fue la independencia funcional (ERm 0-2) a los 90 días, en el grupo intervenido 49 y 13% el grupo control (IC 21-44)12. En desenlaces secundarios se observó que la recanalización fue lograda en el 77% del grupo intervenido y 36% en el grupo con terapia médica estándar. Por otro lado, no hubo diferencia estadísticamente significativa de efectos adversos serios, incluidas muerte relacionada con ACV, muerte por cualquier otra causa o hemorragia intracraneal sintomática12.
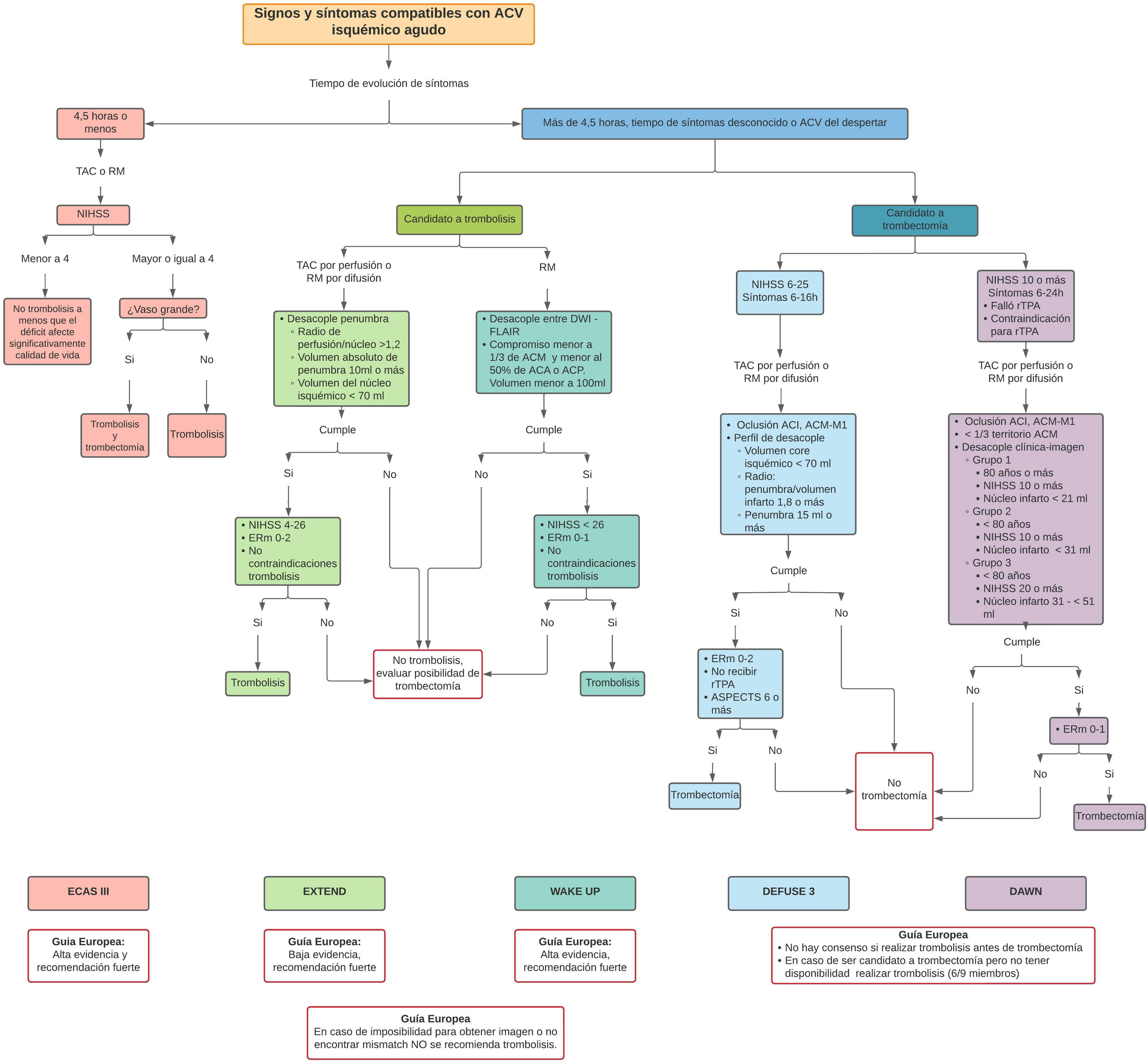
En la figura 1 se presenta un algoritmo de manejo de ACV donde se exponen las diferentes terapias disponibles, dependiendo del tiempo de evolución de síntomas que tenga el paciente; y en la tabla 1 se muestran los criterios de inclusión y exclusión que se tuvieron en cuenta en cada uno de los estudios de alto impacto en esta materia.
Algoritmo de tratamiento de ACV.
ACV: ataque cerebrovascular; ACA: arteria cerebral anterior; ACI: arteria carótida interna; ACM: arteria cerebral media; ACM-M1: arteria cerebral media segmento proximal; ACP: arteria cerebral posterior; DWI: diffusion-weighted imaging; ERm: escala de Rankin modificada; FLAIR: fluid attenuated inversión recovery; RM: resonancia magnética; rTPA: activador del plasminógeno tisular recombinante; TAC: tomografía axial computarizada.
Criterios de inclusión y exclusión de estudios de terapia de reperfusión en ventana extendida
| Estudio | Criterios Inclusión | Criterios Exclusión |
|---|---|---|
| EPITHET (alteplasa después de 3 horas) | - ACV isquémico hemisférico con síntomas de 3-6 h- Edad ≥ 18 años- NIHSS > 4- ERm 0-2 | - Hemorragia aguda- Isquemia > 1/3 territorio de ACM- Contraindicaciones para RM- Contraindicaciones estándar para alteplasa- Enfermedad neurológica de base que pueda confundir: demencia |
| ECASS III(trombólisis 3-4,5 horas) | - ACV isquémico agudo- Edad 18-80 años- Síntomas con 3 a 4,5 h de duración | - Tiempo de síntomas no conocido- Hemorragia intracraneal- NIHSS > 25- Convulsiones- ACV, trauma craneal severo o cirugía mayor en últimos 3 meses- Uso de heparina 48 h antes con PTT excediendo el límite normal- Plaquetas < 100.000- PA > 185/110- Glicemia < 50 o > 400 mg/dL- Tratamiento con anticoagulantes |
| EXTEND(trombólisis ventana extendida hasta 9 h) | - ACV isquémico agudo hemisférico- Edad ≥ 18 años- Pacientes con ACV del despertar- NIHSS ≥ 4-26- Desacople de penumbra:* Perfusión/núcleo > 1,2* Área de penumbra: diferencia absoluta de volumen ≥ 10 mL (usando RM o TAC con Tmáx > 6 seg)* Volumen de núcleo isquémico ≤ 70 mL | - Hemorragia intracraneal- NIHSS < 4 o que mejoren síntomas- ERm previo al ACV ≥ 2- Contraindicación para uso de agentes de contraste- Núcleo isquémico > 1/3 de territorio ACM- Enfermedad terminal con expectativa de vida < 1 año- Embarazo- ACV previo en últimos 3 meses- Historia reciente o presentación clínica con HSA, malformación AV, aneurismas, neoplasia cerebral- Uso de anticoagulantes e INR > 1,7- Uso heparina en últimas 48 horas y TTP prolongado- Hipoglicemia clínica significativa- PA no controlada > 185/110 mmHg en al menos dos ocasiones separadas por 10 min o que requiera tratamiento agresivo para reducirla- Diátesis hemorrágica hereditaria o adquirida- Sangrado gastrointestinal o urinario en últimos 21 días- Cirugía mayor en últimos 14 días- Exposición a agente trombolítico en últimas 72 h |
| ECASS 4 | - ACV isquémico agudo- Edad ≥ 18 años- Tratamiento entre edad ≥ 4,5 a 9 h post-ACV- Pacientes con ACV del despertar- NIHSS ≥ 4-26 con signos clínicos de infarto hemisférico- Imagen de penumbra con relación (volumen perfusión/infarto) > 1,2 y la lesión de perfusión con un volumen mínimo de 20 mL | - Rápida mejoría de síntomas, particularmente si resultado probable es NIHSS < 4 en la aleatorización.- ERm > 1 antes del ACV- Contraindicaciones para realizar RM- Núcleo de infarto > 1/3 del territorio de ACM o > 100 mL- Participar en estudio de investigación en los últimos 30 días- Expectativa de vida menor a 3 meses- Condición que implique riesgo para el paciente si se inicia el tratamiento (microangiopatía)- Embarazadas o en lactancia- ACV previo en últimos 3 meses- Historia de hemorragia intracraneal, hemorragia subaracnoidea, malformación AV, aneurismas, neoplasia cerebral.- Uso de anticoagulantes orales en últimas 48 h o tiempo de protrombina prolongado (INR > 1,6) o tiempo de tromboplastina que exceda 1,5 veces el rango normal o tiempo de trombina prolongado- Uso de heparina, excepto heparina subcutánea de bajo peso molecular en últimas 48 h. Uso de inhibidores de glicoproteína IIb/IIIa en últimas 72 h- Plaquetas < 100.000- Glucosa < 50 o más de 400 mg/dL- Hipertensión no controlada: PAS > 185 mmHg o > 110 mmHg en al menos dos ocasiones separadas por 10 min o que requiera manejo agresivo para reducirla- Diátesis hemorrágica hereditaria o adquirida- Sangrado gastrointestinal o urinario en últimos 21 días- Pancreatitis aguda reciente- Enfermedad hepática severa: falla hepática, cirrosis, hipertensión portal, hepatitis activa- Cirugía mayor en últimos 14 días- Masaje cardiaco externo traumático, parto, punción en sitio no compresible en últimos 10 días- Exposición a agente trombolítico en últimas 72 h |
| WAKE-UP(trombólisis: ACV del despertar) | - Criterios clínicos:- ACV isquémico agudo con tiempo de síntomas desconocido- Última vez visto bien > 4,5 h- Déficit neurológico incapacitante (alteración de uno o más: lenguaje, función motora, cognición, mirada, visión, extinción)- Edad 18-80 años- Criterios Imagenológicos:- ACV agudo en RM positivo en DWI y negativo en FLAIR | Criterios clínicos:- Candidato a trombectomía mecánica- Discapacidad previa: ERm > 1- NIHSS > 25- Hipersensibilidad a alteplasa- Embarazo o lactancia- Desorden hemorrágico significativo en últimos 6 meses- Diátesis hemorrágica conocida- Hemorragia intracraneal conocida o sospechada- Hemorragia subaracnoidea sospechada- Historia de daño SNC (neoplasia, aneurismas, cirugía intracraneal o espinal)- Masaje cardiaco externo, parto o punción en vaso sanguíneo no compresible en últimos 10 días- Uso anticoagulantes con INR elevado o heparinas y TTP elevado.- Plaquetas < 100.000- Glicemia < 50 o > 400 mg/dL- Hipertensión no controlada > 185/110 o que requiera tratamiento agresivo para reducirla- Endocarditis bacteriana, pericarditis- Pancreatitis aguda reciente- Enfermedad ulcerativa gastrointestinal en últimos 3 meses, varices esofágicas, aneurisma arterial, malformación AV- Neoplasia con aumento del riesgo de sangrado- Enfermedad hepática severa- Cirugía mayor o trauma severo en últimos 3 meses- ACV en últimos 30 díasEnfermedad terminal con < 6 meses de vida- Cualquier contraindicación para RMCriterios imagenológicos:- Baja calidad de RM- Cualquier signo de hemorragia intracraneal- FLAIR positivo- Lesión > 1/3 de territorio ACM o > 50% de ACA o ACP o más de 100 mL en DWI |
| DEFUSE-3(trombectomía 6-16 h) | - Criterios clínicos:- Signos y síntomas consistentes con diagnóstico de ACV isquémico de circulación anterior- Edad 18-90 años- NIHSS ≥ 6 y mantenerse ≥ inmediatamente antes de aleatorización- Independencia funcional previa ERm 0-2Criterios imagenológicos- Oclusión ACI, ACM M1 por RM o TAC- Perfil de desacople en RM o TAC:* Volumen núcleo isquémico < 70 mL* Radio tejido isquémico/volumen infarto ≥ 1,8 y penumbra ≥ 15 mLCriterios imagenológicos alternos:- TAC o RM demostraran Tmáx > 6 seg con déficit de perfusión consistente con oclusión de ACI o ACM-M1 y perfil de desacople positivo | Criterios clínicos:- Enfermedad terminal con expectativa de vida < 6 meses- Enfermedad médica, neurológica o psiquiátrica- Embarazo- No poder realizar RM o TAC por perfusión con contraste- Alergia a contrastes yodados- Tratamiento con rTPA > 4,5 h- Tratamiento con rTPA 3-4,5 h y cualquiera de las siguientes: > 80 años, uso de anticoagulantes, historia diabetes mellitus y ACV previo, NIHSS > 25- Diátesis hemorrágica hereditaria o adquirida, deficiencia factores de coagulación, anticoagulantes orales con INR > 3- ConvulsionesGlicemia < 50 - > 400 mg/dL- Plaquetas < 50.000Hipertensión arterial severa y sostenida > 185/110 mmHg- Endocarditis bacteriana o embolo séptico sospechadoCriterios imagenológicos:- ASPECTS < 6- Tumor intracraneal o lesión ocupante de espacio- Disección de ACI que limite el flujo o disección aórtica- Stent intracraneal implantado en el mismo territorio vascular- Oclusión arterial sintomática de más de un territorio vascular confirmado por RM o TAC |
| DAWN (trombectomía 6-24 horas) | Criterios clínicos:- Signos y síntomas consistentes con ACV y que pertenezcan a:a. Falla terapia con rTPA (oclusión persistente a los 60 min)b. Contraindicación rTPA- Edad ≥ 18 años- NIHSS ≥ 10- Funcionalidad ERm 0 o 1- Expectativa de vida > 6 meses- Se permitió uso de heparinas en últimas 24 h si perfil de coagulación estable- Pacientes con inhibidores de factor Xa o inhibidores directos de trombinaCriterios imagenológicos:≤ 1/3 de ACM comprometida- Oclusión ACI o ACM-M1- Desacople clínico-imagen:* Edad ≥ 80 años, NIHSS ≥ 10 y núcleo infarto < 21 mL* Edad < 80 años, NIHSS ≥ 10 y núcleo infarto < 31 mL* Edad < 80 años, NIHSS ≥ 20 y núcleo infarto 31 - < 51 mL | Criterios clínicos:- Trauma craneal severo en últimos 90 días con déficit neurológico residual- Mejoría rápida del déficit neurológico (NIHSS < 10) o evidencia de recanalización- Condiciones neurológicas o psiquiátricas- Convulsiones- Glicemia < 50 o > 400 mg/dL- Hemoglobina < 7 mmol/L- Plaquetas < 50.000- Electrolitos: sodio < 130 mmol/L, potasio < 3 mEq/L o > 6 mEq/L- Falla renal: creatinina > 3 mg/dL (pacientes en diálisis si podían incluirse)- Diátesis hemorrágica conocida, deficiencia factores coagulación o terapia anticoagulante con INR > 3 o TTP > 3 veces lo normal- Pacientes en manejo con clopidogrel, aspirina o ambos en últimas 24 h no debían excluirse si el perfil de coagulación era aceptable.- Hemorragia reciente o activa en últimos 30 días- Historia de alergia severa a medios de contraste- Hipertensión severa y sostenida > 185/110 mmHg- Embarazo o lactancia al ingreso- Sospecha de endocarditis bacteriana o émbolo séptico presumible.- Tratamiento con cualquier dispositivo de trombectomía o terapia intraarterial antes de la aleatorización.Criterios imagenológicos:- Evidencia de hemorragia intracraneal- Disección carotidea que limite el flujo, estenosis de alto grado u oclusión completa de arteria carótida cervical que requiriera stent- Tortuosidad excesiva de vasos cervicales- Sospecha de vasculitis cerebral- Sospecha de disección aortica- Implante de stent intracraneal en el mismo territorio vascular- Oclusión en múltiples territorios vasculares- Efecto de masa con desplazamiento de línea media- Presencia de tumor intracraneal |
ACV: ataque cerebrovascular; ACA: arteria cerebral anterior; ACI: arteria carótida interna; ACM: arteria cerebral media; ACM-M1: arteria cerebral media segmento proximal; ACP: arteria cerebral posterior; AV: arteriovenoso; DWI: diffusion-weighted imaging; ERm: escala de Rankin modificada; FLAIR: fluid attenuated inversión recovery; HSA: hemorragia subaracnoidea; INR: índice internacional normalizado; PAS: presión arterial sistémica; RM: resonancia magnética; rTPA: activador del plasminógeno tisular recombinante; SNC: sistema nervioso central; TAC: tomografía axial computarizada; TTP: tiempo parcial de tromboplastina; Tmáx: tiempo máximo.
El tratamiento del ACV isquémico agudo ha ido evolucionando, tanto en el tiempo para la toma de decisiones como en las diferentes estrategias terapéuticas de reperfusión. En cuanto a la trombólisis endovenosa en ventana extendida, existe evidencia de su beneficio en pacientes seleccionados y utilizando técnicas de imagen por perfusión o el desacople DWI/FLAIR por resonancia magnética, sin embargo, es importante tener en cuenta que la mayoría de los estudios mostraron mayores tasas de sangrado. Por otro lado, respecto a la trombectomía mecánica, a la luz de la evidencia actual disponible la consideramos una terapia efectiva en ventana prolongada o de tiempo desconocido en pacientes seleccionados. Falta la implementación y la adopción de estas estrategias en los diferentes centros hospitalarios en Latinoamérica, donde hay menor cantidad de recursos físicos y humanos para el tratamiento el tratamiento de ACV, por lo que producir investigación en español de este tema puede ayudar a difundir el conocimiento en nuestro medio local y regional.
AclaraciónLa valoración de la evidencia aportada, así como el contenido de las tablas y algoritmos presentados han sido confeccionados por los autores. Si bien se hallan basados en publicaciones de alto nivel de evidencia y en guías de sociedades científicas reconocidas, la decisión final del contenido es parte de la revisión narrativa bajo la óptica de los autores.
Aspectos éticosLos autores declaramos haber contribuido y revisado el material escrito en este artículo, así como haber cumplido todos los requisitos éticos para la producción de un artículo científico de revisión.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.