El ictus es la complicación neurológica más frecuente tras una coronariografía. Nuestro objetivo fue estudiar las diferencias clínicas y pronósticas entre los códigos ictus (CI) poscateterismo y el resto de CI intra y extrahospitalarios.
MétodosRegistro prospectivo de activación de CI entre marzo de 2011 y abril de 2016 en nuestro centro. Comparamos características clínicas, radiológicas, tratamiento administrado, situación funcional y mortalidad a 3 meses dependiendo de si se trató de un CI poscateterismo, del resto de CI intrahospitalarios o extrahospitalarios.
ResultadosDe 2.224 activaciones de CI 31 fueron poscateterismo. Los CI poscateterismo presentaron una NIHSS basal menor respecto al resto de CI intrahospitalarios y extrahospitalarios (5 vs. 10 vs. 7 respectivamente, p=0,02), mayor rapidez en la activación (50min vs. 100min vs. 125min, p<0,001), mayor presentación en forma de AIT (38% vs. 8% vs. 9%, p<0,001) y menor tasa de oclusión arterial proximal (17,9% vs. 31.4% vs. 39.2%, p=0,023). El 89,7% de ictus poscateterismo no recibieron tratamiento de reperfusión. En caso de oclusión arterial proximal el 60% recibió tratamiento endovascular. La mortalidad fue del 12,95% en los CI poscateterismo y del 25% en el resto de CI intrahospitalarios. Aunque los ictus poscateterismo presentaron mejor pronóstico funcional, el análisis ajustado mostró que este efecto estaba determinado por su menor gravedad inicial.
ConclusionesEl ictus poscateterismo tiene una menor gravedad inicial, aparece más frecuentemente como AIT y presenta menor incidencia de oclusión arterial proximal. La mayoría no recibe tratamiento de reperfusión, pero cuando existe oclusión arterial, la mayor parte de ellos son tratados mediante trombectomía.
Ischaemic stroke is the most common neurological complication of cardiac catheterisation. This study aims to analyse the clinical and prognostic differences between post-catheterisation stroke code (SC) and all other in-hospital and prehospital SC.
MethodsWe prospectively recorded SC activation at our centre between March 2011 and April 2016. Patients were grouped according to whether SC was activated post-catheterisation, in-hospital but not post-catheterisation, or before arrival at hospital; groups were compared in terms of clinical and radiological characteristics, therapeutic approach, functional status, and three-month mortality.
ResultsThe sample included 2224 patients, of whom 31 presented stroke post-catheterisation. Baseline National Institutes of Health Stroke Scale score was lower for post-catheterisation SC than for other in-hospital SC and pre-hospital SC (5, 10, and 7, respectively; P=.02), and SC was activated sooner (50, 100, and 125minutes, respectively; P<.001). Furthermore, post-catheterisation SC were more frequently due to transient ischaemic attack (38%, 8%, and 9%, respectively; P<.001) and less frequently to proximal artery occlusion (17.9%, 31.4%, and 39.2%, respectively; P=.023). The majority of patients with post-catheterisation strokes (89.7%) did not receive reperfusion therapy; 60% of the patients with proximal artery occlusion received endovascular treatment. The mortality rate was 12.95% for post-catheterisation strokes and 25% for all other in-hospital strokes. Although patients with post-catheterisation stroke had a better functional prognosis, the adjusted analysis showed that this effect was determined by their lower initial severity.
ConclusionsPost-catheterisation stroke is initially less severe, and presents more often as transient ischaemic attack and less frequently as proximal artery occlusion. Most post-catheterisation strokes are not treated with reperfusion; in case of artery occlusion, mechanical thrombectomy is the preferred treatment.
El ictus isquémico es la complicación neurológica más frecuente del cateterismo cardíaco, estimándose una incidencia de 0,05-0,1% en las coronariografías diagnósticas, que asciende hasta un 0,18-0,44% en los procedimientos con intención terapéutica1. Además, su aparición en este contexto puede ser devastadora, condicionando una mortalidad del 22-37%1. Los factores de riesgo asociados al ictus poscateterismo han sido bien caracterizados a través de largas series de pacientes. Se estima que los pacientes con mayor edad, insuficiencia renal crónica y factores de riesgo vascular que se someten a cateterismos de larga duración y de tipo urgente tienen un incremento del riesgo de sufrir un ictus peri o posprocedimiento2.
Durante muchos años el tratamiento del ictus en estos pacientes ha sido controvertido, ya que la infusión de heparina sódica durante la angiografía multiplica por 2 el riesgo hemorrágico tras la administración de fibrinólisis sistémica3–6, única terapia aprobada hasta el año 2015. La revascularización arterial mediante trombectomía mecánica podría suponer una terapia segura y eficaz en el caso de oclusión aguda de gran vaso en estos casos.
Dado que actualmente disponemos de la posibilidad de ofrecer un tratamiento de reperfusión agudo a estos pacientes, es relevante mejorar nuestro conocimiento en cuanto a las características diferenciales y el pronóstico funcional de los ictus poscateterismo. De este modo, el objetivo del presente trabajo es estudiar las diferencias en las características clínicas, radiológicas y terapéuticas entre los pacientes en que se activa código ictus (CI) después de un cateterismo y el resto de CI tanto intra como extrahospitalarios, y analizar las diferencias referentes al pronóstico funcional entre los pacientes que padecen un ictus poscateterismo y el resto de CI intrahospitalarios.
Material y métodosPoblación a estudioLa región sanitaria Barcelonés Nord y Maresme es un área mixta rural y urbana, con un total de 705.803 habitantes en una extensión total de 463km2. La región Barcelonés Nord y Maresme incluye un total de 21 bases del sistema de emergencias médicas, 4 hospitales comarcales y un centro de referencia de ictus (Hospital Universitari Germans Trias i Pujol), que cubre además un área de 2.000.000 de habitantes como centro terciario para el tratamiento endovascular.
Los criterios para la activación del CI son: déficit neurológico sugestivo de ictus de menos de 8horas de evolución, cronología incierta o ictus del despertar en pacientes con independencia funcional previa definida como una puntuación en la escala modificada Rankin≤2 sin límite de edad.
Para la realización de este estudio utilizamos datos de nuestro registro prospectivo, en el que incluimos todos los casos de activación de CI desde marzo de 2011. En él se recogen prospectivamente características demográficas, cronología del episodio, lugar de activación del CI, características clínicas y radiológicas basales y tratamiento realizado, así como el diagnóstico según la clasificación Oxfordshire Community Stroke Project (OCSP)7.
Para este estudio seleccionamos todos los casos de activación de CI desde marzo de 2011 a abril de 2016. Todos los pacientes fueron evaluados por un especialista en neurología y tratados según las guías europeas8,9. En los pacientes con un ictus isquémico de menos de 4,5horas de evolución se administró fibrinólisis sistémica con alteplasa. En el caso de contraindicaciones para el tratamiento con alteplasa intravenosa10, o fracaso del tratamiento trombolítico, se consideró el tratamiento endovascular en aquellos ictus con oclusión arterial de gran vaso (arteria cerebral media, carótida intracraneal, oclusión en tándem o basilar) de menos de 8horas de evolución11.
Variables a estudioRegistramos características demográficas (edad y sexo), tiempo desde el inicio de los síntomas hasta la activación de CI, lugar de activación del CI (extra o intrahospitalario), situación funcional previa mediante la escala modificada de Rankin (mRS) y gravedad clínica del ictus mediante la National Institute of Health Stroke Scale a la llegada. Subdividimos los CI dependiendo de si fueron activados poscateterismo (dentro de las primeras 24horas después del procedimiento), resto de CI intrahospitalarios y CI extrahospitalarios. Valoramos la presencia de signos incipientes de isquemia en la TC o la RM cerebral realizada al ingreso mediante la escala Alberta Stroke Program Early CT Score12 y la existencia y localización de una oclusión arterial mediante angioTC, angioRM o Doppler transcraneal. También registramos el diagnóstico según la clasificación OCSP y el tratamiento de reperfusión administrado en fase aguda, indicando si el paciente recibió fibrinólisis sistémica, tratamiento endovascular primario o de rescate, o si no se realizó tratamiento de reperfusión.
Seguimiento y medidas de resultadoEstudiamos la situación funcional de los pacientes a los 3 meses en visitas de seguimiento neurológico exclusivamente en los pacientes en los que se activó CI intrahospitalario utilizando la escala mRS. Consideramos pronóstico excelente una puntuación mRS igual o menor a 1, y buen pronóstico a una puntuación a una mRS igual o menor a 2. En caso de muerte a los 3 meses se registró su causa para estipular si su origen era vascular.
Análisis estadísticoLos resultados de la estadística descriptiva se muestran como media (desviación estándar) o mediana —rango intercuartílico— en las variables continuas o como frecuencias en las variables categóricas. Se realizaron comparaciones entre los 3 subgrupos: ictus poscateterismo, resto de ictus intrahospitalarios e ictus extrahospitalarios. Estas comparaciones se analizaron mediante la prueba de análisis de la varianza (ANOVA) o la prueba de Kruskall-Wallis para las variables continuas y pruebas de Chi-cuadrado para las variables categóricas. Todas las estimaciones del tamaño del efecto se proporcionan con sus IC del 95% y valores de p, considerándose estadísticamente significativo un valor menor a 0,05. Para el análisis multivariante referente a buen pronóstico y mortalidad se realizó una regresión logística ajustada por aquellas variables que presentaron un p valor<0,05 en el análisis univariante. Todos los análisis estadísticos se realizaron con el paquete estadístico IBM SPSS Statistics 23 (Chicago, IL, EE. UU.).
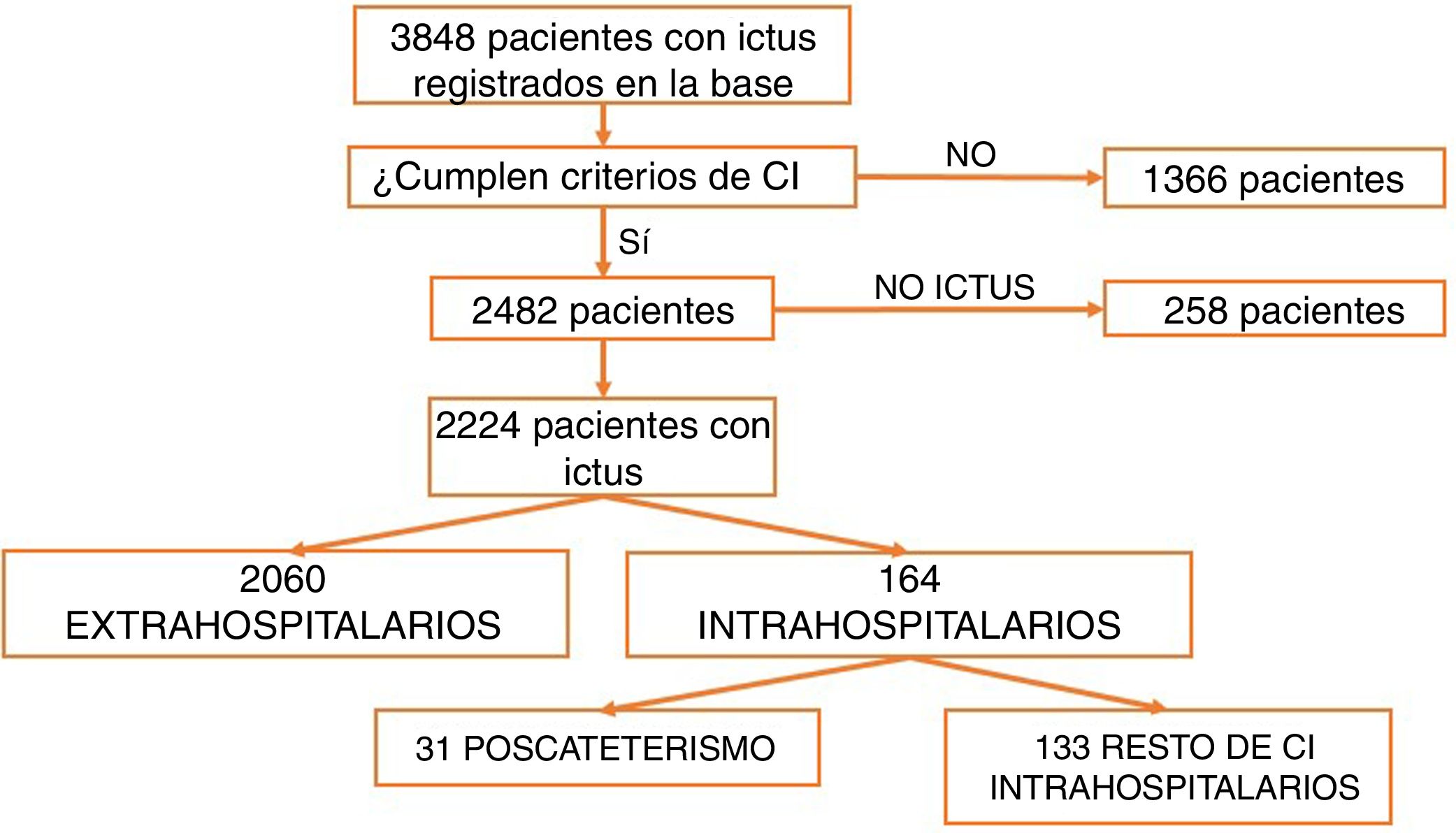
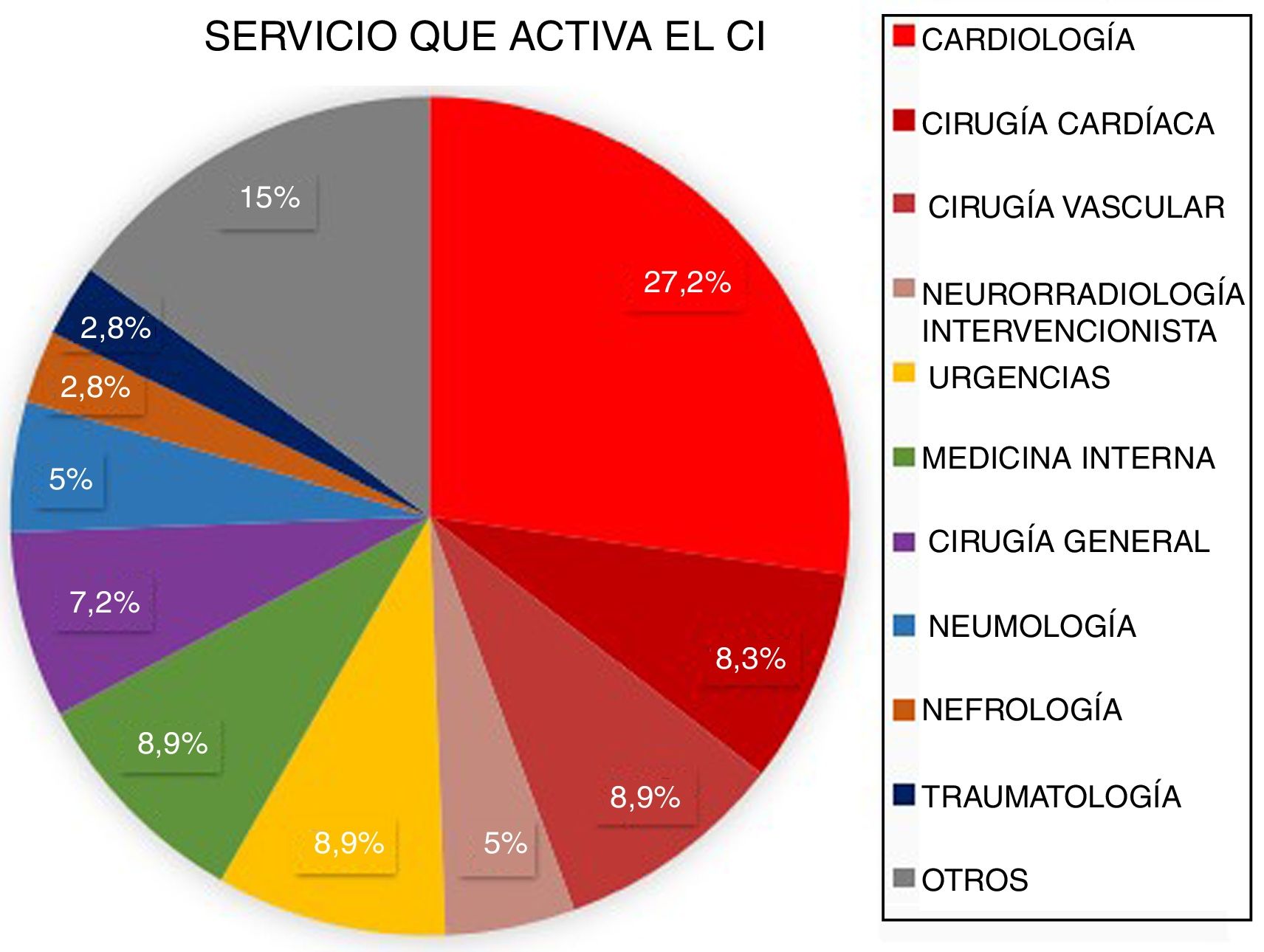
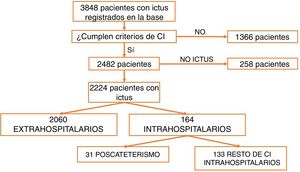
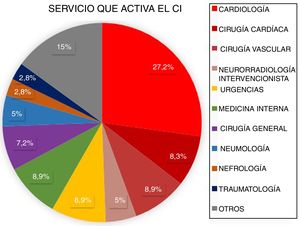
ResultadosDesde marzo de 2011 a abril de 2016 fueron atendidos en nuestro centro 3.848 pacientes tras la activación de CI. Tras excluir aquellos que no cumplían criterios de activación de CI (n=1.366) y los imitadores de ictus o ictus mimic (n=258), 2.224 pacientes fueron incluidos para el análisis. Un total de 2.060 CI fueron activados de forma extrahospitalaria y 164 (7,37%) fueron activados intrahospitalariamente (fig. 1). Los servicios que más CI intrahospitalarios activaron fueron cardiología y cirugía cardíaca (35,5%). Los porcentajes detallados del servicio desde el que se activó el CI se encuentran en la figura 2. Un total de 31 pacientes tuvo un ictus después de un cateterismo cardíaco, representando el 18,9% de los CI intrahospitalarios y el 1,39% del total de activaciones de código ictus. De estos, 17 presentaron un ictus isquémico, 12 un ataque isquémico transitorio (AIT), y 2 un ictus hemorrágico.
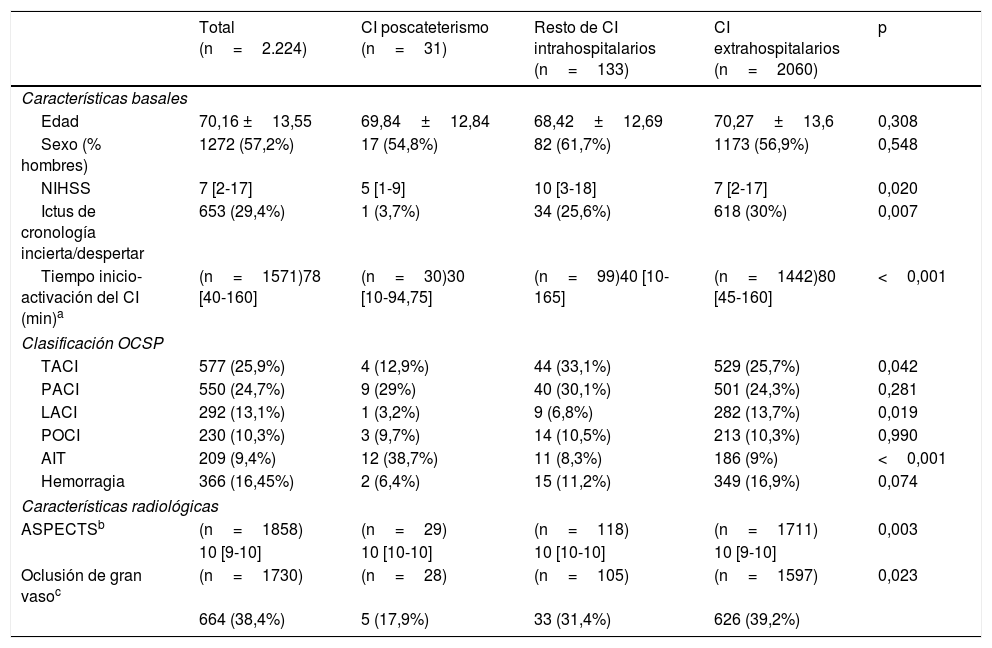
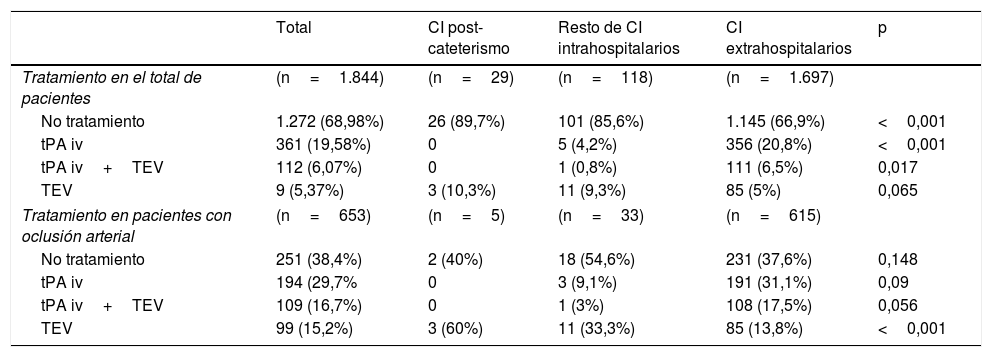
En la tabla 1 se exponen las características basales, diagnóstico según la clasificación OCSP y las características radiológicas del total de la muestra y de cada uno de los grupos estudiados. La media de edad en el total de la muestra fue de 70,16 años y el 57,2% de los pacientes fueron varones. Los ictus poscateterismo se diferenciaron del resto de CI intrahospitalarios y de los CI extrahospitalarios en presentar una menor gravedad inicial y una activación más rápida del código ictus, así como en su presentación clínica, apareciendo menos frecuentemente como infarto total de la circulación anterior y como infarto lacunar, y manifestándose más frecuentemente en forma de AIT (tabla 1). Asimismo, estos pacientes tuvieron una tasa menor de oclusión de gran vaso con respecto al resto de CI intrahospitalarios y extrahospitalarios (17,9% vs. 31,4% vs. 39,2%, respectivamente). Se indicó algún tratamiento de reperfusión a un porcentaje menor de pacientes del grupo CI poscateterismo u otros CI intrahospitalarios en comparación con el grupo CI extrahospitalario (10,3% vs. 14,4% vs. 33,1%, respectivamente). No obstante, en caso de oclusión de gran vaso el 60% de los ictus poscateterismo fueron tratados mediante terapia endovascular, siendo la diferencia de tratamiento con los otros grupos estadísticamente significativa (tabla 2).
Características basales clínicas y radiológicas
| Total (n=2.224) | CI poscateterismo (n=31) | Resto de CI intrahospitalarios (n=133) | CI extrahospitalarios (n=2060) | p | |
|---|---|---|---|---|---|
| Características basales | |||||
| Edad | 70,16 ±13,55 | 69,84±12,84 | 68,42±12,69 | 70,27±13,6 | 0,308 |
| Sexo (% hombres) | 1272 (57,2%) | 17 (54,8%) | 82 (61,7%) | 1173 (56,9%) | 0,548 |
| NIHSS | 7 [2-17] | 5 [1-9] | 10 [3-18] | 7 [2-17] | 0,020 |
| Ictus de cronología incierta/despertar | 653 (29,4%) | 1 (3,7%) | 34 (25,6%) | 618 (30%) | 0,007 |
| Tiempo inicio-activación del CI (min)a | (n=1571)78 [40-160] | (n=30)30 [10-94,75] | (n=99)40 [10-165] | (n=1442)80 [45-160] | <0,001 |
| Clasificación OCSP | |||||
| TACI | 577 (25,9%) | 4 (12,9%) | 44 (33,1%) | 529 (25,7%) | 0,042 |
| PACI | 550 (24,7%) | 9 (29%) | 40 (30,1%) | 501 (24,3%) | 0,281 |
| LACI | 292 (13,1%) | 1 (3,2%) | 9 (6,8%) | 282 (13,7%) | 0,019 |
| POCI | 230 (10,3%) | 3 (9,7%) | 14 (10,5%) | 213 (10,3%) | 0,990 |
| AIT | 209 (9,4%) | 12 (38,7%) | 11 (8,3%) | 186 (9%) | <0,001 |
| Hemorragia | 366 (16,45%) | 2 (6,4%) | 15 (11,2%) | 349 (16,9%) | 0,074 |
| Características radiológicas | |||||
| ASPECTSb | (n=1858) | (n=29) | (n=118) | (n=1711) | 0,003 |
| 10 [9-10] | 10 [10-10] | 10 [10-10] | 10 [9-10] | ||
| Oclusión de gran vasoc | (n=1730) | (n=28) | (n=105) | (n=1597) | 0,023 |
| 664 (38,4%) | 5 (17,9%) | 33 (31,4%) | 626 (39,2%) | ||
AIT: accidente isquémico transitorio; CI: código ictus; LACI: lacunar infarction; PACI: partial anterior circulation infarction; POCI: posterior circulation infarction; TACI: total anterior circulation infarction.
Tratamiento de reperfusión realizado
| Total | CI post-cateterismo | Resto de CI intrahospitalarios | CI extrahospitalarios | p | |
|---|---|---|---|---|---|
| Tratamiento en el total de pacientes | (n=1.844) | (n=29) | (n=118) | (n=1.697) | |
| No tratamiento | 1.272 (68,98%) | 26 (89,7%) | 101 (85,6%) | 1.145 (66,9%) | <0,001 |
| tPA iv | 361 (19,58%) | 0 | 5 (4,2%) | 356 (20,8%) | <0,001 |
| tPA iv+TEV | 112 (6,07%) | 0 | 1 (0,8%) | 111 (6,5%) | 0,017 |
| TEV | 9 (5,37%) | 3 (10,3%) | 11 (9,3%) | 85 (5%) | 0,065 |
| Tratamiento en pacientes con oclusión arterial | (n=653) | (n=5) | (n=33) | (n=615) | |
| No tratamiento | 251 (38,4%) | 2 (40%) | 18 (54,6%) | 231 (37,6%) | 0,148 |
| tPA iv | 194 (29,7% | 0 | 3 (9,1%) | 191 (31,1%) | 0,09 |
| tPA iv+TEV | 109 (16,7%) | 0 | 1 (3%) | 108 (17,5%) | 0,056 |
| TEV | 99 (15,2%) | 3 (60%) | 11 (33,3%) | 85 (13,8%) | <0,001 |
CI: código ictus; TEV: tratamiento endovascular; tPA iv: fibrinólisis intravenosa.
Excluidos los pacientes con hemorragia (n=366) y los pacientes que fueron tratados según un ensayo clínico de reperfusión (n=14).
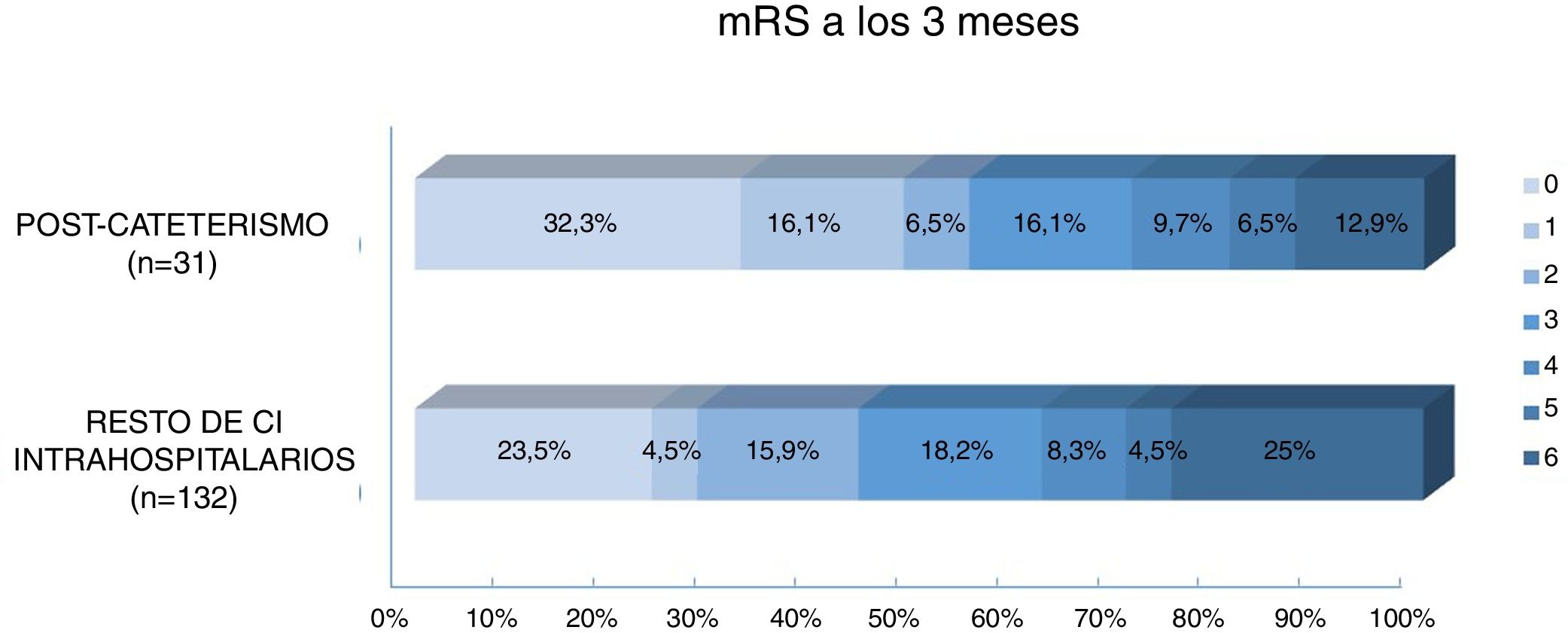
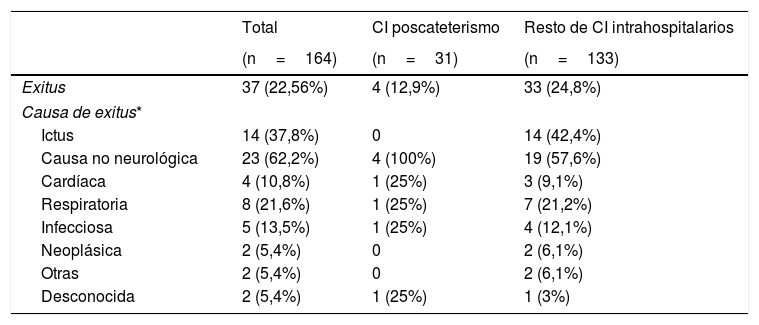
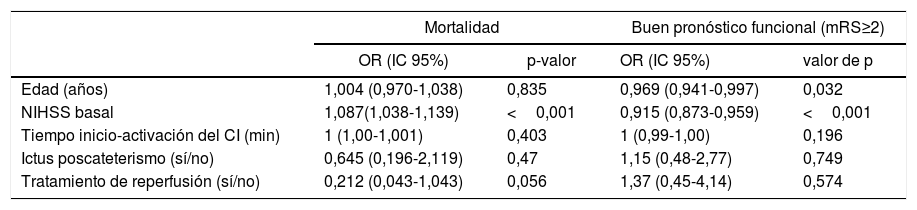
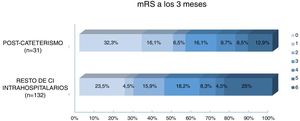
Al comparar el pronóstico funcional de los pacientes con ictus poscateterismo respecto al resto de CI intrahospitalarios observamos una mayor frecuencia de pronóstico excelente (48% vs. 28%, p=0,029) y un menor porcentaje de mortalidad (12,9% vs. 25%, p=0,14) en los pacientes con ictus poscateterismo, mientras que no se observaron diferencias en cuanto a la proporción de buen pronóstico entre ambos grupos (54,8% vs. 44,7%, p=0,31) (fig. 3). El 42,4% de las muertes en el resto de ictus intrahospitalarios fueron debidas al ictus, mientras que en los ictus poscateterismo la causa de muerte nunca fue debida al ictus (tabla 3). El ictus poscateterismo no se asoció de forma independiente al buen pronóstico clínico (p=0,75) ni a la mortalidad (p=0,47); solo la National Institute of Health Stroke Scale basal se mantuvo como predictor independiente para mortalidad, mientras que la edad se asoció a buen pronóstico funcional (tabla 4).
Exitus en los ictus poscateterismo y el resto de CI intrahospitalarios
| Total | CI poscateterismo | Resto de CI intrahospitalarios | |
|---|---|---|---|
| (n=164) | (n=31) | (n=133) | |
| Exitus | 37 (22,56%) | 4 (12,9%) | 33 (24,8%) |
| Causa de exitus* | |||
| Ictus | 14 (37,8%) | 0 | 14 (42,4%) |
| Causa no neurológica | 23 (62,2%) | 4 (100%) | 19 (57,6%) |
| Cardíaca | 4 (10,8%) | 1 (25%) | 3 (9,1%) |
| Respiratoria | 8 (21,6%) | 1 (25%) | 7 (21,2%) |
| Infecciosa | 5 (13,5%) | 1 (25%) | 4 (12,1%) |
| Neoplásica | 2 (5,4%) | 0 | 2 (6,1%) |
| Otras | 2 (5,4%) | 0 | 2 (6,1%) |
| Desconocida | 2 (5,4%) | 1 (25%) | 1 (3%) |
CI: código ictus.
Análisis multivariante para mortalidad y buen pronóstico funcional
| Mortalidad | Buen pronóstico funcional (mRS≥2) | |||
|---|---|---|---|---|
| OR (IC 95%) | p-valor | OR (IC 95%) | valor de p | |
| Edad (años) | 1,004 (0,970-1,038) | 0,835 | 0,969 (0,941-0,997) | 0,032 |
| NIHSS basal | 1,087(1,038-1,139) | <0,001 | 0,915 (0,873-0,959) | <0,001 |
| Tiempo inicio-activación del CI (min) | 1 (1,00-1,001) | 0,403 | 1 (0,99-1,00) | 0,196 |
| Ictus poscateterismo (sí/no) | 0,645 (0,196-2,119) | 0,47 | 1,15 (0,48-2,77) | 0,749 |
| Tratamiento de reperfusión (sí/no) | 0,212 (0,043-1,043) | 0,056 | 1,37 (0,45-4,14) | 0,574 |
CI: código ictus; IC: intervalo de confianza; mRS: escala modificada de Rankin; OR: odds ratio.
De acuerdo con los resultados de nuestro estudio el ictus poscateterismo origina la activación del 1,4% del total de CI, comprendiendo aproximadamente el 19% de las activaciones intrahospitalarias. Nuestros resultados distan de los observados en un estudio previo13, que cifra la presencia de ictus periprocedimiento, ya sea en sala de hemodinámica o de neurointervencionismo, en torno a un 6% de los ictus intrahospitalarios. Esta disparidad puede ser debida a diferencias interhospitalarias en cuanto al total de coronariografías realizadas, o a una mayor sensibilidad por parte del equipo de cardiología en la identificación de pacientes con síntomas neurológicos.
Por otra parte, solo el 6,4% de los CI poscateterismo fueron debidos a una hemorragia intracraneal. Aunque datos provenientes de un estudio previo elevan hasta un 50% la proporción de ictus hemorrágicos en este tipo de pacientes14, se ha de destacar que dicho estudio incluyó todos aquellos casos en que se realizó cirugía de revascularización coronaria con uso de circulación extracorpórea y, por tanto, en los que se había usado heparina sódica, lo que podría incrementar el riesgo hemorrágico en este grupo de pacientes.
Las activaciones de CI poscateterismo se realizaron de manera más precoz que el resto de activaciones, posiblemente por tratarse de pacientes en áreas hospitalarias bajo monitorización semiintensiva. Por otro lado, estos pacientes se diferenciaron del resto de CI por presentarse más frecuentemente en forma de AIT y menos frecuentemente en forma de infarto lacunar o infarto total de la circulación anterior, así como por presentar una gravedad inicial menor y una menor incidencia de oclusión de gran vaso. Estas diferencias podrían ser debidas a una mayor frecuencia de mecanismo embólico en los ictus poscateterismo, ya sea por desprendimiento de placas de ateroma del arco aórtico, por formación de trombos en la punta del catéter o por embolismos aéreos durante la inyección de contraste15, que producirían una oclusión de vasos distales, en muchos casos con recanalización espontánea. La menor gravedad de este tipo de ictus podría explicar que hasta en un 90% de los pacientes con ictus isquémicos poscateterismo se optara por un manejo conservador. Además, el uso de heparina sódica durante la coronariografía probablemente condicionó que en todos aquellos pacientes que recibieron tratamiento se optara por la terapia endovascular primaria en detrimento de la fibrinólisis sistémica. Algunos expertos han generado algoritmos respecto a la estrategia terapéutica más adecuada en este tipo de pacientes, sugiriendo la posibilidad de realizar una angiografía cerebral en la misma sala de hemodinámica, solo en caso de que el equipo médico tenga experiencia en angiografía cerebral selectiva. En caso contrario se recomienda seguir los cauces diagnóstico-terapéuticos habituales tras la activación de código ictus15.
Los pacientes con un ictus poscateterismo presentaron una mayor tasa de pronóstico funcional excelente y una menor mortalidad que el resto de CI intrahospitalarios. El mejor pronóstico de este grupo de pacientes se encontró condicionado por una menor gravedad inicial del ictus.
Aunque estudios previos muestran una alta mortalidad (22-37%)2,14,16–18 en los pacientes que presentan un ictus poscateterismo, en nuestra serie la mortalidad quedó reducida al 12,9%. En estudios previos, atendiendo al periodo en que se realizó el reclutamiento, y a la ausencia de información respecto a la terapia realizada, podemos intuir que los pacientes probablemente no recibieron un tratamiento específico para el ictus. Por el contrario, los pacientes de nuestra cohorte fueron ingresados en una unidad de ictus y tratados de acuerdo a las guías europeas, lo que podría explicar la diferencia de mortalidad observada. Al analizar la causa de la muerte de los pacientes de nuestra cohorte ninguno de los fallecimientos de los CI poscateterismo fue debido al propio ictus, mientras que, en el caso de los CI intrahospitalarios, el ictus fue la causa de la muerte en un 39,2% de los casos.
Nuestro estudio presenta varias limitaciones. En primer lugar, se trata de un estudio de diseño retrospectivo con los problemas inherentes a este tipo de diseño, aunque los datos fueron extraídos de un registro prospectivo. En segundo lugar, la generalización de algunos resultados puede estar limitada por el escaso tamaño de la muestra de ictus poscateterismo y por las diferencias tecnológicas y en recursos humanos especializados en la atención del ictus en los diferentes hospitales en los que se realiza hemodinámica cardíaca.
Concluimos que los ictus poscateterismo tienen una gravedad menor que el resto de CI, se presentan más a menudo en forma de AIT y presentan una oclusión de gran vaso en menor medida. El tratamiento de reperfusión de elección es el tratamiento endovascular primario en caso de que exista una oclusión de gran arteria. Mientras que el ictus sufrido tiene una relevancia determinante en la mortalidad de los CI intrahospitalarios, su importancia es marginal en el caso de los CI poscateterismo.
Conflicto de interesesNinguno de los autores presenta conflicto de intereses con relación a este artículo.
A todos los residentes y adjuntos del Hospital Germans Trias i Pujol, por su gran labor y esfuerzo en la cumplimentación de los registros. Especialmente a Anna Planas Ballvé, Joaquim Broto Fantova, Ane Miren Crespo Cuevas, Nicolau Guanyabens Buscà, Laura Abraira del Fresno, Tamara Canento Sánchez, Jordi Ciurans Molist, Daniela Samaniego Toro, Martí Paré Curell, Agustín Sorrentino Rodríguez, Nuolé Zhu, Sara Forcén Vega, Mireia Gea Rispal y Marta Álvarez Larruy.
El trabajo ha sido presentado como poster en la reunión anual de la Sociedad Española de Neurología en noviembre de 2016.