El estatus epiléptico (EE) es una urgencia neurológica asociada a una elevada mortalidad y morbilidad. Uno de los factores pronósticos es el tipo de EE. El objetivo de este trabajo es analizar las últimas recomendaciones de las distintas sociedades científicas y grupos de expertos sobre el tratamiento del EE, así como los estudios más recientes, para evaluar las referencias sobre el manejo del EE de tipo focal.
MétodosSe realizó una búsqueda en PubMed entre el 01/08/2008 y el 01/08/2018 sobre el tratamiento farmacológico del EE focal y sus distintos tipos en adultos.
ResultadosSe encontraron 29 publicaciones entre revisiones, guías terapéuticas, metaanálisis, ensayos clínicos y estudios de casos sobre el tratamiento del EE. De estas, solamente 3 tienen en cuenta si el EE es focal o generalizado, 4 se centran exclusivamente en EE focales y 7 diferencian entre EE convulsivo o no convulsivo especificando si incluyen crisis focales. Las recomendaciones terapéuticas para un EE focal no difieren de las de un EE generalizado en las fases I y II: inicialmente lorazepam o diazepam intravenoso si hay acceso venoso o midazolam intramuscular en caso contrario, seguido de fenitoína, valproato, levetiracetam o lacosamida intravenosos si persisten las crisis. En EE focales refractarios se recomienda retrasar en lo posible el inicio de fármacos anestésicos.
ConclusionesActualmente no disponemos de suficiente evidencia científica para afirmar que el tratamiento farmacológico del EE focal debe ser distinto al del EE generalizado. Son necesarios más registros con un amplio número de pacientes.
Status epilepticus (SE) is a neurological emergency associated with high morbidity and mortality. One prognostic factor is the type of SE. The purpose of this review is to analyse the most recent recommendations of different scientific societies and expert groups on the treatment of SE, and the latest studies, to assess the literature on the management of focal SE.
MethodsWe searched PubMed for studies published between 1 August 2008 and 1 August 2018 on the pharmacological treatment of focal SE and its different types in adults.
ResultsWe identified 29 publications among reviews, treatment guidelines, meta-analyses, clinical trials, and case series on the treatment of SE. Only 3 of them accounted for whether SE was focal or generalised; 4 focused exclusively on focal SE, and 7 differentiated between convulsive and non-convulsive SE and also record the presence of focal seizures. Treatment recommendations for focal SE do not differ from those of generalised SE in stages I and II: initially intravenous lorazepam or diazepam, if the intravenous route is available, and otherwise intramuscular midazolam, followed by intravenous phenytoin, valproate, levetiracetam, or lacosamide if seizures persist. Use of anaesthetic drugs should be delayed for as long as possible in patients with refractory focal SE.
ConclusionsThe available scientific evidence is insufficient to claim that pharmacological treatment of focal SE should be different from treatment for generalised SE. More studies with a greater number of patients are needed.
El estatus epiléptico (EE) es una urgencia neurológica que requiere una atención médica inmediata. Su tasa de incidencia anual, basada en diferentes estudios realizados en Europa y Estados Unidos, varía de 6,2 a 41 por 100.0001-3. Su pronóstico depende de varios factores: tipo de estatus, etiología, duración, nivel de conciencia al inicio, edad y respuesta al tratamiento. Teniendo en cuenta estos factores, se ha descrito una mortalidad global entre el 8 y 65%4.
La clasificación semiológica más reciente del EE5 establece dos grandes grupos en función de la presencia o no de síntomas motores, y dentro de cada grupo los EE pueden tener origen focal o generalizado (tabla 1). Aunque en la última clasificación de las crisis epilépticas6 se sustituye el término «parcial» por «focal», y estas crisis pasan a ser «con o sin alteración del nivel de conciencia» en lugar de «simples o complejas», en esta revisión se seguirán utilizando los términos «parcial» y «complejo» debido a que la mayoría de los artículos revisados son previos a dicha clasificación.
Clasificación del estatus epiléptico (EE) según semiología
| A. Con síntomas prominentemente motores |
| A.1. EE convulsivo (EEC, sinónimo: EE tónico-clónico) |
| A.1.a. Convulsivo generalizado |
| A.1.b. Inicio focal evolucionando a EE convulsivo bilateral |
| A.1.c. Desconocido si focal o generalizado |
| A.2. EE mioclónico (sacudidas mioclónicas epilépticas prominentes) |
| A.2.a. Con coma |
| A.2.b. Sin coma |
| A.3. Motor focal |
| A.3.a. Crisis motoras focales repetidas (Jacksonianas) |
| A.3.b. Epilepsia parcial continua (EPC) |
| A.3.c. Estatus versivo |
| A.3.d. Estatus oculoclónico |
| A.3.e. Paresia ictal (EE inhibitorio focal) |
| A.4. EE tónico |
| A.5. EE hipercinético |
| B. Sin síntomas prominentemente motores (EE no convulsivo, EENC) |
| B.1. EENC con coma (incluyendo el llamado EE «sutil») |
| B.2. EENC sin coma |
| B.2.a. Generalizado |
| B.2.a.a. Estatus de ausencia típica |
| B.2.a.b. Estatus de ausencia atípica |
| B.2.a.c. Estatus de ausencia mioclónica |
| B.2.b. Focal |
| B.2.b.a. Sin alteración del nivel de conciencia (aura continua, con síntomas autonómicos, sensitivos, visuales, olfatorios, gustativos, auditivos, emocionales/psíquicos/experimentales) |
| B.2.b.b. Estatus afásico |
| B.2.b.c. Con alteración del nivel de conciencia |
| B.2.c. Desconocido si focal o generalizado |
| B.2.c.a. EE autonómico |
Fuente: adaptado de Fisher et al.6.
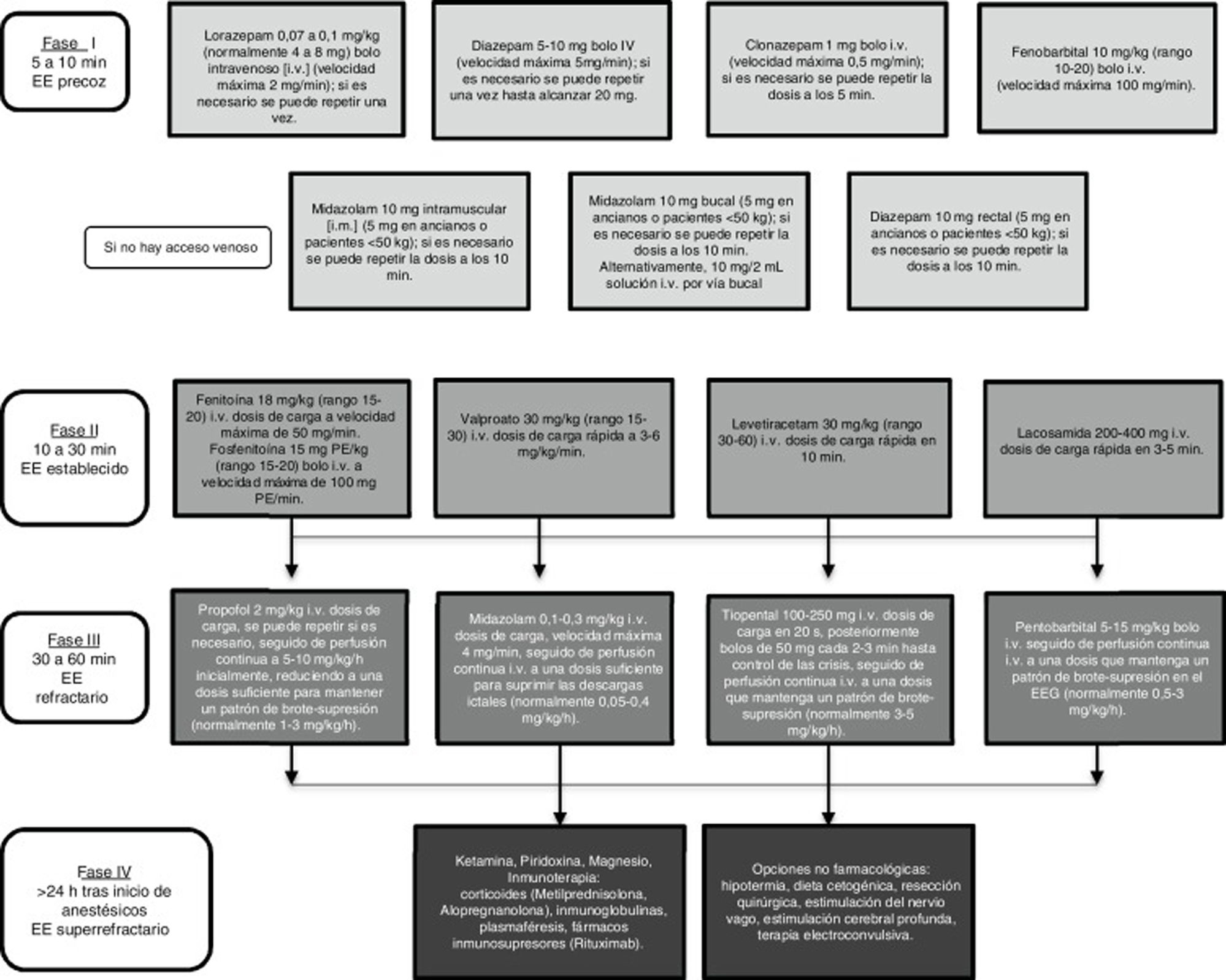
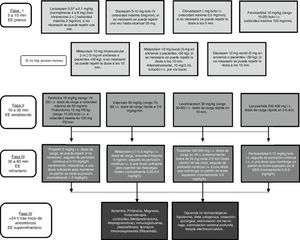
Hay consenso en que ante una situación de urgencia como un EE de cualquier tipo las medidas diagnósticas y terapéuticas deben implementarse en el menor tiempo posible. El control de un EE comienza con una fase de estabilización donde se aplican las medidas generales, seguido de tratamiento farmacológico dividido en distintas fases en función de la evolución del paciente, como se muestra en la figura 11,7,8.
En los últimos años ha habido más avances en cuanto a la definición y clasificación del EE, conocimiento de su fisiopatología y en las técnicas electroencefalográficas (que cada vez permiten identificar mejor si estamos ante un EE de origen focal o generalizado) que en cuanto al manejo terapéutico del mismo. De este modo, observamos que la mayoría de las publicaciones sobre el tratamiento del EE hacen referencia al EE convulsivo (EEC), o no especifican el tipo de EE que están tratando. Parece razonable pensar que, si los distintos fármacos antiepilépticos (FAE) de que disponemos, con sus diversos mecanismos de acción, en su mayoría no tienen la misma eficacia en los distintos tipos de crisis, no serán tampoco igual de eficaces en la resolución de los distintos tipos de EE.
Por tanto, los objetivos de este trabajo son revisar y analizar las últimas recomendaciones de las diferentes sociedades científicas y grupos de expertos sobre el tratamiento del EE, así como las publicaciones más recientes, para evaluar las referencias encontradas sobre el manejo terapéutico del EE de origen focal, y valorar, de este modo, si sería posible establecer una serie de recomendaciones terapéuticas orientadas a la práctica clínica para este tipo de estatus.
Material y métodosSe ha realizado una revisión sistemática de documentos, publicaciones y estudios de diferentes entidades científicas en relación con el tratamiento del EE focal. Se ha llevado a cabo una búsqueda en PubMed utilizando como descriptores: «partial/focal status epilepticus» y «drug therapy», además de «repeated focal motor seizures», «epilepsia partialis continua», «aphasic status epilepticus», «versive status epilepticus», «oculoclonic status epilepticus», «inhibitory status epilepticus», «secondarily generalized status epilepticus». La búsqueda se delimitó con los siguientes filtros:
- •
Periodo de tiempo: 01/08/2008 a 01/08/2018
- •
Tipos de estudios: revisiones, guías terapéuticas, metaanálisis, ensayos clínicos y estudios de casos.
- •
Idiomas: inglés, francés, alemán, portugués y español.
- •
Rango de edad: mayores de 13 años.
- •
Solo estudios en humanos.
Asimismo, se analizaron las referencias bibliográficas de los artículos seleccionados con el fin de rescatar otros estudios potencialmente incluibles en la revisión.
De todos los artículos encontrados con los parámetros especificados, se consideró como principal criterio de inclusión que se centrasen en el tratamiento farmacológico del EE.
Los criterios de exclusión fueron los siguientes:
- -
Tratar exclusivamente aspectos del EE distintos al terapéutico (i.e. definición, clasificación, diagnóstico).
- -
Un tipo exclusivo de epilepsia (p.ej., epilepsia por encefalitis de Rasmussen).
- -
Terapias farmacológicas dirigidas a una etiología específica de las crisis o empleadas en fases muy avanzadas del EE, como inmunoterapia, piridoxina, magnesio, etc.
- -
Terapias no farmacológicas del EE, como la neurocirugía o la dieta cetogénica.
Tras la búsqueda inicial se localizaron 789 estudios que posteriormente fueros revisados de manera exhaustiva para proceder a la selección según los criterios de inclusión y exclusión expuestos.
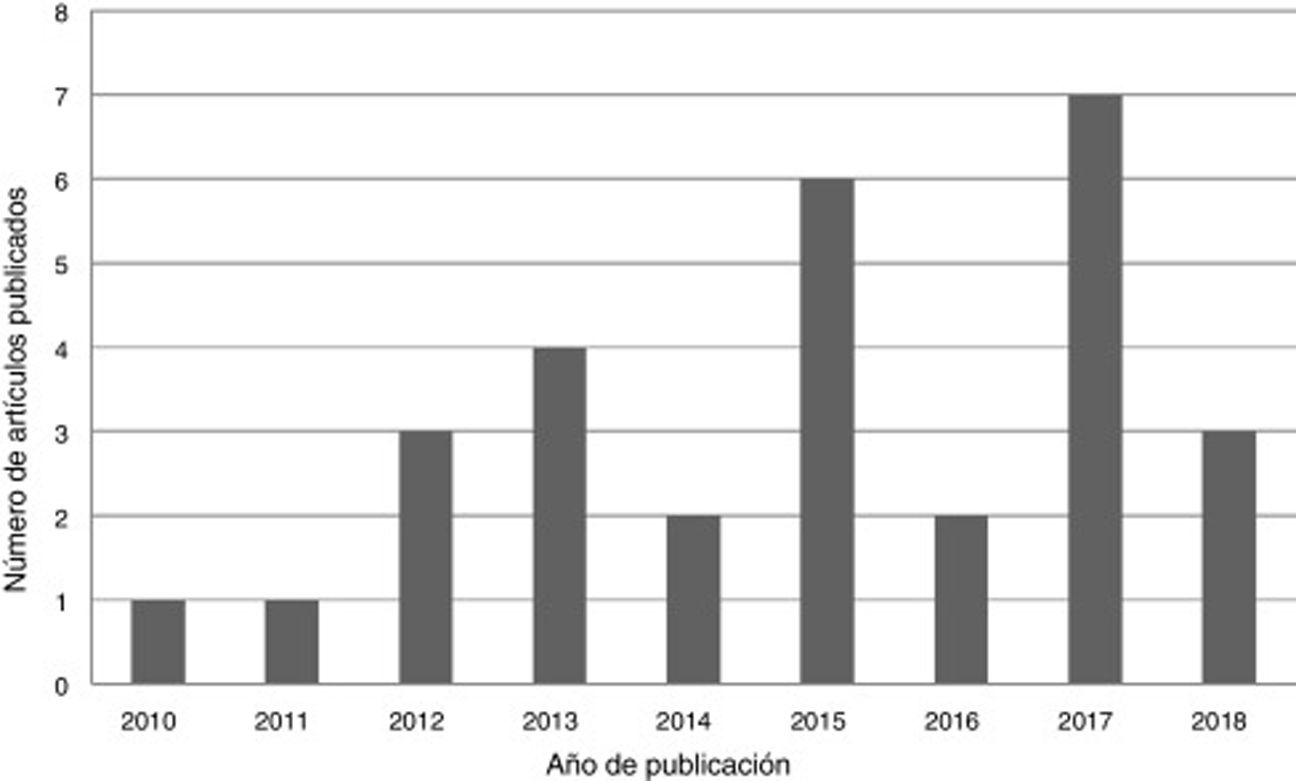
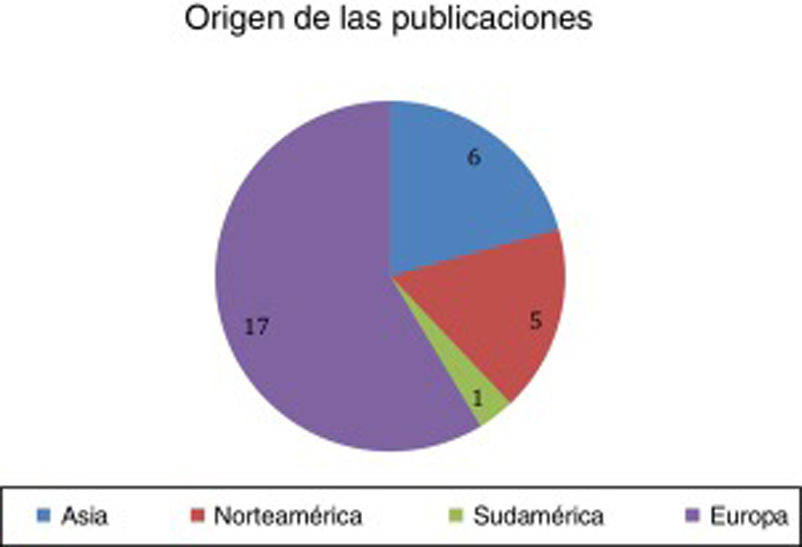
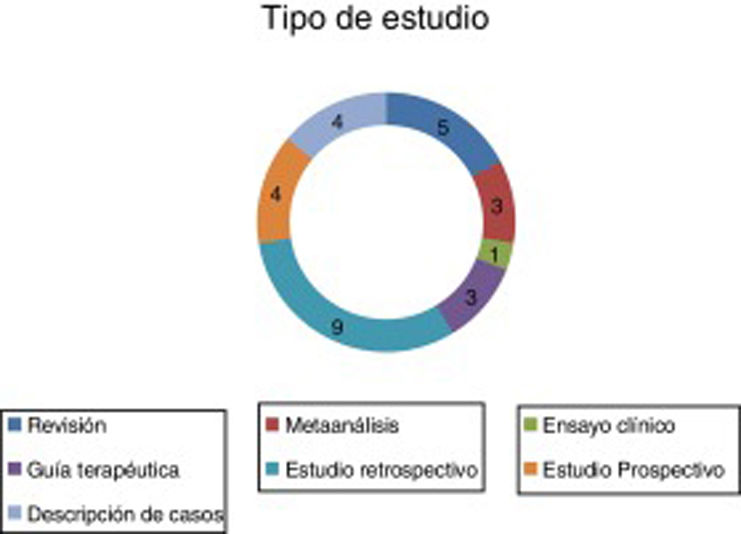
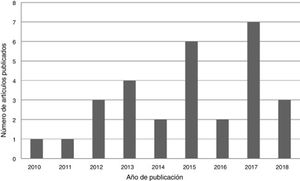
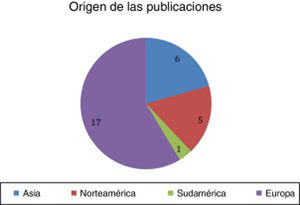
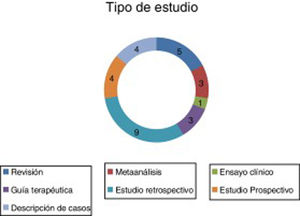
ResultadosSe encontraron un total de 29 artículos que cumplían las condiciones requeridas (figs. 2-4).
Entre estas publicaciones seleccionadas se encuentran distintos tipos de estudios que hacen referencia al tratamiento farmacológico de las distintas fases del EE (tabla 2).
Resumen de las características de los estudios incluidos
| Fase del estatus | Tipo de estudio | Año | Autor | Episodios de EE (n) | Tipo de estatus | Conclusión |
|---|---|---|---|---|---|---|
| Todas | Guía terapéutica | 2010 | Meierkord et al.9 | — | EEC, EENC, EE parcial | LZP o DZP i.v.+PTH (nivel de evidencia A) |
| Se recomienda retrasar la sedación en EE con crisis parciales complejas | ||||||
| Todas | Guía terapéutica | 2012 | Brophy et al.10 | — | EEC | LZP i.v. o MDZ i.m. (clase I, nivel de evidencia A) + VPA (nivel de evidencia A) |
| MDZ primera opción para coma terapéutico (clase IIa, nivel de evidenica B) | ||||||
| Todas | Guía terapéutica | 2016 | Mercadé Cerdá et al.11 | — | EEC, EENC, EE parcial | LZP o DZP i.v.+PTH o PB en EEC (nivel de evidencia IV) |
| Se recomienda retrasar la sedación en EENC | ||||||
| Fase I | Ensayo clínico aleatorizado doble ciego | 2012 | Silbergleit et al.12 | 893 | EEC | MDZ i.m. controla mayor número de crisis frente a LZP i.v. |
| Fase I | Metaanálisis | 2016 | Brigo et al.13 | 656 | EEC | LZP i.v. y DZP i.v. similar eficacia como primera línea de tratamiento |
| Fase II | Estudio retrospectivo | 2011 | Alvarez et al.14 | 187 | No especifica | LEV menos eficaz que PTH y VPA |
| Fase II | Estudio prospectivo aleatorizado controlado | 2015 | Mundlamuri et al.15 | 150 | EEC | PTH, VPA y LEV similar eficacia como segunda línea de tratamiento tras LZP |
| Fase II | Estudio prospectivo aleatorizado | 2015 | Chakravarthi et al.16 | 44 | No especifica | LEV similar eficacia a PTH en EE que persisten tras LZP |
| Fase II | Metaanálisis | 2014 | Yasiry y Shorvon17 | 798 | EEC | PTH es menos eficaz que VPA, PB y LEV |
| Fase II | Estudio prospectivo | 2015 | Atmaca et al.18 | 30 | EEC, EENC, EPC | LEV es bien tolerado y efectivo tanto en EE focal como generalizado |
| Fases I y II | Estudio retrospectivo | 2013 | Rantsch et al.19 | 167 | EEC, EENC, EPC | CLP es superior a DZP, MDZ, LEV y VPA en EEC generalizado, no existen diferencias en EENC y EPC |
| Fases I y II | Metaanálisis | 2014 | Prasad et al.20 | 2.755 | No especifica | LZP i.v. es mejor que DZP i.v. o PHT en el control del EE |
| En manejo prehospitalario, MDZ i.m. parece más efectivo que LZP i.v. en el control de crisis | ||||||
| Fase III | Estudio retrospectivo | 2013 | Höfler y Trinka21 | 136 | EEC, EENC, EE parcial | LCM puede ser una alternativa a los FAE clásicos en el tratamiento de segunda línea de un EE establecido |
| Fase III | Descripción de casos | 2013 | Hawkes et al.22 | 2 | EE parcial | LCM oral puede ser una opción terapéutica en EE parcial simple refractario |
| Fase III | Descripción de casos | 2013 | Spalletti et al.23 | 1 | EPC | LCM i.v. mejora un caso de EE parcial motor refractario |
| Fase III | Estudio retrospectivo | 2017 | Newey et al.24 | 84 | EEC, EENC | LCM i.v. parece una opción prometedora en el manejo de un EE |
| Fase III | Estudio retrospectivo | 2018 | Santamarina et al.25 | 165 | EEC, EENC | La respuesta a LCM es mejor en EE resistentes a benzodiacepinas y con dosis de carga >5,3mg/kg |
| Fase III | Estudio retrospectivo | 2015 | Redecker et al.26 | 10 | EEC, EENC, EE parcial | PER a dosis de 6mg en 10 EE refractarios favorece el cese de crisis en 2 a 6 episodios (dependiendo de distintos criterios de eficacia) |
| Fase III | Estudio prospectivo aleatorizado | 2018 | Masapu et al.27 | 23 | No especifica | Propofol similar a MDZ en control de crisis, complicaciones, estancia hospitalaria y mortalidad |
| Fase III | Estudio retrospectivo | 2015 | Marchi et al.28 | 467 | EEC, EENC, EE parcial | El coma terapéutico se asocia a peor pronóstico, especialmente en EE con crisis parciales complejas |
| Todas | Estudio retrospectivo | 2017 | De la Morena Vicente et al.29 | 84 | EE generalizado/EE parcial | No se encontraron diferencias en las secuelas o fallecimiento en función del tipo de estatus |
| Fase III | Cuestionario enviado a centros hospitalarios seleccionados de manera aleatoria | 2015 | Patel et al.30 | — | EEC | Solo 21 de los 75 hospitales evaluados tienen un protocolo terapéutico para EEC refractario en UCI en Reino Unido |
| Fases III y IV | Revisión | 2018 | Holtkamp31 | — | EEC generalizado, EE focal complejo | En EE focal complejo refractario deben administrarse FAE de segunda línea que no hayan sido administrados: LEV, PHT, VPA, LCM |
| Fases III y IV | Revisión | 2018 | Rai y Drislane32 | — | EEC generalizado, EE ausencias típicas, EE parcial complejo, EPC, EE mioclónico | En los EE distintos del EEC generalizado se recomiendan fármacos no sedantes: PHT, fosfenitoína, PB, VPA, LCM, LEV i.v.; TPM, CBZ entera |
| Todas | Revisión | 2017 | Trinka y Kälviäinen7 | — | No especifica | Un 40% de los pacientes con EE no responde a la administración precoz de benzodiacepinas. Destacan la importancia de determinar la causa del EE |
| Todas | Revisión | 2017 | Bauerschmidt et al.1 | — | No especifica | Refuerzan el uso precoz e intensivo de benzodiacepinas en fase I, y destacan los resultados de LCM i.v. en fase II y ketamina y clobazam en fase III |
| Todas | Revisión | 2017 | Zaccara et al.8 | — | EEC | Destacan la importancia de inicio rápido de tratamiento, las desventajas de PHT en fase II y las ventajas de MDZ en fase III |
| Todas | Descripción de casos | 2017 | Qiu et al.36 | 1 | EE afásico | Este caso mejoró con OXC. Los EE afásicos suelen tratarse con DZP y PHT por su frecuencia de uso |
| Todas | Revisión | 2016 | Mameniskiené y Wolf37 | — | EPC | El tratamiento de la EPC depende de la etiología. Suele ser farmacorresistente, los mejores resultados con TPM y LEV |
CBZ: carbamazepina; CLP: clonazepam; DZP: diazepam; EE: estatus epiléptico; EEC: estatus epiléptico convulsivo; EENC: estatus epiléptico no convulsivo; EPC: epilepsia parcial continua; FAE: fármaco antiepiléptico; i.m.: intramuscular; i.v.: intravenoso; LCM: lacosamida; LEV: levetiracetam; LZP: lorazepam; MDZ: midazolam; OXC: oxcarbazepina; PB: fenobarbital; PER: perampanel; PHT: fenitoína; TPM: topiramato; UCI: unidad de cuidados intensivos; VPA: valproato.
La más antigua es la guía europea, publicada en 20109. Esta guía recomienda en los EEC la administración de lorazepam (LZP) intravenoso (i.v.) (nivel de evidencia A) o, en los casos en que no esté disponible, diazepam (DZP) i.v. seguido de fenitoína (PHT) (nivel de evidencia A). No encuentran evidencia suficiente para incluir valproato (VPA) en la terapia de primera línea en estos EE. En los EE no convulsivos (EENC) [parciales complejos y sutiles] se establecen las mismas recomendaciones iniciales que en los EEC. En caso de que persista el EEC se recomienda infusión inmediata de anestésicos con manejo en una unidad de cuidados intensivos (UCI). En caso de que persista un EE con crisis parciales complejas se recomienda posponer en lo posible la sedación.
La última guía de la Sociedad Americana de Epilepsia fue publicada en 201210. Todas las recomendaciones van dirigidas a EEC, sin diferenciar entre origen generalizado o focal. En primera línea de tratamiento afirman que para la terapia i.v. se prefiere LZP (clase I, nivel de evidencia A) y que midazolam (MDZ) es el idóneo en la terapia intramuscular (i.m.), bucal o nasal (clase I, nivel de evidencia A). Respecto a la fase II, recomiendan VPA (clase IIa, nivel de evidencia A), PHT (clase IIa, nivel de evidencia B) o levetiracetam (LEV) (clase IIb, nivel de evidencia C). En fase III, los más recomendados son MDZ (clase IIa, nivel de evidencia B), propofol y pentobarbital (clase IIb, nivel de evidencia B).
El Grupo de Epilepsia de la Sociedad Española de Neurología (GE-SEN) elaboró durante el año 2012 las últimas guías oficiales para el diagnóstico y tratamiento de la epilepsia11. Sus recomendaciones terapéuticas para el EEC son iniciar LZP o DZP i.v. seguido de PHT o fenobarbital (PB) i.v. si no se controla con las primeras (nivel de evidencia IV). VPA, LEV o lacosamida (LCM) pueden emplearse si está contraindicada PHT, como alternativa a PB o en EE refractarios (nivel de evidencia III). En estos últimos el GE-SEN recomienda el uso de inductores del coma anestésico en función de la experiencia o los protocolos de la UCI correspondiente. En EENC especifican que los FAE de segunda línea deben elegirse teniendo en cuenta si se trata de un estatus de ausencias o de crisis parciales complejas: PHT, PB, VPA, LEV, LCM, lamotrigina (LTG) o topiramato (TPM), y en caso de refractariedad no recomiendan la terapia intensiva en pacientes sin coma profundo, por buen pronóstico.
Primera línea de tratamientoUn ensayo clínico12 que compara MDZ i.m. con LZP i.v. en EEC encuentra que MDZ controla las crisis en el 73,4% de los casos frente al 63,4% de LZP, aunque la desaparición de los síntomas comiciales ocurre antes tras la administración de LZP (1,6min vs. 3,3min).
Un metaanálisis13 compara LZP i.v. y DZP i.v. en EEC (generalizados o focales), sin encontrar diferencias estadísticamente significativas en el control de los síntomas comiciales ni en la persistencia del EE que requiera otro tipo de fármacos.
Segunda línea de tratamientoUn estudio retrospectivo14 compara PHT, VPA y LEV en EE (únicamente se especifica que se excluyen los postanóxicos), observando que LEV es significativamente menos eficaz que VPA y PHT. Sin embargo, un estudio prospectivo posterior que compara estos mismos FAE en EEC no encuentra diferencias estadísticamente significativas entre ellos (tasa de éxito del 68, 68 y 78%, respectivamente)15. Otro estudio prospectivo compara PHT y LEV en EE de tipo no especificado sin encontrar diferencias estadísticamente significativas ni en cuanto al control de crisis ni en cuanto a su recurrencia, efectos adversos o pronóstico funcional16.
Por otra parte, un metaanálisis17 que compara la efectividad de PHT, VPA, PB, LEV y LCM en EEC en los que habían fallado las benzodiacepinas encuentra que VPA presenta una tasa de control de las crisis del 75,7%, PB del 73,6% y LEV del 68,5%, mientras que PHT muestra la tasa más baja de eficacia con el 50,2%. No consiguen datos suficientes para valorar la eficacia de LCM.
El primer estudio prospectivo publicado sobre LEV i.v. como tratamiento del EE incluye EEC, EENC o epilepsia parcial continua (EPC), y evidencia que las crisis cedieron en el 76,6% de los pacientes18.
Primera y segunda líneas de tratamientoUn estudio retrospectivo que compara la eficacia de clonazepam (CLP), DZP, MDZ, LEV y VPA encuentra mayor eficacia de CLP frente a los demás en la supresión de EEC generalizados, mientras que no encuentra diferencias estadísticamente significativas en la supresión de EENC y EPC19.
Un metaanálisis que valora la efectividad y seguridad de diversos fármacos de primera y segunda línea comparándolos entre ellos o con placebo20 encuentra que LZP i.v. es mejor que DZP i.v. en el control de crisis y disminución del riesgo de prolongación del EE; en el manejo prehospitalario, MDZ i.m. es al menos igual de efectivo (probablemente más) que LZP i.v. en el cese de crisis y la frecuencia de hospitalización e ingreso en UCI; LZP i.v. es mejor que PHT i.v. en la reducción del riesgo de continuación del EE.
Tercera y cuarta líneas de tratamientoVarios artículos evalúan la eficacia de LCM en EE: una revisión que incluye EEC (19%), EENC (50%) y EE de origen parcial (31%)21 encuentra una tasa de éxito del 56%; la descripción de 2 casos de EE parcial simple refractario tratados satisfactoriamente con LCM oral (300mg)22; la descripción de un caso con EE focal motor refractario que mejora tras LCM i.v. (400mg)23; una revisión retrospectiva con el 59,5% de EENC observa un control de crisis en el 84,4% de los casos24; otro estudio retrospectivo reciente con un 52,7% de EENC encuentra que la respuesta a LCM es mayor si se han administrado benzodiacepinas previamente y si la dosis de carga es mayor de 5,3mg/kg25.
Un estudio encuentra que perampanel puede ser efectivo en EE refractarios tipo EENC, EPC y EE con crisis parciales complejas en los que previamente habían fallado una media de 5 FAE26.
Un estudio prospectivo evalúa la eficacia de propofol y MDZ en EE refractario y superrefractario (SR) sin especificar el tipo y no encuentra diferencias entre ambos fármacos27.
Una revisión retrospectiva que evalúa la evolución de pacientes con EE refractario generalizado o parcial28 encontró que el 51,1% volvió a su estado basal, el 34,6% tuvo un nuevo episodio o discapacidad, el 14,3% falleció y el 10,7% fueron manejados con coma terapéutico. Concluyen que el coma terapéutico se asocia a peor resultado después del EE y a un aumento notable de la prevalencia de infecciones y tiempo de hospitalización, siendo este efecto más importante en pacientes con crisis parciales complejas en comparación con EE generalizado convulsivo o no convulsivo en coma.
Otro estudio retrospectivo posterior que también evalúa la evolución de estos pacientes29 cuantifica los distintos tipos de EE: 47,6% tónico-clónico; 21,4% parcial complejo; 17,9% parcial motor; 6% parcial simple; 3,6% mioclónico y 3,6% sutil. Encuentran que el EE cedió en las siguientes fases: 13,1% precoz; 20,2% establecido; 41,7% refractario y 13,1% SR. El 11,9% falleció sin haberse controlado el estatus. Afirman que el ingreso en UCI y las complicaciones sistémicas fueron más frecuentes en los EE tónico-clónicos, pero no se encuentran diferencias en secuelas o fallecimiento según el tipo de estatus.
Se encontró una publicación que evidencia que de 75 centros hospitalarios evaluados de manera aleatoria en el Reino Unido solo 21 tenían un protocolo terapéutico para EEC en UCI. Además, dichos protocolos difieren significativamente entre ellos y carecen de información sobre cuál es el fármaco idóneo, su dosis y momento de administración, así como el intervalo de tiempo antes de iniciar la sedación. Esto favorece tanto un retraso en la eficacia del tratamiento como un riesgo potencialmente prevenible para los pacientes30.
Una revisión reciente sobre tratamiento farmacológico del EE refractario y SR especifica las pautas recomendadas en EE focal complejo y EEC generalizado refractarios. En el primero no se recomiendan anestésicos porque supondrían más complicaciones que las esperadas por el propio tipo de EE31. Esta misma recomendación se emite en otra revisión similar, en la que destaca la referencia a los distintos tipos de EE: por una parte, el EEC generalizado (y la forma «sutil» o no convulsiva que le sigue), y, por otra, los EE de ausencia típica, de crisis parciales complejas, la EPC o el EE mioclónico, en los que se recomienda ser menos agresivo32.
Revisiones sobre el tratamiento del estatus epiléptico en todas sus fasesSe encuentran 3 revisiones completas sobre el tema publicadas en 2017:
En la primera de ellas7 no se tiene en cuenta el tipo de EE en la esfera terapéutica, pero la mayoría de las recomendaciones se dirigen a EEC (fig. 1). En la fase inicial siguen recomendando por su eficacia la administración precoz de benzodiacepinas i.v. (LZP, DZP, CLP) o MDZ i.m. Sin embargo, encuentran que el 40% de los pacientes con EEC generalizado no responden a estos fármacos iniciales. Así, en la segunda fase de tratamiento recomiendan el uso de PHT, PB, VPA, LEV y LCM i.v. Ninguno de ellos ha demostrado un nivel de evidencia I para escogerlo frente a los demás7,12,33,34. En caso de EE refractario encuentran que el anestésico más usado es MDZ (59%), seguido de propofol (32%) y barbitúricos (8%). En los EE SR encuentran varios estudios en desarrollo que demuestran la eficacia de anestésicos como ketamina, o neuroesteroides como alopregnanolona.
La segunda revisión referida1 no evidencia diferencias significativas en cuanto a eficacia entre los distintos fármacos empleados en cada nivel de actuación, pero tampoco tiene en cuenta el tipo de EE. En la fase I insisten en la administración temprana e intensiva de benzodiacepinas, recomendando LZP i.v. si el acceso ya se ha establecido o MDZ i.m. en caso contrario. En la fase II resaltan el reciente apoyo que tiene LCM i.v. como terapia de control urgente para el tratamiento del EE parcial. En la fase III destacan el reciente uso de clobazam, ketamina y perampanel.
La última revisión de este grupo se centra en EEC8. Incide en que en la fase inicial la elección de un agente concreto es menos importante que el rápido tratamiento. No obstante, encuentran datos a favor de la efectividad de MDZ frente a LZP i.v. en adultos con EE sin acceso venoso establecido35. Por otra parte, resaltan la cuestionabilidad del uso de PHT basándose en las guías de práctica clínica más recientes y en metaanálisis que muestran su menor eficacia frente a otros FAE de segunda línea, teniendo en cuenta además su mala tolerabilidad y efectos adversos17. En cuanto a los fármacos de fase III, evidencian que MDZ parece ser el mejor tolerado y el más frecuentemente usado, seguido de propofol y tiopental (pentobarbital en EE.UU.).
Publicaciones sobre estatus epiléptico de origen conocido focalSolamente 2 artículos hacen referencia al tratamiento de algún tipo de EE de origen focal: uno describe un caso de EE afásico que mejora con oxcarbazepina (OXC)36 y otro es una revisión de la EPC que afirma que los mejores resultados farmacológicos se han observado con TPM y LEV37.
DiscusiónSi restringimos la búsqueda bibliográfica al tratamiento farmacológico del EE focal en los últimos 10 años, que es el objetivo de nuestro trabajo, encontramos relativamente pocas publicaciones (29). De todas ellas, solamente 3 tiene en cuenta si el estatus es focal o generalizado, y 4 se centran exclusivamente en pacientes con estatus focal. Siete publicaciones diferencian entre EEC o EENC y también especifican si incluyen episodios de crisis focales. Dos trabajos diferencian entre convulsivo y no convulsivo y 7 incluyen solo EEC. En 6 publicaciones no se especifica el tipo de EE de los pacientes incluidos. De los trabajos que incluyen distintos tipos de EE, solo 6 evalúan si la evolución de los pacientes difiere con un mismo tratamiento en función del tipo de estatus.
Aunque la mayoría de las publicaciones encontradas se concentran en los últimos 5 años, las guías terapéuticas vigentes no se han actualizado desde 2010 y 2012. Las recomendaciones de todas ellas tienen en cuenta en general si se trata de un EEC o de un EENC, aunque las guías española11 y europea9 hacen referencia a las crisis de origen focal: la primera recomienda tener en cuenta el tipo de crisis en los EENC para la elección del FAE de segunda línea y la segunda recomienda precaución en caso de sedación de pacientes con crisis parciales complejas.
En la primera fase de tratamiento existe un consenso general en que los fármacos más idóneos son las benzodiacepinas, pero ninguno de los estudios encontrados al respecto tiene en cuenta si el EE es focal o generalizado. Sí se encuentra un estudio que compara FAE de primera y segunda línea en EE generalizados y focales sin obtener diferencias estadísticamente significativas19.
En la fase II de tratamiento una publicación demuestra la eficacia de LEV en EE focales18 y varios estudios evidencian la eficacia de LCM en pacientes con EE refractarios de origen focal21-23, extendiéndose la recomendación de su uso cada vez más como segunda línea de tratamiento1,21. Otro fármaco de reciente aparición evaluado con éxito en el tratamiento de EE refractarios, incluidos focales, es perampanel26.
Cuando nos enfrentamos a un EE refractario que no ha respondido a la primera ni a la segunda línea de tratamiento, parece que se tiene aún menos en cuenta el tipo de EE a la hora de administrar sedación. De este modo, parece que no existe una respuesta clara a día de hoy sobre qué tipo de EE se beneficia más del coma terapéutico, o sobre cómo o cuándo debe procederse a la sedación en caso de estatus refractario, aunque los últimos estudios abogan por no inducir un coma en pacientes con EENC o focales en los que el pronóstico a priori podría ser mejor31,32.
Por tanto, la mayoría de los estudios sobre la eficacia de fármacos de primera, segunda o tercera línea en el tratamiento del EE no tienen en cuenta el tipo de estatus o, si lo tienen, diferencian fundamentalmente entre convulsivo y no convulsivo. Sin embargo, tanto los EEC como los EENC pueden tener un origen focal o generalizado. Este hecho podría constituir un factor pronóstico independiente y resultar un sesgo a la hora de valorar la eficacia de los FAE, justificando la gran variabilidad de conclusiones que se presentan en los distintos estudios.
Asimismo, en la mayoría de los estudios sobre pacientes, ensayos clínicos, guías estandarizadas o protocolos hospitalarios revisados se le da más importancia a la rapidez de instauración del tratamiento que al tipo de fármaco administrado.
Además, observamos que la práctica clínica diaria difiere mucho entre distintos hospitales, en función fundamentalmente de los fármacos disponibles y de la experiencia de cada centro. Es recomendable, con base en estos parámetros y en la evidencia disponible, elaborar protocolos hospitalarios específicos de cada grupo de trabajo para facilitar el manejo de esta situación de urgencia vital y reducir los intervalos de tiempo hasta la administración de cada fármaco, además de emplear las dosis adecuadas de los mismos.
En las publicaciones valoradas se pone de manifiesto que muchos estudios observacionales o ensayos clínicos que comparan distintos FAE en el manejo del EE cuentan con pocos pacientes, por lo que la evidencia encontrada para establecer recomendaciones terapéuticas en cuanto a efectividad, dosis, tolerabilidad o toxicidad de estos fármacos es escasa.
Teniendo en cuenta todo lo expuesto, en el momento actual no disponemos de suficiente evidencia científica para afirmar que el tratamiento farmacológico del EE focal debe ser distinto al del EE generalizado. Las recomendaciones terapéuticas que se podrían emitir en caso de tener la certeza de un origen focal no difieren de las establecidas para un EE generalizado en las fases I y II: inicialmente LZP o DZP i.v. si hay acceso venoso o MDZ i.m. en caso contrario, seguido de PTH, VPA, LEV o LCM i.v. si persisten las crisis. Lo único que podría cambiar en la actitud terapéutica sería retrasar en lo posible el inicio de terapia intensiva con fármacos anestésicos en caso de EE focales refractarios.
Son necesarios más ensayos aleatorizados controlados prospectivos con un amplio número de pacientes para identificar cuáles son los fármacos óptimos en cada tipo de estatus, y poder así establecer un protocolo terapéutico más o menos unificado para el manejo urgente de los EE. Hasta entonces, los datos de estudios observacionales y retrospectivos pueden sernos de utilidad.
FinanciaciónNo hubo financiación para este artículo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.