El manejo de la epilepsia durante la gestación requiere un control óptimo de las crisis, evitando los potenciales efectos teratogénicos del tratamiento antiepiléptico.
ObjetivosDescribir las características clínicas y los resultados perinatales de las pacientes con epilepsia gestantes. Analizar los factores que se asocian a la presencia de crisis durante la gestación. Describir los fármacos antiepilépticos más utilizados y analizar los cambios en el régimen terapéutico en dos periodos: de 2000-2010 y 2011-2018.
MétodosSe realizó un estudio prospectivo observacional de pacientes con epilepsia que notificaron su gestación en el periodo de 2000-2018. Se evaluó a las pacientes en el primer y segundo trimestre de gestación, tras el parto y al año. Se recogieron variables demográficas, relacionadas con la epilepsia, perinatales y obstétricas.
ResultadosSe incluyeron 101 gestaciones. La edad media fue de 32,6 años, el 55,4% tenía una epilepsia focal, el 38,6% una epilepsia generalizada y el 5,9% indeterminada. Se registraron 90 nacidos vivos, nueve abortos espontáneos y cinco malformaciones congénitas, cuatro de ellas en monoterapia con valproato. En 40 gestaciones (39,6%) se registraron crisis, siendo tónico-clónicas generalizadas en 16 (40%). Las variables asociadas con la presencia de crisis durante el embarazo fueron el mal control el año previo a la gestación (66,7% vs. 15,1%, p < 0,001), el tratamiento con dos o más fármacos antiepilépticos (30% vs. 14,8% p < 0,001) y no recibir tratamiento (25% vs. 0% p < 0,001). Los fármacos antiepilépticos más utilizados en monoterapia fueron lamotrigina (n = 19, 27,1%), valproato (n = 17, 24,2%) y levetiracetam (n = 12, 17,1%). En el periodo más reciente (2011-2018) se encontró una mayor proporción de monoterapias (81,5% vs. 55,3%), además de un descenso en el uso de carbamazepina (23,1% vs. 2,3%) y valproato (30,8% vs. 20,5%); y un aumento marcado de levetiracetam (0% vs. 27,3%).
ConclusionesLos factores asociados con la presencia de crisis durante la gestación fueron el mal control previo, el tratamiento con dos o más fármacos antiepilépticos y la ausencia de tratamiento. Los fármacos más utilizados fueron lamotrigina, valproato y levetiracetam, con un incremento de este último y un descenso de valproato en el periodo más reciente (2011-2018).
The management of epilepsy during pregnancy requires optimal seizure control, avoiding the potential teratogenic effects of antiepileptic drugs.
ObjectivesThis study aims to describe the clinical characteristics and perinatal outcomes of pregnant patients with epilepsy; to analyse the factors associated with seizures during pregnancy; to describe the most commonly used antiepileptic drugs in these patients; and to analyse changes in treatment regimens in 2 periods, 2000-2010 and 2011-2018.
MethodsWe conducted a prospective observational study of patients with epilepsy who reported their pregnancy between 2000 and 2018. Patients were evaluated in the first and second trimesters of pregnancy, after delivery, and at one year. Data were collected on demographic variables, epilepsy, and perinatal and obstetric variables.
ResultsA total of 101 pregnancies were included. Patients’ mean age was 32.6 years; 55.4% had focal epilepsy, 38.6% had generalised epilepsy, and 5.9% had undetermined epilepsy. We recorded 90 live births, 9 miscarriages, and 5 cases of congenital malformations, 4 of which were born to women who received valproate monotherapy. Forty patients (39.6%) presented seizures, with 16 (40%) presenting generalised tonic-clonic seizures. The variables associated with seizures during pregnancy were poor seizure control in the year prior to pregnancy (66.7% vs. 15.1%; P < .001), treatment with 2 or more antiepileptic drugs (30% vs. 14.8%; P < .001), and untreated epilepsy (25% vs. 0%; P < .001). The antiepileptic drugs most widely used in monotherapy were lamotrigine (n = 19; 27.1%), valproate (n = 17; 24.2%), and levetiracetam (n = 12; 17.1%). In the most recent period (2011-2018), we observed a greater proportion patients receiving monotherapy (81.5%, vs. 55.3%), as well as a decrease in the use of carbamazepine (2.3%, vs. 23.1%) and valproate (20.5%, vs. 30.8%); and a marked increase in the use of levetiracetam (27.3%, vs. 0%).
ConclusionsThe factors associated with the presence of seizures during pregnancy were previous poor seizure control, treatment with 2 or more antiepileptic drugs, and lack of treatment during pregnancy. The most commonly used drugs were lamotrigine, valproate, and levetiracetam, with an increase in levetiracetam use and a decrease in valproate use being observed in the later period (2011-2018).
La epilepsia es la enfermedad neurológica más frecuente que requiere tratamiento durante la gestación, afectando a un 0,5% del total de gestantes. La mayoría de las pacientes con epilepsia tiene un embarazo y un parto normales, pero se ha descrito un mayor riesgo de complicaciones durante la gestación1. Las crisis durante el embarazo se han asociado a un mayor riesgo de bajo peso del recién nacido, parto pretérmino y de ser pequeño para la edad gestacional (PEG), término pediátrico que se refiere a un recién nacido cuyo peso y/o longitud se encuentran dos o más desviaciones estándar (DE) por debajo de la media establecida para su población de referencia, su sexo y su edad gestacional2–8. Por otro lado, los fármacos antiepilépticos (FAE) pueden producir teratogenicidad no sólo a nivel morfológico sino también neurocognitivo9–12. El fármaco antiepiléptico más teratogénico es el valproato, con una prevalencia de malformaciones congénitas mayores del 10%, siendo dosis dependiente. La politerapia también supone un mayor riesgo, especialmente si incluye valproato. Esto ha hecho que el patrón de utilización de los fármacos antiepilépticos haya cambiado en los últimos años13,14.
En cuanto a los factores asociados a crisis durante la gestación se ha descrito que la presencia de al menos una crisis en el año previo a la concepción, las crisis focales y la politerapia se comportan como predictores de crisis durante la gestación15–17.
La mayoría de información respecto a la evolución de la gestación en mujeres con epilepsia proviene de registros de pacientes bajo tratamiento con fármacos antiepilépticos, existen pocos trabajos de pacientes a las que se les ha retirado el tratamiento antiepiléptico por buen control18. En nuestro trabajo describimos los resultados perinatales y la presencia de crisis durante la gestación de pacientes con epilepsia tratadas y no tratadas con fármacos antiepilépticos; analizamos los factores asociados con la presencia de crisis y describimos los fármacos antiepilépticos más utilizados, analizando los cambios en el régimen terapéutico en dos periodos: de 2000 a 2010 y de 2011 a 2018.
MétodosSe realizó un registro observacional y prospectivo de las pacientes con epilepsia gestantes seguidas en la unidad de epilepsia de un hospital terciario durante el periodo 2000-2018, según el protocolo del registro EURAP en el que participa el centro. Se realizaron entrevistas en el primer (notificación de embarazo) y segundo trimestres, tras el parto y al año de seguimiento. También se incluyeron pacientes no tratadas. Se recogieron variables demográficas, relacionadas con la epilepsia (tipo, etiología, presencia de crisis tónico-clónicas generalizadas y de otros tipos durante la gestación, tratamiento farmacológico realizado), obstétricas (hallazgos ecográficos, complicaciones durante la gestación, tratamiento con ácido fólico, tipo de parto), del recién nacido (sexo, peso, perímetro cefálico, longitud, Apgar, presencia de malformaciones congénitas mayores hasta el año de vida) y de otras variables de riesgo de malformación congénita (consumo de otros fármacos, tabaco, alcohol, antecedentes familiares de malformaciones congénitas mayores). De forma retrospectiva, se revisó el control previo de las crisis el año previo a la gestación. Se definió como pacientes mal controladas el haber tenido al menos una crisis epiléptica el año previo a la concepción y bien controladas las pacientes sin crisis el año previo a la concepción.
Para el cálculo de la prevalencia de malformaciones congénitas se excluyeron las pacientes con abortos espontáneos e interrupciones voluntarias del embarazo por causas que no fueran malformaciones congénitas mayores, y las que todavía no habían completado el año de seguimiento tras el parto.
Análisis estadísticoPara el análisis de las variables asociadas con la presencia de crisis durante la gestación, se utilizaron las pruebas de X2 para variables categóricas y t Student /Wilcoxon para variables continuas. Se consideró significación estadística si p < 0,05. Se utilizó el paquete estadístico SPSS versión 21 IL Chicago.
ResultadosCaracterísticas de la muestra:Se registraron 101 gestaciones de 76 mujeres distintas, que notificaron su embarazo en el periodo 2000-2018. Hubo 57 mujeres con un embarazo, 14 con dos embarazos, 4 con 3 embarazos y una con cuatro embarazos. Del total de gestaciones, 96 han completado el seguimiento de un año tras el parto. Las características basales de la muestra se reflejan en la tabla 1.
Características basales de la muestra
| Edad (concepción) | 32,6 ± 5,1 años |
| Tipo epilepsia | Focal 56 (55,4%)Generalizada 39 (38,6%)Indeterminada 6 (5,9%) |
| Ausencia crisis año previo a la gestación | 58 (57,4%) |
| Consumo de tabaco | 20 (19,8%) |
| Consumo de alcohol | 1 (1%) |
| Tratamiento adecuado ácido fólico | 34 (33,7%) |
| Antecedentes familiares malformaciones congénitas | 4 (4%) |
Se registraron 101 gestaciones, de las cuales 88 finalizaron con éxito dando lugar a 90 nacidos vivos (dos fueron gemelares y 86 únicas. De las 13 gestaciones restantes, se registraron nueve abortos espontáneos (9,3%) y cuatro interrupciones del embarazo (3,96%) (tres por malformaciones detectadas a nivel prenatal y una por un retraso de crecimiento intrauterino severo). Hubo 38 partos eutócicos (43,2%), 38 cesáreas (43,2%) y 11 partos instrumentalizados (12,5%). Todos los partos fueron a término excepto seis prematuros (6,8%). La media de peso al nacer fue de 3.169,5 ± 486,5 g.
En las gestaciones con un mínimo de seguimiento de un año (n = 96) y tras haber excluido los abortos espontáneos (n = 9) y una interrupción voluntaria del embarazo no debida a malformación (n = 86), se detectaron cinco malformaciones congénitas (5,81%), que se describen en la tabla 2. En cuatro casos, la madre recibía tratamiento con valproato en monoterapia, con una dosis media de 1.000 mg/día. El quinto caso recibía un biterapia de levetiracetam y carbamazepina. La prevalencia de malformaciones congénitas mayores4 fue del 23,5% en las tratadas con valproato (n = 17, tras excluir abortos espontáneos).
Malformaciones congénitas mayores
| Edad materna (años) | Descripción malformación | Tratamiento | Dosis (mg) | Antecedentes familiares MCM | Detección | |
|---|---|---|---|---|---|---|
| Paciente 1 | 34 | Siameses unidos por el tórax | Valproato | 1000 | No | Prenatal(12 sg) |
| Paciente 2 | 29 | Espina bífida, hidrocefalia | Valproato | 900 | No | Prenatal(20 sg) |
| Paciente 3 | 40 | Comunicación interventricular, estenosis aórtica leve | Valproato | 1300 | No | 0 meses |
| Paciente 4 | 29 | Craneosinostosis | Valproato | 800 | No | 6 meses |
| Paciente 5 | 30 | Acráneo | Carmazepina/levetiracetam | 400/1000 | No | Prenal(13 sg) |
En 40 gestaciones (39,6%) se registraron crisis, siendo tónico-clónicas generalizadas en 16 de ellas (40%). Una paciente presentó un estatus de ausencias peri-parto, con buena respuesta al tratamiento farmacológico y sin complicaciones para el recién nacido.
La tabla 3 muestra los factores asociados a la presencia de crisis epilépticas durante el embarazo.
Factores asociados con la presencia de crisis durante la gestación
| No crisis (n = 61) | Crisis (n = 40) | p | |
|---|---|---|---|
| Edad materna | 32,6 ± 5,1 años | 32,5 ± 5,2 años | 0,87 |
| Tipo epilepsia | |||
| Focal | 29 (47,5%) | 27 (67,5%) | |
| Generalizada | 28 (45,9%) | 11 (27,5%) | 0,14 |
| Indeterminada | 4 (6,6%) | 2 (5%) | |
| Peor control (>1 crisis año previo) | 8 (15,1%) | 24 (66,7%) | <0,001 |
| Tratamiento | |||
| Monoterapia | 52 (85,2%) | 18 (45%) | |
| >2 FAES | 9 (14,8%) | 12 (30%) | <0,001 |
| No tratamiento | 0 (0%) | 10 (25%) | |
| Monoterapia valproato | 12 (19,7%) | 5 (12,5%) | 0,42 |
| Monoterapia lamotrigina | 15 (24,6%) | 4 (10%) | 0,07 |
| Monoterapia levetiracetam | 10 (16,4%) | 2 (5%) | 0,12 |
| Aborto | 7 (11,5%) | 2 (5%) | 0,31 |
La presencia de crisis durante la gestación se asoció de forma significativa con el mal control de la epilepsia el año previo a la concepción. Tuvieron crisis durante el embarazo el 75% de las pacientes mal controladas (al menos una crisis el año previo a la concepción) y sólo el 25% de las pacientes bien controladas previamente (sin crisis el año previo) (RR 11,25% IC:4,05-31,28, p < 0,001).
El tratamiento con dos o más fármacos antiepilépticos y la ausencia de tratamiento se asociaron de forma significativa con la presencia de crisis durante la gestación. El 57,1% de las gestaciones de pacientes tratadas con dos o más fármacos antiepilépticos presentaron crisis durante la gestación, en comparación con sólo el 27,5% de las pacientes en monoterapia (p < 0,001). Todas las pacientes no tratadas con fármacos antiepilépticos tuvieron crisis durante el embarazo. De las 10 pacientes no tratadas con fármacos antiepilépticos, seis eran pacientes con epilepsia bien controlada a las que se les había retirado el tratamiento por buen control, con un periodo libre de crisis de tres a nueve años y sin tratamiento de cuatro meses a seis años. En cuatro pacientes la epilepsia debutó durante la gestación. Las características de las pacientes sin tratamiento antiepiléptico se detallan en la tabla 4.
Características de las pacientes sin tratamiento antiepiléptico en la concepción
| Edad materna (años) | Debut gestación | Tipo epilepsia/etiología | Tiempo sin crisis | Tiempo sin tratamiento | MCM | Aborto | Complicación obstétrica | Conducta | |
|---|---|---|---|---|---|---|---|---|---|
| Paciente 1 | 31 | No | Focal criptogénica | 4 años | 5 meses | No | No | No | Inicio LMT tercer trimestre |
| Paciente 2 | 38 | Sí | Indeterminada | No | No | No | Inicio CBZ segundo trimestre | ||
| Paciente 3 | 35 | Sí | Focal criptogénica | No | No | No | Inicio LMT segundo trimestre | ||
| Paciente 4 | 38 | Sí | Focal sintomática (displasia cortical) | No | No | No | Inicio LEV segundo trimestre | ||
| Paciente 5 | 29 | No | Focal criptogénica | 3 años | 4 meses | No | No | No | Inicio LMT segundo trimestre |
| Paciente 6 | 39 | No | Focal criptogénica | 9 años | 6 años | No | No | No | Inicio CBZ tercer trismestre |
| Paciente 7 | 27 | No | Focal criptogénica | 7 años | Desconocido | No | No | No | Inicio VPA tras parto |
| Paciente 8 | 31 | No | Focal criptogénica | 4 años | 3 años | No | No | No | Inicio OXC |
| Paciente 9 | 37 | No | Focal sintomática (esclerosis múltiple) | 4 años | 2 años | No | No | No | Inicio LEV tercer trimestre |
| Paciente 10 | 2 | Sí | Focal criptogénica | No | No | DPP | Inicio LEV segundo trimestre |
DPP: Desprendimiento prematuro de placenta. LMT: Lamotrigina. CBZ: Carbamazepina. LEV: Levetiracetam. OXC: Oxcarbazepina. VPA: Valproato.
El tipo de epilepsia no se asoció a la presencia de crisis durante la gestación. No se objetivó que la monoterapia con un determinado fármaco antiepiléptico se asociara a un peor control de crisis. Tampoco encontramos una asociación entre la presencia de crisis y variables perinatales como la prematuridad, el peso del recién nacido o el tipo de parto.
Tratamiento farmacológicoSe registraron 91 gestaciones bajo tratamiento antiepiléptico (90,1%), 70 (69,3%) en monoterapia y 21 (20,8%) en tratamiento con dos o más fármacos antiepilépticos. Las 10 restantes no recibían tratamiento (9,9%) en la concepción, en nueve de ellas se inició tratamiento antiepiléptico a partir del segundo trimestre.
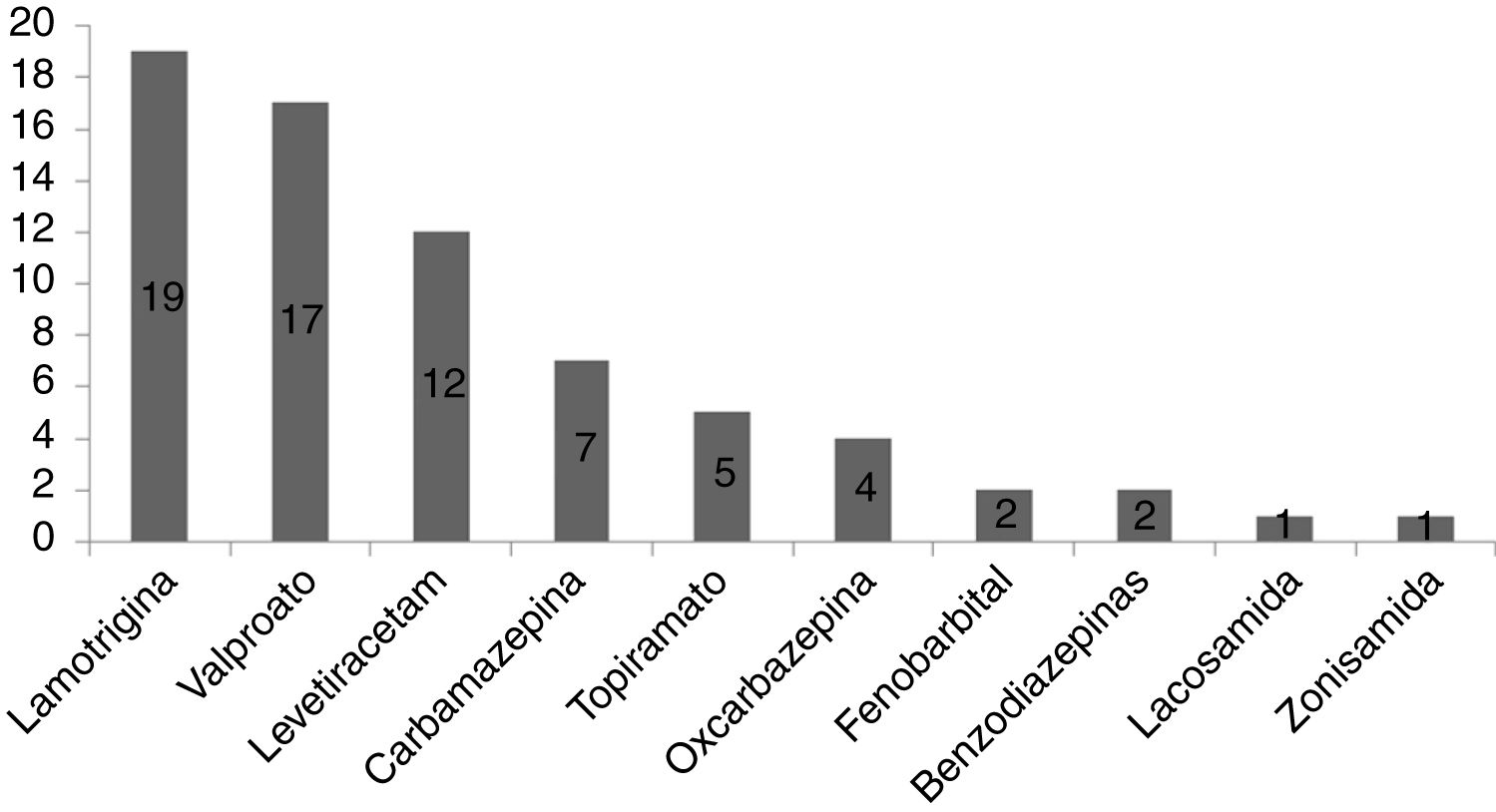
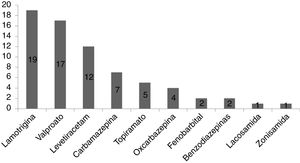
El fármaco más utilizado en monoterapia fue lamotrigina, seguido de valproato y levetiracetam, según muestra la figura 1.
La dosis media diaria de lamotrigina en monoterapia fue de 159,2 ± 65,2 mg, la de valproato de 811,76 ± 323,81 mg y la de levetiracetam de 1145,8 ± 405,34 mg.
En cuanto al tratamiento con dos o más fármacos antiepilépticos (n = 21), había cinco pacientes en tratamiento con tres fármacos antiepilépticos, una de ellas, además, con un estimulador del nervio vago. Las 16 restantes recibían tratamiento con biterapia, las más frecuentemente empleadas fueron topiramato con levetiracetam (n = 3) y vaproato con lamotrigina (n = 2).
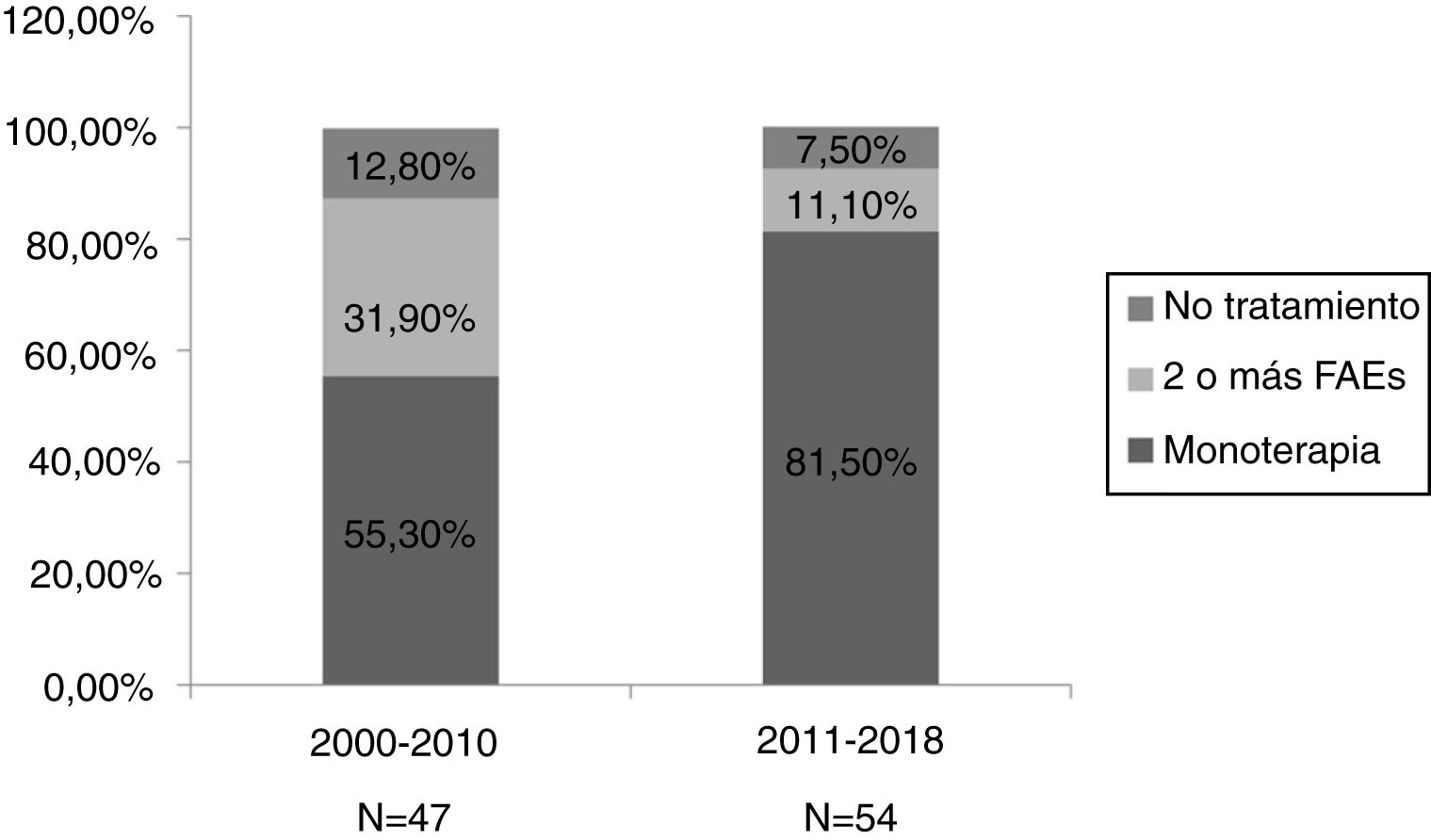
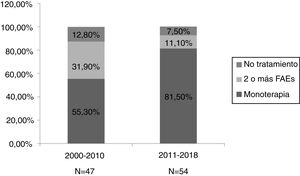
Dividimos la muestra en dos periodos, de 2000 a 2010 (n = 47) y de 2011 a 2018 (n = 54). Objetivamos que en el segundo periodo había una mayor proporción de monoterapias (81,5% vs. 55,3%) y menor de politerapias (11,1% vs. 31,9%) respecto al primer periodo. La figura 2 muestra los resultados. No se encontraron diferencias significativas entre ambos periodos en otras variables como la presencia de crisis durante la gestación, aborto, malformaciones congénitas mayores o prematuridad.
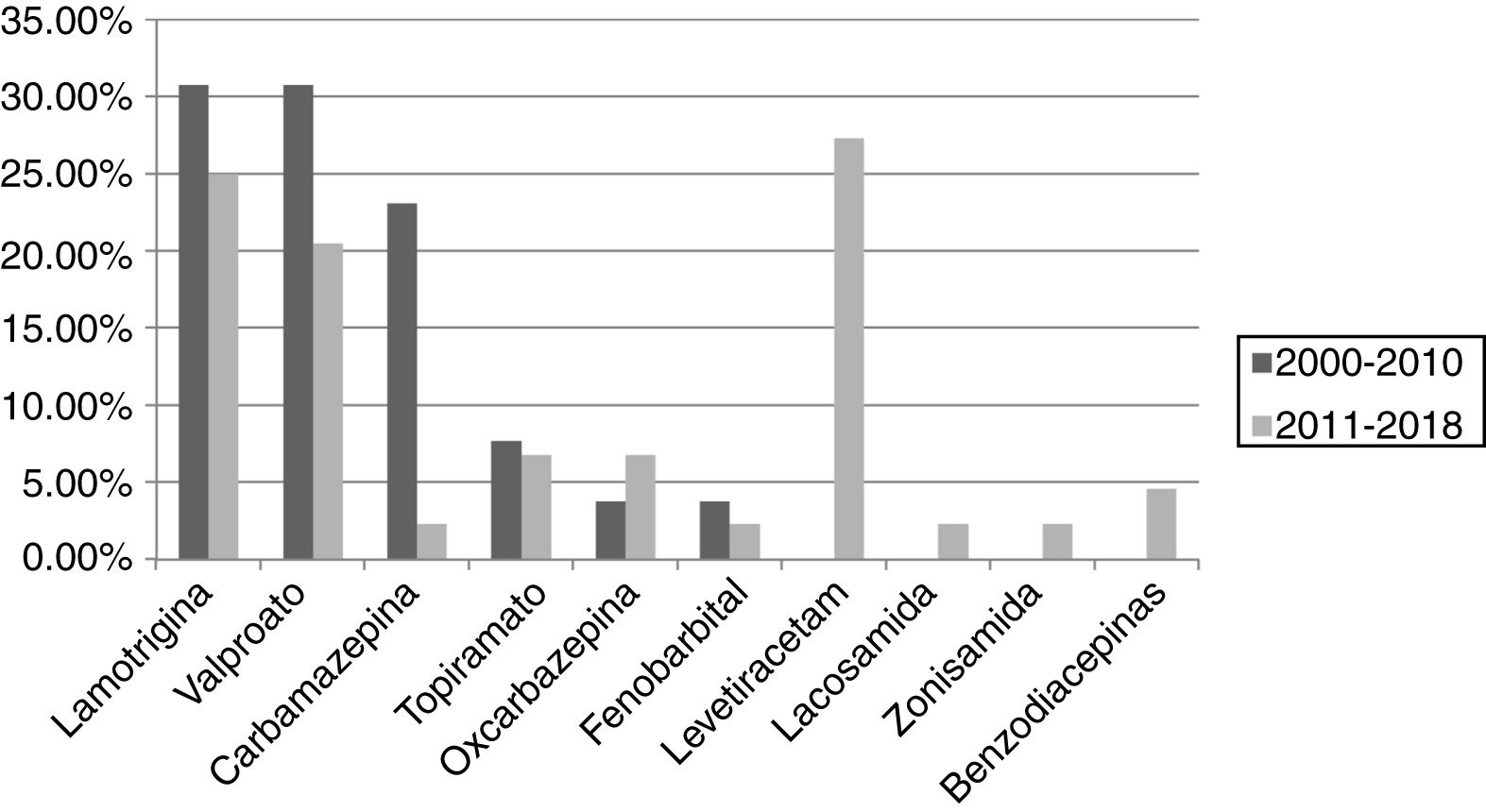
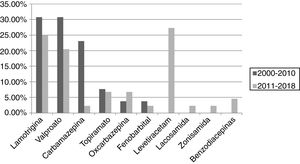
Los fármacos antiepilépticos más utilizados en monoterapia fueron lamotrigina y valproato en el primer periodo (30,8%), y levetiracetam (27,3%) y lamotrigina (25%) en el segundo. Se objetivó un descenso en el uso de carbamazepina (23,1% vs. 2,3%) y de valproato (30,8% vs. 20,5%) en el segundo periodo respecto al primero; así como un incremento marcado de levetiracetam (0% vs. 27,3%) y en menor medida de oxcarbazepina (3,8% vs. 6,8%). Lamotrigina se mantiene observando sólo un ligero descenso (30,8% vs. 25%). Los resultados se muestran en la figura 3.
DiscusiónLa mayoría de las pacientes tuvieron un embarazo sin complicaciones. Se encontró una tasa de abortos espontáneos del 8,9%, que es similar a la de la población general y una tasa de malformaciones congénitas mayores del 5,81%, superior a la de la población general (2% a 3%). Cuatro de las cinco malformaciones congénitas mayores aparecieron en madres que realizaban tratamiento con valproato en monoterapia, con una dosis media de 1.000 mg/día, lo que supone un 23,5% de las pacientes tratadas con valproato. Este resultado es concordante, incluso superior, con los datos publicados en la literatura sobre la teratogenicidad del valproato10–12.
Los factores asociados con crisis durante el embarazo fueron la presencia de al menos una crisis el año previo a la concepción, el tratamiento con dos o más fármacos antiepilépticos y no recibir tratamiento en la concepción. Las pacientes que presentaron al menos una crisis el año previo a la concepción tenían un riesgo 11 veces mayor de presentar crisis durante el embarazo. El tratamiento con dos o más fármacos antiepilépticos se asoció también a un mayor riesgo de crisis durante la gestación, 62,5% en comparación con el 30,5% de las pacientes en monoterapia; probablemente explicado porque la mayoría de las pacientes que recibían este régimen terapéutico habían presentado alguna crisis el año previo al embarazo. Estos resultados coinciden con otros trabajos publicados en la literatura. En un estudio observacional prospectivo de 1.297 pacientes gestantes con epilepsia, Sanjeev et al.15 encontraron que la presencia de al menos una crisis en el mes previo a la concepción (OR 15, 9-25), la politerapia (OR 2,8, 2,3-3,9) y la presencia de crisis focales (OR 1,6, 2-2) fueron factores predictores de crisis durante la gestación.
Hay poca información sobre las pacientes con epilepsia embarazadas que no reciben tratamiento antiepiléptico. En nuestra muestra, las seis pacientes a las que se les había retirado el tratamiento antiepiléptico por el buen control previo tuvieron crisis durante la gestación. Estos hallazgos también los reportan Vajda et al.18 en una cohorte de 148 pacientes no tratadas vs. 1.532 tratadas del registro australiano de embarazo. En este trabajo, el 56,1% de las no tratadas y el 46,9% de las tratadas tuvieron crisis durante la gestación. La probabilidad de crisis durante la gestación en las pacientes no tratadas no dependía del tiempo que llevaran sin tratamiento, sino con que su epilepsia estuviera activa o inactiva. En nuestro caso, las seis pacientes estaban libres de crisis previamente, y a pesar de ello, presentaron crisis durante la gestación. Por estos motivos, ante una planificación de embarazo, parece recomendable mantener el tratamiento antiepiléptico en monoterapia evitando los fármacos con mayor riesgo teratogénico.
Varios trabajos han reportado que la presencia de crisis2–5, especialmente tónico-clónicas generalizadas, durante el embarazo se ha asociado con mayor riesgo de parto pretérmino, bajo peso y recién nacido pequeño para la edad gestacional. En nuestro trabajo no encontramos esa asociación, probablemente por el reducido tamaño muestral.
En cuanto al tratamiento farmacológico, se encontró una mayor proporción de pacientes en monoterapia en los últimos años, lo que sugiere una mejor planificación de la gestación. Además, como en otros trabajos13,14, constatamos un incremento marcado en la utilización de fármacos nuevos y de bajo riesgo teratogénico como levetiracetam y en menor medida oxcarbazepina, y una reducción en el uso de carbamazepina y de valproato. A pesar de que lamotrigina sigue siendo el fármaco más utilizado junto con levetiracetam en los últimos años, su uso se ha reducido ligeramente.
Las limitaciones de nuestro trabajo son el reducido tamaño muestral y que es unicéntrico.
Las conclusiones de nuestro trabajo son las siguientes:
- •
En nuestra serie se confirman los efectos teratogénicos de valproato, incluso con una prevalencia superior a la descrita en la literatura.
- •
En el 39,6% de las gestaciones se registraron crisis. Los factores que se asociaron de forma significativa a la presencia de crisis fueron el mal control previo, el tratamiento con dos o más fármacos antiepilépticos y la ausencia de tratamiento.
- •
Los fármacos más utilizados fueron lamotrigina, valproato y levetiracetam.
- •
En el periodo más reciente (2011-2018),se objetivó una mayor proporción de monoterapias respecto al periodo anterior, además de un descenso en el uso de carbamazepina y valproato y un aumento de levetiracetam y en menor medida de oxcarbazepina.
El manejo de la paciente gestante con epilepsia es complejo; se debe conseguir el control óptimo de las crisis, evitando los posibles efectos teratogénicos en el feto. Las recomendaciones actuales son planificar la gestación y mantener una monoterapia a la dosis mínima eficaz con un fármaco antiepiléptico de bajo riesgo teratogénico como lamotrigina o levetiracetam. Según nuestra experiencia, es preferible no retirar el tratamiento en las pacientes bien controladas, por la alta probabilidad de presentar crisis durante la gestación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.