El número de personas que consultan presentando quejas cognitivas se ha visto incrementado de manera notable durante los últimos años, siendo el aumento en la esperanza de vida de la población una de las principales causas. La realización de una evaluación cognitiva resulta fundamental para la detección de los casos de demencia y para poder precisar el diagnóstico diferencial1. De ella dependerán importantes decisiones que influirán en el nivel de calidad de vida tanto del paciente como de su entorno.
La posibilidad de disponer de pruebas de cribado cognitivo de rápida aplicación resulta de especial utilidad en un sistema de salud con largas listas de espera, donde los recursos impiden la realización de pruebas neuropsicológicas más exhaustivas por parte de especialistas.
El test Addenbrooke's Cognitive Examination-III (ACE-III)2 ha sido recientemente validado al castellano3. Tanto la actual como en sus versiones anteriores son herramientas ampliamente utilizadas en unidades de memoria y centros de investigación para la demencia alrededor de todo el mundo4. Destaca por su capacidad para detectar y diferenciar entre subtipos de demencia5. Sin embargo, se queda fuera del alcance de muchos entornos clínicos al requerir su administración de unos 15-20min.
Con el objetivo de crear una versión reducida de la ACE-III, Hsieh et al. han validado el Mini-Addenbrooke's Cognitive Examination (M-ACE)6, acortando la escala original a través del sistema de escalado «Mokken»7 y aplicándose a pacientes con demencia tipo Alzheimer y frontotemporal, además de a controles sanos, empleando el Minimental State Examination (MMSE) como gold standard8.
El M-ACE consta de 5 elementos (orientación temporal, fluencia semántica, dibujo de un reloj, memoria inmediata y memoria diferida) con un máximo de 30 puntos, y un tiempo de administración de unos 5min. En el estudio de validación original un resultado ≤25/30 se identificó como la puntuación de corte para demencia con una alta sensibilidad (85%) y especificidad (87%). El M-ACE resultó más sensible que el MMSE y con menor «efecto techo».
Empleando la misma metodología planteada por el grupo australiano y aprovechando la completa muestra recientemente recogida en el trabajo de validación al castellano de la ACE-III hemos estudiado las propiedades psicométricas de esta nueva versión de la escala en nuestra población.
Del total de ítems de la escala original se seleccionaron aquellos que conforman la M-ACE y se generó una nueva puntuación. De los 175 casos incluidos, 92 fueron controles cognitivamente sanos (77,0±6,4 años de edad y 8,4±5,8 años de educación) y 83 casos patológicos (78,4±6,8 años de edad y 7,4±4,7 años de educación) con diferentes diagnósticos de demencia en estadio leve: enfermedad de Alzheimer (46 casos, 55,4%), demencia vascular (4 casos, 4,8%), demencia mixta (9 casos, 10,8%), demencia asociada a enfermedad de Parkinson (11 casos, 13,3%), demencia con cuerpos de Lewy (6 casos, 7,2%), demencia frontotemporal (5 casos, 6%), demencia alcohólica (un caso, 1,2%) y parkinsonismo atípico con demencia (un caso, 1,2%). Todos los participantes tenían 65 años o más y fueron reclutados en los Servicios de Neurología del Hospital Clínico San Carlos de Madrid y del Hospital de la Santa Creu i Sant Pau de Barcelona.
Se observa que con respecto a la inglesa la muestra española es significativamente más longeva y con menor nivel educativo. En el análisis de fiabilidad la escala presentó una elevada consistencia interna (α de Cronbach=0,828).
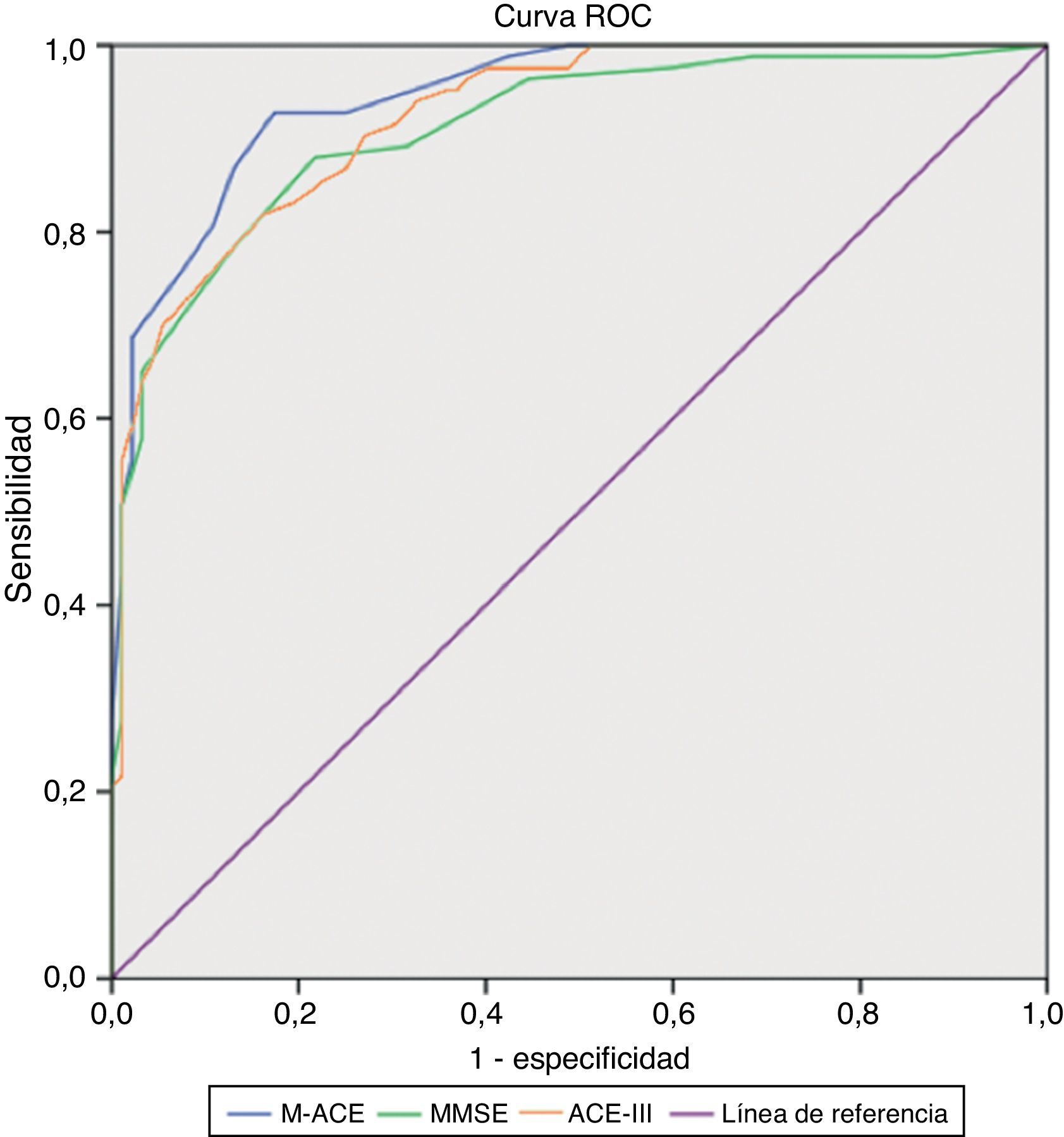
La puntuaciones obtenidas en el M-ACE fueron comparadas con las de las escalas ACE-III y MMSE, empleando el diagnóstico clínico de demencia como factor para encontrar puntuaciones de corte (fig. 1). Con un área bajo la curva (AUC)=0,94 una puntuación en la M-ACE≤16/30 se identificó como el punto de corte para demencia con un alto nivel de sensibilidad (86,7%) y especificidad (87,0%). Esto implica que el M-ACE logra una relación de índices de discriminación mejor que el MMSE (AUC=0,91; puntuación ≤24/30; SEN=88,0; ESP=78,3) y que el ACE-III (AUC=0,92; puntuación ≤65/100; SEN=83,1; ESP=80,4) (tabla 1).
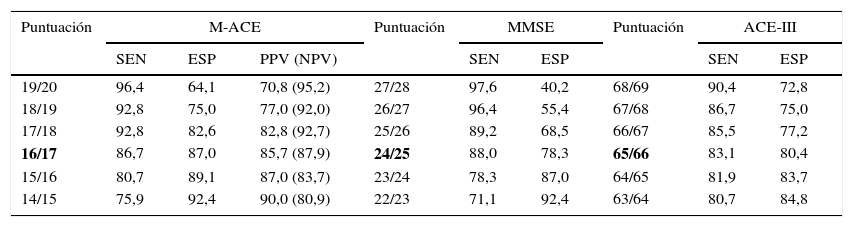
Puntos de corte para el diagnóstico de demencia leve
| Puntuación | M-ACE | Puntuación | MMSE | Puntuación | ACE-III | ||||
|---|---|---|---|---|---|---|---|---|---|
| SEN | ESP | PPV (NPV) | SEN | ESP | SEN | ESP | |||
| 19/20 | 96,4 | 64,1 | 70,8 (95,2) | 27/28 | 97,6 | 40,2 | 68/69 | 90,4 | 72,8 |
| 18/19 | 92,8 | 75,0 | 77,0 (92,0) | 26/27 | 96,4 | 55,4 | 67/68 | 86,7 | 75,0 |
| 17/18 | 92,8 | 82,6 | 82,8 (92,7) | 25/26 | 89,2 | 68,5 | 66/67 | 85,5 | 77,2 |
| 16/17 | 86,7 | 87,0 | 85,7 (87,9) | 24/25 | 88,0 | 78,3 | 65/66 | 83,1 | 80,4 |
| 15/16 | 80,7 | 89,1 | 87,0 (83,7) | 23/24 | 78,3 | 87,0 | 64/65 | 81,9 | 83,7 |
| 14/15 | 75,9 | 92,4 | 90,0 (80,9) | 22/23 | 71,1 | 92,4 | 63/64 | 80,7 | 84,8 |
En negrita aparece el punto de corte considerado óptimo.
ESP: especificidad; NPV: valor predictivo negativo; PPV: valor predictivo positivo; SEN: sensibilidad.
La capacidad diagnóstica de la M-ACE fue elevada, con valores superiores al 85% de discriminación entre controles sanos y sujetos con demencia leve. El punto de corte óptimo se situó en 16,5, aunque probablemente sería recomendable escoger otro ligeramente mayor (17,5) para alcanzar una mayor sensibilidad, que es el objetivo principal de un test de cribado. Este punto de corte se encuentra por debajo del de 25, que es el propuesto en el estudio de la versión inglesa, pero que solo incluía pacientes con demencia tipo Alzheimer y frontotemporal, y que fue desarrollado en poblaciones de menor edad y con más años de escolarización.
En conclusión, nuestro estudio constituye la primera aproximación española a la escala M-ACE y demuestra su utilidad como herramienta de cribado cognitivo. El breve periodo de tiempo requerido para la administración del M-ACE sugiere la posibilidad de generalizar de su uso a ámbitos de mayor presión asistencial o menor especialización. Por otra parte, la mayor sensibilidad y especificidad respecto al test ACE-III apoya el uso de la puntuación del M-ACE en los casos en que se administre el test original completo. Esto a su vez sugiere una posible doble función del ACE-III en la evaluación neuropsicológica: por un lado, como herramienta de cribado, especialmente con el M-ACE; y por otro, como herramienta de evaluación neuropsicológica general breve, con los diferentes dominios incluidos en el ACE-III (atención, lenguaje, memoria, fluencia verbal y visuoespacial).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.