Introducción
Los trastornos funcionales digestivos (TFD) son un grupo heterogéneo de síndromes caracterizados por múltiples síntomas gastrointestinales sin una causa orgánica obvia1 y relacionados con trastornos de la motilidad gastrointestinal y de la sensibilidad visceral.2 El síndrome de intestino irritable (SII) es uno de los más frecuentes. El nombre clínico de este síndrome se utiliza poco en la población mexicana general y en su lugar se distinguen múltiples sinónimos que médicos y pacientes usan de manera coloquial, como "colitis", "colitis espástica", "colitis nerviosa" y "colitis funcional", entre otros.
Definición y epidemiología
El SII es un trastorno funcional crónico y recurrente caracterizado por dolor y distensión abdominales, y cambios en el patrón evacuatorio.3 Es muy frecuente en la población general y constituye una de las primeras causas de consulta a medicina general y gastroenterología.4 Aunque su prevalencia varía de acuerdo con la población estudiada y los criterios diagnósticos utilizados, en general va de 10 a 20% de la población general,5 con predominio del sexo femenino (relación mujer/hombre 2:1); se relaciona con disminución importante de la calidad de vida y altos costos de la atención médica.6 Con base en los criterios de Roma II (véase más adelante), la prevalencia de SII en la población general mexicana urbana puede ser tan alta como 35%.7 En una revisión sistemática realizada entre 1996 y 2000 se encontró que en México la enfermedad es similar a lo publicado en la bibliografía internacional con respecto a su prevalencia y comportamiento clínico.8
Múltiples factores psicosociales determinan la conducta de las personas para buscar o no atención médica, lo que influye en la prevalencia de SII diagnosticado.9 Cerca de dos terceras partes de las personas con SII no consultan y algunos de los que sí lo hacen reciben otro diagnóstico.
El SII es un problema con altos costos de salud; sólo en Estados Unidos consume más de 20 000 millones de dólares en gastos directos e indirectos,10 se relaciona con una disminución importante en la calidad de vida (QOL) y reduce la productividad laboral. Su impacto en la QOL es equiparable al de trastornos como diabetes, hipertensión arterial y enfermedad renal crónica.
Criterios diagnósticos
En el intento de simplificar y estandarizar el diagnóstico de SII, a lo largo de los años se han descrito múltiples criterios diagnósticos basados en síntomas (Cuadro 1). Los primeros que se utilizaron fueron los criterios de Manning, publicados en 1976.11 Si bien son los más evaluados porque tienen más tiempo en la arena clínica, su valor predictivo positivo no excede 75%, con una sensibilidad de 78% y una especificidad de 72%. En 1998, durante el XIII Congreso Internacional de Gastroenterología se creó un comité de trabajo que desarrolló los criterios de Roma I,12 los cuales se modificaron en 1999 (Roma II) y 2006 (Roma III). Los criterios de Roma constituyen un esfuerzo de homologar a los pacientes con el objeto de incluirlos en estudios clínicos. Los criterios de Roma II son más sencillos de recordar y aplicar, pero difieren de los de Roma I en que son más restrictivos y poseen menor sensibilidad (49% vs. 83%, p ≤ 0.001).13
Los criterios de Roma III se basan en el cambio de forma y consistencia de la evacuación, que es uno de los mejores predictores del tránsito intestinal en los pacientes con SII.14 Debido a la falta de una definición pragmática, en fecha reciente la Task Force de SII del American College of Gastroenterology definió el síndrome sencillamente como un malestar o dolor abdominal que ocurre en asociación con alteración del hábito intestinal en un periodo de tres meses.10
Fisiopatología
El SII es un trastorno multifactorial. Hasta el momento no existe una causa bien definida ni un agente etiológico único discernible. Es una alteración a la que puede aplicarse un enfoque biopsicosocial a causa de los múltiples factores que participan en su desarrollo. Con objeto de simplificar las diversas teorías, éstas se dividen en: trastornos de la motilidad; hipersensibilidad visceral y el concepto del eje cerebro-intestino; inflamación de la pared intestinal, y factores psicológicos.14
Trastornos de la motilidad
Los pacientes con SII tienen diversos trastornos de la motilidad con mayor frecuencia que la población general.14 Se describen alteraciones en la actividad eléctrica gástrica,15 aumento de la frecuencia del complejo motor migratorio,16 con incremento de las contracciones yeyunales y la propulsión ileal, y respuestas motoras exageradas al alimento y el estrés emocional, sobre todo en el colon. 17
Cabe destacar que las anormalidades motoras antes descritas pueden verse también en sujetos normales sin síntomas, lo que sugiere que otros factores participan en la percepción consciente de tales anormalidades.
Hipersensibilidad visceral y el eje cerebrointestino
Múltiples estudios demuestran que los sujetos con SII tienen una percepción anormal de dolor ante un estímulo visceral que no es doloroso para un sujeto normal;18 este fenómeno se denomina hipersensibilidad visceral (HV). El ejemplo clásico experimental sería la distensión de un balón en el recto. Los sujetos con HV tendrán una sensación de dolor o de querer evacuar el recto con presiones más bajas que los sujetos control. Esta percepción de las sensaciones viscerales la determinan fibras aferentes de pequeño diámetro que llevan la información a la médula espinal y el tallo cerebral, y de estos sitios de relevo se proyecta al hipotálamo y la amígdala, entre otros.19 A nivel central existe una compleja red de regulación influida por factores emocionales y cognitivos en el procesamiento de la información. En otras palabras, las sensaciones viscerales como dolor, náusea, saciedad y hambre son experiencias subjetivas y conscientes que resultan de sensaciones moduladas por diversos factores emocionales, cognitivos y motivacionales representadas a nivel de la corteza insular. Mediante estudios de resonancia magnética cerebral funcional (MRIf) se han determinado diversos patrones de actividad cerebral en pacientes con SII que difieren de los de sujetos normales y que involucran la corteza insular, la amígdala y el puente dorsal.20 Incluso la actividad cerebral ante el mismo estímulo visceral puede ser diferente entre hombres y mujeres. En un estudio se produjo un estímulo rectal a seis sujetos sanos y seis con SII, y se analizó su efecto en el flujo sanguíneo cerebral con tomografía de emisión de positrones.19-20 Se encontró que en los sujetos sanos se activa la corteza insular anterior mientras que los sujetos con SII presentan una falla para activar esta área y muestran activación en la corteza prefrontal izquierda, lo que demuestra que existen patrones de activación diferentes que quizás expliquen la diferencia en la sensación visceral.
Asimismo se han demostrado anormalidades en el eje hipotálamo-hipófisis-suprarrenal. En los sujetos con SII se observa una hiperrespuesta de este eje a un agente visceral estresante en comparación con controles. Aún más, los pacientes con SII que sufrieron eventos estresantes previos durante su infancia o adolescencia (abuso emocional, físico o sexual) tienden a experimentar mayores anormalidades a este nivel.14
Inflamación
En los últimos años se ha publicado una gran cantidad de trabajos científicos de la relación de la flora intestinal, la inflamación de la mucosa y el SII.21 En 7% a 15% de los individuos con SII puede obtenerse el antecedente de gastroenteritis al inicio de la sintomatología. Se cree que estos pacientes pueden tener una inflamación de bajo grado o inflamación microscópica no específica caracterizada por incremento de la celularidad de la lámina propia del colon con aumento de los mastocitos e hiperplasia de las células enterocromafines, así como mayor permeabilidad de la mucosa.22 Al parecer es posible que un estímulo antigénico induzca una respuesta inmunitaria y la perpetuación de la inflamación de bajo grado.
Alteraciones de la flora intestinal
Con respecto a la flora microbiana, se propone que su interacción con la mucosa intestinal puede relacionarse con la sintomatología. Por ejemplo, en un estudio reciente de genómica bacteriana se determinó que los pacientes con SII, en comparación con sujetos sanos, presentan una anormalidad estadísticamente significativa de la micro-flora fecal.23 Algunos estudios demostraron la existencia de sobrecrecimiento bacteriano, aunque éste aún es tema de debate. También se encontró que la flora colónica productora de metano se vincula con estreñimiento.24
Esta evidencia apoya el uso de probióticos o antibióticos, o ambos, en el tratamiento del SII.
Factores psicológicos
El peso que debe asignársele a los factores psicológicos en la génesis del SII es incierto. Sin embargo, resulta ineludible que más de dos terceras partes de los pacientes con SII presentan trastornos psicológicos relacionados. La prevalencia de problemas psiquiátricos varía de acuerdo con el grupo de población analizado. Los individuos con más perturbación psicológica son los que reciben atención de tercer nivel. Por lo general este subgrupo ha sido visto por muchos médicos, se ha sometido a múltiples tratamientos fallidos y su frecuencia de trastornos de somatización, hipocondriasis, depresión, ansiedad y abuso sexual durante la infancia es más alta.14
Si bien se intenta determinar algún factor genético en el SII, se aprecian poderosos factores familiares y ambientales, más que hereditarios, en el desarrollo del síndrome. Los hijos de pacientes con SII tienen más visitas al médico, más ausentismo escolar y más síntomas gastrointestinales y no gastrointestinales que los de personas sin SII.25,26
Cuadro clínico y datos de alarma
Como el paciente con SII tiene síntomas crónicos, al momento de la entrevista es importante determinar qué fue lo que lo motivó a buscar atención médica en ese momento específico. Muchos individuos con SII tienen miedo de padecer una enfermedad orgánica seria, como cáncer o enfermedad inflamatoria intestinal, o algún evento estresante exacerbó los síntomas.2,3,14 Es importante desarrollar una buena relación médico-paciente desde el principio, porque de ello depende en menor o mayor grado el éxito del tratamiento.
En el SII el dolor abdominal suele localizarse en la parte baja del abdomen, puede ser cólico, calambre o punzante y, por definición, la evacuación debe brindar algún alivio. No obstante, el dolor también puede presentarse en otros sitios del abdomen. Es importante hacer una semiología completa del dolor para establecer el diagnóstico diferencial adecuado con otras causas de dolor abdominal, como trastornos biliares, enfermedad ulceropéptica y urolitiasis, y con problemas ginecológicos, entre otros.10,12,14
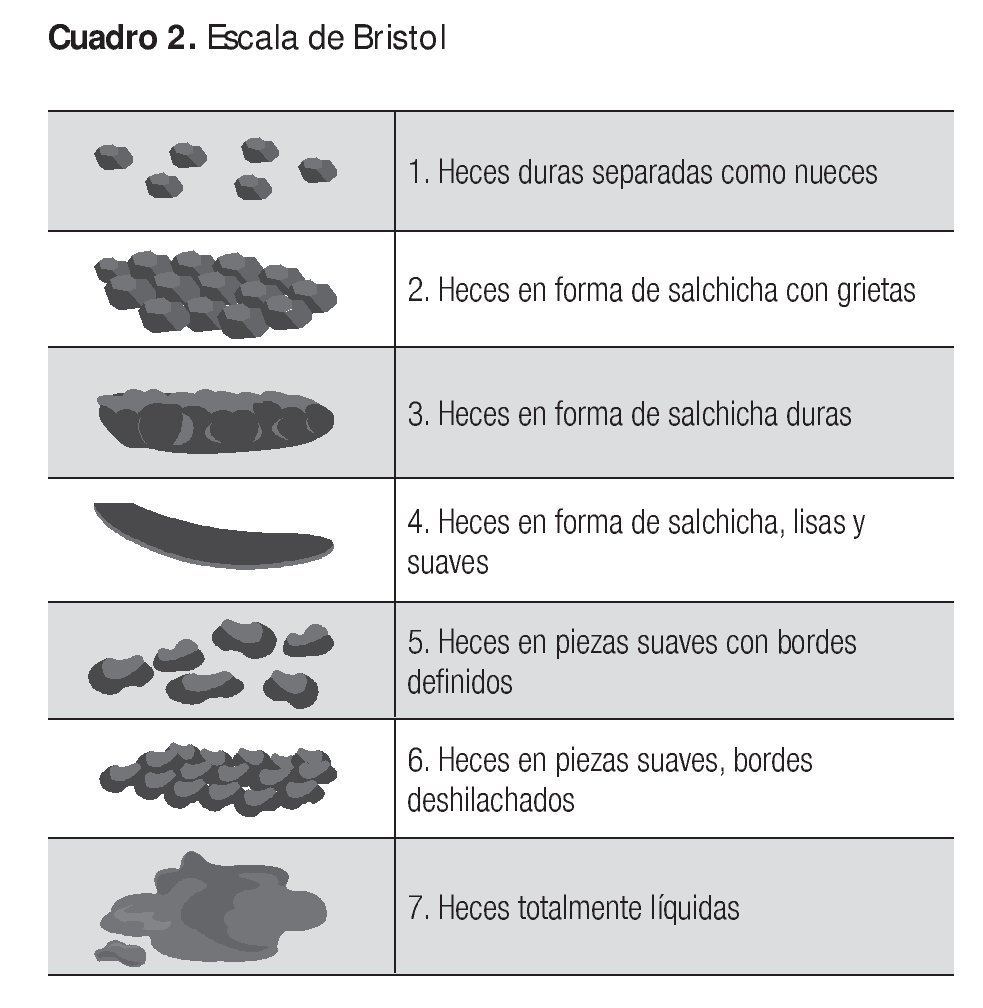
Con respecto al hábito intestinal, debe determinarse lo que estreñimiento o diarrea significan para el paciente. Estreñimiento puede significar frecuencia disminuida para una persona y sólo pujo para otra. La diarrea puede consistir en evacuaciones sólidas pero más frecuentes para alguno mientras que para otro es una sola evacuación líquida diaria.3,10,12,14 La escala visual de Bristol es de gran ayuda para el médico y el paciente a fin de determinar el síntoma de manera correcta (Cuadro 2).
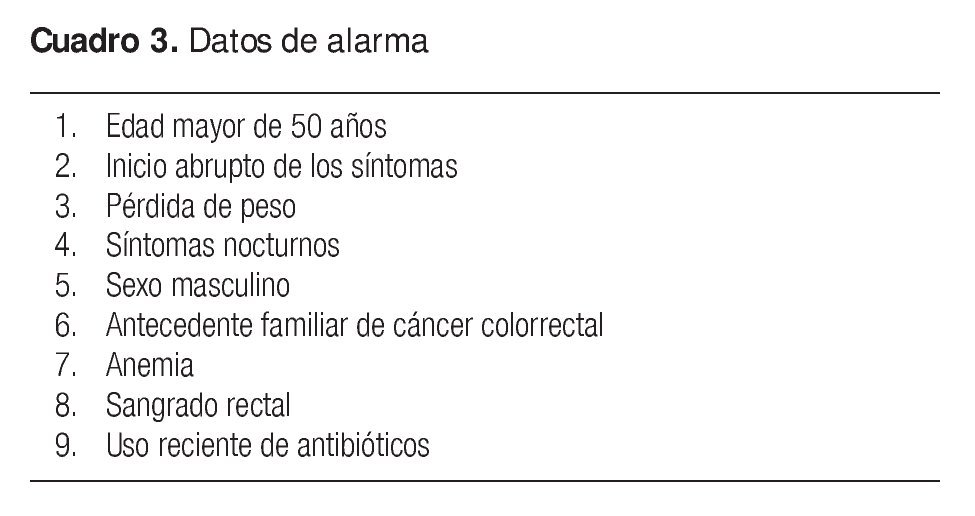
Es de suma importancia buscar si el paciente tiene datos de alarma (Cuadro 3). Cualquier dato de alarma presente requiere una investigación clínica posterior y el diagnóstico de SII no puede establecerse hasta descartar cualquier causa orgánica, sobre todo en personas mayores de 50 años con inicio reciente de sintomatología gastrointestinal.27 El valor discriminatorio de los diversos datos de alarma ha sido objeto de análisis. El sangrado rectal y el dolor nocturno tienen poco valor predictivo. La anemia y la pérdida de peso poseen una sensibilidad muy deficiente pero una especificidad alta para enfermedad orgánica.
Síntomas relacionados
Los pacientes con SII refieren síntomas gastrointestinales relacionados como distensión abdominal, gases, flatulencia, sensación de evacuación incompleta, evacuaciones con moco y urgencia.3,10,12,14 Aunque los criterios de Manning incluían algunos de estos síntomas, los de Roma III no los consideran obligatorios para el diagnóstico porque, si bien son en extremo frecuentes, no son específicos del SII. Hasta la tercera parte o la mitad de los pacientes puede tener otros TFD, como dispepsia y enfermedad por reflujo.
Enfermedades relacionadas
La prevalencia de otros trastornos funcionales es más alta en los pacientes con SII; entre los más frecuentes se encuentra la fibromialgia, el síndrome de fatiga crónica, la migraña, la cefalea tensional, los síntomas urinarios, la dispareunia y el dolor pélvico crónico.28
Subtipos
Con base en el hábito intestinal, los pacientes pueden clasificarse de la siguiente manera: SII con predominio de estreñimiento cuando más de 25% de las veces presentan heces duras y menos de 25% de las veces, heces blandas; SII con predominio de diarrea cuando más de 25% de las evacuaciones son líquidas y menos de 25% duras, y SII mixto si más de 25% de las veces hay heces duras y líquidas. Un pequeño subgrupo se considera indeterminado, pues no entra en ningún de las tres categorías anteriores.14
Evaluación diagnóstica
En pacientes jóvenes sin datos de alarma el diagnóstico de SII puede establecerse con certeza mediante bases clínicas y requieren pocos procedimientos diagnósticos adicionales. En ellos debe evitarse el uso excesivo de pruebas diagnósticas con una probabilidad "pretest" baja porque la mayor parte de tales estudios será falsos positivos, lo que promueve el encarnizamiento diagnóstico. Los estudios mínimos a solicitar consisten en biometría hemática completa para descartar anemia y velocidad de eritrosedimentación o proteína C reactiva para excluir procesos inflamatorios concomitantes.10,12,14 Si el paciente tiene diarrea además se incluye exámenes de heces en busca de leucocitos, sangre, huevos o parásitos. En algunos, según la historia clínica, puede ser útil revisar la función tiroidea y los niveles de calcio sérico. En pacientes con datos de alarma se requieren algunos estudios adicionales de imagen, laboratorio o endoscópicos enfocados a descartar alteraciones específicas como colitis microscópica, cáncer colorrectal, enfermedad inflamatoria intestinal, giardiasis o intolerancia a la lactosa. En México la prevalencia de enfermedad celiaca es menor que en países anglosajones y el escrutinio sistemático con anticuerpos no está recomendado.13,14 Por último debe obtenerse una cuidadosa historia psicosocial, eventos estresantes, preocupaciones del paciente y conductas de búsqueda de atención médica. El diagnóstico de SII puede establecer en forma correcta sin mayor evaluación en quienes cumplen los criterios diagnósticos y carecen de datos de alarma.14
Tratamiento
Relación médico-paciente
La relación médico-paciente es fundamental en el manejo del SII. Una buena relación incluye evitar prejuicios respecto al paciente, una evaluación clínica práctica y efectiva en relación con el costo, preocupación genuina por los síntomas, educación e involucrar al sujeto en las decisiones a tomar. Es importante observar la esfera psicosocial del individuo con objeto de encontrar síntomas escondidos o no expresados que pueden modificar el tratamiento. Las guías europeas14 mencionan 10 puntos necesarios para cumplir las expectativas de los pacientes con SII:
1. Una descripción clara y concisa de la enfermedad.
2. Informar que no hay una cura mágica.
3. Explicación clara respecto al autocontrol del paciente sobre su enfermedad.
4. Dejar claro que puede haber días buenos y días malos, pero que existe luz al final del camino.
5. Ofrecer diferentes opciones de tratamiento.
6. Reconocer que el SII es una enfermedad.
7. Discutir tratamientos alternativos.
8. Ofrecer tratamientos complementarios.
9. Brindar compresión y entendimiento.
10. Estar al tanto de los conflictos emocionales del paciente recién diagnosticado.
Dieta
La función de los alimentos en el SII es controversial. En la práctica clínica es frecuente encontrar que los pacientes informan intolerancia a algunos alimentos, casi siempre aquéllos con alto contenido graso, picantes o con lácteos. Aunque la calidad de la evidencia es baja, se recomienda obtener una historia cuidadosa de los alimentos para identificar cuáles pudieran contribuir a los síntomas, así como revisar el contenido de fibra en la dieta y disminuirla o aumentarla según la sintomatología y la cantidad ingerida.14 Con base en los antecedentes puede intentarse dietas de eliminación de lácteos, trigo o alimentos productores de gas, lo que confiere un beneficio hasta a 50% de los pacientes.29
Fibra
Aunque a menudo los médicos recomiendan aumentar la cantidad de fibra en la dieta para el tratamiento del SII, la evidencia que apoya esta recomendación no es sustancial.30,31 Inclusive es posible que la fibra empeore la sintomatología hasta en la mitad de los casos. La fibra soluble como el psyllium plantago es la más recomendada. Debe iniciarse con dosis bajas e incrementarse de manera paulatina con el propósito de aumentar la tolerancia y disminuir síntomas molestos como dolor abdominal, distensión y flatulencia.
Medicamentos
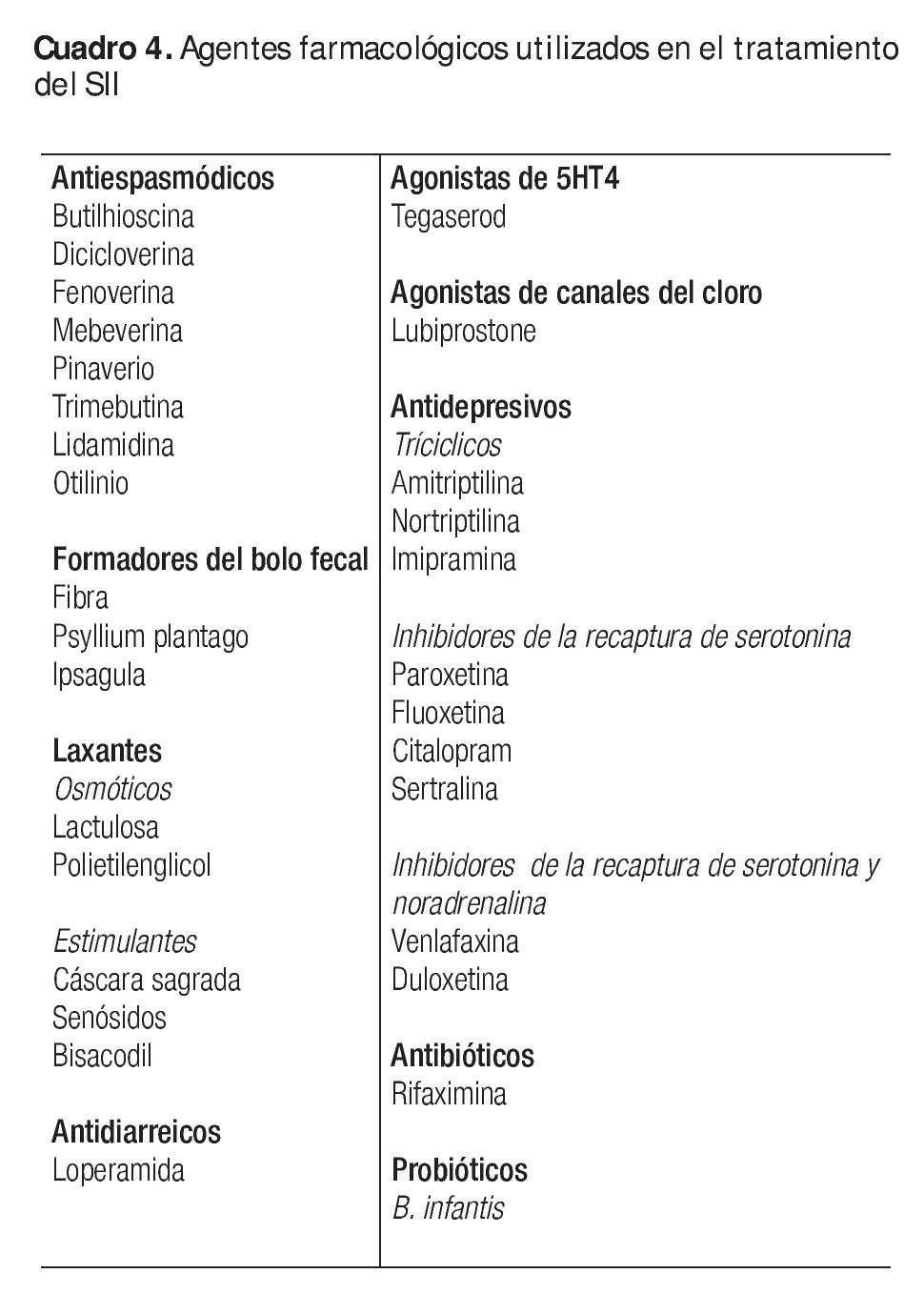
Los medicamentos más utilizados en el tratamiento del SII se resumen en el Cuadro 4.
Antiespasmódicos
Estos fármacos actúan a través de un efecto anticolinérgico o como relajantes directos de la musculatura lisa, ya sea bloqueando los canales de calcio o como antagonistas de opiáceos. Son de uso generalizado, pero su eficacia es variable. Aunque tienen efecto sobre el dolor abdominal, el correspondiente sobre el patrón evacuatorio es poco. En un meta-análisis32 en el que se evaluó la eficacia de cinco antiespasmódicos, se encontró que la respuesta en el grupo activo fue de 56% vs. 38% del grupo placebo (OR de 2.13; p < 0.001; 95% IC: 1.77-2.58) y una diferencia en el riesgo promedio de 22% (p < 0.001; 95% IC: 13-32%).
Antidiarreicos
Como los antiespasmódicos, estos agentes se usan para controlar síntomas de acuerdo con el predominio individual. La loperamida es un agente antidiarreico agonista de los receptores opiáceos que disminuye el tránsito intestinal, la diarrea, la urgencia y la incontinencia. Resulta útil con fines profilácticos, sobre todo si el paciente va a salir de la casa o si va a pasar por un evento estresante (p. ej., un examen).14
Laxantes
En los pacientes con predominio de estreñimiento, los laxantes osmóticos, como el polietilenglicol y el disacárido no absorbible lactulosa, son los agentes de primera elección. Los osmóticos deben emplearse con cuidado y a dosis escaladas porque producen flatulencia y cólico abdominal. En casos refractarios pueden utilizarse laxantes irritantes o una combinación de diferentes grupos de laxantes.
Tegaserod
Este fármaco agonista de los receptores 5HT4 es efectivo y está aprobado para pacientes con SII y predominio de estreñimiento. Es efectivo para disminuir el dolor abdominal, la distensión y el estreñimiento. Una revisión de la biblioteca Cochrane mostró que tegaserod es un agente eficaz; posee RR de 1.17 e IC 95% de 1.08-1.27 con un número necesario a tratar de 17.33 Hace poco tiempo fue retirado del mercado porque incrementa la incidencia de infarto al miocardio. Su administración se restringió y sólo los pacientes refractarios menores de 50 años pueden utilizarlo en determinados casos.
Lubiprostona
Este agente es un ácido graso bíciclico que estimula la secreción de agua al activar los canales tipo 2 que se localizan en la membrana apical del enterocito. Inicialmente se aprobó para el estreñimiento crónico y después se comprobó su eficacia contra placebo en el SII con predominio de estreñimiento.34 El evento adverso más frecuente es náusea. Este medicamento aún no está disponible en México.
Antidepresivos
Actúan como analgésicos viscerales modulando el dolor, lo que se aúna a sus efectos en los síntomas psicológicos relacionados o la actividad anticolinérgica inherente. Los fármacos más usados son los antidepresivos tricíclicos. Deben iniciarse a dosis bajas y administrarse por la noche con el propósito de disminuir los efectos adversos como sedación, estreñimiento, boca seca y visión borrosa.35 Es importante explicar que las dosis bajas de estos agentes tienen un efecto analgésico más que antidepresivo porque muchas personas son reacias a recibir tratamiento con psicofármacos. Los inhibidores de la recaptura de serotonina (IRS) son eficaces en el tratamiento de la depresión, ansiedad, fobias y conductas compulsivas. Deben administrarse en la mañana ya que pueden producir insomnio, agitación y disfunción sexual por su efecto serotoninérgico. Los IRS son eficaces en el mejoramiento de la calidad de vida y los síntomas globales del SII.13,14,35
Antibióticos
Una de las teorías de la patogénesis del SII propone la alteración intrínseca de la flora intestinal y el sobrecrecimiento bacteriano; de ahí la racionalización de usar antibióticos como tratamiento. El antibiótico no absorbible rifaximina es mejor que otros y eficaz en mejorar los síntomas del SII.36,37
En tres estudios aleatorizados y controlados la rifaximina tuvo un efecto positivo en el alivio global de los síntomas de SII. La dosis que se utiliza es de 1000 a 1200 mg diarios por 10 días. Sin embargo, la eficacia a largo plazo no se ha reproducido en todos los estudios. 10
Probióticos
Los probióticos actúan en el SII mediante modificación del balance de citocinas inflamatorias y antiinflamatorias, modulación de la liberación de sales biliares en el colon, cambio en la microflora residente y alteración de la motilidad.10,29 Las bacterias empleadas en estudios clínicos son Bifidobacterium, Lactobacillus y Streptococcus salivarius (la mezcla de estas tres bacterias se conoce como VSL#3). La formulación y concentración de bacterias son diferentes entre los estudios clínicos, lo mismo que sus resultados. En una revisión reciente sólo B. infantis mostró eficacia contra placebo en dos estudios bien diseñados, por lo que no se dispone de suficiente información basada en evidencia para emitir un juicio respecto a la efectividad del resto de los probióticos.38
Psicoterapia
A menudo el tratamiento farmacológico no es eficaz para aliviar los síntomas de los pacientes con SII. Como la depresión y la ansiedad son prevalentes en el SII y con frecuencia el estrés emocional dispara la sintomatología, se sugieren tratamientos psicológicos para el manejo de la enfermedad. Las intervenciones "mente-cuerpo" se dividen en: 1) terapias de relajación, 2) terapia cognitivoconductual, 3) terapia psicodinámica y 4) hipnoterapia (Cuadro 5).
Terapias de relajación
Estos tratamientos incluyen yoga, relajación muscular progresiva y meditación, entre otras. Han mostrado eficacia en algunos estudios, pero no en otros.39 Las terapias de relajación por si solas no ofrecen beneficio, pero son de utilidad cuando se combinan con otros tratamientos psicoterapéuticos.
Terapia cognitivo-conductual (TCC)
En este tratamiento se buscan patrones de conducta o pensamiento que conllevan emociones negativas y limitan el avance a un objetivo determinado. Se enseña al paciente a identificar estas ideas o conocimientos distorsionados, a analizarlos, identificar el patrón de respuesta ante un síntoma determinado y a mostrar formas de respuesta más adaptadas. En pruebas clínicas la TCC disminuyó los síntomas gastrointestinales y el estrés psicológico.11,12,39
Terapia psicodinámica (TPC)
La TPC intenta proveer un entendimiento del modo en que el estrés está ligado al estado emocional y éste a su vez a los síntomas digestivos. En estudios comparativos la TPC aumenta la calidad de vida y mejora los síntomas.14
Hipnoterapia
El mecanismo de acción de la hipnoterapia en SII no se conoce claramente. Su objetivo es crear un estado de sugestión en el cual se intenta modificar la percepción sensorial del paciente a los estímulos viscerales. Aún no se comprueba de manera definitiva un efecto sobre la fisiología gastrointestinal, pero sí sobre la modulación del dolor a nivel central.40 La limitante de la hipnoterapia es que requiere personal entrenado, múltiples sesiones, depende del operador y sólo se ha probado en pruebas clínicas en sujetos con enfermedad refractaria.
Medicina alternativa
La menta piperita (peppermint oil) es una cruza de la menta acuática y la hierbabuena. Considerada como una de las plantas medicinales más antiguas del planeta, los romanos y los egipcios la utilizaron para el tratamiento de los trastornos digestivos. Su ingrediente activo es el metanol, el cual actúa como bloqueador de los canales del calcio del músculo liso intestinal. Un meta-análisis de cinco estudios aleatorizados doble ciego demostró una mejoría significativa en comparación con placebo, aunque inconvenientes metodológicos limitan la interpretación de los resultados. Entre 11 y 36% de los pacientes puede presentar efectos adversos como ardor anal, pirosis y visión borrosa, y en grandes cantidades puede producir insuficiencia renal.41,42,43
Conclusiones
El SII es un trastorno tan frecuente que todos los médicos lo han enfrentado en alguna ocasión. Por su naturaleza crónica y recurrente, limita la calidad de vida de millones de personas en el mundo y constituye una carga económica importante. Una buena relación médico-paciente es fundamental para lograr éxito en la curación, con un enfoque holístico que trate tanto el cuerpo como la mente del individuo.
Correspondencia:
Dr. Rafael Castañeda Sepúlveda.
Departamento de Medicina Interna, Hospital Christus Muguerza Sur. Carretera Nacional 6501, Col. La Estanzuela, CP 64988, Monterrey, Nuevo León. México.
Teléfono: (52 81) 8317 9977.
Correo electrónico:rafacasep@yahoo.com.mx
Aceptado: enero, 2010.