La enfermedad traumática es la primera causa de mortalidad por debajo de 40 años, así como de discapacidad y secuelas, muchas de ellas prevenibles y alguna relacionada con fallos en la organización y provisión de la asistencia médica1. Desde hace años, se vienen comunicando deficiencias importantes en la atención a los pacientes con traumatismo grave (PTG), reflejadas en diferencias en la mortalidad entre países con similar nivel económico, en variabilidad interhospitalaria, por retrasos injustificados o asistencia por profesionales insuficientemente preparados1–4. Supervivencia y recuperación funcional dependen directamente de la rapidez en reconocer y reparar las alteraciones anatómicas y fisiológicas desencadenadas, cobrando la asistencia inicial una relevancia de primer orden1. Su objetivo fundamental es identificar y solucionar, de forma inmediata, sistemática y priorizada, los problemas graves de la vía aérea, respiración y circulación, responsables, en conjunto, de una gran parte de la mortalidad prevenible. Para ello, el protocolo clínico mundialmente aceptado es el Advanced Trauma Life Support (ATLS®)5 que constituye hoy el estándar asistencial para los PTG. Como última prioridad, en la revisión primaria, se investiga la presencia de daño neurológico. En todo momento se asegura la inmovilización cervical hasta constatar por tomografía computarizada (TC) la ausencia de lesión. En esta primera fase se obtienen únicamente radiografías del tórax y pelvis y ecografía focused assessment with sonography in trauma (FAST)6. Posteriormente, durante la revisión secundaria, se realizará una valoración «de cabeza a pies», con las exploraciones de imagen pertinentes.
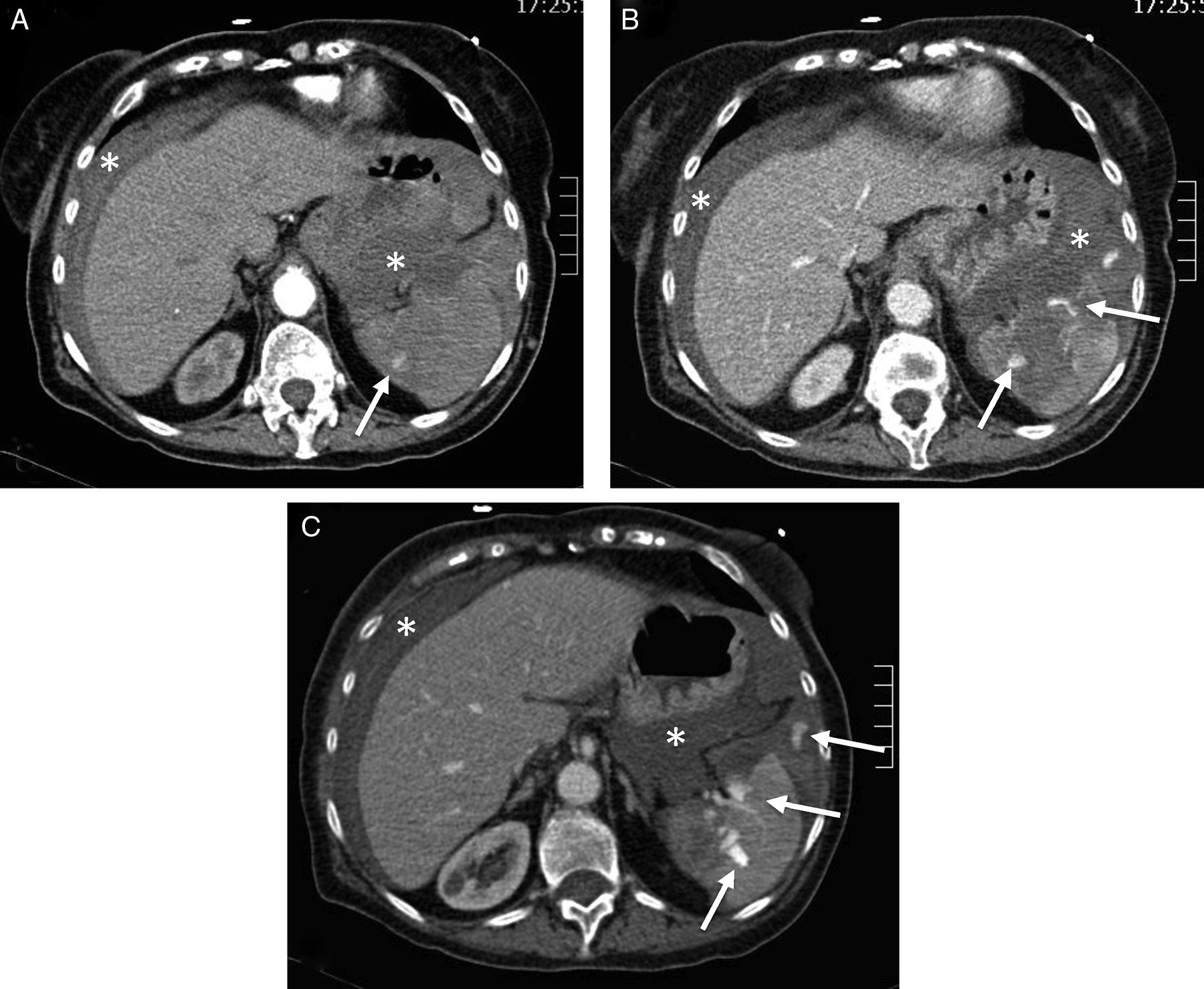
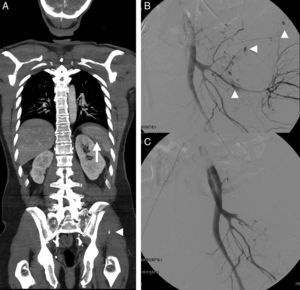
La exploración física en el PTG puede hacer sospechar y abordar de forma inmediata lesiones de riesgo, como neumotórax a tensión, fracturas pelvianas o focos de sangrado externo, pero su fiabilidad es limitada, especialmente cuando el nivel de conciencia está alterado o coexisten otras lesiones llamativas7. Existe riesgo de «lesiones inadvertidas», particularmente en pacientes graves, ancianos, con traumatismo craneoencefálico o lesión vascular visible8 (fig. 1). La información recogida sobre la escena del accidente orienta acerca del posible mecanismo y patrón de lesiones, pero es subjetiva y tiene baja sensibilidad como indicador de lesión grave9.
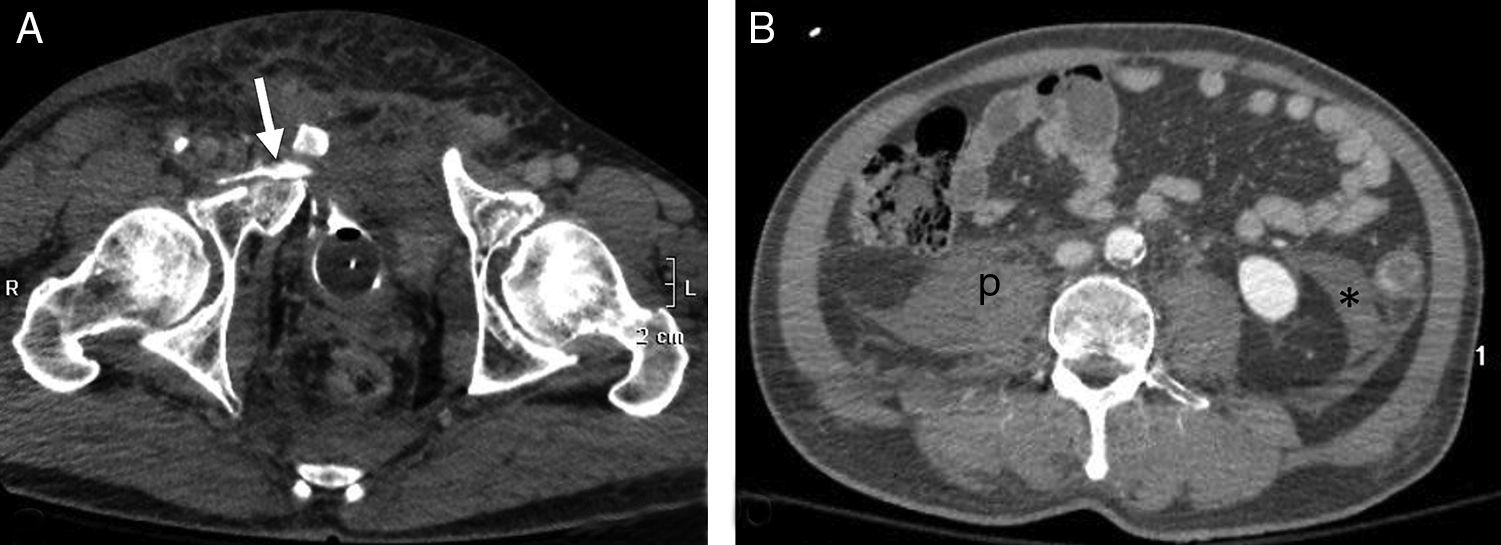
Fractura esplénica. Mujer de 77 años anticoagulada. Caída doméstica como consecuencia de un «mareo». En Urgencias, muestra hipotensión y distensión abdominal. A) TCCC con contraste, cortes axiales del abdomen superior en fase arterial. B y C) Fase venosa. Hemoperitoneo (*).Fuga de contraste e.v. al interior del parénquima esplénico y a la cavidad peritoneal (flecha) que aumenta de tamaño y densidad en la fase portal (b y c) por laceración esplénica con sangrado activo.
La difusión mundial del protocolo ATLS ha supuesto un gran avance en el manejo sistemático de los PTG, pero, en el ámbito de la imagen diagnóstica, tiene algunos déficits de actualización, particularmente en relación con el empleo de la TC10–12. ATLS sigue una orientación clínica «paso a paso», realizando las maniobras de resucitación mientras se evalúa rápidamente al paciente para identificar y «manejar» posibles lesiones de riesgo, en tanto se plantea su tratamiento definitivo. Pero la aplicación del protocolo ATLS es necesariamente diferente cuando la realiza un equipo de rescate en el escenario del accidente, contando con poco más que su pericia clínica, que cuando lo aplica un equipo de politrauma de un hospital de referencia, en un box de críticos, adecuadamente equipado y con una sala de TC adyacente.
Radiología e imagen en el traumatismo graveEl Royal College of Radiologists (RCR) británico, en su guía para la radiología en PTG, establece algunas premisas relevantes en el diseño, localización y dotación tecnológica de las instalaciones de imagen diagnóstica destinadas a tal fin13:
- –
La rapidez es fundamental.
- –
Debe minimizarse el número de desplazamientos y su distancia.
- –
En general, la imagen es más precisa que la exploración clínica.
- –
La modalidad de elección será aquella cuyo resultado sea concluyente, habitualmente la TC de cuerpo completo (TCCC).
- –
Una técnica de imagen concluyente no debe retrasarse por realizar otras exploraciones de menor precisión.
- –
Las instalaciones de radiología deben dotarse de los mismos recursos de soporte vital existentes en la sala de críticos.
- –
Aquellos centros de trauma donde la sala de TC multidetector (TCMD) no se encuentre dentro o próxima al área de críticos deberán ensayar los traslados de pacientes, de acuerdo con protocolos preestablecidos, y planificarán modificar dicha localización en el futuro.
La modalidad de imagen ideal en el PTG debería ser rápida, exhaustiva y capaz de identificar de forma inmediata y sistemática todas las lesiones con riesgo vital, siguiendo las mismas prioridades ABCD14.
Enfoque clásico: radiografía digital, ecografía focused assessment with sonography in trauma y tomografía computarizada dirigidaRadiografías de columna cervical, pelvis y tóraxLas radiografías de tórax (RT) y pelvis (RP) y la ecografía FAST siguen siendo, para el protocolo ATLS, los ejes fundamentales del diagnóstico por imagen del PTG durante la revisión primaria5. Son rápidas, accesibles y aportan información útil de forma puntual, aun con importantes limitaciones técnicas y una calidad de imagen, con frecuencia, subóptima. Su empleo se reduce a medida que los equipos TC van siendo más accesibles desde el área de urgencias. Inicialmente fueron las radiografías de columna cervical; la propia guía ATLS acepta sus limitaciones y sugiere realizar TC, si está indicado para cerebro o cuando así esté protocolizado en el centro. La sensibilidad agrupada de la radiografía cervical es de 52% contra 98% para la TC. Incluso en pacientes con bajo nivel de conciencia, una TC normal excluye lesión traumática relevante, sin necesidad de resonancia magnética (RM), permitiendo la retirada precoz del collarín cervical15.
Hasta una de cada 4 muertes traumáticas guardan relación con la presencia de lesiones torácicas16. Hemo- o neumotórax a tensión pueden identificarse clínicamente, por radiografía o ecografía, pero la visualización de pequeños neumotórax o focos de contusión pulmonar requiere la realización de TC.
La especificidad de la RT supera el 90%, pero su sensibilidad es baja, del 20%16, y empeora en pacientes graves, de forma que en más de la mitad de ellos con RT normal, la TC descubre hallazgos adicionales17. Hasta un 11% de lesiones traumáticas aórticas pasan desapercibidas por radiografía convencional17,18. No se precisa RT en pacientes con traumatismo cerrado, conscientes, estables respiratoria y hemodinámicamente, especialmente si se realizará una exploración por TC16,17. En el otro extremo, una RT normal puede evitar la TC torácica, en pacientes jóvenes con traumatismo leve y sin indicios de lesión19.
Entre el 4 y el 9% de los PTG presentan lesiones pelvianas, con elevada probabilidad de otras lesiones graves y hemorragia14,20, de origen venoso/óseo en el 85% y arterial en el resto12. La TCMD identifica mayor número de fracturas que la RP y define mejor la estabilidad y abordaje terapéutico. Publicaciones recientes desaconsejan realizar rutinariamente RP21. Para prevenir la hemorragia, se recomienda mantener la banda de fijación externa pelviana hasta excluir fractura por TC13.
Las radiografías de las extremidades deben realizarse durante la revisión secundaria, cuando todas las lesiones de riesgo hayan sido identificadas y tratadas, pero en algún caso concreto puede ampliarse la exploración con TC inicial13.
EcografíaLa identificación de hemoperitoneo en un PTG y signos de shock ha sido considerada clásicamente indicación de laparotomía22. La ecografía es una técnica no invasiva, accesible a pacientes graves, barata y que no emplea radiación ionizante, con lo que puede repetirse. La modalidad FAST se limita a la identificación de líquido intraperitoneal, que asume como hemoperitoneo. Su gran difusión clínica desplazó a otras técnicas invasivas como la punción-lavado peritoneal22.
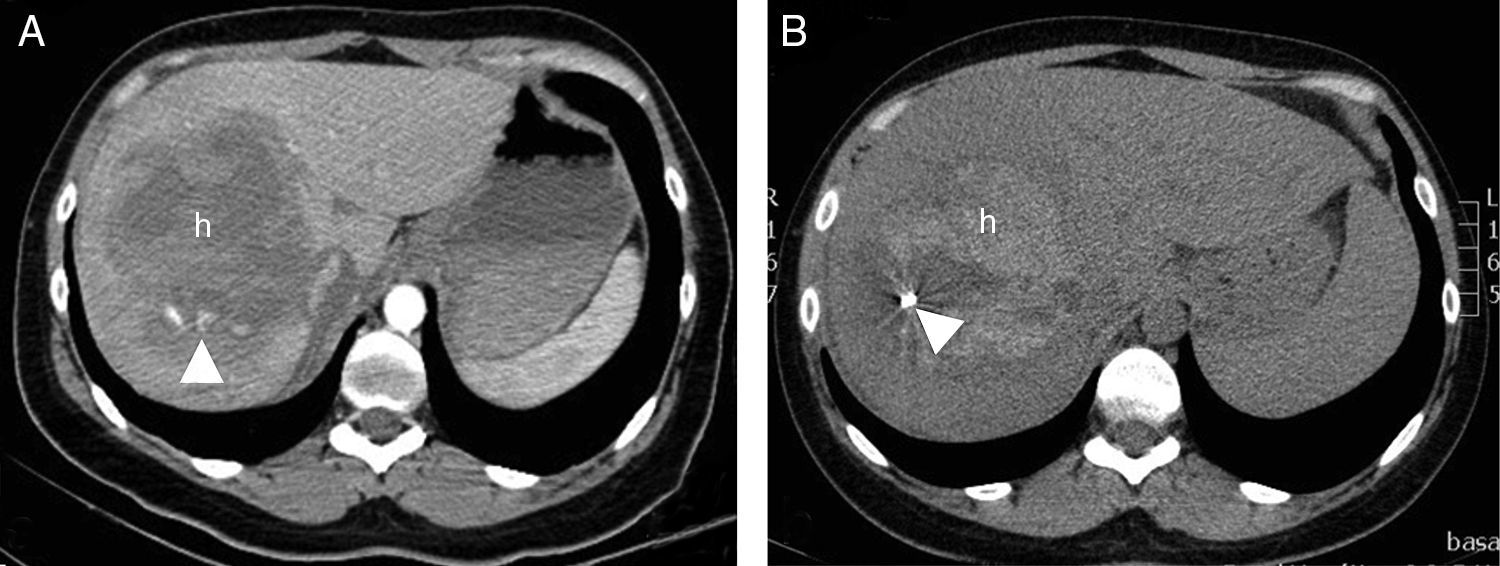
A pesar de su elevada precisión en la detección de líquido intraperitoneal, la ecografía presenta importantes limitaciones para su empleo rutinario en PTG. El 34% de las lesiones viscerales, confirmadas por TC o cirugía, no presentan hemoperitoneo23, es decir, una FAST negativa no excluye lesión abdominal relevante (fig. 2). Debido a esta baja sensibilidad y a la imposibilidad de proporcionar información visceral específica, no se recomienda su empleo en pacientes hemodinámicamente estables, donde la presencia de hemoperitoneo no altera necesariamente la decisión de manejo conservador24,25,. En pacientes inestables su valor predictivo negativo es de 50-63%26, con valor predictivo positivo también bajo. En la serie de Charbit et al.27, únicamente en el 63% de los pacientes con hemoperitoneo y sangrado activo, este era de origen peritoneal, reduciéndose la cifra al 52% si existía hipotensión. Por ello, en pacientes con shock traumático y hemoperitoneo, recomiendan excluir otras posibles fuentes de sangrado en tórax, pelvis o retroperitoneo.
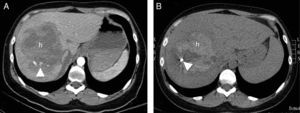
Mujer de 30 años. Golpe contra el manillar de la bicicleta. Consciente. Dolor a la palpación profunda. No irritación peritoneal. Tensión mantenida, hemograma normal. FAST negativo (no hemoperitoneo). A) Imagen axial de TC con contraste e.v., que muestra lesión focal hipocaptante (h) que afecta gran parte del lóbulo derecho, con focos de sangrado activo (cabeza de flecha). Se indica embolización percutánea. B) La TC sin contraste de control tras embolización (una semana) muestra lesión focal hepática hiperdensa (h), correspondiendo con el hematoma, con reducción de tamaño e imagen metálica debida al material de embolización (coil).
Para detección de lesión visceral, intra o retroperitoneal, la sensibilidad de la ecografía es muy baja, del 50%, incluso realizada por médicos entrenados28. Con frecuencia, el aspecto ecográfico del riñón es normal aun en presencia de una lesión traumática aguda6. El empleo de medio de contraste ecográfico puede mejorar la sensibilidad de la ecografía, pero le hace perder su principal ventaja: la inmediatez.
En traumatismos penetrantes la ecografía puede ser útil cuando aporta hallazgos positivos: hemotórax o hemoperitoneo en un paciente hipotenso, como paso previo a la cirugía; cuando son negativos se precisa TC, lo que cuestiona su utilidad6,24.
La ampliación del estudio FAST a las cavidades pericárdica y pleural se denomina Extended FAST (EFAST), y permite identificar hemopericardio y hemo- o neumotórax traumáticos29. La incidencia de neumotórax oculto (visible por TC pero no por RT), se aproxima al 5%, pero alcanza el 55% cuando el Injury Severity Score (ISS) supera 1224. Para la detección de neumotórax traumático, la ecografía obtiene sensibilidad superior a la clínica y a la radiografía convencional29, aproximándose al 100% en la detección de hemotórax24. La ecografía es también útil para detectar líquido pericárdico y para valorar la precarga y la respuesta cardiovascular al aporte de volumen, midiendo el diámetro de la vena cava inferior.
Aparte de ser una técnica operador-dependiente, con problemas de acceso en caso de heridas cutáneas, quemaduras, obesidad o enfisema subcutáneo, la ecografía no aporta información adicional a la TC y su realización no debería retrasarla13. Un estudio negativo no excluye lesión abdominal grave y uno positivo no identifica el origen del sangrado ni aporta información para decidir tratamiento conservador. A pesar del gran volumen de publicaciones, no existe evidencia de un impacto real sobre la supervivencia de los pacientes25. Se ha sugerido su utilidad en casos extremadamente graves, no transportables a la sala de TC, por cerca que se encuentre, y en casos de traumatismo menor en pacientes jóvenes para evitar la TC. Se emplea en el seguimiento de lesiones ya diagnosticadas19 y en el triage de incidentes con múltiples víctimas13.
Resonancia magnéticaLargos tiempos de exploración y un ambiente especialmente «hostil» reducen el empleo de la RM en el PTG. El elevado valor predictivo negativo de la TCMD para traumatismos vertebrales15 reduce el empleo de la RM a los pocos casos con clínica neurológica y TC normal.
Para explorar a un PTG con RM debe garantizarse que cualquier material ferromagnético ha sido extraído del paciente, incluidos posibles cuerpos extraños, y emplearse material de soporte vital compatible. La elevada incidencia de lesión vertebral múltiple obliga a estudiar la columna completa5,12.
Tomografía computarizada dirigida por orientación clínica y de imagenLa guía ATLS reconoce que la TC proporciona información específica sobre las lesiones viscerales y su extensión, y que identifica lesiones retroperitoneales y pelvianas difíciles de valorar por exploración física, FAST y lavado peritoneal; pero previamente ha subrayado que: «…es un procedimiento lento que debe realizarse únicamente a pacientes sin alteración hemodinámica, en los que no existe indicación aparente de laparotomía urgente». Es decir, está prohibida para pacientes inestables.
La observación clínica, con el apoyo de radiografía simple y ecografía, completada con la realización de TC de alguna región concreta «orientada» por los hallazgos de las anteriores, constituye una opción de manejo diagnóstico en pacientes con baja sospecha de lesión, especialmente jóvenes. Este planteamiento reduce el número de exploraciones, la dosis de radiación y los costes. Hasta un 10% de lesiones podrían pasar desapercibidas en la revisión primaria, pero la relevancia clínica del retraso diagnóstico no parece significativa30. Es importante evitar exploraciones adicionales sucesivas de varias zonas anatómicas, que requieren nuevos traslados y aumentan la dosis al solapar los campos de irradiación.
Paciente con traumatismo grave: tomografía computarizada de cuerpo completo integrada en la revisión primariaLos antiguos equipos de TC de un solo corte tardaban 30 min en obtener un estudio de baja calidad y rendimiento diagnóstico. En tal contexto, se acuñaron algunos mitos, aún persistentes, referidos a la escasa utilidad de la radiología en el PTG, al análisis subjetivo de los hallazgos radiológicos o a «la rosquilla de la muerte», donde ningún paciente hemodinámicamente inestable debía ser introducido.
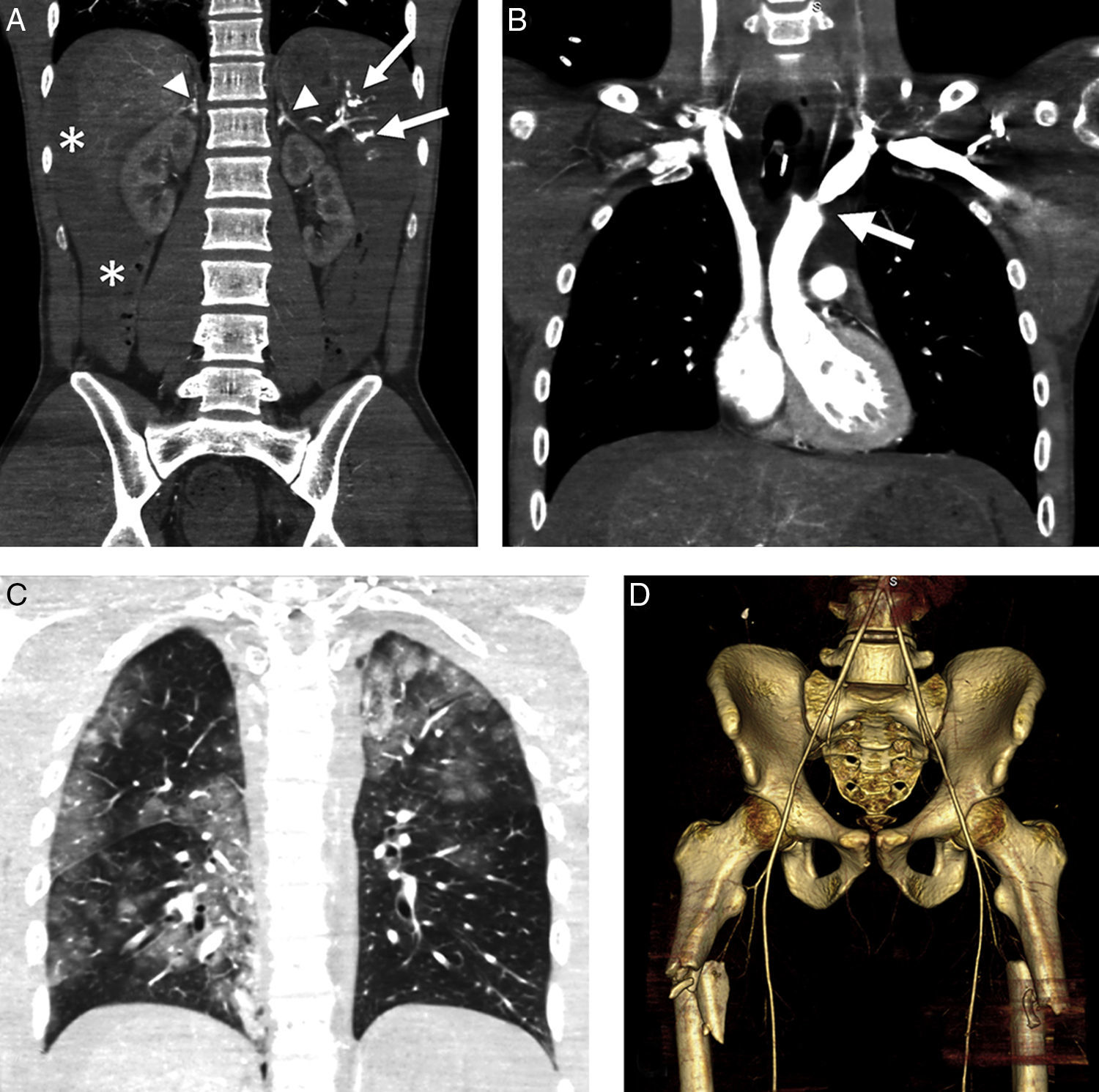
Aunque el posicionamiento y la conexión de vías y tubos pueden llevar varios minutos, los equipos de TC actuales permiten explorar en segundos a un paciente «de cabeza a pies», incluyendo simultáneamente cabeza, columna cervical, tórax, abdomen y pelvis, la llamada exploración «TC de cuerpo completo» para trauma (TCCC). Su gran resolución de imagen propicia mayor sensibilidad y especificidad que la exploración clínica, la radiografía y la ecografía, para identificar y clasificar lesiones16,17, con superior concordancia inter- e intraobservador que cualquier otra técnica de imagen31. La TCCC realizada durante la revisión primaria permite efectuar un balance global de lesiones de forma rápida y detallada, identificando aquellas de riesgo vital, incluidos posibles focos de hemorragia activa y, con frecuencia, lesiones no sospechadas1,11,32–35 (fig. 3). Sus principales ventajas en la revisión primaria son la disponibilidad de un diagnóstico definitivo de forma previa a la decisión terapéutica y la rapidez13. Comparada con el planteamiento convencional, la TCCC emplea la cuarta parte de tiempo y hace innecesarios la mitad de los traslados36. Los pacientes estudiados con esta técnica precisan menos estancia en unidades de cuidados intensivos (UCI), menos días de ventilador y muestran menor porcentaje de fracaso orgánico37. Durante las revisiones secundaria o terciaria, acelera el tratamiento definitivo y, eventualmente, el alta hospitalaria38. Reduce al mínimo las lesiones inadvertidas16,39 y disminuye drásticamente todos los indicadores de tiempo40, con efecto beneficioso sobre la mortalidad, especialmente en pacientes graves41.
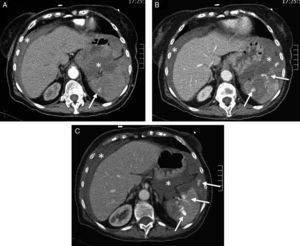
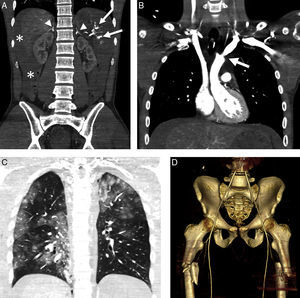
Complejo hipoperfusión-shock. Varón de 24 años. Accidente de automóvil sin cinturón de seguridad con salida del habitáculo. Signos de shock hipovolémico. TCCC con reformateos multiplanares (MPR) coronales del abdomen. A) Abdomen con hemoperitoneo (*) por estallido esplénico (flechas) e hiperrealce de ambas suprarrenales. B) MPR coronal de tórax/mediastino con lesión traumática de aorta ascendente, sin evidencia de hematoma mediastínico (flecha). C) MPR coronal de tórax/parénquima: múltiples focos de contusión pulmonar. D) Reformateo tridimensional de la pelvis: fractura de ambos fémures proximales (nótese el calibre reducido de aorta y arterias ilíacas).
La TCMD es hoy la técnica de imagen fundamental en los PTG, cuyo empleo, en condiciones adecuadas, cuestiona, desde el punto de vista de la imagen, la actualización del planteamiento diagnóstico de la guía ATLS. Entre otras, la idea clásica de que los pacientes inestables no deben desplazarse a la sala TC, aunque ampliamente extendida, no se sustenta en ninguna evidencia científica1 y ha sido cuestionada, en los últimos años, por el desarrollo tecnológico de la TC y por la opinión de múltiples autores, apoyada en una evidencia creciente, si bien aún de bajo nivel10,33–35,, al igual que la propia guía ATLS. La TC es hoy la única modalidad de imagen capaz de proporcionar información fiable sobre posibles lesiones intratorácicas o de la pared vascular con o sin hemorragia activa asociada. El número de laparotomías no terapéuticas es mayor en pacientes inestables, debido a la imposibilidad de acceder quirúrgicamente al vaso sangrante42 y la TC puede reducir dicho número43. Está en marcha un estudio prospectivo que compara ambas opciones en su aspecto diagnóstico, TCCC en la revisión primaria y protocolo ATLS (radiografía y FAST con TC a demanda)43.
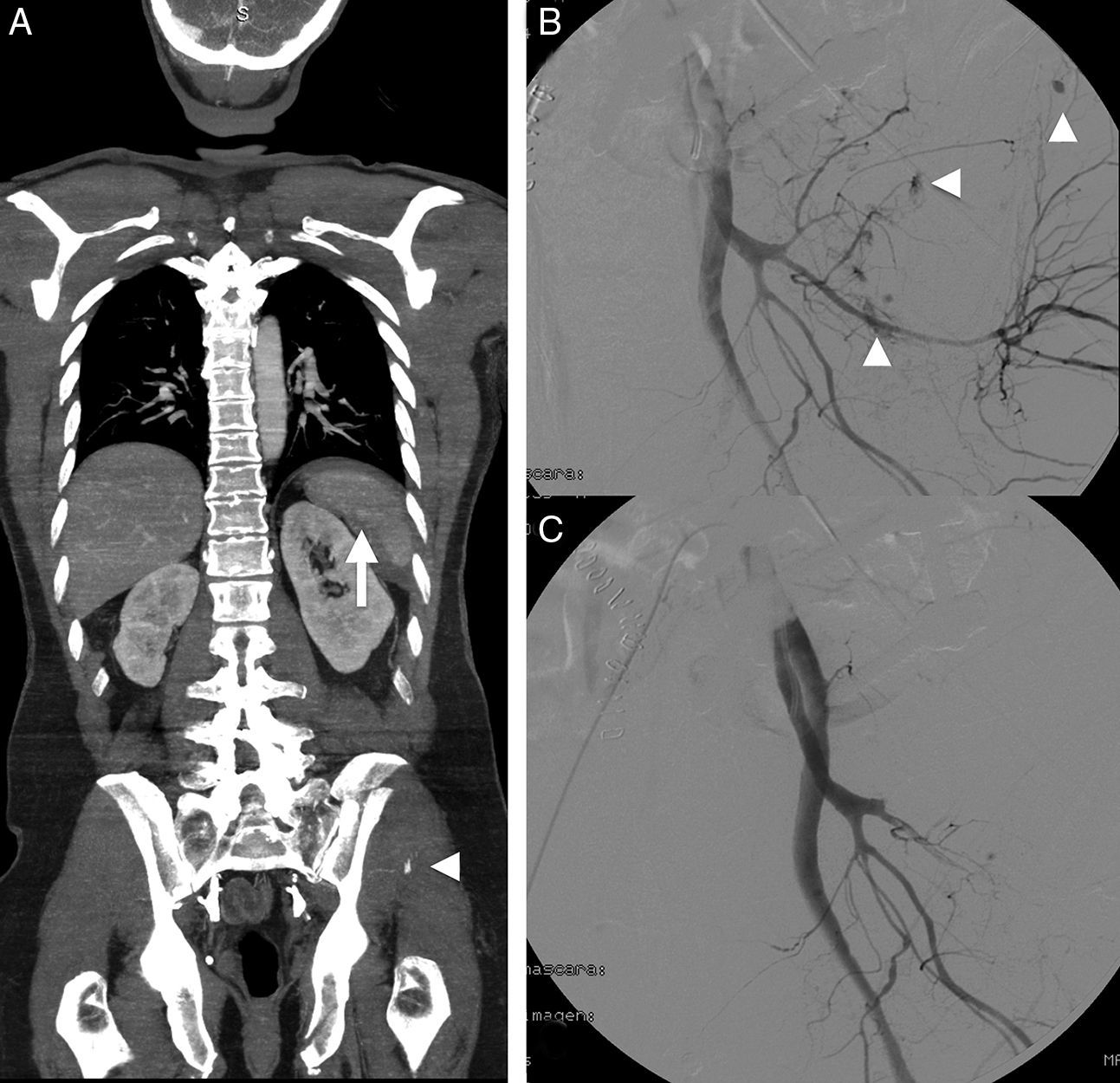
Ante sospecha de sangrado activo se realiza un barrido inicial (angio-TC) con el contraste intraarterial, seguido de otro cuando está intravenoso. El rendimiento diagnóstico de la angio-TC es equiparable a la angiografía convencional44, permitiendo detectar sangrado y caracterizarlo como arterial o venoso. La lesión traumática de la pared arterial ocasiona hemorragia activa cuando es completa y, ocasionalmente, la formación de fístula arteriovenosa o pseudoaneurisma, con riesgo de rotura y sangrado tardío, por lo que suelen embolizarse. Por TC aparecen como una dilatación de la luz arterial en la fase arterial que desaparece en la fase venosa, a diferencia de la hemorragia activa, donde persiste la extravasación del contraste (figs. 1 y 4).
Varón de 54 años con traumatismo múltiple por accidente de automóvil. Constantes vitales mantenidas. A) TCCC en fase portal, reformateo MPR coronal, que muestra laceración esplénica con pequeño hematoma periesplénico y seudoaneurisma (flecha). Fractura compleja de pelvis izquierda con focos de sangrado activo (cabeza de flecha). B) La angiografía confirma múltiples focos de sangrado activo (cabezas de flecha). C) Focos de sangrado que se resuelven tras la embolización al igual que el seudoaneurisma esplénico (no mostrado).
La aplicación del protocolo TCCC tiene dos requisitos fundamentales: accesibilidad de la sala TC y adecuada selección de pacientes. La sala TC debe encontrarse dentro del área de urgencias y contar con material de monitorización y soporte vital. La dosis de radiación administrada a una población eminentemente joven constituye un problema importante. Toda exposición a radiación ionizante debe justificarse por un beneficio clínico esperable y debe seguir el criterio ALARA («tan bajo como sea razonablemente posible»). Aunque alrededor del 30% de estudios TCCC no muestran lesiones32, ciertamente, para desarrollar complicaciones por exposición a la radiación, primero hay que sobrevivir al traumatismo.
Parece que la TCCC asocia una dosis de radiación menor que la TC segmentada, debido a las zonas de solapamiento43,45. No obstante, esta se aplica a pacientes menos graves, restringiendo su extensión a la región anatómica sospechosa31, mientras que la TCCC quedaría reservada para los PTG, en los que el tiempo es un factor crítico19. Los servicios de radiología deben actualizar tecnológicamente sus equipos y ajustar los protocolos de exploración según edad, peso y objetivo diagnóstico19. La coordinación con el resto de servicios implicados debe realizarse en el seno del equipo multidisciplinar, consensuando las pautas de actuación, incluida la movilización, para cada perfil de pacientes.
La TCMD en urgencias es más coste-efectiva que ninguna otra técnica, tanto para decidir manejo terapéutico inicial, incluidos ingreso o alta precoz, como posteriormente, debido a los costes asociados de las lesiones inadvertidas32.
Criterios de selección de pacientes para tomografía computarizada de cuerpo completoEl RCR sugiere restringir el empleo de TCCC a pacientes con ISS > 1513, pero la naturaleza inicialmente oculta de algunas lesiones y el cálculo retrospectivo dificultan su empleo. Las ventajas de la TCCC en PTG son evidentes, pero su dosis de radiación y costes se justifican únicamente en este grupo de pacientes. La alteración de las constantes vitales combinada con la exploración física son los marcadores más sensibles de traumatismo grave, pero su sensibilidad para predecir ISS > 15 es del 56%, por lo que se añade el mecanismo de lesión7,32 (tabla 1).
Criterios de selección para la TCCC en pacientes con traumatismo grave
| 1. Mecanismo de lesión de alto riesgo |
| • Accidente de tráfico |
| – Peatón/ciclista/motorista arrollado por un automóvil |
| – Extricación prolongada (>15 min) |
| – Muerte de otro pasajero |
| – Eyección del vehículo |
| – Colisión de automóvil a alta velocidad |
| – Accidente de motocicleta |
| • Caída desde más de 3 m, altura desconocida, escaleras |
| • Desplome de edificio |
| • Sospecha de incluido en el radio de acción de una explosión |
| 2. Evidencia de lesiones anatómicas |
| • Lesiones visibles en 2 regiones anatómicas (cabeza/cuello/tórax/abdomen/pelvis/huesos largos) |
| • Signos de lesión vascular (hematoma expansivo, herida profunda en trayecto arterial) |
| • Signos de lesión medular |
| • Fractura pelviana inestable |
| • Fracturas > un hueso largo |
| 3. Constantes vitales |
| • Glasgow < 12, intubado |
| • Tensión arterial sistólica < 100mmHg |
| • Frecuencia respiratoria: <10 o >30 por min |
| • Pulso > 120 lpm |
| • Saturación arterial de oxígeno < 90% |
| • Edad > 65 años |
| • Anticoagulación |
Tras el sistema musculoesquelético, el abdomen es la segunda localización en frecuencia de lesiones inadvertidas, y la posibilidad de error es mayor en algunas estructuras anatómicas39. La lesión traumática mesentérico-intestinal aparece en el 5% de pacientes con trauma abdominal, siendo característicos su carácter insidioso y la gravedad de sus complicaciones, de forma que retrasos diagnósticos de solo 8-12 h aumentan la morbimortalidad por peritonitis y sepsis46. La visualización de gas extraluminal se considera diagnóstica de perforación, pero tanto radiografía como ecografía la identifican en menos de un tercio de los casos. La TC no solo detecta pequeñas cantidades de gas extraluminal, sino también zonas de hipoperfusión, engrosamiento mural, edema mesentérico o lesión vascular, que pueden preceder a la perforación. Una TC negativa con sospecha de perforación sería una de las pocas indicaciones para punción-lavado peritoneal.
La lesión pancreática puede no mostrar inicialmente ningún hallazgo clínico. La aparición de dolor abdominal difuso y vómitos son signos de alarma que llevan a realizar un segundo estudio TC que descubre la lesión. La pancreatografía endoscópica identifica posible compromiso ductal, de peor pronóstico46.
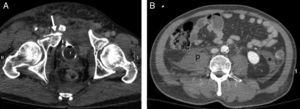
La rotura de la vejiga urinaria suele asociarse con fractura de la pelvis y se confirma mediante TC-cistografía, que permite además diferenciar rotura intra- o extraperitoneal, con diferente enfoque terapéutico, quirúrgico para la primera y conservador para la segunda47 (fig. 5). La lesión traumática del diafragma suele asociarse con un aumento violento de la presión abdominal y entraña riesgo de herniación intratorácica (e isquemia) de las vísceras abdominales. Su diagnóstico se ve facilitado por la revisión meticulosa de los planos sagitales, coronales y axiales de TC, manteniendo un alto nivel de sospecha y buscando los signos específicos46.
Varón de 40 años. Accidente de motocicleta. A) TCCC, plano axial de la pelvis mostrando fractura compleja del anillo pelviano, con fuga de contraste intravesical (sonda de Foley) a tejidos blandos (flecha). B) Plano axial del abdomen demostrando la ausencia de hemoperitoneo. Hematoma retroperitoneal ocupando el músculo psoas derecho (p) y la fascia retromesentérica (*).
El retroperitoneo puede ser asiento de colecciones hemáticas no detectables por FAST, siendo la fractura pelviana la causa más frecuente48. Las alternativas terapéuticas dependerán del estado hemodinámico del paciente, del crecimiento del hematoma y de la presencia de hemorragia activa por TC46.
Imagen en el complejo hipoperfusión-shockLos hallazgos de TC pueden orientar sobre el estado hemodinámico del PTG y sobre la persistencia de hipovolemia46. El conjunto de hallazgos, denominado «complejo de hipoperfusión-shock», se caracteriza por la disminución de calibre de aorta y vena cava inferior, engrosamiento difuso e hiperrealce de la pared intestinal, disminución del realce esplénico y aumento del renal y suprarrenal, aumento del tamaño pancreático y signos de edema suprarrenal49 (fig. 3).
Localización, dotación y estructura idóneas de la sala de tomografía computarizada en los centros de traumatologíaEl factor limitante para el empleo de la TC en pacientes graves ya no es la rapidez de los equipos, sino su lejanía del área de críticos. Para obtener rentabilidad máxima se han de poder estudiar los pacientes más graves41, con tres requisitos: TC adecuada tecnológicamente, ubicada cerca del punto de llegada de PTG y personal entrenado con disponibilidad las 24 h del día y todos los días de la semana (24/7). Idealmente, la sala TC debería estar integrada en el área de resucitación del servicio de urgencias, como ocurre ya en muchos países desarrollados50. Cuando ello no sea posible, rige el principio: «cuanto más cerca, mejor», no siendo aceptable un proyecto nuevo que no la contemple1,13. En su diseño, la seguridad del paciente es la principal consideración, siendo necesarias las aportaciones de todo el equipo de politrauma, en relación con necesidades de equipos de monitorización, gases, material fungible y fármacos. La ubicación del equipo dentro de la sala debe permitir la observación y monitorización continua del paciente. La provisión de servicios debe garantizarse de forma ininterrumpida 24/7, con el entrenamiento adecuado.
Tras la recepción del paciente, y situado ya sobre una mesa polivalente compatible o integrada en el equipo de TC de la sala de reanimación, tras su monitorización, se revisan vía aérea y ventilación, solucionándose eventuales problemas, incluido el establecimiento de una vía aérea definitiva. Aseguradas ambas, y con un adecuado acceso venoso para iniciar una eventual reposición de volumen, se efectúa la exploración TCCC, incluso en pacientes inestables. El radiólogo revisa las imágenes iniciales1,13,32, para identificar lesiones de riesgo vital que requieran tratamiento inmediato e investiga la presencia de hemorragia activa y su origen. Con la información de la exploración clínica, mecanismo lesional, analítica o cualquier otra, se realiza un balance inicial de lesiones objetivables por TC, siguiendo la pauta A, B, C, D, E. Sobre estos datos objetivos se plantea la actuación terapéutica: observación, ingreso en UCI, intervención endovascular o cirugía11,50.
La radiología intervencionista en los traumatismos gravesPuede considerarse una técnica de control de daños, como la compresión manual o el empaquetamiento quirúrgico13. Tras acceder al vaso sangrante, se libera material embolígeno o bien se colocan stents para reforzar la pared arterial dañada, como ocurre en la lesión traumática de la aorta51. Entre otras ventajas, reduce el número de órganos resecados, de laparotomías no terapéuticas, evita el estrés asociado a la cirugía y disminuye requerimientos transfusionales y costes32,51.
La información proporcionada por la TCMD es clave para decidir entre manejo no operatorio e intervención hemostática y, en esta última, acceso endovascular, quirúrgico o mixto. Así, el manejo no operatorio requiere ausencia de sangrado activo, mientras que tanto su presencia como la de un pseudoaneurisma, son indicación de intervención hemostática (figs. 2 y 4). Para la embolización, la angio-TC orienta sobre el punto de sangrado y proporciona una «hoja de ruta» muy útil que reduce tiempo de sala, dosis de radiación y de medio de contraste. Con este planteamiento se consigue el manejo no operatorio de hasta el 95% de las lesiones traumáticas sangrantes52. Será difícil disponer de evidencia de primer nivel para las técnicas endovasculares en trauma, pero existe evidencia de nivel 2 y 3 que apoya su seguridad, eficacia, rapidez y coste-efectividad44,52.
Manejo diagnóstico y terapéutico de la hemorragia traumáticaAunque la lesión neurológica es la primera causa de mortalidad postraumática, la hemorragia responde del 30-40% de muertes y del 80% de la mortalidad precoz intrahospitalaria53. Además de la exanguinación, la hipotensión por pérdida hemática aguda es directamente responsable de la lesión cerebral secundaria y contribuye al desarrollo de fallo multiorgánico1,20,53,54. Se considera que es la primera causa de mortalidad postraumática potencialmente evitable1,20.
El tiempo es un factor crítico en el control de la hemorragia traumática13. En pacientes con traumatismo abdominal, por cada tres minutos de retraso terapéutico se incrementa la mortalidad un 1%55. Si existe inestabilidad hemodinámica, cada hora de retraso en la aplicación de terapéutica hemostática endovascular incrementa el riesgo de muerte un 47%56.
El control de la hemorragia se realiza simultáneamente al tratamiento del shock hipovolémico, con el fin de minimizar el riesgo vital y el de síndrome compartimental secundario54. En la práctica, la selección de pacientes subsidiarios de cirugía inmediata suele establecerse según las características del traumatismo y el grado de respuesta al tratamiento con la información, necesariamente limitada, que aportan técnicas diagnósticas no concluyentes, como radiografía y FAST5,54. Información incompleta y necesidad de rápida respuesta complican la decisión, como demuestra el hecho de que las equivocaciones en el control de la hemorragia traumática constituyen la principal causa de error con resultado de muerte57. Hipotensión no implica necesariamente hemorragia activa, pudiendo obedecer a otras causas de shock (obstructivo, neurogénico), o ser un efecto colateral de la analgesia/anestesia54. La hemorragia puede haber cesado y persistir la hipotensión, cuya ausencia o incluso la respuesta al tratamiento tampoco excluyen shock hemorrágico en fase inicial27. Por último, aunque con mayor frecuencia, el origen de una hemorragia grave es una fractura pelviana, el punto de sangrado puede tener otra localización, intra- o retroperitoneal, o bien ser múltiple, con lo que el planteamiento y abordaje terapéutico serán diferentes20,50.
La cirugía, con planteamiento de «control de daños», ha sido la principal opción terapéutica en el shock hemorrágico, con acceso a la cavidad corporal sangrante y control de la hemorragia mediante sutura, compresión directa o empaquetamiento. Pero, con frecuencia, la cirugía no consigue controlar el sangrado, debiendo complementarse con técnicas endoluminales. La angiografía es de elección ante cualquier sangrado arterial, especialmente de origen pelviano o extraperitoneal, pero su utilidad es limitada cuando existen múltiples focos de sangrado o son de origen venoso, situaciones donde la cirugía abierta es de elección50. El alejamiento de salas de angiografía y quirófanos del área de urgencias hace que tanto la decisión de trasladar a un paciente inestable a cualquiera de ellas como el orden en que se haga tengan impacto sobre la morbimortalidad50.
La guía ATLS reconoce la utilidad de la embolización angiográfica5, pero no del empleo de TC en pacientes inestables. No obstante, es precisamente en ellos donde su utilidad es mayor, y en un centro de trauma convenientemente equipado, la inestabilidad hemodinámica, más que un obstáculo para realizar el estudio con TCCC debiera ser su principal indicación. El riesgo de posponer la cirugía unos minutos es probablemente menor que el de realizarla «a ciegas»1,11–13,33,41. La única forma de estabilizar a un paciente con hemorragia activa es identificar y cortar el sangrado. No tiene sentido retrasar la TC y, eventualmente, la embolización o la cirugía, en espera de una supuesta estabilización «espontánea». Si la situación del paciente no aconseja su traslado a la TC, debe ser trasladado de inmediato al quirófano o a la sala de angiografía, pero las cosas allí pueden no ser exactamente como se imaginaron.
Centros de traumaLas diferencias de mortalidad en PTG pueden alcanzar un 20% entre países de similar nivel económico según dispongan o no de un sistema organizado de atención al trauma y existen indicios de que estos pacientes podrían recibir cuidados subóptimos en hospitales de baja complejidad1,2,4,32. La gran mayoría de los PTG acuden al hospital fuera de horas de trabajo, cuando los profesionales experimentados ya no se encuentran en él, lo que eleva la morbimortalidad («efecto fin de semana»)58. Los traumatismos graves son infrecuentes, menos del 0,2% de la actividad del servicio de urgencias, y muchos hospitales no asisten un caso a la semana1,58. Los mejores resultados (estancia media, UCI, mortalidad) se consiguen cuando la asistencia está a cargo de profesionales experimentados, en centros que atienden a más de 650 PTG/año59. No parece factible ni eficiente que todos los hospitales dispongan de la infraestructura, profesionales y entrenamiento adecuados para atender a PTG, con un planteamiento 24/71. Al igual que en otros países, parece imprescindible la organización de la asistencia a los PTG hacia un modelo en red, con centros de trauma regionales coordinados con otros de segundo nivel1,3,32,58. El indicador relevante que debe regir el funcionamiento de ambos es el tiempo hasta el tratamiento definitivo.
Las funciones principales de la radiología en el manejo del PTG han sido estandarizadas para el ámbito europeo13,60. Básicamente consisten en proporcionar acceso 24/7 a dos servicios fundamentales, uno es la exploración TCCC, con informe experto, de forma inmediata, y el otro la radiología intervencionista para el control de la hemorragia traumática.
El radiólogo a cargo de la TC debe tener experiencia suficiente para recibir al PTG, aplicar el protocolo de exploración adecuado, incluidas las modificaciones oportunas según el patrón de lesiones y situación clínica del paciente, y establecer un balance inicial de lesiones, a modo de revisión primaria TC, que oriente el manejo terapéutico inicial. Se asegurará de que el estudio está completo antes de que el paciente abandone la sala. Finalmente, tras realizar la revisión exhaustiva de todas las imágenes y el oportuno posproceso, emitirá el informe definitivo. La posibilidad de transferir imágenes digitales a distancia permite la teleconsulta especializada. Se considera que los servicios de RM deberían estar disponibles en un plazo de 12 h13.
La disponibilidad de radiología intervencionista se considera hoy obligada en los centros que atienden PTG. Es alternativa a la cirugía o complemento en el manejo conservador de algunas lesiones traumáticas1,51. Mantener una unidad de radiología intervencionista con un planteamiento 24/7, conlleva importantes dificultades de gestión y entrenamiento del personal, por lo que debería estar centralizada en los hospitales de referencia de trauma. El RCR británico establece algunas recomendaciones y estándares sobre el nivel de actualización y equipamiento de las salas de angiografía, su localización próxima al área de urgencias, pautas de transporte de los pacientes graves e inestables y tiempos de respuesta, que fija en 30 minutos13.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.