Varón de 56 años de edad, pescadero de profesión, ex-fumador de 60 cigarrillos al día desde hace 4 años y bebedor de 75g/día. Presenta disnea de mínimos esfuerzos y edemas en los miembros inferiores.
El hemograma, la PCR, la coagulación, el proteinograma y el análisis de orina son normales. Los valores de la bioquímica básica son: glucosa 110; creatinina 1,06; Na 139; K 5,2; LDL 84; CT 141; HDL 41; AST 25; ALT 27; GGT 52; FA 53; TSH 0,9; ferritina 22; Fe 52 y Ca 9,8. La serología de VHC, VHB y VIH son negativas. La serología para virus de Epstein-Barr y CMV son compatibles con infección pasada. En el estudio inmunológico, los ANA y los ENA son negativos. El péptido natriurético tipo B (BNP) está elevado (1.453pg/ml), y el enzima convertidor de la angiotensina (ECA) es de 28μg/l.
En la espirometría, la capacidad vitral forzada (CVF) es del 82%, el volumen espirado máximo (FEV1) del 75% e IT del 73%.
En el ecocardiograma se detecta miocardiopatía dilatada con disfunción biventricular grave, fracción de eyección del 20-25%, insuficiencia mitral moderada-grave e hipoquinesia global grave.
Se realiza resonancia magnética (RM) cardiaca y tomografía computarizada (TC) coronaria. En ellas se aprecian adenopatías mediastínicas de tamaño significativo.
Se instaura tratamiento con nebivolol, ramipril, ivabradina, furosemida y eplerenona.
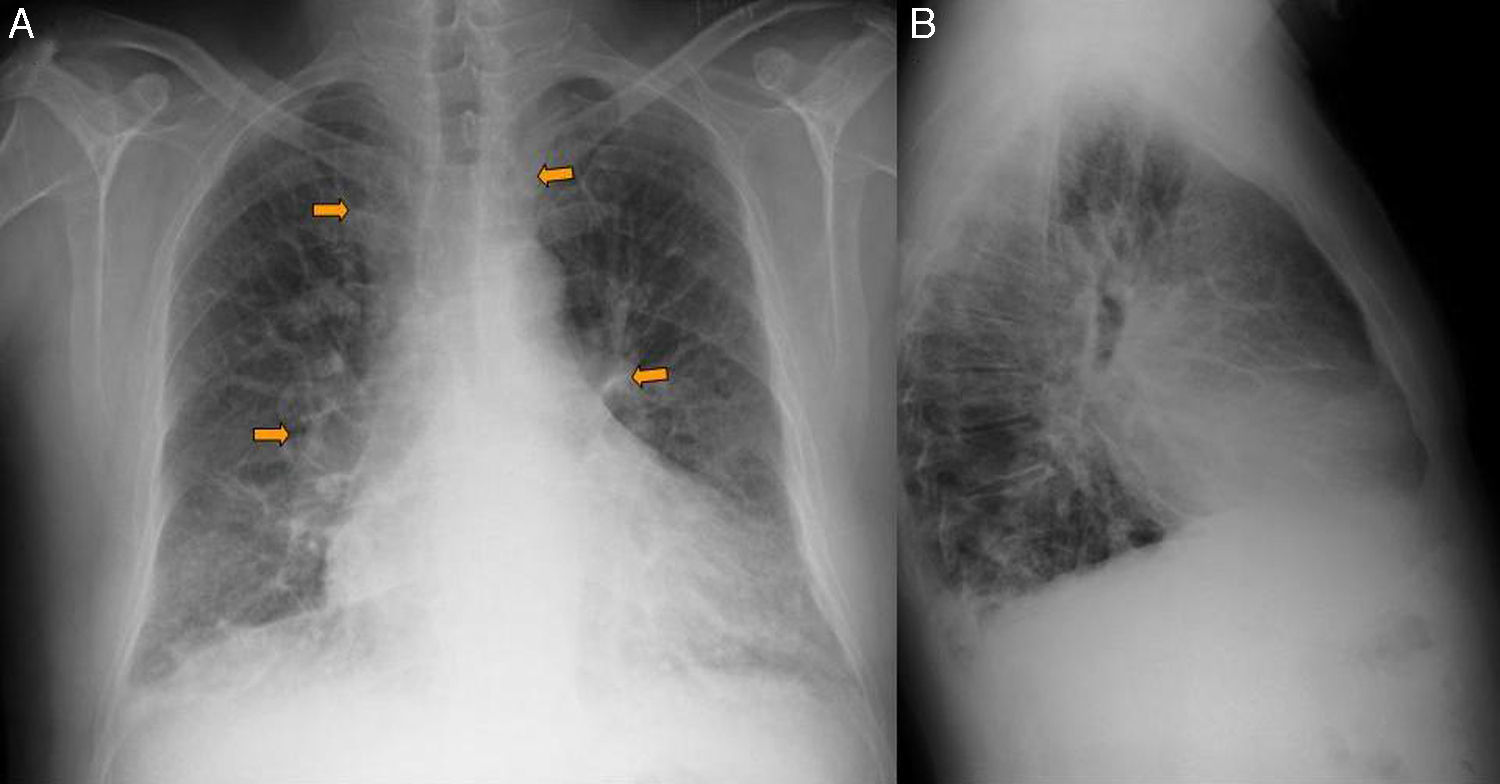
En la radiografía pósteroanterior (PA) y lateral de tórax (figs. 1A y 1B) se observa ensanchamiento mediastínico, patrón retículo-nodular en ambas bases y deformidad en la pared costal izquierda, compatible con fracturas costales antiguas.
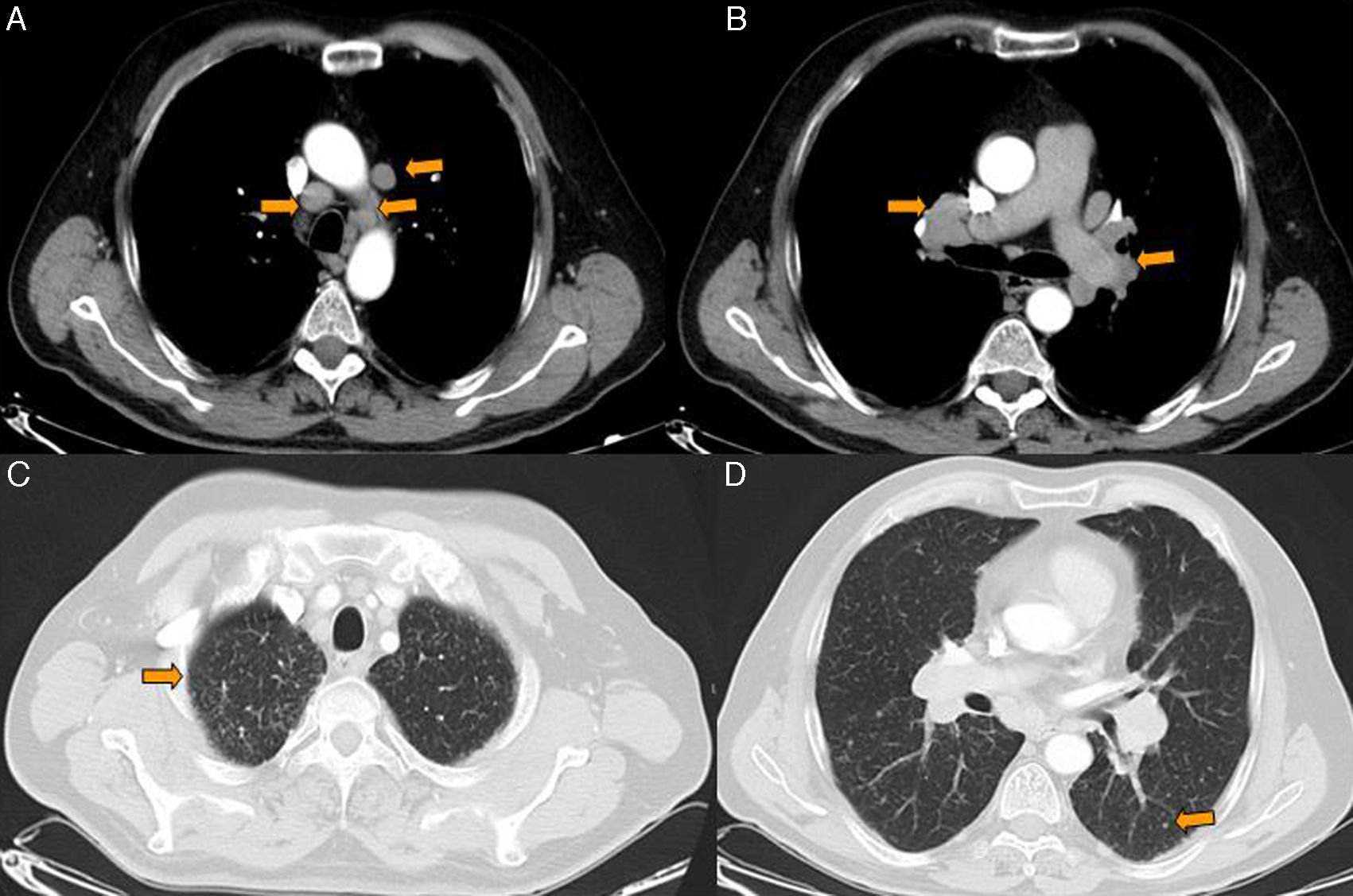
En la TC de tórax se aprecian múltiples adenopatías subcarinales, hiliares y paratraqueales bilaterales en ventana aorto-pulmonar (figs. 2A y 2B). En el parénquima pulmonar se aprecian lesiones nodulares aisladas de 5mm en todos los lóbulos, así como un patrón intersticial con nodulillos milimétricos peribroncovasculares y subpleurales (figs. 2C y 2D).
Se realizan biopsias transbronquial y de adenopatía subcarinal, que resultan negativas para neoplasia, pero no fueron concluyentes para sarcoidosis.
El paciente rechaza la realización de mediastinoscopia, por lo que se realiza tomografía con emisión de positrones (PET), cuyo resultado es sugerente de proceso granulomatoso.
El paciente está clínicamente estable, con afectación pulmonar y ganglionar, que corresponde al grado ii de sarcoidosis, aunque sin diagnóstico de certeza. Se decide realizar tratamiento con esteroides (deflazacort).
Se realiza TC de control tras 6 meses de tratamiento. Desaparece la afectación pulmonar y mejora la miocardiopatía dilatada tras la suspensión de la ingestión de alcohol.
El paciente continúa asintomático desde el punto de vista clínico en las revisiones anuales.
ComentarioLa sarcoidosis es una enfermedad multisistémica de etiología desconocida, caracterizada por la formación de granulomas no necrotizantes. Los órganos afectados presentan acumulación de linfocitos T y de fagocitos mononucleares, granulomas epitelioides no caseificantes y alteraciones de la estructura normal. La etiología y secuencia patogénica exactas permanecen desconocidas.
Su distribución es mundial, con afectación preferente de adultos jóvenes, sobre todo en la tercera década de la vida. La incidencia es 10 veces más alta en la raza negra, especialmente en las mujeres, en las que hay peor pronóstico y mayor tendencia a la cronicidad. El mejor pronóstico corresponde a la forma de presentación aguda con adenopatías hiliares, eritema nudoso o uveítis y en mujeres de raza blanca1.
Manifestaciones clínicas2En el 10-20% de los casos, la sarcoidosis se detecta por primera vez como adenopatía hiliar asintomática. El inicio puede ser agudo o insidioso.
La sarcoidosis aguda supone entre el 20-40% de los casos. Comprende 2 formas de presentación:
- •
Síndrome de Löfgren: adenopatía hiliar, eritema nudoso y artritis aguda que se presenta en uno o ambos tobillos y se extiende para afectar a otras articulaciones.
- •
Síndrome de Heerfordt-Waldenström: hipertrofia parotídea, fiebre, uveítis anterior y parálisis facial.
La sarcoidosis de aparición insidiosa afecta entre el 40-70% de los casos. Los síntomas respiratorios son los más frecuentes, al principio:
- •
Síntomas generales: fiebre, pérdida de peso, anorexia y fatiga.
- •
El pulmón es el órgano más frecuentemente afectado. El 90% de los pacientes tendrá afectación en la radiografía de tórax durante la evolución, con adenopatías hiliares, alveolitis y neumonitis intersticial.
- •
La piel se afecta en el 25% de los casos. Aparece eritema nudoso, placas, erupciones máculo-papulosas, nódulos subcutáneos y lupus pernio.
- •
Uveítis en el 25% de los casos, que puede evolucionar a ceguera.
- •
Vías respiratorias superiores: afectación de la mucosa nasal en el 25% y de la laringe en el 5% de los casos.
- •
Médula ósea y bazo: anemia y trombocitopenia leves.
- •
Hígado: se encuentra afectado entre el 60-90% de las biopsias, pero con escasa relevancia clínica.
- •
Riñón: nefrolitiasis por afectación del metabolismo del calcio.
- •
Las alteraciones del sistema nervioso son variadas: neuropatía craneal/periférica, meningitis crónica, afectación hipofisaria, lesiones ocupantes de espacio y convulsiones.
- •
Corazón: pericarditis, alteraciones del ritmo y/o de la contractilidad.
- •
Sistema músculo-esquelético: lesiones óseas corticales entre el 3-13% de los casos, dactilitis, mono u oligoartritis de rodilla, tobillo y articulaciones interfalángicas proximales.
Se inicia con la historia clínica y la exploración física para descartar exposiciones y otras causas de enfermedad pulmonar intersticial. Debe incluir hemograma completo, estudio de calcio, pruebas de función hepática, ECA, Mantoux y pruebas cutáneas de control, radiografías de tórax, TC torácico de alta resolución, electrocardiograma y pruebas de función respiratoria.
El diagnóstico suele precisar la biopsia del pulmón o del órgano afectado. El lavado broncoalveolar y la gammagrafía pulmonar con galio pueden ser útiles como marcadores de actividad cuando esté indicado el tratamiento.
Diagnóstico4Se basa en hallazgos clínicos, radiológicos e histológicos. La biopsia del pulmón o de otro órgano afectado es obligada para confirmar el diagnóstico antes de empezar el tratamiento, ya que no existe ningún dato analítico en la sangre que sea diagnóstico.
El diagnóstico diferencial incluye las neoplasias, las infecciones y otros procesos granulomatosos.
El patrón radiológico clásico consiste en adenopatías hiliares bilaterales y simétricas con adenopatías paratraqueales derechas (tríada de Garland). A veces se implican otras cadenas ganglionares, tales como las mediastínicas anteriores y las infracarinales.
Los infiltrados parenquimatosos aparecen entre el 40-50% de las ocasiones y son generalmente simétricos, difusos e intersticiales, y predominan los del tipo nodular.
Es menos frecuente el patrón alveolar, representado por opacidades algodonosas mal definidas o por áreas focales nodulares bien definidas, también llamada sarcoidosis de nódulos grandes.
Los cambios secundarios a fibrosis varían desde opacidades lineales cicatriciales localizadas a un patrón más extenso y característico reticular tosco, que afecta a los tercios superior y medio del pulmón desde del hilio. También se ha descrito la enfermedad fibrobullosa apical, y la panalización en estadio final.
Otros hallazgos menos frecuentes son la distribución unilateral de las adenopatías o los infiltrados, el derrame pleural, el neumotórax, la alteración bronquial intrínseca o extrínseca, la cavitación y la calcificación de las adenopatías, incluso en «cáscara de huevo».
El aspecto radiológico no se correlaciona en muchos casos con la clínica, la alteración y la actividad de la enfermedad5.
Se establecen 3 estadios radiológicos, de acuerdo con los hallazgos en la radiografía de tórax, como se muestra en la tabla 16,7.
Estadios de la sarcoidosis
| Estadio | Radiografía de tórax |
|---|---|
| 0 | Normal |
| I | Adenopatías hiliares bilaterales con parénquima normal |
| II | Adenopatías hiliares bilaterales con alteraciones parenquimatosas |
| IIIA | Alteraciones parenquimatosas sin adenopatías con fibrosis pulmonar |
| IIIB | Alteraciones parenquimatosas sin adenopatías sin fibrosis pulmonar |
Muchos casos remiten espontáneamente. La enfermedad ocular, cardiaca, del sistema nervioso central y la pulmonar progresiva son indicadores de iniciar tratamiento con glucocorticoides, habitualmente prednisona; el metotrexato es el tratamiento de segunda línea.
Las alteraciones respiratorias son la mayor causa de morbimortalidad.
La mayoría de los pacientes con enfermedad aguda quedan sin secuelas. En conjunto, el 50% de los pacientes sufrirá cierto grado de disminución orgánica permanente, el 15-20% permanece en actividad o con recurrencias y el 10% fallece como consecuencia directa de la enfermedad.