La hiperplasia benigna de próstata (HBP) es una patología con una alta incidencia. Su diagnóstico y tratamiento son compartidos entre urólogos y médicos de atención primaria. Su manejo consume una enorme cantidad de recursos. La Sociedad Española de Médicos de Atención Primaria (SEMERGEN), la Sociedad Española de Médicos Generales y de Familia (SEMG), la Sociedad Española de Medicina de Familia y Comunitaria (semFYC) y la Asociación Española de Urología (AEU) han elaborado un documento sobre pautas de actuación y seguimiento de la HBP, presentado aquí de manera resumida, en el que se pretende actualizar las guías anteriormente publicadas, en base a las últimas evidencias.
Estas nuevas recomendaciones tienen como objetivo principal sensibilizar al médico de atención primaria y ayudarle en la evaluación diagnóstica, el tratamiento y el seguimiento, además de aportar criterios unificados y consensuados de derivación al segundo nivel asistencial.
Benign prostate hyperplasia (BPH) is a high-incidence condition. Its diagnosis and treatment is shared between urologists and Primary Care physicians. Its management uses up a significant amount of resources. The Spanish Society of Primary Care Physicians (SEMERGEN), the Spanish Society of General Practitioners and Family Doctors (SEMG), the Spanish Society of Family and Community Medicine (semFYC), and the Spanish Association of Urology (AEU) have prepared a document on the management and monitoring of BPH, in which the aim is to incorporate the latest evidence in order to update the previously published guidelines, and present them here in condensed form.
The main objective of these new recommendations is to raise the awareness of Primary Care physicians and assist them in its diagnostic evaluation, treatment and monitoring, as well as providing unified consensus criteria for referral to the secondary care level.
La hiperplasia benigna de próstata (HBP) es una patología con una elevada prevalencia1, pudiendo afectar al 50% de los varones entre 50 y 60 años. La edad es un factor importante en su aparición y desarrollo1 y afecta a la calidad de vida del paciente2.
Su manejo consume una enorme cantidad de recursos, y tanto el diagnóstico como el tratamiento son compartidos entre urólogos y médicos de atención primaria.
La Sociedad Española de Médicos de Atención Primaria (SEMERGEN), la Sociedad Española de Médicos Generales y de Familia (SEMG), la Sociedad Española de Medicina de Familia y Comunitaria (semFYC) y la Asociación Española de Urología (AEU) han elaborado este documento en el que se pretende actualizar, en base a las últimas evidencias, las guías anteriormente publicadas: Criterios de derivación de HBP3 y Pautas de actuación y seguimiento en hiperplasia benigna de próstata4.
Estas nuevas recomendaciones tienen como objetivo principal sensibilizar al médico de atención primaria y ayudarle en la evaluación diagnóstica, el tratamiento y el seguimiento, además de aportar criterios unificados y consensuados de derivación en los casos de HBP complicada o severa, o cuando en el transcurso de la historia natural de la enfermedad aparezcan complicaciones que sean tributarias de ser valoradas en el segundo nivel asistencial.
MetodologíaEl documento ha sido elaborado por un grupo de trabajo perteneciente a las 4 sociedades firmantes del consenso. Para la constitución del grupo de trabajo, cada sociedad ha elegido a especialistas en la materia de reconocido prestigio profesional y científico. La mayoría habían participad en las 2 ediciones previas del consenso. El comité científico, para hacer más operativo el trabajo, se ha dividido en 3 subgrupos, y a cada uno de ellos se le ha responsabilizado de uno de los 3 capítulos en los que se dividió el documento (diagnóstico, tratamiento y seguimiento). Los subgrupos elaboraron un material con el consenso de los integrantes de ese subgrupo, y posteriormente se ha sometido al consenso general de todo el grupo científico firmante del consenso.
Todos los integrantes del grupo de trabajo presentaron una declaración de intereses.
Las recomendaciones que se presentan en este consenso son el resultado de la búsqueda, la evaluación crítica y la síntesis de la evidencia científica existente sobre la HBP. Siempre que ha sido posible, se ha incluido el nivel de evidencia y el grado de recomendación que sustenta cada una de las recomendaciones utilizadas en este documento, siguiendo la clasificación de la Agency for Healthcare Research and Quality (AHRQ) (tabla 1). Las recomendaciones se han llevado a cabo mediante consenso alcanzado en las reuniones del grupo elaborador. Cuando se clasifican las recomendaciones, no existe una relación automática entre nivel de evidencia disponible y grado de la recomendación. En determinadas actuaciones, especialmente procedimientos diagnósticos, no se dispone de ensayos controlados aleatorios, en muchas ocasiones por razones éticas, financieras o de otro tipo, pero el grupo considera que existe una considerable experiencia clínica que apoya el valor de determinada intervención considerándola imprescindible, pues permite adoptar una decisión clínica y un uso racional de los recursos. Las recomendaciones controvertidas o con ausencia de evidencia científica se han resuelto por consenso del grupo de trabajo. En algunas ocasiones las recomendaciones han sido adaptadas de otras guías y contextualizadas en nuestro medio.
Niveles de evidencia científica y grados de recomendación
| Clasificación de las recomendaciones en función del nivel de evidencia disponible según la Agency for Healthcare Research and Quality (AHRQ) |
| Ia. La evidencia científica procede de metaanálisis de ensayos clínicos controlados y aleatorizados |
| Ib. La evidencia científica procede de al menos un ensayo clínico controlado y aleatorizado |
| IIa. La evidencia científica procede de al menos un estudio prospectivo controlado, bien diseñado y sin aleatorizar |
| IIb. La evidencia científica procede de al menos un estudio casi experimental, bien diseñado |
| III. La evidencia científica procede de estudios descriptivos no experimentales, bien diseñados como estudios comparativos, de correlación o de casos y controles |
| IV. La evidencia científica procede de documentos u opiniones de expertos y/o experiencias clínicas de autoridades de prestigio |
| Grados de recomendación |
| A. Existe buena evidencia en base a la investigación para apoyar la recomendación. Recoge niveles de evidencia Ia y Ib |
| B. Existe moderada evidencia en base a la investigación para apoyar la recomendación. Recoge niveles de evidencia IIa, IIb y III. Recoge el nivel de evidencia IV |
| C. La recomendación se basa en la opinión de expertos o en un panel de consenso |
| X. Existe evidencia de riesgo para esta intervención |
La HBP se manifiesta clínicamente mediante los síntomas del tracto urinario inferior (STUI), aunque la presencia de dicha sintomatología no siempre se debe a la HBP.
Los STUI pueden ser de 3 tipos: síntomas de vaciado, posmiccionales o de llenado. La HBP suele manifestarse con sintomatología mixta, por lo que la presencia de un solo tipo de síntomas nos hará dudar de que éstos se deban a HBP2.
Todas las guías de buena práctica clínica en HBP4 coinciden en reconocer como obligatorias las siguientes pruebas: anamnesis detallada, examen físico completo que incluya la realización del tacto rectal y análisis de orina.
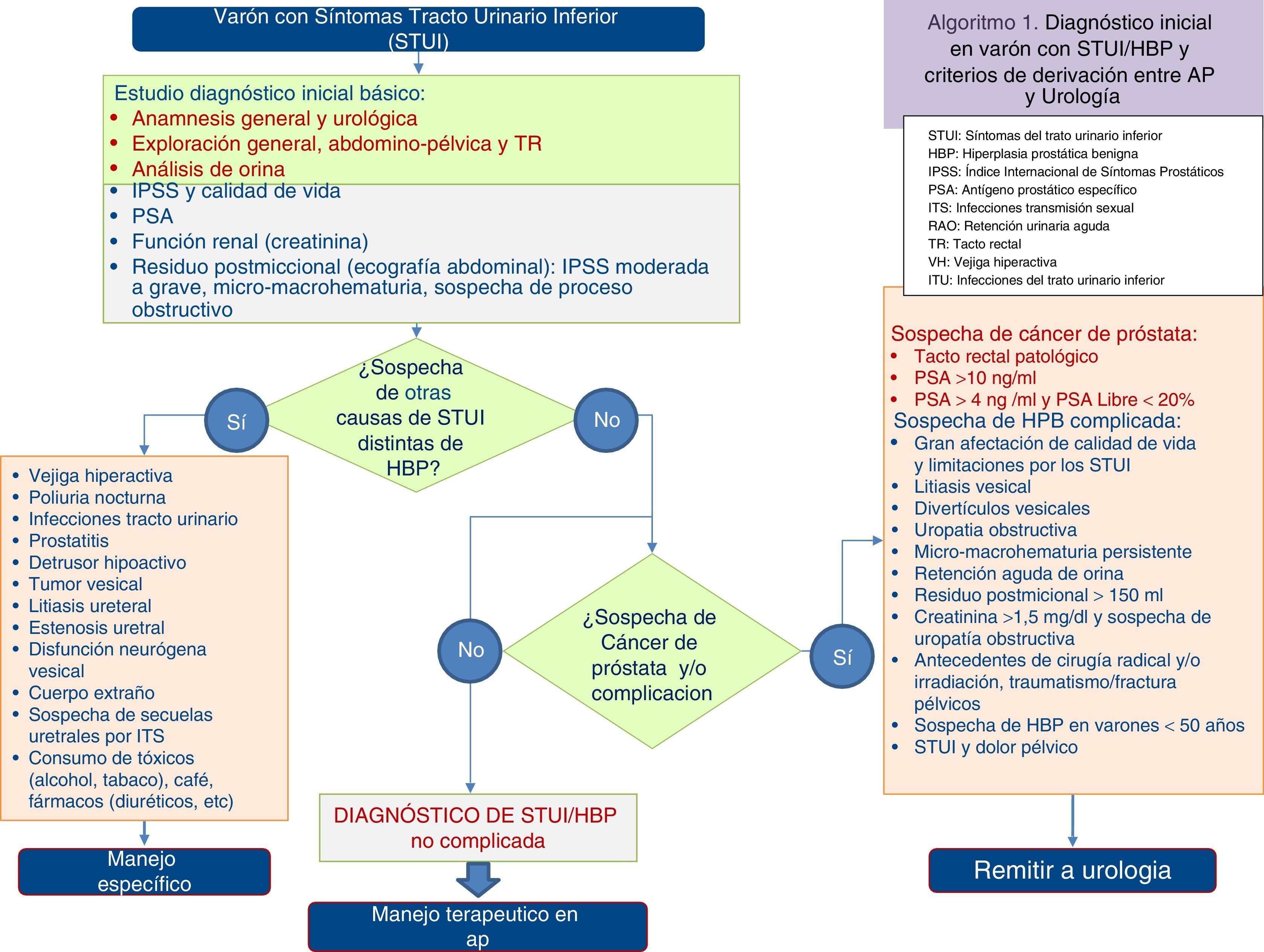
En atención primaria el resto de las pruebas diagnósticas se pueden clasificar en función de su prioridad como pruebas recomendadas, opcionales o no recomendadas3,4 (tabla 2). Utilizando las pruebas obligatorias y recomendadas, se obtiene un valor predictivo positivo cercano al 80%5. Desde atención primaria se puede diagnosticar la HBP no complicada sin necesidad de utilizar inicialmente en su diagnóstico pruebas de imagen y/o funcionales3 (fig. 1). Tras la evaluación inicial, se remitirán a la consulta de urología aquellos pacientes que requieran ampliar el estudio diagnóstico (fig. 1).
Clasificación, según prioridad, de las pruebas diagnósticas de hiperplasia benigna de próstata en atención primaria
| Obligatorias |
| Historia clínica: general y urológica |
| Examen físico: general y abdominogenital |
| Tacto rectal |
| Urianálisis |
| Recomendadas |
| IPSS y calidad de vida |
| PSA |
| Función renal |
| Medición del residuo posmiccional |
| Eco abdominal (STUI moderados-graves) |
| Opcionales |
| Flujometría |
| Diario miccional |
| Valorar la función sexual (cuestionarios SHIM-IIFE5) |
| No recomendadas |
| Citología |
| Cistoscopia |
| Eco transrectal |
| Urografía endovenosa |
| TAC |
| RMN transrectal |
Recomendadas: cuando su uso se generaliza a todos los pacientes con STUI al existir suficiente evidencia del beneficio de su empleo.
Opcionales: su elección dependerá de los resultados obtenidos en las pruebas iniciales, recomendadas y del profesional que las solicita.
No recomendadas: no existe suficiente evidencia de beneficio con su uso rutinario; se utilizarán únicamente en circunstancias especiales o en ensayos clínicos.
IPSS: International Prostate Symptoms Score; PSA: antígeno prostático específico; RMN: resonancia magnética nuclear; SHIM-IIFE5: Sexual Health Inventory for Men; STUI: síntomas del tracto urinario superior; TAC: tomografía axial computarizada.
Es un procedimiento fundamental que permite descartar otro tipo de patologías distintas de la HBP que cursen con STUI. Se deberá recoger la siguiente información:
- •
Antecedentes patológicos médicos y quirúrgicos.
- •
Tratamientos actuales con fármacos que pueden favorecer la presencia de STUI1,3,4,6.
- •
Presencia de enfermedades que causen STUI.
- •
Hábitos higiénico-dietéticos que favorecen la presencia de STUI.
- •
Presencia de disfunciones sexuales por su asociación con otros trastornos urológicos.
- •
Presencia de alteraciones de la función vesical.
- •
Antecedentes de infecciones de transmisión sexual.
Se recomienda emplear el cuestionario International Prostate Symptoms Score (IPSS)3,4,6, validado y traducido al castellano7.
Exploración física general, abdomino-pélvico-genital y tacto rectal (nivel de evidencia III, grado de recomendación A-B)6Se deberá explorar toda el área abdomino-pélvico-genital para descartar alteración de la puñopercusión en ambas fosas renales, presencia de globo vesical o masas pélvicas, patologías testiculares o del epidídimo (epididimitis, hidrocele, varicocele y masas induradas), valoración del meato uretral para descubrir posibles obstrucciones al flujo (estenosis, hipospadias) o la presencia de supuraciones del glande2,6.
En la valoración inicial de todos los varones con STUI se debe realizar además un tacto rectal (nivel de evidencia III, grado de recomendación A). Cualquier hallazgo sospechoso en la exploración del tacto rectal debe remitirse a urología para descartar la presencia de un cáncer de próstata. Ante la sospecha de neuropatía/vejiga neurógena, la integridad neurológica de la metámera S2-4 se comprueba mediante la valoración del reflejo bulbocavernoso2. Próstatas >40cc pueden aumentar el riesgo de complicaciones como retención aguda de orina (RAO) y necesitar tratamiento quirúrgico8.
Urinoanálisis (nivel de evidencia III, grado de recomendación A)6Es una prueba sencilla que permite realizar un diagnóstico diferencial1,3,4,9. Sirve para detectar la presencia de nitritos, glucosuria, leucocituria, hematuria y proteinuria2,6,9. La hematuria en pacientes con HBP suele ser consecuencia de la congestión glandular, carcinoma vesical o litiasis, por lo que debe confirmase mediante sistemático de orina, sedimento y anormales6. La leucocituria puede ser indicativa de infección, por lo que se deberá realizar un urocultivo. Si resultara negativo, solicitaremos una citología de orina para descartar neoplasia y un cultivo de orina específico de micobacterias para descartar tuberculosis genitourinaria2.
Función renal (nivel de evidencia III, grado de recomendación A)6Se aconseja la determinación de creatinina en la evaluación inicial de paciente con HBP si hubiese sospecha de un proceso obstructivo que genere insuficiencia renal o ante la presencia de hidronefrosis6. En la actualidad se consideran más indicativos de fallo renal los valores de filtrado glomerular4,6,9.
Antígeno prostático específico (Nivel de evidencia Ib, grado recomendación A)Es un marcador específico de crecimiento prostático. De manera aislada el antígeno prostático específico (PSA) carece de sensibilidad como marcador de carcinoma prostático3. El valor del PSA es de gran utilidad para ayudar a predecir la evolución natural de la HBP10 y para evaluar el riesgo de cirugía relacionado con la HBP y/o desarrollo de RAO6. Valores de PSA >1,4ng/ml triplican el riesgo de RAO11.
Los valores de PSA establecidos para detectar volúmenes prostáticos mayores de 30cc según la edad serían:
- •
1,4 ng/ml en hombres de 50-59 años.
- •
1,5 ng/ml en hombres de 60-69 años.
- •
1,7 ng/ml en hombres de 70-79 años
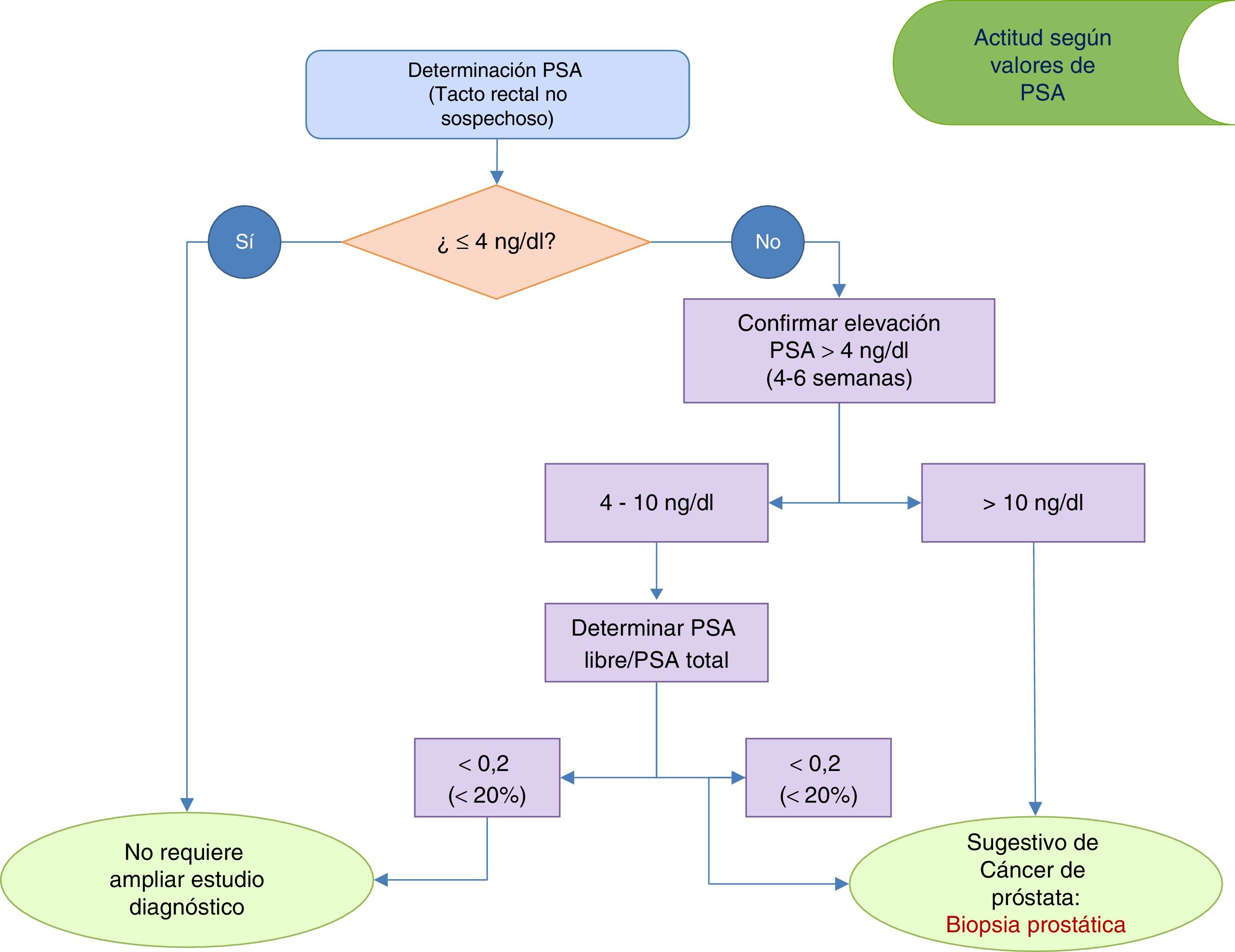
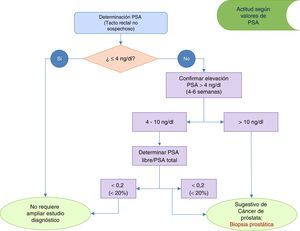
En la figura 2 se muestra la actuación clínica recomendada según los niveles de PSA detectados en la valoración inicial. Valores de PSA>4ng/ml deben confirmarse en 4-6 semanas, tras lo cual valores de PSA>10ng/ml serían indicativos de derivación al urólogo para la realización de una biopsia guiada por ecografía3,4. Ante valores confirmados de PSA entre 4-10 ng/ml se aconseja determinar PSA libre y PSA libre/PSA total.
Medición del residuo posmiccional mediante ecografía abdominal (nivel de evidencia III, grado de recomendación B)6Se aconsejan la determinación basal del residuo posmiccional en los pacientes con mayor riesgo de progresión (sintomatología moderada a grave)6. La ecografía es el método de elección para la medida semicuantitativa del residuo posmiccional. Un nivel basal elevado de volumen posmiccional se asocia con un mayor riesgo de deterioro de los síntomas6. Se consideran potencialmente patológicos los residuos superiores a 50ml.
La ecografía abdominal determina, con mayor exactitud que el tacto rectal, el volumen y la forma de la próstata y permite objetivar las anomalías que se generan sobre el tracto urinario inducidas por la HBP12. Se recomienda la realización de ecografía abdominal en pacientes con STUI/HBP en los que se sospeche la presencia de complicaciones3,4 (sospecha de residuo posmiccional patológico, sospecha de uropatía obstructiva, sospecha de patología neuropática, sintomatología grave, macro o microhematuria, globo vesical, antecedentes de urolitiasis).
TratamientoLos objetivos del tratamiento de los varones con STUI/HBP son mejorar los síntomas y la calidad de vida, evitar la progresión clínica de la enfermedad y disminuir el riesgo de complicaciones y/o la necesidad de cirugía por la enfermedad4,6,9.
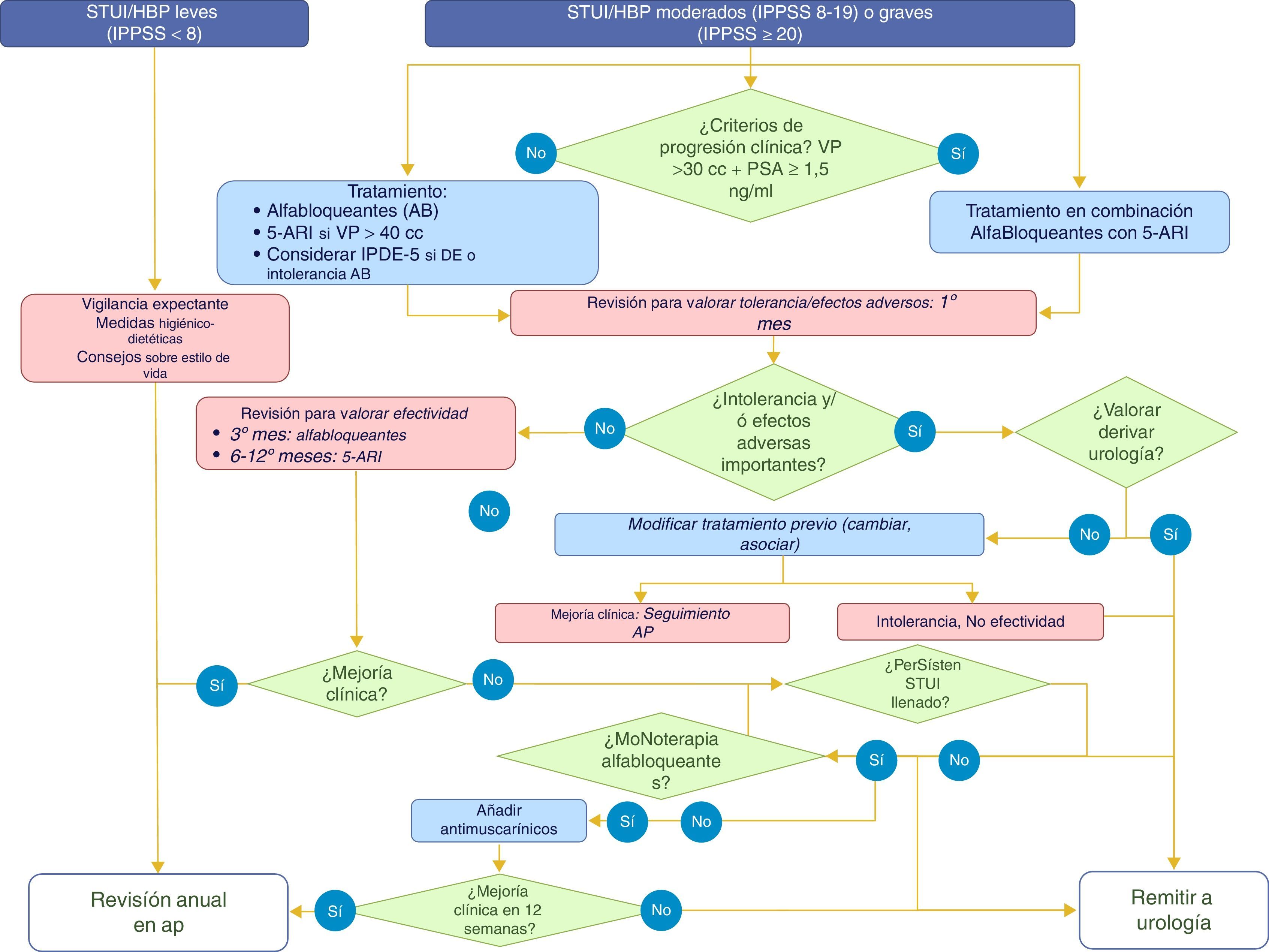
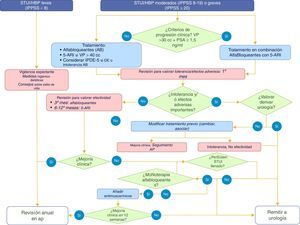
La decisión sobre el tratamiento de los pacientes con STUI/HBP se debe adoptar tras su estratificación en función de riesgo de progresión clínica, con el objetivo de identificar e intensificar el tratamiento en aquellos pacientes con mayor riesgo de progresión (nivel de evidencia Ia, grado de recomendación A). Existen una serie de factores de riesgo de progresión de la HBP validados en diferentes estudios13,14. La estratificación se debe realizar en función de la edad (mayores de 50años), de la gravedad de la sintomatología (moderada a grave), del volumen prostático (≥30cc o gradoii/iv en tacto rectal) y nivel de PSA (≥1,5ng/ml) (nivel de evidencia 1b, grado de recomendación A) (fig. 3).
Se recomienda realizar una vigilancia activa periódica (nivel de evidencia Ia, grado de recomendación A) en los pacientes asintomáticos o con síntomas leves, con buena calidad de vida y sin un aumento del tamaño de la próstata. En este grupo de pacientes se puede retrasar la aparición de los síntomas o su progresión realizando cambios en el estilo de vida y reforzando una serie las medidas higiénico-dietéticas (nivel de evidencia Ib, grado de recomendación A)15-17. Factores como la obesidad, el síndrome metabólico, la diabetes o el sedentarismo aumentan el riesgo de progresión/empeoramiento de los STUI/HBP.
Tratamiento farmacológicoEstá indicado en pacientes con síntomas de intensidad moderada a grave que repercuten en la calidad de vida, en ausencia de complicaciones y sin una indicación absoluta de cirugía (nivel de evidencia Ia, grado de recomendación A). La tabla 3 muestra las características de los tratamientos farmacológicos disponibles.
Características de los tratamientos farmacológicos disponibles
| Tipo tratamiento | Rapidez de inicio | Mejoría STUI | Cambio flujometría (Qmax) | Tamaño prostático | Volumen residual posmiccional | Progresión clínica y/o complicaciones | Evidencia recomendación |
|---|---|---|---|---|---|---|---|
| Espera vigilada | Meses | + | ? | 1b/A | |||
| Alfabloqueantes | Días | ++ | ++ | −/+ | +++ Síntomas | Ia/A | |
| 5-ARI | Meses | + | ++ | +/++ | − | +++ Síntomas ++ RAO Cirugía | Iab/A |
| Alfabloqueantes + 5-ARI | Días | ++ | ++ | +/++ | −/+ | 1b/A | |
| IPDE-5 Tadalafilo | Días | ++ | −/+ | −/+ | ? | Ia/A | |
| Antimuscarínicos | Semanas. | ++ STUI vaciado | + | ? | − | ||
| Alfabloqueantes + antimuscarínicos | Días | ++ | ++ | ? | 1b/B |
5 ARI: inhibidores de la 5-α-reductasa; IPDE5: inhibidores de la fosfodiesterasa tipo 5; PSA: antígeno prostático específico; RAO: retención aguda de orina; STUI: síntomas del tracto urinario inferior.
Los agentes fitoterapéuticos más empleados tradicionalmente son Serenoa repens y Pygeum africanum.
Estudios publicados han mostrado resultados que oscilan desde una eficacia moderada, similar a placebo, hasta una mejoría significativa en el control de los síntomas (nicturia) y medidas del flujo urinario, similares a tamsulosina18,19. En ningún estudio los agentes fitoterapéuticos han demostrado mejoras significativas en el tamaño de la próstata, en la obstrucción del tracto urinario inferior o en la progresión de la enfermedad20.
Actualmente no existen datos basados en estudios clínicos aleatorizados que permitan recomendar los extractos de fitoterapia como un tratamiento específico de los STUI/HBP.
Bloqueantes de los receptores alfa-1-adrenérgicosLos alfabloqueantes, preferentemente uroselectivos y de acción prolongada, son fármacos de primera línea en pacientes con STUI/HBP moderada a grave y próstatas de menor tamaño (<40cc). Además son útiles para el uso intermitente en pacientes con intensidad fluctuante de los síntomas que no necesitan tratamiento a largo plazo (nivel de evidencia Ia, grado de recomendación A).
Son fármacos que actúan sobre el componente dinámico de la obstrucción al flujo de salida de la orina en HBP.
Los alfabloqueantes autorizados para el tratamiento de los STUI/HBP muestran diferente afinidad por los receptores alfa-1: terazosina, doxazosina y alfuzosina son menos selectivos al actuar sobre los receptores alfa-1A, 1B, y 1D. La tamsulosina —con una selectividad predominante sobre los receptores alfa-1A y 1D— y la silodosina —antagonista muy potente y selectivo de los receptores alfa-1A— son considerados uroselectivos. La eficacia clínica global de todos los alfabloquentes es muy similar21, y en general no depende del tamaño de la próstata o de la edad.
Los principales efectos secundarios son cardiovasculares (hipotensión postural, mareos, palpitaciones, edema periférico, síncope), sobre el sistema nervioso central (fatiga, astenia, cefalea, somnolencia), rinitis y trastornos eyaculatorios6,9,22. Los uroselectivos son en general mejor tolerados. Todos deben evitarse si existen antecedentes de hipotensión ortostática. Terazosina y doxazosina están contraindicados en el uso conjunto con inhibidores de la fosfodiesterasa tipo5, y el resto deberían usarse con precaución. Los menos uroselectivos deberían administrarse en dosis nocturnas, titulando la dosis.
Inhibidores de la 5-alfa-reductasaLos inhibidores de la 5-alfa-reductasa (5-ARI) son la opción terapéutica recomendada para tratamiento a largo plazo en pacientes con sintomatología moderada a grave, especialmente en aquellos con próstatas de mayor tamaño (>40cc) (nivel de evidencia Ia, grado de recomendación A).
Actúan sobre el crecimiento glandular reduciendo el volumen prostático y mejorando el componente obstructivo estático al flujo de salida vesical de la HBP.
Los principales 5-ARI comercializados son finasterida y dutasterida. En tratamientos superiores a un año, además de reducir el riesgo de progresión de los síntomas, reducen en un 50% el riesgo de complicaciones como la RAO y la necesidad de intervención quirúrgica23,24. Además, los 5-ARI reducen las cifras de PSA al menos un 50% de su valor inicial a los 6 meses de tratamiento25.
La incidencia de eventos adversos es baja y disminuyen con el uso. El perfil de efectos adversos a largo plazo es similar en ambos fármacos: disfunción eréctil (5-8%), disminución de la libido (2-6%), reducción del volumen eyaculatorio (5%) o trastornos en la eyaculación (1,5-2%) y ginecomastia (1,3-3%)24.
Inhibidores de la fosfodiesterasa 5El tadalafilo, un inhibidor de la fosfodiesterasa5 (IPDE-5), a 5mg/día podría ser una opción en pacientes con STUI/HBP moderados a graves seleccionados, especialmente los que padecen disfunción eréctil (nivel de evidencia Ia, grado de recomendación A)26,27. También se podrían emplearse como monoterapia en pacientes que no toleran los alfabloqueantes o asociados a 5-ARI en varones que empeoraron la función eréctil durante el tratamiento con 5-ARI (nivel de evidencia IIA, grado de recomendación B).
Los efectos adversos más frecuentes son cefalea, dolor de espalda, rubor facial y dispepsia. Están contraindicados en pacientes isquémicos recientes (IAM, ACVA), con hipotensión, presión arterial mal controlada, insuficiencia renal y/o hepática significativa, neuropatía óptica isquémica anterior tratados con nitratos y en tratados con los alfabloqueantes menos uroselectivos (doxazosina o terazosina).
Combinación de alfabloqueantes y 5-ARILa terapia combinada de un alfabloqueante y un 5-ARI se recomienda como tratamiento a largo plazo (4-7años) en pacientes con STUI/HBP moderados a graves con otros factores de riesgo de progresión clínica: volumen prostático moderado (≥ 30cc medido por ecografía o ≥ii/iv por tacto rectal) o grande (≥40cc medido por ecografía) y PSA ≥1,5ng/dl (nivel de evidencia Ia, grado de recomendación A)28–30.
Las 2 únicas asociaciones que han demostrado su eficacia en ensayos clínicos a largo plazo son dutasterida/tamsulosina y finasterida/doxazosina. Al no existir datos de seguridad y eficacia con otras asociaciones, se recomienda no emplear otras combinaciones diferentes.
En general los efectos adversos son significativamente más frecuentes durante el tratamiento combinado que en cualquier monoterapia, aunque son consistentes con los descritos en monoterapia28,29,31.
Combinación de alfabloqueantes y antimuscarínicosLa combinación antimuscarínicos asociados a alfabloqueantes se podría reservar como segunda línea de tratamiento en varones con síntomas moderados a graves, en los que persisten los síntomas de almacenamiento, a pesar del tratamiento con alfabloqueantes (nivel de evidencia 1b, grado de recomendación B). En estos casos se recomienda usar en pacientes seleccionados, descartando situaciones que indiquen alto riesgo de obstrucción del tracto urinario inferior (Qmax< 0ml/s, residuo posmiccional >200ml, síntomas graves, volumen prostático >50cc o historia de RAO)30 y realizar un control preciso y periódico del residuo posmiccional cada 4-6meses.
Los antimuscarínicos reducen la hiperactividad vesical y aumentan la capacidad funcional de la vejiga, mejorando preferentemente los síntomas de llenado.
La monoterapia con antimuscarínicos tiene usos muy limitados. Podría estar indicada en varones con STUI/HBP exclusivamente de llenado y vejiga hiperactiva, tras descartar suficientemente obstrucción del tracto urinario inferior (tabla 4).
Recomendaciones para el uso de antimuscarínicos
| Antimuscarínico | Antimuscarínico + α-Bloqueantes |
|---|---|
| Recomendado STUI de llenado sin STUI de vaciado con sospecha de vejiga hiperactivaa | Recomendado HBP y síntomas de llenado que no han respondido a tratamiento con alfabloqueantesb |
| No recomendado STUI de vaciado Riesgo de RAO como resultado de: • Aumento del volumen prostático (> 50 cc) • Valores PSA sérico > 1,4 ng/ml • Disminución del flujo miccional (Qmax < 8 ml/s) • IPSS > 19 puntos • Volumen residual > 200 ml | No recomendado STUI de llenado con historia muy significativa de STUI de vaciado o en los hombres con importante clínica obstructiva por HBP y aumento del residuo miccional |
El seguimiento clínico en los casos de STUI/HBP que no requieren tratamiento quirúrgico debe realizarse por el médico de familia en atención primaria6. En la tabla 5 se muestran las situaciones en las que se recomienda la derivación a urología. La figura 3 describe el manejo del paciente ante diferentes situaciones durante su seguimiento.
Criterios de derivación de atención primaria a atención urológica hospitalaria durante el seguimiento
| Situaciones en las que se recomienda derivación a urología |
|---|
| 1. Pacientes que, tras iniciar el tratamiento farmacológico de la HBP, no responden al tratamiento (no modificación de IPSS) o presentan una respuesta clínica insuficiente, que definimos como un descenso inferior a 4 puntos en el cuestionario IPSS, respecto al resultado basal antes del tratamiento: • Después de 3 meses de tratamiento con alfa-bloqueantes • Después de 3 meses de tratamiento con IPDE-5 • Después de 3 meses de tratamiento combinado de alfa-bloqueantes con antimuscarínicos • Después de 6 meses de tratamiento combinado de alfa-bloqueantes con 5-ARI • Después de 6 a 12 meses de tratamiento con 5-ARI en monoterapia 2. Cuando durante el seguimiento de la enfermedad, en pacientes que habían respondido al tratamiento farmacológico de la HBP, se agraven los síntomas y presenten un aumento de la puntuación del IPSS igual o superior a 4 puntos Signos de carcinoma de próstata: tacto rectal patológico, PSA > 10 ng/ml o PSA > 4 ng/ml y PSA libre <20%. 3. Retención aguda de orina 4. Elevación de la creatinina sérica por encima de 1,5 mg/dl secundaria a uropatía obstructiva 5. Vejiga neurógena por enfermedad neurológica concomitante 6. Agravamiento de su patología con residuos posmiccionales altos (> 150 cc), divertículos vesicales, litiasis vesicales, hematuria de repetición o infecciones urinarias de repetición 7. En pacientes tratados con 5-ARI, una elevación del PSA mayor o igual a 0,3 ng/ml respecto al nivel más bajo obtenido durante el tratamiento, confirmada y mantenida a las 4-6 semanas |
5-ARI: inhibidores de la 5-α-reductasa; HBP: hiperplasia benigna de próstata; PSA: antígeno prostático específico; STUI: síntomas del tracto urinario inferior.
Las recomendaciones respecto al seguimiento para todas las modalidades de tratamiento conservador o quirúrgico se basan en datos empíricos o en consideraciones teóricas, pero no en estudios basados en evidencias (nivel de evidencia III-IV, grado de recomendación C).
Podemos concretar las siguientes situaciones:
Pacientes con síntomas leves (IPSS 0-7) en tratamiento no farmacológico.Requieren únicamente un seguimiento anual mientras el aumento del IPSS sea menor de 4 puntos en cada revisión. Si por el contrario hay empeoramiento de la sintomatología acompañado de aumento del IPSS≥4 puntos en dicha revisión, se revaluará al paciente solicitando las mismas pruebas que en la primera valoración.
Pacientes con síntomas moderados (IPSS 8-19) o graves (IPSS>20) con tratamiento farmacológicoPacientes tratados con alfabloqueantes, IPDE-5 y/o antimuscarínicos- •
Seguimiento al primer mes para valorar posibles efectos adversos (anamnesis). En caso de intolerancia, se cambiará de tratamiento.
- •
Seguimiento al tercer mes para valorar la eficacia de la medicación (anamnesis con IPSS y valoración del cumplimiento). Si no hay mejoría (disminución del IPSS<4 puntos), se valorará cambio de tratamiento o derivación a urología; si hay mejoría (disminución del IPSS≥4 puntos), revisión anual.
- •
Seguimiento anual (anamnesis con IPSS, valoración del cumplimiento y PSA cada 4años). Si presenta empeoramiento de los síntomas con aumento de la puntuación del IPSS≥4 puntos o el valor del PSA≥1,5ng/ml, se deberá revaluar al paciente: exploración física con tacto rectal, tira reactiva de orina/sedimento de orina, bioquímica (glucemia, creatinina y PSA) y ecografía urológico-abdominal para descartar uropatía obstructiva, valorar el tamaño de la glándula prostática y el residuo posmiccional.
Si se cumplen los criterios de progresión, se cambiará a la combinación de alfabloqueante con 5-ARI.
Pacientes tratados con 5-ARI en monoterapia o combinado con alfabloqueantes- •
Seguimiento al primer mes para valorar posibles efectos adversos (anamnesis). En caso de intolerancia, se cambiará de tratamiento.
- •
Seguimiento al sexto mes para valorar la eficacia de la medicación (anamnesis, IPSS, valoración del cumplimiento y PSA). Si no hay mejoría (disminución del IPSS<4 puntos) se derivarán a urología; si hay mejoría (disminución del IPSS≥4 puntos), revisión anual. Se solicitará la PSA para confirmar una reducción del 50% respecto del valor antes de iniciar tratamiento.
- •
Seguimiento anual (anamnesis, IPSS, valoración del cumplimiento y PSA). Elevación del PSA mayor o igual a 0,3ng/ml respecto al nivel más bajo obtenido durante el tratamiento, confirmada y mantenida a las 4-6 semanas, indicará derivación a urología para descartar un cáncer de próstata. Si presentan empeoramiento de los síntomas con aumento de la puntuación del IPSS≥4 puntos o el valor del PSA≥1,5 ng/ml, se deberá revaluar al paciente.
Son pacientes monitorizados habitualmente por urología, por lo que cualquier recidiva de los síntomas deberá ser valorada por el urólogo.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
El trabajo ha sido corporativo, con un nivel similar de responsabilidad, de distribución y elaboración del trabajo. Por este motivo hemos decidido una ordenación alfabética de los autores atendiendo al primer apellido, sin que en ningún momento signifique diferente nivel de participación en la elaboración del artículo.