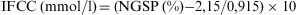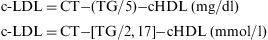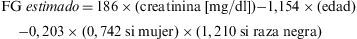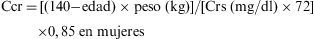En el paciente diabético se han de realizar analíticas para conocer su control metabólico, así como los factores de riesgo cardiovascular. En este artículo se analizan las determinaciones analíticas recomendadas y la frecuencia de su realización.
La hemoglobina glucosilada es el parámetro que valora el control metabólico; hemos revisado el consenso para la armonización de los resultados y la reciente aceptación de esta determinación para el diagnóstico de diabetes tipo 2. Para el estudio de la dislipemia diabética hemos explicado todos los parámetros que son útiles, aunque el colesterol LDL es el aceptado para el diagnóstico y seguimiento. Para la valoración de la nefropatía diabética se utiliza la excreción urinaria de albúmina y la creatinina sérica para estimar el filtrado glomerular. Debido a que la disfunción tiroidea es común en los pacientes diabéticos, también se recomienda la determinación de TSH.
Laboratory tests must be performed on diabetic patients in order to monitor metabolic control and their cardiovascular risk factors. In this paper, we review the recommended analytical determinations and the frequency of performing them.
Glycosylated haemoglobin is the parameter used for assessing metabolic control. We have reviewed the Consensus for result harmonisation and the recent acceptance of this determination for the diagnosis of type 2 diabetes. We have explained all useful parameters for the study of diabetic dyslipidaemia, although LDL cholesterol is the accepted parameter for diagnosis and follow-up. Albumin excretion in urine is used in order to assess diabetic nephropathy and serum creatinine is used in order to assess glomerular filtration. As thyroid dysfunction is common in diabetic patients, TSH determination is recommended.
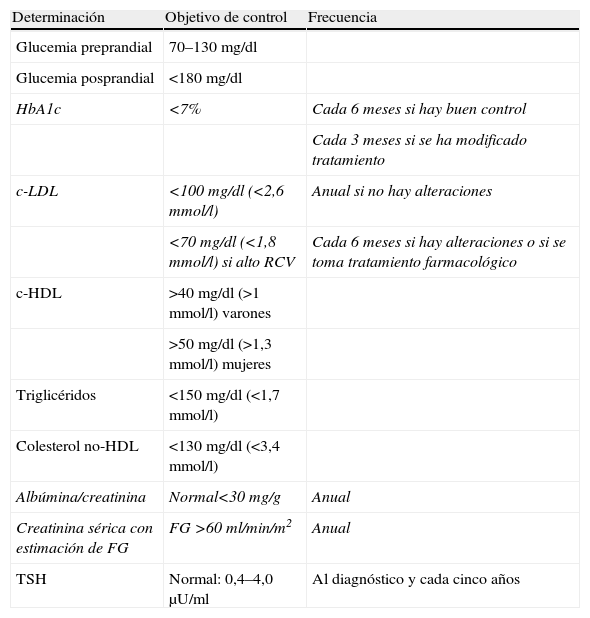
En el control y seguimiento del paciente diabético precisamos la realización de analíticas para la valoración de distintos parámetros: el control glucémico, mediante la determinación de la hemoglobina glucosilada (HbA1c), el control del perfil lipídico, estudiar si hay afectación de la función renal y descartar alteraciones tiroideas (tabla 1).
Determinaciones, objetivos de control y frecuencia de realización. En cursiva: determinaciones de obligada realización
| Determinación | Objetivo de control | Frecuencia |
| Glucemia preprandial | 70–130mg/dl | |
| Glucemia posprandial | <180mg/dl | |
| HbA1c | <7% | Cada 6 meses si hay buen control |
| Cada 3 meses si se ha modificado tratamiento | ||
| c-LDL | <100mg/dl (<2,6mmol/l) | Anual si no hay alteraciones |
| <70mg/dl (<1,8mmol/l) si alto RCV | Cada 6 meses si hay alteraciones o si se toma tratamiento farmacológico | |
| c-HDL | >40mg/dl (>1mmol/l) varones | |
| >50mg/dl (>1,3mmol/l) mujeres | ||
| Triglicéridos | <150mg/dl (<1,7mmol/l) | |
| Colesterol no-HDL | <130mg/dl (<3,4mmol/l) | |
| Albúmina/creatinina | Normal<30mg/g | Anual |
| Creatinina sérica con estimación de FG | FG >60ml/min/m2 | Anual |
| TSH | Normal: 0,4–4,0μU/ml | Al diagnóstico y cada cinco años |
La hemoglobina del hematíe tiene capacidad para reaccionar con la glucosa circulante formando un complejo estable (HbA1c). La reacción de formación de esta hemoglobina es lenta, aparentemente irreversible y proporcional a la cantidad de glucosa presente en el medio, por lo que refleja la cifra media de glucemia de un periodo de 6 a 8 semanas previo a la extracción de la muestra de sangre, dado el tiempo de vida promedio del eritrocito de 120 días. En la actualidad sus resultados se expresan como el porcentaje del total de la hemoglobina. Las cifras de HbA1c deben evaluarse con precaución en los pacientes con diabetes inestable ya que en estos pacientes las cifras de glucemia fluctúan durante el día.
Constituye el mejor parámetro de control glucémico ya que se correlaciona con la aparición de complicaciones micro y macrovasculares a largo plazo.
El «objetivo de control» será «HbA1c <7%». Este parámetro es el que se utilizará para evaluar el control metabólico. Se realizarán «determinaciones cada 6 meses» en pacientes que han conseguido el objetivo y están muy estables y «cada 3 meses», hasta conseguir los objetivos, si se ha modificado el tratamiento.
Esta determinación no es útil para el diagnóstico en determinadas situaciones que afecten a la supervivencia de los eritrocitos o disminuyan su vida media (hemorragias agudas, anemia hemolítica o ferropénica, transfusión sanguínea), así como en pacientes diabéticos con insuficiencia renal crónica y anemia tratada con eritropoyetina (por la presencia de hematíes jóvenes), en hemoglobinopatías y en el embarazo (por la hemodilución)1.
Nuevo consenso para la armonización de resultados de HbA1c2En la actualidad los análisis para la determinación de HbA1c no están normalizados y los laboratorios comerciales utilizan métodos diferentes, lo que dificulta la utilización de los resultados. Siguiendo el consenso internacional, se ha acordado utilizar el método propuesto por la International Federation of Clinical Chemistry (IFCC) para calibrar las distintas técnicas de determinación de HbA1c y se decide emitir los resultados en dos tipos de unidades de forma simultánea en todos los informes de laboratorio: 1) En porcentaje (%), basado en el trabajo del National Glycohemoglobin Stardardization Program (NGSP), y 2) en unidades IFCC (mmol/mol).
La inclusión de la glucosa media estimada junto a la glucemia y HbA1c no tiene una evidencia científica suficiente que permita su utilización, aunque este parámetro es útil en la práctica clínica para explicar al paciente qué cifras promedio de glucemia presenta en función de la HbA1c resultante.
Utilización de la HbA1c en el diagnóstico de la diabetes mellitus tipo 2 (DM2)3Recientemente un Comité de expertos de la Asociación Americana de Diabetes (ADA), recomienda la utilización de la HbA1c para el diagnóstico de la DM2, basándose en que es una medida fiable de la exposición de glucosa a lo largo del tiempo y su determinación analítica es más exacta que la determinación de la glucemia, siendo aún más fácil su utilización con la reciente introducción de métodos para normalizar la prueba.
«El diagnóstico de la diabetes se realiza si el nivel de HbA1c es ≥6,5%». Se ha de confirmar con una repetición de la prueba de HbA1c a menos que los niveles de glucosa sean ≥200mg/dl (≥11,1mmol/l) o estén presentes síntomas clínicos.
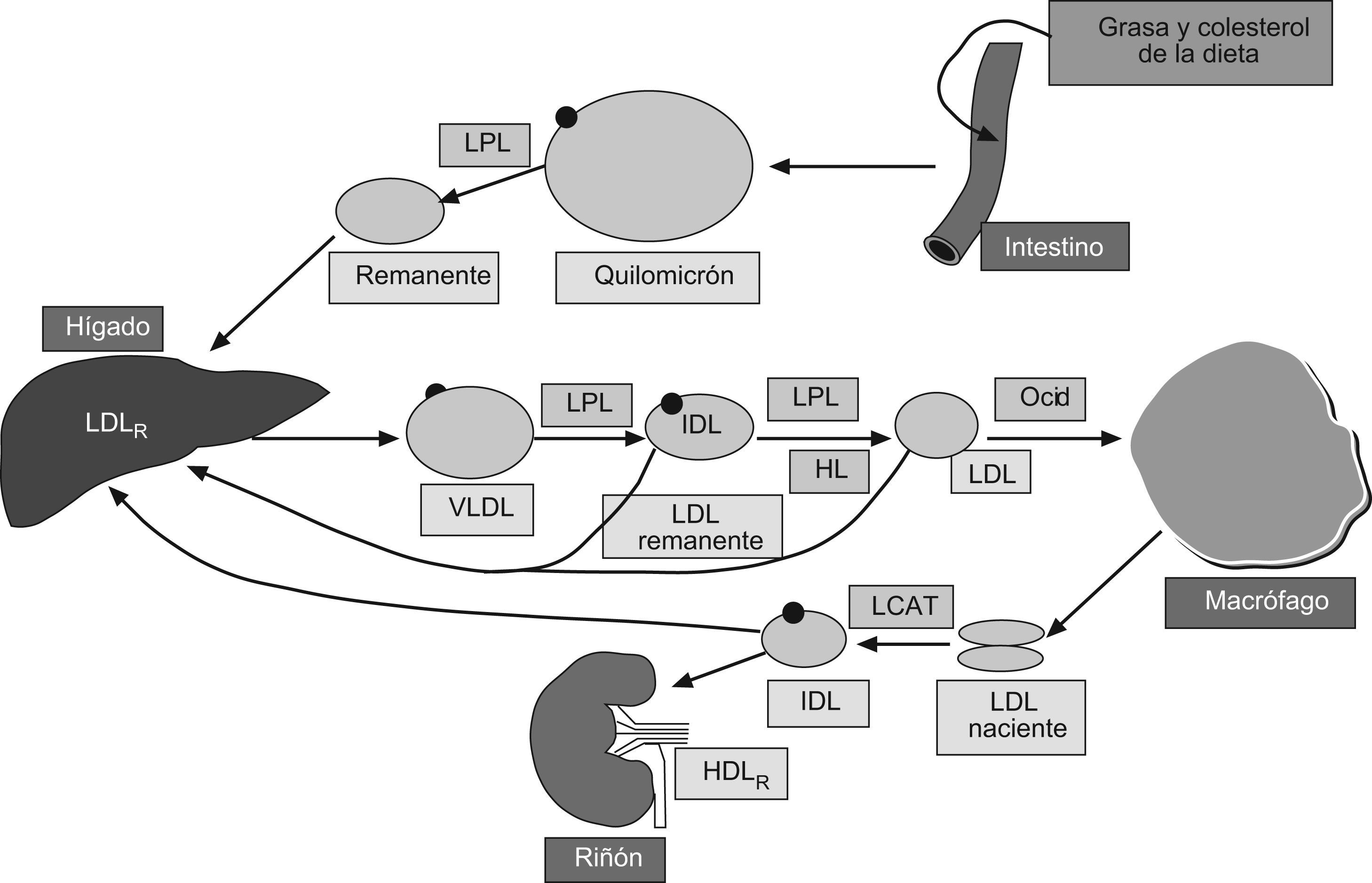
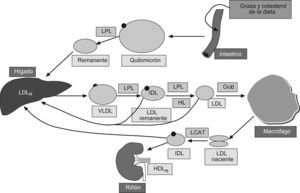
Valoración de la dislipemia diabética (fig. 14)La dislipemia diabética hace referencia a las alteraciones lipídicas características de los pacientes con diabetes tipo 2 y que están relacionadas con la insulinrresistencia. Está presente en el 60% de los pacientes, siendo uno de los principales factores de riesgo que contribuyen al aumento del riesgo cardiovascular total, por lo que requiere una evaluación precisa para establecer objetivos terapéuticos adecuados y seleccionar el tratamiento más apropiado. Se define por la presencia de5:
- •
Colesterol LDL (c-LDL) normal o ligeramente aumentado.
- •
La tríada aterogénica que incluye hipertrigliceridemia moderada, colesterol HDL (c-HDL) bajo y predominio de partículas LDL pequeñas y densas (fenotipo B de las LDL).
- •
Aumento del número de partículas aterogénicas (de densidad muy baja [VLDL], intermedia [IDL] y baja [LDL]), que se refleja en un aumento en las concentraciones de apolipoproteína B (apoB) y del colesterol no HDL.
Las condiciones para establecer el diagnóstico de dislipemia son las siguientes: comprobar la alteración en «al menos dos ocasiones, tras un ayuno de 12 a 14h», sin cambios de peso, siguiendo la dieta habitual durante las tres semanas previas, en ausencia de enfermedades intercurrentes y sin administración de fármacos que alteren el metabolismo lipídico. Las guías internacionales recomiendan la realización de un «perfil lipídico completo» en ayunas, que incluya «colesterol total (CT), triglicéridos (TG), c-HDL y c-LDL». En estos pacientes se han de descartar otras causas de dislipemia secundaria y dislipemias familiares, en especial cuando los niveles de c-LDL son >160mg/dl (4,43mmol/l). Si la concentración de TG excede los 150mg/dl (1,7mmol/l), puede existir una abundancia anormal de partículas LDL pequeñas y densas. En este contexto, la determinación de «apolipoproteína B» y el «cálculo del colesterol no HDL» permitirá obtener una estimación del número de partículas aterogénicas circulantes.
Colesterol totalExisten multitud de estudios epidemiológicos que muestran una fuerte correlación entre el colesterol sérico y la enfermedad cardiovascular, pero el CT ha sido sustituido por el c-LDL en cuanto a objetivo terapéutico, ya que este es mejor predictor de enfermedad cardiovascular.
Colesterol LDLLas partículas lipoproteícas de baja densidad (LDL) contienen aproximadamente el 70% de todo el colesterol circulante, y su función es transportar el colesterol procedente del hígado a los tejidos periféricos. El poder aterogénico del c-LDL y su utilidad como objetivo terapéutico se basan en estudios experimentales, epidemiológicos y de intervención. El c-LDL es el mejor predictor de enfermedad coronaria en pacientes con diabetes6. Además existen medidas eficaces que reducen el c-LDL en más de un 50%, y la reducción de episodios coronarios que se obtiene en los estudios de intervención es proporcional a la reducción de colesterol, independientemente del fármaco o medida no farmacológica utilizada. El método más ampliamente utilizado para la estimación del c-LDL es el cálculo mediante la fórmula de Friedewald:
Este método es económico, puesto que se compone de parámetros que ya se determinan de forma habitual, pero tiene limitaciones y es muy inexacto cuando los TG sobrepasan los 300mg/dl (3,36mmol/l).
«El c-LDL es el principal objetivo diagnóstico y terapéutico» en el manejo de la dislipemia, recomendándose como objetivo a conseguir cifras «<100mg/dl (2,6mmol/l) y <70mg/dl (1,8mmol/l)»7,8 si existe un riesgo muy elevado de sufrir un evento cardiovascular, por lo que debe estar siempre incluido en la evaluación del paciente con diabetes, a pesar de sus limitaciones metodológicas; estas podrían ser reducidas si se utilizaran otros parámetros complementarios en la valoración del riesgo en el paciente con dislipemia (concentraciones de apoB y colesterol no-HDL).
Colesterol HDLLas partículas de alta densidad (HDL) son las protagonistas del transporte reverso de colesterol, pero además tienen propiedades antioxidantes y antiinflamatorias sobre la pared vascular. Numerosos estudios epidemiológicos han establecido que la concentración del c-HDL es un factor predisponente, independiente de la incidencia de enfermedad coronaria, tanto en pacientes diabéticos como no diabéticos. Se estima que por cada mg/dl (0,03mmol/l) que aumenta la concentración de c-HDL, se reduce el riesgo de enfermedad coronaria en un 2–3%. Su determinación se realiza por métodos directos basados en la distinta solubilidad de las diferentes lipoproteínas.
Los objetivos terapéuticos establecidos para el c-HDL son >50mg/dl (1,3mmol/l) para la mujer y >40mg/dl (1,0mmol/l) para el varón6,7. Dada la escasa eficacia de los tratamientos disponibles en la actualidad para modificar y mantener sus concentraciones, su utilidad en clínica es limitada.
TriglicéridosEl reconocimiento del papel independiente de los TG como predictor del riesgo cardiovascular es relativamente reciente y controvertido. Un metaanálisis estima que, por cada 1mmol/l (88,7mg/dl) que aumenta la concentración plasmática de TG existe un incremento del riesgo cardiovascular del 14% en hombres y del 37% en mujeres9. Para la cuantificación de los TG se utilizan métodos enzimáticos que tienen una inexactitud en torno al 5%, por lo que la principal limitación es la elevada variabilidad biológica que puede llegar a ser hasta el 30% en un mismo individuo, por lo que su utilidad es muy limitada.
El objetivo para los TG es <150mg/dl (1,7mmol/l)7,8
Otros componentes de la dislipemia diabética5Aunque el c-LDL es el principal objetivo terapéutico en el manejo de las dislipemias, su medición conlleva dificultades metodológicas y sus concentraciones no representan a todas las partículas aterogénicas, que también incluyen a las IDL y las VLDL. Para paliar esta situación, se han propuesto alternativas al c-LDL, como son sobre todo la apolipoproteína B (apoB) y el colesterol no HDL (c-noHDL).
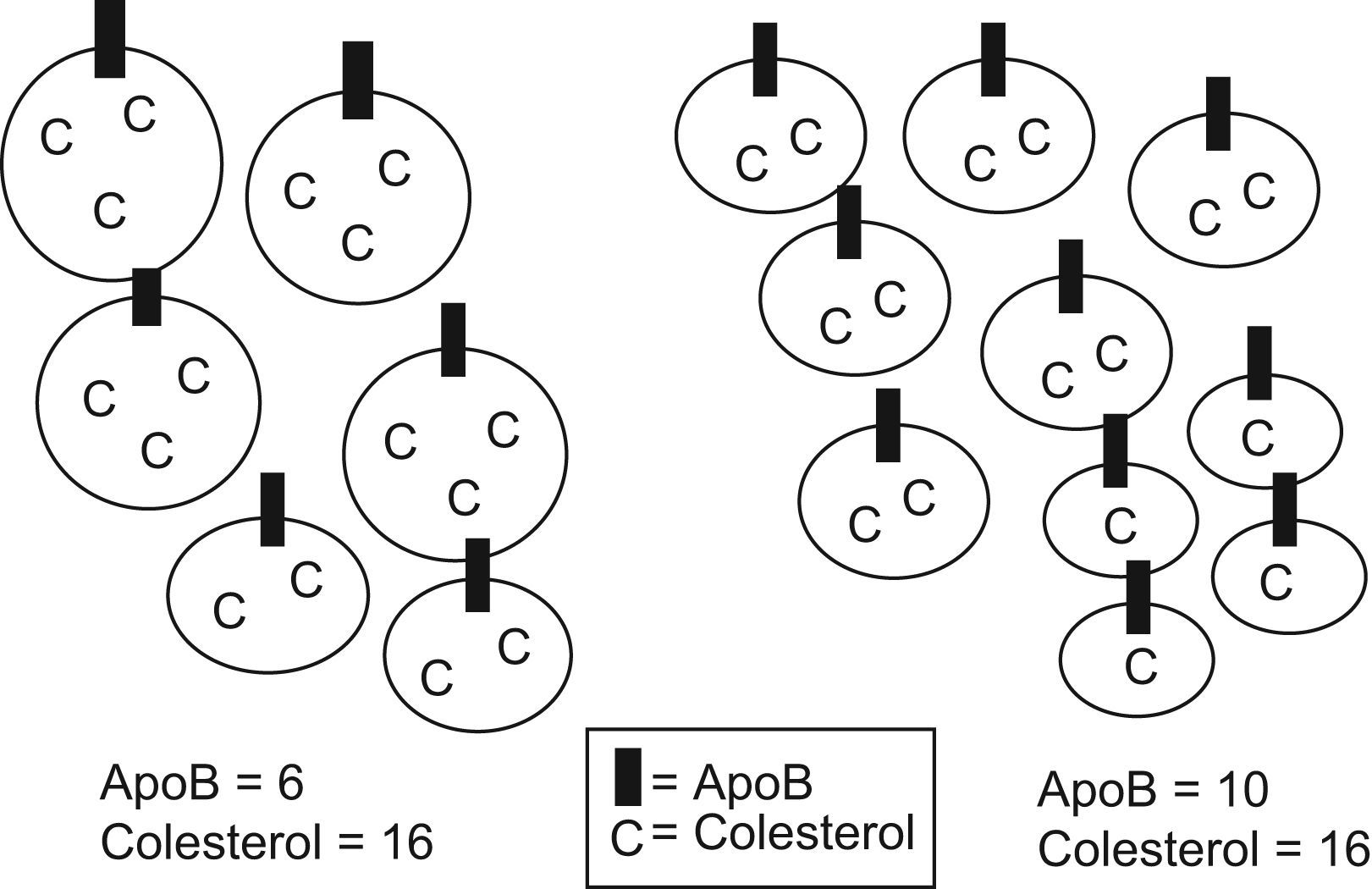
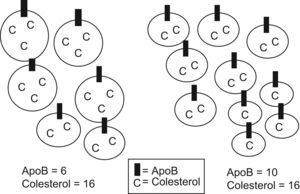
Apolipoproteína B: (fig. 2). La apoB forma parte estructural de las partículas aterogénicas (VLDL, IDL, LDL) a razón de una molécula por partícula, por lo que la concentración de apoB refleja el número total de dichas partículas. Como el 90% de la apoB se haya ligado a las partículas de LDL, para una concentración determinada de c-LDL, unos niveles de apoB elevados sugieren la presencia de partículas relativamente pobres en colesterol, con una menor razón lípido/proteína, es decir partículas pequeñas y densas, situación característica en la diabetes. Existen estudios que sugieren que la apoB es mejor factor pronóstico de episodios vasculares que el c-LDL y una proporción importante de los pacientes, alcanzan los objetivos terapéuticos de c-LDL, pero no de apoB. Ello indica que la apoB permite valorar de forma más precisa el riesgo residual en los pacientes tratados. La cuantificación de apoB es un método caro y tiene como limitación que se han de establecer valores de referencia para cada población, no existiendo objetivos terapéuticos internacionalmente establecidos.
Colesterol no HDL: el c-noHDL se calcula restando el c-HDL del colesterol total y refleja el colesterol transportado por las partículas aterogénicas. Es mejor factor pronóstico de episodios cardiovasculares que el c-LDL, tanto en pacientes diabéticos como no diabéticos, aunque similar o inferior a la apoB. Su estimación es fácil y barata, sin determinaciones adicionales a las que se hacen de forma habitual, lo que ha contribuido a su inclusión en algunas guías diagnósticas/terapéuticas en la evaluación de los pacientes con hipertrigliceridemia7.
Se recomienda determinación anual del perfil lipídico en pacientes que no presentan alteraciones lipídicas y cada 6 meses si hay dislipemia o el paciente recibe tratamiento para la misma10.
Cribaje de nefropatía diabéticaLa nefropatía diabética está presente en 10–20% de los pacientes diabéticos. Es la primera causa de insuficiencia renal terminal11, habiendo aumentado la prevalencia al mejorar el abordaje de las complicaciones cardiovasculares clásicas, lo que a su vez aumenta la supervivencia de los pacientes diabéticos, dando lugar a la aparición de complicaciones más tardías, como la nefropatía.
Fijarnos solamente en la excreción urinaria de albúmina, no es suficiente para el diagnóstico de nefropatía diabética, ya que un 40% de los pacientes pueden estar en distintos estadios de enfermedad renal crónica (ERC) con ausencia de excreción de albúmina en orina, por lo tanto debe medirse la creatinina para calcular el filtrado glomerular (FG) de estos pacientes.
La ERC representa un factor de riesgo vascular independiente y aditivo. Los enfermos diabéticos con nefropatía tienen, a medio plazo, un riesgo de enfermedad cardiovascular 20 veces mayor que los que no tienen afectación renal12.
La ADA recomienda13:
- •
Valorar «excreción urinaria de albúmina anual», desde el momento del diagnóstico.
- •
Medir niveles de «creatinina sérica al menos anualmente», independientemente del grado de excreción urinaria de albúmina, para posteriormente «estimar el FG» y valorar el «estadio de ERC» si está presente.
La creatinina deriva del metabolismo de la creatina y se ve afectada por diversos factores: la masa muscular (se eleva menos en mujeres o ancianos con poca masa muscular) o la ingesta de carne. Es por ello que, con frecuencia, descensos moderados del FG no se acompañan de elevaciones paralelas de la creatinina sérica. Se considera insuficiencia renal (IR) cifras de:
- •
1,5mg/dl (130μmol/l) en varones
- •
1,4mg/dl (121μmol/l) en mujeres
La determinación de creatinina sérica no debe ser utilizada como único parámetro para evaluar la función renal, ya que los valores no se elevan por encima del rango normal hasta que se ha producido un descenso de la mitad del FG, dificultando el diagnóstico precoz del deterioro de la función renal.
Aclaramiento de creatininaEl aclaramiento de creatinina, calculado en muestra de orina de 24h, puede permanecer elevado y sobreestimar la función renal, en casos de descenso de FG, por lo que se considera un método muy inexacto, siendo además dificultoso por la necesidad de recoger orina de 24h. Los estudios que han valorado los métodos para el estudio de la función renal, muestran que este método no es más exacto que utilizar fórmulas que permiten estimar el FG a partir de una muestra simple de orina.
Estimación del filtrado glomerular mediante ecuaciones14La estimación del FG mediante ecuaciones es el mejor índice disponible en la práctica clínica para evaluar la función renal. Estas ecuaciones utilizan fórmulas a partir del nivel de creatinina sérica y de alguna de las siguientes variables: edad, sexo, raza y masa corporal.
La más recomendada es la fórmula del estudio Modification of Diet in Renal Disease (MDRD). Como alternativa puede utilizarse la «fórmula de Cockcroft-Gault»:
- •
MDRD:
La fórmula MDRD incluye únicamente la edad del paciente y el valor de la creatinina sérica y se corrige en las mujeres multiplicando por 0,742 y en los afroamericanos multiplicando por 1,210.
- •
Cockcroft-Gault:
Esta fórmula incluye la edad y el peso del paciente y el valor de creatinina sérica, y precisa corregirse por la superficie corporal.
El FG es el parámetro que mejor resume la función renal, ya que refleja la masa renal funcionante, permite monitorizar la progresión de la función renal y facilita el ajuste de fármacos excretados por filtración glomerular. Se considera que en adultos jóvenes sanos el FG se encuentra entre 120 y 130ml/min/m2 y que disminuye con la edad. Un FG menor de 60ml/min/m2 representa la pérdida de aproximadamente la mitad de la función renal del adulto sano y por debajo de ese límite el riesgo de complicaciones cardiovasculares aumenta.
Las ecuaciones no son adecuadas en las siguientes circunstancias: peso corporal extremo (IMC<19kg/m2 o > a 35kg/m2), alteraciones en la masa muscular (amputaciones, pérdida de masa muscular, enfermedades musculares o parálisis), insuficiencia renal aguda, embarazo, hepatopatía grave, edema generalizado y ascitis. En estos casos se ha de estimar el FG por otros métodos: aclaramiento de creatinina convencional (orina de 24h) o métodos isotópicos.
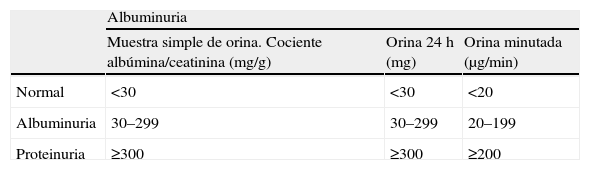
Valorar excreción urinaria de proteínas14 (tabla 2)Debe valorarse de forma preferente como «cociente albúmina/creatinina en muestra aislada de orina (normal<30mg/g)», preferiblemente primera orina de la mañana. Este cociente representa una buena estimación de la proteinuria y evita utilizar la recogida de orina de 24h. «La albuminuria siempre debe confirmarse en al menos dos de tres muestras en el plazo de 3 a 6 meses». Si es negativa repetir anualmente.
Definiciones de albuminuria según el tipo de muestra utilizada13
| Albuminuria | |||
| Muestra simple de orina. Cociente albúmina/ceatinina (mg/g) | Orina 24h (mg) | Orina minutada (μg/min) | |
| Normal | <30 | <30 | <20 |
| Albuminuria | 30–299 | 30–299 | 20–199 |
| Proteinuria | ≥300 | ≥300 | ≥200 |
Falsos positivos a excluir serían: ejercicio, infecciones urinarias, crisis hipertensivas, insuficiencia cardiaca, procesos febriles y ejercicios vigorosos.
La «ERC15 (tabla 3) se define» como una disminución de la función renal expresado por un «filtrado glomerular<60ml/min/1,73m2 o como la presencia de daño renal de forma persistente» durante al menos 3 meses. Por lo tanto incluye:
- •
Daño renal diagnosticado por método directo (alteraciones histológicas en biopsia renal) o de forma indirecta por marcadores como la albuminuria o proteinuria, alteraciones en el sedimento urinario o en pruebas de imagen.
- •
Alteración del FG (<60ml/min/1,73m2).
Estadios de enfermedad renal crónica (ERC) (K/DOQI 2002 de la National Kidney)14
| Estadío | FG (ml/min/1,73m2) | Descripción |
| 1 | ≥90 | Daño renal con FG normal |
| 2 | 60–89 | Daño renal, ligero descenso del FG |
| 3 | 30–59 | Descenso moderado del FG |
| 4 | 15–29 | Descenso grave del FG |
| 5 | <15 o diálisis | Prediálisis/diálisis |
El diagnóstico precoz de la ERC en estadios 1 y 2 resulta fundamental para la posible prevención de la pérdida de función renal y de las complicaciones cardiovasculares.
Los estadios 3–5 constituyen lo que se conoce habitualmente como insuficiencia renal. En estos estadios es importante la vigilancia de anemia y si la Hb <11d/dl, se ha de estimar remisión a hematología para valorar tratamiento con factores estimulantes de la eritropoyesis.
La «derivación a nefrología» para valoración del paciente diabético, se realizará si:
- •
Albuminuria: cociente albúmina/creatinina (confirmada) >300mg/g, a pesar de un adecuado tratamiento y control de la presión arterial.
- •
Aumento de la albuminuria a pesar de un tratamiento adecuado.
- •
HTA refractaria (tres fármacos en dosis plenas y ausencia de control).
La alteración tiroidea es frecuente en pacientes diabéticos y puede producir importantes alteraciones metabólicas. «La determinación de TSH se ha de realizar en el momento del diagnóstico, y repetir al menos cada 5 años», sobre todo en pacientes con obesidad, dislipemia o mujeres mayores de 50 años.
Se consideran valores normales entre 0,4 y 4,0μU/ml.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.