Notificamos un caso de microangiopatía trombótica, caracterizado por un proceso de agregación plaquetaria amenazante para la vida, que presentó afectación multisistémica y rápida evolución en una paciente con infección por el VIH. En este caso exponemos ampliamente los síntomas, la evolución y, finalmente, la necropsia clínica. Esta enfermedad es ahora infrecuente tras la llegada de los antirretrovirales de gran actividad, no obstante, se presenta con síntomas inespecíficos y evoluciona rápidamente a la afectación multisistémica y muerte. En consecuencia, un diagnóstico precoz con base en criterios clínicos y analíticos es fundamental para instaurar el tratamiento adecuado y mejorar la supervivencia.
We report on a case of thrombotic microangiopathy, defined as an extensive and dangerous intravascular platelet aggregation disorder, which progressed to multisystem involvement in a patient with HIV infection. For this clinical case, we detail the symptoms, evolution and, ultimately, the clinical autopsy. This disease is now uncommon due to the arrival of high-activity antiretroviral drugs; however, it can appear with nonspecific symptoms and rapidly progress to multisystem involvement and death. An accurate diagnosis on the basis of clinical and analytical criteria is essential to starting treatment and improving survival.
La púrpura trombótica trombocitopénica-síndrome hemolítico urémico (PTT-SHU) se define por la tríada: anemia hemolítica microangiopática, trombocitopenia e insuficiencia renal aguda; en formas graves existe afectación cardíaca y neurológica. Su incidencia se estima en torno a 1-10 casos por millón de habitantes, observándose un predominio en el sexo femenino y entre la tercera y la cuarta década de la vida. Su fisiopatología radica en la presencia de microangiopatía trombótica (MAT) extensa, que afecta preferentemente a los vasos renales, observándose engrosamiento de las paredes, microtrombos hialinos plaquetares y obstrucción de la luz vascular. Actualmente se diferencian 3 entidades que pueden producir MAT: la PTT, producida por déficit de actividad de ADAMST-13<5% (una enzima plasmática responsable de la escisión de los multímeros de factor Von Willebrand), el SHU típico, secundario a una infección por Escherichia coli productora de toxina Shiga, que causa lesiones endoteliales que conducen al desarrollo directo de MAT, y el SHU atípico, relacionado con mutaciones o polimorfismos de proteínas reguladoras de la activación del complemento por la vía alternativa. A su vez, existen múltiples causas que conducen al desarrollo de MAT secundaria, como el síndrome HELLP, las enfermedades autoinmunes sistémicas, las neoplasias, la hipertensión arterial maligna, o las secundarias a fármacos o a la infección por el VIH, generalmente en estadios avanzados de la enfermedad. Debemos incluir la coagulación intravascular diseminada dentro del diagnóstico diferencial, prestando especial atención a alteraciones en la coagulación como claves para diferenciarla del PTT-SHU. Presentamos el caso de una paciente con síndrome de inmunodeficiencia adquirida (sida), que tras consultar inicialmente por síntomas inespecíficos presentó paulatinamente la constelación de síntomas de forma rápida y fulminante.
Descripción del casoSe trata de una mujer de 35 años de edad, fumadora activa y con hábito enólico, con antecedentes de infección por VIH estadio C3 por tuberculosis pulmonar y ganglionar, en tratamiento antirretroviral desde 1996 (último esquema terapéutico emtricitabina/tenofovir+darunavir/ritonavir), con unos CD4+ de 545/mm3 y una carga viral de 30 copias/ml. Es exconsumidora de cocaína y cannabis, no usuaria de drogas por vía parenteral. Sin coinfección con los virus de las hepatitis C y B.
Acudió a Urgencias por dolor abdominal difuso acompañado de náuseas y vómitos, junto con deposiciones diarreicas de un día de evolución, sin productos patológicos ni fiebre. A su llegada estaba afebril y hemodinámicamente estable, pálida e ictérica. En la exploración abdominal destacó la presencia de hepatoesplenomegalia, sin puntos dolorosos o peritonismo. La analítica urgente mostró anemia microcítica (hemoglobina 9,2g/dL, VCM 66), trombocitopenia de 20.000 plaquetas, coagulación normal, creatinina 3,3mg/dL, urea 134mg/dL, bilirrubina total 3,47mg/dL, con GOT 102U/L y GPT 50U/L. La amilasemia y la proteína C reactiva eran normales; pH 7,36, HCO3 19mmol/L, lactato 2,5mmol/L. El diagnóstico inicial fue gastroenteritis e insuficiencia renal aguda prerrenal, descartándose coagulación intravascular diseminada.
Durante las primeras 48h la paciente mejoró con fluidoterapia y antieméticos, sin embargo, se evidenció una mayor anemización y trombocitopenia, detectándose una hemólisis (LDH 3.472U/L, haptoglobina 2mg/dL) no inmune (test de Coombs negativo), aumento de reticulocitos (103.000cél/mm3), un empeoramiento de su insuficiencia renal (creatinina 3,7mg/dL y urea 178mg/dL) y una elevación de enzimas pancreáticas (amilasa 148U/L, lipasa 350U/L). Los cultivos de orina y sangre fueron negativos. El examen de orina reveló hemoglobinuria con discreta hematuria y proteinuria de 1,7g/L. Se diagnosticó pancreatitis aguda y anemia hemolítica secundaria. La TAC mostró hepatoesplenomegalia, líquido perihepático y periesplénico, aumento global del tamaño del páncreas y difusión enzimática extensa. El diagnóstico evolutivo de pancreatitis aguda y anemia hemolítica secundaria estaba justificado.
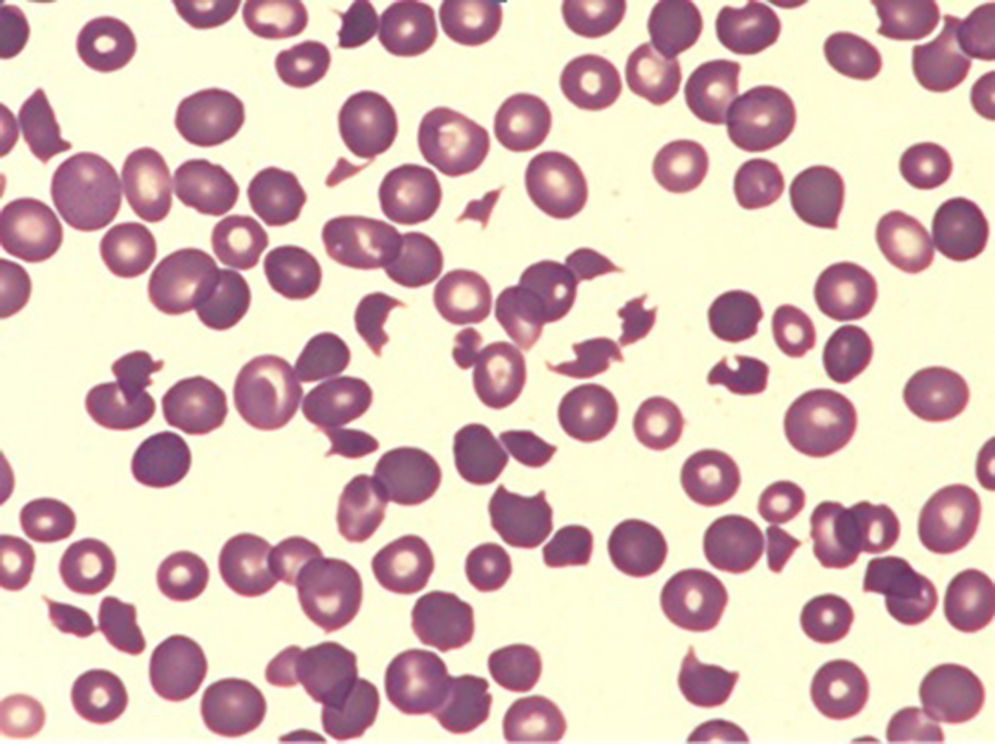
Se inició tratamiento con corticoides, solicitándose un frotis de sangre periférica. La mañana del tercer día la paciente empeoró clínicamente, con disminución del nivel de conciencia seguida de convulsión tónico-clónica generalizada, interpretada como de privación alcohólica, pero sin mejoría con bomba de diazepam, presentando rigidez de descerebración y taquicardia supraventricular. La TAC cerebral urgente no mostró alteraciones, y el ECG, elevación del segmento ST en cara inferior. Tras su intubación orotraqueal fue trasladada a la UCI, sin embargo, 3h después la paciente sufrió una parada cardiorrespiratoria que no se pudo revertir. Finalmente, se recibieron los resultados del frotis (fig. 1) y los niveles de troponina I (17ng/mL) y de procalcitonina (0,2ng/mL).
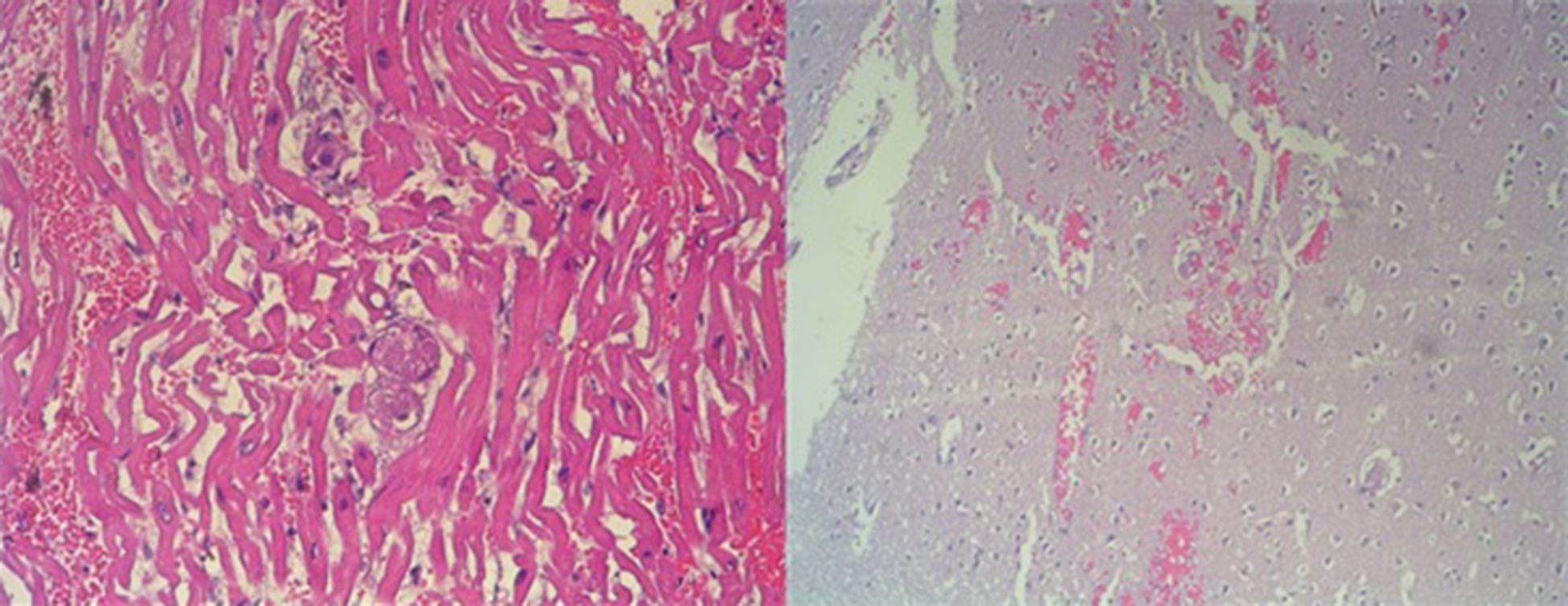
La necropsia fue definitiva para el diagnóstico (fig. 2). Los diagnósticos macroscópicos incluyeron: necrosis hemorrágica de 7×6cm en el tabique interventricular, endocarditis hemorrágica de ventrículo derecho y pericarditis hemorrágica en pericardio visceral; esteatosis hepática con hepatomegalia; esplenomegalia; enfisema bulloso apical bilateral; hemorragias superficiales pancreáticas; gastritis petequial hemorrágica.
Izquierda: detalle del miocardio donde se visualizan numerosos hematíes en el espacio extravascular y trombos hialinos en la microvascularización miocárdica (coagulación intravascular). Derecha: tejido cerebral con importante edematización, hemorragias multifocales intersticiales y trombos hialinos en la microvascularización.
A nivel microscópico los diagnósticos anatomopatológicos fueron: hemorragia miocárdica y pericárdica con coagulación intravascular de vasos capilares con trombos hialinos y necrosis miocitaria focal; microhemorragias acompañadas de trombos hialinos en los riñones, la corteza cerebral y las glándulas suprarrenales; hiperesplenismo con expansión de pulpa roja; depleción linfoide parcial de pulpa blanca; pulmones de estasis crónico; enfisema bulloso apical con fibrosis y neumonitis descamativa; hígado de estasis crónico con esteatosis leve.
DiscusiónLas MAT son entidades clínicas con unos criterios diagnósticos claramente definidos y que sobre el papel son fácilmente reconocibles; no obstante, en la práctica clínica, debido a su baja incidencia en la población global y a unas manifestaciones clínicas poco específicas, su diagnóstico pasa desapercibido o incluso se desconoce dada la ausencia de experiencia de los clínicos que se enfrentan a ella, situación que es más evidente si no se presentan de modo epidémico.
El diagnóstico inicial sospechado se alejó mucho de la severidad del cuadro clínico; el hecho de presentarse con vómitos y diarrea no enteroinvasiva de corta evolución sin afectación del estado general ni criterios de sepsis probablemente banalizó el cuadro clínico, atribuyendo la insuficiencia renal aguda a la hipovolemia secundaria a una gastroenteritis. Sin embargo, no explicaba la anemización de nueva aparición ni la severa trombocitopenia adquirida. Se descartó la coagulación intravascular diseminada al no existir datos de consumo de factores de la coagulación ni alteraciones en el TP. Este paso en el proceso de diagnóstico diferencial es vital, pues excluye una entidad difícil de descartar que constituye una amenaza vital para el paciente.
El deterioro clínico de la paciente condujo a un esfuerzo diagnóstico adicional. Se diagnosticó de anemia hemolítica no inmune, que se consideró secundaria a una inflamación pancreática evidenciada tanto en los análisis clínicos como en las pruebas de imagen. A pesar del tratamiento con fluidoterapia inicial, el agravamiento de la función renal nos hizo valorar una causa parenquimatosa. La posibilidad de PTT-SHU se consideró, solicitándose un frotis de sangre periférica e iniciándose corticoterapia a falta de un diagnóstico confirmatorio para iniciar terapia de recambio plasmático.
No obstante, en las últimas horas se precipitó el fracaso multiorgánico de la paciente, iniciándose tratamiento intensivo tras presentar complicaciones cerebrales y cardiovasculares. La afectación isquémica multisistémica no se contempló hasta que tuvo lugar el infarto agudo de miocardio, tratándose el cuadro convulsivo como de privación alcohólica, sin sospechar que la causa era isquémica.
La asociación entre MAT e infección por VIH se describió por primera vez en 1984, y en ocasiones como manifestación de infección aguda por VIH1. Actualmente esta asociación ha disminuido desde la introducción de la terapia antirretroviral de gran actividad (TARGA). La presentación clínica de estos casos es similar a la observada en las formas atípicas de SUH. Muchos de estos pacientes presentan niveles bajos de CD4 y han desarrollado sida.
En un estudio de 92 pacientes con insuficiencia renal aguda rápidamente progresiva en la era pre-TARGA, se documentó el SHU como causa en 32 pacientes (35%). En estos enfermos, el recuento medio de linfocitos CD4 fue de 43/mm3, 7 pacientes requirieron hemodiálisis y 7 fallecieron (22%)2.
Por su parte, en otro estudio de pacientes ya en tratamiento con TARGA se describieron 17 casos de MAT. Se observó una media inferior de CD4, 197 vs. 439cél/mm3, y un mayor log10 de niveles de ARN viral, 4,6 vs. 3,3, en estos pacientes. Existió una asociación significativa con el virus de la hepatitis C y con infección por Mycobacterium avium complex. Aunque la incidencia de MAT en pacientes con TARGA fue baja (0,3%) en comparación con las descritas en la era pre-TARGA (1,5-7%), la mortalidad siguió siendo elevada, y la mayor parte de los pacientes con MAT había desarrollado sida3.
La mortalidad previa al tratamiento con recambio plasmático relacionada con las MAT era superior al 50%; actualmente, con su introducción, es del 10%, siendo también el tratamiento de elección en las MAT asociadas al VIH1,4. Aunque la utilización de los corticoides como terapia adyuvante está ampliamente extendida, no se recomienda en pacientes inmunodeprimidos5. Los niveles de LDH y de plaquetas se emplean para valorar la eficacia del tratamiento1. Sin embargo, la mortalidad en pacientes con infección por VIH sigue siendo elevada, entre el 67-100% según las series, sobre todo en pacientes con sida4. No obstante, un diagnóstico y un tratamiento precoces pueden mejorar el pronóstico1,5.
Retrospectivamente, este caso evidencia la importancia de un diagnóstico temprano de MAT. La presencia de trombocitopenia y hemólisis microangiopática no inmune con niveles elevados de LDH, indetectables de haptoglobina y la presencia de esquistocitos que confirman la hemólisis intravascular, junto con uno de los siguientes: síntomas neurológicos, afectación gastrointestinal y/o afectación renal6, debería ser suficiente para el diagnóstico y el inicio de un tratamiento con recambio plasmático.
Nuestra paciente presentó al inicio afectación hematológica, digestiva y renal, y en 48h desarrolló afectación del SNC y cardíaca, siendo exitus a las 72h del ingreso. La infección por VIH en nuestra paciente era de larga evolución, pero desde su diagnóstico recibió TARGA y había mantenido recuentos de CD4 superiores a 450cél/mm3. Sin embargo, existió un aumento de los niveles de ARN, que pasaron de ser indetectables a 1,67log10, lo que motivó un cambio de tratamiento los días previos. Durante su ingreso los niveles de CD4 fueron de 267cél/mm3. Este deterioro inmunológico, junto con la reactivación viral, la baja sospecha clínica, la demora del frotis de sangre periférica, la confusión que aportaron las pruebas de imagen y el retraso en identificar los criterios de gravedad de la paciente, así como no considerar un proceso sistémico isquémico que explicase la globalidad de los síntomas, precipitaron la afectación isquémica renal, del SNC y, finalmente, del miocardio, con el fatal desenlace de la paciente.
Como conclusión, ante todo paciente con infección por VIH, especialmente con sida, que presente trombocitopenia y anemia hemolítica microangiopática de nueva aparición o insuficiencia renal rápidamente progresiva de etiología no aclarada, debe descartarse en menos de 24h la presencia de una MAT subyacente, y en el caso de confirmarse, iniciar recambio plasmático, el cual ha cambiado el pronóstico de esta enfermedad.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.