La obesidad es una enfermedad muy prevalente en un gran número de países desarrollados y en vías de desarrollo, que además muestra una tendencia a la progresión. La franja de pacientes obesos susceptibles de ser tratados mediante técnicas endoscópicas puede ser muy amplia. El balón intragástrico de Allergan es el tratamiento con mayor aplicación en España y en Europa. Presenta un perfil de eficacia a corto plazo bueno, a largo plazo subóptimo y su perfil de seguridad es elevado, aunque pueden aparecer complicaciones graves, por lo que no debe trivializarse su indicación ni su implantación. Además, existen diferentes dispositivos endoscópicos que consiguen que los pacientes obesos pierdan peso mediante diferentes mecanismos de acción, pero están en fase de desarrollo tecnológico y de validación científica. Es pronto para recomendarlos, y solamente deberían ser evaluados en el contexto de ensayos clínicos.
Obesity is highly prevalent in many developed and developing countries and is on the increase. The range of obese patients suitable for endoscopic treatment may be very broad. The most widely applied treatment in Spain and elsewhere in Europe is the Allergan intragastric balloon. The effectiveness of this technique is good in the short-term but suboptimal in the long term and its safety profile is high. However, severe complications may occur and consequently the indication and implantation of this technique should not be trivialized. In addition, there are distinct endoscopic devices that help patients lose weight, through distinct mechanisms of action, but these devices are currently under technological development and awaiting scientific validation. It is too soon to recommend these techniques and they should only be evaluated in the context of clinical trials.
La obesidad es un factor de riesgo determinante para la salud que mediatiza su daño en el organismo humano a través de diferentes enfermedades como la hipertensión arterial, las enfermedades cardiovasculares, la diabetes mellitus, la hiperlipidemia, la esteatohepatitis no alcohólica, la apnea del sueño, la osteoartritis, la enfermedad por reflujo gastroesofágico o algunos tipos de cáncer1-3 Por otra parte, la obesidad afecta la esfera psicoafectiva tendiendo a reducir la autoestima, y puede constituir un hándicap y una traba en la relación social4,5.
La obesidad se cuantifica según el índice de masa corporal (IMC), que es el resultado de dividir el peso en kilogramos por la altura al cuadrado en metros. Así pues, se considera un peso normal aquel cuyo IMC se sitúa entre 20 y 25. Se considera sobrepeso un IMC situado entre 25 y 30. Se considera obesidad un IMC entre 30 y 40. Finalmente, se considera obesidad mórbida un IMC superior a 406. Conforme se incrementa el IMC se observa un aumento progresivo de las enfermedades asociadas antes comentadas. En España, el sobrepeso afecta al 39,2% de la población, la obesidad afecta al 14,9% y la obesidad mórbida al 0,63%7. En Estados Unidos, los datos emitidos por el Centers for Disease Control and Prevention indican que en el año 2008 la obesidad afectaba al 36,6% de los adultos y al 16,9% de los niños8.
Resulta particularmente preocupante, en términos de salud pública, el incremento de peso que está experimentando la población infantil en España; este segmento de la población ha visto como se ha duplicado el porcentaje de niños obesos entre 6 y 13 años9. Hasta tal punto es veraz el avance de la obesidad en la población infantil y juvenil, que en el estado norteamericano de California, entre los años 2005 al 2007, 590 adolescentes con edades comprendidas entre los 13 y los 20 años de edad fueron sometidos a tratamientos específicos de cirugía bariátrica (cirugía propia de la obesidad), como son la colocación quirúrgica de una banda gástrica ajustable por vía laparoscópica o la realización quirúrgica de una gastrosplastia más un bypass gastroyeyunal laparoscópico10. En su conjunto, se considera que la obesidad es una epidemia que afecta a muchos países desarrollados o en vías de desarrollo, con previsiones funestas para la salud pública, tal como indica en un artículo especial publicado en New England Journal of Medicine, en donde predice que por primera vez en la historia de Estados Unidos puede aparecer una reducción en la esperanza de vida durante el siglo xxi, como resultado del aumento de la obesidad en la población norteamericana11. Es muy probable que estas previsiones sean extrapolables a otros países desarrollados, como es el caso de España.
Los directrices de manejo terapéutico ante un paciente con obesidad se estructuran de la siguiente forma: cuando el paciente obeso tiene un IMC entre 30 y 40 y además no presenta comorbilidades asociadas a la obesidad, la primera opción terapéutica consiste en realizar una dieta hipocalórica junto con la incorporación de una actividad física acorde con el gasto energético. Cuando esta primera opción no resulta eficaz, pueden utilizarse fármacos como la sibutramina o el orlistat, aunque la eficacia de estos medicamentos es bastante baja y sus efectos secundarios y riesgos pueden ser importantes. Por lo general, los fármacos anorexígenos mantienen una relación eficacia-riesgo subóptima. En esta franja de obesidad no estarían indicados los tratamientos quirúrgicos. Por el contario, en este segmento es donde encuentran su mejor indicación los tratamientos endoscópicos. Tengamos en cuenta que el número de pacientes obesos con IMC entre 30 y 40 es mucho más amplio que el segmento poblacional de pacientes obesos mórbidos, pues por cada paciente obeso mórbido existen 24 pacientes obesos. En otras palabras, el potencial de tratamiento de la obesidad mediante tratamientos endoscópicos es muy amplio.
Cuando el paciente presenta un IMC superior a 40, es decir, presenta obesidad mórbida, o bien el IMC es superior a 35 y además presenta comorbilidades importantes, el tratamiento recomendado en primera instancia es el tratamiento quirúrgico12, mediante técnicas de cirugía bariátrica, entendiendo por cirugía bariátrica los procedimientos quirúrgicos que pretenden modificar anatómica, funcional y metabólicamente el tracto digestivo para reducir el exceso de peso corporal y tratar de minimizar las comorbilidades asociadas (fig. 1). Las principales técnicas de cirugía bariátrica son la gastroplastia asociada a bypass gastroyeyunal, la manga gástrica (sleeve gastrectomy), la derivación biliopancreática, el Switch duodenal y la banda gástrica13,14. Estas intervenciones presentan una morbilidad variable en función del tipo de intervención, de las características del paciente y de la experiencia quirúrgica. Las complicaciones más frecuentes son la fuga de la anastomosis, la obstrucción de intestino delgado, la estenosis y la úlcera de la anastomosis15. Otras complicaciones menos frecuentes son el síndrome de Dumping, déficits de vitaminas (tiamina, hierro, cobalamina y folato), diarrea o enfermedad metabólica ósea16. Su mortalidad promedio en las series publicadas se sitúa en el 0,88%17-19.
Sistemas endoscópicos para tratar la obesidadExisten diferentes enfoques fisiopatológicos para tratar de reducir peso en los pacientes obesos mediante sistemas o técnicas endoscópicas. Todos ellos actúan inicialmente provocando cambios o modificaciones orgánicas, que a su vez alteran la normal ingesta, digestión o absorción de los alimentos. Muchos de ellos modifican la distensión y el vaciamiento gástrico, y la liberación de hormonas, en especial la colecistoquinina. Todo ello afecta a la sensación de saciedad, reduce el deseo de apetito y acaba facilitando la pérdida de peso20-25.
Un primer grupo de sistemas endoscópicos para tratar la obesidad actúa produciendo una ocupación o restricción de espacio en el estómago. El más difundido de todos ellos es el balón intragástrico, fabricado por Allergan (Irvine, CA, EE.UU.), aunque fue la empresa Bioenterics el fabricante original y quien introdujo el balón por vez primera en el mercado. Bioenterics fue adquirida posteriormente por Allergan. Otros sistemas menos conocidos son el balón rellenable con aire (comercializado con el nombre Heliosphere), el balón intragástrico ajustable (de Spatz), la prótesis intragástrica ajustable (de EndogAst) y el balón antral estático.
Un segundo grupo de sistemas endoscópicos para tratar la obesidad actúa produciendo una malabsorción de los nutrientes a nivel yeyunal. El sistema que así actúa se denomina funda duodenoyeyunal (comercializado como Endobarrier).
Un tercer grupo de sistemas endoscópicos produce una reducción de la capacidad volumétrica gástrica mediante la colocación de puntos de sutura que intentan reproducir endoscópicamente intervenciones quirúrgicas bariátricas que son efectivas en el tratamiento de la obesidad. Entre ellos están la gastroplastia vertical endoluminal (de EndoCinch), la gastroplastia transoral (TOGA), el sistema restrictivo endoscópico transoral y la plataforma operativa endoscópica sin incisiones (denominada en España con el acrónimo POSE, como traducción del inglés primary obesity surgery endolumenal).Un cuarto sistema endoscópico actúa modificando la neuromodulación gástrica mediante la inyección gástrica de toxina botulínica o la implantación quirúrgica o endoscópica de dispositivos que producen modificaciones en la estimulación eléctrica gástrica, que se han popularizado como «marcapasos gástricos».
Finalmente, existe un conjunto de sistemas que intentan «rescatar» pacientes que han vuelto a engordar después de haber sido sometidos a una intervención quirúrgica bariátrica. Entre ellos figuran el StomaphyX®, el Over-the-scope-clip (de la empresa Ovesco) y el sistema POSE antes mencionado (tabla 1).
Sistemas de tratamiento endoscópico de la obesidad
| Sistemas para ocupar espacio en el estómago |
| Bioenterics Intragastric Balloon (BIB) (Allergan) |
| Balón rellenable con aire (Heliosphere BAG) |
| Balón intragástrico ajustable (Spatz) |
| Prótesis intragástrica ajustable (EndogAst) |
| Balón antral estático |
| Bypass intestinal |
| Funda duodenoyeyunal (Endobarrier) |
| Sistemas para reducir la capacidad gástrica |
| Gastroplastia vertical endoluminal (EndoCinch) |
| Transoral gastroplastia (TOGA) |
| Trans-oral endoscopic restrictive implant system |
| Incisionless operating platform (IOP) |
| Inyección gástrica de toxina botulínica |
| Estimulación eléctrica gástrica |
| Sistemas endoscópicos de rescate post cirugía bariátrica |
| Incisionless operating platform |
| StomaphyX |
| Over-the-scope-clip |
Es el sistema endoscópico más difundido en Europa, en Sudamérica y en diferentes países asiáticos. No está comercializado todavía en Norteamérica. Consiste en un balón de silicona resistente, pero a la vez dúctil y flexible, que mantiene su estanqueidad gracias a una válvula radioopaca y unidireccional que permite el relleno o inflado pero impide su vaciamiento. El balón se rellena con suero fisiológico, al que se suelen añadir 2cc de azul de metileno con el fin de desvelar un hipotético desinflado si el paciente observa la emisión de una orina de color verde turquesa. El balón se rellena con 450-650cc de suero fisiológico y permanece colocado por un periodo no superior a 6 meses, por ser el periodo de garantía del fabricante y porque transcurrido este periodo la eficacia del balón disminuye muy considerablemente. El volumen de llenado ha sido motivo de polémica, pues se ha creído que los resultados de eficacia y tolerancia pueden depender del volumen de llenado del balón. En la mayoría de los estudios se indica que el volumen de llenado no modifica los resultados de eficacia y seguridad26-28. Sin embargo, una serie corta de pacientes demostró que el rellenado del balón con un volumen de 500cc obtenía un porcentaje de exceso de peso perdido de 38±28,5%, mientras que el rellenado del balón con un volumen de 600cc obtenía un porcentaje de exceso de peso perdido de 48,8±31,0%29.
El mecanismo de acción del balón es inicial y fundamentalmente mecánico: provoca una ocupación de espacio que se traduce en una sensación de saciedad precoz tras la ingesta, lo que conlleva una menor ingesta calórica y su consiguiente pérdida de peso. Durante las primeras 48-72h tras la colocación del balón el paciente presenta náuseas, vómitos, sensación de plenitud y dolor epigástrico tipo espasmódico que responden deficientemente a la medicación convencional, pero que ceden por lo general. La colocación y la extracción se realizan mediante sedación con o sin intubación orotraqueal. Para la extracción debe utilizarse una aguja de punción y un fórceps tipo «gancho» ad hoc. Se desaconseja no utilizar otro material que no sea el específico y que suministra la empresa comercializadora.
Tal como se ha comentado anteriormente, el balón intragástrico se halla particularmente indicado en los pacientes obesos que presentan un IMC entre 30 y 40 sin comorbilidades asociadas a la obesidad. Sin embargo, puede aceptarse su indicación en otros supuestos, tales como un paso previo a la cirugía bariátrica en pacientes afectos de «super obesidad» mórbida con elevado riesgo quirúrgico30-37, en pacientes con un IMC>40 y con contraindicaciones para la cirugía bariátrica, en pacientes con un IMC>40 que rechazan la cirugía bariátrica y en pacientes con un IMC<30 en circunstancias especiales tras un análisis individual de cada caso12,38,39.
Por otro lado, existen contraindicaciones a la colocación de un balón intragástrico. Estas deben conocerse y deben aplicarse sin hacer un uso trivial de un producto que se presta a ceder antes tentaciones comerciales. La eficacia del procedimiento pivota sobre una correcta selección del paciente, aplicando de forma rigurosa los criterios de indicación y de contraindicación. El balón intragástrico podría estar contraindicado en pacientes con trastornos psicológicos graves (en casos de duda sobre el trastorno psicológico, debe solicitarse una valoración psicológica o psiquiátrica), en pacientes afectos de drogodependencias, en pacientes que presenten una insuficiente comprensión del proyecto, en pacientes afectos de enfermedades crónicas y graves (hepática, renal, cardiaca o pulmonar), en pacientes que han sido sometidos previamente a cirugía gástrica, incluida la cirugía de la enfermedad por reflujo gastroesofágico, en pacientes portadores de hernia de hiato de gran y mediano tamaño y en pacientes portadores de úlcera duodenal y gástrica activa26,40.
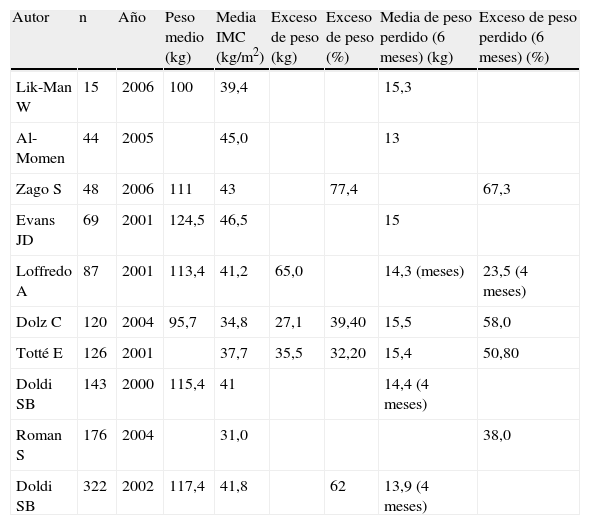
Son numerosas la referencias bibliográficas del balón intragástrico de Allergan, pero solamente hemos hallado 36 citas en forma de ensayos clínicos y únicamente 4 ensayos clínicos prospectivos, aleatorizados, a doble ciego y controlados con dieta hipocalórica41-44. La mayoría de los estudios publicados incluyen poblaciones de pacientes obesos bastante heterogéneas, muchos son estudios retrospectivos, la metodología técnica y las opciones de seguimiento son diversas o bien utilizan diferentes parámetros evaluadores de la eficacia. Por todo ello, resulta difícil globalizar los resultados, tal como se muestra en la tabla 2. No obstante, un metaanálisis publicado en el año 2008 recopila 3.608 pacientes de 15 estudios en los que aprecia una pérdida de peso de 14,7kg en un periodo de 6 meses, lo que se traduce en un porcentaje de exceso de peso perdido del 32,1%. Con respecto a la tolerancia, la tasa de retirada precoz del balón por diferentes motivos fue del 4,2%45. Aunque el perfil de seguridad es bastante bueno, se han descrito diferentes complicaciones, tales como perforación gástrica en pacientes portadores de funduplicatura, dilatación gástrica en paciente afectos de diabetes mellitus insulinodependiente, perforación gástrica encubierta con formación de plastrón, oclusión intestinal por desinflado del balón, perforación esofágica, fibrilación auricular grave, fracaso renal agudo y también casos de fallecimiento40,46-55.
Resultados de los datos basales y pérdida de peso con el balón intragástrico de Allergan. Estudios prospectivos
| Autor | n | Año | Peso medio (kg) | Media IMC (kg/m2) | Exceso de peso (kg) | Exceso de peso (%) | Media de peso perdido (6 meses) (kg) | Exceso de peso perdido (6 meses) (%) |
| Lik-Man W | 15 | 2006 | 100 | 39,4 | 15,3 | |||
| Al-Momen | 44 | 2005 | 45,0 | 13 | ||||
| Zago S | 48 | 2006 | 111 | 43 | 77,4 | 67,3 | ||
| Evans JD | 69 | 2001 | 124,5 | 46,5 | 15 | |||
| Loffredo A | 87 | 2001 | 113,4 | 41,2 | 65,0 | 14,3 (meses) | 23,5 (4 meses) | |
| Dolz C | 120 | 2004 | 95,7 | 34,8 | 27,1 | 39,40 | 15,5 | 58,0 |
| Totté E | 126 | 2001 | 37,7 | 35,5 | 32,20 | 15,4 | 50,80 | |
| Doldi SB | 143 | 2000 | 115,4 | 41 | 14,4 (4 meses) | |||
| Roman S | 176 | 2004 | 31,0 | 38,0 | ||||
| Doldi SB | 322 | 2002 | 117,4 | 41,8 | 62 | 13,9 (4 meses) |
Los mejores resultados se consiguen cuando tras la colocación del balón intragástrico, y durante los 6 meses que permanece el implante, se instaura un programa estructurado y supervisado consistente en la reeducación alimentaria y en la modificación de los hábitos alimentarios del paciente obeso, con incorporación del ejercicio físico en la rutina diaria y en la adecuación del gasto energético diario con la ingesta calórica. Los pacientes que siguen un programa de este tipo y que posteriormente incorporan la farmacoterapia pueden conseguir mejores resultados a medio y a largo plazo56,44.
Sin embargo, tras una pérdida de peso satisfactoria durante el periodo en que el balón permanece implantado, ¿qué ocurre después de la extracción del balón intragástrico? La evolución seguida en una serie de 100 pacientes cuyo IMC inicial fue de 35,0±5,6kg/m2, que perdieron 12,6±8,3kg al cabo de 6 meses y fueron seguidos durante 2,5años, evidenció que el 38% mantenían el peso perdido, el 46% habían vuelto a ganar peso y el 14% habían pasado por cirugía bariátrica57.
Podríamos resumir diciendo que el balón intragástrico de Allergan es una sistema endoscópico para tratar la obesidad con una complejidad técnica media, que respeta por completo la anatomía gástrica sin producir modificaciones irreversibles, con una eficacia a corto plazo buena, con un efecto beneficioso sobre las enfermedades asociadas a la obesidad moderada, con una eficacia a largo plazo subóptima y con un perfil de seguridad bastante bueno.
Balón rellenable con aire (Heliosphere)La morfología y las características de este balón son muy parecidas al balón de Allergan, y su principal diferencia consiste en que presenta una doble capa, lo que hace incrementar ligeramente su grosor. Se rellena de aire, a diferencia del balón de Allergan. Los estudios publicados indican que la eficacia entre ambos puede ser parecida, pero se describen una mayor dificultad técnica en su extracción y unas tasas de desinflado espontáneo superiores58-61. Cuando se comparan frente a frente ambos balones en una serie que incluye 18 pacientes tratados con balón rellenado con aire frente a 16 pacientes tratados con balón de Allergan, se obtienen los siguientes resultados en cuanto a eficacia: pérdida de IMC de 4,6±3kg/m2 y porcentaje de exceso de peso perdido de 27±16% para el balón rellenado de aire, mientras que la pérdida de IMC fue de 5,5±3,3kg/m2 y el porcentaje de exceso de peso perdido de 30,2±17% para el balón de Allergan62. La extracción endoscópica fue señalada como más complicada en el balón rellenado con aire; así mismo, la tasas de desinflado y de extracción precoz, que se situaron en el 20%, fueron mayores en este último tipo de balón62.
Balón intragástrico ajustable (de Spatz)El balón intragástrico ajustable presenta un innovador diseño que lo hace atractivo, pues es capaz de reducir o aumentar su tamaño sin necesidad de extraer el balón del estómago. Esta posibilidad viene a dar solución a la necesidad de reducir el tamaño del balón cuando los síntomas de intolerancia son muy intensos, o bien incrementar su tamaño cuando el estómago va adaptándose a las dimensiones del balón y el efecto de ocupación de espacio decrece, algo que ocurre de forma sistemática después de los primeros 2 meses.
El primer estudio realizado en 18 pacientes con un IMC de 37,3kg/m2 demostró una pérdida de peso de 24,4kg al cabo de 52 semanas, y el porcentaje de exceso de peso perdido fue del 48,8% al cabo de 52 semanas. Como complicaciones se reportaron 7 casos de extracción precoz del balón, un caso de disfunción de la válvula, un caso de perforación gástrica asociada al consumo de AINE, otro caso de desinflado, un caso de tubo doblado y otro de laceración esofágica durante la extracción que precisó una reparación quirúrgica. Como puede comprobarse, la tasa de efectos adversos fue elevada63. Probablemente cabe atribuirla a las dimensiones, a la rigidez y a las conexiones del balón que se requieren para realizar el inflado o desinflado. Todo ello, acaba constituyendo un dispositivo en exceso aparatoso64.
Prótesis intragástrica ajustable (EndogAst)Este implante consiste en un balón intragástrico que se conecta mediante un tubo conector con el exterior de la pared abdominal, atravesando la pared gástrica y la propia pared abdominal, al más puro estilo de una gastrostomía endoscópica percutánea. Ello permite el inflado o desinflado a voluntad según las necesidades antes comentadas. El único estudio publicado que analizó la eficacia y la seguridad de este balón en una serie de 57 pacientes destacó por la elevada tasa de complicaciones infecciosas en el estoma de la pared abdominal65.
Balón antral estáticoConsiste en un balón con forma de pera con un extremo distal tubular que intenta mantener el balón situado en el antro de forma permanente. El único estudio publicado aporta información de una serie de 26 pacientes, indicando que la pérdida de peso observada fue de 6,5kg al cabo de 4 meses; las complicaciones fueron: desinflado en 4 pacientes y obstrucción intestinal, también por desinflado y migración, que requirió una intervención quirúrgica en un paciente66.
Funda duodenoyeyunal (Endobarrier)Este sistema consiste en una funda fabricada por GI Dynamics Inc. (Lexington, Massachusetts, EE.UU.) consistente en un polímero plástico impermeable, de unos 60cm de longitud, que se fija mediante anclajes metálicos en el píloro y desciende en forma de funda cilíndrica a lo largo del yeyuno. Impide el contacto de los nutrientes con la mucosa intestinal, y en consecuencia provoca malabsorción. Las características flexibles y suaves de la funda no son impedimento para que la secreción biliopancreática fluya fácilmente por el espacio que se establece entre la mucosa intestinal y la propia funda hasta alcanzar el contacto con los alimentos ingeridos una vez alcanzado el extremo distal de la funda. Su extracción se realiza mediante fórceps de cuerpos extraños; la extracción puede ser traumática, pues deben deshacerse los anclajes y retirarse a lo largo del estómago y del esófago67.
Este dispositivo ha experimentado algunas modificaciones en su diseño y estructura desde su primera implantación, que han permitido mejorar especialmente su seguridad68-70. Cuando se ha evaluado su eficacia y seguridad en un estudio multicéntrico y aleatorizado en una serie de 26 pacientes que iban a acceder a cirugía bariátrica, demostró que en 4 pacientes fracasó la colocación de la funda por motivos técnicos, la duración del procedimiento fue de 35min, el porcentaje de exceso de peso perdido al cabo de 3meses fue del 19,0% en el grupo tratado con la funda duodenoyeyunal versus el 6,9% para el grupo control, siendo la diferencia estadísticamente significativa (p<0,002). Llamó mucho la atención la mejoría del metabolismo glucídico observada en 7 de los 8 pacientes con diabetes mellitus tipo271. Este último dato ha sido recibido con un cauteloso entusiasmo por la comunidad médica endocrinológica.
Gastroplastia vertical endoluminal (EndoCinch)Con la gastroplastia vertical endoluminal iniciamos la exposición de una serie de sistemas terapéuticos endoscópicos orientados a reducir la capacidad del estómago para albergar alimentos, provocando una sensación de plenitud precoz. Todos los sistemas que vamos a describir permiten colocar puntos de sutura a través de un endoscopio convencional o de un endoscopio de doble canal. Unos lo hacen mediante el mismo endoscopio, otros se ayudan de sobretubos más o menos complejos. El punto de sutura a través de un endoscopio constituye uno de los retos actuales de la endoscopia terapéutica avanzada. El punto de sutura debería ser transmural, firme, seguro, estable y permanente. En buena parte, el desarrollo futuro de la cirugía endoscópica a través de orificios naturales (NOTES) depende de que seamos capaces de diseñar sistemas y aplicar puntos de sutura de calidad. Los sistemas que vamos a describir han sido aplicados en series cortas de pacientes. Todos ellos han sido publicados pero no todos han conseguido perpetuarse, pues algunos han dejado de aplicarse debido a su eficacia moderada, a su complejidad o a su bajo perfil de seguridad.
El sistema de gastroplastia vertical endoluminal (EndoCinch) encuentra su antecesor en un desarrollo tecnológico realizado por Swain et al.72, que posteriormente fue modificada por Bard Endoscopic Technologies (Billerica, Massachussets, EE.UU.). Este sistema fue diseñado para tratar endoscópicamente la enfermedad por reflujo gastroesofágico. La base de este tratamiento consistía en realizar 2 o 3 puntos de sutura formando pliegues en la mucosa gástrica justo por debajo de la línea Z, en la vertiente de la curvatura menor, tanto de forma horizontal como vertical; con ello se conseguía aumentar el grosor de las capas musculares y mejorar la presión del esfínter esofágico inferior73-76. Tras realizar diferentes mejoras técnicas, el sistema EndoCinch se ha aplicado en 2 series cortas de pacientes obesos, consiguiendo un porcentaje de exceso de peso perdido del 58% al cabo de 12meses77,78. Mediante este sistema se colocan los puntos de sutura de tal forma que simula la gastrectomía tipo manga (sleeve gastrectomy), intentando tubular el estómago, pero presenta el inconveniente de que los puntos de sutura no son transmurales, por lo que tienen tendencia a soltarse y a deshacer la restricción gástrica con el paso del tiempo.
Gastroplastia transoralLa gastroplastia transoral (TOGA) es un sistema igualmente restrictivo que también realiza puntos de sutura mediante un sobretubo transportador del endoscopio y de un voluminoso sistema de sutura automática tipo grapadora que coloca puntos de sutura formando una manga tubular estrecha a lo largo de la curvatura menor gástrica. La experiencia comunicada indica que el procedimiento es efectivo, con un porcentaje de exceso de peso perdido al cabo de 12 meses del 52,2%. La técnica precisa unas 2h para su realización en las que el paciente está sometido a intubación orotraqueal. Los puntos de sutura son transmurales, aparece un síndrome postintervención caracterizado por náuseas y vómitos de 7 días de duración hasta que el paciente presenta una buena tolerancia a los alimentos ingeridos. Las complicaciones descritas fueron leves79,80. Sin embargo, durante el seguimiento endoscópico se ha podido observar que algunas de las suturas colocadas se desprendían. De hecho, la pérdida de peso que se manifestaba progresiva durante los primeros 4 meses, se estabilizaba sin descender más de forma significativa81. La pérdida de los puntos de sutura constituye una seria contrariedad técnica, que podrá condicionar seriamente la continuidad de este desarrollo tecnológico. En términos quirúrgicos, un sistema de sutura que pierde los puntos de sutura y desmonta una construcción realizada es un sistema no aceptable.
Sistema de implante restrictivo transoralEl sistema consiste en un sugerente artilugio que se implanta subcardialmente configurando una «cazoleta» de pequeño tamaño en la que se alberga el alimento ingerido una vez ha sobrepasado el cardias. Las pequeñas dimensiones de este receptáculo y su estrecho orificio de salida, de 10mm, hacia la cavidad gástrica representan un obstáculo y una incomodidad que frenan la ingesta de los alimentos por parte del paciente obeso. Para fijar la «cazoleta» restrictiva se colocan unos anclajes que se fijan utilizando un sistema especial liberador de puntos de sutura. El único estudio publicado hasta la fecha en 13 pacientes indica que el porcentaje de exceso de peso perdido al cabo de 3 meses fue del 28%. Hubo que contabilizar un caso de perforación gástrica y 2 casos en los que produjo un neumoperitoneo, que se trató de forma conservadora no quirúrgica82. No se ha comunicado ningún artículo más sobre este interesante sistema.
Incisionless operating plataformLa incisionless operating plataform (POSE), plataforma fabricada por UGI Medical (San Clemente, Califormia, EE.UU.), consiste en un sobretubo transportador que permite el paso de un endoscopio de diámetro fino (pediátrico) y de instrumentos de trabajo endoscópico de forma simultánea a través de 3 canales de trabajo. Los instrumentos de trabajo pueden ser genéricos de endoscopia terapéutica, o bien instrumentos específicos de este sistema endoscópico. Estos últimos permiten fijar, traccionar y colocar puntos y anclajes de sutura. Se denominan gLix, gProx y gCath. La plataforma es potencialmente versátil como herramienta multiusos en endoscopia terapéutica, pero cuando se aplica al tratamiento endoscópico de la obesidad se denomina, en inglés, primary obesity surgery endoluminal. El acrónimo español del mismo es POSE, y como POSE se está popularizado en España. Los anclajes de este sistema absorben las fuerzas dinámicas de tracción y evitan a rotura de las suturas (según el fabricante), lo que permitiría una compresión continua durante el proceso postoperatorio.
La plataforma en su conjunto es realmente atractiva, pues permitiría realizar procedimientos NOTES a través de un único sobretubo transportador, con visión endoscópica permanente en retroversión, y además dispone de 3 canales de trabajo accesorios. Mientras que los instrumentos de trabajo son reciclables, la plataforma es de un solo uso. Cada una de las suturas y anclajes tiene su coste económico, que es elevado.
Esta plataforma ha sido utilizada en procedimiento NOTES híbridos tales como colecistectomía vía transvaginal o transgástrica, en apendicectomía por vía transgástrica, colecistectomía a través de puerto único transumbilical y en cirugía bariátrica83,84.
Aplicada al tratamiento de la obesidad, los puntos de sutura se colocan en el fundus y en el segmento distal del cuerpo gástrico intentando, de nuevo y al igual que la mayoría de los procedimientos descritos, tunelizar el estómago, imitando la gastrectomía en forma de «manga» (sleeve gastrectomy). No existen datos publicados acerca de la eficacia y la seguridad del sistema POSE en el tratamiento de pacientes obesos, a pesar de que su aplicación está muy publicitada. En España, el sistema POSE se viene realizando desde hace más de un año y medio. Información no publicada indica que el sistema es efectivo y consigue una pérdida de peso durante los primeros meses, pero que se estabiliza transcurridos los primeros 6 meses. Esperaremos la publicación de los diferentes estudios de eficacia y seguridad que deben estar realizándose.
Inyección gástrica de toxina botulínicaLa toxina botulínica es fabricada por el Laboratorio Allergan, Inc., con el nombre comercial de Botox®. La aplicación de toxina botulínica produce una parálisis sobre la zona inyectada mediante el bloqueo de la liberación de acetilcolina en las terminaciones neuromusculares colinérgicas. El efecto de la toxina botulínica es temporal; se pierde de forma paulatina pasados los primeros 3 a 6 meses, sin producir ninguna lesión permanente sobre las estructuras en las que actúa85.
Las dosis administrada en los pacientes afectos de obesidad pueden oscilar entre 100 y 500UI de toxina botulínica. El lugar de inyección más utilizado es el antro gástrico, aunque también se ha asociado la inyección en el antro con la inyección en el fundus gástrico86,87. El número de inyecciones realizadas oscila entre 8 y 24. Los resultados de efectividad, todos ellos en series cortas de pacientes, indican resultados discrepantes: en 4 estudios no se observó eficacia88-91, y en 3 estudios la pérdida de peso fue de entre 4,0 y 4,9 puntos de IMC86,87,92. Los datos de seguridad de todos ellos indican que no existen efectos secundarios, con independencia de la técnica utilizada, dosis o lugar de inyección en el estómago93,94.
Estimulación eléctrica gástricaLa estimulación eléctrica gástrica consiste en un generador de impulsos eléctricos conectado a unos electrodos que se implantan en la pared gástrica. El generador emite una corriente eléctrica predeterminada que se sincroniza con la actividad eléctrica gástrica normal. Aplicado adecuadamente, produce un retraso en el vaciamiento gástrico, induce la distensión gástrica y puede acelerar el tránsito intestinal95. También se ha comprobado que la estimulación gástrica reduce los niveles de una hormona relacionada con el apetito, la grelina, en el tejido gástrico, así como incrementa los niveles de la colecistoquinina, hormona relacionada con la sensación de saciedad96. Los estudios clínicos publicados han utilizado la vía laparoscópica o la vía laparotómica para colocar el generador de estímulos eléctricos, pero también se han colocado electrodos en la pared intestinal bajo control endoscópico97, de ahí que nos permitamos repasar esta opción terapéutica en esta revisión endoscópica. Un primer estudio valoró la eficacia de la estimulación eléctrica gástrica aplicada a 14 pacientes tras un seguimiento de 6 meses, y mostró que el peso se redujo de 107,7±21,1 a 102,4±20,5kg98. Un segundo estudio determinó que la estimulación eléctrica gástrica aplicada a 12 pacientes durante un periodo de 20 semanas consiguió una reducción de peso de 107,7±21,1 a 102,4±20,5kg99. El estudio más amplio y metodológicamente de mayor calidad es un estudio multicéntrico, prospectivo, aleatorizado placebo-control, doble ciego, que incluyó 190 pacientes obesos a quienes se colocó un estimulador electricogástrico tipo Trascend de Medtronic por vía laparoscópica. Los pacientes fueron seguidos durante 12 meses, al cabo de los cuales el grupo control (pacientes en los que se había colocado el estimulador pero se había dejado desactivado) presentaron un porcentaje de exceso de peso perdido de 11,7±16,9%, mientras que los del grupo con el estimulador activado presentaron un porcentaje de exceso de peso perdido de 11,8±17,6% (p=0,7)100. Los resultados de este estudio no dan soporte a este tipo de generador eléctrico gástrico para el tratamiento de la obesidad.
Tratamientos endoscópicos emergentes para el rescate de pacientes obesos sometidos a cirugía bariátricaLa cirugía bariátrica es el tratamiento más efectivo para reducir peso en pacientes obesos mórbidos101-106. Tras la intervención quirúrgica aparece un descenso del peso corporal muy marcado durante los primeros 12 meses, que puede oscilar entre 15 y 20 puntos de IMC. El peso suele estabilizarse, y en algunos casos los pacientes vuelven a engordar106. La mayoría de estos pacientes son portadores de una gastroplastia asociada a una bypass gastroyeyunal, dado que este tipo de intervención ha sido la que se ha venido realizando con mayor frecuencia. El reservorio gástrico construido quirúrgicamente tiene tendencia a irse adaptando o a incrementar sus dimensiones con el paso del tiempo, permitiendo albergar y tolerar mayores volúmenes de alimentos, lo que se traduce en un aumento de peso106. En estos casos, una segunda intervención quirúrgica conlleva una importante complejidad técnica y riesgo quirúrgico. ¿Qué puede hacerse en estos casos? En estas circunstancias, los tratamientos endoscópicos pueden ser eficaces.
La plataforma de trabajo antes comentada y denominada incisionless operating plataform (POSE) ha demostrado su eficacia107. En una serie de 116 pacientes que habían experimentado un incremento de peso después de una cirugía tipo gastroplastia asociada a un bypass intestinal se utilizó la técnica POSE aplicando plicaturas y reducción del tamaño del reservorio gástrico. Al cabo de 6meses, 96 pacientes analizados habían perdido un 32% del exceso de peso que habían recuperado después de la cirugía84. Un sistema parecido a este, denominado Stomaphyx, ha sido utilizado igualmente con buenos resultados. Stomphyx X suturing system, fabricado por Endogastric Solutions Inc. (Redmond, WA, EE.UU), consiste en un dispositivo adaptado al extremo distal del endoscopio que coloca varias suturas de polipropileno en el reservorio gástrico, con lo que consigue reducir su tamaño. En una serie de 39 pacientes la aplicación de esta técnica consiguió que al cabo de un año el porcentaje del exceso de peso perdido fuera del 19,5%, sin complicaciones significativas108. En otra serie de 64 pacientes el tratamiento mediante esta misma técnica consiguió, al cabo de 3 meses, que se perdieran 7,3kg, sin describir igualmente complicaciones significativas109. El sistema over-the-scope-clip (OTSC), fabricado por Ovesco (Tubingen, Alemania), consiste en un clip metálico que se coloca sobre el extremo distal del endoscopio y se libera mediante un dispositivo acoplado al cabezal del endoscopio. El sistema guarda muchas similitudes con las bandas elásticas que se utilizan para la ligadura de varices esofágicas. Son muchas las aplicaciones descritas al sistema OTSC: el tratamiento de fístulas, de perforaciones y de hemorragias del tracto gastrointestinal110. Recientemente ha sido utilizado en una serie de 94 pacientes que habían sido sometidos a cirugía bariátrica tipo bypass gástrico y que había ganado peso tras haber dilatado la gastroyeyunoanastomosis. Tras la colocación de 2 clips en la anastomosis, el IMC pasó de 32,8±1,9 a 27,4±3,8kg/m2 al cabo de año, todo ello sin presentar complicaciones111.
Los tratamientos endoscópicos de rescate en pacientes previamente sometidos a cirugía bariátrica, constituyen una opción atractiva, dado que una reintervención quirúrgica puede ser técnicamente muy compleja.
Conflicto de interesesEl autor declara no tener ningún conflicto de intereses.