La trombosis representa la formación de un trombo en el sistema circulatorio, en el interior de un vaso sanguíneo o del corazón. El trombo, del griego thrombos (grumo, coágulo) es un cuerpo sólido integrado por plaquetas y fibrina, que se forma a causa de una lesión endotelial, un retardo de la corriente sanguínea o una alteración de la composición química de la sangre.
En condiciones normales, la trombosis es un proceso ligado al mantenimiento de la salud orgánica, pero en presencia de factores que lo favorecen, este proceso, y sobre todo sus consecuencias en forma de complicaciones circulatorias, se convierten, como se ha subrayado, en una de las causas de mayor mortalidad en los países industrializados occidentales.
Para comprender mejor el proceso de trombosis hay que hacer referencia a la hemostasia.
HEMOSTASIA
La hemostasia es el proceso fisiológico que mantiene la integridad del árbol vascular evitando las hemorragias y restituyendo a la normalidad las lesiones del endotelio vascular. El proceso de hemostasia consta de 4 fases:
Vasoconstricción localizada del área afectada.
Formación de un agregado o trombo de plaquetas sobre la superficie vascular lesionada.
Formación de fibrina que refuerza el trombo plaquetario, produciéndose la verdadera coagulación de la sangre.
Eliminación de los depósitos de fibrina o fibrinólisis.
El endotelio vascular, es decir, la capa más interna que recubre las paredes interiores de los vasos sanguíneos, cuando se lesiona, por la causa que sea, inicia una reacción en cadena que tiene como resultado la formación de un trombo o coágulo sanguíneo. Esta reacción tiene como objetivo inicial evitar o prevenir una hemorragia y posteriormente, restituir la lesión endotelial.
Vasoconstricción
La vasoconstricción, que dura unos 30 segundos, tiene como objetivo enlentecer la circulación sanguínea y facilitar la formación del trombo o coágulo plaquetario.
La reacción plaquetaria se desarrolla a través de dos mecanismos: adhesión y agregación. En la fase de adhesión, las plaquetas se adhieren a la superficie del endotelio vascular lesionada, gracias a unas glucoproteínas, especialmente las GP IIb, IIIa, presentes en la membrana celular de las plaquetas, y a la presencia en el plasma de un factor de la coagulación, el factor von Willebrand (vWF).
Agregación plaquetaria
Para la fase de agregación plaquetaria, además de la presencia de estos factores y de calcio, entre otros elementos, es necesaria la presencia de la prostaglandina tromboxano A2 (TXA2). El TXA2, un potente vasoconstrictor e inductor de la agregación plaquetaria, es el producto formado por la acción de la enzima ciclooxigenasa (COX) sobre el ácido araquidónico, un fosfolípido presente en todas las membranas celulares, incluidas las plaquetas y las células del endotelio vascular. La plaqueta, al ser una célula sin núcleo, solamente es capaz de producir este compuesto como resultado de la acción de la enzima ciclooxigenasa. Sin embargo, las células endoteliales son capaces de metabolizar el ácido araquidónico para producir otra prostaglandina, la prostaciclina o PGI2. Las acciones de la prostaciclina son las opuestas a las del TXA2, es decir, tiene acción vasodilatadora y antiagregante plaquetaria. El equilibrio en este sistema es una de las claves del mantenimiento de una correcta función de la hemostasia.
Formación de fibrina
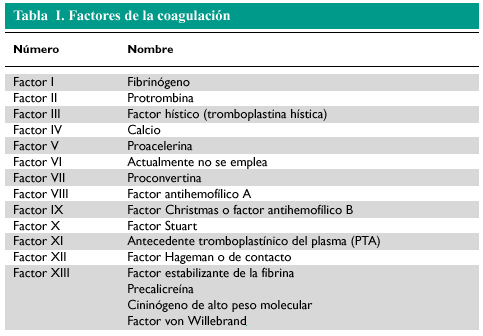
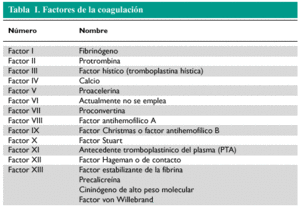
La formación de fibrina, para estabilizar y reforzar el trombo, tiene lugar gracias a la coagulación plasmática que consiste en la transformación del fibrinógeno en fibrina. Para ello, tiene que formarse una enzima proteolítica llamada trombina a partir de la activación de su precursor, la protrombina. Este proceso tiene lugar gracias a la reacción en cascada de activación de los llamados factores de la coagulación, que se identifican mediante números romanos, del I al XIII (tabla I). La activación de la protrombina a través de los factores de coagulación puede realizarse mediante dos vías o sistemas distintos: el intrínseco y el extrínseco, en el que participan distintos factores de la coagulación, aunque ambos tienen una vía final común. El resultado es la producción de trombina, que transforma el fibrinógeno en fibrina y da estabilidad al trombo.
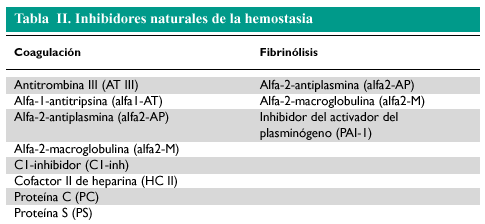
Por supuesto, existen compuestos inhibidores naturales de la coagulación (tabla II) para que no haya un desequilibrio en este sistema. Son los siguientes: antitrombina III (ATIII), alfa-2-macroglobulina (alfa2-M), alfa-1-antitripsina (alfa1-AT), C1-inhibidor (C1-inh), alfa-2-antiplasmina (alfa2-AP), cofactor II de heparina (HC II), proteína C (PC) y proteína S (PS).
Fibrinólisis
El proceso de fibrinólisis, es decir de destrucción de la fibrina que se ha formado durante la coagulación sanguínea, es necesario para la destrucción del coágulo, lo cual permitirá la mejora del flujo sanguíneo. Para ello, debe formarse una sustancia activa llamada plasmina a partir de un precursor inactivo que se encuentra en el plasma, el plasminógeno. Su activación se produce básicamente a través de la acción de un activador que se encuentra en las células endoteliales. Este compuesto se denomina activador hístico o tisular del plasminógeno (tPA).
También existen inhibidores de la fibrinólisis, como la alfa2-AP, la alfa 2-M, y el inhibidor del activador del plasminógeno o PAI-1.
ENFERMEDADES DE LA HEMOSTASIA
Las alteraciones de cualquiera de los componentes de la hemostasia producen el desequilibrio entre factores procoagulantes y anticoagulantes, dando lugar a trastornos por defecto de la coagulación (enfermedades hemorrágicas; tabla III) o por exceso de la coagulación (enfermedades trombóticas o trombosis). Antes de analizar estas últimas, conviene distinguir la trombosis en el territorio arterial y en el venoso.
Trombosis arterial
La trombosis en el territorio arterial tiene como principal responsable a las plaquetas. El trombo arterial o trombo blanco (rico en plaquetas) tiene un papel fundamental en el desarrollo de la placa de ateroma, característica que define a la aterosclerosis y a sus enfermedades derivadas, sobre todo a nivel cardíaco, cerebral y de la circulación periférica
Si el trombo crece en la pared del vaso arterial que lleva sangre a un órgano, se va reduciendo el flujo de sangre que pasa a través de éste y consecuentemente, disminuye el aporte de sangre que llega al órgano en cuestión, produciéndose de este modo una situación de isquemia. Si el trombo crece hasta obstruir totalmente el flujo de sangre o llega otro trombo por la circulación sanguínea arterial que obstruye totalmente el flujo sanguíneo, se produce una situación de infarto.
En el primer caso de la isquemia, si esto ocurre en la circulación coronaria, se hablará de angina; si ocurre a escala cerebral, se hablará de accidente isquémico transitorio (AIT), y si es en las extremidades inferiores, se hablará de claudicación intermitente o «síndrome del escaparate».
En el segundo caso, el del infarto, si ocurre en el ámbito coronario, se hablará de infarto agudo de miocardio; si ocurre en el cerebro, se hablará de ictus, accidente cerebrovascular, infarto cerebral o apoplejía (son términos que significan lo mismo) y si ocurre en otro territorio arterial se hablará, por ejemplo, de infarto renal, retiniano o mesentérico.
La embolia cerebral representa una complicación producida por un émbolo, un fragmento de un trombo que se ha desprendido de su localización y que circula por el territorio arterial hasta que el diámetro de una arteria cerebral es más pequeño que el del émbolo y se produce entonces una obstrucción brusca del aporte de sangre. Sus consecuencias son similares a las del ictus o infarto cerebrovascular y su causa suelen ser los émbolos desprendidos de trombos de válvulas cardíacas protésicas o producidos en la fibrilación auricular.
Trombosis venosa
En el territorio venoso el principal factor responsable de la trombosis es la estasis venosa o enlentecimiento y casi detención del flujo sanguíneo, con la subsiguiente lesión de las válvulas venosas, trombosis venosa y riesgo de embolismos. Si se produce la rotura de un trombo venoso o trombo rojo (rico en fibrina y hematíes), normalmente pegado a la pared del vaso, ese pedazo suelto o émbolo, circulará con la corriente sanguínea y aumentará el riesgo de que se produzca una embolia u obstrucción brusca del flujo sanguíneo por la impactación de este trombo circulante en los vasos sanguíneos de otro órgano.
Si el trombo crece en la pared de un vaso venoso, va reduciendo el flujo venoso y produce una situación de insuficiencia venosa. La localización más frecuente de este trastorno es en las venas de las extremidades inferiores. Si la obstrucción llega a ser completa, se hablará de trombosis venosa superficial o profunda; tromboflebitis si además hay afección del propio tejido vascular venoso. Si se desprende un émbolo que circula por la sangre hasta obstruir un vaso de menor tamaño que el del émbolo, se hablará de tromboembolismo. Si alcanza la circulación pulmonar, que es lo más frecuente, se hablará de tromboembolismo pulmonar (TEP). Este es el caso de las graves, aunque por suerte infrecuentes, complicaciones, entre otros del síndrome de la clase turista, desencadenado por largos períodos de inmovilidad, en general superior a 4 horas, en los vuelos transoceánicos.
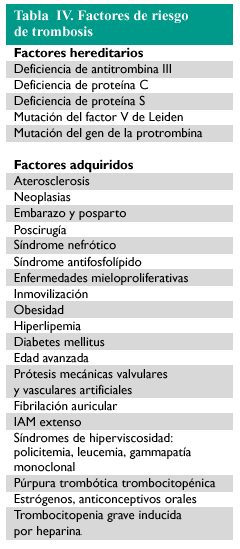
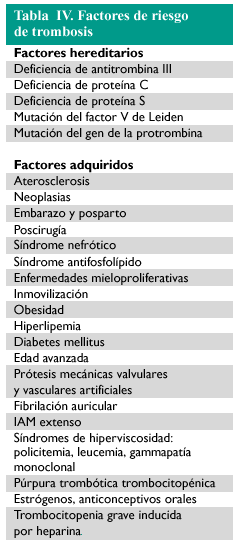
La tabla IV recoge los principales factores de riesgo para la aparición de trombosis.
TRATAMIENTO ANTITROMBÓTICO
La lesión en el órgano se produce por la falta brusca de aporte de sangre, como consecuencia de la trombosis. La variedad, gravedad e intensidad de las manifestaciones dependerán de la localización de la trombosis, ya que cuanto antes se trate la trombosis mejor será el pronóstico de la lesión. Para ello se dispone de gran variedad de medicaciones antitrombóticas.
Tratamiento de la trombosis o de los coágulos sanguíneos
Los coágulos sanguíneos que se producen en la trombosis pueden provocar enfermedades críticas por el bloqueo del aporte de sangre al corazón, al cerebro, a los pulmones o a las piernas. Los coágulos sanguíneos que se desarrollan en las arterias pueden producir ataques cardíacos, como infarto agudo de miocardio (IAM), angina o ictus (infarto cerebral) y dolor intenso en las piernas con dificultad para caminar (claudicación intermitente). Los coágulos sanguíneos de las venas o el sistema venoso pueden producir trombosis venosa profunda (TVP) en las venas de la pelvis, las piernas o las extremidades superiores. Si se desprende un émbolo de uno de estos trombos y viaja por el interior de la circulación sanguínea hasta el corazón y de éste a los vasos sanguíneos del pulmón, puede producir allí una embolia pulmonar aguda o tromboembolismo pulmonar (TEP).
La medicación antitrombótica puede actuar a través de tres mecanismos distintos y en tres grados del proceso de la hemostasia:
Medicación antiplaquetaria o antiagregante. Inhibe el funcionamiento plaquetario.
Medicación anticoagulante. Inhibe el proceso de la coagulación plasmática.
Medicación trombolítica. Acelera la destrucción del trombo ya formado.
Fármacos antiplaquetarios o antiagregantes
Los fármacos antiplaquetarios o antiagregantes que se administran por vía oral son básicamente: ácido acetilsalicílico (Aspirina, Adiro 100 y 300, Bioplak y Tromalyt), triflusal (Disgren), dipiridamol (Persantin, Miosen), ticlopidina (Ticlodone, Tiklid, Ticlopidina Bayvit, Ticlopidina Cinfa, Ticlopidina Merck, Ticlopidina Normon, Ticlopidina Qualix, Ticlopidina Ratiopharm, Ticlopidina UR ) y clopidogrel (Iscover, Plavix). El ácido acetilsalicílico (AAS) es el más estudiado y mejor conocido y normalmente, el de primera elección, reservándose el resto para aquellos pacientes que no pueden tomarla. El AAS actúa inhibiendo la producción del TXA2 plaquetario, que es procoagulante a través del bloqueo de la acción de la enzima COX. Son antiplaquetarios inyectables abciximab (Reopro), eptifibatida (Integrilin) y tirofibán (Agrastat), que normalmente se emplean en tratamiento intrahospitalario y siempre en asociación con AAS.
Fármacos anticoagulantes
Dentro del grupo de los anticoagulantes se diferencian los de administración inyectable y los orales.
El anticoagulante de administración intravenosa es la heparina no fraccionada o heparina sódica, mientras que la heparina cálcica puede administrarse por vía subcutánea. Las heparinas de bajo peso molecular (HBPM), como bemiparina (Hibor, Phivor), dalteparina (Boxol, Fragmin), enoxaparina (Clexane, Decipar), nadroparina (Fraxiparina), y tinzaparina (Innohep), se administran por vía subcutánea. Todos ellos actúan inhibiendo el factor X de la coagulación a través de la acción de la AT III. Las hirudinas son anticoagulantes sintéticos análogos al anticoagulante natural de la sanguijuela, como desirudina (Revasc) y lepirudina (Refludin) que también se administran por vía parenteral y que actúan directamente sobre la trombina.
Los anticoagulantes orales o antivitaminas K (su nombre se debe a que actúan impidiendo la activación de los factores de la coagulación que dependen de la vitamina K) son los derivados cumarínicos, fundamentalmente el acenocumarol (Sintrom) y la warfarina (Aldocumar, Tedicumar). Se espera la próxima comercialización de un nuevo anticoagulante oral, el ximelagatran (Exanta), un inhibidor de la trombina.
Fármacos trombolíticos o fibrinolíticos
Los trombolíticos o fibrinolíticos, que actúan destruyendo la fibrina que estabiliza el trombo, son estreptoquinasa (Kabikinase, Streptase), que es el patrón del grupo y el de primera elección, alteplasa (Actilyse), reteplasa (Rapilysin), tenecteplasa (Metalyse) y uroquinasa (Urokinase Vedim, Uroquidan), de empleo estrictamente intrahospitalario y administración casi exclusivamente intravenosa.
FARMACOTERAPIA DE LA TROMBOSIS ARTERIAL
El tratamiento farmacológico de los coágulos arteriales se basa en el empleo de agentes antiplaquetarios orales, como AAS o clopidogrel; anticoagulantes como la heparina, y los agentes trombolíticos, que destruyen los coágulos ya formados. Además de la medicación, suelen emplearse técnicas quirúrgicas, como la angioplastia mediante catéteres especiales para eliminar o comprimir estos coágulos arteriales.
Agentes antiplaquetarios
La administración de un comprimido de AAS (500 mg) al inicio de los síntomas de un ataque cardíaco puede aumentar la supervivencia en al menos un 20%. Por tanto, un profesional de la salud (médico o paramédico) puede administrar AAS al paciente que se sospecha que está presentando un ataque cardíaco para reducir la gravedad de la lesión del músculo cardíaco antes de que llegue el personal médico de urgencias.
Recientemente se ha introducido un nuevo fármaco antiplaquetario, clopidogrel, que administrado junto con AAS, ayuda a reducir el riesgo de mortalidad por un ataque cardíaco.
También pueden emplearse los agentes antiplaquetarios intravenosos para impedir o frenar la evolución del ataque cardíaco, en combinación con AAS y clopidogrel. Esta terapia antiplaquetaria triple es muy potente y predispone al paciente a la hemorragia, sin embargo, las complicaciones hemorrágicas graves, incluida la hemorragia de una úlcera de estómago, son raras.
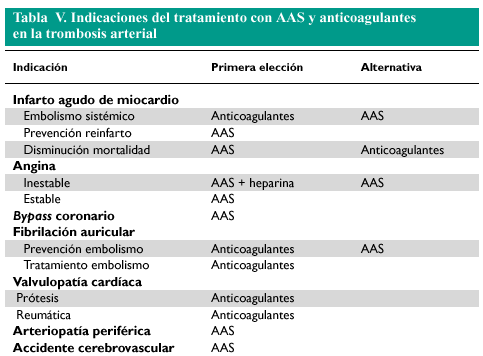
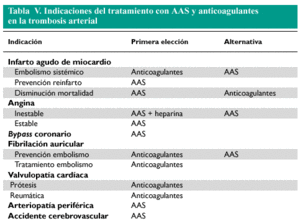
La tabla V recoge las indicaciones del tratamiento con AAS y anticoagulantes en casos de trombosis arterial.
Anticoagulantes
La heparina intravenosa, administrada de forma continuada, es el anticoagulante tradicionalmente prescrito para prevenir el aumento del tamaño de un coágulo sanguíneo. Alcanzar la dosis más eficaz requiere la valoración frecuente de las pruebas de coagulación sanguínea, mediante el registro del tiempo de tromboplastina parcial (TTP). Para el tratamiento de un paciente con un ataque cardíaco se requiere una dosis de heparina ajustada a un TTP de entre 50 y 70 segundos.
Las llamadas heparinas de bajo peso molecular (HBPM) constituyen un importante avance sobre la heparina tradicional. Las HBPM administradas una o dos veces al día mediante inyección, a una dosis calculada en función del peso del paciente, normalmente no requieren un ajuste de la dosis y poco o ningún control con las pruebas de coagulación. Al igual que la heparina, pueden producir como efecto secundario una hemorragia no deseada.
Agentes trombolíticos
Estos medicamentos son capaces de disolver los coágulos arteriales, pero causan problemas hemorrágicos más graves que los agentes antiplaquetarios o los anticoagulantes. Los agentes trombolíticos no son capaces de diferenciar entre un coágulo peligroso que está produciendo un ataque cardíaco y un coágulo beneficioso que está impidiendo una hemorragia de una úlcera de estómago o de una arteria cerebral lesionada. Por tanto, aunque se asocian a una tasa aproximada de un 20% de mejoría sobre la supervivencia de un ataque cardíaco, también se asocian a una tasa de hemorragia cerebral del alrededor del 1%.
FARMACOTERAPIA DE LA TROMBOSIS VENOSA
Los anticoagulantes previenen la formación de más coágulos y permiten que los procesos naturales de disolución de los coágulos del organismo hagan frente a la producción de una TVP o de un TEP. El tratamiento de la trombosis venosa requiere heparina por su rápida acción anticoagulante, junto con cumarínicos (anticoagulantes orales). Los cumarínicos se administran una vez al día y, normalmente, requieren al menos 5 días para ser completamente eficaces. Los pacientes con una TVP o un TEP masivos pueden recibir agentes trombolíticos además de heparina y warfarina.
Al 5% de pacientes, aproximadamente, que no pueden tolerar los anticoagulantes o en los que no resultan eficaces, se suele insertar un filtro metálico permanente en el interior de la vena cava inferior, la principal vena que recoge toda la sangre por debajo del corazón. Este filtro impide que lleguen a los pulmones los coágulos de gran tamaño que se han desprendido de las venas pélvicas o de las piernas. De todos modos, el filtro no detiene el proceso de coagulación de la sangre.
HBPM
Las HBPM han hecho que la TVP aguda no complicada pase de ser una enfermedad que requería al menos 5 días de ingreso hospitalario, a ser una enfermedad que normalmente puede ser tratada de forma ambulatoria o con una única noche de ingreso en el hospital. Las HBPM autorizadas para el tratamiento ambulatorio de la TVP se administran dos veces al día. La dosis debe reducirse en presencia de enfermedad renal o gran obesidad. La acción anticoagulante de las HBPM es totalmente eficaz ya a las pocas horas de su administración y los pacientes o los miembros de la familia pueden aprender a inyectarla.
Heparina intravenosa
El tratamiento estándar del TEP requiere la infusión intravenosa continuada de heparina, administrada a mayor intensidad que para los coágulos arteriales, con una dosis ajustada a un TTP de 60-80 segundos. La heparina intravenosa se administra durante todo el ingreso hospitalario, que normalmente se prolonga de 5 a 7 días, hasta que el anticoagulante oral warfarina es ya totalmente eficaz. Existe una tendencia creciente a emplear HBPM en lugar de heparina intravenosa, especialmente tras el primer día o dos de hospitalización, una vez es aparente la mejoría clínica. Algunos pacientes con TEP de bajo riesgo pueden ser dados de alta tras varios días de administración de HBPM como puente hasta la eficacia de los cumarínicos.
Anticoagulantes orales
Como se ha señalado, los cumarínicos, acenocumarol y warfarina, también denominados antivitaminas K, actúan como anticoagulantes orales por disrupción del sistema natural de coagulación dependiente de la vitamina K del organismo. Los cumarínicos son la base del tratamiento a largo plazo de la TVP y del TEP y son esenciales para la prevención del infarto cerebral a causa de una fibrilación auricular y para la prevención de la trombosis de las válvulas cardíacas mecánicas.
Seguridad y eficacia
Los cumarínicos constituyen un reto en cuanto a la seguridad y eficacia de su administración, puesto que requieren mucha colaboración entre el paciente y su médico y generan más preguntas y cuestiones a los profesionales de la salud que cualquier otro medicamento que se receta (tabla VI). Los pacientes se enfrentan a un doble riesgo: poco anticoagulante oral puede producir una trombosis catastrófica; demasiado anticoagulante oral puede producir hemorragias muy graves.
Al igual que la heparina intravenosa y a diferencia de otras muchas medicaciones, los cumarínicos no pueden prescribirse a una dosis fija o según el peso. Por el contrario, su dosis debe ajustarse de acuerdo a una prueba sanguínea de laboratorio que mide la duración del tiempo que tarda en empezar a formarse el coágulo, el llamado tiempo de protrombina (TP) o tiempo de Quick. Esta prueba está estandarizada para diferentes procesos de laboratorio y se denomina INR (por las siglas en inglés de International Normalized Ratio, o Razón Internacional Normalizada). El INR de un individuo sano que no toma cumarínicos es de 1,0. El INR aumenta con la intensidad creciente de la anticoagulación. Para los pacientes con TVP o TEP, el INR habitual es entre 2,0 y 3,0. En algún paciente individual puede ser necesaria una anticoagulación aún más intensa, para la que el INR se establece en hasta 4,0.
La tabla VII refleja los valores recomendados del INR de los anticoagulantes orales.
Interacciones
Cuando se administran cumarínicos existen numerosas interacciones con fármacos y con alimentos que afectan al INR. Por tanto, la monitorización periódica del INR es esencial para establecer la dosis óptima. Normalmente, al principio del tratamiento, el INR se obtiene varias veces a la semana. Cuando se alcanzan un INR y una dosis estables de cumarínicos, la frecuencia del INR se va reduciendo gradualmente hasta una vez al mes. Es necesaria una monitorización más frecuente cuando se empiezan a tomar o se interrumpen otras medicaciones, como por ejemplo las que se dispensan sin receta médica, las vitaminas, los remedios naturales a partir de hierbas, minerales o plantas. En este sentido, amiodarona es un fármaco antiarrítmico frecuentemente recetado. También muchos antibióticos aumentan marcadamente el efecto anticoagulante de los cumarínicos, produciendo un aumento excesivo del INR. El consumo elevado o la abstinencia de los alimentos que contienen vitamina K, como las espinacas, el brócoli y las coles de Bruselas, afectarán al INR. La combinación de alcohol con warfarina aumentará la probabilidad de hemorragia, aun en situaciones en que el INR no aumenta marcadamente. En ocasiones pueden aparecer importantes fluctuaciones del INR sin una causa aparente o identificable.
La tabla VIII detalla los principales fármacos que pueden emplearse en individuos tratados con anticoagulantes orales y aquéllos que interaccionan.
Alternativas a los cumarínicos
Las estrategias alternativas son limitadas. Por ahora incluyen las HBPM autoinyectables (tabla IX), una o dos veces al día, y la heparina tradicional autoinyectable, dos o tres veces al día. En el futuro se dispondrá de nuevos agentes orales que proporcionarán anticoagulación inmediata con una menor necesidad de monitorización sanguínea.
Más recientemente se ha introducido el primer anticoagulante inhibidor selectivo del factor Xa, el fondaparinux sódico, un antitrombótico sintético indicado exclusivamente en la prevención de la trombosis tras cirugía ortopédica mayor, como cirugía electiva o de emergencia de cadera y cirugía mayor de rodilla. Su mecanismo de acción se basa en la adhesión de gran afinidad, rápida y reversible a las moléculas de AT III, incrementando 300 veces su efecto inhibidor del factor Xa, lo que interrumpe el proceso clave de la cascada de coagulación, previniendo la formación y el desarrollo de los trombos. Se administra mediante inyección única diaria, a las mismas dosis para todos los pacientes e indicaciones.
BIBLIOGRAFÍA GENERAL
Fuster V, Ryden LE, Asinger RW, et al. ACC/AHA/ESC guidelines for the management of patients with atrial fibrillation: executive summary: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines and the European Society of Cardiology Committee for Practice Guidelines and Policy Conferences (Committee to Develop Guidelines for the Management of Patients With Atrial Fibrillation) Developed in Collaboration With the North American Society of Pacing and Electrophysiology. Circulation 2001;104:2118-50.
Gelfand EV, Piazza G, Goldhaber SZ. Venous thromboembolism guidebook. Critical Pathways in Cardiology 2002; 1:26-43.
Goldhaber SZ, Morrison RM. Pulmonary embolism and deep vein thrombosis. Circulation 2002;106:1436-8.
ISIS-2 (Second International Study of Infarct Survival) Collaborative Group. Randomised trial of intravenous streptokinase, oral aspirin, both, or neither among 17,187 cases of suspected acute myocardial infarction: ISIS-2. Lancet 1988;2:349-60.
Ornato JP, Hand MM. Warning signs of a heart attack. Circulation 2001;104:1212-13.
Well PS, Büller HR. Outpatient treatment of patients with pulmonary embolism. Seminars in Vascular Medicine 2001; 1:229-33.
Yusuf S, Zhao F, Mehta SR, et al. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndromes without ST-segment elevation. N Engl J Med 2001;345:494-502.