Se analizan en este trabajo los diversos factores que intervienen en las políticas de fijación de precios de los medicamentos y las estrategias de contención de la factura farmacéutica pública en los países desarrollados, haciendo especial hincapié en las luces y las sombras de los sistemas de precios de referencia, que ocupan un lugar destacado en este contexto.
El aumento del gasto público en medicamentos en buena parte de los países de nuestro entono justifica la necesidad de plantear una reforma de los mecanismos de reembolso de los fármacos. Actualmente el llamado «gasto farmacéutico» representa entre el 19 y el 29% del gasto sanitario en todos los países de la Unión Europea (UE)1. Las principales causas que se asocian con este aumento de la factura farmacéutica pública son:
El envejecimiento de la población, dado que comporta el desarrollo de enfermedades crónicas que requieren medicamentos relativamente más caros desarrollados a raíz de innovaciones tecnológicas de la biotecnología. Ello puede traer unas consecuencias progresivas más importantes en los próximos 30 años.
La inclusión de medicamentos patentados y generalmente más caros en la prestación farmacéutica que no siempre están asociados a una innovación que presente unos efectos muy significativos sobre el estado de salud.
La ineficacia de los mecanismos de control de precios para limitar el gasto público.
POLÍTICAS DE ACTUACIÓN
Los objetivos de contención del gasto público en medicamentos guían el establecimiento de diferentes políticas que pueden clasificarse en políticas de demanda y políticas de oferta2.
Políticas de demanda
Las políticas de demanda se refieren esencialmente al control de la prescripción (por ejemplo, a través de incentivos al proveedor o el establecimiento de un presupuesto para fármacos) y la utilización de medicamentos, el establecimiento de sistemas de copago que reduzcan los incentivos a sobreconsumir cuando los medicamentos están subsidiados, medidas de educación sanitaria y de racionalización del consumo de medicamentos, así como el desarrollo de un mercado de medicamentos OTC.
Políticas de oferta
Las políticas de oferta se dirigen al control de la conducta y la innovación tecnológica por parte de la industria, al establecimiento de listas positivas o negativas de medicamentos, al fomento de la importación paralela, los controles legislativos de precios, el control de la tasa de beneficios y especialmente al establecimiento de un sistema de precios de referencia (SPR).
Objetivos
Mientras que las políticas de oferta tienen como objetivo la regulación de la industria y el fomento de la innovación a la vez que el control de precios, las políticas de demanda en general tienden a controlar los incentivos que desde el propio consumidor o el médico llevan al sobreconsumo. En este trabajo nos centraremos en las medidas de oferta, y en especial en el análisis de los precios de referencia como medida para el control del gasto y el fomento de la competencia en el mercado de medicamentos.
LA NECESIDAD DE REGULACIÓN DE PRECIOS Y DE LA COMPETENCIA
Los diferentes argumentos que justifican la regulación de precios giran alrededor de la imperfección del mercado de los productos farmacéuticos. En particular, el mecanismo de precios que equilibra un mercado convencional no es el sistema aplicable a este mercado; ello lleva en ocasiones a las empresas farmacéuticas a vender por encima del precio que los consumidores estarían dispuestos a pagar. La competencia en el sector se centra en dimensiones de calidad, lo que contribuye a la monopolización del mercado. No obstante las principales razones que nos llevan a argumentar la necesidad de una regulación de precios son las siguientes:
Los productos farmacéuticos constituyen desde una perspectiva económica un input (o un recurso) esencial en el proceso de producción de servicios sanitarios. Su papel esencial por sí mismo ya podría justificar el hecho de que existiera una regulación de precios, ya que si bien el mercado puede satisfacer una demanda, no siempre el precio al que las empresas están dispuestas o ofrecer un producto es el precio más deseable.
Los medicamentos son bienes que están sujetos a una elevada innovación tecnológica, generalmente protegida por un sistema de patentes. La patente concede una prima al innovador con la finalidad de garantizar que la empresa innovadora recupere los costes de la innovación y tenga incentivos para seguir innovando al asignar un poder de mercado temporal sobre el producto registrado. No obstante, ¿qué sucede cuando la patente agota su período de vigencia? Entonces, la estrategia de la empresa es la de explotar la marca o diferenciar el producto con la finalidad de sacar el máximo rendimiento posible haciendo innovaciones mínimas en el proceso o en la presentación del producto. La consecuencia de ello es que los productos farmacéuticos se estructuran en diferentes submercados terapéuticos en los que existe una importante diferenciación vertical y horizontal, es decir, tanto de producto como de marca. Ello, a su vez, exige una regulación que evite o incentive la extensión de productos con unos beneficios terapéuticos marginales.
La demanda de productos farmacéuticos esta sujeta a una relación de agencia entre médico y paciente, en la que el médico es el principal (o el decisor) y el paciente es un agente (o el que realiza en consumo en sí), de tal modo que es el médico el que determina el medicamento a consumir por el paciente, pero no el que soporta el coste. En ocasiones, se argumenta que el médico es «inductor de demanda», especialmente cuando la prescripción de un medicamento determinado conlleva un beneficio personal para el médico (por ejemplo, la financiación de la asistencia del facultativo a un congreso por parte de la empresa farmacéutica fabricante del producto en cuestión). La consecuencia de este fenómeno es que salvo que existan incentivos adecuados, la demanda de medicamentos será poco sensible al precio de éstos. Ello puede explicar la todavía limitada penetración de los medicamentos genéricos en mercados como el español, ya que el efecto de los mismos ha sido el de bajar el precio de los medicamentos en general. Por otra parte, algunos trabajos constatan la reducida sensibilidad de la demanda de un medicamentos cuando varía el precio de los productos sustitutivos, ya sean del mismo o de grupos terapéuticos similares (en función del sistema de cada país). Ello motiva la necesidad de que «el tercer pagador» o la Administración sanitaria deba establecer algún sistema de regulación. Incluso en el supuesto de que la relación médico-paciente fuera la de una agencia perfecta (es decir, que no existieran problemas de inducción de demanda y que las decisiones del médico fueran en todas sus dimensiones las mejores decisiones para el paciente) no siempre será posible informar al médico sobre las alternativas con menor coste, lo que hace necesaria la intervención pública para corregir imperfecciones en el mercado.
CÓMO REGULAR LOS PRECIOS
Si aceptamos que es necesario un determinado nivel de regulación de precios, la siguiente cuestión es: ¿cómo regular los precios? ¿Cuál es el sistema más deseable? De lo anterior cabe destacar que (al menos teóricamente) la regulación de precios por parte de las autoridades debería estar dirigida a la consecución de unos objetivos de eficiencia y bienestar. En todo mercado regulado, existen objetivos contrapuestos entre mantener precios suficientemente bajos (con lo que se mejora el bienestar del consumidor) y establecer precios suficientemente elevados como para que fomenten la innovación tecnológica, y que a través de ello mejoren la salud de la población. Estudios recientes muestran que la innovación farmacéutica ha incrementado la esperanza de vida y la renta vital entre un 0,75 y un 1% anual3. La regulación de precios vendrá determinada por:
El tamaño del mercado de genéricos y, en general, por aquellos otros factores que aumentarán la competencia y la sensibilidad al precio de los productos farmacéuticos.
El grado de innovación de la industria, ya que una limitación del precio aumentaría los costes de una menor innovación de acuerdo con la sensibilidad de la innovación tecnológica al precio de los medicamentos. No obstante, ¿qué se puede clasificar como innovación? ¿Cómo determinamos si un medicamento añade un beneficio terapéutico?
El establecimiento de un criterio científico para dar respuesta a la primera pregunta es complicado ya que siempre resulta difícil establecer la frontera de lo que se entiende por aportación real al producto. En cuanto a la segunda cuestión, cabe destacar que el Reino Unido es el único país que cuenta con una agencia específica a escala estatal que aplique un criterio de coste-efectividad también conocido como «cuarta barrera» (fourth hurdle) a la aprobación de medicamentos para su financiación pública.
INFLUENCIA DE LA REGULACIÓN EN LOS PRECIOS
La influencia de la regulación en el precio de los medicamentos es muy significativa y efectiva. Del análisis de la evidencia entre países se pone de manifiesto que los precios de los medicamentos son efectivamente inferiores en aquellos países con restricciones de precios más severas No obstante, la regulación de precios no siempre es efectiva para limitar el gasto, ya que la consecuencia de unos precios bajos es el aumento del consumo y el desarrollo de nuevos productos, por lo que los efectos de la regulación de precios sobre el gasto son cuestionables4.
Los principales sistemas de regulación de precios se pueden clasificar de acuerdo con el grado de regulación. En general, el grado de regulación de la industria responde a diferentes objetivos de política industrial. Como hecho estandarizado se observa que aquellos países que presentan una mayor innovación tecnológica son aquellos que muestran una regulación más flexible. Así, destacan en primer lugar países como Alemania, Dinamarca o Estados Unidos, donde hay precios libres. En segundo lugar, el Reino Unido se caracteriza porque si bien allí está regulada la tasa de beneficios de la industria, existe una elevada flexibilidad en la definición de las reglas del juego. En tercer lugar, en otro grupo de países tiene lugar una negociación entre industria y Administración con objetivos de gasto, como sucede en sistema francés o en el sueco y finalmente cabe citar los sistemas del sur de Europa y Finlandia, en los que la regulación de la industria es más intensa.
PRECIOS DE REFERENCIA
Los sistemas de precios de referencia operan a través del establecimiento de un precio de reembolso de referencia a una agrupación de productos similares o grupo homogéneo (depende del sistema), previamente especificados. La Administración sanitaria tan sólo paga el precio establecido de referencia por el medicamento consumido, y por lo tanto cualquier exceso por encima de ese precio será satisfecho por el asegurado (el ciudadano en un sistema nacional de salud). La consecuencia de este sistema es que el consumidor conoce cuál es el precio de referencia de cada medicamento, generalmente asesorado por el farmacéutico, cuya misión es informar sobre la posible «sustitución por genéricos». Actualmente los países de la Unión Europea que cuentan con este sistema son Alemania, Suecia, Dinamarca, Italia, Bélgica, Países Bajos y por último, más recientemente, se ha implantado en España. Como países de la OCDE con este sistema destacan Noruega, Australia, Nueva Zelanda, Canadá y Estados Unidos. Los principales efectos del sistema de precios de referencia se centran en determinadas circunstancias en la reducción de precios, al incentivarse la sustitución de genéricos, y por ello la competencia en el submercado, así como en su impacto en la innovación.
Los efectos del SPR sobre el gasto público en medicamentos y el bienestar de los pacientes y ciudadanos no son concluyentes
SISTEMAS DE REFERENCIA
Teóricamente, cabe distinguir dos sistemas a partir de los que establecer el precio de referencia:
Sistemas de referencia externa
Son aquéllos en los que el precio está determinado a través de comparaciones internacionales, ya sea adoptando el precio de otros países o estableciendo una media ponderada de diversos países. El problema de este sistema es la selección de los países de referencia: ¿bajo qué criterios se seleccionan? ¿Criterios de renta? Por otra parte, los reguladores tienen una menor información sobre la evolución del mercado del país de referencia que las propias empresas. Además, la información sobre los precios de los medicamentos en términos reales resulta muy difícil de obtener. Asimismo, si los países que se seleccionan para referenciar el precio están fuera del ámbito de la Unión Monetaria Europea, surge la problemática de los posibles efectos de variaciones en el tipo de cambio sobre el precio de referencia de los medicamentos.
Sistemas de referencia interna
Estos sistemas se basan en el establecimiento de diferentes tipos de agrupaciones de medicamentos bajo el principio de la «intercambiabilidad de productos». El precio de referencia no tiene por qué ser el precio real de mercado, pero cualquier diferencia será desembolsada por el consumidor, y de hecho se observa cómo se produce un ajuste del precio de los medicamentos de marca al de los genéricos con precio igual o inferior al de referencia para evitar quedar por debajo del PR y perder cuota de mercado. Este sistema, si bien no está exento de complejidades, es el que acostumbra a utilizarse en los sistemas implantados de precios de referencia.
DETERMINANTES DE LA EFECTIVIDAD DEL SPR
Ocho factores actúan como determinantes de la efectividad que puede tener un sistema de precios de referencia:
El nivel de cobertura del mercado sujeto al SPR
Entre otros aspectos, quizás el más relevante es el grado de detalle en la delimitación de los productos incluidos en cada grupo. De mayor a menor detalle, cabe distinguir:
a) Grupos de medicamentos que presenten un principio activo similar.
b) Medicamentos que presenten principios activos terapéuticamente comparables o
c) Medicamentos que tengan efectos terapéuticos comparables.
El principal problema derivado de realizar una clasificación muy detallada es la exclusión del grupo de medicamentos cuyos efectos terapéuticos son similares, lo que en teoría incentiva el consumo de medicamentos del grupo cuyo precio de referencia es mayor. Actualmente, en Alemania el SPR cubre el 50% del mercado, si bien el proceso de extensión del sistema se inició en 1989 y ha presentado dos modificaciones sustanciales desde su implantación.
El precio usado como referencia
Dicho precio puede determinarse como el menor precio del grupo, como el precio medio del grupo o como una media ponderada de los menores precios del grupo.
La extensión del mercado de medicamentos genéricos
Los medicamentos genéricos presentan un precio inferior al de las marcas (dado que no incorporan los «costes hundidos» de promoción e I+D). Así, en un país donde la extensión de los genéricos es elevada, cabe esperar que un sistema de precios de referencia tenga unos efectos más importantes en la contención de los precios. Por otra parte, una baja extensión de los medicamentos genéricos puede ser una limitación a la aplicabilidad del sistema. De hecho la mayoría de países en los que se ha aplicado este sistema se caracterizaba por una elevada implantación del mercado de medicamentos genéricos.
Para la profesión farmacéutica los precios de referencia suponen un reto, pues le ofrecen un mayor protagonismo en la contención del gasto e introducen mayor complejidad en la dispensación
Inclusión de medicamentos patentados
El hecho de que el sistema incluya o no medicamentos patentados también es decisivo. Entre los países que incluyen medicamentos patentados en la Unión Europea destacan Alemania y Países Bajos. La inclusión de medicamentos patentados limita considerablemente la explotación de innovaciones marginales en los productos ya incluidos en el SPR. Así, la estrategia de las empresas se concentrarán en la investigación de productos que no presenten sustitutos incluidos en el SPR. La consecuencia de ello es un incremento de los precios en el caso de que se produzca una innovación.
Sistema de precios del resto del mercado
Otro factor importante es el sistema de precios que se establezca para el resto del mercado, esto es, un sistema de precios libres, de precios basados en el coste, etc. Generalmente, los países que han optado por SPR han sido países en los que existían precios libres (como es el caso de Alemania) o precios negociados (como sucede en Suecia).
Conducta de los prescriptores
La eficacia del sistema de precios de referencia depende especialmente de la conducta de los prescriptores, y por tanto de la existencia de incentivos a los médicos para prescribir medicamentos de precios bajo. En Alemania, los médicos han protegido a los pacientes de los copagos y de los precios de referencia, ya sea prescribiendo medicamentos por debajo del precio de referencia o bien medicamentos más caros fuera del sistema5.
Evoluciones del mercado
De la experiencia alemana y holandesa (y últimamente también de la española) se observa que los laboratorios productores de medicamentos de marca han reducido sus precios hasta equipararlos con los de referencia. También se han apreciado incrementos del precio de los productos de precio reducido. Por otra parte en Alemania y Países Bajos las especialidades farmacéuticas genéricas han ido aumentado su cuota de mercado a pesar del relativo incremento de su precio, por lo que se ha producido un desplazamiento de beneficios hacia las empresas productoras de genéricos.
Costes humanos y sociales
Otros aspectos de la implantación de los precios de referencia son los costes humanos y sociales. Evidencia de este tipo de costes se ha obtenido de las opiniones de la profesión médica y de los profesionales de la farmacia. Según un estudio desarrollado en Canadá, la sustitución de los medicamentos prescritos como consecuencia de la implantación del SPR generó algunos problemas6. Desde la profesión farmacéutica se detectaron inconvenientes y confusiones: casos de falta de cumplimiento en personas mayores, pacientes que se quejaban de los efectos del sistema sobre su economía familiar y efectos adversos derivados de la sustitución de medicamentos dentro un mismo grupo terapéutico (conforme al funcionamiento del modelo canadiense).
Sostenibilidad del efecto ahorro
Los efectos de la aplicación del sistema de precios de referencia en Alemania y Suecia fueron significativos en su día pero su duración fue muy corta, de manera que el resultado final ha sido incierto en términos agregados sobre el gasto. Si bien tuvo un efecto en la reducción de los precios, no tuvo el mismo efecto sobre el volumen sino todo lo contrario: la reducción de precios aumentó el volumen de medicamentos consumidos. En cuanto a los medicamentos no incluidos en el SPR, se observó un aumento del consumo, tanto en valores como en unidades, debido a una cambio en las pautas de prescripción.
SPR EN ESPAÑA
En España, el escenario de implantación del SPR es notoriamente distinto al del resto de países de la Unión Europea en los que se ha implantado el sistema. Entre sus características merece la pena destacar las siguientes:
La cobertura del mercado del sistema de precios de referencia es aún reducida, por lo que independientemente de otros factores, el impacto en el gasto también debería ser moderado, ya que éste dependerá especialmente de la evolución de los precios de los productos que están excluidos del SPR.
La implantación del mercado de medicamentos genéricos es muy limitada y se sitúa en torno al 3%, mientras que en países como Alemania es 12 veces mayor. Ello es debido a que la legislación sobre patentes de producto en España es relativamente nueva, el farmacéutico tiene una capacidad de sustitución muy limitada y la regulación es bastante rígida. Si bien el SPR puede fomentar la extensión de medicamentos genéricos en España, a corto plazo el peso de este mercado, aún reducido, limitará la efectividad del SPR.
En cuanto al resto del mercado, se mantiene el sistema de precios intervenidos basados en el coste, por lo que los objetivos de competencia en precios propios del SPR quedan limitados. Tal como muestran estudios realizados para el mercado sueco, la existencia de una intervención en los precios reduce el grado de competencia en el mercado de medicamentos7.
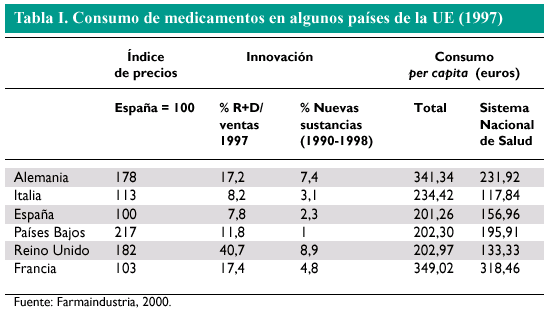
La escasa innovación tecnológica de los laboratorios españoles en relación con otros países de la UE hace esperar pocos beneficios de los precios de referencia. Tal como muestra la tabla I, en relación al resto de países de su entorno, el esfuerzo innovador de la industria española es moderado, al igual que sus resultados. La introducción de productos innovadores incentivados por su no inclusión en el SPR es poco probable que tenga unos efectos importantes.
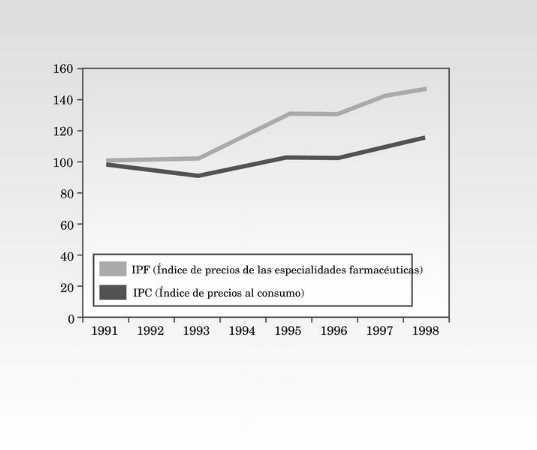
Dado que el sistema de precios de referencia tiene como finalidad la reducción del gasto a través de la contención de los precios de los medicamentos, los países para los que se diseñó este sistema fueron países con elevados niveles de precio unitario. No obstante, si bien en España los precios de los productos farmacéuticos en la década de los noventa registraron un crecimiento significativo (fig. 1), comparados con los de otros países de la UE son sustancialmente más bajos (tabla I), por lo que no parece que éste fuera el país paradigmático para aplicar el SPR.
Quizás la única característica que España comparte con los países que han implantados sistemas de precios de referencia es que el sector público es el comprador mayoritario de medicamentos (cerca del 75% de los medicamentos en España, frente al 73% en Alemania y al 80% en los Países Bajos (tabla I).
APORTACIONES FINALES
Los efectos del SPR sobre el gasto público en medicamentos y el bienestar de los pacientes y ciudadanos no son concluyentes. De las experiencias alemana y holandesa se puede concluir que el sistema de precios de referencia no tuvo un impacto significativo sobre el gasto, si bien redujo los precios de los medicamentos incluidos en el SPR. La consecuencia en términos de economía industrial fue una redistribución de beneficios desde las empresas innovadoras a las no innovadoras. Las consecuencias humanas y sociales tienen que ver con la mayor complejidad de la actividad de dispensación de medicamentos, así como con los efectos adversos que la sustitución de medicamentos pueden generar.
Los efectos del sistema de precios de referencia sobre la innovación se pueden resumir en:
Cambio en la estrategia de penetración en el mercado de las empresas innovadoras así y desincentivo para las innovaciones marginales de los productos ya existentes. Todo ello aumentará el riesgo de las actividades de innovación.
Un aumento de los precios en el caso de los medicamentos nuevos, por lo que el efecto final sobre el gasto es incierto.
Si aceptamos que la innovación tecnológica protegida por patentes aumenta el poder de mercado de la empresa innovadora, el sistema puede incentivar un aumento del grado de concentración del mercado. Para la empresa farmacéutica española, la introducción de este sistema implicará un esfuerzo en investigación.
Los efectos del SPR sobre el paciente no son tan evidentes. El sistema tiene repercusiones en la vertiente humana, desde el momento en que el consumo de medicamentos está muy influenciado por una «cultura de la marca» difícil de cambiar. A la vez, según algunas voces, sobre todo procedentes del colectivo médico, la sustituibilidad es fuente de problemas, porque los genéricos de un mismo grupo homogéneo son bioequivalentes respecto de la marca original pero no puede garantizarse, al parecer, que sean bioequivalentes entre ellos.
Quizás la razón por la que este sistema se ha implantado en España, más allá de unos objetivos de contención de gastos, esté más relacionada con motivos políticos, en tanto que es una respuesta a la recomendación de la Comisión Europea de 1998. Para la profesión farmacéutica supone un reto, dado que le ofrece un mayor protagonismo en la contención del gasto, a la vez que introduce una mayor complejidad en el proceso de dispensación. *