El virus de la hepatitis C (VHC) es un virus RNA de cadena sencilla que pertenece a la familia Flaviviridae. Actualmente se conocen seis genotipos del VHC, que se nombran mediante cifras arábigas, y un número variable de subtipos que se distinguen unos de otros mediante letras minúsculas (1a, 1b, 2a, 2b, etc.). La genotipificación es de gran interés, porque existen diferencias de patogenicidad en los diversos genotipos. Supuestamente, el genotipo 1b es más virulento, patogénico y resistente a la terapia con interferón que otros genotipos.
PREVALENCIA Y CLÍNICA
El virus de la hepatitis C infecta a más de 170 millones de personas en el mundo y es responsable del 20% de las hepatitis agudas y más del 70% de las hepatitis crónicas. La hepatitis C es la causa más frecuente de hepatitis crónica en nuestro medio.
La prevalencia de la hepatitis C se incrementa con la edad, desde 0,1% en menores de 15 años hasta el 8% en mayores de 55. En España afecta aproximadamente al 2% de la población. Existen, por tanto, alrededor de unos 800.000 portadores anti-VHC.
La infección aguda por VHC cursa de forma asintomática en un 80% de los casos. Por otro lado, se considera que el 85% de las hepatitis agudas C se cronifican.
La infección crónica por virus C puede evolucionar con o sin alteración de las transaminasas. Se sabe que los pacientes con GPT (transaminasa glutámino pirúvico) persistentemente normal (hasta el 40% de los pacientes con infección crónica por VHC) exhiben un curso más benigno.
Una gran proporción de los pacientes infectados de forma crónica por el virus C muestran una forma leve de hepatitis crónica, permaneciendo estables durante décadas. Sin embargo, otros pacientes evolucionan de forma rápida, desarrollando fibrosis hepática que progresa hacia cirrosis, incluso con implantación posterior de un carcinoma hepático.
El tiempo medio calculado de progresión a cirrosis es de unos 30 años, si bien hay pacientes que evolucionan de forma más rápida (en menos de 20 años) y otros que no lo hacen nunca o de forma muy lenta (al menos hasta en 50 años).
El consumo de alcohol y la coinfección por el virus de la hepatitis B (VHB) o el virus de la inmunodeficiencia humana (VIH) aceleran de forma importante la progresión de la enfermedad.
La infección crónica por VHC es subclínica en la mayoría (70% a 80%) de los casos. La mayor parte de los pacientes están asintomáticos o presentan síntomas leves e inespecíficos, fundamentalmente astenia o molestias en el hipocondrio derecho.
VÍAS DE TRANSMISIÓN DE LA ENFERMEDAD
Las vías de transmisión del VHC pueden ser parenterales y no parenterales. Son factores demostrados de riesgo de adquisición parenteral del VHC:
Transfusiones. El VHC es el virus de las hepatitis postransfusionales (hepatitis no-A y no-B). La determinación del anti-VHC en las donaciones sanguíneas disminuyó el riesgo de hepatitis postransfusional de 10% antes de 1990 al 1% en la actualidad.
Hemodiálisis. La prevalencia de VHC en hemodializados es del 20%. El número de transfusiones y el tiempo en hemodiálisis son factores directamente relacionados con la probabilidad de adquirir la infección.
Adicción a drogas parenterales (ADVP). Este colectivo muestra prevalencias de anti-VHC de hasta el 90%, siendo la primera causa de infección en adultos jóvenes. Ésta se adquiere al compartir jeringuillas, habitualmente en los primeros 6 meses de adicción. La vía intranasal asociada al consumo de cocaína es también una posible vía de infección.
Trasplante de órganos. Se han encontrado prevalencias de anti-VHC hasta en el 96% de receptores de órganos de donantes anti-VHC positivos, quienes desarrollan mayoritariamente enfermedad hepática sin que se haya demostrado que ello influya en la supervivencia de estos pacientes ni en las tasas de rechazo.
Personal sanitario. Enfermería es el colectivo de mayor riesgo, sobre todo en las unidades de hemodiálisis. En estudios españoles, tras una punción accidental con material contaminado VHC positivo el riesgo de transmisión es del 1%.
Hospitalización. A pesar de estar controladas las transfusiones y utilizar material desechable, se siguen comunicando casos de hepatitis C tras hospitalización y brotes tras estancia en una sala común. Estos casos se relacionan con la utilización de viales multidosis o con transmisión paciente a paciente si no se aplican estrictas medidas de asepsia. Se han documentado algunos casos tras endoscopia digestiva.
Otras vías parenterales. Tatuajes, acupuntura, pendientes, piercings y otras punciones percutáneas son posibles vías de infección de la hepatitis C.
Las vías de transmisión no parenteral comprenden:
Intrafamiliar. La mayoría de estudios en familiares de pacientes anti-VHC positivos muestran prevalencias de anti-VHC similares a la población general.
Vertical. La transmisión vertical es aquella que acontece de madre a hijo durante el parto. La coinfección por el VIH y la carga viral C elevada son factores que se relacionan de forma directa con la posibilidad de transmisión vertical. Se estima que es de un 5% en madres VIH negativas y de un 20% en madres VIH positivas o con una carga viral elevada.
Si bien se ha detectado RNA-VHC en la leche de madres VHC positivo, no se han detectado casos en los cuales la vía de transmisión pueda ser atribuida a la lactancia materna.
Sexual. Las relaciones sexuales no se consideran una vía efectiva de transmisión de la hepatitis C en parejas heterosexuales estables.
Las hepatitis C en las que no se reconoce un contagio parenteral se denominan hepatitis C esporádicas o adquiridas en la comunidad.
PREVENCIÓN
Para prevenir la posible transmisión por vías diferentes a la parenteral, la Conferencia de Consenso de la Asociación Europea para el Estudio del Hígado (EASL), celebrada en París en febrero de 1999, estableció los siguientes puntos:
1. No está justificado el uso del preservativo en parejas estables.
2. Se recomienda el uso del preservativo en pacientes VHC positivos con múltiples parejas sexuales.
3. El embarazo no está contraindicado en mujeres VHC positivas.
4. No se desaconseja la lactancia materna (no hay asociación entre ésta y transmisión madre/hijo).
5. No se recomienda realizar detección de VHC en embarazadas.
6. El tipo de parto (cesárea/vaginal) no influye en la tasa de transmisión vertical.
Extremar las medidas higiénicas en los centros sanitarios es necesario, sobre todo en hemodiálisis, cateterismos, cirugía y administración parenteral de fármacos.
Conocer a los portadores de VHC contribuye a la prevención. Se recomienda realizar tests anti-VHC a la población de especial riesgo: consumidores de drogas por vía parenteral, hemodializados, receptores de sangre, hemoderivados y trasplantados antes de 1990.
En caso de pinchazo contaminado con material VHC positivo debe hacerse seguimiento de VHC y transaminasas inicialmente y hasta pasados 6 meses de la inoculación.
La tabla I recoge recomendaciones importantes sobre el manejo de la hepatitis C y la tabla II resume algunos consejos decisivos para evitar su transmisión.
DIAGNÓSTICO
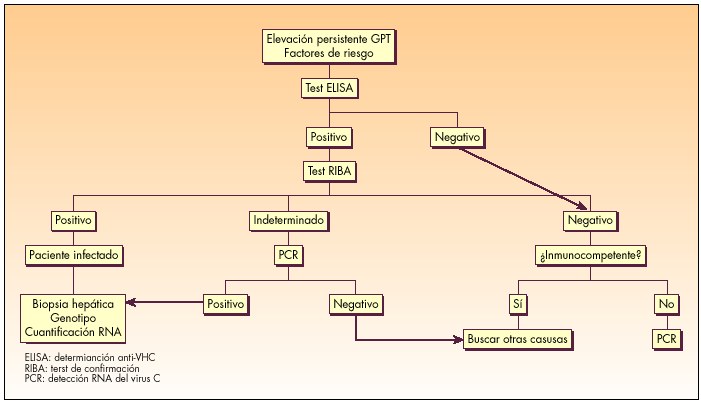
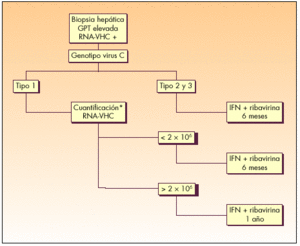
El diagnóstico de la infección por VHC es fundamentalmente virológico. Se basa en la detección de anticuerpos anti-VHC mediante un test de ELISA (inmunoanálisis). Actualmente se puede determinar de forma cuantitativa y cualitativa la presencia de ARN del VHC mediante técnica de PCR (Polymerase Chain Reaction; reacción en cadena de la polimerasa). La figura 1 muestra el algoritmo diagnóstico de la infección crónica por VHC.
Fig. 1. Algoritmo diagnóstico de la infección crónica por VHC
La cuantificación (carga viral) y la determinación del genotipo del VHC son útiles con miras al tratamiento.
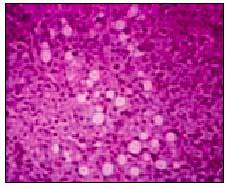
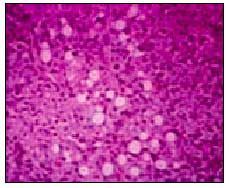
La biopsia hepática (fig. 2) permite precisar un diagnóstico, establecer un pronóstico y, en ocasiones, puede influir en el planteamiento terapéutico.
Fig. 2. Biopsia hepática
TRATAMIENTO FARMACOLÓGICO
Actualmente el tratamiento de la hepatitis crónica C está indicado en aquellos pacientes que presentan transaminasas persistentemente elevadas, positividad de los anticuerpos anti-VHC y del RNA del VHC en el suero y lesiones de hepatitis crónica en la biopsia hepática.
El tratamiento actual de la hepatitis crónica C es la combinación de interferón (IFN) y ribavirina. La pauta recomendada es 3 millones de unidades de interferón recombinante administrado por vía subcutánea, tres veces por semana, asociado a 1.000-1.200 mg/día de ribavirina por vía oral, dependiendo del peso corporal.
Recientemente se ha incorporado el interferón pegilado (Peg-IFN) que requiere una administración única semanal por vía subcutánea. Administrado a dosis de 1,5 µg/kg/semana produce una respuesta sostenida similar al tratamiento combinado estándar.
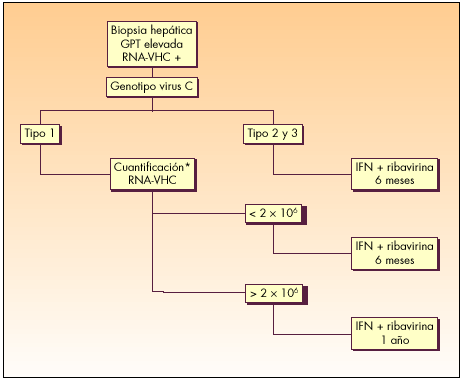
Fig. 3. Algoritmo terapéutico de la hepatitis crónica C
El interferón pegilado, una vez administrado por vía subcutánea, se absorbe de forma más lenta, tiene una aclaración sérica hasta 10 veces más lenta, una vida media de eliminación mucho más larga y alcanza niveles plasmáticos más prolongados y estables que el IFN normal. Por todo ello puede administrarse una sola vez a la semana, con la mejora que ello supone del cumplimiento terapéutico. En estos momentos hay disponibles dos tipos de Peg Interferón bien diferenciados y con propiedades farmacocinéticas distintas. Uno es de cadena ramificada y mayor peso molecular y el otro de cadena lineal.
Diferentes ensayos clínicos han identificado una serie de factores pretratamiento predictores de respuesta sostenida. Entre los factores positivos destacan el sexo femenino, ausencia de fibrosis en la biopsia hepática, genotipo viral 2 o 3, edad menor de 40 años y viremia (carga viral) baja.
La duración del tratamiento depende de dichos factores predictores, fundamentalmente el genotipo y la carga virales.
La respuesta al tratamiento se define según:
Criterios bioquímicos: normalización de las transaminasas.
Criterios virológicos: negativización del RNA-VHC.
Criterios histológicos: mejoría en el índice de actividad inflamatoria hepática.
La respuesta más utilizada es la virológica y se valora al terminar el tratamiento y pasados 6 meses. Si el paciente presenta una respuesta virológica sostenida, aquélla se prolongará como mínimo durante 10 años.
La pauta referida, en pacientes no tratados previamente, consigue una respuesta sostenida del 33% a los 6 meses de tratamiento y del 41% al año (frente al 5-15% en pacientes tratados con interferón en monoterapia durante 6-12 meses).
La respuesta al tratamiento es distinta según el genotipo del VHC. Los pacientes con genotipo 1 presentan una respuesta del 29% con tratamiento combinado durante 1 año. Por otro lado, en los pacientes con genotipos 2 o 3 la respuesta al tratamiento es la misma, en torno al 65%, con independencia de que se prolongue 6 o 12 meses. Por tal motivo, se recomienda que los pacientes con genotipo 1 sean tratados durante 12 meses, mientras que los pacientes con genotipos 2 o 3 es aconsejable que reciban tratamiento durante 6.
Otro factor que predice la respuesta al tratamiento es la carga viral. En pacientes con altos niveles de viremia (más de 2 millones de copias/ml) el tratamiento combinado durante 1 año produce una tasa de respuesta del 48%, frente al 28% si se prolonga durante 6 meses. Por dicha razón estos pacientes deberán recibir tratamiento durante 1 año.
Por el contrario, en los pacientes con bajos niveles de viremia (menos de 2 millones de copias/ml) el tratamiento combinado durante 6 meses ofrece la misma eficacia que durante 1 año, por lo que en ellos se aconseja el tratamiento durante 6 meses.
Los efectos adversos del tratamiento combinado son frecuentes, aunque generalmente leves y en raras ocasiones obligan a suspenderlo (tabla III).
BIBLIOGRAFÍA GENERAL
Bellentani S, Pozzato G, Saccoccio G, Crovatto M, Croce L, Mazzoran L et al. Clinical course and risk factors of hepatitis C virus related liver disease in the general population: report from the Dionysos study. Gut 1999;44:874-80.
Hernández E, Bruguera M, Puyuelo T, Barrera JM, Sánchez Tapias JM, Rodes J. Risk of needle-stick injuries in the transmission of hepatitis C virus in hospital personnel. J Hepatol 1992;16:56-8.
Manns M, McHutchison JC, Gorgon S et al. Peginterferon alfa-2b plus ribavirin compared to interferon alfa-2b plus ribavirin for the treatment of chronic hepatitis C: 24 week treatment analysis of a multicenter multinacional phase III randomised controlled trial. Hepatology 2000;32:297A.
McHutchison JG, Gordon SC, Schiff ER, Shiffman ML, Lee WM, Rustgi VK et al Interferon alpha-2b alone or in combination with ribavirin as initial treatment for chronic hepatitis C. N Engl J Med 1998; 339: 1485-1492.
Poynard T, Marcellin P, Lee SS, Niderau C, Minuk GS, Ideo G et al. Randomised trial of interferon alpha-2b plus ribavirin for 48 weeks or 24 weeks versus interferon alpha-2b plus placebo for 48 weeks for treatment of chronic infection with hepatitis C virus. Lancet 1998;352: 1426-32.
Poynard T, McHutchison J, Goodman Z, Ling M-H, Albrecht J Is an à la carte combination interferon alpha-2b plus ribavirin regimen possible for the first line treatment in patients with chronic hepatitis C? Hepatology 2000;31:211-8.
Reichard O, Norkrans G, Fryden A, Braconier JH, Sonnerborg A, Weiland O Randomised, double-blind, placebo-controlled trial of interferon alpha-2b with and without ribavirin for chronic hepatitis C. The Swedish Study Group. Lancet 1998; 351:1660-4.
Van der Poel CL Hepatitis C virus and blood transfusion: past and present risks. J Hepatol 1999; 31(Supl 1):101-6.