Datos epidemiológicos recientes han demostrado que cada año se realizan en Estados Unidos más de 70 millones de prescripciones de antiinflamatorios no esteroides (AINE). En el Reino Unido el consumo de AINE supera la cifra de los 20 millones y en España está por encima de los 25.
Una encuesta reciente señala que más del 60% de los españoles consume habitualmente analgésicos, entre los que se encuentran el ácido acetilsalicílico (AAS) y otros AINE. El 14% de la población mayor de 30 años los consume a diario y sólo menos del 5% de los encuestados afirma no necesitarlos nunca. El consumo de AINE aumenta de manera progresiva de año en año aunque sólo el 20% de las prescripciones provienen del reumatólogo, lo que sugiere que existe una prescripción inadecuada.
Los AINE constituyen un grupo heterogéneo de sustancias químicas ampliamente utilizadas en medicina por sus potenciales efectos sobre el dolor y la fiebre.
Estos fármacos son especialmente útiles y, en muchos casos, esenciales en el tratamiento de las manifestaciones clínicas producidas por las enfermedades articulares de carácter inflamatorio y degenerativo. Sin embargo, su uso prolongado puede ocasionar diversas lesiones gastrointestinales, algunas con potenciales complicaciones serias, incluso con riesgo para la vida del paciente. Las lesiones por AINE producen en Estados Unidos más de 70.000 hospitalizaciones y 70 muertes al año.
Su utilización no está exenta de riesgo, ya que en hasta un 25% de los casos se asocian a efectos adversos de diversa consideración. Los efectos sobre el tubo digestivo son los más conocidos y llegan a provocar que un 10% de los pacientes interrumpan el tratamiento. Dentro de los primeros 90 minutos tras la toma de una dosis tan baja como 75 mg de AAS, la mucosa del estómago presenta punteado hemorrágico y erosiones.
Se entiende por gastrolesividad las lesiones, la intolerancia, las complicaciones y los efectos adversos de sustancias potencialmente lesivas, como los AINE, en la zona gastroduodenal. En estos momentos es más correcto hablar de gastroenterolesividad en lo que a los AINE se refiere, ya que no sólo ocasionan lesiones gastroduodenales sino también en el intestino y el colon.
Gastroprotección es el conjunto de medidas encaminadas a evitar o prevenir la aparición de efectos adversos gastrointestinales. Estas medidas son muy importantes cuando se vayan a utilizar estos fármacos.
La prevención farmacológica supone el enfoque más razonable actualmente. Esta será primaria, cuando el paciente no tenga antecedentes digestivos, o secundaria, cuando los tenga.
MECANISMOS DE ACCIÓN DE LOS AINE
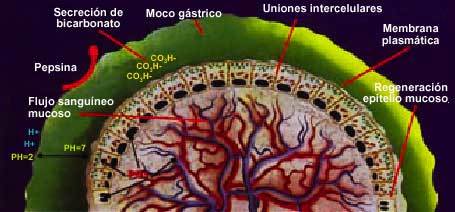
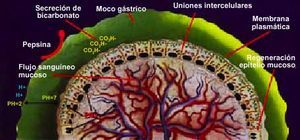
La barrera mucosa gástrica mantiene su integridad anátomo-funcional a pesar de la existencia de factores citoprotectores: el moco y bicarbonato (CO3H-) gástricos, los fosfolípidos de membrana, la regeneración celular y el flujo sanguíneo mucoso (fig. 1).
Fig. 1. Barrera mucosa gástrica
Las prostaglandinas (Pgs) intervienen de manera específica en los procesos inflamatorios como mediadores biológicos, a la vez que ejercen, entre otras, actividades biológicas en la zona gastrointestinal que van a permitir la citoprotección.
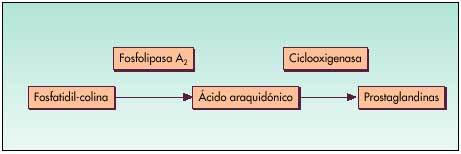
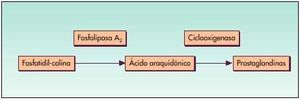
El principal mecanismo de acción (fig. 2) de los AINE es la inhibición competitiva y reversible de la enzima ciclooxigenasa (COX), encargada de la síntesis de Pgs, que cataboliza el paso del ácido araquidónico de las membranas celulares a endoperóxidos cíclicos (Pgs y tromboxanos).
Fig. 2. Acción de los AINE
De esta manera, los AINE no sólo inhiben la acción proinflamatoria de las Pgs (efecto farmacológico buscado), sino que alteran de forma importante la citoprotección gastrointestinal mediada por las Pgs y dan lugar a la aparición de reacciones adversas en el tubo digestivo.
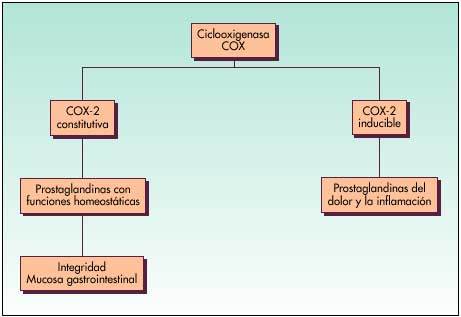
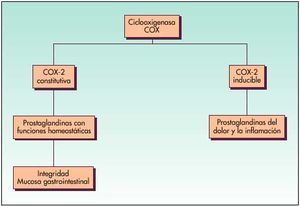
Existen, a su vez, dos isoenzimas de ciclooxigenasa: la COX-1 o constitutiva y la COX-2 o inducida. La primera va a mediar en la síntesis de las Pgs que intervienen en funciones fisiológicas; la segunda, en la síntesis de las Pg proinflamatorias (fig. 3).
Fig. 3. Isoenzimas ciclooxigenasa
Un AINE será tanto más gastrolesivo cuanto más inhiba la COX-1; por tanto, el índice COX-2/COX-1 será más alto. Por contra, un AINE será mejor tolerado a nivel gastrointestinal cuanto menos inhiba la COX-1, con lo que su índice COX-2/COX-1 será más bajo.
La investigación farmacológica actual sobre los AINE se centra precisamente en conseguir fármacos con un índice COX-2/COX-1 cada vez más bajo para evitar todo lo posible sus reacciones adversas gastrointestinales, aunque ello suele conllevar también un efecto antiinflamatorio menor.
EFECTOS SECUNDARIOS GASTROINTESTINALES
Los AINE suponen el 4% de todas las prescripciones farmacéuticas. La FDA americana ha documentado que son responsables del 20 al 25% de todas las reacciones adversas a drogas que se comunican espontáneamente. Una cuarta parte de esas reacciones adversas corresponden a efectos gastrointestinales. Como consecuencia, un 10% de los pacientes tiene que suspender el consumo de fármaco.
Roth introdujo en 1986 la denominación de gastropatía por AINE para referirse a las lesiones del tracto gastrointestinal superior relacionadas con el tratamiento con AINE. Este término se ha quedado corto y debe hablarse de gastroduodenopatía o, mejor aún, gastroenteropatía por AINE.
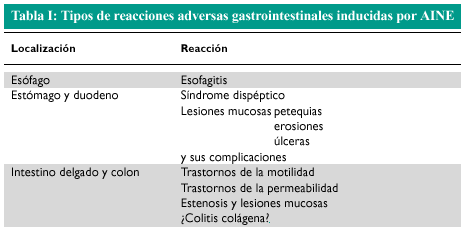
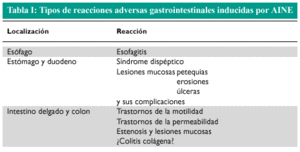
En la tabla I se enumeran los diferentes tipos de reacciones adversas gastrointestinales inducidas por los AINE.
Cada vez se están detectando más efectos adversos por estos fármacos. Algunos son tan suficientemente importantes y frecuentes que han motivado su retirada (p. ej., droxicam). Ningún AINE es completamente seguro.
MECANISMOS GASTROLESIVOS
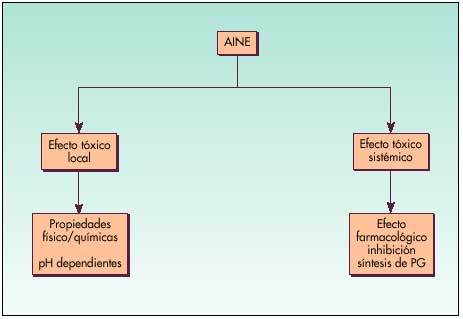
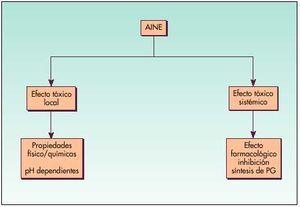
Los AINE pueden alterar los factores defensivos de la mucosa por un doble mecanismo (fig. 4):
Fig. 4. Mecanismos gastrolesivos de los AINE
Efecto tóxico local, ácido-dependiente:
i) Atrapamiento iónico: los AINE y el AAS son ácidos orgánicos débiles, que en medio ácido (pH gástrico) permanecen no ionizados y son liposolubles, por lo que atraviesan con facilidad la capa de moco y las células epiteliales y quedan atrapados intracelularmente. Ello produce un aumento de la permeabilidad de la membrana celular que permite la retrodifusión de H+, con el consiguiente daño celular.
ii) Inhiben la secreción de bicarbonato, disminuyen la secreción de moco y alteran su composición.
iii) Efecto vásculo-lesivo y, en algunos casos (p. e. indometacina) produce una inhibición sobre el flujo sanguíneo mucoso.
iiii) Efecto sobre la regeneración celular: disminución del índice de mitosis y de la síntesis de ADN en los bordes de las úlceras inducidas por los AINE, con lo que los mecanismos de reparación son defectuosos.
Efecto tóxico sistémico: inhibición de la síntesis de Pgs.
La administración parenteral o rectal de AINE también se asocia con la aparición de lesiones en la mucosa gastrointestinal. Ello es debido a la inhibición de la síntesis de Pgs que conlleva igualmente una disminución de la secreción de moco y CO3H-, del flujo vascular mucoso y de la regeneración celular.
Otros factores patogénicos: papel de los neutrófilos.
Experimentalmente se ha observado en ratas neutropénicas que las lesiones gástricas inducidas por AINE son menores que en ratas normales. Del mismo modo, el empleo de anticuerpos monoclonales contra receptores de membrana del neutrófilo también inhibe la aparición de estas lesiones. Por tanto, parece que los neutrófilos contribuyen patogénicamente a través del papel que desempeñan en los mecanismos inflamatorios.
FACTORES DE RIESGO
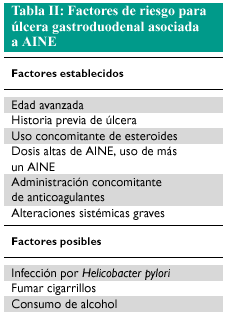
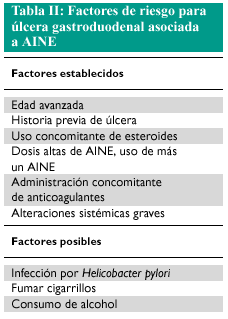
Se han señalado diversos factores de riesgo (tabla II) para el desarrollo de complicaciones en pacientes que utilizan AINE, pero sólo unos pocos tienen el consenso general al estar basados en estudios epidemiológicos amplios. Así, la existencia de una historia ulcerosa o complicación ulcerosa previa es el factor que más riesgo confiere. Casi la mitad de los pacientes que han tenido una úlcera péptica tendrán una recidiva con el uso de AINE en un período no superior a los 6 meses. El otro factor de amplio consenso es la edad. La barrera se ha situado en los 60 años, pero el riesgo está claramente aumentado a partir de los 70, donde el riesgo se multiplica por 4. Desde el punto de vista del paciente, sólo en estas circunstancias debe de efectuarse profilaxis.
Existen otros riesgos ampliamente aceptados que exigen profilaxis y que son inherentes a los fármacos utilizados. La utilización de dosis elevadas o combinadas de AINE y la coadministración de corticoides y anticoagulantes incrementan el riesgo y exigen prevención.
MANIFESTACIONES CLÍNICAS
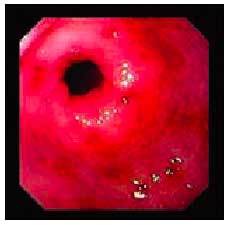
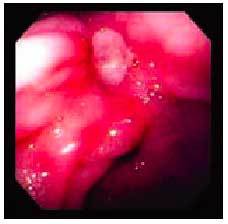
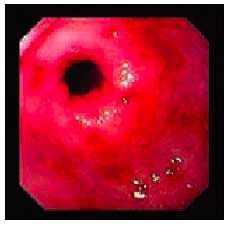
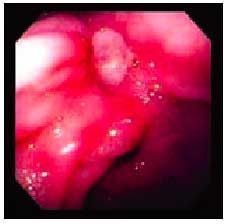
En cuanto a las manifestaciones clínicas de la gastropatía por AINE, entre un 20 y un 30% de los pacientes que toman AINE desarrollan síntomas persistentes. De éstos, un 20% no presenta lesiones, un 50% tiene lesiones de poca significación clínica (fig. 5) y el 30% restante suele presentar úlceras evidentes (fig. 6).
Fig. 5. Lesiones endoscópicas
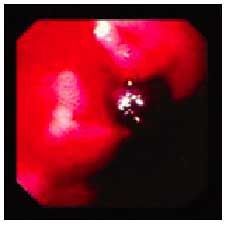
Fig. 6. Lesiones endoscópicas por AINE: úlcera gástrica
Entre un 75-80% de los individuos que consumen AINE son asintomáticos. El 50% de éstos no presenta lesiones endoscópicas y otro 45% sólo tiene lesiones superficiales; el 5% restante presenta lesiones potencialmente peligrosas. Por tanto, el riesgo de complicaciones reales en este grupo es pequeño pero no previsible.
Una anemia ferropénica por hemorragia digestiva crónica puede ser la primera manifestación de las reacciones adversas gastrointestinales inducidas por AINE y un 30% de los pacientes reumáticos que son remitidos para valoración endoscópica lo son por este motivo.
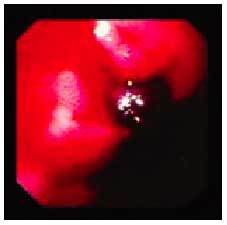
La incidencia de hemorragia digestiva se ha estimado en 1/6.000-10.000 prescripciones de AINE. Entre un 18 y un 45% de las hemorragias digestivas agudas se asocian con la ingesta de AINE (fig. 7). La mitad de ellas no presentan síntomas digestivos previos.
Fig. 7. Lesiones endoscópicas por AINE: úlcera duodenal sangrante
La aparición de hemorragia digestiva se asocia con una edad mayor de 65 años, dosis altas de AINE y las 4 primeras prescripciones.
Un 44% de las perforaciones de origen ulceroso se relaciona con la ingesta de AINE y tienen mal pronóstico: 12-24% de mortalidad y una alta morbilidad postoperatoria (33%).
Un 24% de las muertes por ulcus péptico se asocia a la toma de AINE, dos terceras partes como consecuencia de hemorragia digestiva. Las mujeres mayores de 75 años son el grupo de mayor riesgo. Hasta un tercio de los fallecimientos tiene lugar de forma súbita en casa, sin diagnóstico previo.
TRATAMIENTO Y PREVENCIÓN DE LAS LESIONES
Los fármacos actualmente disponibles para el tratamiento de estas lesiones gastrointestinales por AINE son:
Antagonistas H2: ranitidina, famotidina.
Inhibidores de la bomba de protones: omeprazol (fármaco de referencia).
Citoprotectores: acexamato de cinc, dosmalfato, análogos de las Pgs (misoprostol).
Todos ellos son eficaces (según las dosis a que se utilicen) en la curación de las lesiones gástricas y duodenales, aunque existen diferencias significativas en la curación cuando se sigue consumiendo el AINE. El objetivo del tratamiento y la prevención deben ser las úlceras, ya que son las que se asocian con la aparición de complicaciones serias.
Tratamiento de las lesiones
En los pacientes que suspenden el uso del antiinflamatorio, en muchos casos se produce la curación espontánea de la lesión.
El problema se plantea en los pacientes que precisan seguir tomando el AINE. En los últimos 4 años, en este sentido se han llevado a cabo varios ensayos clínicos, controlados, aleatorios y multinacionales, englobando a gran cantidad de pacientes, tanto en cicatrización como en profilaxis de lesiones por AINE, que se han agrupado en dos ensayos fundamentales: ASTRONAUT (Acid Supression Trials: Ranitidine versus Omeprazole as NSAIDAssociated Ulcer Management) y OMNIUM (Omeprazole versus Misoprostol for NSAID Induced Ulcer Management).
En el primero de ellos se incluyeron 541 pacientes que recibían AINE de forma continua y que habían desarrollado una gastroenteropatía en forma de úlcera (gástrica o duodenal) o un número significativo de erosiones comprobadas por endoscopia.
Los pacientes se dividieron de forma aleatoria en tres grupos y recibieron ranitidina 150 mg/12 h al día y omeoprazol 20 y 40 mg/día, respectivamente durante 4-8 semanas.
El estudio concluía que 20 mg de omeprazol una vez al día es un tratamiento eficaz (80% de cicatrizaciones a las 8 semanas) para las úlceras/erosiones gástricas/duodenales asociadas a los AINE. El uso de dosis mayores (40 mg de omeprazol) o la ranitidina no se asociaban con mejores resultados de tratamiento.
En el estudio OMNIUM se incluyeron 935 pacientes que estaban recibiendo de forma continua algún AINE y que habían desarrollado una gastroenteropatía.
Los pacientes también se dividieron de forma aleatoria en tres grupos, recibiendo misoprostol 200 (gramos/6h, 20 y 40 mg de omeprazol al día, respectivamente, durante 4-8 semanas.
De forma similar al anterior, los resultados eran superiores en el grupo tratado con 20 mg de omeprazol (76% de cicatrizaciones a las 8 semanas). Dosis mayores de omeprazol (40 mg) o misoprostol no producían mejores resultados. Aparte, como ya se había comprobado en otros ensayos, misoprostol a la dosis utilizada era mal tolerado por los frecuentes (>=30%) efectos secundarios en forma de calambres abdominales y diarrea.
Una vez cicatrizada la úlcera es necesario realizar un tratamiento antiulceroso de mantenimiento, si continúa la toma de AINE. Parece razonable seguir utilizando el omeprazol.
A la luz de los resultados de estos dos grandes ensayos clínicos, parece razonable el uso de omeprazol 20 mg/día durante unas 8 semanas para garantizar la correcta cicatrización de las lesiones.
Si el paciente tiene una ulcera gástrica o duodenal activa y necesita seguir en tratamiento con AINE es recomendable, en primer lugar, intentar la curación de la úlcera y, posteriormente, elegir el AINE menos gastrolesivo, de vida media más corta y en la menor dosis eficaz.
Profilaxis de las lesiones
El objetivo de la prevención es evitar la aparición de úlceras y, lo que es más importante, prevenir la aparición de complicaciones ulcerosas.
Hasta fechas recientes, sólo ranitidina y misoprostol habían sido evaluados en estudios controlados, aleatorios y doble ciegos en tratamientos preventivos. En todos ellos, los pacientes incluidos no presentaban lesiones gastroduodenales y no tenían antecedentes de ulcus péptico (prevención primaria).
Los estudios demuestran que ranitidina sólo es eficaz en la prevención de las úlceras duodenales. La incidencia de úlceras gástricas era similar en el grupo ranitidina y placebo.
Los estudios con misoprostol han demostrado su eficacia en la prevención de las lesiones gástricas y duodenales en tratamientos de 12 semanas y a dosis de 200 µg 4 veces al día al reducir las complicaciones ulcerosas de los AINE en aproximadamente el 40%. Sin embargo, la aparición de efectos secundarios, especialmente diarrea, limita la calidad de vida del paciente de forma importante, hasta el extremo de obligar a suspenderlo. Estos efectos adversos pueden disminuir iniciando el tratamiento con dosis menores. Dosis menores (200 (µg dos veces al día) no parecen tener un efecto claramente preventivo de las lesiones ulcerosas.
Los referidos estudios ASTRONAUT y OMNIUM, en profilaxis de lesiones inducidas por AINE, incluyeron a 432 y 732 pacientes, respectivamente, que recibían AINE de forma continua, pero que no habían desarrollado úlcera gastroduodenal ni un número significativo de erosiones y no tenían síntomas dispépticos o eran leves.
En el estudio ASTRONAUT se administró tratamiento de mantenimiento con ranitidina (150 mg/12 h) u omeprazol (20 mg/día) según los grupos, de forma controlada y aleatoria. En el segundo estudio, los pacientes se dividieron en tres grupos que recibieron 20 mg/día de omeprazol, 200 µg de misoprostol l/12 h o placebo. Los pacientes salieron del estudio cuando fracasó el tratamiento, definido como la aparición de úlcera gástrica o duodenal, más de 10 erosiones en estómago/duodeno, aparición de síntomas dispépticos moderados/graves o cuando hubo de interrumpirse el tratamiento por la aparición de efectos adversos.
Los resultados del estudio ASTRONAUT indican que omeprazol, a dosis de 20 mg/día, es superior a ranitidina 150 mg/12 h en la profilaxis de úlceras gastroduodenales, erosiones y síntomas dispépticos en consumidores de AINE. A los 6 meses del estudio el 94 y el 80% de los pacientes tratados con omeprazol y ranitidina, respectivamente, estaban sin úlceras.
Los resultados fueron superpuestos en el estudio OMNIUM. Los porcentajes de pacientes sin lesiones a los 6 meses fueron 70, 59 y 34% en los grupos tratados con omeprazol, misoprostol y placebo, respectivamente.
Los estudios con ranitidina son inequívocos al señalar que la dosis de 300 mg/día no es mejor que placebo en la prevención primaria y secundaria de úlcera gástrica y sí lo es para reducir la tasa de úlcera duodenal.
Famotidina, a dosis de 40 mg/día es sólo efectiva en profilaxis para úlcera duodenal.
Acexamato de cinc, a dosis de 300 mg/día es efectivo en la prevención primaria de la úlcera gástrica y duodenal.
Ni los alcalinos ni el sucralfato han demostrado eficacia en la prevención de lesiones ulcerosas inducidas por AINE.
INDICACIONES DE PROFILAXIS
La prevención no parece razonable de forma generalizada. Es recomendable tan sólo en pacientes con factores de riesgo:
Mayores de 65 años.
Historia de úlcera péptica o hemorragia digestiva alta.
Utilización conjunta con corticoides o anticoagulantes.
Con artritis reumatoide.
Uso de AINE a dosis altas.
Pacientes con enfermedad grave concomitante.
Medidas generales para reducir el riesgo
Algunas medidas generales para reducir el riesgo de desarrollar gastroenteropatía por AINE son las siguientes:
Elegir el AINE con menor potencial lesivo (ver tabla II).
Emplear las dosis mínimas necesarias.
Utilizar el AINE sólo el tiempo necesario.
Cambiar a un inhibidor específico de la COX-2 (ver más adelante) en el paciente de alto riesgo.
Evitar asociaciones de AINE y no asociarlos con corticoides.
No prescribir AINE en los grupos de riesgo antes mencionados.
Control clínico periódico durante tratamientos prolongados (grupos de riesgo). Ante la aparición de dispepsia interrumpir el tratamiento.
Realizar endoscopia previa al tratamiento con AINE si hay antecedentes digestivos.
NUEVOS AINE ESPECÍFICOS (COX-2 SELECTIVOS)
Pensando en la seguridad gastrointestinal de los AINE se han desarrollado preparados con diferente selectividad para la ciclooxigenasa, partiendo de la premisa de que si la COX-2 sólo aparece en los lugares de inflamación, los AINE que únicamente inhiban ésta deberán respetar el tracto gastrointestinal, cuya isoenzima responsable del mantenimiento de la barrera mucosa, la COX-1, no se inhibe.
En la tabla III aparecen los tipos de AINE según su selectividad para la ciclooxigenasa.
Los nuevos AINE COX-2 selectivos son rofecoxib y celecoxib. Para evaluar la seguridad gastrointestinal de ambos frente a otros AINE «convencionales» no selectivos se han llevado a cabo varios ensayos clínicos, entre los que destacan dos: el estudio VIGOR y el CLASS, con rofecoxib y celecoxib, respectivamente.
En el estudio VIGOR, realizado con un total de 8.076 pacientes, se comparaba la toxicidad gastrointestinal de rofecoxib (dosis de 50 mg diarios) y naproxeno (dosis de 500 mg, dos veces al día) en pacientes con artritis reumatoide. Las conclusiones fueron que en los pacientes con artritis reumatoide tratados con rofecoxib se produce un número significativamente menor de efectos secundarios gastrointestinales clínicamente importantes (perforación, obstrucción y hemorragia digestiva alta) en comparación con los pacientes tratados con naproxeno.
De otro lado, en el estudio CLASS, se comparaba la toxicidad gastrointestinal de celecoxib (400 mg, dos veces al día) con la de ibuprofeno (800 mg, tres veces al día) y la de diclofenaco (75 mg, dos veces al día). El estudio incluyó a un total de 8.059 pacientes con osteoartritis o artritis reumatoide, asignados aleatoriamente en tres grupos para recibir celecoxib, ibuprofeno o diclofenaco. El estudio concluía que celecoxib a dosis más altas que las indicadas clínicamente (dos y cuatro veces las dosis máximas para la artritis reumatoide y la osteoartritis, respectivamente), y comparado con los otros dos AINE a dosis estándar, se asociaba con una menor incidencia de úlceras sintomáticas y de complicaciones ulcerosas, así como de otros efectos tóxicos clínicamente importantes.
Desde el punto de vista del coste sanitario de las complicaciones gastrointestinales severas por ingesta de AINE, el uso de los nuevos AINE selectivos (con su mejor perfil de seguridad gastrointestinal) podría contribuir a disminuir el gasto sanitario derivado del manejo de las complicaciones gastrointestinales severas ocasionadas por los AINE clásicos.
BIBLIOGRAFÍA GENERAL
Bombardier C, Laine L, Reicin A, Shapiro D, Burgos-Vargas R, Davis B, et al. Comparison of upper gastrointestinal toxicity of rofecoxib and naproxen in patients with rheumatoid arthritis. VIGOR Study Group. N Engl J Med 2000;343(21):1520-8.
Ekstrom P, Carling L, Wetterhus S, Wingren PE, Anker-Hansen O, Lundegardh G, et al. Prevention of peptic ulcer and dyspeptic symptoms with omeprazole in patients receiving continuous non-steroidal anti-inflammatory drug therapy. A Nordic multicentre study. Scand J Gastroenterol 1996;31(8):753-8.
Hawkey CJ, Karrasch JA, Szczepanski L, Walker DG, Barkun A, Swannell AJ, et al. Omeprazole compared with misoprostol for ulcers associated with nonsteroidal antiinflammatory drugs. Omeprazole versus Misoprostol for NSAID-induced Ulcer Management (OMNIUM) Study Group. N Engl J Med 1998;338(11): 727-34.
Silverstein FE, Faich G, Goldstein JL, Simon LS, Pincus T, Whelton A, Makuch R, et al. Gastrointestinal toxicity with celecoxib vs nonsteroidal anti-inflammatory drugs for osteoarthritis and rheumatoid arthritis: the CLASS study: A randomized controlled trial. Celecoxib Long-term Arthritis Safety Study. JAMA 2000;284(10):1247-55.
Silverstein FE, Graham DY, Senior JR, Davies HW, Struthers BJ, Bittman RM, et al. Misoprostol reduces serious gastrointestinal complications in patients with rheumatoid arthritis receiving nonsteroidal anti-inflammatory drugs. A randomized, double-blind, placebo-controlled trial. Ann Intern Med 1995;123(4): 241-9.
Vargas E, Cabrera L, Morón A, García M, Soto J y Rejas J. Complicaciones gastrointestinales severas potencialmente relacionadas con el consumo de antiinflamatorios no esteroideos: coste del tratamiento hospitalario para el Sistema Nacional de Salud en nuestro país. An Med Interna 2001;18(11):564-8.
Wallace JL. Nonsteroidal anti-inflammatory drugs and gastroenteropathy: the second hundred years. Gastroenterology 1997;112(3):1000-16.
Yeomans ND, Tulassay Z, Juhasz L, Racz I, Howard JM, van Rensburg CJ, et al. A comparison of omeprazole with ranitidine for ulcers associated with nonsteroidal antiinflammatory drugs. Acid Suppression Trial: Ranitidine versus Omeprazole for NSAID-associated Ulcer Treatment (ASTRONAUT) Study Group. N Engl J Med 1998;338(11):719-26.