En este trabajo se revisa el concepto de estudio de utilización de medicamentos, analizando sus posibles objetivos y utilidades, tipologías y distintas metodologías de elaboración.
La OMS define los estudios de utilización de medicamentos (EUM) como «estudios sobre comercialización, distribución, prescripción y uso de los medicamentos en la sociedad, con acento especial sobre las consecuencias médicas, sociales y económicas»1.
LA ELECCIÓN DE UN TRATAMIENTO
Muchas intervenciones tanto preventivas como curativas en el medio sanitario incluyen la utilización de un fármaco como mecanismo intermedio para obtener un objetivo de salud concreto2. Tanto la elevada frecuencia de utilización de recursos farmacológicos como su extensión entre la población justifican la importancia que el medicamento tiene en los valores culturales y sociales de nuestro entorno. Si bien la prescripción farmacológica es una decisión médica, otros factores como son el paciente, el farmacéutico, la industria farmacéutica y el sistema sanitario influyen en los hábitos de prescripción y, por lo tanto, condicionan la forma de resolver los problemas de salud3.
Los profesionales de la salud deben garantizar que los pacientes recibirán el medicamento adecuado en la dosis correcta, durante el tiempo necesario y con el mínimo coste posible, y para ello han de tener un profundo conocimiento de la terapéutica y tener en cuenta los aspectos de rentabilidad social y económica en la aplicación de los mismos. Los aspectos socioeconómicos son consecuencia de la limitación de los recursos disponibles. Los tratamientos, además de perseguir la prevención, el alivio de la enfermedad o la restauración de la salud tendrían que devolver al individuo a su vida activa, cuanto antes y en las mejores condiciones viables. Por ello en la elección del tratamiento debe también valorarse el coste social que implican las alternativas posibles4.
OBJETIVOS DE LOS EUM
Aunque el objetivo último de los EUM es mejorar la prescripción farmacéutica, que ha adquirido mayor importancia con la aparición de nuevos agentes potentes y costosos, se pueden distinguir varios objetivos intermedios1:
Descripción cuantitativa de la utilización de los medicamentos.
Valoración cualitativa de los datos obtenidos para identificar posibles problemas.
Intervención sobre los problemas identificados.
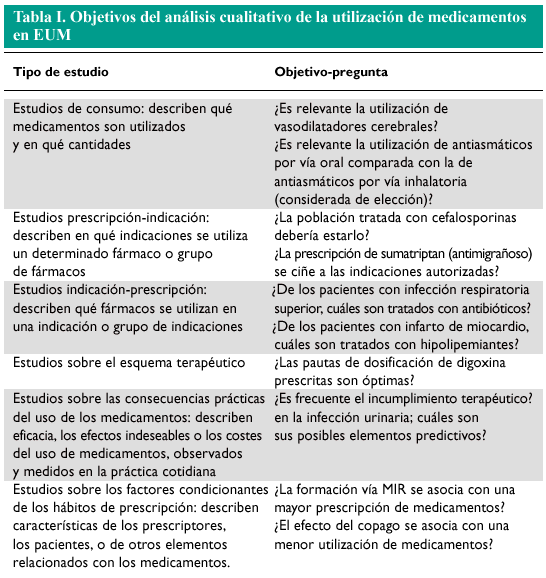
En la valoración cualitativa se compara la utilización de medicamentos observada con unos «patrones de referencia» o «estándares», que se suelen basar en las evidencias publicadas en la literatura médica (resultados de ensayos clínicos controlados, revisiones bibliográficas, protocolos, etc.). Los indicadores son los parámetros que miden las diferencias entre la utilización de medicamentos observada y el «patrón de referencia»1,5. Este tipo de valoración trata de identificar problemas que, en caso de ser modificados, pueden mejorar los beneficios terapéuticos obtenidos o bien disminuir los efectos adversos producidos o los costes del tratamiento (tabla I).
CLASIFICACIÓN DE LOS EUM
Teniendo en cuenta la amplia definición de EUM, éstos se pueden agrupar en tres tipologías: estudios sobre la oferta, estudios sobre la prescripción y estudios sobre el uso de medicamentos.
Estudios sobre la oferta
Estos estudios proporcionan una descripción cuantitativa y cualitativa de la oferta de medicamentos. Los elementos que se estudian desde el punto de vista cuantitativo son el número de principios activos ofertados, el número de especialidades6, de presentaciones7, de asociaciones de fármacos presentes en el mercado farmacéutico y, desde el punto de vista cualitativo, la calidad farmacológica de las especialidades ofertadas.
También se pueden incluir aquellos trabajos que estudian la información que sobre los medicamentos reciben tanto los facultativos2,8 (bien sea en el prospecto, a través de la visita médica, de las revistas científicas o de los catálogos elaborados por los laboratorios farmacéuticos, etc.) como los pacientes o posibles pacientes en la prensa y medios de comunicación.
Estudios sobre la prescripción
Aquí se incluyen aquellos estudios relativos a los factores que influyen sobre la prescripción9,10 como, por ejemplo, la formación del facultativo, las características de la población o del sistema sanitario y aquellos otros que estudian la calidad de la misma11, centrados en la prescripción de fármacos de primera elección, de baja utilidad terapéutica, etc.
Dentro de este grupo también se pueden incluir los estudios sobre el cumplimiento de la prescripción12 y el impacto de un programa educativo dirigido a mejorar el cumplimiento de la terapia prescrita13.
Estudios sobre la utilización de medicamentos
Dentro de este grupo cabe hablar de estudios cuantitativos y cualitativos.
Estudios cuantitativos
Los estudios cuantitativos tienen como objetivo principal la descripción de qué medicamentos se consumen y en qué cantidad. En muchas ocasiones, constituyen el primer nivel de análisis acerca de la utilización de medicamentos. Permiten realizar un análisis de situación para establecer las bases de un estudio más amplio acerca de cómo se están utilizando y en quién5. También son útiles para calcular las tendencias temporales del uso de fármacos con determinadas variables (medidas reguladoras, información, etc.).
Estudios cualitativos
Facilitan el conocimiento del tipo de fármacos que se prescriben. También aportan información sobre la calidad de uso de los fármacos, para lo cual hay que utilizar indicadores adecuados. Ello conduce a la creación de un patrón de referencia óptimo, puesto que los indicadores deben ser un instrumento de medida que permita cuantificar una valoración de la prescripción, en principio cualitativa.
METODOLOGÍA
Para que los EUM sean útiles y puedan hacerse comparaciones entre países, regiones, áreas básicas de salud, etc., es necesario seguir una metodología común. Esta comprende:
Clasificación de los principios activos
Es necesaria una clasificación uniforme de las especialidades farmacéuticas, ampliamente aceptada y precisa, para sistematizar y comparar los datos obtenidos en los EUM1,2.
Clasificación de la EPhMRA
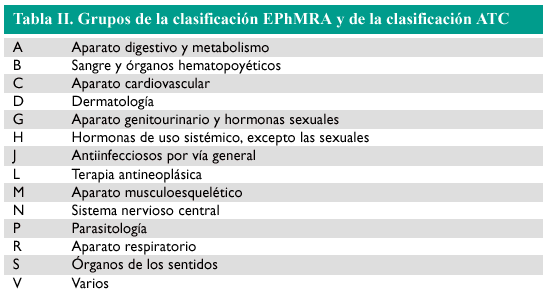
En la clasificación de la EPhMRA (European Pharmaceutical Market Research Association) las especialidades farmacéuticas se distribuyen en 14 grupos principales, designados por una letra (tabla II). Cada uno de estos grupos está dividido en un número variable de subgrupos, indicados con dos dígitos numéricos (01, 02, 03, etc). A su vez, cada subgrupo está subdividido en otros subgrupos, en un tercer nivel de división, que corresponde a subgrupos terapéuticos. Por ejemplo, para la cimetidina sería:
A: aparato digestivo y metabolismo (primer nivel, órgano o sistema).
A02: antiácidos, antiflatulentos, antiulcerosos (segundo nivel, grupo terapéutico principal).
A02B1: antihistamínicos (tercer nivel, subgrupo terapéutico).
Cuando la especialidad farmacéutica es una combinación a dosis fijas que contiene dos o más principios activos, se clasifican según su indicación principal. Así por ejemplo, un medicamento que contenga un analgésico y un ansiolítico indicado para el tratamiento del dolor se clasifica como analgésico. Esta clasificación presenta dos limitaciones principales: 1) los códigos no permiten la identificación de especialidades con un principio activo determinado; 2) dado que las combinaciones a dosis fijas se clasifican según la indicación principal de la especialidad, pueden contener un principio activo «oculto» que puede pasar inadvertido.
Clasificación anatómica-terapéutica-química (ATC)
Está basada en los mismos principios que la clasificación EPhMRA. Los tres primeros niveles de clasificación son comunes, pero la clasificación ATC incluye dos niveles adicionales; un cuarto nivel que corresponde al subgrupo químico-terapéutico y un quinto nivel que designa cada principio activo en particular. Se expone como ejemplo de la clasificación la codificación de la amoxicilina:
J: antiinfecciosos vía general (primer nivel).
J01: antibióticos sistémicos (segundo nivel).
J01C: penicilinas con efecto incrementado sobre bacilos gram- (tercer nivel).
J01CA: ampicilina y antibióticos similares.
J01CA04: amoxicilina.
Aunque la adición de estos dos niveles permite realizar EUM más detallados, presenta también alguna limitación. Así, un medicamento con distintas indicaciones sólo puede estar incluido en un grupo o subgrupo con un único código. La OMS recomienda aplicar la clasificación ATC1.
Los perfiles terapéuticos son una herramienta de gran utilidad en el análisis de las prescripciones que se realizan en un país, en una zona geográfica o por un médico o grupo de médicos. Si se dispone del consumo farmacéutico informatizado, pueden representarse de una manera sencilla los perfiles de prescripción a nivel de grupos terapéuticos o de subgrupos, con tal de que se utilicen para ello parámetros de medida comparativos14.
Los perfiles por grupos terapéuticos tienen el inconveniente de su escasa sensibilidad para detectar un uso no racional de los medicamentos, ya que dentro de un mismo grupo terapéutico existen diferentes subgrupos de muy diferente valor terapéutico. Por ejemplo, dentro del grupo C (aparato cardiovascular), hay subgrupos de menor utilidad como los vasodilatadores periféricos y los venotónicos, junto con otros de reconocida eficacia como los antihipertensivos o la terapia del miocardio. Pueden tener cierta utilidad en comparaciones muy generales, como puede ser el caso de diferencias entre países.
Los perfiles por subgrupos terapéuticos presentan sensibilidad para detectar utilizaciones inadecuadas superior a la de los grupos, ya que permiten obtener perfiles de los medicamentos más prescritos o bien de aquellos que sea de interés estudiar a la hora de plantearse las actuaciones que pretenden implantarse en una zona.
Parámetros de medida (indicadores) para la valoración cuantitativa
La cuantificación del consumo de medicamentos puede ser abordada desde distintos enfoques, que dependen fundamentalmente de las aplicaciones del análisis que se realiza2. Con el fin de poder realizar comparaciones en el consumo de medicamentos es necesario que existan unos parámetros de medida que sean aceptados y utilizados por todos los que van a realizar EUM4.
Existen numerosas formas de expresar los resultados de un estudio cuantitativo de consumo como el número de envases dispensados, el valor económico, las unidades físicas consumidas (g, mg, ml) etc. Pero en la mayoría de los casos el empleo de estas unidades de medida tiene poco valor epidemiológico y limita mucho la posibilidad de comparación. Los indicadores cuantitativos más habituales son, en cualquier caso, los siguientes:
Indicadores económicos globales
La medida del gasto económico en medicamentos ha sido utilizada desde hace tiempo, sobre todo por los sistemas públicos de atención a la salud, como indicador para la elaboración de presupuestos y la contención del gasto2. En una primera etapa se utilizaron indicadores globales, tales como15:
Número de recetas dispensadas.
Importe a precio de venta al público (PVP).
Gasto (= PVP aportación del asegurado).
Estos datos se desglosan en los correspondientes a los contingentes que integran la prestación farmacéutica. Por una parte, figuran los relativos a activos y pensionistas. Por otra, las cuantías de los diferentes bloques de productos que componen la prestación: especialidades farmacéuticas, fórmulas magistrales y efectos y accesorios (productos sanitarios).
Indicadores económicos relativos
La utilización del gasto como unidad de medida de consumo puede llevar a conclusiones equívocas5, debido a la inflación y a la variabilidad existente entre los distintos países (moneda, PIB y nivel de vida).
Al no estar referidos a población, estos indicadores globales resultan poco útiles para hacer comparaciones, por lo que se introdujeron los siguientes indicadores15:
a) Importe en PVP/habitante o asegurado.
b) Gasto/habitante o asegurado.
c) Recetas/habitante o asegurado.
d) RAP, que es un cociente entre el número de recetas por cada persona activa y el número de recetas por cada pensionista, siendo tanto más desfavorable cuanto más se aleja, por debajo, del valor 0,5-0,3, que es el considerado normal en países como Reino Unido y Estados Unidos.
Gracias a estos indicadores se pueden detectar diferencias interprovinciales e incluso dentro de una misma provincia, diferencias entre centros sanitarios en los que el consumo se encuentra por encima de la media y por tanto, serían más susceptibles de realizar un esfuerzo mayor en la contención del gasto farmacéutico, etc. Asimismo, estos indicadores se calculan para los colectivos que integran la prestación, activos y pensionistas, y permiten observar que existe un comportamiento diferenciado entre ambos grupos al experimentar crecimiento año a año en el de los pensionistas.
Envases
La utilización del envase como unidad de medida tiene el inconveniente de que no todas las especialidades farmacéuticas que contienen el mismo principio activo presentan la misma dosificación ni el mismo número de formas farmacéuticas o unidades por envase. Así, una caja de 10 grageas de 5 mg de un determinado fármaco se contabiliza como una unidad, al igual que una caja de 50 grageas de 10 mg. En consecuencia, si se expresa el consumo total de unidades, el resultado sería una suma de elementos de magnitudes distintas2. Esta unidad sólo servirá para comparar, de forma aproximada, pautas de utilización de un subgrupo terapéutico dentro de un país.
Otro problema que presenta este método de cuantificación es que el contenido ponderal de una misma especialidad puede variar en un mismo país a lo largo del tiempo, o puede variar también de un país a otro, por lo que las variaciones en el número de unidades vendidas pueden no reflejar variaciones reales del consumo.
Dosis Diaria Definida
Para los problemas referidos se necesitaba una unidad de medida que permitiese hacer comparaciones entre diferentes zonas geográficas y entre períodos de tiempo distintos independientemente de variaciones en la composición de unidades y el precio de las especialidades farmacéuticas. Así, la OMS propuso una unidad técnica internacional de medida del consumo de medicamentos denominada Dosis Diaria Definida (DDD), que es independiente de las variaciones en el precio y en el contenido ponderal de las especialidades farmacéuticas del medicamento. La DDD se define como «la dosis media diaria de mantenimiento de un medicamento, en adultos, cuando se usa rutinariamente en su principal indicación».
Esta DDD debe tomarse únicamente como una unidad técnica de medida y comparación. Nunca reflejan, por definición, la dosis terapéutica recomendada. Estas DDD se establecen de forma arbitraria según las recomendaciones de las publicaciones científicas, de los laboratorios fabricantes y según la experiencia acumulada.
Las directrices para establecer la DDD son las siguientes2:
En general, la DDD se expresará en forma de peso de sustancia activa.
La DDD se basa en el uso en adultos, excepto para ciertos fármacos utilizados exclusivamente en niños.
Cuando la dosis inicial del fármaco administrado es distinta de la dosis de mantenimiento, la DDD corresponde a esta última.
En fármacos administrados para profilaxis y para tratamiento, la DDD se refiere a la dosis de tratamiento; sin embargo, si la administración profiláctica es la principal indicación del medicamento, la DDD corresponde a esta última.
Para fármacos administrados en dosis distintas según la vía de administración, se establecen distintas DDD: una para cada vía.
En la tabla III se muestran algunas aplicaciones de esta unidad de medida en el estudio cuantitativo del consumo de medicamentos. La DDD tampoco está exenta de limitaciones, que deben tenerse en cuenta cuando se interpreten los resultados1,2,4:
A veces un mismo principio activo tiene más de una indicación, con dosis diferentes para cada una.
No todos los fármacos prescritos o dispensados se consumen.
No equivale necesariamente a la dosis media prescrita.
No equivale necesariamente a la dosis media ingerida, por la diferente biodisponiblidad de las formas farmacéuticas.
Es poco útil para reflejar el consumo de medicamentos cuando las combinaciones a dosis fijas de dos o más principios activos constituyen una parte importante del mercado.
En el caso de medicamentos en asociación, la unidad de medida será la Dosis Diaria de Asociación (DDA), que se define como el número diario de cápsulas, comprimidos o unidades de volumen4.
En general, el número de DDD consumidas en un área geográfica se expresa por 1.000 habitantes y por día (DDD/1000 habitantes/día o DHD). Este parámetro puede proporcionar una estimación del número de personas de cada 1.000 de la población estudiada que están recibiendo al día una DDD de un determinado medicamento o subgrupo terapéutico. La figura 1 muestra la fórmula que se emplea para el cálculo de la DHD e ilustra su utilidad mediante un ejemplo práctico.
Dosis Diaria Prescrita
La DDP es la dosis media prescrita de un fármaco determinado en su principal indicación. En general, los EUM se nutren de datos sobre ventas y es bien conocido que no todos los medicamentos prescritos son necesariamente consumidos. Como se ha señalado, la DDD como unidad de medida no es necesariamente equivalente a la dosis diaria prescrita ni a la dosis diaria ingerida. Aunque para algunos fármacos (antihipertensivos, antidiabéticos) la utilización de DDD o DDP no genera gran disparidad de resultados, para la mayoría de los demás grupos farmacológicos (analgésicos, psicofármacos) pueden existir diferencias importantes. En comparación con la DDD, la DDP permite una mejor estimación de la proporción de la población tratada; sin embargo, no es uniforme porque puede variar en las distintas zonas geográficas y dentro de una misma zona geográfica a lo largo del tiempo y, por tanto, perder utilidad en los estudios comparativos. Hay que tener en cuenta que son pocos los estudios en los que se evalúa directamente cuál es la dosis que toman realmente los pacientes, y estos trabajos suelen, además, tener unos costes muy elevados.
Coste Tratamiento Día
Otra de las aplicaciones de la DDD es el cálculo del CTD, que se define como el coste a PVP de la DDD de un determinado medicamento. Su utilización permite comparar el CTD de distintas especialidades que tienen la misma composición o comparar el CTD de especialidades con distinto principio activo pero que se utilizan para la misma indicación. La fórmula de cálculo del CTD aparece en la figura 2.
Índice de exposición
El índice de exposición se define como el número de impactos de unidades de dosificación (cápsulas, comprimidos, cucharadas de jarabe, inhalaciones, inyecciones, etc.) que recibe una persona en un año. Es una unidad intermedia entre las unidades vendidas por persona y las DHD15. Para hallarlo debemos conocer la población, las unidades vendidas y la media ponderada de unidades de dosificación por envase. Por ejemplo, un índice de exposición de 30 para antiasmáticos, en un año determinado, significaría que una persona tomaría 30 unidades de dosificación (cápsulas, inhalaciones, etc.) al año de medicamentos antiasmáticos.
Parámetros de medida (indicadores) para la valoración cualitativa
En la valoración cualitativa se compara la utilización de medicamentos observada con unos «patrones de referencia» o «estándares» (resultados de ensayos clínicos controlados, revisiones bibliográficas, etc.) mediante parámetros de medida o indicadores. Un análisis cualitativo ayudará a conocer los costes y riesgos excesivos relacionados con la utilización de medicamentos, como consecuencia del uso de alternativas con una relación beneficio/coste y beneficio/riesgo desfavorables, o bien los beneficios insuficientes por una inadecuada selección del fármaco en cuestión1,2,5.
El empleo de la DDD supone una serie de ventajas sobre los demás métodos de cuantificación del consumo. Sin embargo, la mera cuantificación del número de medicamentos prescritos, aun si se refiere a un denominador de población (DHD), tiene un papel limitado en la evaluación de la calidad de los medicamentos consumidos.
El principal problema de los estudios cualitativos radica en la dificultad de definir estándares o indicadores de calidad. Para poder evaluar desde la información proporcionada por los datos de consumo de medicamentos la calidad de la prescripción, se han diseñado unos «indicadores de la calidad de la prescripción» (ICP). Un ICP es un instrumento de medida que nos permite cuantificar una valoración, en principio cualitativa, de la prescripción.
Indicadores de utilidad terapéutica
La valoración de la eficiencia del uso de los medicamentos en un sistema sanitario puede realizarse a dos niveles: el valor intrínseco (VI) de las especialidades farmacéuticas consumidas y el modo en que éstas son utilizadas. El valor intrínseco de las especialidades se obtiene atendiendo a criterios farmacológicos de valoración basados en la literatura científica. Según este criterio las especialidades farmacéuticas se clasifican en aquellas de VI «elevado», VI «relativo», VI «dudoso» y VI «nulo» (tabla IV).
A partir de estos conceptos se pueden crear dos grupos de indicadores. El primer grupo es el de indicadores de utilidad terapéutica alta (UTA), que incluyen las especialidades de VI «elevado». Este tipo de indicadores cuantificaría la adhesión de la prescripción a unos criterios de selección científicos, es decir, la preferencia por aquellas alternativas terapéuticas con una relación beneficio/riesgo/coste más favorables.
El segundo grupo o indicadores de utilidad terapéutica baja (UTB) pretenden cuantificar el consumo de especialidades sin eficacia demostrada o de VI «relativo», «dudoso» o «nulo».
Indicadores de uso relativo
Otro tipo de indicadores de calidad son los de uso relativo. El uso relativo (UR) es el cociente entre las DHD de los medicamentos que guardan una relación o es interesante relacionar, y que se expresa4 según la fórmula de la figura 3.
Es útil fundamentalmente para comparar valores de años sucesivos o en los casos en que existe una relación determinada entre la incidencia de las patologías para las cuales se utilizan los medicamentos relacionados, es decir, permiten identificar desviaciones a lo largo del tiempo en la calidad del tratamiento farmacológico de una patología.
RECOGIDA DE DATOS
En los EUM, la fuente básica que proporciona la información del estudio suele ser la prescripción. Sin embargo, en algunos EUM la información básica se obtiene a partir de la historia clínica o registros especiales sobre la prescripción de fármacos (administración crónica). En algunos estudios es imprescindible obtener la información básica a partir de una entrevista con el paciente, el médico prescriptor u otros profesionales sanitarios relacionados con el uso de medicamentos. *