Objetivos generales
Dotar al farmacéutico de conocimientos suficientes para realizar una correcta selección de los complementos alimenticios que dispensa en su oficina de farmacia, atendiendo tanto a la legislación vigente al respecto como a la evidencia científica sobre sus indicaciones, contraindicaciones y propiedades.
Objetivos específicos
Al término de este curso, el alumno debería:
Conocer la normativa legal aplicable a la puesta en el mercado y comercialización de complementos alimenticios.
Conocer las características del etiquetado correcto de este tipo de productos.
Ser capaz de sospechar cuándo un supuesto producto alimenticio puede ser, en realidad, un producto milagro.
Apoyar con evidencia científica disponible la indicación de los complementos alimenticios analizados: minerales, ácidos grasos y vegetales de pescado, fibras y preparados para reducción de peso, vitaminas liposolubles e hidrosolubles y otros productos. Ser capaz de seleccionar los productos más adecuados para responder a las necesidades y solicitudes de los usuarios de la farmacia en este ámbito.
Conocer las contraindicaciones, los riesgos asociados al uso y pautas de administración de los complementos alimenticios analizados.
Metodología
El curso se articula en 6 temas, que se irán publicando en los 6 números de farmacia profesional que aparecerán en 2010, también en su versión electrónica en www.dfarmacia.com, a partir del 1 de marzo del 2010.
Evaluación
El período de evaluación se iniciará en el mes de marzo. Para realizar los test de autoevaluación de cada tema (diez preguntas con respuesta múltiple) es necesario registrarse y acceder a: www.dfarmacia.com. El alumno recibirá la calificación de apto o no apto de forma automática, tras la realización del test correspondiente a cada tema. Al final del curso se dará acceso a las respuestas correctas razonadas y el alumno apto podrá descargarse el diploma.
Sumario
Tema 1. Complementos alimenticios y otros alimentos en la farmacia: normativa legal y criterios de selección.
Tema 2. Minerales.
Tema 3. Ácidos grasos vegetales y de pescado.
Tema 4. Fibras y preparados para reducción de peso. Tema 5. Vitaminas hidrosolubles y liposolubles.
Tema 6. Otros productos (jalea real, ginseng, própolis, etc.).
Más información: a partir del 1 de marzo en www.dfarmacia.com.
Para esta actividad se ha solicitado acreditación al Consell Català de la Formació Farmacèutica Continuada. Comisión de Formación Continuada del SNS.
Curso básico
Dispensación de complementos alimenticios
JUAN DEL ARCO ORTIZ DE ZÁRATE
Doctor en Farmacia. Director Técnico del Colegio Oficial de Farmacéuticos de Bizkaia.
Tema 1
Complementos alimenticios y otros alimentos en la farmacia: normativa legal y criterios de selección
La dispensación de complementos alimenticios en la oficina de farmacia es un acto cada vez más frecuente, y suele tener en su origen la petición de los propios ciudadanos. Conocer el marco legal que los regula y disponer de unos criterios de selección rigurosos es el punto de partida ineludible de esta tarea.
Contexto
La farmacia es un establecimiento que se ha relacionado tradicionalmente con la alimentación, facilitando consejos nutricionales y preparados alimenticios para situaciones especiales. Así, por ejemplo, fueron estos establecimientos sanitarios los que iniciaron, a mediados del pasado siglo, la comercialización de las leches infantiles para sustituir lactancia materna cuando la madre no podía amamantar a su hijo1.
En los últimos años se está incrementando en las farmacias la presencia de preparados alimenticios destinados tanto a situaciones especiales como a complementar la alimentación de las personas sanas. Así, en el año 2009 los alimentos suponen el 10,04% de los productos de parafarmacia codificados por el Consejo General de Colegios Oficiales de Farmacéuticos, mientras que en 2006 eran sólo el 8,75%1,2. El grupo más numeroso lo constituyen los complementos alimenticios (de aquí en adelante CA) 1, que son también objeto de una mayor publicidad y en consecuencia están experimentando una creciente demanda.
Tradicionalmente en España los complejos vitamínicos y minerales se comercializaban como medicamentos y estaban, por tanto, sometidos a la estricta regulación que caracteriza estos productos. Sin embargo, hace ya varias décadas que comenzaron a comercializarse productos destinados a complementar la dieta con determinados nutrientes, fundamentalmente vitaminas y minerales, denominados «complementos alimenticios», «complementos nutricionales» o «complementos o suplementos dietéticos», no registrados como medicamentos y cuya puesta en el mercado no exige realizar los complicados trámites que conlleva la de estos últimos.
La mayoría de estos productos se asemejan mucho a los medicamentos, tanto en sus presentaciones (comprimidos, cápsulas...) y en el aspecto de sus envases, como en su composición e incluso a menudo en sus alegaciones publicitarias. Sin embargo, constituyen un grupo de artículos cuya regulación es muy diferente a la de aquéllos, tanto en lo que se refiere a su fabricación y puesta en el mercado, como a su promoción entre los potenciales consumidores.
Ahora bien, son pocos los farmacéuticos conscientes de esta situación y muchos los que piensan que las garantías de seguridad, eficacia y calidad que las autoridades sanitarias exigen a los medicamentos son también extensibles a éstos y otros productos de parafarmacia. Sin embargo, no es en absoluto así, y en este campo es el propio farmacéutico quien debe seleccionar cuidadosamente los productos que introduce en su farmacia, basándose en primer lugar en criterios profesionales, para impedir la entrada en su farmacia no sólo de los que incumplan la normativa vigente, sino de aquéllos que no tengan la calidad suficiente o se atribuyan propiedades basadas en afirmaciones carentes de rigor científico3.
Para poder hacer una selección adecuada es importante conocer la normativa aplicable y poseer una formación basada en la evidencia científica disponible sobre este tipo de productos. Éste es precisamente el propósito de este curso sobre CA que iniciamos con este primer capítulo dedicado a las normas legales y los criterios de selección.
Alimentos y complementos alimenticios
Desde el punto de vista legal, la mayor parte de los alimentos o productos relacionados con la nutrición que generalmente se encuentran en las oficinas de farmacia pertenecen a dos grupos:
Preparados alimenticios para regímenes dietéticos y/o especiales
En este grupo se encuadran:
Los productos alimenticios destinados a ser utilizados en dietas de bajo valor energético para reducción de peso.
Los preparados para lactantes y preparados de continuación.
Los alimentos elaborados a base de cereales y alimentos infantiles para lactantes y niños de corta edad.
Los alimentos destinados a personas que se encuentran en condiciones fisiológicas particulares o cuyos procesos de asimilación o de metabolismo se encuentran alterados.
Complementos alimenticios
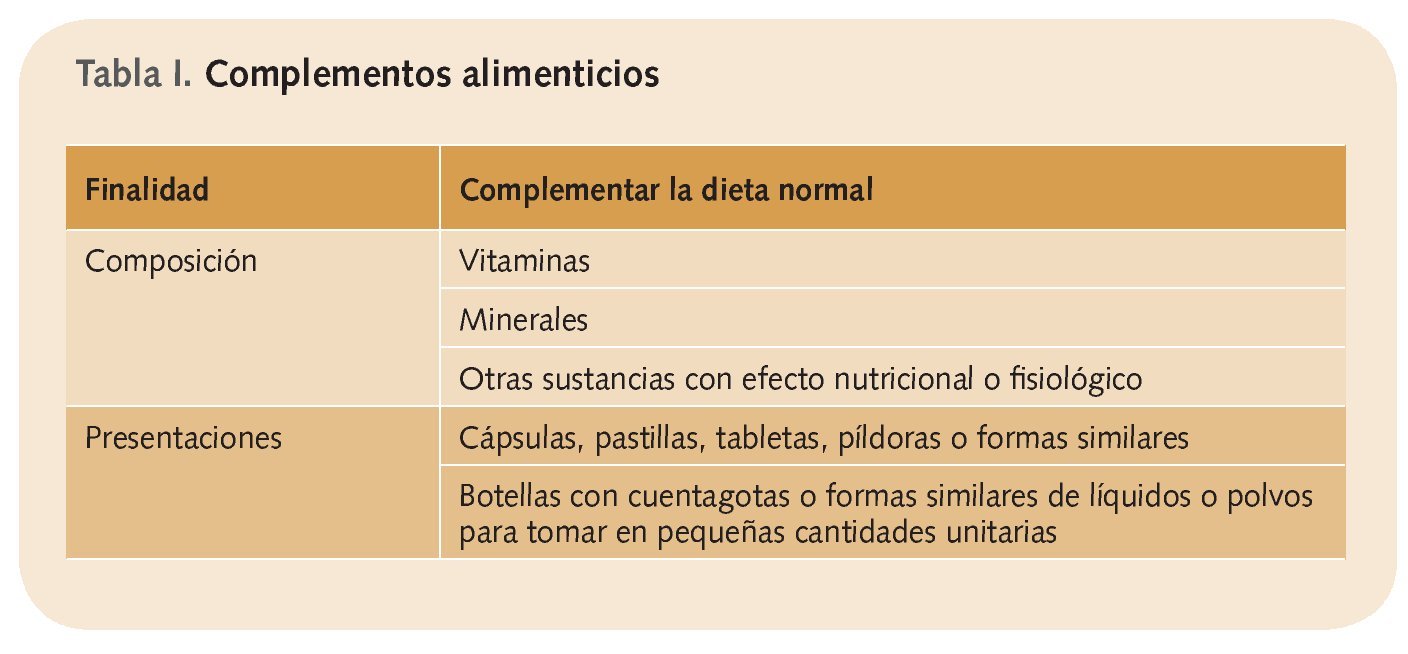
Como su nombre indica, los CA son productos destinados a complementar la dieta normal. El RD 1487/2009 establece, además, que consisten en fuentes concentradas de nutrientes o de otras sustancias que tengan un efecto nutricional o fisiológico y, a diferencia de la normativa anterior, detalla incluso las formas en que pueden presentarse (tabla 1)4,5.
Este real decreto deroga el anterior de 2003, que incorporó al ordenamiento jurídico español la Directiva 2002/46/ CE del Parlamento Europeo y del Consejo, y constituyó la primera ocasión en que se regularon expresamente en España estos productos, adoptando el propio término de complementos alimenticios y estableciéndose una definición muy similar a la actual5,6.
Una de las principales diferencias entre estos productos y el resto de los preparados alimenticios son las presentaciones en las que suelen comercializarse, aspecto éste en el que están mucho más cerca de los medicamentos7. Se encuentran, sin embargo, muy lejos de estos últimos en lo que se refiere a los requisitos necesarios para su comercialización y, por tanto, en las garantías que ofrecen a los potenciales consumidores.
Componentes de los complementos alimenticios
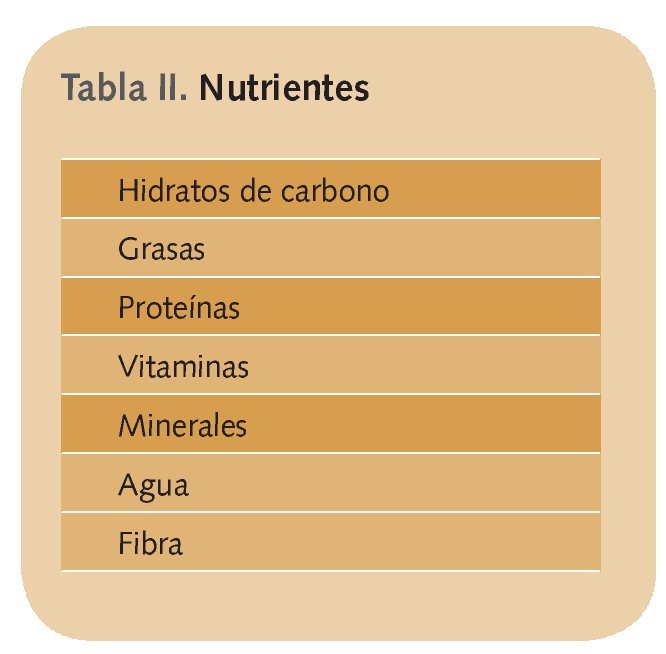
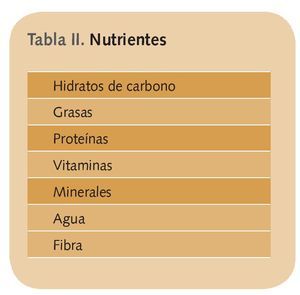
Aunque los nutrientes son los componentes básicos de los alimentos que nuestro organismo precisa para el crecimiento y mantenimiento de sus funciones (tabla II), muchos alimentos contienen también otras sustancias, en cantidades muy pequeñas, que ayudan a ciertas funciones corporales8.
Como puede apreciarse en la definición, a pesar de que la función de los CA es completar la dieta, en esta denominación caben no sólo los productos que contienen los distintos nutrientes, sino los que presentan esas otras sustancias con efecto nutricional y fisiológico.
Este planteamiento, que tiene su lógica a la luz de los avances científicos, presenta, sin embargo, importantes dificultades a la hora de regular estos productos y proteger la salud de sus consumidores potenciales.
De hecho, en el Real Decreto RD 1487/2009 sólo se establecen limitaciones y criterios de pureza para las vitaminas y los minerales4, aunque la propia Directiva Europea reconoce que existe una amplia gama de nutrientes y otros elementos que pueden estar presentes en los CA, incluyendo diversas plantas y extractos de hierbas, y convendría adoptar normas para estas otras sustancias utilizadas como ingredientes de CA6.
Se da, por consiguiente, la paradoja de que, en tanto se produzcan los avances científicos que permitan adoptar esas normas, únicamente se regulan las sustancias cuyos efectos (tanto beneficiosos como perjudiciales) son bien conocidos, y se deja a criterio de los propios fabricantes la inclusión del resto de «sustancias con actividad nutricional o fisiológica», sin establecer ni siquiera un listado de componentes admitidos o prohibidos.
Condiciones para la puesta en el mercado de complementos nutricionales
Por otra parte, para la puesta en el mercado de un complemento alimenticio, la empresa responsable de su comercialización no tiene que solicitar autorización alguna, y ni siquiera es necesario que lo inscriba en el registro general sanitario de alimentos. Aunque la empresa sí debe estar inscrita en dicho registro, para comercializar un CA únicamente debe notificar su puesta en el mercado a las autoridades competentes, enviándoles un ejemplar de la etiqueta del producto. Esta notificación se realiza en la comunidad autónomaa donde radica la empresa y puede efectuarse incluso el mismo día de su puesta en el mercado4.
La ausencia de un registro y la inexistencia de un plazo entre la comunicación de puesta en mercado y la comercialización efectiva suponen que, a diferencia de los medicamentos, en los CA las autoridades sanitarias no realizan ninguna evaluación de eficacia, seguridad y calidad antes de ser puestos a disposición de los consumidores. De hecho, en la normativa aplicable no se establece ni siquiera que deba realizarse un control del cumplimiento de la normativa de etiquetado antes de autorizar su comercialización.
Si bien parece razonable que los medicamentos tengan una regulación más estricta y sean sometidos a mayor control que los alimentos en general, es difícil de justificar la abismal diferencia existente entre aquellos y los CA, máxime cuando éstos no sólo se parecen a los medicamentos en cuanto a sus presentaciones, sino que en algunos casos tienen incluso idéntica composición. Ya que ambos tipos de productos pueden dispensarse en las farmacias, es importante que los farmacéuticos seamos conscientes de estas importantes diferencias y las tengamos en cuenta a la hora de aconsejar a los usuarios y de ayudarles a seleccionar los productos que ofrecen mayores garantías, que son, sin lugar a dudas, lo que se hallan registrados como medicamentos.
Etiquetado de los CA
Al contrario que los medicamentos, los CA no disponen de fichas técnicas y tampoco es obligatorio que incluyan un prospecto en el que se informe a los potenciales consumidores de sus posibles efectos adversos, contraindicaciones o interacciones, aunque contengan sustancias sobre las que exista evidencia científica suficiente como para que éstos sean sobradamente conocidos.
La normativa sobre etiquetado4,9-11 comprende la aplicable a los productos alimenticios en general y la específica de estos productos. Por el primero de estos conceptos deben incluir en sus etiquetas:
El nombre del producto.
La lista de ingredientes y la cantidad de nutrientes (hidratos de carbono, lípidos, proteínas, vitaminas, minerales...).
La cantidad neta.
La fecha de duración mínima o la fecha de caducidad.
Las condiciones especiales de conservación y de utilización.
El modo de empleo o instrucciones de correcta utilización cuando sea necesario para su uso adecuado.
La identificación de la empresa: el nombre, la razón social o la denominación del fabricante o el envasador o de un vendedor establecido dentro de la Unión Europea y, en todo caso, su domicilio.
El lote.
El lugar de origen o procedencia.
Y en particular por tratarse de CA:
La denominación «complemento alimenticio».
La denominación de las categorías de nutrientes o sustancias que caractericen el producto, o una indicación relativa a la naturaleza de dichos nutrientes o sustancias.
La dosis del producto recomendada para consumo diario.
La advertencia de no superar la dosis diaria expresamente recomendada.
La afirmación expresa de que los CA no deben utilizarse como sustituto de una dieta equilibrada.
La indicación de que el producto se debe mantener fuera del alcance de los niños más pequeños.
Además, está prohibido que el etiquetado, la presentación y la publicidad de los CA:
Incluya afirmaciones que declaren o sugieran que una dieta equilibrada y variada no aporta las cantidades adecuadas de nutrientes en general.
Atribuya a los CA la propiedad de prevenir, tratar o curar una enfermedad humana o haga referencia a dichas propiedades.
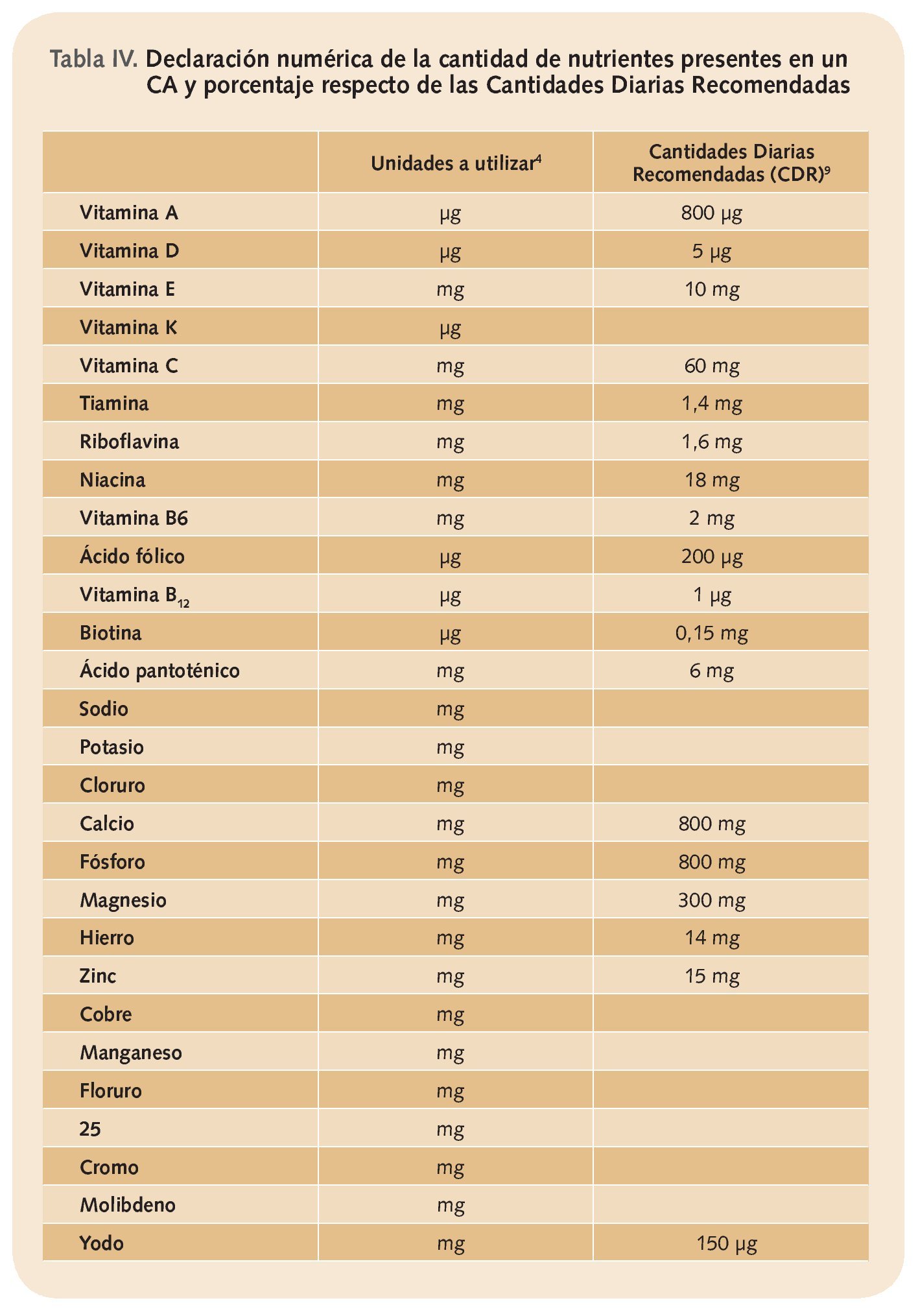
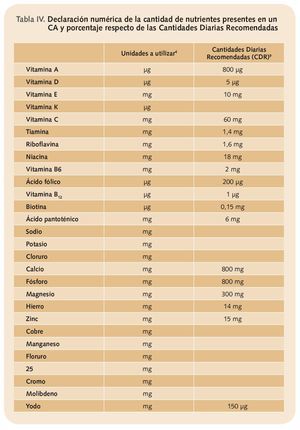
Por otra parte, en la etiqueta tienen que declarar numéricamente la cantidad de nutrientes o de sustancias con un efecto nutricional o fisiológico por dosis recomendada de producto. Para las vitaminas y los minerales tienen que emplearse las unidades recogidas en la tabla 4 y hay que consignar también el porcentaje que esto supone con respecto a los valores de referencia (tabla IV).
En cuanto a las propiedades nutritivas, en la etiqueta, la presentación o la publicidad, sólo se admiten las declaraciones relativas al valor energético (en kJ o kcal) o al contenido o ausencia de los nutrientes siguientes (en g por cada 100 g o ml de producto): proteínas, hidratos de carbono, azúcares, grasas, fibra, sodio, las vitaminas y minerales recogidas en la tabla III. No obstante, también se permite mencionar el contenido (en g) de almidón, polialcoholes, monoinsaturadosb, poliinsaturadosb y colesterolb (en este caso en mg). Esta información debe figurar en una tabla con caracteres bien visibles e indelebles.
Complementos alimenticios, medicamentos y productos milagro
La Ley de Garantías y Uso Racional de los Medicamentos y Productos Sanitarios establece que se considera medicamento cualquier sustancia que pueda usarse con el fin de restaurar, corregir o modificar las funciones fisiológicas ejerciendo una acción farmacológica, inmunológica o metabólica. Dispone, además, que ningún medicamento elaborado industrialmente podrá ser puesto en el mercado sin haber obtenido autorización y haberse inscrito en el registro de medicamentos12.
Sin embargo, en cumplimiento de la Directiva Europea y el Real Decreto antes mencionados se encuentran comercializadas en España sustancias (generalmente de origen vegetal) con capacidad de modificar funciones fisiológicas mediante acciones farmacológicas o metabólicas. Así, por ejemplo, nos encontramos con productos que contienen fitoflavonas de soja comercializados como medicamentos, junto a otros con idéntica composición puestos en el mercado como CA.
Como ya hemos indicado anteriormente, esta diferencia no es puramente administrativa y conlleva que los requisitos que se deben satisfacer para comercializar ambos tipos de productos son radicalmente distintos. Así las autoridades sanitarias garantizan, mediante sus controles preceptivos, que el contenido de los medicamentos responde a lo que figura en sus fichas técnicas, prospectos y etiquetas, mientras que en el caso de los CA esta garantía sólo la aporta el propio fabricante.
Esta situación es similar a la que se produce en los Estados Unidos, donde en el año 2001 se publicó un estudio en el que se demostraba que un gran número de los CA allí comercializados contenían cantidades de fitoestrógenos muy diferentes, y en la mayoría de los casos inferiores, a las declaradas en el etiquetado13. Aunque no disponemos de datos que permitan afirmar que esta situación se da también en nuestro país, resulta evidente que también en Europa los medicamentos aportan más garantías.
La mayoría de las compañías que comercializan CA son empresas de prestigio, que en muchos casos también fabrican medicamentos, y aplican rigurosos controles de calidad a todo lo que ponen en el mercado. Sin embargo, existen algunos casos en que se han detectado graves reacciones adversas asociadas al consumo de ciertos CA y la propia Agencia Española de Seguridad Alimentaria y Nutrición, aunque aporta una explicación alternativa para estos problemas, no descarta que pudieran deberse a identificaciones erróneas de plantas, adulteraciones o contaminaciones14.
Como ya hemos indicado, a los CA no se les pueden atribuir propiedades curativas o preventivas de enfermedades. Sin embargo, la falta de regulación que ha caracterizado durante muchos años este mercado ha propiciado que en algunos casos se realizara una promoción sin control de determinados productos a los que ha dado en calificarse de productos milagro15,16. La venta de productos milagro disfrazados de CA no es algo exclusivo de nuestro país17 y aparece a menudo relacionada con el tratamiento de la obesidad18 y otras alegaciones nutricionales19 o incluso terapéuticas20.
Muchos de estos productos milagro intentan introducirse en el mercado a través de las farmacias, amparándose en el carácter sanitario y el prestigio de estos establecimientos, por lo que es importante que el farmacéutico actualice sus conocimientos para poder detectar la presencia de este tipo de productos y contribuya a erradicarlos del mercado18. Así, debemos saber que está prohibido que cualquier producto que no sea un medicamento o un producto sanitario21:
Se destine a la prevención, tratamiento o curación de enfermedades o pretenda una utilidad terapéutica para ellas.
Sugiera propiedades adelgazantes o contra la obesidad.
Proporcione seguridades de alivio o curación cierta.
Utilice como respaldo cualquier clase de autorizaciones, homologaciones o controles de autoridades sanitarias de cualquier país.
Haga referencia a su uso en centros sanitarios o a su distribución a través de oficinas de farmacia.
Pretenda aportar testimonios de profesionales sanitarios, de personas famosas o conocidas por el público o de pacientes reales o supuestos, como medio de inducción al consumo.
Pretenda sustituir el régimen de alimentación o nutrición comunes, especialmente en los casos de maternidad, lactancia, infancia o tercera edad.
Atribuya a determinadas formas, presentaciones o marcas de productos alimenticios de consumo ordinario, propiedades preventivas, terapéuticas o curativasc.
Sugiera o indique que su uso o consumo potencian el rendimiento físico, psíquico, deportivo o sexual.
Utilice el término «natural» como característica vinculada a pretendidos efectos preventivos o terapéuticos.
Atribuya carácter superfluo a los medicamentos y productos sanitarios o a las consultas o intervenciones de los profesionales sanitarios o pretenda sustituirlos.
Atribuya efectos preventivos o terapéuticos que no estén respaldados por suficientes pruebas técnicas o científicas acreditadas y expresamente reconocidas por la Administración sanitaria del Estado.
Conclusiones
Los CA son productos a base de nutrientes y/o de otras sustancias que tengan un efecto nutricional o fisiológico cuyas presentaciones son similares a las de los medicamentos
No existe un registro de CA y para comercializarlos basta con que la empresa responsable notifique su puesta en el mercado a las autoridades competentes, enviándoles un ejemplar de la etiqueta del producto.
Algunos de ellos puede incluso tener la misma composición que determinados medicamentos de fabricación industrial, pero éstos están sometidos a una regulación mucho más estricta que garantiza su calidad, seguridad y eficacia.
El farmacéutico debe poseer formación suficiente para detectar los posibles productos milagro y contribuir a su eliminación del mercado. Para ello es importante conocer las normativas sobre etiquetado y publicidad y aplicar criterios científicos a la hora de evaluar los productos que se presentan para su venta en las farmacias.
Notas
a. Las comunidades autónomas deben dar conocimiento de estas notificaciones a la Agencia Española de Seguridad Alimentaria y Nutrición, y es directamente a esta Agencia a quien deben notificar la comercialización de un complemento alimenticio las empresas que no tengan establecido su domicilio social en España o cuyo producto proceda de un país no comunitario.
b. En caso de que se declaren estas sustancias, debe mencionarse también el contenido de saturados.
c. Hay resoluciones que consideran que expresiones como «acción antiinflamatoria» o «capacidad para aumentar las defensas» contravienen este apartado (V).