Valorar si un programa de atención farmacéutica integrada (PAFI) en pacientes crónicos mejora la evolución clínica, la calidad de vida de los pacientes y disminuye el consumo de recursos sanitarios.
Material y métodosEnsayo clínico, paralelo, abierto y multicéntrico de un PAFI en pacientes con insuficiencia cardiaca (IC) y/o enfermedad pulmonar obstructiva crónica (EPOC) en 8 áreas de salud de Cataluña. Al paciente en intervención le realizaban seguimiento farmacoterapéutico los farmacéuticos de hospital, atención primaria y farmacia comunitaria. Al control, seguimiento habitual. Todos los pacientes fueron seguidos 12 meses y se les realizó un test de calidad de vida al inicio y final del seguimiento.
ResultadosParticiparon 8 hospitales, 8 centros de atención primaria y 109 farmacias comunitarias. Finalizaron el estudio 238 pacientes con un porcentaje de pérdidas del 2,9%. No hubo diferencias significativas en reingresos, visitas al médico o urgencias. Se detectaron 50 problemas relacionados con medicamentos (PRM) en 37 pacientes, siendo estadísticamente significativa la diferencia de PRM entre el grupo intervención y control en pacientes con IC y casi significativa en pacientes con EPOC. El 36% de los PRM fueron moderados-graves. El 94% PRM fueron evitables y el farmacéutico los resolvió en el 90% de los casos. No hubo diferencias entre la calidad de vida al inicio y final del estudio ni en el consumo de recursos sanitarios.
ConclusionesLos programas de atención farmacéutica integrada permiten la mejora de la calidad asistencial al paciente, no obstante es necesaria la utilización de registros electrónicos que faciliten la comunicación entre niveles asistenciales.
To assess whether an integrated pharmaceutical care programme (IPCP) improves clinical evolution, patient quality of life, and reduces health costs in chronic patients.
Material and methodsA parallel, open, and multi-centre clinical trial of an IPCP in patients with heart failure (HF) and/or chronic obstructive pulmonary disease (COPD) in 8 different health areas in Cataluña. The intervened patient was monitored for pharmacotherapeutic evolution by hospital pharmacists, primary care physicians, and community pharmacists. Controls received normal follow-up. All patients were monitored for 12 months, with quality of life tests administered at the beginning and end of follow-up.
ResultsWe had the participation of 8 different hospitals, 8 primary care centres, and 109 community pharmacies. 238 patients completed the study, with 2.9% of participants lost during the study period. There were no significant differences in terms of readmissions, visits to the doctors, or to emergency services. We detected 50 different medication-related problems (MRP) in 37 patients, with a statistically significant difference in terms of MRP between the control and treatment groups of patients with HF, and almost significant differences in COPD patients. MRP were moderate-severe in 36% of cases. MRP were avoidable in 94% of cases, and the pharmacist resolved the issue in 90% of cases. There were no differences in terms of patient quality of life or health costs between the start and end of the study.
ConclusionsIntegrated pharmaceutical care programs facilitate an improvement in the quality of patient care, but electronic registries are necessary to promote communication between sections of the health care network.
La creciente complejidad en el tratamiento farmacológico de los pacientes ha provocado un cambio de paradigma en la actividad del farmacéutico. Las actividades englobadas dentro del concepto de atención farmacéutica (AF), especialmente el seguimiento farmacoterapéutico, le han posicionado como un agente activo y corresponsable de los resultados en salud. El farmacéutico constituye un elemento fundamental en el equipo de asistencia sanitaria de los pacientes, especialmente de aquellos que están afectados por enfermedades crónicas1.
Los acontecimientos adversos causados por errores de medicación, las dosis subóptimas, las prescripciones inapropiadas o la baja adherencia a los tratamientos pueden ser la causa de la elevada morbilidad y mortalidad por fármacos y los altos costes para la sociedad. Hasta un 30% de los ingresos hospitalarios están directamente vinculados a problemas relacionados con los medicamentos (PRM), siendo las causas más frecuentes de estos ingresos los acontecimientos adversos evitables y la baja adherencia a los tratamientos2.
La insuficiencia cardiaca (IC) y la enfermedad pulmonar obstructiva crónica (EPOC) son 2 enfermedades crónicas que constituyen una de las principales causas de morbilidad y mortalidad en pacientes mayores de 65 años, constituyendo un grave problema de salud pública por su creciente prevalencia, elevado número de ingresos hospitalarios y mortalidad3,4.
La repercusión clínica, económica y en calidad de vida de estas enfermedades es elevada, debido a la morbilidad y mortalidad que generan. Estos pacientes requieren de la atención primaria (AP) de forma continuada y de la atención especializada (AE) en determinados procesos o agudizaciones de su enfermedad crónica. El farmacéutico, dada su fácil accesibilidad al paciente, puede desarrollar un importante papel en el seguimiento integral del tratamiento farmacológico a través de la AF.
Numerosos estudios en diferentes ámbitos (hospital, ambulatorio, geriátrico, comunitario, psiquiátrico) han evaluado la efectividad de la AF en los pacientes pero los resultados son muy diversos, debido fundamentalmente al tipo de paciente sobre el que han actuado, al número de pacientes evaluados, al tiempo de seguimiento de los pacientes y a la propia naturaleza de la intervención. En general los estudios muestran una mejoría significativa en las variables clínicas intermedias o subrogadas pero menos en variables finales como reingresos o mortalidad5–26.
Algunos estudios han evaluado la AF coordinada en los diferentes niveles asistenciales y esta se ha caracterizado por una gran variedad de objetivos de investigación, escenarios, características de los pacientes, tamaños de muestra, intervenciones y medidas de resultados como demuestra la revisión sistemática realizada por Ellitt et al.27 A pesar de ello, de los 21 estudios revisados, 15 reportaron resultados estadísticamente significativos en las variables propuestas de resultados económicos, clínicos y humanísticos. Es por ello que se considera necesario evaluar en nuestro medio la AF integrada y establecer un modelo de atención que pueda ser reproducible y realizable en otros entornos.
En este contexto se pretende enmarcar el presente ensayo para valorar un Programa de Atención Farmacéutica Integrada (PAFI) en el enfermo con IC y/o EPOC con un abordaje novedoso, coordinado y continuo que permita evaluar el nivel de salud de estos pacientes mediante un mejor manejo, seguimiento y supervisión del tratamiento farmacológico. La hipótesis de partida es que la implantación de un PAFI mejora la evolución clínica y la calidad de vida de los pacientes y disminuye el consumo de recursos sanitarios.
Material y métodosDiseñoEnsayo clínico comparativo, prospectivo, aleatorizado, paralelo, abierto y multicéntrico de un PAFI en pacientes con enfermedad crónica frente a un grupo control con seguimiento clínico habitual. El periodo de seguimiento de los pacientes fue de 12 meses después del alta hospitalaria.
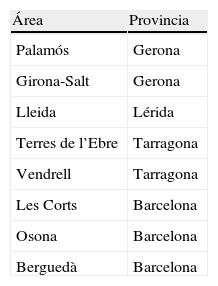
Participantes en el estudioEl estudio se realizó en 8 áreas de salud de Cataluña (tabla 1), con una estructura definida para la AF integrada y coordinada entre los farmacéuticos de hospital (FH), farmacéuticos de atención primaria (FP) y farmacéuticos de farmacia comunitaria (FC).
Los criterios de inclusión fueron: edad igual o superior a 65 años, descompensación y/o agudización de la IC y/o de la EPOC como diagnóstico de ingreso a cargo de los servicios de medicina interna, neumología o cardiología, toma de 4 o más medicamentos crónicos al ingreso, perteneciente al área de salud donde se realizaba el estudio, con posibilidad de seguimiento en una farmacia comunitaria que participara en el estudio, estimación de la posibilidad de seguimiento superior a un año y que el paciente comprendiera y otorgara su consentimiento para participar en el estudio.
Los criterios de exclusión fueron que el paciente tuviera demencia, enfermedad mental o incapacidad para entender el estudio y/o otorgar su consentimiento, con expectativa de vida inferior a un año, que no estuviera incluido en otro ensayo clínico en el año anterior al estudio o que participara en un programa de seguimiento específico dentro de un proyecto de investigación y que no fuera derivado a otro centro (hospital, larga estancia o centro sociosanitario) al alta hospitalaria.
El estudio fue aprobado por los comités de ensayos clínicos de los hospitales participantes.
El tamaño de la muestra se calculó en función de la hipótesis de que el PAFI disminuiría el número de reingresos en un 12% absoluto, asumiendo un error alfa de un 5%, para una potencia del estudio del 80% con los datos de incidencia de EPOC e IC en nuestro medio era necesario reclutar 198 pacientes por grupo (intervención vs control) y para cada brazo (IC y EPOC). Asumiendo unas pérdidas del 20% de los pacientes necesitaban un total de 952 pacientes.
AleatorizaciónLos pacientes que aceptaron participar en el estudio fueron aleatorizados al grupo intervención y control de forma centralizada. Al introducir un paciente, en la intranet utilizada para el estudio, de forma automática lo asignaba a uno u otro grupo. La selección de pacientes se llevó a cabo de mayo a diciembre del 2007 y lo realizó el FH durante el ingreso del paciente por una descompensación de su IC y/o EPOC y luego los pacientes fueron derivados para su seguimiento de AF a los recursos farmacéuticos existentes en su área de salud (FP y FC).
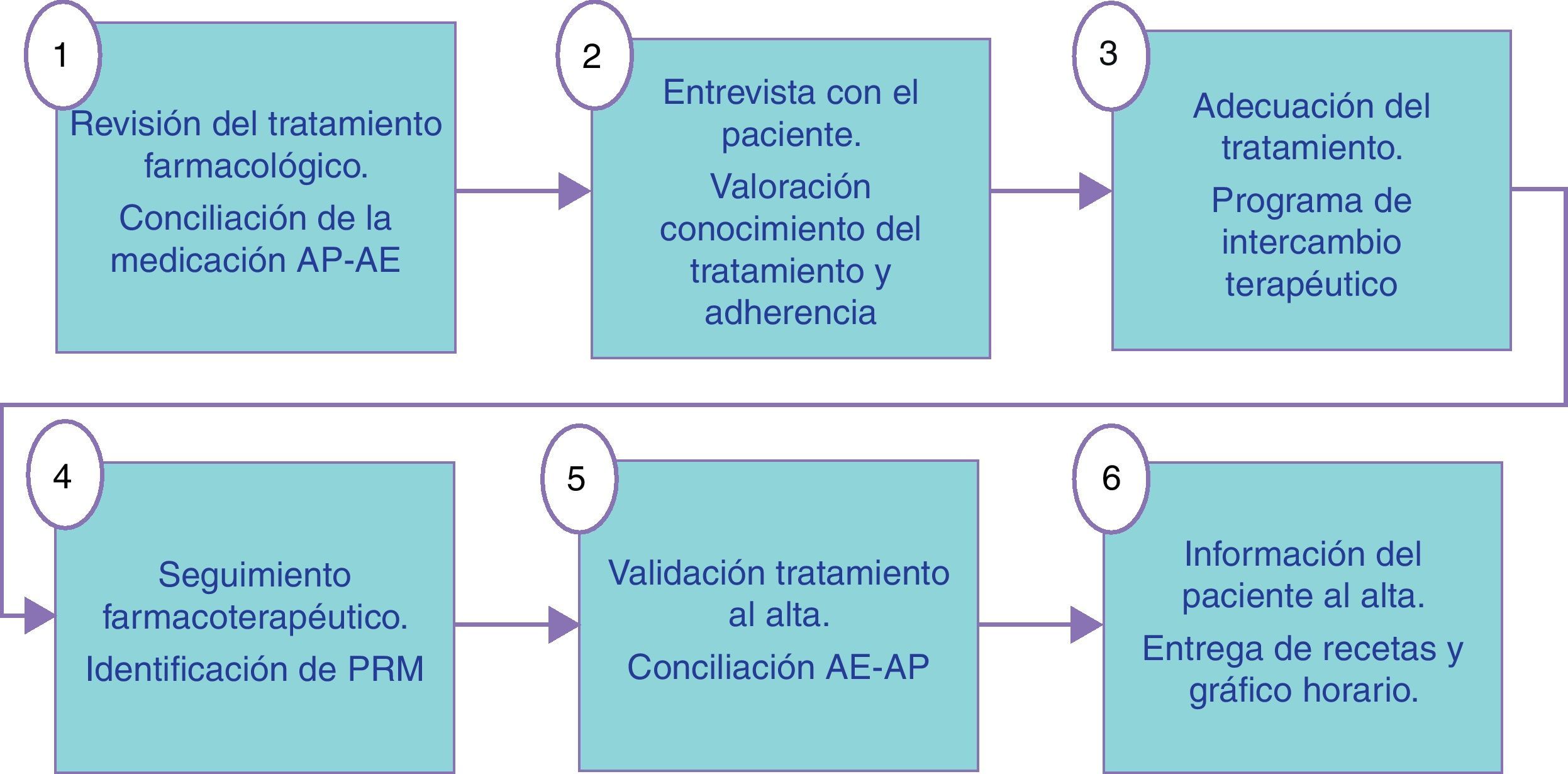
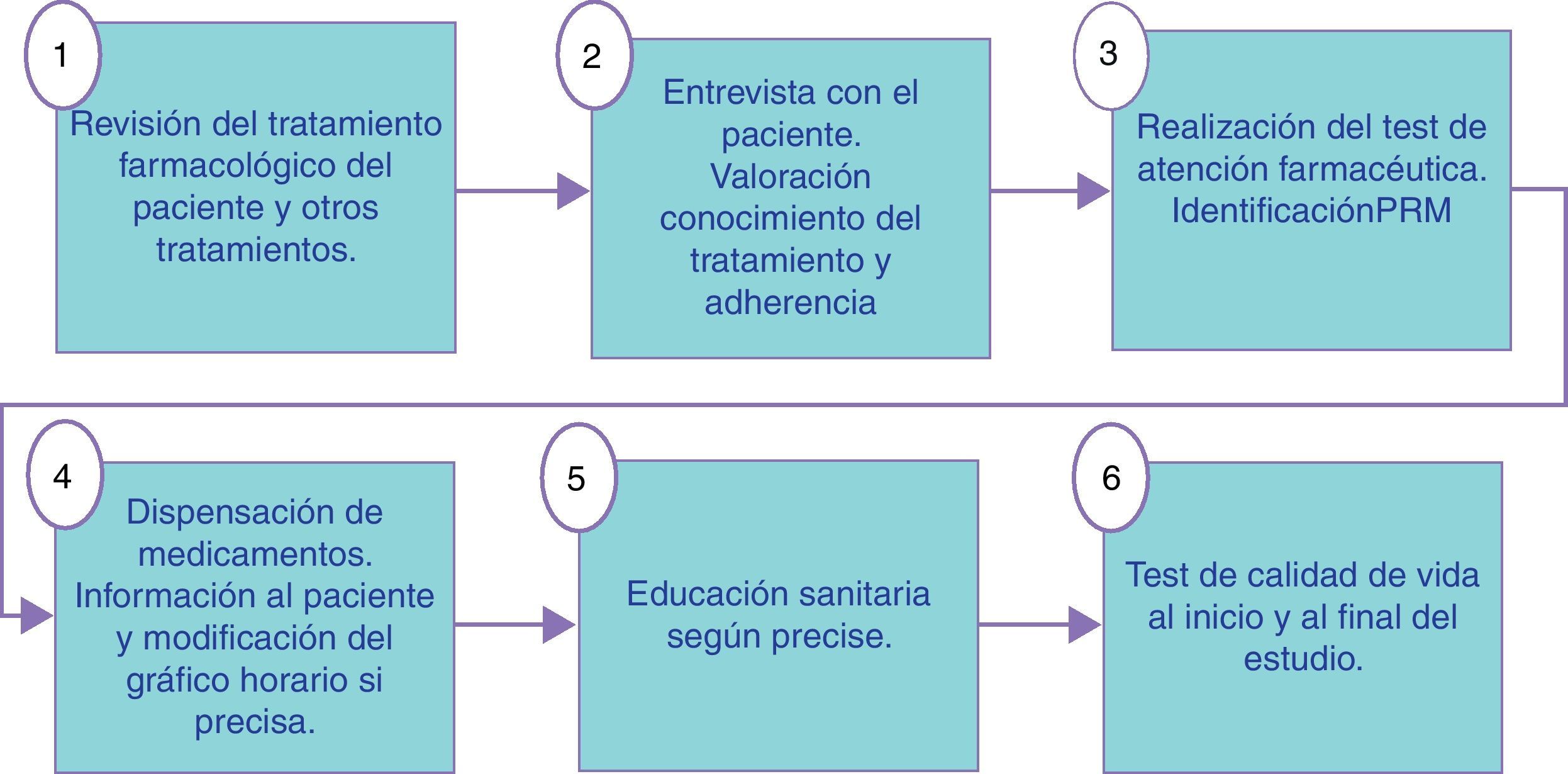
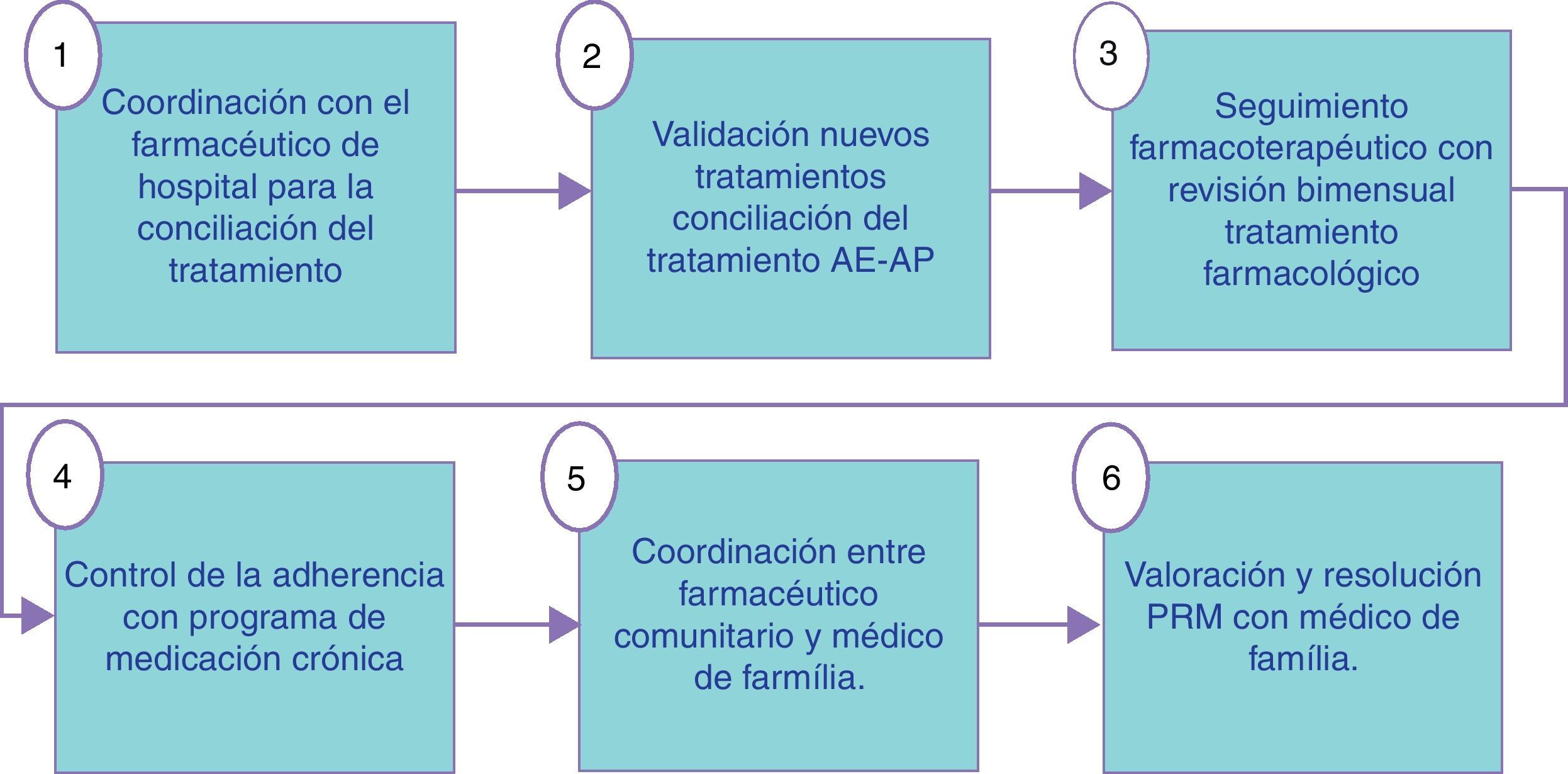
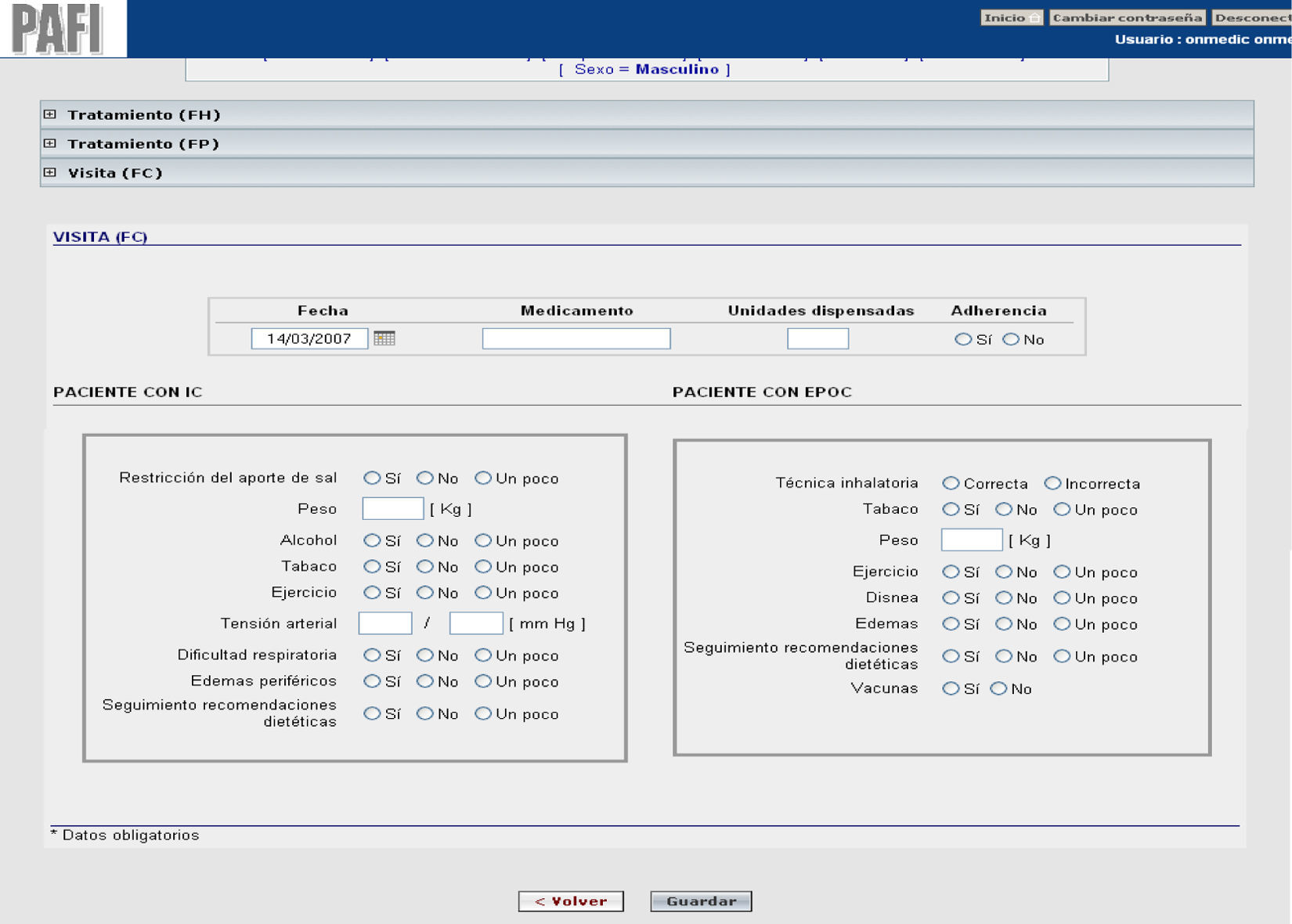
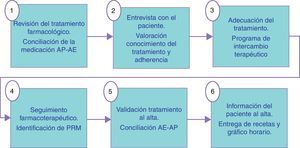
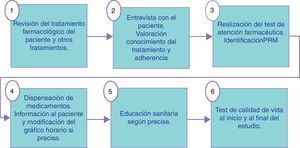
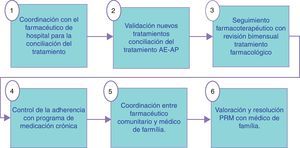
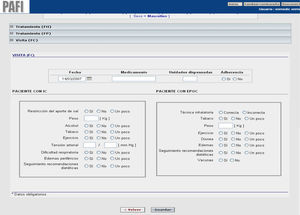
Descripción de la intervenciónLa intervención realizada por los farmacéuticos de los 3 niveles asistenciales en el grupo intervención se describe en las figuras 1-3. En las visitas para la dispensación de medicamentos en la farmacia comunitaria se realizaba un test de AF para el seguimiento y monitorización del tratamiento del paciente (fig. 4). Los PRM detectados en el periodo de seguimiento del paciente fueron clasificados según el segundo Consenso de Granada y se valoró su gravedad28 y su evitabilidad29. En el grupo control se realizó el seguimiento habitual. En ambos grupos, intervención y control, se realizó un test de calidad de vida al inicio y al final del estudio que fue el cuestionario de Minnesota para la IC y el St. George para EPOC.
En todas las áreas sanitarias se realizaron talleres de formación y se suministró material educativo para estandarizar la AF prestada.
Variables del estudioLa variable principal del estudio fue el número de reingresos totales del paciente. Las variables secundarias fueron: visitas a hospital de día y urgencias (hospitalarias y de AP); mortalidad relacionada con los diagnósticos iniciales; número y tipo de PRM, su gravedad y su evitabilidad; coste del tratamiento farmacológico (tratamiento hospitalario en el ingreso y coste del tratamiento en recetas); coste de los recursos sanitarios utilizados (ingresos, visitas a hospital de día, urgencias y visitas médicas realizadas por el especialista y en atención primaria, todos calculados teniendo en cuenta el precio que paga el Servicio Catalán de la Salud por dicha actividad a los hospitales concertados) y la variación de la calidad de vida al inicio y al final del estudio medida por un cuestionario específico validado.
Análisis estadísticoEl análisis estadístico se realizó mediante el programa PASW 17.0. Se trabajó sobre una base de datos matricial e informatizada en la que se incluyeron los valores recogidos de cada uno de los pacientes. Las variables se describieron mediante tablas de frecuencias absolutas y relativas, medias y estadísticos de dispersión (mínimo-máximo). Para comparar las variables cuantitativas, entre los grupos de intervención, se utilizó la prueba de la t de Student o el análisis de la varianza (ANOVA de un factor). Para el estudio estadístico de la relación entre variables cualitativas se empleó una prueba de independencia de ji cuadrado o la prueba exacta de Fischer. Para el estudio de la variación de la calidad de vida se empleó la prueba de la t de Student para datos pareados.
El nivel de significación se estableció bilateral para una p<0,05.
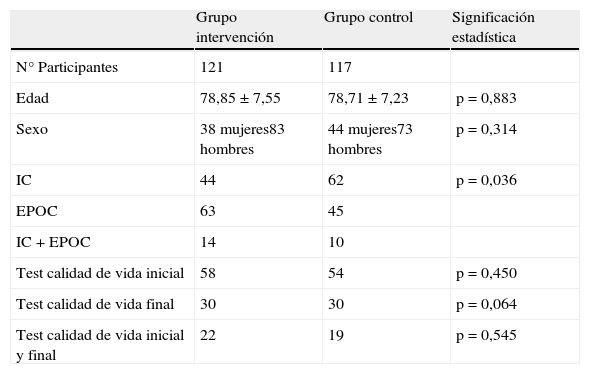
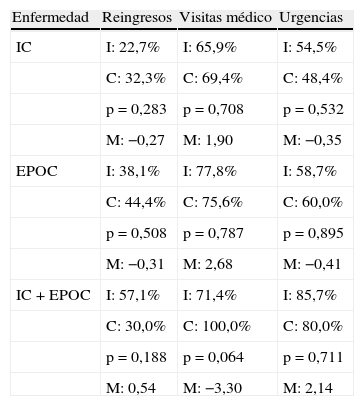
ResultadosEn el estudio participaron 8 hospitales, 8 centros de atención primaria y 163 farmacias comunitarias pero solo 109 farmacias recibieron pacientes del grupo intervención y control. En el anexo I se describe la relación de farmacéuticos de los 3 niveles asistenciales que realizaron el seguimiento farmacoterapéutico a los pacientes documentado en la intranet. El número de pacientes que concluyeron el estudio fue de 238, con un porcentaje de pérdidas del 2,9% (3 pacientes en el grupo intervención y 4 en el grupo control). Las características de los pacientes se describen en la tabla 2. Los grupos intervención y control estratificados por enfermedad no fueron diferentes en cuanto a la distribución por sexos ni por edad. La media de seguimiento de pacientes por farmacia comunitaria fue de 2 con un intervalo entre 1-6. En la tabla 3 se muestran el porcentaje de reingresos, visitas al médico o visitas a urgencias de los pacientes en las 3 enfermedades, sin que existan diferencias significativas entre el grupo intervención y el grupo control.
Características de los pacientes
| Grupo intervención | Grupo control | Significación estadística | |
| N° Participantes | 121 | 117 | |
| Edad | 78,85±7,55 | 78,71±7,23 | p=0,883 |
| Sexo | 38 mujeres83 hombres | 44 mujeres73 hombres | p=0,314 |
| IC | 44 | 62 | p=0,036 |
| EPOC | 63 | 45 | |
| IC+EPOC | 14 | 10 | |
| Test calidad de vida inicial | 58 | 54 | p=0,450 |
| Test calidad de vida final | 30 | 30 | p=0,064 |
| Test calidad de vida inicial y final | 22 | 19 | p=0,545 |
EPOC: enfermedad pulmonar obstructiva crónica; IC: insuficiencia cardiaca.
Porcentaje de reingresos, visitas al médico y visitas a urgencias de los pacientes
| Enfermedad | Reingresos | Visitas médico | Urgencias |
| IC | I: 22,7% | I: 65,9% | I: 54,5% |
| C: 32,3% | C: 69,4% | C: 48,4% | |
| p=0,283 | p=0,708 | p=0,532 | |
| M: −0,27 | M: 1,90 | M: −0,35 | |
| EPOC | I: 38,1% | I: 77,8% | I: 58,7% |
| C: 44,4% | C: 75,6% | C: 60,0% | |
| p=0,508 | p=0,787 | p=0,895 | |
| M: −0,31 | M: 2,68 | M: −0,41 | |
| IC+EPOC | I: 57,1% | I: 71,4% | I: 85,7% |
| C: 30,0% | C: 100,0% | C: 80,0% | |
| p=0,188 | p=0,064 | p=0,711 | |
| M: 0,54 | M: −3,30 | M: 2,14 |
C: grupo control; EPOC: enfermedad pulmonar obstructiva crónica; I: grupo intervención, IC: insuficiencia cardiaca; M: diferencia entre la media de reingresos, visitas al médico o urgencias del grupo intervención respecto al control.
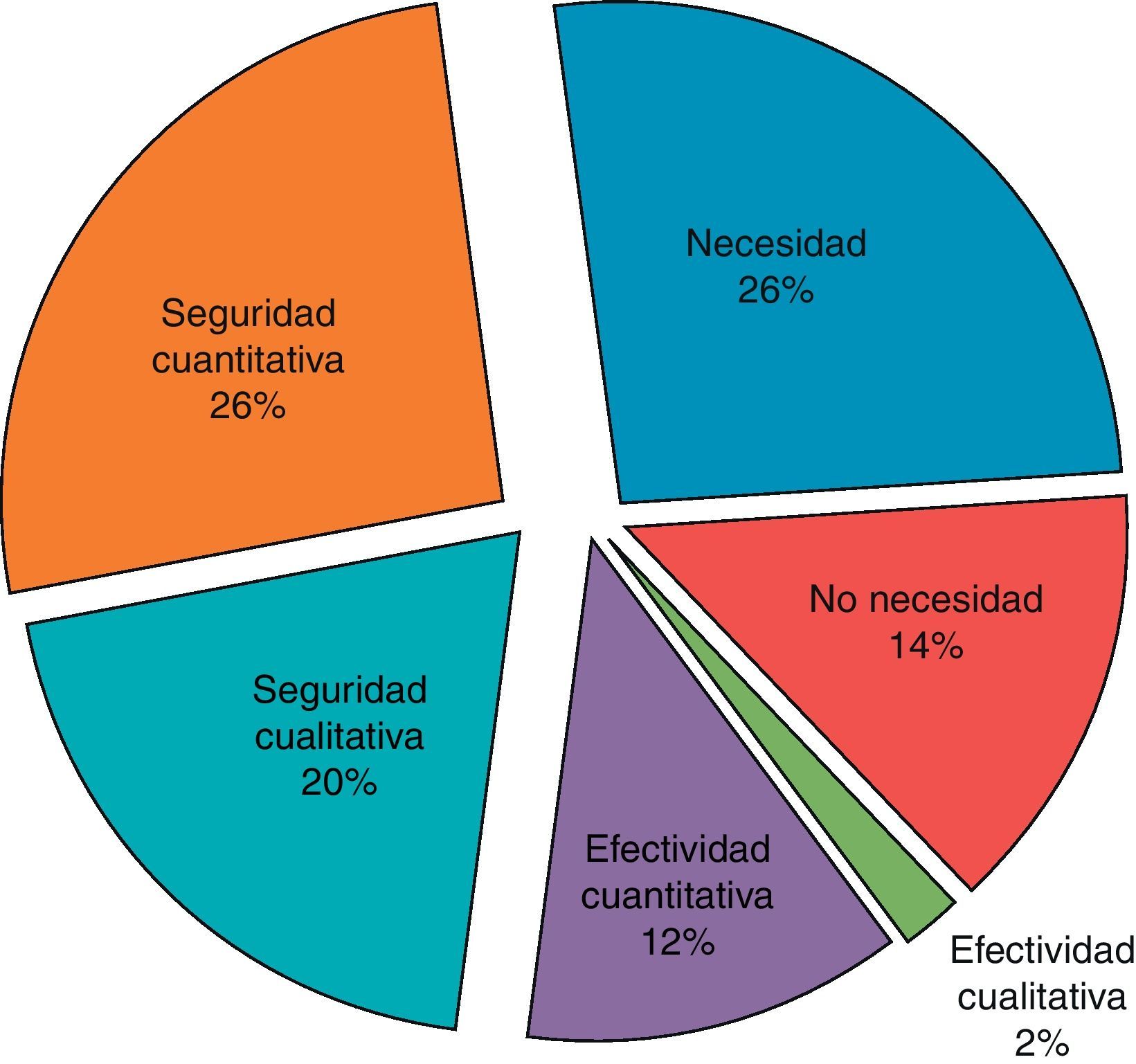
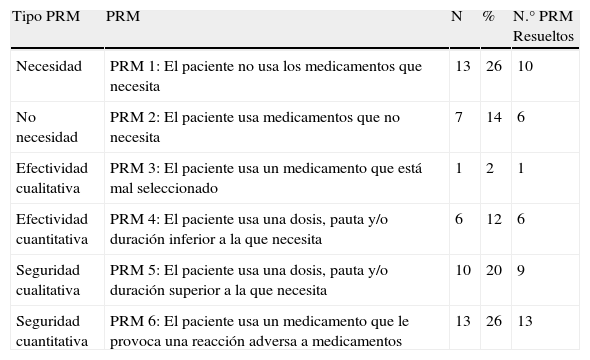
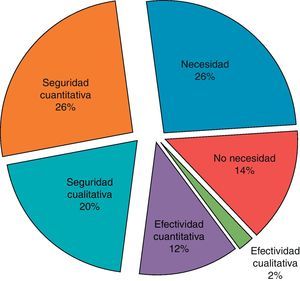
El número de PRM detectados fue de 50 en 37 pacientes. La distribución de PRM en los grupos se muestra en la tabla 4, siendo estadísticamente significativa la diferencia entre el número de PRM detectados en el grupo intervención y el control en los pacientes con IC y casi significativa en EPOC. El tipo de PRM detectados se detalla en la tabla 5 y la figura 5. La gravedad de los PRM fue leve en el 64% de los casos, moderada en un 23% y grave en el 13%. Un 94% de los PRM fueron evitables y el farmacéutico resolvió el PRM en un 90% de los casos.
Tipo de problemas relacionados con los medicamentos detectados
| Tipo PRM | PRM | N | % | N.° PRM Resueltos |
| Necesidad | PRM 1: El paciente no usa los medicamentos que necesita | 13 | 26 | 10 |
| No necesidad | PRM 2: El paciente usa medicamentos que no necesita | 7 | 14 | 6 |
| Efectividad cualitativa | PRM 3: El paciente usa un medicamento que está mal seleccionado | 1 | 2 | 1 |
| Efectividad cuantitativa | PRM 4: El paciente usa una dosis, pauta y/o duración inferior a la que necesita | 6 | 12 | 6 |
| Seguridad cualitativa | PRM 5: El paciente usa una dosis, pauta y/o duración superior a la que necesita | 10 | 20 | 9 |
| Seguridad cuantitativa | PRM 6: El paciente usa un medicamento que le provoca una reacción adversa a medicamentos | 13 | 26 | 13 |
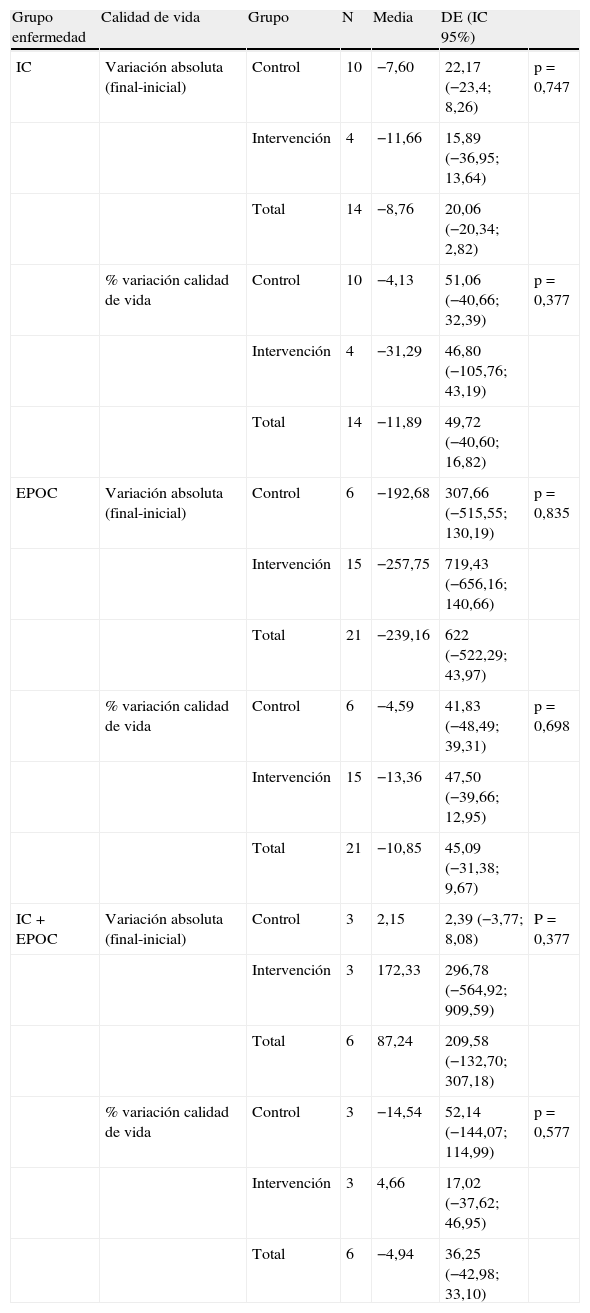
El test de calidad de vida inicial y final solo se realizó en 41 pacientes como muestra la tabla 2. El porcentaje de variación entre el test inicial y final de los grupos de estudio, en las diferentes enfermedades, no mostró diferencias significativas (tabla 6).
Porcentaje de variación entre el test de calidad de vida inicial y final
| Grupo enfermedad | Calidad de vida | Grupo | N | Media | DE (IC 95%) | |
| IC | Variación absoluta (final-inicial) | Control | 10 | −7,60 | 22,17 (−23,4; 8,26) | p=0,747 |
| Intervención | 4 | −11,66 | 15,89 (−36,95; 13,64) | |||
| Total | 14 | −8,76 | 20,06 (−20,34; 2,82) | |||
| % variación calidad de vida | Control | 10 | −4,13 | 51,06 (−40,66; 32,39) | p=0,377 | |
| Intervención | 4 | −31,29 | 46,80 (−105,76; 43,19) | |||
| Total | 14 | −11,89 | 49,72 (−40,60; 16,82) | |||
| EPOC | Variación absoluta (final-inicial) | Control | 6 | −192,68 | 307,66 (−515,55; 130,19) | p=0,835 |
| Intervención | 15 | −257,75 | 719,43 (−656,16; 140,66) | |||
| Total | 21 | −239,16 | 622 (−522,29; 43,97) | |||
| % variación calidad de vida | Control | 6 | −4,59 | 41,83 (−48,49; 39,31) | p=0,698 | |
| Intervención | 15 | −13,36 | 47,50 (−39,66; 12,95) | |||
| Total | 21 | −10,85 | 45,09 (−31,38; 9,67) | |||
| IC+EPOC | Variación absoluta (final-inicial) | Control | 3 | 2,15 | 2,39 (−3,77; 8,08) | P=0,377 |
| Intervención | 3 | 172,33 | 296,78 (−564,92; 909,59) | |||
| Total | 6 | 87,24 | 209,58 (−132,70; 307,18) | |||
| % variación calidad de vida | Control | 3 | −14,54 | 52,14 (−144,07; 114,99) | p=0,577 | |
| Intervención | 3 | 4,66 | 17,02 (−37,62; 46,95) | |||
| Total | 6 | −4,94 | 36,25 (−42,98; 33,10) |
EPOC: enfermedad pulmonar obstructiva crónica; IC: insuficiencia cardiaca.
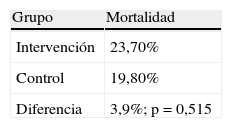
La mortalidad en el grupo de intervención respecto al control fue ligeramente superior pero con diferencias no significativas (tabla 7).
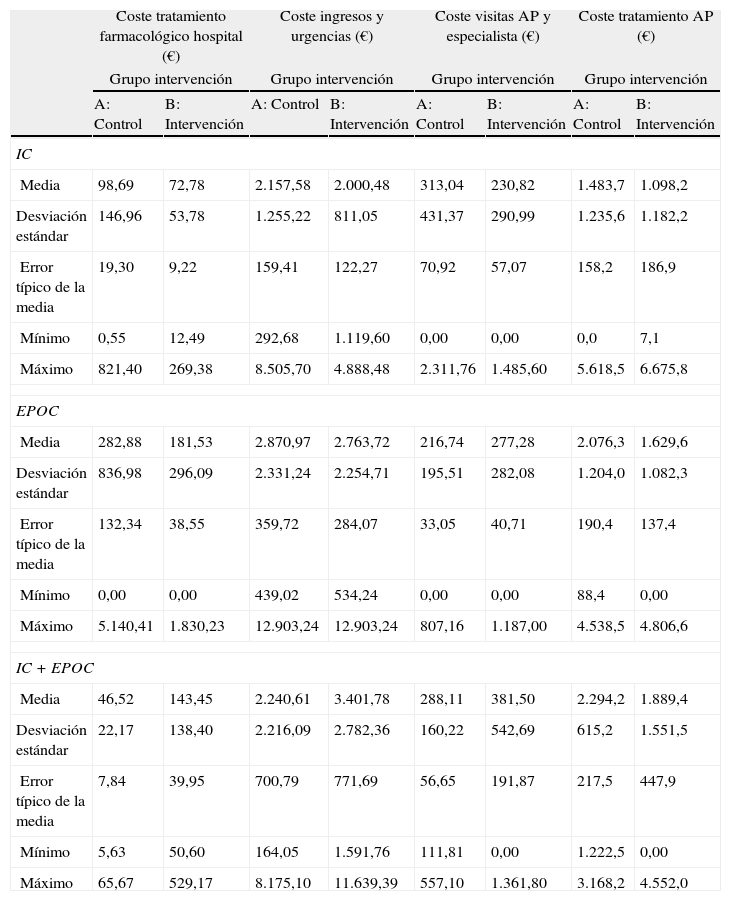
La media del coste del tratamiento farmacológico (coste del tratamiento utilizado en el hospital y coste de las recetas prescritas) y el coste de los recursos sanitarios utilizados (visitas al médico de cabecera, al especialista, visitas a urgencias e ingresos) en cada enfermedad se detalla en la tabla 8 siendo las diferencias entre el grupo intervención y control no estadísticamente significativas aunque en todos los casos la media fue menor en el grupo intervención (tabla 9).
Coste del tratamiento farmacológico y de los recursos sanitarios utilizados
| Coste tratamiento farmacológico hospital (€) | Coste ingresos y urgencias (€) | Coste visitas AP y especialista (€) | Coste tratamiento AP (€) | |||||
| Grupo intervención | Grupo intervención | Grupo intervención | Grupo intervención | |||||
| A: Control | B: Intervención | A: Control | B: Intervención | A: Control | B: Intervención | A: Control | B: Intervención | |
| IC | ||||||||
| Media | 98,69 | 72,78 | 2.157,58 | 2.000,48 | 313,04 | 230,82 | 1.483,7 | 1.098,2 |
| Desviación estándar | 146,96 | 53,78 | 1.255,22 | 811,05 | 431,37 | 290,99 | 1.235,6 | 1.182,2 |
| Error típico de la media | 19,30 | 9,22 | 159,41 | 122,27 | 70,92 | 57,07 | 158,2 | 186,9 |
| Mínimo | 0,55 | 12,49 | 292,68 | 1.119,60 | 0,00 | 0,00 | 0,0 | 7,1 |
| Máximo | 821,40 | 269,38 | 8.505,70 | 4.888,48 | 2.311,76 | 1.485,60 | 5.618,5 | 6.675,8 |
| EPOC | ||||||||
| Media | 282,88 | 181,53 | 2.870,97 | 2.763,72 | 216,74 | 277,28 | 2.076,3 | 1.629,6 |
| Desviación estándar | 836,98 | 296,09 | 2.331,24 | 2.254,71 | 195,51 | 282,08 | 1.204,0 | 1.082,3 |
| Error típico de la media | 132,34 | 38,55 | 359,72 | 284,07 | 33,05 | 40,71 | 190,4 | 137,4 |
| Mínimo | 0,00 | 0,00 | 439,02 | 534,24 | 0,00 | 0,00 | 88,4 | 0,00 |
| Máximo | 5.140,41 | 1.830,23 | 12.903,24 | 12.903,24 | 807,16 | 1.187,00 | 4.538,5 | 4.806,6 |
| IC+EPOC | ||||||||
| Media | 46,52 | 143,45 | 2.240,61 | 3.401,78 | 288,11 | 381,50 | 2.294,2 | 1.889,4 |
| Desviación estándar | 22,17 | 138,40 | 2.216,09 | 2.782,36 | 160,22 | 542,69 | 615,2 | 1.551,5 |
| Error típico de la media | 7,84 | 39,95 | 700,79 | 771,69 | 56,65 | 191,87 | 217,5 | 447,9 |
| Mínimo | 5,63 | 50,60 | 164,05 | 1.591,76 | 111,81 | 0,00 | 1.222,5 | 0,00 |
| Máximo | 65,67 | 529,17 | 8.175,10 | 11.639,39 | 557,10 | 1.361,80 | 3.168,2 | 4.552,0 |
EPOC: enfermedad pulmonar obstructiva crónica; IC: insuficiencia cardiaca.
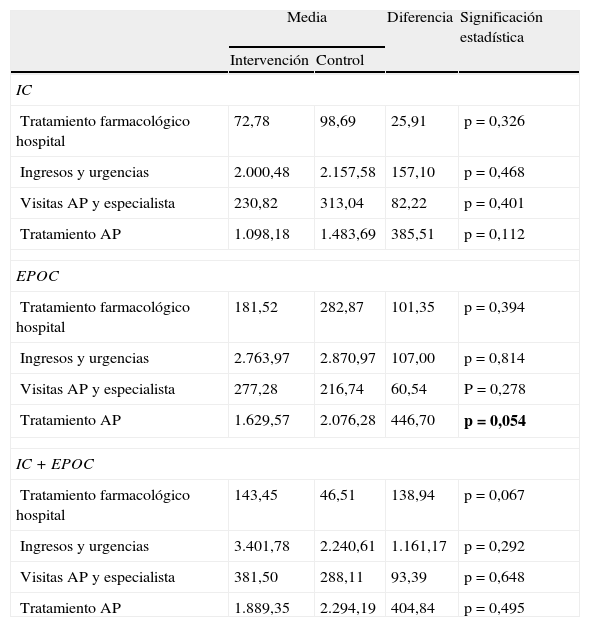
Diferencias en el coste del tratamiento farmacológico y los recursos sanitarios utilizados (€)
| Media | Diferencia | Significación estadística | ||
| Intervención | Control | |||
| IC | ||||
| Tratamiento farmacológico hospital | 72,78 | 98,69 | 25,91 | p=0,326 |
| Ingresos y urgencias | 2.000,48 | 2.157,58 | 157,10 | p=0,468 |
| Visitas AP y especialista | 230,82 | 313,04 | 82,22 | p=0,401 |
| Tratamiento AP | 1.098,18 | 1.483,69 | 385,51 | p=0,112 |
| EPOC | ||||
| Tratamiento farmacológico hospital | 181,52 | 282,87 | 101,35 | p=0,394 |
| Ingresos y urgencias | 2.763,97 | 2.870,97 | 107,00 | p=0,814 |
| Visitas AP y especialista | 277,28 | 216,74 | 60,54 | P=0,278 |
| Tratamiento AP | 1.629,57 | 2.076,28 | 446,70 | p=0,054 |
| IC+EPOC | ||||
| Tratamiento farmacológico hospital | 143,45 | 46,51 | 138,94 | p=0,067 |
| Ingresos y urgencias | 3.401,78 | 2.240,61 | 1.161,17 | p=0,292 |
| Visitas AP y especialista | 381,50 | 288,11 | 93,39 | p=0,648 |
| Tratamiento AP | 1.889,35 | 2.294,19 | 404,84 | p=0,495 |
AP: atención primaria; EPOC: enfermedad pulmonar obstructiva crónica; IC: insuficiencia cardiaca.
En negrita, resultado estadisticamente significativo.
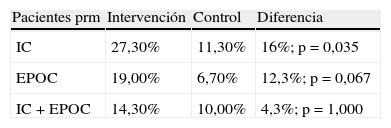
Los resultados obtenidos muestran una disminución absoluta en el número de reingresos del grupo intervención respecto al control en los pacientes con IC y EPOC y un aumento en los pacientes que tienen ambas enfermedades, pero en ningún caso las diferencias son estadísticamente significativas. No obstante, estos resultados son comparables a la mayoría de estudios similares realizados en pacientes con trastornos crónicos en diferentes ámbitos5–12, aunque en algunos estudios los reingresos disminuyen de forma significativa en el grupo intervención2,13–15 y en otros solo disminuyen en los primeros meses de seguimiento pero no en los siguientes16,17.
Las visitas a urgencias y al médico especialista o de atención primaria tampoco disminuyeron de forma significativa en el grupo intervención, sino al contrario, en la mayoría de casos aumentaron. Esto ocurre en casi todos los estudios publicados6–9,15,18–20 excepto en algunos, en que sí disminuyeron las visitas a urgencias2,13,14. Algunos estudios señalan que las estrategias realizadas para aumentar la implicación de los pacientes en su problema de salud se traduce en un aumento de la utilización de los servicios sanitarios18.
El porcentaje de pacientes con PRM detectados es superior en el grupo intervención en los 3 grupos de enfermedades pero solo en IC las diferencias son significativas, no obstante en EPOC son casi significativas y en los pacientes con ambas enfermedades la muestra es muy pequeña para detectar diferencias. Estos resultados son similares a los publicados en la literatura especializada7,19,21,22,. No obstante, el número de PRM por paciente en nuestro estudio es más bajo, seguramente debido a que la clasificación adoptada es diferente y a que en algunos estudios consideran PRM la educación sanitaria, los fármacos no incluidos en guía o la adherencia al tratamiento7,22. El porcentaje de resolución de los PRM fue del 90%, resultado superior a los estudios publicados7,19 que no alcanzan el 80%. Todos los PRM resueltos menos uno corresponden a PRM de eficacia y seguridad, esto podría explicar el menor número de reingresos y un mayor número de visitas o urgencias para ajuste de dosis o pauta en el grupo intervención, al igual que en otros estudios publicados de nuestro ámbito17.
Como en la mayoría de los estudios publicados7,9,11,12,14,17–19,23 la variación de la calidad de vida del paciente inicial y final, en cualquiera de las 3 enfermedades, no muestra diferencias significativas entre el grupo intervención y el control, solo en algún estudio se muestra una mejoría de la calidad de vida a los 9 meses pero no a los 12 meses15 o en el primer año pero no a los 2 años24. No obstante, en una revisión realizada por Pickard y Hung, la mayoría de estudios (62%) que incluyeron un grupo control no encontraron diferencias significativas en la calidad de vida. Sin embargo, en un estudio25 para intervenciones relacionadas con asma, hipertensión o IC mostraron un impacto positivo en alguna o en todas las subescalas de calidad de vida, al igual que en otro estudio más reciente en pacientes con EPOC13. En nuestro caso la muestra es pequeña para detectar diferencias significativas ya que solo 41 pacientes en todos los grupos se les realizó el test de calidad de vida al inicio y al final del estudio.
La mortalidad en el periodo de seguimiento no mostró diferencias estadísticamente significativas entre el grupo intervención y el control. Estos resultados concuerdan con los datos de la literatura médica5,6,10–12,14,20, excepto en un estudio en que la mortalidad a los 12 meses fue inferior en el grupo intervención17. La media del coste del tratamiento farmacológico en IC y EPOC fue menor en el grupo intervención que en el control aunque las diferencias no fueron estadísticamente significativas, resultados comparables a los estudios publicados8,19,26, excepto en un caso que el coste del tratamiento fue superior en el grupo intervención6. En general, los costes directos de la utilización de recursos sanitarios en los pacientes con IC y EPOC fueron menores en el grupo intervención pero no de forma significativa, al igual que en la mayoría de estudios publicados7,19 aunque en algunos de ellos sí que son significativos2,6. No obstante, para establecer comparaciones hay que tener en cuenta la variabilidad de métodos de estimación de costes empleados en los diferentes estudios y considerar la ratio coste-beneficio y no solo los costes directos observados30.
Una de las principales limitaciones del estudio ha sido el tamaño insuficiente de la muestra, motivado por los criterios restrictivos de ingreso en el estudio y por una estimación optimista de la mejora de la AF en los resultados en salud del paciente. El simple hecho de no incluir pacientes que fueran derivados a otro centro (hospital, larga estancia o centro sociosanitario) al alta hospitalaria no permitió alcanzar el tamaño de muestra previsto y en consecuencia disminuyó la potencia del estudio. Esto ha propiciado la obtención de resultados estadísticamente no significativos, no obstante, no significa que los resultados no fueran clínicamente relevantes. Otra de las limitaciones del estudio fue que no se realizó una comparación inicial entre el grupo intervención y el control en las variables clínicas primarias como clase funcional o número de reingresos previos al inicio del estudio que hubieran permitido establecer la homogeneidad de ambos grupos en estas variables. En cuanto a la valoración económica solo se tuvieron en cuenta los costes directos utilizados aunque no se contemplaron los costes de los recursos farmacéuticos. Además, no se estableció un ratio coste-beneficio. No obstante, los resultados, aunque no fueron positivos, en la mayoría de las variables fueron comparables a los obtenidos en otros estudios. Algunos inconvenientes que se han traducido en una mala cumplimentación de los registros han sido: la dificultad de mantener el seguimiento del paciente en los reingresos en el hospital debido a que una vez concluido el periodo de selección no se disponía de becario para ello. En la farmacia comunitaria el paciente acudía pocas veces y en algunas ocasiones el familiar era poco colaborador, además de disponer en algunos casos de poco tiempo para la AF. La laboriosidad en la cumplimentación de los registros en los 3 ámbitos ha sido otra de las dificultades encontradas. A pesar de ello, el programa PAFI ha permitido iniciar la coordinación asistencial farmacéutica en la atención al paciente entre los 3 niveles asistenciales y ha de ser el punto de partida para la continuidad de esta asistencia facilitado por la implantación de las nuevas tecnologías como la receta electrónica o la historia clínica compartida.
ConclusionesLos programas de atención farmacéutica integrada permiten la mejora de la calidad de la asistencia al paciente y los resultados asistenciales, no obstante es necesaria la utilización de registros electrónicos que faciliten la comunicación de los datos del paciente entre los 3 niveles asistenciales. La conciliación del tratamiento en la transición entre niveles es una actividad básica para la realización de la atención farmacéutica. La coordinación de los farmacéuticos de los 3 niveles asistenciales permitirá reducir los problemas de salud derivados de la utilización de medicamentos.
M. Compte. Oficina de Farmacia. Falset. Tarragona
- A.
Barbero. Oficina de Farmacia. Flix. Tarragona
J.A. Mora. Oficina de Farmacia. Miravet d’Ebre. Tarragona
C. Hernandez. Oficina de Farmacia. Benissanet. Tarragona
J. C. Molina. Oficina de Farmacia. Mora d’Ebre. Tarragona
- A.
Veciana. Oficina de Farmacia. Mora La Nova. Tarragona
J. Ferras. Oficina de Farmacia. Horta de Sant Joan. Tarragona
F. Villanueva. Oficina de Farmacia. Caseres. Tarragona
M.A. Bove. Oficina de Farmacia. Corbera d’Ebre. Tarragona
C. Ruiz. Oficina de Farmacia. Gandesa. Tarragona
F. Paez. Hospital Comarcal Móra d’Ebre. Tarragona
- A.
Alvarez-Saz. Oficina de Farmacia. Berga. Barcelona
M. Cosp-Boixader. Oficina de Farmacia. Berga. Barcelona
D. Cosp-Sitges. Oficina de Farmacia. Berga. Barcelona
J. Badia. Oficina de Farmacia. Berga. Barcelona
M. I. Boixeda. Oficina de Farmacia. Borredà. Barcelona
C. Palau. Oficina de Farmacia. Cercs. Barcelona
L. Guillen. Oficina de Farmacia. Vilada. Barcelona
J. Vilades. Oficina de Farmacia. Guardiola del Berguedà. Barcelona
R. Cascante. Oficina de Farmacia. Bagà. Barcelona
M.T. Anfruns. Oficina de Farmacia. La Pobla de Lillet. Barcelona
J. Costa. Oficina de Farmacia. Saldes. Barcelona
L. Barniol. Oficina de Farmacia. Gironella. Barcelona
M. T. Bovet. Oficina de Farmacia. Gironella. Barcelona
M. C. Raich. Oficina de Farmacia. Gironella. Barcelona
M. Pico. Oficina de Farmacia. Puigreig. Barcelona
R.M. Bertran. Oficina de Farmacia. Puigreig. Barcelona
M. Estivill. Oficina de Farmacia. Casserres. Barcelona
M. R. Ferrer. Oficina de Farmacia. Olvan. Barcelona
M. Q. Gorgas. Hospital Comarcal Sant Bernabé. Berga. Barcelona
E. Baró. Hospital Comarcal Sant Bernabé. Berga. Barcelona
L. Robert. Hospital Comarcal Sant Bernabé. Berga. Barcelona
C. Rovira. Farmacéutica Atención Primaria. Berga. Barcelona
M. Andion. Oficina de Farmacia. Lérida
C. Pratdepadua. Oficina de Farmacia. Alpicat. Lérida
J. A. Schoenenberger. Hospital Universitario Arnau de Vilanova. Lérida
B. Terricabras. Oficina de Farmacia. Vic. Barcelona
M. Autonell. Oficina de Farmacia. Taradell. Barcelona
J. Bardolet. Oficina de Farmacia. Torelló. Barcelona
B. Nofre. Oficina de Farmacia. Torelló. Barcelona
E. Homs. Consorci Sanitari de Vic. Barcelona
M. T. Casajuana. Consorci Sanitari de Vic. Barcelona
G. Valdés. Farmacéutica Atención Primaria. Vic. Barcelona
M. J. Goñi. Oficina de Farmacia. La Bisbal. Gerona
J. Suñer. Oficina de Farmacia. Palafrugell. Gerona
L. Presas. Oficina de Farmacia. Palafrugell. Gerona
J. Massaneda. Oficina de Farmacia. Palamós. Gerona
I. Olivé. Oficina de Farmacia. Sant Feliu de Guixols. Gerona
J. Camós. Hospital Comarcal de Palamós. Gerona
T. Ball-llosera. Hospital Comarcal de Palamós. Gerona
M. Cols. Farmaceutica Atención Primaria. Palamós. Gerona
J. L. Juste. Oficina de Farmacia. El Vendrell. Tarragona
J. Rovira. Oficina de Farmacia. El Vendrell. Tarragona
V. Bueno. Oficina de Farmacia. El Vendrell. Tarragona
P. Parras. Oficina de Farmacia. El Vendrell. Tarragona
C. Gracia. Oficina de Farmacia. Calafell. Tarragona
P. Jolonch. Hospital Sant Pau i Santa Tecla. Tarragona
C. Gomez Blasco. Hospital del Vendrell. Tarragona
N. Gotanegra. Farmacéutica Atención Primaria. El Vendrell. Tarragona
M. Saurí. Oficina de Farmacia. Llagostera. Gerona
J. Saurí. Oficina de Farmacia. Llagostera. Gerona
A. Bonmatí. Oficina de Farmacia. Anglès. Gerona
E. de Puig. Parc Hospitalari Martí Julià. Gerona
M. Perpinyà. Parc Hospitalari Martí Julià. Gerona
C. Codina. Hospital Clínico. Barcelona