Sr. Director:
La leucoencefalopatía posterior reversible (LPR) es una alteración del sistema nervioso central que afecta fundamentalmente a la sustancia blanca de los lóbulos parietales y occipitales1. Se presenta tanto en adultos como niños y su etiopatogenia no es claramente conocida, aunque parece estar relacionada con una alteración de la autorregulación sanguínea cerebral con vasodilatación y edema. Las causas más frecuentes que pueden producir este síndrome son: encefalopatía hipertensiva, eclampsia, insuficiencia renal, alteraciones del colágeno, púrpura trombocitopénica trombótica, porfiria, sida, inmunosupresores y fármacos citotóxicos. Numerosos fármacos, como ciclosporina, interferón alfa, inmunoglobulinas intravenosas, cisplatino o tacrolimus, se han relacionado con la aparición de este síndrome. El tacrolimus es un inmunosupresor con estructura tipo macrólido, que actúa suprimiendo las respuestas inmunitarias tanto de tipo humoral como las mediadas por células. Está indicado en la profilaxis del rechazo del trasplante en receptores de aloinjertos hepáticos, renales o cardíacos y en el tratamiento del rechazo de aloinjertos resistentes al tratamiento con otros inmunosupresores. Presenta un gran número de reacciones adversas; las más frecuentes son: gastrointestinales (diarrea, náuseas), neurológicas (dolor de cabeza, temblor), insuficiencia renal, hiperglucemia e hipertensión. La mayoría de ellas suelen ser reversibles y/o responden a la reducción de la dosis.
Describimos el caso de una paciente con trasplante renal que presentó un episodio de leucoencefalopatía posterior reversible tras recibir dosis altas de tacrolimus.
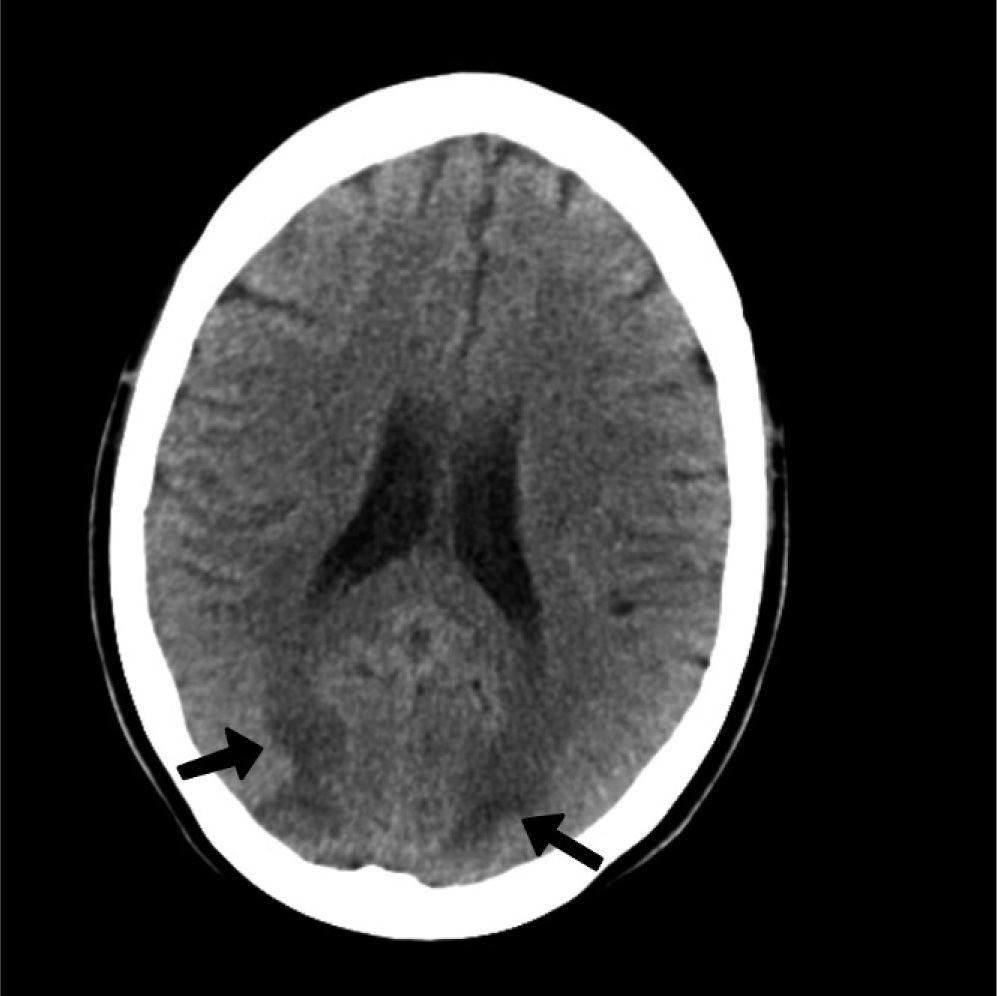
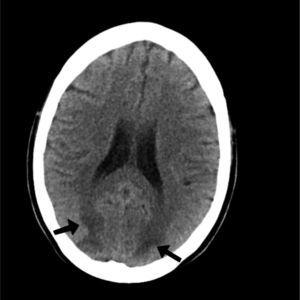
Mujer de 22 años, de 52 kg de peso, con antecedentes de trasplante renal en el año 2004, en tratamiento con tacrolimus (FK), micofenolato de mofetilo (MMF), prednisona y basiliximab, que ingresó en nefrología por un cuadro de astenia y vómitos. En la analítica presentó valores de FK y MMF de 2 y 0,18 ng/ml, respectivamente (intervalo terapéutico de FK, 5-15 ng/ml, y MMF, 1-6 ng/ml), y creatinina sérica de 3,2 mg/dl, por lo que se decidió realizar una biopsia renal ante la sospecha de un probable rechazo agudo por un abandono del tratamiento inmunosupresor. Ante este cuadro, se decidió iniciar sesiones de hemodiálisis y tratamiento intravenoso con metilprednisolona 1 g/día, micofenolato de mofetilo 1 g/12 h y tacrolimus 3 mg en perfusión continua cada 24 h. En los días posteriores, los valores de FK y MMF fueron de 8 y 2,7 ng/ml, respectivamente, y se decidió el cambio de tacrolimus a vía oral a dosis de 8 mg/12 h (0,3 mg/kg/día). El resultado de la biopsia fue compatible con rechazo agudo de categoría 3 de la clasificación de Banff con signos de necrosis tubular en vías de reparación. Después de 5 días, presentó un episodio de ceguera brusca y crisis tonicoclónicas que no cedieron con diazepam, por lo que se decidió su ingreso en la unidad de cuidados intensivos, donde precisó intubación orotraqueal y conexión a ventilación mecánica por bajo nivel de conciencia. Tras estabilizar a la paciente, se realizó una tomografía computarizada (TC) craneal urgente, donde se observaron hipodensidades subcorticales bilaterales en ambos lóbulos occipitales (fig. 1), y una punción lumbar, con parámetros dentro de la normalidad. Ante la sospecha de la posible etiología del cuadro, se solicitaron concentraciones de tacrolimus que resultaron ser de 46 ng/ml. Tras este hallazgo, y ante la inminente intoxicación por este fármaco, se decidió retirar el tacrolimus y mantener la terapia inmunosupresora con corticoides y micofenolato de mofetilo, con control estricto de los valores y manteniéndolos dentro de intervalos terapéuticos.
A las 72 h, la paciente recuperó totalmente el nivel de conciencia sin presentar ninguna focalidad ni nuevas crisis convulsivas. Transcurridos 7 días del cuadro agudo convulsivo, se realizó una resonancia magnética (RM) craneal donde se observó la desaparición completa de las hipodensidades occipitales. La paciente fue diagnosticada finalmente de leucoencefalopatía posterior reversible inducida por altas concentraciones de tacrolimus.
La fisiopatología de la LPR en pacientes con tratamiento inmunosupresor es controvertida, pero parece tener relación con numerosos factores de riesgo, entre los que se encuentran las concentraciones elevadas del fármaco inmunosupresor. En nuestra paciente, la administración de dosis más elevadas, el deterioro de la función renal y la escasa monitorización terapéutica llevaron a unos valores de tacrolimus de 46 ng/ml, lo que supuso 3 veces más que el límite superior del intervalo terapéutico considerado eficaz y seguro.
La clínica característica de este cuadro incluye cefalea, náuseas, vómitos, alteraciones visuales, crisis convulsivas y disminución del nivel de conciencia, que incluso puede llevar al coma y producir la muerte en algunas ocasiones1,2. El diagnóstico se basa en la clínica y en las pruebas de imagen craneales. La TC suele ser la primera prueba por su disponibilidad y porque permite detectar hipodensidades en las zonas cerebrales posteriores. La RM, que posee una mayor resolución, ayuda en el diagnóstico diferencial con entidades como accidentes isquémicos cerebrales, trombosis venosas, síndrome de obstrucción de la arteria basilar o cuadros de encefalitis y enfermedades desmielinizantes1.
El tratamiento de esta entidad requiere tanto el control de los síntomas como del mecanismo causal sospechado. La característica fundamental es una completa reversibilidad clínica y radiológica, en nuestro caso, comprobada con RM. Tras la revisión bibliográfica se encontraron casos similares de LPR en relación con el tratamiento con tacrolimus3-5 y uno en relación con otro inmunosupresor, el sirolimus6. En todos ellos la descripción y la evolución fue similar a la de nuestra paciente, en que la clínica desapareció tras la retirada de los fármacos. En un caso recientemente publicado3, se habla de un paciente que desarrolló LPR, en el contexto de un trasplante hepático, 7 meses después de comenzar tratamiento inmunosupresor y que mantuvo siempre valores dentro del intervalo terapéutico. En cambio, nuestra paciente desarrolló LPR tras alcanzar valores altos de FK en relación con dosis altas empleadas para el tratamiento del rechazo agudo de un trasplante renal.
El algoritmo de causalidad de Naranjo estableció como "probable" la relación entre tacrolimus y LPR. Este hecho, unido a que la retirada del fármaco supuso la reversión del cuadro, pone de manifiesto su posible implicación como causa "probable" de la leucoencefalopatía posterior reversible.
Por lo tanto, la terapia inmunosupresora no sólo requiere un cumplimiento riguroso por parte del paciente, sino que, además, es necesario una monitorización farmacocinética y farmacoterapéutica estrecha para evitar, en lo posible, sus posibles efectos adversos y complicaciones. Esta reacción adversa fue notificada al Sistema de Farmacovigilancia mediante la tarjeta amarilla.