INTRODUCCIÓN
El cáncerde mama es el tumor con mayor prevalencia en las mujeres;así pues, se considera que una de cada ocho mujeres enEstados Unidos desarrollará un cáncer de mama a lolargo de su vida. No obstante, se han logrado avances importantesque han permitido prolongar la supervivencia de estos pacientes,fundamentalmente mediante la puesta en marcha de programaspreventivos. De este modo, la realización de cribadosmediante mamografías sobre la población de riesgo hafacilitado la detección de los tumores en estadios inicialesy su diagnóstico precoz, mejorando las posibilidadesterapéuticas. Además, el mayor conocimiento de subiología molecular y el desarrollo de quimioterapiasadyuvantes más potentes incrementan las expectativasfavorables en este grupo de pacientes. Sin embargo, laevolución y tratamiento del carcinoma metastásico demama (CMM) está condicionado por su elevadaproporción de recidivas, su resistencia a los agentesantineoplásicos y su facilidad para desarrollarmetástasis (1, 2).
El tratamientoquimioterápico se basa en combinaciones de diferentesfármacos que han demostrado una mayor frecuencia derespuestas objetivas en el tratamiento del CMM. Actualmente seestán utilizando esquemas basados en la combinaciónde antraciclinas, principalmente la doxorubicina, conciclofosfamida, fluorouracilo o metotrexato. La instauracióndel tratamiento quimioterápico se realiza cuando el pacientepresenta un tumor diseminado o metatásico, la terapiahormonal ha fracasado o el tumor es receptor hormonal negativo. Sinembargo, no existe un esquema quimioterápico deelección claramente definido. Actualmente se considerantratamientos de elección o de primera línea losesquemas FAC (fluorouracilo/adriamicina/ciclofosfamida), AC(adriamicina/fluorouracilo), AC(fluorouracilo/epirrubicina/ciclofosfamida) o el CMF(ciclofosfamida/metotrexato/fluorouracilo). Cuando tras laadministración de la quimioterapia de primera líneano se alcanza la respuesta esperada o aparecen resistencias sepuede optar, dependiendo del estado clínico del paciente,por otras combinaciones quimioterápicas (esquemas de segundalínea) (1-4).
El paclitaxel yel docetaxel son dos nuevos agentes antineoplásicospertenecientes al grupo de los taxanos. Ambos fármacospresentan unas características similares en cuanto a sumecanismo de acción y espectro de actividad,observándose una elevada efectividad en el tratamiento delcáncer de mama, lo que ha permitido su implantaciónen diferentes esquemas de tratamiento (5).
No obstante,además de la efectividad y seguridad de un fármaco,su implantación en el sistema sanitario debe abordarse desdela óptica de su eficiencia, es decir, a la evidencia sobresu eficacia y seguridad debe acompañarle un coste soportablepara los actuales estamentos sanitarios.
Elobjetivo de este estudio es realizar un análisiscoste-efectividad comparativo entre el paclitaxel y el docetaxel enel tratamiento del CMM.
MÉTODO
Búsqueda bibliográfica
Serealizó una búsqueda bibliográfica mediante labase de datos MEDLINE (Index Medicus, National Library of Medicine,Bethesda, Estados Unidos) en soporte óptico CD-ROM (SilverPlatter Information Inc, Norwood, Bethesda, Estados Unidos) desdeenero de 1995 hasta julio de 1999. Las palabras claves empleadasfueron paclitaxel, docetaxel metastatic breastcancer, así como su acrónimo en inglésMBC. Las referencias citadas en los artículos seleccionadosy en otros trabajos de revisión fueron revisadas con objetode seleccionar aquellos artículos no identificados mediantela búsqueda informatizada, aumentando así lasensibilidad de la búsqueda bibliográfica. Lasreferencias se limitaron a aquellas publicadas en inglés oespañol. Se seleccionaron aquellos artículos queconsideraban la opción del paclitaxel y/o docetaxel comotratamiento en el carcinoma metastásico de mama como primerao segunda opción.
Para cadaartículo de revisión se identificaron las diferentesramas de tratamiento utilizado, seleccionándose aquellas quecumplían los criterios de selección de nuestroestudio.
Criterios deselección
Laselección de los estudios se realizó enfunción de aspectos metodológicos para reducirposibles sesgos de selección. Los criterios deinclusión de los artículos fueron:
-- Ensayosclínicos en paciente mayores de dieciocho añosdiagnosticados de carcinoma de mama metastásico.
--Administración de taxanos (paclitaxel o docetaxel) comopoliquimioterapia o monoterapia.
-- Pacientes conuna función medular, hepática y renal normal en elmomento de iniciarse el tratamiento con taxanos.
--Performance status según el WHO ¾ 2 oíndice de Karnofsky >= 60%.
Los criterios deexclusión fueron: casos clínicos, estudios enanimales, modelos de experimentación o cuando noproporcionase datos suficientes para su análisis.
Cuando losresultados de un ensayo clínico fueron publicados enmás de una ocasión se utilizó el estudiomás completo (mayor número de casos) y másreciente.
Análisis de los datos
Efectividad
La efectividaddel tratamiento se valoró como respuesta objetiva (RO),obtenida como la suma de la respuesta completa (RC),desaparición del tumor, y respuesta parcial (RP) odisminución de al menos el 50% del tamaño tumoralmedido como la suma de los productos de los mayoresdiámetros perpendiculares del tumor, sin evidencia de nuevaslesiones.
Los resultadosse obtuvieron según línea de tratamiento: primeralínea de tratamiento o tratamiento de elección ysegunda línea de tratamiento en pacientes tratadosanteriormente con otros esquemas quimioterápicos cuyaenfermedad progresó durante la administración de unesquema de primera línea o recidivaron durante la terapiaadyuvante. Posteriormente éstos se evaluaron según elesquema de los fármacos empleados, ya fuese en monoterapia oen poliquimioterapia.
Otro criterio deefectividad evaluado fue la mediana del tiempo paraprogresión de la enfermedad (IPE). Debido a que estosresultados no se recogen en la mayoría de los estudios, seobtuvieron de forma global (docetaxel frente a paclitaxel) y entremonoterapia frente a poliquimioterapia.
Análisis de costes
Se consideraronlos costes de adquisición de los agentes citotóxicosque componen los regímenes quimioterápicos,así como el material fungible empleado para sureconstitución y los costes de preparación. Loscostes obtenidos fueron por ciclo y para un total de seis ciclospor paciente.
Los esquemas dequimioterapia aplicados pueden presentar variaciones entresí. En el análisis básico para determinar loscostes en monoterapia se utilizaron los más habituales en lapráctica clínica de nuestro hospital, consistente enla administración de docetaxel 75 mg/m2 frente apaclitaxel 175 mg/m2 cada veintiuno-veintiochodías. Posteriormente en el análisis de sensibilidadse consideraron las distintas pautas de dosificación y surepercusión en el índicecoste-efectividad.
Losfármacos empleados en los diferentes esquemas depoliquimioterapia asociados a los taxanos es variable. Por ello laevaluación inicial de los costes se realizó medianteuna estimación del valor medio obtenido a partir de loscostes individuales de los diferentes esquemasempleados.
Los costes delos diferentes fármacos se obtuvieron a partir de los PVL(precio venta laboratorio). Los principios activos y especialidadesfarmacéuticas evaluadas fueron: paclitaxel(Taxol®) de 100 mg, docetaxel(Taxotere®) de 80 mg, gencitabina(Gemzar®), ifosfamida (Tronoxal®) de1 g, mesna (Uromitexan®) de 200 mg, cisplatino(Neoplatin®) de 50 mg, adriamicina(Farmiblastina®) de 50 mg, epirrubicina(Farmirrubicina®) de 50 mg, folinato cálcico(Folidan®) de 350 mg, vinorelbina(Navelbina®) de 50 mg y 5-FU(Fluorouracil®) en ampollas de 250 mg. Los costes depersonal fueron convertidos en unidades de coste a partir de losdatos proporcionados por el SIE de la Comunidad Valenciana(6).
Análisis farmacoeconómico
Elanálisis farmacoeconómico se realizó desde unaperspectiva hospitalaria y con la preparación de loscitostáticos desde la unidad de mezclas intravenosas. Porello no se evaluaron los costes asociados a la caducidad de losviales abiertos ante la posibilidad de poder utilizarlos para otropaciente durante el mismo día.
Se determinaronlos siguientes índices para cada uno de losparámetros de efectividad:
--Coste-efectividad (C/E) de cada esquemaquimioterápico.
--Coste-efectividad incremental.
Análisis de sensibilidad
La consistenciade las conclusiones obtenidas se evaluó mediante larealización de un análisis de sensibilidad. Lasvariables estudiadas fueron:
1.Variación en los costes
-- Aumento delos costes de los esquemas con monoterapia.
-- Aumento delos costes de los esquemas con poliquimioterapia.
--Modificación en la duración de los tratamientos ynúmero de ciclos administrados según el tiempo deprogresión (TPE).
-- Incremento enel coste asociado al tratamiento de la toxicidad
2.Variación de la efectividad. Se consideró unaumento del 10% en la opción considerada menosefectiva.
3.Variación de la relación coste/efectividadpara los diferentes esquemas de poliquimioterapia.
Análisis estadístico
Elánálisis estadístico de la efectividad porcategorías se realizó mediante un análisis devarianza de una vía (ANOVA). Cuando la prueba unilateral Fde Snédecor es significativa se aplicó el test decomparaciones múltiples de Tukey. Las diferencias seconsideraron estadísticamente para valores de p ¾0,01. Todos los resultados obtenidos fueron ponderados por elnúmero de pacientes.
RESULTADOS
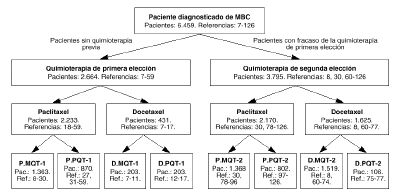
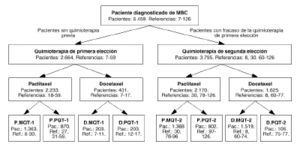
Se seleccionaron119 artículos que evaluaban la efectividad de los taxanos enpacientes con CMM y cumplían los criterios deinclusión anteriormente citados. Los ensayos evaluadosengloban un total de 6.459 pacientes. La figura 1 recoge los diferentes trabajos incluidosen el estudio, así como el número de pacientes,línea de tratamiento y tipo de esquema.
Figura 1.--Resultado de la búsquedabibliográfica, clasificada según fármaco,línea, tipo quimioterapia, referencia y número depacientes. D.MQT-1: docetaxel en monoterapia de primeraelección. D.PQT-1: docetaxel en poliquimioterapia de primerelección. P.MQT-1: paclitaxel en monoterapia de primeraelección. P.PQT-1: paclitaxel en poliquimioterapia deprimera elección. D.MQT-2: docetaxel en monoterapia desegunda elección. D.PQT-2: docetaxel en poliquimioterapia desegunda elección. P.MQT-2: paclitaxel en monoterapia desegunda elección. P.PQT-2: paclitaxel en poliquimioterapiade segunda elección. Pac.: pacientes. Ref.: número dereferencias.
En las tablas 1 y 2 se muestran los costes de losdiferentes esquemas, tanto en monoterapia como enpoliquimioterapia, en los que participan tanto el paclitaxel comoel docetaxel. El principal factor que determina el coste en losesquemas de poliquimioterapia, tanto para el paclitaxel como parael docetaxel, es el coste de adquisición de los taxanos, yaque en la mayoría de los casos éste supera el 90% delcoste total del esquema.
Tabla 1. Análisis de costes. Resultado de los costesde los diferentes esquemas con paclitaxel calculados para unasuperficie corporal de 1,7 m y por ciclo | ||||
| Esquema | Composición | Coste porciclo(1,7 m2) | Coste relativo | |
| Paclitaxel | Paclitaxel: 135-175-250mg/m2 | 163.222*-211.500-301.920 | 1-1,29-1,85 | |
| Paclitaxel/adriamicina | Paclitaxel: 175-250mg/m2 | 222.488-313.269 | 1,36-1,91 | |
| Adriamicina: 60mg/m2 | (95)-(96) | |||
| Paclitaxel/epirrubicina | Paclitaxel: 175mg/m2 | 231.055 | 1,41 | |
| Epirrubicina: 60mg/m2 | (92) | |||
| Paclitaxel/cisplatino | Paclitaxel: 90-135mg/m2 | 117.973-174.504 | 0,7-1,06 | |
| Cisplatino: 60-75mg/m2 | (92)-(93) | |||
| Paclitaxel/vinorelbina | Paclitaxel: 135mg/m2 | 173.908 | 1,06 | |
| VNR: 25 mg/m2 | (94) | |||
| Paclitaxel/5-FU | Paclitaxel: 175mg/m2 | 226.534-226.860 | 1,38-1,39 | |
| 5-FU: 1.500-2.000mg/m2 | (93)-(93) | |||
| Paclitaxel/5FU/AF | Paclitaxel: 75mg/m2 | 234.081 | 1,43 | |
| 5-FU: 350 mg/m2 (tresdías) | (90) | |||
| AF: 300 mg (tresdías) | ||||
| Paclitaxel/ciclofosfamida | Paclitaxel: 135-175mg/m2 | 169.100-212.378 | 1,03-1,30 | |
| Ciclofosfamida: 750mg/m2 | (96)-(99) | |||
Coste medio poliquimioterapia por ciclo: 209.285 pesetas. ( ):porcentaje del coste de cada esquema que corresponde a laadministración de paclitaxel. *: coste considerado dereferencia (correspondiente a paclitaxel: 135 mg/m2)para determinar los costes relativos de los diferentesesquemas. | ||||
Tabla 2. Análisis de coste. Resultado de los costes delos diferentes esquemas con docetaxel. Calculados para unasuperficie corporal de 1,7 m2y porciclo | ||||
| Fármaco | Esquema | Coste porciclo(1,7 m2) | Costerelativo | |
| Docetaxel | Docetaxel: 60-75-100mg/m2 | 121.140*-151.477-201.875 | 1-1,25-1,67 | |
| Docetaxel/adriamicina | Docetaxel: 60-75mg/m2 | 132.127-160,574 | 1,09-1,32 | |
| Adriamicina: 60-50mg/m2 | (91)-(94) | |||
| Docetaxel/vinorelbina | Docetaxel: 60 mg/m2 | 129.818 | 1,07 | |
| Vinorelbina: 20mg/m2 | (93) | |||
| Docetaxel/gencitabina | Docetaxel: 100mg/m2 | 229.840 | 1,89 | |
| Gencitabina: 900mg/m2 | (88) | |||
| Docetaxel/5-FU | Docetaxel: 60 mg/m2 | 136.260 | 1,12 | |
| 5-FU: 1.500 mg/m2 | (89) | |||
| Docetaxel/5-FU | Docetaxel: 40-60mg/m2 | 81.503-123.010 | 0,67-1,01 | |
| 5-FU: 150-500 mg/m2 (cincodías) | (99)-(98) | |||
Coste medio poliquimioterapia por ciclo: 141.876 pesetas. ( ):porcentaje del coste de cada esquema que corresponde a laadministración de docetaxel. *: coste considerado dereferencia (correspondiente a docetaxel: 60 mg/m2) paradeterminar los costes relativos de los diferentesesquemas. | ||||
El coste mediode la poliquimioterapia con paclitaxel es de 209.286 pesetas, y condocetaxel, de 141.876 pesetas por ciclo y paciente (s.c.: 1,7m2).
En la tabla 3 se muestran los resultados deefectividad, medidos como respuesta, ya sea objetiva, completa yparcial, según las diferentes posibilidades y líneasde tratamiento. Las comparaciones se han realizado entre aquellosesquemas considerados similares (paclitaxel frente a docetaxel enmonoterapia y en poliquimioterapia). Los resultados obtenidosmuestran diferencias, estadísticamente significativas, alevaluar RO en primera línea (60,89 frente a 65,16 parapaclitaxel y docetaxel, respectivamente). La principal diferenciase observa en la administración de poliquimioterapia,obteniéndose un índice de respuestas objetivas entratamiento de primera línea del 78,31% frente al 63,88%para los esquemas constituidos con docetaxel y paclitaxel,respectivamente.
| Tabla 3. Resultados deefectividad. Respuesta objetiva, respuesta parcial y respuestacompleta, observadas para cada una de las diferentesopciones | |||||||||
| Respuestaobjetiva | Respuestaparcial | Respuestacompleta | |||||||
| Paclitaxel | Docetaxel | p | Paclitaxel | Docetaxel | p | Paclitaxel | Docetaxel | p | |
| Primera línea. | 60,89 | 65,16 | p < 0,01 | 46,9 | 55,84 | p < 0,01 | 14,03 | 9,32 | p < 0,01 |
| (59,85-61,93) | (63,98-66,34) | (46,18-47,66) | (54,45-57,23) | (13,35-14,71) | (8,66-9,97) | ||||
| MT. Primera línea | 50,6 | 57,95 | p < 0,01 | 42,36 | 48,57 | p < 0,01 | 8,24 | 9,37 | NS |
| (48,84-52,36) | (57,11-58,78) | (40,92-43,8) | (47,59-49,56) | (7,55-8,93) | (8,84-9,91) | ||||
| PQT. Primera línea | 63,88 | 78,31 | p < 0,01 | 48,03 | 69,08 | p < 0,01 | 15,43 | 9,22 | p < 0,01 |
| (62,76-65,00) | (77,44-79,17) | (47,19-48,68) | (67,05-71,11) | (14,63-16,24) | (7,36-10,8) | ||||
| Segunda línea | 36,44 | 40,19 | p < 0,01 | 30,16 | 35,50 | p < 0,01 | 6,30 | 4,68 | p < 0,01 |
| (35,75-37,13) | (39,47-40,90) | (29,60-30,73) | (34,93-36,07) | (6,01-6,59) | (4,47-4,90) | ||||
| MT. Segunda línea | 29,56 | 39,41 | p < 0,01 | 25,05 | 35,24 | p < 0,01 | 4,5 | 4,17 | NS |
| (28,92-30,20) | (38,67-40,15 | (24,47-25,62) | (34,63-35,85) | (4,26-4,75) | (3,98-4,36) | ||||
| PQT. Segundalínea | 47,20 | 48,22 | NS | 38,3 | 38,18 | NS | 9,16 | 10,03 | NS |
| (46,14-48,26) | (46,03-50,41) | (37,42-39,19) | (36,71-39,66) | (8,56-9,75) | (9,15-10,90) | ||||
| Los resultados se expresancomo porcentajes con su intervalo de confianza para cada una de lasalternativas, así como la significaciónestadística observada. NS: diferenciasestadísticamente no significativas. | |||||||||
Se observandiferencias estadísticamente significativas entre losdiferentes esquemas cuando se determina la RO en tratamientos desegunda línea, excepto entre D.PQT-2 y P.PQT-2. Las mayoresdiferencias se observan entre los esquemas con monoterapia (29,56%para el pacliaxel frente al 39,41% en el docetaxel).
Se hadeterminado un mayor porcentaje de RP tras la administraciónde esquemas que contienen docetaxel, obteniéndosediferencias estadísticamente significativas favorables entodos los casos, excepto cuando se compara D.PQT-2 frente aP.PQT-2. Estas diferencias se hacen más notorias cuando secomparan los esquemas con poliquimioterapia como tratamientos deprimera elección (paclitaxel: 48,03%; docetaxel: 69,08%), yentre los esquemas de monoterapia como tratamientos de segundaelección (paclitaxel: 25,05%; docetaxel: 35,24%). Se haobservado un mayor porcentaje de RC en tratamiento de primeraelección tras la administración de los esquemas quecontienen paclitaxel (14,03 frente a 9,32). Esta diferencia vienedeterminada por la mayor efectividad observada en los esquemas deP.PQT-1 frente al D.PQT-1 (15,43 frente a 9,22).
El porcentaje deRC obtenido tras la administración de los tratamientos desegunda línea es de 6,30 y 4,68 para el paclitaxel ydocetaxel, respectivamente. Sin embargo, no se han observadodiferencias entre D.MQT-2 frente a P.MQT-2 y entre D.PQT-2 yP.PQT-2.
En la tabla 4 se muestra los TPE obtenidos paracada una de las opciones. Sin embargo, en muchos de losartículos revisados este factor no se evaluó. Debidoa la reducida validez externa que se obtendría al evaluar elTPE según la línea de tratamiento sólo seobtuvieron los resultados en monoterapia, poliquimioterapia yglobal (monoterapia + poliquimioterapia), apareciendo diferenciasestadísticamente significativas en todos los casos. Eldocetaxel presentó TPE superiores, tanto en monoterapia(18,20 frente a 16,85) como en poliquimioterapia (42,58% frente a37,85%). No obstante, se observa un TPE superior para el paclitaxelcuando nos referimos a los resultados de forma global (21,89 frenteal 19,74); esta aparente contradicción se debefundamentalmente a la diferencia en el número de pacientesevaluados en cada una de las diferentes opciones.
| Tabla 4. Resultados de efectividad. Tiempo deprogresión (semanas) | ||||
| Tiempo paraprogresión (semanas) | ||||
| Paclitaxel | Docetaxel | p | ||
| Global | 21,89 | 19,74 | p < 0,01 | |
| (20,77-21,81)* | (19,21-20,26) | |||
| 1.630** | 1.444 | |||
| Monoterapia | 16,85 | 18,20 | p < 0,01 | |
| (16,6-17,1) | (17,79-18,61) | |||
| 1.286 | 1.351 | |||
| Poliquimioterapia | 37,85 | 42,58 | p < 0,01 | |
| (36,81-38,99) | (40,1-45,06) | |||
| 344 | 93 | |||
| Los resultados se expresan ensemanas, así como la significación estadísticaobservada. *: intervalo de confianza para cada una de lasalternativas. **: número de pacientes. | ||||
En la tabla 5 se muestra el resultado del estudiocoste-efectividad. Se han clasificado los resultados segúnla unidad de medida de la efectividad, comparándose laopción de referencia (definida como máseconómica) frente al resto de opciones existentes, tanto enmonoterapia como poliquimioterapia. Los resultados reflejan que laopción de poliquimioterapia con docetaxel (D.PQT-1 yD.PQT-2) es la opción de referencia en la mayoría delos casos, siendo también la que presenta una mejorrelación coste-efectividad debido a su menor coste y a suelevada efectividad. Al considerar la efectividad en lostratamientos de primera elección como RC, la eleccióndel tratamiento P.PQT-1 supondría un incremento de 6.513.075pesetas por unidad de efectividad respecto al D.PQT-l.
Tabla 5. Resultados del estudio farmacoeconómico.Cálculo de la relación coste-efectividad y costeefectividad incremental | |||||||
| Respuesta objetiva | Respuesta parcial | Respuesta completa | |||||
| Coste | Coste/efectividad | Coste/efectividad | Coste/efectividad | ||||
| Primera línea | |||||||
| --D. MQT-1 | 908.862 | 1.568.355 | NP | 1.871.241 | NP | 9.699.701 | NP |
| --D. PQT-1 | 851.256 | 1.087.033 | Referencia | 1.232.275 | Referencia | 9.232.711 | Referencia |
| --P. MQT-1 | 1.269.000 | 2.507.905 | NP | 2.995.750 | NP | 15.400.485 | NP |
| --P. PQT-1 | 1.255.718 | 1.965.744 | NP | 2.614.445 | NP | 8.138.159 | 6.513.075* |
| Segunda línea | |||||||
| --D. MQT-2 | 908.862 | 2.306.171 | NP | 2.579.063 | NP | 21.795.251 | NP |
| --D. PQT-2 | 851.256 | 1.765.358 | Referencia | 2.229.586 | Referencia | 8.487.098 | Referencia |
| --P. MQT-2 | 1.269.000 | 4.292.963 | NP | 5.065.868 | NP | 28.200.000 | NP |
| --P. PQT-2 | 1.255.718 | 2.660.419 | NP | 3.278.637 | NP | 13.708.711 | NP |
| Referencia: es la opción considerada de referenciapor ser económicamente más rentable,independientemente de su efectividad. NP: no procede realizar elanálisis C/E, ya que dicha opción eseconómicamente más cara y con una efectividad igual oinferior a la considerada de referencia. *: incremento del costepor unidad de efectividad que supondría elegir dichaopción respecto a la considerada de referencia. Todos losparámetros se han determinado para 100 individuos (coste yefectividad). | |||||||
Análisis de sensibilidad
Variación de los costes
Variación del coste de los esquemas enmonoterapia
Para elcálculo de los costes de los esquemas de monoterapia se hanescogido las dosis intermedias de 75 mg/m2 para eldocetaxel y de 175 mg/m2 para el paclitaxel al serpautas realistas, conservadoras y de amplia utilización ennuestro centro hospitalario. Partiendo de esta base, los costes detratamiento para D.MQT y P.MQT son, respectivamente, 908.862 y1.269.000 pesetas por paciente. Para que el coste de ambos esquemasfuese similar la dosis de docetaxel se debería incrementar30 mg/m2 (aproximadamente el 40% de la dosis), hastaalcanzar una dosis de 105 mg/m2 (la dosis máximaobservada en los artículos revisados es de 100mg/m2 por ciclo). Esta pauta supondría un costede 1.270.000 pesetas, por lo que en este caso, desde el punto devista económico, ambos esquemas serían similares y elparámetro de coste no influiría en lavaloración comparativa de ambos esquemas, siendo el factordeterminante la efectividad.
Otra posibilidadsería disminuir el coste de los esquemas de P.MQT hastaconverger con el de D.MQT. En este caso se tendría quereducir un 30% la dosis de paclitaxel hasta alcanzar una pauta dedosificación de 125 mg/m2, siendo el costeatribuible de 905.250 pesetas. Esta dosificación en P.MQT essensiblemente inferior a la encontrada en la mayoría de losestudios revisados, así como a la utilizada en nuestrocentro para esta indicación.
En ambos casosse considera que no existe variación de efectividad almodificar la dosis, por lo que se mantendría la preferenciadel esquema D.MQT frente al P.MQT como las más efectiva. Laefectividad en los tratamientos de segunda línea, medidacomo RC, sería similar entre ambas opciones.
Aumento en elnúmero de ciclos
En este estudiose ha considerado el mismo número de ciclos para ambosesquemas, independientemente de la línea de tratamiento. Sinembargo, la realidad puede ser diferente. Así pues, serecomienda la administración de quimioterapia hasta que seobserve progresión de la enfermedad (TPE) o, en algunoscasos, hasta que aparece la primera respuesta.
En nuestroestudio el TPE es superior para el D.PQT (42,58 frente a 37,85semanas), aunque los resultados globales no muestran diferenciasclínicamente significativas. Por otra parte, la frecuenciade administración de ambos esquemas es deveintiuno-veintiocho días; por tanto, al considerar el TPE,a los pacientes con D.PQT se les podría administrar, enprincipio, un ciclo más. En este caso el coste por pacientesería de 1.060.339 pesetas, manteniéndosetodavía como la opción más rentable desde elpunto de vista económico (independientemente de laefectividad atribuible). Para que se igualasen costes entre las dosopciones debería obtenerse una variación en el TPEpara el docetaxel superior a las seis a ocho semanas, dependiendode la frecuencia de administración e independientemente delposible incremento de efectividad.
Aumento en elcoste de la poliquimioterapia
Los costescalculados para D.PQT y P.PQT son costes medios obtenidos a partirde los costes individualizados para cada uno de los diferentesesquemas revisados. Por este motivo la particularización enuno de estos esquemas puede llevar consigo la obtención deunos costes más favorables respecto al valor medioconsiderado. Éste es el caso del paclitaxel/cisplatino, querepresenta entre el 83-56% del coste medio de lapoliquimiotera-pia, según las dosis elegidas, y elpaclitaxel/vinorelbina, que representa el 83% del mismo. Losesquemas de paclitaxel que sobrepasan el coste del P.PQT calculado(1.255.718 pesetas) son paclitaxel/adriamicina (incremento en elcoste entre el 6-49%, según dosis), paclitaxel/epirrubicina(incremento del 10%), paclitaxel/5-FU a altas dosis (incremento del12%). Las combinaciones de paclitaxel/5-FU a bajas dosisrepresentan entre el 81-100% del coste medio obtenido para lapoliquimioterapia.
Laelección del esquema D.PQT-l frente al esquema paclitaxel 90mgm2/cisplatino 60 mg/m2 (esquema máseconómico con paclitaxel, con un coste de 707.838 pesetas)en tratamiento de primera elección supondría un costeincremental entre 993.887 y 681.320 pesetas por unidad extra deefectividad para la RO y RP, respectivamente.
El esquemapaclitaxel 90 mg/m2/cisplatino 60 mg/m2 seconsideraría de referencia en los tratamientos de segundaelección, independientemente de la unidad de efectividadutilizada o cuando la RC se utilice como modida de efectividad enlos tratamientos de primera elección.
En caso deldocetaxel, la particularización en un determinado esquematambién podrían hacer variar los costes consideradosen el análisis principal. Los esquemas formados porcombinación de docetaxel/adriamicina (dosis bajas),docetaxel/vinorelbina o docetaxel/ 5-FU reducen el coste de lapoliquimioterapia al 93, 92 y 57-86%, respectivamente, mientras queel esquema docetaxel/adriamicina a dosis elevadas supone unincremento del 13% en el coste de la D.PQT, que sigue siendomás económica que la alternativa conpaclitaxel.
Únicamente la combinación docetaxel/gencitabinaes más costosa que la P.PQT, por lo que la elecciónde esta pauta supondría recalcular los resultadosobtenidos.
Si se mantuviesela efectividad, las opciones con D.PQT debería considerarsede referencia en la mayoría de las ocasiones.
Coste detratamiento de la toxicidad
El costediferencial asociado al tratamiento de las reacciones adversas delpaclitaxel y docetaxel viene condicionado por sus diferentesperfiles toxicológicos.
La principaltoxicidad asociada a los esquemas con paclitaxel y docetaxel es lapresencia de neutropenia, aunque la frecuencia y gravedad de lamisma difieren según el tipo de taxano empleado. Eldocetaxel se asocia a neutropenias más graves y de menorduración. La frecuencia de aparición de neutropeniaen pacientes tratados con paclitaxel depende de la duraciónde la administración, siendo más habitual con lautilización de perfusiones de veinticuatro horas respecto alas perfusiones de tres horas.
El tratamientode la neutropenia presenta diversos planteamientosterapéuticos, desde la profilaxis con factores decrecimiento hematopoyético a todos los pacientes hasta laadministración sólo en los pacientes que desarrollencuadros neutropénicos. En el primer caso no seobservarán diferencias en los costes asociados al mismo,pues todos los pacientes recibirían dicho tratamiento. Elincremento de coste que se experimentaría en el segundo casovendrá determinado por la diferencia en la frecuencia deaparición de neutropenia con cada taxano. En los esquemascon paclitaxel la frecuencia de aparición de neutropenia porciclo oscila entre un 70-90% (127), mientras que con docetaxelvaría entre el 80-100% (1, 128). Así pues, ladiferencia entre ambos esquemas no supera el 20%. Por tanto, elcoste diferencial asociado al tratamiento de la neutropeniaserá, considerando la administración de 300µg/día, de G-CSF * diezdías, de 20.200 pesetas por ciclo (121.200 pesetas portratamiento).
El mayorincremento en el coste de las opciones con docetaxel es debido altratamiento de la neutropenia febril, cuya frecuencia deaparición es del 12,5% para los esquemas con paclitaxelfrente al 22% en los esquemas con docetaxel (129). En estos casos,junto con la administración de los factores de crecimientohematopoyéticos, se recomienda la administración de(130): un aminoglucósido (por ejemplo, amikacina, 500mg/doce horas o 1 g/veinticuatro horas) más unbetalactámico antipseudomonas (por ejemplo, ceftazidima, 2g/ocho horas). Si se sospecha la presencia de estafilocos seaconseja añadir vancomicina (1 g/doce horas). Ante unaposible infección fúngica se debe utilizaranfotericina B. Además, el coste del tratamiento puedevariar, dependiendo de las posibles complicaciones existentes,así como por la mayor o menor duración del mismo.Así pues, para una media de diez días de tratamientoéste puede oscilar entre las 57.000 hasta las 113.900pesetas. A este valor habría que añadirle el costeasociado a
la estancia, que en nuestro centro es de 34.667 pesetas en la salade oncología (coste estancia medio en oncología sinel coste de farmacia) (6), obteniendo un gasto global entre 403.670a 460.570 pesetas. Por tanto, el coste diferencial, atribuible altratamiento con anibióticos, por paciente/ciclooscilaría entre 242.202-276.342 pesetas.
Teniendo encuenta el incremento de los costes atribuible al tratamiento confactores de crecimiento y con antibióticos para eltratamiento de la neutropenia febril, a los esquemas con docetaxelel coste final oscilaría entre 1.214.658 (D.PQT) y 1.272.264pesetas (D.MQT), similares a los obtenidos para el paclitaxel(1.269.000 y 1.255.000 pesetas para el P.MQT y P.PQT,respectivamente).
Así,cuando la efectividad se mide como RC en tratamiento de primeraelección, la elección de la mejor opcion conpaclitaxel (P.PQT) frente a la mejor opción con docetaxel(D.PQT), supondría un incremento del coste por unidad extrade efectividad de 649.629 pesetas. En el resto de casos laopción D.PQT se mantendría como la opciónmás coste-efectiva.
Otros efectosadversos que pueden observarse tras la administración de losdiferentes esquemas son retención hídrica en el casode docetaxel o presencia de cardiotoxicidad o neurotoxicidad en elcaso del paclitaxel (5, 128, 129). Sin embargo, larepercusión de los mismos sobre los costes totales no essignificativa. Así, mientras que el coste asociado altratamiento de la retención de fluidos es bajo(dexametasona), el incremento de los costes asociados altratamiento de la cardiotoxicidad y neurotoxicidad producidas porpaclitaxel se traduciría en una mayor diferencia de costesentre ambos esquemas a favor del docetaxel.
Variaciones en los resultados deefectividad
Aumento de un10% la efectividad del paclitaxel
Seconsideró un aumento del 10% en la efectividad del mejoresquema de paclitaxel (P.PQT) tanto para tratamientos de primeracomo de segunda línea. Así pues, la RO y RP fijada entratamiento de primera línea sería del 73,88 y del58,03%, respectivamente, siendo todavía inferior a losresultados obtenidos con la opción de referencia (D.PQT).Sin embargo, la frecuencia de RC ascendería al 25,43% frenteal 9,22% del D.PQT, por lo que la elección de la pauta conpaclitaxel supondría un incremento del coste por unidadextra de efectividad de 2.495.138 pesetas. La elección delesquema P.PQT-2 supondría una efectividad del 57,20, 48,3 y19,16% para la RO, RP y RC, respectivamente, lo quesupondría un incremento de coste por unidad extra deefectividad entre 3.996.660 y 4.504.031 pesetas según launidad de efectividad considerada.
Consideración de la efectividad y coste para undeterminado esquema de poliquimioterapia
Los datosempleados en el análisis principal son valores medios deefectividad, ponderados por el número de pacientes. Noobstante, los esquemas de poliquimioterapia tienen distintaefectividad. Los esquemas con paclitaxel que poseen una mayorefectividad son la combinación paclitaxel/antraciclinas(adriamicina o epirrubicina) y el paclitaxel/cisplatino. Laasociación docetaxel/antraciclinas es el esquema depoliquimioterapia con docetaxel de una mayor efectividad.Únicamente se han considerado en la particularizaciónde los esquemas aquellos que mostraban una efectividad superior osimilar a la media ponderada. Además éstosdebían haber sido revisados en dos o más ensayos(tabla 6).
Tabla 6. Esquemas de poliquimioterapia, tanto con docetaxelcomo con paclitaxel, que presentan una mayorefectividad | ||||||
| Tratamiento de primera elección | Tratamiento de segunda elección | |||||
| RO | RP | RC | RO | RP | RC | |
| Paclitaxel/antraciclinas* | 75,86 | 54,18 | 21,67 | 56,77 | 40,75 | 16,01 |
| (74,49-72,24) | (52,96-55,41) | (54,20-59,28) | (39,11-42,39) | (14,42-17,61) | ||
| Paclitaxel/adriamicina | 77,09 | 51,99 | 26,08 | 69,5 | 50,63 | 18,86 |
| (75,62-78,57) | (50,63-53,35) | (24,21-7,95) | (66,66-72,93) | (50,18-51,08) | (15,87-21,86) | |
| Paclitaxel/epirubicina | 71,03 | 61,52 | 9,50 | 47,7 | 33,76 | 14 |
| (67,6-74,43) | (59,3-63,7) | (8,3-10,64) | (46,8-48,6) | (33,02-34,36) | (12,38-5,6) | |
| Paclitaxel/cisplatino | 62,76 | 48,50 | 14,26 | 47,28 | 36,58 | 10,70 |
| (60,72-64,8) | (47,04-49,96) | (13,37-15,14) | (45,3-49,27) | (35,24-37,9) | (9,39-12,00) | |
| Docetaxel/antraciclina | 79,27 | 75,18 | 3,27 | NR | NR | NR |
| (78,39-80,15) | (73,27-77,09) | (2,63-3,90) | ||||
| *Engloba los resultados de los esquemaspaclitaxel/adriamicina y paclitaxel/epirrubicina. NR: no sedisponen de datos para este esquema como tratamiento de segundaelección. | ||||||
La efectividadde la combinación paclitaxel (90 mg/ m2) ycisplatino (60 mg/m2) es inferior a la observada con elD.PQT; sin embargo, supone un coste inferior al del docetaxel. Laelección de los esquemas con docetaxel supondría unincremento del coste por unidad de efectividad que oscilaríaentre 696.800-922.302 pesetas, según la unidad deefectividad considerada (RP y RO, respectivamente) en tratamientode primera línea. En el resto de situaciones el esquema deelección sería la combinación de paclitaxel ycisplatino, ya que ésta sería la opción dereferencia. Sin embargo, al considerar el mismo esquema a dosisaltas (paclitaxel: 135 mg/m2, y cisplatino: 75mg/m2) el coste del mismo sería de 1.047.024pesetas. Este coste es superior al obtenido para el docetaxel, conuna efectividad ligeramente inferior, por lo que el esquema deelección sería el de D.PQT.
Del mismo modoque se han evaluado los diferentes esquemas de paclitaxel, serealizó con el docetaxel, observándose mejoresresultados con la combinación de docetaxel y antraciclinas,con una RO del 79,27%, RP 75,18% y con una RC del 3,27% inferior ala media calculada como tratamiento de primera línea. Elcoste variará dependiendo de las dosis utilizadas,así el coste del esquema compuesto por docetaxel (60mg/m2) y adriamicina (60 mg/m2) es inferioral ponderado, mientras que el coste supera el obtenido para elD.PQT cuando la dosificación es de 75 y 50 mg/m2para el docetaxel y la adriamicina, respectivamente (coste esquema:963.444 pesetas). Sin embargo, el coste asociado a estaúltima pauta es inferior a la considerada para el P.PQT, porlo que independientemente de la pauta utilizada semantendrían las condiciones del análisis principal.En la tabla 7 se recogen losresultados más significativos del análisis desensibilidad.
Tabla 7. Resultados del análisis desensibilidad | ||||||
| Tratamiento de primeraelección | Tratamiento de segundaelección | |||||
| RO | RP | RC | RO | RP | RC | |
| Variación de costes | ||||||
| --Monoterapia* | ||||||
| -- * Aumento 30% dosis dedocetaxel | D.MQT | D.MQT | D.MQT | D.MQT | D.MQT | D.MQT |
| -- * Disminución 30% dosisde paclitaxel | D.MQT | D.MQT | D.MQT | D.MQT | D.MQT | D.MQT |
| --Poliquimioterapia1 | ||||||
| -- * Disminución costeP.PQT (P/C) | 993.8873 | 681.3203 | P/C | P/C | P/C | P/C |
| -- * Disminución costeD.PQT2 | D.PQT | D.PQT | 7.455.0084 | D.PQT | D.PQT | D.PQT |
| --Aumento número ciclos (TPE) | D.PQT | D.PQT | 3.146.1994 | D.PQT | D.PQT | D.PQT |
| --Incremento coste asociado a toxicidad | D.PQT | D.PQT | 649.2694 | D.PQT | D.PQT | D.PQT |
| Variación efectividad | ||||||
| --Aumento 10% efectividad paclitaxel | D.PQT | D.PQT | 2.495.1384 | 4.504.0314 | 3.996.6604 | 4.430.0324 |
| Variación coste/efectividad | ||||||
| --Paclitaxel 90 mg/m2 +cisplatino 60 mg/m2 | 922.3023 | 696.8803 | P/C | P/C | P/C | P/C |
| --Paclitaxel 175 mg/m2 +adriamicina 60 mg/m2 | D.PQT | D.PQT | 2.868.7544 | 2.272.8945 | 3.884.9155 | 5.017.3445 |
| --Paclitaxel 175 mg/m2 +epirubicina 60 mg/m2 | D.PQT | D.PQT | D.PQT | D.PQT | D.PQT | 13.477.9346 |
1El análisis se ha realizado entre opcionessimilares, ya sea en monoterapia o en poliquimioterapia,manteniendo la efectividad considerada en el análisisprincipal para cada opción. 2Los esquemas quecumplen esta condición (coste inferior al coste medio de laD.PQT) son: docetaxel/adriamicina a dosis bajas,docetaxel/vinorelbina o decetaxel/fluoracilo. 3Coste porunidad extra de efectividad que debería pagarse si seeligiese la opción D.PQT frente al P/C (paclitaxel 90mg/m2 + cisplatino 60 mg/m2).4Coste por unidad extra de efectividad quedebería pagarse si se eligiese la opción P.PQT frenteal D.PQT. 5Coste por unidad extra de efectividad quedebería pagarse si se eligiese la opción paclitaxel +adriamicina frente al D.PQT. 6Coste por unidad extra deefectividad que debería pgarse si se eligiese laopción paclitaxel/epirubicina frente al D.PQT. | ||||||
DISCUSION
Lautilización de quimioterapia sistémica en eltratamiento del cáncer de mama ha reducido la incidencia derecidivas y aumentado la supervivencia en los estadios iniciales dela enfermedad (1, 3). No obstante, los pacientes con enfermedadmetastásica o diseminada no han visto mejorada susupervivencia, cuya mediana se sitúa en dos años. Eltratamiento del CMM es esencialmente paliativo y el objetivo finales la reducción de la sintomatología, el disconfort yla morbilidad asociada.
Laincorporación de los taxanos al arsenalfarmacoterapéutico se ha visto favorecido por losprometedores resultados obtenidos en ensayos clínicos depacientes con CMM. Sin embargo, el elevado coste deadquisición de estos fármacos requiere una adecuadavaloración y ponderación tanto de su efectividad comode los recursos necesarios para su inclusión, de formaestandarizada, en los diferentes esquemasquimioterápicos.
La necesidad deseleccionar un determinado taxano, paclitaxel o docetaxel requiererealizar una adecuada evaluación de ambos fármacosque nos permita elegir la opción farmacoterapéuticamás eficiente.
La principaldificultad para la valoración de su efectividad es laausencia de estudios que recojan como resultado del tratamiento lasupervivencia como indicador final, por lo que tenemos quelimitarnos a indicadores surrogados como la respuesta objetiva ycuyo impacto sobre la mayor o menor supervivencia no estábien definida. Diversos estudios coste-efectividad utilizanindicadores intermedios para medir los efectos sobre la salud, yaque éstos están relacionados de formaimplícita o explícita con un objetivo a máslargo plazo. Este tipo de indicadores presenta la ventaja de queson fácilmente objetivables, aunque permitan comparacionesmuy limitadas.
La diferenciatemporal respecto al período de aparición entre ambosfármacos se pone de manifiesto en nuestro estudio alcomparar el número de trabajos revisados, así como depacientes englobados en cada grupo. Esta diferencia podríafalsear los resultados globales (tratamiento de primera o segundaelección), ya que diferencias escasas de una opciónsobre la otra pueden compensarse por el mayor número depacientes. Así, por ejemplo, el índice de RC obtenidoen tratamientos de segunda elección es para la opciónP.MQT del 4,5% y para el P.PQT del 9,16%, mientras que para laopción del D.MQT es del 4,17% y la del D.PQT es del 10,03%;sin embargo, los resultados globales son del 6,30% para losesquemas con paclitaxel frente al 4,68% de los esquemas condocetaxel. Esta diferencia viene determinada al ponderar por elnúmero de pacientes, teniendo más peso en elresultado final, el grupo de tratamiento que incorpora un mayornúmero de pacientes. La medida de los índices derespuesta queda reflejada de forma más consistente cuando lacomparación se realiza como grupos independientes entre losdiferentes esquemas dentro de una misma línea detratamiento.
Como se observaen las tablas 2 y 3, el principal elemento que determina el costede cada esquema es el derivado de la adquisición delpaclitaxel o docetaxel, ya que independientemente de los esquemas,en la mayoría de ellos más del 90% del coste esatribuido a los taxanos. Por tanto, el mayor o menor coste de undeterminado esquema estará en función de la dosis delpaclitaxel o docetaxel. De esta forma los esquemas depoliquimioterapia, donde la dosificación de los taxanos esinferior, son claramente más económicos que losesquemas de monoterapia.
La dosisutilizada en poliquimioterapia varía entre 60-75mg/m2, mientras que en el paclitaxel varía en lamayoría de los casos entre 135-175 mg/m2,llegando raramente a los 200 mg/m2. De la misma forma,las dosis utilizadas en monoterapia varían entre losdiferentes estudios; así, en el caso del docetaxel existendos tendencias, mientras que en Estados Unidos se tiende a utilizardosis de 100 mg/m2, en Japón es de 70mg/m2, siendo ésta una dosificaciónmás conservadora (129). Se ha observado que con dosis altasse obtienen respuestas ligeramente superiores, pero que vienenacompañadas de toxicidad grave (mayor índice deneutropenias en grado 4, así como de neutropenias febriles)que pueden comprometer el seguimiento del tratamiento, mientras quecon dosis inferiores se obtienen un menor índice dereacciones adversas (5, 129, 131).
Por otra parte,aunque el coste por miligramo de docetaxel es más elevado(1.185,8 frente a 709,9 pesetas), la mayor dosificación delpaclitaxel hace a estos esquemas más caros. Esto determinaque independientemente de la efectividad, los esquemas másrentables sean, en principio, los D.PQT.
En elanálisis de sensibilidad queda reflejada la gran importanciaque adquiere el coste, sobre todo en tratamientos de segundalínea, donde los resultados de efectividad son similares. Deestos resultados se desprende que futuros cambios en los costes deadquisición de ambos fármacos pueden hacer variar lasconclusiones obtenidas en nuestro estudio.
Los resultadosde efectividad obtenidos en nuestro estudio muestran una mayorfrecuencia tanto de respuestas objetivas y parciales con laadministración de docetaxel, pero con una menor tasa derespuestas completas. Una de las conclusiones que se derivan delestudio es el alto índice de respuestas que se obtienencuando se administran en pacientes resistentes a antraciclinas(tratamiento de segunda elección).
Estos resultadosde efectividad, sobre todo cuando se determina como RO o RP, unidoa sus costes asociados, hacen de los esquemas con docetaxel,principalmente el D.PQT, como la opción máscoste-efectiva. Sin embargo, en el tratamiento de segundalínea no se observan diferencias significativas en laefectividad de los tratamientos. Por ello, las variaciones en loscostes (por modificación de los precios deadquisición o de las pautas de dosificación), en lascaracterísticas de cada uno de los fármacos(farmacocinéticas, farmacodinámicas otoxicológicas) o en la evaluación de otros factoresno recogidos en este estudio (calidad de vida o supervivenciapueden ser determinantes en el proceso deselección).
El estudiomuestra una mayor efectividad con los esquemas de poliquimioterapiatanto para la opción del paclitaxel como para el docetaxel.Por otra parte, este tipo de administración puede modificarel perfil de seguridad observado. Así, se ha observado quela administración conjunta del paclitaxel (en primer lugar)con la adriamicina potencia considerablemente la cardiotoxicidaddel esquema debido a una disminución del aclaramiento de laadriamicina. Se ha intentado cambiar la adriamicina por laepirrubicina con el fin de disminuir la cardiotoxicidad delesquema; sin embargo, esta variación también hadeterminado una disminución de la efectividad. Estainteracción no se ha puesto de manifiesto en los esquemascon docetaxel y adriamicina (5, 129).
En lacombinación paclitaxel/cisplatino se ha observado unincremento considerable de la neurotoxicidad, siendo en algunoscasos dosis limitante, no apareciendo cuando se emplea el docetaxela las dosis habituales (5).
Los resultadosobtenidos en nuestro estudio deben evaluarse dentro del contextodonde se ha realizado. Entre sus limitaciones se encuentran lasdiferencias del tamaño muestral de cada grupo, motivado porsu diferencia temporal de aparición, así como lafalta de un esquema de administración consensuado. Otroaspecto importante que puede afectar la robustez de los resultadosobtenidos radica en la falta de ensayos clínicoscomparativos directos entre el paclitaxel y el docetaxel.Además existen pocos ensayos clínicos que comparanambos fármacos en monoterapia con un control común,la adriamicina (26, 27, 30, 70, 72). La respuesta del paclitaxel essimilar a la obtenida con la adriamicina; sin embargo, la respuestaobtenida con el docetaxel era superior a la obtenida con laadriamicina en monoterapia. Por otra parte, la informacióndisponible sobre cada uno de los taxanos es otro factor que puedeafectar la consistencia de los resultados. Así pues, laaparición más tardía del docetaxel puede serel motivo de la menor documentación existente sobre suspotenciales combinaciones, interacciones o toxicidades.
Enconclusión, parece ser que la opción del docetaxel(D.PQT) es más coste-efectiva, y se presenta como laopción de referencia en la mayoría de los casos. Sinembargo, es necesario la realización de estudioscomparativos directos entre ambos fármacos, así comola evaluación de determinados indicadores finales deefectividad como la supervivencia (mayor número derespuestas) o la calidad de vida (menor número de reaccionesadversas) para facilitar el proceso de selección de unadeterminada opción.