En este trabajo se analiza la utilización de cetuximab en el tratamiento de cáncer colorrectal metastásico (CCRm) en un hospital de tercer nivel, determinando las condiciones de uso en los pacientes de nuestro centro con relación a las aprobadas en ficha técnica en el momento. También, se compara la duración del tratamiento en las distintas condiciones de uso y con los datos disponibles en la bibliografía publicada hasta la fecha de realización de este trabajo.
MétodosSe realizó un estudio de indicación-prescripción de cetuximab en CCRm para todos los pacientes tratados con cetuximab en CCR en el período 2004-2007 en nuestro hospital. Se determina el número de prescripciones que no se ajusta a la ficha técnica aprobada para cetuximab en CCRm y el motivo por el que no se adapta. Se realiza el análisis estadístico descriptivo para las distintas variables recogidas y un análisis de Kaplan-Meier para la variable duración de tratamiento para determinar si hay diferencia de efectividad para los usos habituales en nuestro hospital.
ResultadosSe recogieron los datos de 74 pacientes tratados con cetuximab. El coste medio por paciente fue de 14.399 € y un número medio de dosis administradas de 15,3 por paciente. La dosis media de inicio fue 710 mg y la de mantenimiento, de 446 mg. La duración media de los tratamientos fue 15,4 semanas. Cetuximab se administró a 7 pacientes en primera línea de tratamiento, y a 32 pacientes sin que previamente se hubiese utilizado irinotecan. En 9 pacientes no se asoció irinotecan al tratamiento con cetuximab y se empleó en 14 pacientes con resultado negativo para la prueba de EFGR. La duración de los tratamientos fue mayor en caso de utilización en primera línea de tratamiento (27,7 semanas), si no se empleó irinotecan previo (23,3 semanas), si se asociaba irinotecan al tratamiento (20,5 semanas) y en pacientes EFGR positivo (19,6 semanas). Las medianas de duración de tratamiento en las diferentes condiciones recogidas eran menores en magnitud a la media, no presentando diferencias significativas entre ellas. El 70,3 % de las prescripciones no se ajustaba a la ficha técnica.
ConclusionesLa utilización de cetuximab en condiciones distintas a las aprobadas en ficha técnica origina un aumento en el número de pacientes tratados y una mayor duración de los tratamientos, lo que implica un aumento en el consumo. La media y la mediana de tiempo de tratamiento para las condiciones de utilización encontradas no presentaron diferencia estadísticamente significativa. Hay un pequeño número de pacientes que se beneficia de este tratamiento, como puede ponerse de manifiesto por la mayor magnitud de la media respecto a la mediana, sin que ninguna de las condiciones en las que se realizó el análisis parezca ser determinante de una respuesta mayor. La duración de los tratamientos en nuestro estudio fue del orden de las encontradas en la bibliografía para esas condiciones de utilización.
In this study we will analyse the use of cetuximab in the treatment of metastatic colorectal cancer (MCC) in a third level hospital. We will establish the usage conditions in our centre in keeping with those approved in current technical records. We will also record the treatment duration under the different usage conditions and use the information available in material that has been published to date.
MethodsAn indication-prescription study of cetuximab in MCC was carried out on all patients treated with cetuximab for colorectal cancer in the period between 2004 and 2007 in our hospital. The number of prescriptions that do not fit the approved recommendations for cetuximab in MCC treatment (and why they do not fit) is determined. Descriptive statistical analysis was carried out for the different variables collected, and a Kaplan-Meier analysis was carried out for the treatment duration variable, so as to determine whether there is a difference in effectiveness for the common uses in our hospital.
ResultsData was recorded for 74 patients treated with cetuximab. The average cost per patient was €14,399 and on average, 15.3 dosages were administered per patient. The average initial dosage was 710 mg with an average dosage of 446 mg after that. The average duration of the treatments was 15.4 weeks. cetuximab was administered to 7 patients as first-line treatment and to 32 patients who had not used Irinotecan previously. Irinotecan was not associated with cetuximab treatment in 9 patients, and it was used in 14 patients resulting in a negative outcome for the EFGR test. Treatment duration was longer in the case of its use as first-line treatment (27.7 weeks), if Irinotecan had not been used before (23.3 weeks), if Irinotecan was used (20.5 weeks) and in patients with positive EFGR results (19.6 weeks.) The median treatment duration, under the different conditions, was less than the average but with no major differences between them. 70.3 % of prescriptions did not fit with the data sheet.
ConclusionsThe use of cetuximab under different conditions to those approved on the technical data sheet creates an increase in the number of patients treated and a longer duration of the treatments which implies an increase in intake. The average and the mean treatment times for the usage conditions found did not present any significant statistical differences. There are a small number of patients who benefit from this treatment which can be seen by the large average, in comparison with the mean, without any of the conditions in which the analysis was carried out seeming to determine a higher response. The treatment duration in our study was similar to the durations recorded in relevant literature for these usage conditions.
Cetuximab es un fármaco anticanceroso constituido por un anticuerpo IgG1 monoclonal quimérico que actúa bloqueando el receptor del factor de crecimiento epidérmico (EFGR) y, por consiguiente, su función, inhibiendo de esta manera la proliferación y favoreciendo la apoptosis celular. La primera indicación aprobada para cetuximab fue: "En combinación con irinotecan está indicado para el tratamiento de pacientes con cáncer colorrectal metastásico (CCRm) que exprese el EGFR después del fracaso de un tratamiento citotóxico que haya incluido irinotecan". Actualmente, cetuximab también está indicado en el tratamiento del cáncer de cabeza y cuello asociado a radioterapia1, sin bien en este trabajo nos centraremos en el uso en CCRm.
La utilización de fármacos en oncología en condiciones distintas a las aprobadas es frecuente debido a la peculiaridad de la patología oncológica y al deseo de trasladar las nuevas terapias al tratamiento de estos pacientes. Diferentes trabajos realizados en este campo2,3 estiman en aproximadamente un 50 % de las prescripciones como no ajustadas a la ficha técnica para el grupo de fármacos oncológicos estudiados; en el caso de cetuximab, su utilización en la práctica clínica habitual puede ser diferente a la recogida en la ficha técnica. En la literatura médica aparecen referencias al tratamiento de pacientes en primera línea de CCRm4-8, que no expresen el EFGR9-12 o de utilización conjunta con fármacos distintos a irinotecan5,13. La utilización de cetuximab en estos supuestos podría originar un incremento en el consumo que tendría 2 causas:
- –
Un mayor número de pacientes tratados tanto por su empleo en primera línea de tratamiento, como por la ampliación a pacientes que no expresen el EFGR o por el mayor número de tratamientos al asociarse a fármacos diferentes de irinotecan. En este sentido, algunos autores14 estiman en un 3 % de los pacientes diagnosticados de CCR o en 1,8 tratamientos por cada 100.000 habitantes el número de pacientes subsidiario de recibir tratamiento con cetuximab, si nos atenemos a la ficha técnica.
- –
Un mayor tiempo de tratamiento de los pacientes como consecuencia de un incremento en la tasa de respuesta15, mediana del tiempo de progresión o en la supervivencia libre de progresión.
En el presente trabajo se analiza la utilización de cetuximab en CCRm en un hospital que presta atención oncológica a toda el área sanitaria, con especial atención a la influencia que pueden tener las situaciones en las que cetuximab se utilice fuera de indicación sobre el tiempo de tratamiento, como posible causa de un incremento en el consumo.
MétodosSe realizó un estudio de indicación-prescripción de cetuximab en CCRm incluyendo los datos de todos los pacientes con tratamiento instaurado en nuestro hospital desde la comercialización de cetuximab en 2004 hasta noviembre de 2007 y que no estuvieran incluidos en alguno de los protocolos de ensayo clínico con cetuximab activos en nuestro hospital. Para la recogida de datos se utilizaron los sistemas de información de la aplicación de farmacia oncológica y admisión, la historia clínica y los registros de anatomía patológica. Las variables recogidas fueron edad y sexo de los pacientes, línea de tratamiento, existencia o no de terapia previa con irinotecan, fármaco asociado a cetuximab, dosis de cetuximab, resultado de la prueba de expresión EFGR, duración del tratamiento y su continuidad en el momento del cierre del estudio. Se recogieron también los datos de consumo de cetuximab en el período analizado, así como el número de preparaciones elaboradas desde el servicio de farmacia.
Las variables cualitativas se analizaron descriptivamente mediante frecuencias y las cuantitativas con medidas de tendencia central y de dispersión (media, mediana, desviación estándar [DE]); además, a la variable tiempo de tratamiento se le practicó un análisis de Kaplan-Meier (global y en función de las variables línea de tratamiento, asociación de irinotecan, tratamiento previo con irinotecan y resultado de la prueba EFGR), y el evento delimitador de éste fue la supresión del tratamiento por cualquier causa. Para todos los análisis se utilizó el paquete estadístico SPSS. El tiempo de tratamiento según la ficha técnica de cetuximab se prolonga hasta que el paciente progresa, presenta reacción adversa o muere; se compararon los tiempos de tratamiento que se recogieron en nuestro hospital con los de los estudios clínicos publicados u otra variable de eficacia disponible. Sobre esta base, el tiempo de tratamiento podría ser un buen estimador del tiempo a fracaso del tratamiento15; sin embargo, esta variable no se considera una buena medida de eficacia en los ensayos clínicos al medir eficacia y seguridad al mismo tiempo, y como variable de eficacia se utiliza el tiempo libre de progresión, supervivencia libre de progresión.
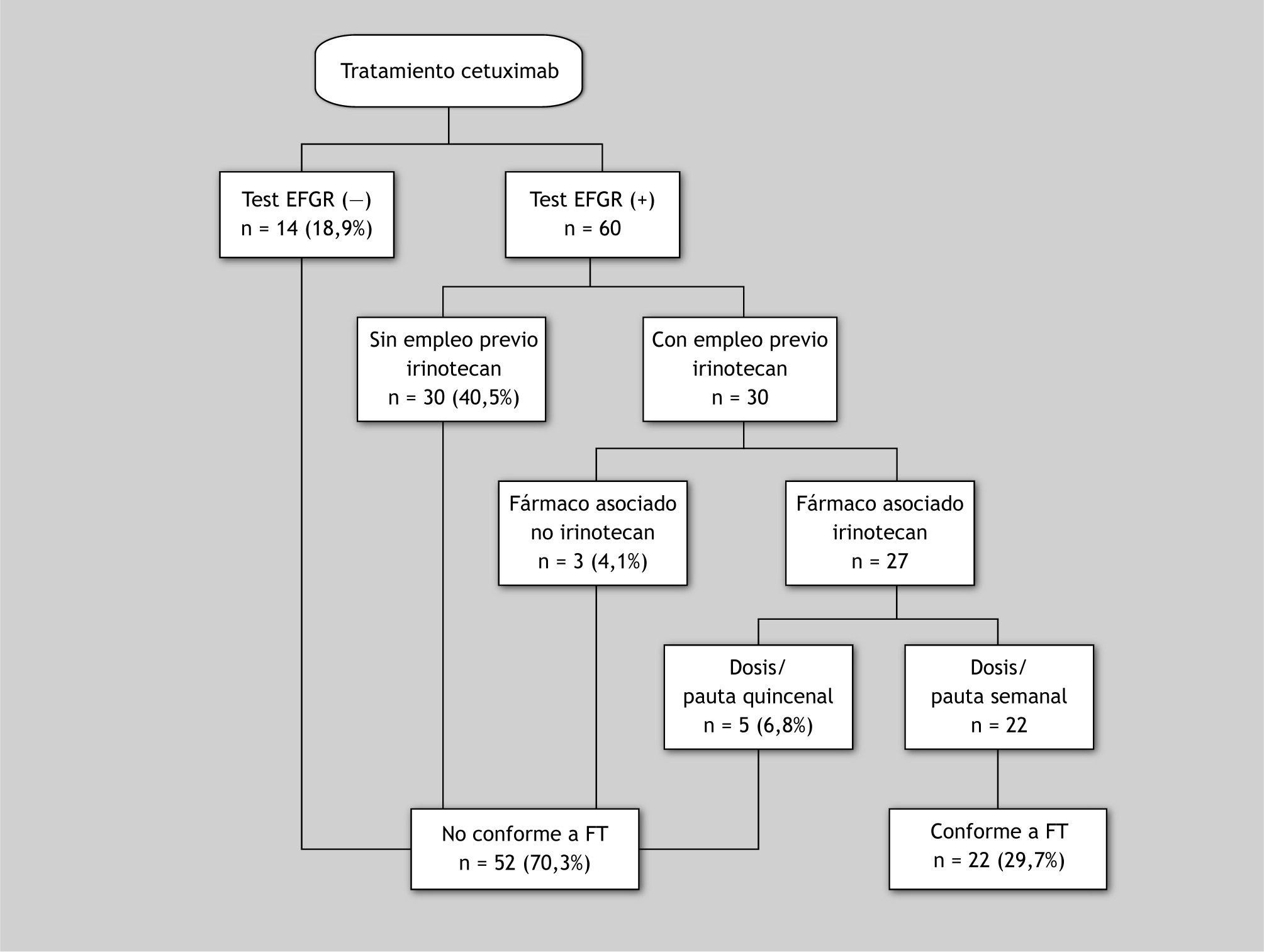
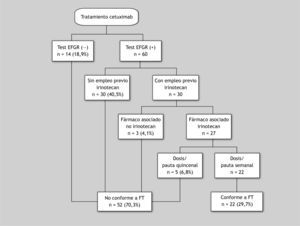
La coincidencia de la indicación utilizada con la autorizada se estableció basándose en la aprobada en la ficha técnica de cetuximab1 en el momento de realizar este estudio. Ya que había la posibilidad que un tratamiento pudiera tener 2 o más causas para que no cumpliese con las especificaciones de la ficha técnica, se utilizó el algoritmo de la figura 1 para determinar si un tratamiento cumplía o no con éstas.
ResultadosEn el período estudiado se trataron un total de 74 pacientes de CCRm, de los que 56 eran varones y 18 mujeres. En este mismo período el número de pacientes atendidos por el servicio de oncología fue de 694, lo que supone una utilización de cetuximab en un 10,6 % del total de pacientes de cáncer de colon atendidos. La edad media de los pacientes fue de 66 años (39-84 años). En el momento de realizar el estudio permanecen en tratamiento con cetuximab 17 pacientes.
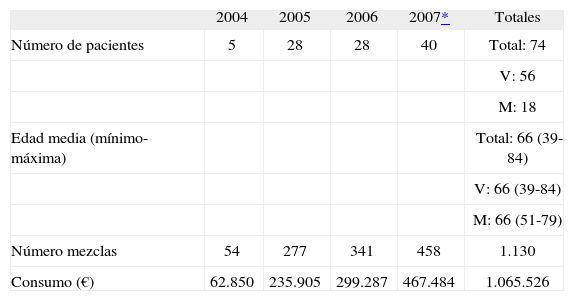
El coste medio por paciente ha sido de 14.399 €, lo que ha supuesto un consumo de cetuximab de 1.065.526 € en todo el período. El consumo anual de cetuximab pasó de 62.850 € durante 2004 a 467.484 € en 2007 (enero a octubre) (tabla 1). El número total de dosis administradas fue de 1.130, con una media por paciente 15,3 (1-68), y una mediana de 10.
Número de pacientes y consumo de cetuximab
| 2004 | 2005 | 2006 | 2007* | Totales | |
| Número de pacientes | 5 | 28 | 28 | 40 | Total: 74 |
| V: 56 | |||||
| M: 18 | |||||
| Edad media (mínimo-máxima) | Total: 66 (39-84) | ||||
| V: 66 (39-84) | |||||
| M: 66 (51-79) | |||||
| Número mezclas | 54 | 277 | 341 | 458 | 1.130 |
| Consumo (€) | 62.850 | 235.905 | 299.287 | 467.484 | 1.065.526 |
M: mujeres; V: varones.
Las situaciones en que se utilizó cetuximab de forma diferente a la aprobada representan un 70,3 % respecto al total (fig. 1). De acuerdo a la normativa en vigor durante el período objeto de estudio, el uso de medicamentos en condiciones distintas a las autorizadas debería tramitarse a la Agencia Española de Medicamentos y Productos Sanitarios como "uso compasivo"; sin embargo, en este estudio sólo se recogieron las solicitudes como "uso compasivo" en 12 casos, un 23,1 % de los susceptibles de tramitarse.
Cetuximab se administró en primera línea de tratamiento en 7 (9,5 %) pacientes, en segunda en 25 (33,8 %), en tercera o sucesivas en 42 (56,8 %). El tratamiento con irinotecan previo a cetuximab se dio en 42 pacientes (56,7 %). Irinotecan se administró asociado a cetuximab en 63 (85,1 %) pacientes, de los que 5 tenían asociado además fluorouracilo, a 7 (9,5 %) pacientes se les administró monoterapia con cetuximab y la asociación con fármacos distintos a irinotecan se dio en 4 (5,4 %) (tabla 2). Los fármacos distintos a irinotecan a los que se asoció cetuximab fueron fluorouracilo y oxaliplatino, en 11 y 9 pacientes, respectivamente. Siete pacientes cambiaron su tratamiento durante la terapia con cetuximab + irinotecan, teniendo una segunda opción de tratamiento con cetuximab en monoterapia o asociado a oxaliplatino. Sólo 34 pacientes tenían resultado de la prueba EFGR, que fue positivo en 20 (58,9 %) y negativo en 14 (41,1%).
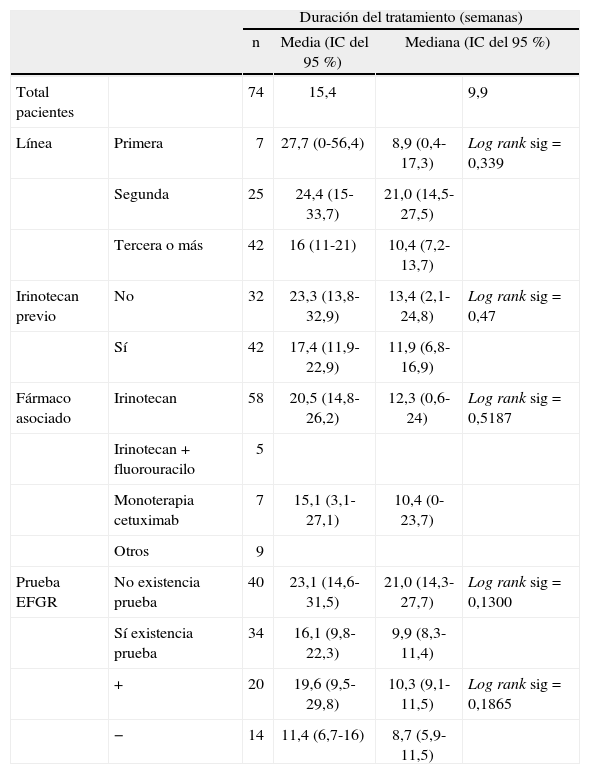
Duración de los tratamientos según las condiciones de utilización
| Duración del tratamiento (semanas) | |||||
| n | Media (IC del 95 %) | Mediana (IC del 95 %) | |||
| Total pacientes | 74 | 15,4 | 9,9 | ||
| Línea | Primera | 7 | 27,7 (0-56,4) | 8,9 (0,4-17,3) | Log rank sig = 0,339 |
| Segunda | 25 | 24,4 (15-33,7) | 21,0 (14,5-27,5) | ||
| Tercera o más | 42 | 16 (11-21) | 10,4 (7,2-13,7) | ||
| Irinotecan previo | No | 32 | 23,3 (13,8-32,9) | 13,4 (2,1-24,8) | Log rank sig = 0,47 |
| Sí | 42 | 17,4 (11,9-22,9) | 11,9 (6,8-16,9) | ||
| Fármaco asociado | Irinotecan | 58 | 20,5 (14,8-26,2) | 12,3 (0,6-24) | Log rank sig = 0,5187 |
| Irinotecan + fluorouracilo | 5 | ||||
| Monoterapia cetuximab | 7 | 15,1 (3,1-27,1) | 10,4 (0-23,7) | ||
| Otros | 9 | ||||
| Prueba EFGR | No existencia prueba | 40 | 23,1 (14,6-31,5) | 21,0 (14,3-27,7) | Log rank sig = 0,1300 |
| Sí existencia prueba | 34 | 16,1 (9,8-22,3) | 9,9 (8,3-11,4) | ||
| + | 20 | 19,6 (9,5-29,8) | 10,3 (9,1-11,5) | Log rank sig = 0,1865 | |
| − | 14 | 11,4 (6,7-16) | 8,7 (5,9-11,5) | ||
EFGR: receptor del factor de crecimiento epidérmico; IC: intervalo de confianza.
La dosis media administrada como inicio del tratamiento fue de 710 mg (DE = 101), y la de mantenimiento de 446 mg (DE = 53,4). A 13 pacientes se les disminuyó la dosis durante el tratamiento, con una reducción media del 30 %, y a 8 se les administró cetuximab con pauta quincenal (500 mg/m2).
La media de duración de los tratamientos con cetuximab (tabla 2) para el total de pacientes del estudio fue de 15,4 semanas (DE = 16,1). Teniendo en cuenta la línea de tratamiento, la duración media fue de 27,7 semanas en primera línea, 24,4 en segunda y 16 en tercera o sucesivas. En los pacientes que habían estado en tratamiento previo con irinotecan la duración media de los tratamientos fue de 17,4 y 23,3 semanas si no lo habían estado.
Tras la revisión de las historias clínicas y la búsqueda en la base de datos de anatomía patológica, sólo se encontró el resultado de la prueba de EFGR en 34 de los 74 pacientes del estudio. En los pacientes con resultado positivo, la duración media de los tratamientos fue de 19,6 semanas y de 11,4 en los que el resultado fue negativo (tabla 2). La media de duración de los tratamientos en los pacientes a los que no se había realizado esta prueba era de 23,1 semanas.
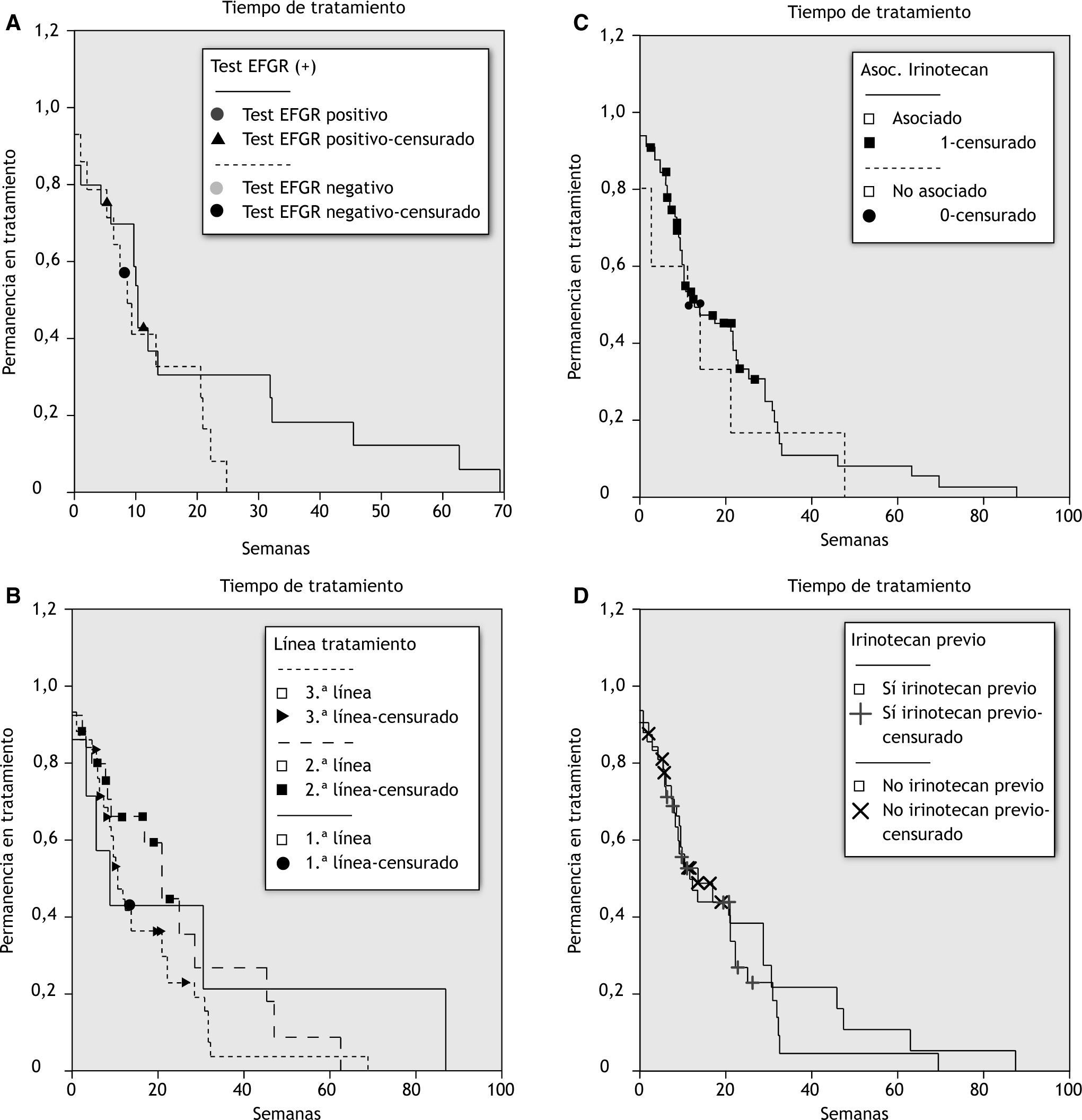
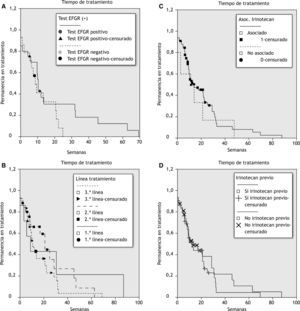
Los valores para la mediana del tiempo de tratamiento para toda la población y para cada estrato (línea de tratamiento, empleo previo de irinotecan, asociación de irinotecan y test EFGR) se muestran también en la tabla 2 y la figura 2; en todos los casos la mediana de duración del tratamiento fue menor que la media.
Curvas de supervivencia del tiempo de tratamiento. A) Estratificada por el resultado de la prueba del receptor del factor de crecimiento epidérmico (EFGR). B) Estratificada por línea de tratamiento. C) Estratificada si se administró irinotecan, asociado o no a cetuximab. D) Estratificada si se administró irinotecan previo.
Como se observa en la tabla 1, ha habido un incremento paulatino tanto en el consumo como en el número de pacientes de CCRm tratados con cetuximab. El incremento en el consumo (56 %) ha sido superior al de pacientes (42 %), lo que pensamos que está motivado por el elevado grado de utilización en condiciones distintas a las aprobadas en la ficha técnica, 70,3 % de casos. Se muestran situaciones como el empleo en líneas iniciales de tratamiento o en casos donde no se administró previamente irinotecan, situaciones que originan un mayor tiempo de utilización del fármaco y un aumento en el consumo de cetuximab proporcionalmente mayor al de número de pacientes.
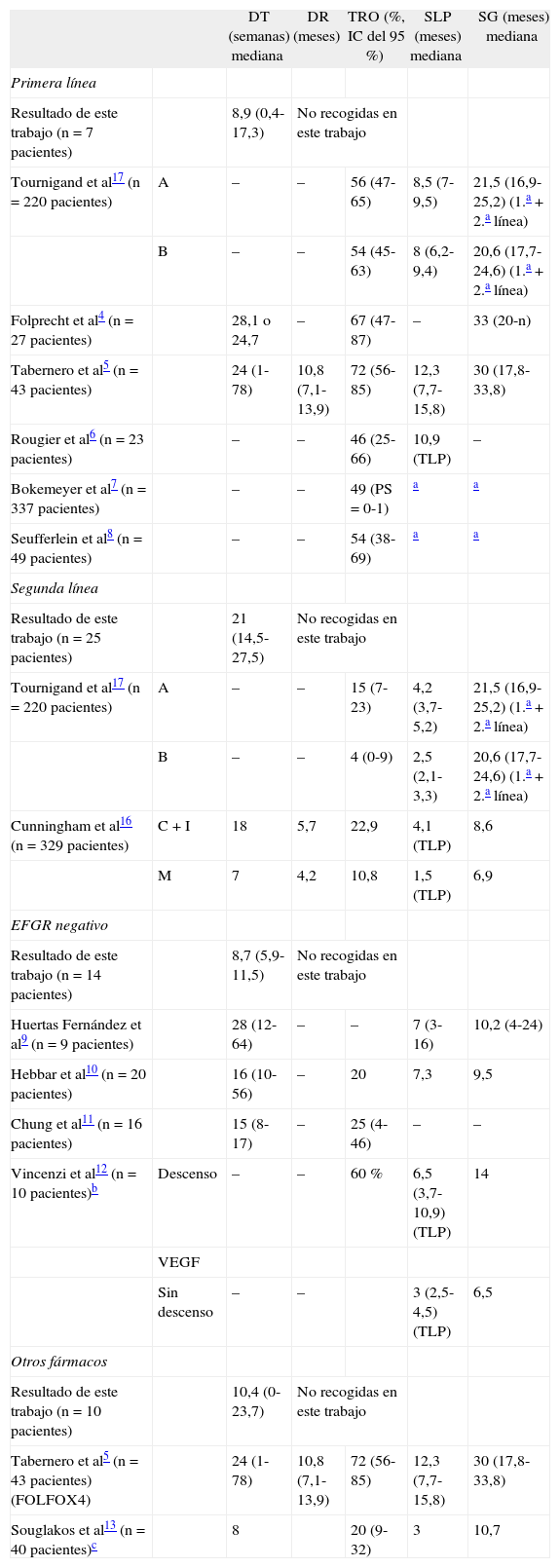
En la tabla 3 se presenta un resumen de los datos obtenidos en este estudio y los de los ensayos publicados para la misma condición clínica. Como referencia, también se muestran los datos del estudio pivotal de Cunninghan16 y el trabajo de Tournigand et al17 que compara 2 secuencias de tratamiento con los esquemas FOLFIRI y FOLFOX.
Resultados de eficacia en ensayos clínicos de cetuximab
| DT (semanas) mediana | DR (meses) | TRO (%, IC del 95 %) | SLP (meses) mediana | SG (meses) mediana | ||
| Primera línea | ||||||
| Resultado de este trabajo (n = 7 pacientes) | 8,9 (0,4-17,3) | No recogidas en este trabajo | ||||
| Tournigand et al17 (n = 220 pacientes) | A | – | – | 56 (47-65) | 8,5 (7-9,5) | 21,5 (16,9-25,2) (1.a + 2.a línea) |
| B | – | – | 54 (45-63) | 8 (6,2-9,4) | 20,6 (17,7-24,6) (1.a + 2.a línea) | |
| Folprecht et al4 (n = 27 pacientes) | 28,1 o 24,7 | – | 67 (47-87) | – | 33 (20-n) | |
| Tabernero et al5 (n = 43 pacientes) | 24 (1-78) | 10,8 (7,1-13,9) | 72 (56-85) | 12,3 (7,7-15,8) | 30 (17,8-33,8) | |
| Rougier et al6 (n = 23 pacientes) | – | – | 46 (25-66) | 10,9 (TLP) | – | |
| Bokemeyer et al7 (n = 337 pacientes) | – | – | 49 (PS = 0-1) | a | a | |
| Seufferlein et al8 (n = 49 pacientes) | – | – | 54 (38-69) | a | a | |
| Segunda línea | ||||||
| Resultado de este trabajo (n = 25 pacientes) | 21 (14,5-27,5) | No recogidas en este trabajo | ||||
| Tournigand et al17 (n = 220 pacientes) | A | – | – | 15 (7-23) | 4,2 (3,7-5,2) | 21,5 (16,9-25,2) (1.a + 2.a línea) |
| B | – | – | 4 (0-9) | 2,5 (2,1-3,3) | 20,6 (17,7-24,6) (1.a + 2.a línea) | |
| Cunningham et al16 (n = 329 pacientes) | C + I | 18 | 5,7 | 22,9 | 4,1 (TLP) | 8,6 |
| M | 7 | 4,2 | 10,8 | 1,5 (TLP) | 6,9 | |
| EFGR negativo | ||||||
| Resultado de este trabajo (n = 14 pacientes) | 8,7 (5,9-11,5) | No recogidas en este trabajo | ||||
| Huertas Fernández et al9 (n = 9 pacientes) | 28 (12-64) | – | – | 7 (3-16) | 10,2 (4-24) | |
| Hebbar et al10 (n = 20 pacientes) | 16 (10-56) | – | 20 | 7,3 | 9,5 | |
| Chung et al11 (n = 16 pacientes) | 15 (8-17) | – | 25 (4-46) | – | – | |
| Vincenzi et al12 (n = 10 pacientes)b | Descenso | – | – | 60 % | 6,5 (3,7-10,9) (TLP) | 14 |
| VEGF | ||||||
| Sin descenso | – | – | 3 (2,5-4,5) (TLP) | 6,5 | ||
| Otros fármacos | ||||||
| Resultado de este trabajo (n = 10 pacientes) | 10,4 (0-23,7) | No recogidas en este trabajo | ||||
| Tabernero et al5 (n = 43 pacientes) (FOLFOX4) | 24 (1-78) | 10,8 (7,1-13,9) | 72 (56-85) | 12,3 (7,7-15,8) | 30 (17,8-33,8) | |
| Souglakos et al13 (n = 40 pacientes)c | 8 | 20 (9-32) | 3 | 10,7 | ||
DR: duración de la respuesta; DT: duración de tratamiento; EFGR: receptor del factor de crecimiento epidérmico; IC: intervalo de confianza; SG: supervivencia global: SLP: supervivencia libre de progresión; TLP: tiempo libre de progresión; TRO: tasa de respuestas objetivas; VEGF: factor de crecimiento endotelio vascular.
Puede observarse como la media de tiempo en tratamiento es mayor si cetuximab se usa en primera línea de CCRm (27,7 semanas) frente a segunda (24,4) y tercera (16). La media de los tiempos de tratamiento con cetuximab en primera línea están en la magnitud de los tiempos de tratamiento obtenidos por Folprecht et al4 y Tabernero et al5. Al realizar el análisis de Kaplan-Meier para los pacientes de nuestro estudio la mediana de duración de tratamiento en primera línea fue de 8,9 semanas; en segunda, de 21,0, y en tercera, de 10,4, sin mostrar diferencia estadísticamente significativa. En nuestra población puede observarse como la mediana de duración de tratamiento en primera línea es marcadamente inferior a las reflejadas en los estudios de Folprecht et al4 y Tabernero et al5, incluso si se compara con la media de nuestra población. Este hecho se puede deber al pequeño número de pacientes con tratamiento en primera línea en nuestro trabajo (7 pacientes).
Si se tiene en cuenta si previamente se había empleado irinotecan, la media en la duración del tratamiento fue de 17,4 semanas (23,3 semanas si no se había empleado), y este valor fue similar al obtenido en el trabajo de Cunninghan16.
Cuando cetuximab se utilizó asociado a irinotecan, la media de tratamiento fue de 20,5 semanas frente a las 15,1 semanas si no llevaba asociado irinotecan, si bien en este grupo cetuximab podía ir asociado a otros fármacos, como oxaliplatino y/o fluoruracilo. De nuevo la mediana de estos grupos es de menor magnitud a la media, 12,3 y 10,4 semanas, respectivamente, si se asocia o no a irinotecan.
Las diferentes guías de tratamiento de CCRm hacen referencia a la carencia de valor predictivo de la prueba de EFGR, no recomendando esta prueba como criterio determinante del tratamiento con cetuximab18. En nuestra población el 54 % de los pacientes carecía de resultado (positivo o negativo) de esta prueba, con una media de tiempo de tratamiento de 23,1 semanas, frente al 46 % de los pacientes que sí disponía de resultado y una duración del tratamiento de 16,1 semanas. En este último grupo, la media del tiempo de tratamiento fue superior en los pacientes con valor positivo de la prueba de EFGR (19,6 semanas) frente a los que el resultado fue negativo (11,4), sin que esta diferencia fuese significativa; tampoco hubo diferencia significativa si el análisis se realizaba en función de la mediana del tiempo de tratamiento (tabla 2). Tanto la media como la mediana del tiempo de tratamiento en pacientes con resultado negativo para la prueba de EFGR resultan claramente inferiores en nuestro estudio a las recogidas en la bibliografía (tabla 3).
El hecho que la media del tiempo de tratamiento presente un valor mayor a la mediana puede deberse a que el beneficio de cetuximab se produzca en pacientes determinados y no de una forma homogénea, y no se encontró que los estratos analizados (línea de tratamiento, empleo previo de irinotecan, asociación de irinotecan y test EFGR) tengan influencia en la duración del tratamiento y, por tanto, en su eficacia.
ConclusionesLa utilización de cetuximab en distintas situaciones clínicas en nuestro hospital va paralela a la publicación de nuevos trabajos (tabla 3). Los valores de la media de tiempo de tratamiento eran del orden de las medianas de duración de tratamiento encontradas en la bibliografía publicada para esas condiciones de utilización. El hecho que se tramite un número bajo de peticiones como uso compasivo puede deberse a la falsa creencia de que se hayan ampliado las indicaciones del fármaco que se trate ante la publicación de nuevas evidencias.
Asimismo, la utilización en esta nuevas condiciones de uso origina un aumento en el consumo motivado por las 2 causas, tal como se esperaba en la hipótesis de trabajo evaluada, aumento en el número de pacientes y mayor duración de éstos.
No se observa diferencia significativa en los tiempos de tratamiento en las diferentes condiciones de uso detectadas en nuestro hospital. Sin embargo, un aspecto que se debe resaltar es que la mayor duración se observa en la media del tiempo de tratamiento no con la mediana, debido, muy probablemente, a que son determinados pacientes los que se benefician de esta terapia. Se debería determinar qué pacientes son los que verdaderamente se benefician de la terapia con cetuximab, debido al impacto económico que representa la introducción de esta terapia para CCRm.