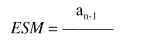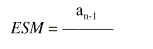ORIGINALES
ESTABILIDAD Y ESTERILIDAD DE UN COLIRIODE FENILEFRINA AL 2,5%
Pérez Maroto, M.T.,Especialista en Farmacia Hospitalaria;Luque Infantes, R.*,Especialista en Farmacia Hospitalaria, Farmacéutica Adjunta;Santolaya Perrín, R.*;Especialista en Farmacia Hospitalaria, Farmacéutica Adjunta;Tornero Torres, O.*, Especialista en Farmacia Hospitalaria;Requena Cartula, T.*;Especialista en Farmacia Hospitalaria, Jefa de Sección.
*Servicio de Farmacia. Hospital Universitario Príncipe de Asturias. Alcalá de Henares. Madrid
Correspondencia: M.a Teresa Pérez Maroto. c/ Pamplona, n.o 5 Esc A 2.o 6.a. 28850 Torrejon de Ardoz, Madrid.
Fecha de recepción: 3-09-98
Palabras clave: Colirio. Estabilidad. Esterilidad. Fenilefrina.
Resumen: Para disminuir los efectos adversos sistémicos producidos por el colirio de fenilefrina al 10% se elaboró un preparado al 2,5% a partir de la forma comercializada. Se determinó su estabilidad (concentración, pH y osmolaridad) y la esterilidad durante un período de 60 días bajo dos condiciones de conservación diferentes: temperatura ambiente (25 °C) o refrigerado (4-8 °C), ambos protegidos de la luz.
Los valores de concentración determinados por espectrofotometría (94,97-108,22% a 25 °C y 98,63-108,32% a 4-8 °C) se encontraron dentro de los márgenes permitidos por la U.S.P. Tanto el pH como la osmolaridad se mantuvieron dentro de los márgenes fisiológicos para el ojo a lo largo de todo el estudio en las dos condiciones estudiadas. No se apreció crecimiento microbiológico.
El colirio de fenilefrina al 2,5% permanece estable y estéril durante al menos 60 días cuando se almacena protegido de la luz tanto a temperatura ambiente como en refrigeración.
STABILITY AND STERILITY OF A 2,5% PHENYLEPHRINE EYE DROP FORMULATION
Key words: Eyedrops. Stability. Sterility. Phenylephrine.
Summary: To decrease the adverse systemic effects caused by 10% phenylephrine eyedrops, we prepared a 2,5% formulation from a commercial form of this medication. Stability (concentration, pH and osmolarity) and sterility were determined during a 60-day period under two different storage conditions: room temperature /(25 °C) in the dark, and refrigeration (4-8 °C) in the dark. Concentration, determined spectrophotometrically (94,97-108,22% at 25 °C, and 98,63-108,32% at 4-8 °C) was within the range permitted by the USP.pH and osmolarity remained within physiological limits for the eye throughout the study period under both storage conditions. No growth of microorganisms was seen. The 2,5% formulation of phenylephrine eyedrops remains stable and sterile during ant least 60 days of storage away from light at room temperature or under refrigeration.
Farm Hosp 1999; 23: 48-52
INTRODUCCION
La fenilefrina es un simpaticomimético adrenérgido que se utiliza por vía tópica oftálmica como agente midriático: produce contracción del músculo dilatador del iris sin suprimir la acomodación ocular por parálisis del músculo, es decir, sin ciclopejía. Se utiliza principalmente en el examen de fondo de ojo, cirugía intraocular, tratamiento de la uveítis anterior (prevención de sinequia posterior), iritis, iridociclitis, glaucoma o alérgicos a la atropina. Su efecto midriático se produce a concentraciones que oscilan entre el 10% y el 2,5% e incluso menores. Los efectos secundarios más frecuentes son escozor, fotofobia y lagrimeo. Ocasionalmente se produce irritación ocular o liberación de gránulos pigmentados flotantes en el humor acuosos. Más raramente puede haber incremento de la presión intraocular en glaucoma de ángulo abierto o desencadenamiento de glaucoma de ángulo cerrado. Todos estos son efectos locales pero pueden producirse también efectos sistémicos como palpitaciones, taquicardia, arritmia, hipertensión, cefalea, palidez, temblor, vértigo, hiperhidrosis, y reacciones cardiovasculares graves, a veces mortales (hipertensión arterial severa, arritmia ventricular, hemorragia subaracnoidea, infarto agudo de miocardio) sobre todo en ancianos con enfermedad cardiovascular preexistente y en niños. Aunque la incidencia de estas reacciones adversas más graves es baja, se recomienda precaución en esta población (1-4).
Para evitar estos efectos sistémicos se han propuesto algunas alternativas: comprimir el conducto nasolacrimal tras la administración del colirio, reducir el tamaño de la gota para que la dosis suministrada sea menor o disminuir la concentración del colirio (5, 6).
El ochenta por ciento de la fenilefrina instilada en el ojo se pierde en 15-30 segundos por el conducto nasolacrimal. por derramarse fuera del ojo o por la absorción sistémica que se produce en la conjuntiva o en la mucosa nasal. Esta absorción sistémica carece de efecto de primer paso por el hígado, asemejándose a la producida en una administración intravenosa (6).
Las gotas de volumen reducido presentan dos factores limitantes para su empleo. En primer lugar no es fácil su administración por tener que recurrir a artefactos no comercializados y de manejo complicado. En segundo lugar, las gotas de volumen reducido al ser instiladas en el ojo son menos molestas, estimulan menos el lagrimeo y el parpadeo por lo que se facilita el contacto del colirio con el ojo. Como resultado la biodisponibilidad de la fenilefrina aumenta y con ello también lo hace la posibilidad de seguir produciendo efectos adversos aunque el tamaño de la gota sea menor (6).
La única concentración de fenilefrina comercializada en España es la del 10%. En algunos países como Estados Unidos o Reino Unido existen otras presentaciones colirio de fenilefrina al 2,5%. El efecto midriático máximo se consigue con las concentraciones a los 60 minutos. La recuperación de la midriasis se produce entre las 5,5 y las 7 horas a concentración de 2,5% y en más de siete horas a concentración del 10%. Sin embargo, la probabilidad de producir efectos cardiovasculares adversos es menor con la fenilefrina al 2,5% (1, 7, 8). Por esta razón, el servicio de oftalmología solicita al servicio de farmacia la preparación de este colirio.
El objetivo de este estudio es comprobar la estabilidad y esterilidad de un colirio de fenilefrina al 2,5% bajo dos condiciones distintas de almacenamiento, preparado a partir de la forma comercializada en España.
MÉTODO
Material
Para la elaboración del colirio se emplea:
-- Colicusí Fenilefrina® al 10% de Laboratorio Cusí que contiene: Fenilefreina 10%, Timerosal 0,01%, sulfito sódico 0,1%, Fosfato Disódico 0,4% y agua.
-- Cloruso Sódico 0,9% de Laboratorio B. Braun.
-- Timerosal Sódico, distribuido por Guinama, S.L.
Para las determinaciones analíticas se emplea:
-- Filtro Millex®-GS de 0,22 micras de Laboratorio Millipore.
-- Espectrofotómetro programable SpectronicTM modelo 2100.
-- Microosmómetro Advancec Instruments IncTM modelo 3MO.
-- pHmetro MeteorTM modelo 991A.
-- Visor de partículas.
Método de elaboración
Los colirios se prepararon en condiciones asépticas de trabajo en campana de flujo laminar para asegurar las condiciones de esterilidad del producto final.
Para preparar el colirio de fenilefrina al 2,5% se diluyó Colicursi Fenilefrina® al 10% en una proporción 1:4 con cloruro sódico al 0,9% para mantener la osmolaridad adecuada al ojo. Al cloruro sódico al 0,9% previamente se le añadió la cantidad necesaria de timerosal sódico como conservante, para mantener una concentración final del 0,01%. Esta concentración es adecuada para la acción antiséptica (0,01-0,02%) (3). Posteriormente se realiza una filtración esterilizante a través de un filtro de 0,22 micras. La adición de sulfito sódico, como antioxidante, no fue necesaria puesto que la concentración final del 0,025% se encuentra dentro de los márgenes recomendados (0,01-1%) (3).
Condiciones del estudio
Las condiciones de almacenamiento estudiadas fueron temperatura ambiente (25 °C) y refrigeración (4-8 °C). Ambas muestras se mantuvieron en recipientes de vidrio y protegidos de la luz puesto que la fenilefrina se altera en presencia de la luz. Para cada condición de almacenamiento se prepararon cuatro lotes.
En el estudio se analizó las condiciones requeridas para un colirio: estabilidad, pH (5,5-11,4), isotonicidad, esterilidad y ausencia de partículas.
Estabilidad
Para determinar la estabilidad fisico-química de la fenilefrina, la técnica elegida para la valoración analítica de las muestras fue la espectrofotometría UV-visible a 273 nm. La determinación de la concentración de fenilefrina se realizó a los tiempos 0 (inmediatamente, tras la preparación de la muestra), 2, 4, 7, 9, 11, 14, 17, 21, 25, 28, 31, 41, 45, 49, 52, 55 y 60 días. Se diluyó la muestra con H2SO4 0,5 M inmediatamente antes de cada lectura, hasta una concentración teórica de 0,01%, según procedimiento de la British Pharmacopeia (9).
La concentración de fenilefrina se calcula por extrapolación en una curva patrón, elaborada con concentraciones crecientes de fenilefrina comprendidas en un ámbito de 0,005 a 0,02% en H2S04 0,5 M. Se obtuvo un coeficiente de correlación r=0,9808, lo que demuestra la validez de la técnica en ese intervalo de concentraciones.
Además de las determinaciones de absorbancia realizadas a 273 nm se registraron los espectros UV-Visible entre 190 y 700 nm de las muestras analizadas al principio del estudio y a los 60 días.
Control de pH
El pH de las muestras se midió con el fin de conocer su evolución con el tiempo. Las medidas se realizaron en paralelo a las lecturas espectrofotométricas.
Control de osmolaridad
Se realizaron medidas de la osmolaridad al principio del estudio y a los 60 días.
Control de esterilidad
Desde un punto de vista microbiológico se comprobó la esterilidad del producto enviando muestras del corilio periódicamente al servicio de microbiología del hospital. Las muestras del colirio que se utilizaron fueron las recogidas quincenalmente en las consultas de oftalmología tras su utilización por el paciente. Estos colirios recogidos no guardaron condiciones especiales de conservación. Se empleó la técnica de siembra en un medio enriquecido de tioglicolato y posterior incubación en medios de agar-chocolate y Saboureaut para detectar el crecimiento de bacterias y hongos.
Ausencia de partículas
La ausencia de partículas en el colirio se analizó quincenalmente.
Análisis estadístico
Las medidas de cada lote fueron realizadas por duplicado. Los resultados obtenidos se expresan mediante la media aritmética (X)±el error estándar de la media (ESM), donde:
siendo:
an-1 la desviación estándar de la muestra.
n el número de medidas realizadas.
La determinación o no de la existencia de diferencias significativas entre los valores medios de las distintas determinaciones se ha realizado mediante el test estadístico de la «t» de Student. A partir del valor de «t» se calculó el nivel de significancia (p) con el siguiente criterio: significativo p<0,05 y no significativo p>0,05. Estos cálculos han sido realizados directamente por el programa de ordenador empleado para el procesamiento de datos (Instat).
RESULTADOS Y DISCUSIÓN
En la tabla 1 se recogen las concentraciones detectadas por espectrofotometría en los tiempos que se indican, así como la variación en tanto por ciento de la concentració inicial de cada muestra del estudio. Para los resultados obtenidos a tiempo cero (día de elaboración del colirio), se consideró una concentración de fenilefrina del 100%. Se observa que el colirio elaborado de fenilefrina mantiene el 96,57% de su concentración inicial a 25 °C y 99,89% a 4 °C a los 60 días de su elaboración. El porcentaje de concentración remanente está comprendido entre 94,97=108,22% a 25 °C y 98,63-108,32% a 4 °C. Estos valores se encuentran dentro del margen de variación, entre el 90-115% de la concentración inicial que permite la U.S.P. para una solución oftálmica (10).
Tabla 1. Variación de la concentración de colirio de fenilefrina 2,5% y porcentaje de concentración remanente con el tiempo, en diferentes condiciones de conservación. Los datos representan X ± ESM (n=4) | ||||
| Temperatura ambiente (25 °C) | Nevera (4 °C) | |||
| Tiempo (días) | Concentración Fenilefrina (%) | Concentración Remanente (%) | Concentración Fenilefrina (%) | Concentración Remanente (%) |
| 0 | 2,73 ± 0,032 | 100 | 2,70 ± 0,079 | 100 |
| 2 | 2,79 ± 0,068 | 102,14 | 2,92 ± 0,066 | 108,32 |
| 4 | 2,68 ± 0,031 | 98,05 | 2,81 ± 0,144 | 104,23 |
| 7 | 2,76 ± 0,024 | 101,25 | 2,82 ± 0,101 | 104,62 |
| 9 | 2,77 ± 0,192 | 101,48 | 2,96 ± 0,082 | 109,71 |
| 11 | 2,71 ± 0,055 | 99,20 | 2,89 ± 0,134 | 106,94 |
| 14 | 2,83 ± 0,054 | 103,65 | 2,82 ± 0,054 | 104,51 |
| 17 | 2,95 ± 0,129 | 108,22 | 2,83 ± 0,066 | 104,97 |
| 21 | 2,82 ± 0,088 | 103,43 | 2,66 ± 0,073 | 98,63 |
| 25 | 2,59 ± 0,083 | 94,87 | 2,73 ± 0,114 | 101,15 |
| 28 | 2,85 ± 0,251 | 97,71 | 2,74 ± 0,119 | 101,39 |
| 31 | 2,67 ± 0,018 | 98,74 | 2,75 ± 0,071 | 102,04 |
| 41 | 2,70 ± 0,036 | 95,54 | 2,73 ± 0,014 | 101,27 |
| 45 | 2,61 ± 0,127 | 97,14 | 276 ± 0,076 | 102,31 |
| 49 | 2,65 ± 0,102 | 98,40 | 290 ± 0,102 | 107,28 |
| 52 | 2,69 ± 0,014 | 102,28 | 2,80 ± 0,166 | 103,58 |
| 55 | 2,79 ± 0,079 | 102,28 | 2,77 ± 0,078 | 102,77 |
| 60 | 2,64 ± 0,074 | 96,57 | 2,70 ± 0,108 | 99,89 |
En la tabla 2 se reflejan los datos obtenidos de medidas de pH y osmolaridad durante los días y condiciones del estudio. El pH muestra una tendencia a disminuir desde valores de 7,41 (tiempo 0) hasta valores de 6,91 (60 días) a 25 °C; y desde valores de 7,50 (tiempo 0) hasta 6,98 (60 días) a 4 °C. En ambas condiciones hubo una disminución significativa del pH desde el principio hasta el final del estudio (p=0,0488 a 25 °C y p=0,0004 a 4 °C). A pesar de esta disminución, el pH se mantuvo dentro de los márgenes fisiológicos para el ojo y dentro de los especificados por la U.S.P.; por esto no consideramos necesario adicionar ningún tipo tampón ya contenido en el preparado comercial. Así mismo, la osmolaridad no varía significativamente desde el inicio hasta los 60 días de duración del estudio (p=0,90 a 25 °C y p=0,42 a 4 °C) manteniendo valores tolerables de 426 y 430 mOsm/Kg a 25 °C y 4 °C respectivamente.
Tabla 2. Valores de pH y osmolaridad de las muestras de fenilefrina al 2,5% según período y condiciones de conservación. | ||||
| Temperatura ambiente (25 °C) | Nevera (4 °C) | |||
| Tiempo (días) | pH | Presión Osmótica (mOsm/kg) | pH | Presión Osmótica (mOsm/kg) |
| 0 | 7,41 ± 0,034 | 426,5 ± 3,00 | 7,50 ± 0,040 | 430 ± 0,95 |
| 2 | 7,28 ± 0,045 | -- | 7,42 ± 0,014 | -- |
| 4 | 7,70 ± 0,750 | -- | 7,30 ± 0,072 | -- |
| 7 | 7,13 ± 0,091 | -- | 7,40 ± 0,037 | -- |
| 9 | 7,05 ± 0,090 | -- | 7,25 ± 0,060 | -- |
| 11 | 7,14 ± 0,087 | -- | 7,28 ± 0,069 | -- |
| 14 | 7,11 ± 0,073 | -- | 7,28 ± 0,028 | -- |
| 17 | 6,98 ± 0,076 | -- | 7,21 ± 0,210 | -- |
| 21 | 7,13 ± 0,063 | -- | 7,20 ± 0,033 | -- |
| 25 | 7,06 ± 0,052 | -- | 7,20 ± 0,017 | -- |
| 28 | 7,07 ± 0,066 | -- | 7,11 ± 0,010 | -- |
| 31 | 6,82 ± 0,061 | -- | 7,06 ± 0,050 | -- |
| 41 | 7,10 ± 0,074 | -- | 7,06 ± 0,030 | -- |
| 45 | 7,17 ± 0,051 | -- | 7,30 ± 0,060 | -- |
| 49 | 7,12 ± 0,150 | -- | 6,64 ± 0,080 | -- |
| 52 | 7,00 ± 0,190 | -- | 6,88 ± 0,480 | -- |
| 55 | 6,95 ± 0,075 | -- | 6,71 ± 0,140 | -- |
| 60 | 6,91 ± 0,200 | 426 ± 2,45 | 6,98 ± 0,068 | 429 ± 2,85 |
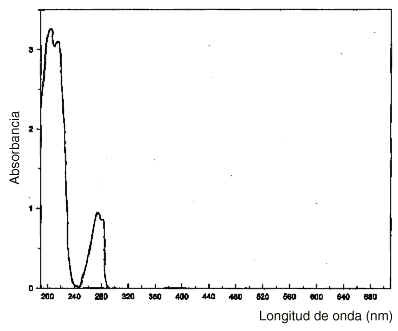
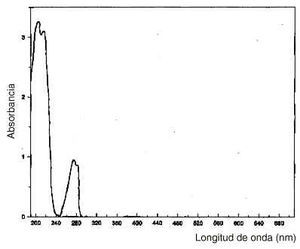
En la figura 1 puede observarse el espectro de absorción UV-visible (190-700 nm) del colirio de fenilefrina al 2,5% a 25 °C y 4 °C, a una concentración de 0,01% en H2S04 0,5 M, en el momento de iniciarse el estudio y a los 60 días. En el espectro de absorción puede apreciarse un máximo de absorción a 200 nm y un mínimo a 275 nm. Durante el tiempo que duró el estudio y en las condiciones definidas no se observaron variaciones cualitativas ni cuantitativas, lo que parece indicar que no se produjo ninguna sustancia de degradación. Las muestras para el estudio microbiológico se tomaron a partir de colirios abiertos que ya se habían utilizado, con el fin de conocer la eficacia del conservante en la práctica habitual. Los resultados indican que el timerosal a la concentración de 0,01% es apropiada.
Figura 1.--Espectro de absorción UV-visible del colirio de fenilefrina en H2SO4 0,5 M a temperatura ambiente (25 oC) y en nevera (4 °C); t = 0; t = 60 días.
Durante el período de estudio no se ha apreciado crecimiento microbiológico alguno ni presencia de partículas que fueran indicativos de posibles alteraciones del producto.
Como conclusión del presente estudio se establece una caducidad de al menos 60 días en cualquiera de las formas de conservación estudiadas (25 °C o 4 °C) para el colirio de fenilefrina al 2,5% elaborado a partir del comercializado al 10%. Esto evita la necesidad de preparar dosis extemporáneas previas a cada administración.
BIBLIOGRAFÍA
1. Unidad de Información de Medicamentos. Instituto Nacional de Salud de Asturias. Selección y utilización de Medicamentos. Tomo II. Principado de Asturias. Eujoa; 1994. p. 128.
2. American Society of Hospital Pharmaceutics: ASFS drug information 95. Ed. Staff. American Society of Health-system Pharmacists 1997:2196-2200.
3. Martindale: The extra pharmacopoeia, 28.a ed. London: The Pharmaceutical Press; 1982. p. 23-5.
4. Mirmanesh SJ, Abbasi S and Bhutani VK. Alpha-adrenergic bronchoprovocation in neonates with bronchopulmonary dysplasia. J Pediatr 1992; 121:622-5.
5. Fraunfelder FT and Meyer SM. Systemic reactions to opthalmic drug preparations. Med Toxicol Adverse Drug Exp 1987;2:287-93.
6. Craig EW and Griffiths PG. Effect on mydriasis of modifying the volume of phenylephrine drops. Br J Ophthalmol 1991;75:222-3.
7. Paggiarino DA, Brancato LJ and Newton RE. The effects on pupil size and accomodation of sympathetic and parasympatholytic agents. Ann Ophthalmol 1993; 25:244-9.
8. Lynch MG, Brown RH, Goode SM, Schoenwald RD and Chien DS. Reduction of phenylephrine drop size in infants achieves equal dilation with decreased systemic absorption Arch Ophthalmol 1987; 105:1364-5.
9. B.P. 1988 vol I:436.
10. U.S.P. XXI edition: 829.