Evaluar la efectividad y seguridad del esquema FLAG-IDA en pacientes con leucemias agudas refractarias o recidivantes.
MétodoEstudio observacional descriptivo retrospectivo en el que se revisaron las historias clínicas de pacientes con el esquema FLAG-IDA en el periodo 2005-2010. La efectividad se evaluó mediante la respuesta objetiva, el intervalo libre de progresión y la supervivencia global. La seguridad se midió según el sistema de clasificación NCI, Criterios comunes de Toxicidad para Acontecimientos Adversos.
ResultadosFueron 12 pacientes (52,17 ± 8,26 años entre las mujeres y 54,83 ± 7,22 años en los hombres), 11casos fueron leucemias mieloides agudas (5 resistentes, 3 en recaída, una secundaria a leucemia mieloide crónica (LMC) resistente y 2 secundarias a síndrome mielodisplásico (SMD), de las que una fue resistente y la otra no había sido tratada previamente) y un caso de leucemia linfoide aguda (LLA) resistente. Seis pacientes (50%) alcanzaron una respuesta completa (RC). Un paciente consiguió una respuesta parcial (RP) tras la cual se administró otro protocolo indicado consiguiendo posteriormente una RC, 2 fallecieron por progresión de la enfermedad y 3 por complicaciones secundarias al tratamiento.
El intervalo libre de progresión para los pacientes que alcanzaron la RC fue de 24,38 semanas (6 meses). La mediana de supervivencia global fue de 8,4 semanas.
La media del tiempo necesario para la recuperación de la neutropenia fue de 23 y 37 días en el primer y segundo ciclo respectivamente. La media del tiempo necesario para la recuperación de la trombocitopenia fue de 24 y 35 días en cada ciclo.
ConclusionesEl esquema de inducción FLAG-IDA para el tratamiento de pacientes con leucemias de alto riesgo es un esquema establecido, bien tolerado y con una toxicidad aceptable que ofrece una oportunidad para optar al trasplante de progenitores hematopoyéticos.
To evaluate the effectiveness and safety of the FLAG-IDA regimen in patients with acute refractory and/or recurrent leukaemia.
MethodDescriptive, retrospective, observational study of the clinical histories of patients with the FLAG-IDA regimen during the period of 2005-2010. Effectiveness was measured using objective response, progression-free interval, and global survival. Safety was measured using the NCI classification system of common toxicity criteria for adverse events.
ResultsWe registered 12 patients (52.17±8.26 years in women, and 54.83±7.22 years in men), 11 cases were acute myeloid leukaemia (5 refractory, 3 in recurrence, 1 secondary to chronic refractory myeloid leukaemia (CML) and 2 secondary to myelodysplastic syndrome (MDS), one of which was refractory and the other had not been previously treated) and one case was acute refractory lymphoblastic leukaemia (ALL). Six patients (50%) reached a complete response (CR). One patient reached a partial response (PR), which was followed by another protocol that produced a CR, two died due to disease progression, and three due to secondary complications from treatment.
The progression-free interval for patients that reached a CR was 24.38 weeks (6 months). Median global survival was 8.4 weeks.
Mean time needed for the recovery of neutropenia was 23 and 37 days in the first and second cycle, respectively. The mean time required for recuperation of thrombocytopenia was 24 and 35 days in each cycle.
ConclusionsThe FLAG-IDA induction regimen for the treatment of high-risk leukaemia patients is an established protocol, with good tolerance and acceptable toxicity levels that offers an opportunity for facilitating the transplantation of haematopoietic progenitors.
La leucemia aguda resistente o recidivante ha sido siempre un reto para los hematólogos. En la pasada década se desarrollaron regímenes que contenían fludarabina combinada con Ara-C para el tratamiento de las leucemias agudas, síndromes mielodisplásicos (SMD) y casos de leucemias agudas resistentes o recidivantes1,2. Fludarabina y Ara-C (FA) fueron ensayados por primera vez en 1991. En 1992 se añadieron al esquema FA los factores estimulantes de colonias (G-CSF) resultando la combinación FLAG. Por último, el fármaco idarrubicina se combinó con FA con o sin G-CSF.
La utilización de estos regímenes (FLAG y FLAG-IDA)3–5 en LMA de mal pronóstico, SMD y LLA resistente y/o recidivante, ha logrado alentadores resultados6–8 con una toxicidad siempre aceptable. Sin embargo, la fludarabina no cuenta con este uso entre sus indicaciones aprobadas.
El trifosfato de fludarabina, el metabolito activo de la fludarabina, inhibidores de la ribonucleótido reductasa y la acumulación intracelular del trifosfato de citarabina son factores que contribuyen a la eficacia de este régimen9,10. Se ha encontrado una relación entre los niveles de trifosfato de citarabina intracelular y los índices de remisión de la enfermedad.
La utilización de G-CSF previo a fludarabina aumenta el número de células en división, que son más vulnerables a Ara-C y mejora la incorporación del Ara-C al DNA11,12. Idarrubicina se utiliza porque es menos susceptible a la multirresistencia en células leucémicas humanas comparado con otras antraciclinas13,14.
En la mayoría de LMA, al igual que muchos casos de LLA, la resistencia a los tratamientos se relaciona con múltiples genes y rutas genéticas. Cerca de 100 genes han sido asociados al fallo de tratamientos, de los que más de 20 están relacionados con rutas específicas de señales de transducción. En las leucemias agudas, al igual que en otras neoplasias hematológicas, las recaídas están asociadas con la aparición de clones de células resistentes. En los pacientes que consiguen una remisión completa (RC), el riesgo de recaída es actualmente del 45-50%, pero esta cifra es muy variable15.
En niños con LLA el periodo de tiempo libre de progresión (EFS) y el índice de supervivencia global son del 80% con las estrategias de tratamiento actuales. Sin embargo, en las recaídas, la tasa de curación global es de solo el 35%16. Los pacientes que progresan tras la inducción inicial raramente o nunca se curan con quimioterapias posteriores. El trasplante de progenitores hematopoyéticos (TPH) ha supuesto la curación del 10-20% de estos pacientes17.
Protocolos terapéuticos como el FLAG-IDA se han postulado como regímenes de quimioterapia de inducción en caso de LMA secundarias o en presencia de cariotipo desfavorable con buenos resultados, aunque todavía están pendientes de comparar en estudios prospectivos con los esquemas clásicos.
El objetivo principal de este estudio es evaluar la efectividad del esquema FLAG-IDA en pacientes con leucemias agudas resistentes y/o recidivantes. La variable principal para medir la efectividad fue la respuesta objetiva y las variables secundarias el intervalo libre de progresión y la supervivencia global. El objetivo secundario es evaluar el perfil de seguridad del esquema FLAG-IDA según criterios de toxicidad para acontecimientos adversos del National Cancer Institute.
Material y metodosEstudio observacional descriptivo retrospectivo, en el que se han revisado las historias clínicas de los pacientes que iniciaron tratamiento con fludarabina dentro del esquema de inducción FLAG-IDA, desde el año 2005 hasta el 2010 en un hospital de especialidades de 605 camas. Los pacientes se seleccionaron de una base de datos del servicio de farmacia llamada «Medespe» donde se registran las utilizaciones de medicamentos en indicaciones diferentes a las autorizadas.
El protocolo FLAG-IDA consiste, según el Grupo Español de SMD y PETHEMA SMD/9818, en: 30mg/m2 de fludarabina y 2g/m2 de citarabina durante 4 días consecutivos (días 1 a 4), 10mg/m2 de idarubicina 3 días consecutivos (día 1 a 3) y 300μg/m2 de factor estimulante de colonias G-CSF del día 0 hasta el día 5.
Las variables recogidas fueron: 1) variables demográficas: sexo y edad en que se aplica el fármaco; 2) variables relacionadas con el diagnóstico: fecha y edad al diagnóstico, se analiza también si el tratamiento se aplica al diagnóstico, tras progresión de la enfermedad o tras una recaída; 3) variables relacionadas con el tratamiento: la variable principal de efectividad fue la respuesta objetiva según criterios del Standard National Cancer Institute19. Como variables secundarias se midieron el intervalo libre de progresión y la supervivencia global.
Se evaluó la tasa de pacientes que alcanzó respuesta completa según los mejores criterios encontrados en la bibliografía, para lo que se definieron los siguientes términos:
- (a)
RC (respuesta completa) en LA de alto riesgo y SMD: recuento de blastos < 5% en médula ósea de morfología normal, con citogénesis normal.
- (b)
RC en el caso de LMC con crisis de blastos: recuento de blastos < 5% y la pérdida alguna nueva estructura (sin embargo, los análisis citogenéticos del paciente pueden permanecer Ph+ o BCR/ABL positivo en los análisis moleculares).
- (c)
RP (respuesta parcial): recuento de blastos 5-15% y/o la persistencia de alguna anteración citogenética.
- (d)
Enfermedad resistente: recuento de blastos > 15%.
La seguridad se evaluó identificando en tipo y número los efectos adversos producidos por el tratamiento, principalmente los de tipo hematológico como anemia, neutropenia y trombocitopenia, clasificando su intensidad según el sistema de clasificación NCI Criterios comunes de Toxicidad para Acontecimientos Adversos (NCI, 1988).
Se consideró la recuperación de la neutropenia al alcanzar valores de neutrófilos superiores a 0,5 × 109/l y la recuperación de la trombocitopenia al alcanzar valores de plaquetas superiores a 50 × 109/l.
Se contabilizó el número de concentrados de hematíes y de plaquetas que se transfundieron a cada paciente para conseguir la recuperación hematológica (valores superiores a 8g/dl).
El análisis estadístico de los datos es descriptivo y se llevó a cabo mediante el paquete estadístico SPSS® versión 15.0 para Windows®. Al tratarse de estadística descriptiva los valores de las variables se expresaron como medianas, rangos, porcentajes y frecuencias.
La realización de este estudio fue aprobada por el Comité Ético de Investigaciones Clínicas del hospital, que consideró necesario el consentimiento informado de los pacientes.
Además, los datos de carácter personal de todos los sujetos participantes se trataron según lo dispuesto en la Ley Orgánica 15/1999, de 13 de diciembre de protección de datos de carácter personal.
ResultadosCaracterísticas de los pacientes, la enfermedad y el tratamientoSe identificaron 12 pacientes en tratamiento con el esquema de inducción FLAG-IDA. Del total de pacientes seleccionados el 50% (6) eran mujeres y el otro 50% (6) eran hombres. La media de edad en el momento en que inician el tratamiento con este esquema en las mujeres fue de 52,17 ± 8,26 años y en los hombres 54,83 ± 7,22 años.
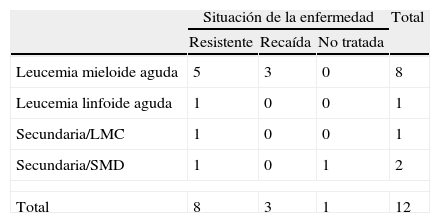
Se utilizó el esquema de inducción FLAG-IDA en 11 casos de LMA (5 fueron LMA resistentes, 3 en recaída, una secundaria a LMC resistente y 2 secundarias a SMD, de las que una fue resistente y la otra no había sido tratada previamente) y un caso de LLA resistente (tabla 1)
En los pacientes en los que se utilizó FLAG-IDA tras resistencia, la quimioterapia previa utilizada fue el protocolo ICE (idarubicina, Ara-C y etopósido) con el que no se consiguió una respuesta completa. En los casos en que se utilizó tras recaída, la quimioterapia previa fue variable.
Se completó un solo ciclo en el 50% de los pacientes, en los que se administraron las dosis completas en todos ellos excepto en uno por toxicidad hematológica. En el otro 50% de los pacientes se completaron los 2 ciclos y se administraron las dosis completas en todos ellos.
EfectividadEn cuanto a la respuesta objetiva, seis pacientes (50%) alcanzaron una respuesta completa (RC). Uno consiguió una respuesta parcial (RP) tras la cual se administró otro protocolo indicado (FLAT: fludarabina, ARA-C y topotecán) consiguiendo posteriormente una RC, dos pacientes fallecieron por progresión de la enfermedad y tres por complicaciones secundarias al tratamiento.
De los pacientes que alcanzaron una RC, uno (8,33%) falleció por complicaciones hemorrágicas como reacción adversa del tratamiento, uno (8,3%) falleció por progresión de la enfermedad, 3 (25%) sufrieron una recaída, y uno (8,3%) fue trasladado a otro centro sin haber presentado hasta entonces signos de recaída (tabla 2).
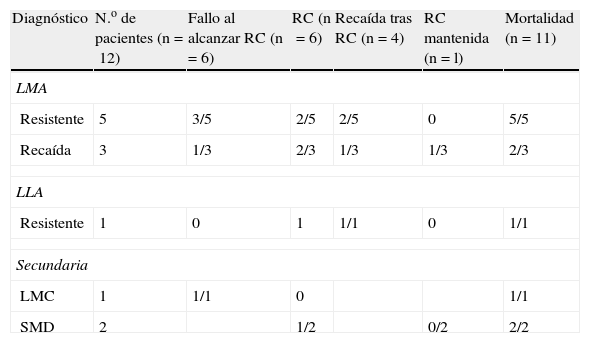
Respuesta objetiva
| Diagnóstico | N.o de pacientes (n=12) | Fallo al alcanzar RC (n=6) | RC (n=6) | Recaída tras RC (n=4) | RC mantenida (n=l) | Mortalidad (n=11) |
| LMA | ||||||
| Resistente | 5 | 3/5 | 2/5 | 2/5 | 0 | 5/5 |
| Recaída | 3 | 1/3 | 2/3 | 1/3 | 1/3 | 2/3 |
| LLA | ||||||
| Resistente | 1 | 0 | 1 | 1/1 | 0 | 1/1 |
| Secundaria | ||||||
| LMC | 1 | 1/1 | 0 | 1/1 | ||
| SMD | 2 | 1/2 | 0/2 | 2/2 | ||
LLA: leucemia linfoide aguda; LMA: leucemia mieloide aguda; LMC: leucemia mieloide crónica; RC: remisión completa; SMD: síndrome mielodisplásico.
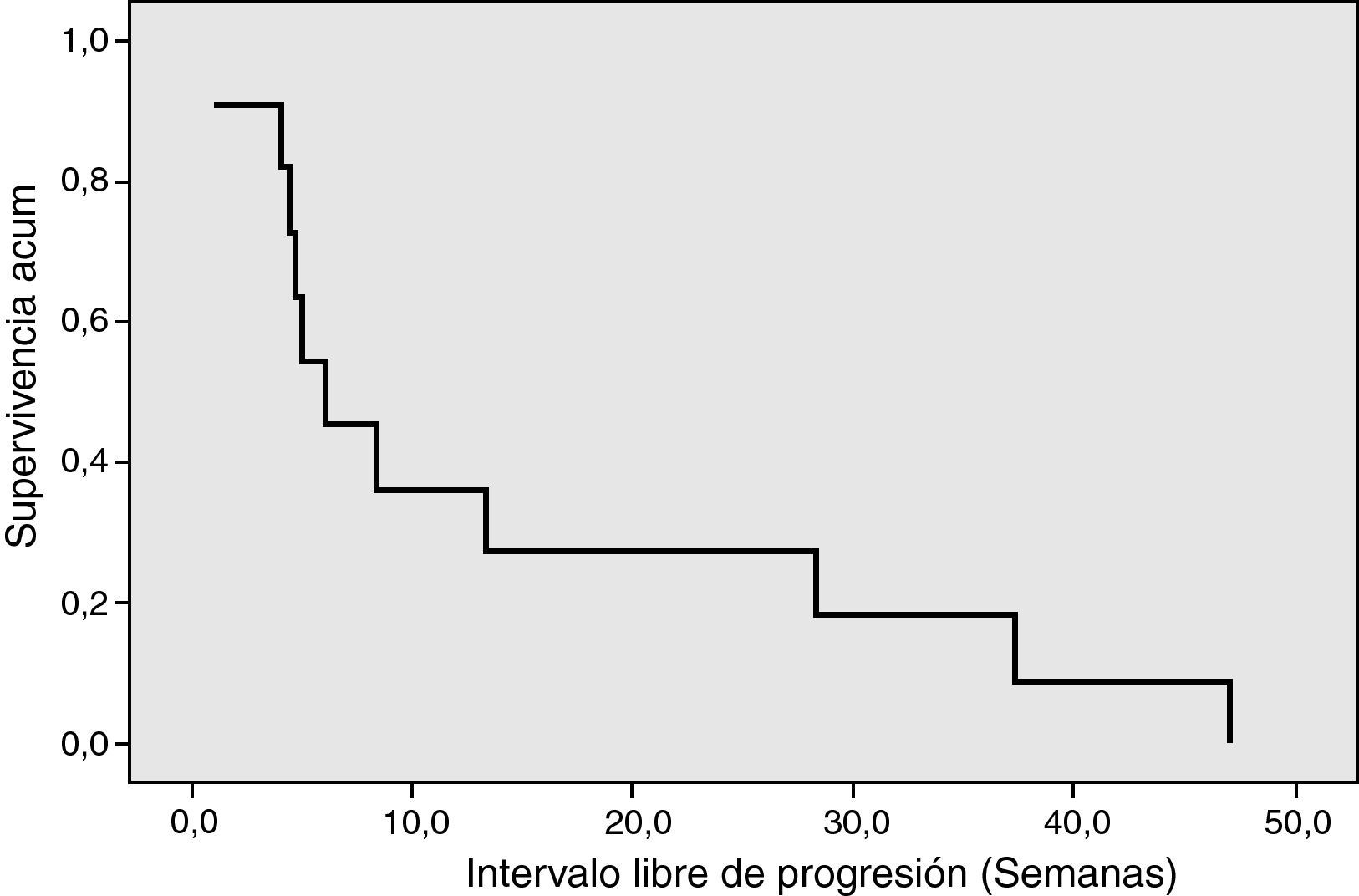
El intervalo libre de progresión para los pacientes que alcanzaron la RC fue de 24,38 semanas (6 meses) y para todos los pacientes en global fue de 6,1 semanas.
La mediana de la supervivencia global para los pacientes que alcanzaron la RC fue de 26 semanas y para todos los pacientes fue de 8,4 semanas.
SeguridadEn cuanto a la seguridad, la toxicidad observada fue principalmente anemia, neutropenia y trombocitopenia.
Toxicidad en el primer cicloLa media de los valores de hemoglobina más bajos alcanzados en cada paciente fue de 8g/dl. La anemia presentada en los pacientes fue de grado 2 en el 58,3% (7) de los pacientes y de grado 3 en el 41,3% (5). La mediana de concentrados de hematíes que fueron transfundidos a los pacientes durante el mes consecutivo a la administración de la quimioterapia, fue de 11 concentrados con un máximo de 22 y un mínimo de 7.
La media de los valores de neutrófilos totales más bajos alcanzados en cada paciente fue de 0,009 ± 0,01 × 109/l neutrófilos. La neutropenia presentada en los pacientes fue en todos los casos de grado 4. La media del tiempo necesario para la recuperación de la neutropenia (neutrófilos > 0,5 × 109/l) fue de 22,7 ± 9 días y en el 33,3% (4) de los pacientes no se llegó a alcanzar dicha recuperación.
La media de los valores de plaquetas más bajos alcanzados en cada paciente fue de 8 × 109/l. La trombocitopenia fue por tanto de grado 4 en todos los pacientes. La media del tiempo necesario para la recuperación de la trombocitopenia (plaquetas > 50 × 109/l) fue de 24,3 ± 7 días y en el 41,6% (5) de los pacientes no se llegó a alcanzar dicha recuperación. La mediana de concentrados de plaquetas transfundidos fue de 22 con un máximo de 63 y un mínimo de 3.
Toxicidad en el segundo cicloDe los 12 pacientes del estudio 6 llegaron a completar el segundo ciclo.
La media de los valores de hemoglobina más bajos alcanzados en cada paciente fue de 7,9 ± 1,13g/dl. La anemia presentada en los pacientes fue de grado 2 en el 66,6% de los pacientes, de grado 3 en el 16,6% y de grado 4 en el 16,6%. La mediana de concentrados de hematíes que fueron transfundidos a los pacientes durante el mes consecutivo a la administración de la quimioterapia fue de 8 concentrados con un máximo de 15 y un mínimo de ninguno.
La media de los valores de neutrófilos totales más bajos alcanzados en cada paciente fue de 0,002 ± 0,003 × 109/l neutrófilos. La neutropenia presentada en los pacientes fue en todos los casos de grado 4. La media del tiempo necesario para la recuperación de la neutropenia* fue de 37 días y en el 16,6% (1) de los pacientes no se llegó a alcanzar dicha recuperación.
La media de los valores de plaquetas más bajos alcanzados en cada paciente fue de 9,6±5,3 × 109/l. La trombocitopenia fue de grado 4 en todos los pacientes. La media del tiempo necesario para la recuperación de la trombocitopenia fue de 35,5±4,4 días y en el 33,3% (2) de los pacientes no se llegó a alcanzar dicha recuperación. La mediana del número de concentrados de plaquetas recibidos fue de 8,5 concentrados con un máximo de 45 y un mínimo de ninguno.
La tabla 3 muestra la incidencia de toxicidades no hematológicas de grados III-IV. La principal toxicidad fue gastrointestinal, sobre todo náuseas y vómitos.
Hubo 4 (33,3%) muertes relacionadas con el tratamiento, es decir, muertes como consecuencia de una complicación del tratamiento que no se recupera.
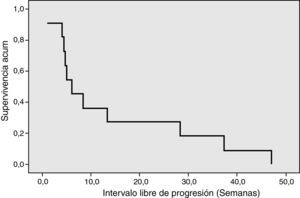
La figura 1 muestra la curva de supervivencia de Kaplan-Meier, que relaciona la supervivencia acumulada y el intervalo libre de progresión en semanas.
DiscusiónAunque se han conseguido importantes avances en el tratamiento de novo de las leucemias agudas, el tratamiento de las leucemias agudas resistentes y/o en recidivantes y leucemias mieloides agudas en transformación blástica es aún complicado. En la práctica médica habitual estos casos son tratados con regímenes de quimioterapia que contienen fludarabina consiguiendo buenos resultados20.
En la actualidad en nuestro hospital los pacientes con estos diagnósticos son tratados con FLAG-IDA, donde la fludarabina se utiliza en una indicación diferente a la autorizada.
El esquema FLAG-IDA se ha postulado como régimen de quimioterapia de inducción en caso de LMA secundarias o en presencia de cariotipo desfavorable con buenos resultados, aunque todavía están pendientes de comparar en estudios prospectivos con los esquemas clásicos.
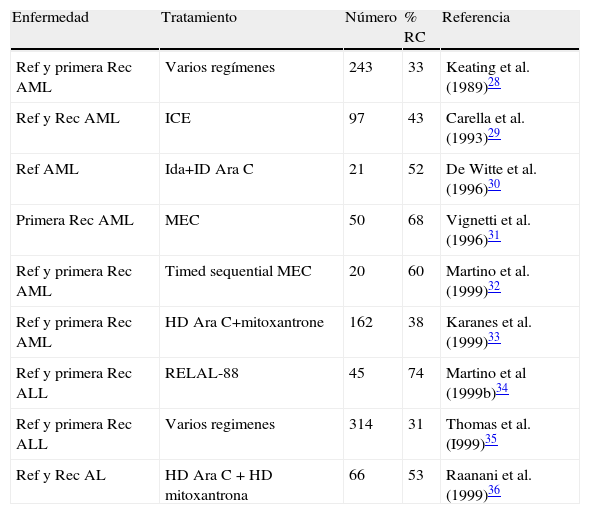
En estudios con otros regímenes de quimioterapia para las mismas indicaciones, el índice de RC está en un rango de 31-74%21. Nuestro resultado (50%) en cuanto a índice de RC es comparable al de estos estudios (tabla 4).
Índice de recaídas completas en leucemias agudas resistentes y en recaída en otros estudios publicados
| Enfermedad | Tratamiento | Número | % RC | Referencia |
| Ref y primera Rec AML | Varios regímenes | 243 | 33 | Keating et al. (1989)28 |
| Ref y Rec AML | ICE | 97 | 43 | Carella et al. (1993)29 |
| Ref AML | Ida+ID Ara C | 21 | 52 | De Witte et al. (1996)30 |
| Primera Rec AML | MEC | 50 | 68 | Vignetti et al. (1996)31 |
| Ref y primera Rec AML | Timed sequential MEC | 20 | 60 | Martino et al. (1999)32 |
| Ref y primera Rec AML | HD Ara C+mitoxantrone | 162 | 38 | Karanes et al. (1999)33 |
| Ref y primera Rec ALL | RELAL-88 | 45 | 74 | Martino et al (1999b)34 |
| Ref y primera Rec ALL | Varios regimenes | 314 | 31 | Thomas et al. (I999)35 |
| Ref y Rec AL | HD Ara C + HD mitoxantrona | 66 | 53 | Raanani et al. (1999)36 |
ALL: leucemia linfoblástica aguda; AML: leucemia mieloide aguda; HD: high dose (altas dosis); HD Ara C y etopósido; ICE: idarubicina, Ara C y etopósido; ID: intermediate dose (dosis intermedia); ID Ara C: prednisolona y metotrexato; LA: leucemia aguda; MAE: mitoxantrona; MEC: mitoxantrona, etopósido y Ara C; Rec: recaída; Ref: resistente; RELAL-88: vindesina, mitoxantrona, ciclofosfamida.
De la misma manera podemos comparar nuestros datos con estudios llevados a cabo con FLAG-IDA en leucemias agudas resistentes y/o recidivantes.
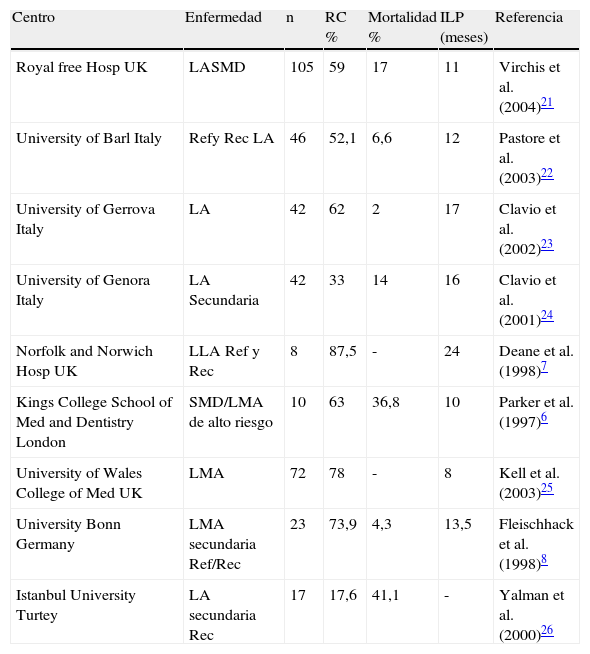
Los datos publicados son variables21–27. Los índices de RC oscilan en un rango que va desde el 17,6% como valor más bajo en el estudio de Yalman et al. (2000) hasta el 87,5% como valor más elevado en el estudio de Deane et al. (1998) en Norfolk y Norwich Hospital UK. Nuestro resultado de un 50% de RC es un resultado intermedio (tabla 5).
Índice de recaídas completas y mortalidad en leucemia aguda (LA) resistentes (Ref) y en recaída (Rec) tratadas con FLAG-IDA en otros estudios publicados
| Centro | Enfermedad | n | RC % | Mortalidad % | ILP (meses) | Referencia |
| Royal free Hosp UK | LASMD | 105 | 59 | 17 | 11 | Virchis et al. (2004)21 |
| University of Barl Italy | Refy Rec LA | 46 | 52,1 | 6,6 | 12 | Pastore et al. (2003)22 |
| University of Gerrova Italy | LA | 42 | 62 | 2 | 17 | Clavio et al. (2002)23 |
| University of Genora Italy | LA Secundaria | 42 | 33 | 14 | 16 | Clavio et al. (2001)24 |
| Norfolk and Norwich Hosp UK | LLA Ref y Rec | 8 | 87,5 | - | 24 | Deane et al. (1998)7 |
| Kings College School of Med and Dentistry London | SMD/LMA de alto riesgo | 10 | 63 | 36,8 | 10 | Parker et al. (1997)6 |
| University of Wales College of Med UK | LMA | 72 | 78 | - | 8 | Kell et al. (2003)25 |
| University Bonn Germany | LMA secundaria Ref/Rec | 23 | 73,9 | 4,3 | 13,5 | Fleischhack et al. (1998)8 |
| Istanbul University Turtey | LA secundaria Rec | 17 | 17,6 | 41,1 | - | Yalman et al. (2000)26 |
Hubo 4 (33,3%) muertes relacionadas con el tratamiento. La mayoría de estas complicaciones eran de tipo infeccioso y/o hematológico. Esta cifra es también comparable con los datos publicados para otros estudios en los que los índices de mortalidad están en un rango de 2-41,1% (tabla 5)21–27.
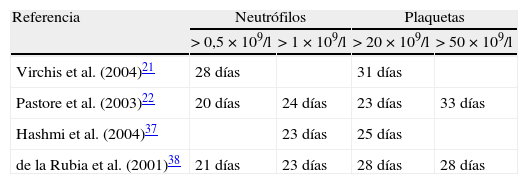
En el estudio el tiempo medio de recuperación de la neutropenia (neutrófilos > 0,5 × 109/l) y trombocitopenia (plaquetas > 50 × 109/l) en el primer ciclo fue 22,7 y 24,29 días respectivamente. No se alcanzó la recuperación de la neutropenia en 4 pacientes ni la recuperación de la trombocitopenia en 5. En el segundo ciclo los tiempos se prolongaron hasta 37 y 35,5 días, no alcanzándose la recuperación de la neutropenia en un paciente ni de la trombocitopenia en 2. Estos períodos de tiempo son comparables a los obtenidos en otros estudios (tabla 6) aunque el tiempo para la recuperación hematológica es algo más largo en el caso de los segundos ciclos.
Los estudios señalan que el trasplante de progenitores hematopoyéticos (TPH) de forma temprana, seguido de reinducción con quimioterapia, constituye una estrategia efectiva en pacientes de alto riesgo26. En nuestro centro los pacientes con un donante emparentado con HLA compatible fueron sometidos a alo-TPH consiguiéndose un aumento significativo en la supervivencia. En todos estos pacientes es probable que suceda una segunda remisión de la enfermedad, por lo que es importante tener en cuenta lo antes posible el tipo de HLA de los familiares.
A la vista de los resultados obtenidos, el esquema de inducción FLAG-IDA utilizado para el tratamiento de pacientes con leucemias de alto riesgo (leucemias mieloides agudas de mal pronóstico, síndromes mielodisplásicos [SMD] y leucemias linfoides agudas resistentes y/o recidivantes) puede considerarse un esquema efectivo que ofrece una oportunidad para optar al trasplante de progenitores hematopoyéticos. En cuanto a la seguridad, este régimen parece ser más mielotóxico comparado con otras opciones de quimioterapia convencional de inducción, sin embargo la toxicidad es aceptable ya que permite en la mayor parte de los pacientes recibir tratamiento adicional, incluyendo trasplante de progenitores hematopoyéticos.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.