ORIGINALES
EFECTIVIDAD DE LA QUIMIOTERAPIA ADYUVANTEEN PACIENTES CON SARCOMA DE TEJIDOS BLANDOS
Ferriols Lisart, R., Licenciado en Farmacia. Farmacéutico Adjunto. Servicio de Farmacia. Hospital Comarcal de Vinarós. Castellón.Ferriols Lisart, F.,Doctor en Farmacia. Servicio de Farmacia. Hospital Clínico Universitario. Valencia.
XLIII Congreso de la SEFH. Granada, Octubre de 1998
Correspondencia: Rafael Ferriols Lisart. Servicio de Farmacia. Hospital Comarcal de Vinaròs. Avda. Gil de Atrocillo, s/n. 12500 Vinaròs (Castellón).
Fecha de recepción: 29-07-98
Nota: Parte de este trabajo ha sido objeto de una comunica-ción preliminar al XLIII Congreso de la SEFH. Granada, octubre de 1998.
Palabras clave: Sarcoma de tejidos blandos. Quimioterapia. Supervivencia.
Resumen: En oncología, la selección de un determinado tratamiento debe basarse no sólo en la supervivencia alcanzada, sino también en la calidad de vida asociada, fundamentalmente, cuando las diferencias en la supervivencia no son significativas.
Objetivo: Evaluar la efectividad de la quimioterapia adyuvante en pacientes con sarcoma de tejidos blandos mediante el cálculo de los años de vida ganados ajustados a la calidad de vida.
Método: Se calculó el tiempo de supervivencia alcanzado sin síntomas de enfermedad y toxicidad, ajustado según la calidad de vida conseguida (Q-TWiST), como: Q-TWiST = uTOX*TOX + uTWiST *TWIST + uREL*REL; donde uTOX, uTWiST y uREL son los coeficientes de utilidad, TOX el tiempo transcurrido con síntomas de toxidad asociada al tratamiento y REL el tiempo con enfermedad metastásica evidente o recidiva. Se calculó la diferencia entre el Q-TWiST obtenido en los pacientes con sarcoma y quimioterapia adyuvante y el Q-TWiST del grupo control (sin quimioterapia) como indicador del tratamiento con mejor índice de efectividad. Los datos se obtuvieron a partir de un meta-análisis de 14 ensayos clínicos con 1.568 pacientes.
Resultados: Q-TWiSTquimioterapia = 39,54; Q-TWiSTcontrol = 36,24 meses; Q-TWiSTdiferencial = 3,3 meses.
Conclusión: La administración de quimioterapia adyuvante en pacientes con sarcoma de tejidos blandos no mejora la supervivencia total de forma significativa. Sin embargo, sí incrementa el tiempo sin recidivas y la supervivencia ajusta a la calidad de vida alcanzada.
EFFECTIVENESS OF ADJUVANT CHEMOTHERAPY IN PATIENTS WITH SOFT TISSUE SARCOMA
Key words: Soft tissue sarcoma. Chemotherapy. Survival.
Summary: Oncological treatment should be selected on the basis not only of survival time gained, but also with a view to quality of life, especially when the differences in survival are not significant.
Objective: To evaluate the effectiveness of adjuvant chemotherapy in patients with soft tissue sarcoma, by calculation of the years of life gained, adjusted for quality of life.
Method: We calculated survival time attained without symptoms of disease or toxicity, adjusted for quality of life (Q-TWIST) with the formula Q-TWIST = UTOX *TOX + UTWIST *TWIST + UREL *REL, where UTOX, UTWiST and UREL are coefficients of usefulness, TOX is the duration of symptoms of toxicity associated with treatment, and REL is the duration of evident or recurrent metastatic disease. We calculated the difference in Q-TWIST betwen patients with sarcoma treated with adjuvant chemotherapy and a control group (without chemotherapy) as an indicator of the treatment with the better effectiveness index. The data were obtained by meta-analysis of 14 clinical trials involving a total of 1.568 patients.
Results: Q-TWISTchemotherapy= 39.54 months; Q-TWISTcontrol = 36.24 months; Q-TWISTdifference = 3.3 months.
Conclusion: Adjuvant chemotherapy in patients with soft tissue sarcoma did not significantly improve total survival. However, it did increase the time to recurrence and survival adjusted for quality of life.
Farm Hosp 1999; 23: 53-56
INTRODUCCION
Los sarcomas de tejidos blandos son neoplasias del tejido mesenquimatoso, con una mortalidad del 50 % en los pacientes con enfermedad diseminada (1). Son más frecuentes en ancianos, de localización preferente en extremidades y de difícil diagnóstico inicial. Pueden ser clasificados como lipomas debido a que no provocan dolor ni alteración funcional o del estado de salud, a pesar de llegar a tener diámetros de hasta nueve centímetros (2). La quimioterapia adyuvante con doxorrubicina mejora el tiempo de enfermedad sin recidivas e igualmente muestra una tendencia a incrementar la supervivencia global de los pacientes. No obstante, en oncología, la selección de un determinado tratamiento no debe basarse sólo en la supervivencia alcanzada, sino también en la calidad de vida asociada, fundamentalmente, cuando las diferencias en la supervivencia no son significativas. El cálculo de los años de supervivencia ajustados a la calidad de vida (AVACs, QUALYs) se pueden obtener mediante el denominado análisis Q-TWiST (quality-adjusted time without symptoms and toxicity) que integra en un sólo parámetro la supervivencia, en calidad y cantidad, alcanzada permitiendo la comparación entre diferentes alternativas terapéuticas.
El objetivo del presente trabajo es evaluar la efectividad de la quimioterapia adyuvante en pacientes con sarcoma de tejidos blandos mediante el cálculo del Q-TWiST, que compara las diferencias obtenidas en la supervivencia, tanto en cantidad como en calidad de vida conseguida.
MÉTODO
Los datos se obtuvieron de un meta-análisis con 14 ensayos clínicos controlados y 1.568 pacientes (3). Todos los esquemas emplearon doxorrubicina (dosis media: 460 ± 90 mg/m2). En seis estudios se empleó la doxorrubicina en monoterapia, y en los restantes siete estudios se asoció a ciclofosfamida y otros citostáticos. Un estudio empleó la ifosfamida como monoterapia. Todos los estudios incluidos en el meta-analisis evaluaban el papel de la quimioterapia adyuvante en pacientes con sarcoma de tejidos blandos localmente resecable tras tratamiento local (3). La asignación de los pacientes a los grupos de tratamiento debía ser aleatoria, evaluándose los resultados obtenidos por intención de tratamiento.
Desde el diagnóstico del sarcoma hasta la muerte del paciente es posible identificar tres períodos de tiempo, asociados a distintos niveles de calidad de vida: tiempo con toxicidad (TOX), tiempo hasta la aparición de recidivas o muerte (DFS), y tiempo con enfermedad metastásica evidente o recidiva (REL), y que viene definido por REL = OS (supervivencia total) - DFS. A partir de estos valores, es posible definir el tiempo transcurrido sin síntomas de la enfermedad ni de toxicidad (TWiST) como DFS - TOX.
Así pues, es posible definir como índice de efectividad, el tiempo o supervivencia sin presencia de síntomas de enfermedad y toxicidad, ajustado a la calidad (Q-TWiST), como (4):
Q-TWiST = uTOX *TOX + uTWiST *TWiSTuREL *REL
donde uTOX, uTWiST y uREL son los coeficientes de utilidad, y reflejan el valor asumido para cada uno de los períodos de tiempo respecto al TWiST. El uTWiST es 1, puesto que se trata de un período de tiempo de salud relativamente óptima. Los valores utilizados en el análisis primario para uTOX y uREL son 0,5, que indica que un mes de supervivencia en TOX o REL es equivalente a medio mes con la mejor calidad de vida, la cual caracteriza al TWiST (5).
Se calculó la diferencia entre el Q-TWiST obtenido en los pacientes con sarcoma y quimioterapia adyuvante y el Q-TWiST del grupo control (sin quimioterapia) como indicador del tratamiento como mejor índice de efectividad (utilidad).
Se realizó un análisis del umbral de utilidad, que consiste en un análisis de sensibilidad para todo el intérvalo de los posibles valores de utilidad (0 a 1), calculándose el par de valores de los coeficientes de utilidad para el cual los dos tratamientos tienen igual Q-TWiST.
A partir de las curvas de supervivencia se calcularon los valores de OS y DFS a los 10 años de seguimiento, como las áreas bajo la curva (5). El valor de TOX empleado fue de tres meses.
RESULTADOS
Los pacientes evaluados eran, fundamentalmente, mayores de 31 años (77 %), con un sarcoma primario (74 %) de localización preferente en extremidades (58 %) o útero (17 %). Los pacientes recibieron tratamiento local más quimioterapia adyuvante o tratamiento local unicamente (grupo control). El tratamiento local consistió en cirugía con o sin radioterapia (el 47 % de los pacientes recibió radioterapia). La mediana de seguimiento de los ensayos clínicos incluídos en el meta-análisis fue de 9,4 años (4,9-17,6 años).
La tabla 1 muestra los resultados obtenidos en los distintos parámetros evaluados para cada uno de los grupos. La supervivencia global se incrementa sólo en 1,44 meses.
Tabla 1. Análisis Q-TWiST. Resultados expresados en meses, a los 10 años de seguimiento | |||||
| Grupo | TOX | TWiST | REL | OS | RFS |
| Quimioterapia | 3 | 35,28 | 2,52 | 40,80 | 38,28 |
| Control | 0 | 33,12 | 6,24 | 39,36 | 33,12 |
| TOX = tiempo con efectos tóxicos derivados del tratamiento; TWiST = tiempo sin síntomas ni toxicidad; REL = tiempo con enfermedad o recidiva; OS = supervivencia global; RFS = tiempo libre de recidivas. | |||||
Los valores de Q-TWiST obtenidos con valores de uTOX = uREL = 0,5, fueron Q-TWiSTquimioterapia = 39,54 meses; Q-TWiSTcontrol = 36,24 meses. Por lo tanto, el Q-TWiSTdiferencial = 3,3 meses. Este valor indica el tiempo de supervivencia ajustado a la calidad de vida ganado con la utilización de la quimioterapia adyuvante. Según estos resultados, la quimioterapia adyuvante provoca en los pacientes que la reciben efectos adversos o tóxicos (TOX) durante un período de tiempo de tres meses, pero se reduce el REL, puesto que tiene un efecto más significativo sobre el RFS (5,16 meses) que sobre la supervivencia total (OS). Por tanto, el tiempo transcurrido como Q-TWiST es mayor con la administración de quimioterapia adyuvante. Estos resultados están restringidos a un seguimiento de 10 años, y por los tres meses de duración de la toxicidad asociada a la quimioterapia adyuvante.
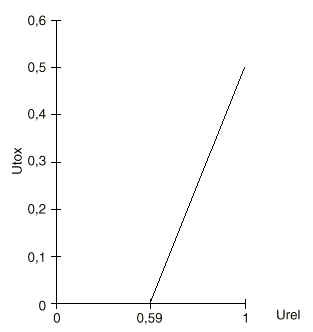
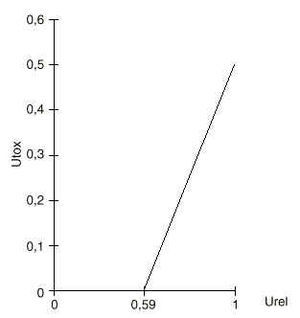
La figura 1 muestra el análisis del umbral de utilidad. La línea continua indica los valores de los coeficientes de utilidad para los cuales ambos tratamientos tienen igual Q-TWiST. Los valores superiores serán consistentes con un mayor valor de Q-TWiST para los pacientes que reciban quimioterapia. Por otra parte, los valores inferiores provocaran un Q-TWiST inferior al administrar la quimioterapia. Así pues, los pacientes que valoren mucho el tiempo con presencia de efectos tóxicos (uTOX = 0,8) y no den tanta importancia al tiempo transcurrido recidiva de la enfermedad (uREL = 0,7) obtendrán un beneficio con la administración de la quimioterapia adyuvante en términos de supervivencia ajustada a la calidad de vida alcanzada.
+Figura 1.--Análisis del umbral de utilidad. La línea indica los valores de los coeficientes de utilidad para los cuales las opciones evaluadas tienen igual Q-TWiST.
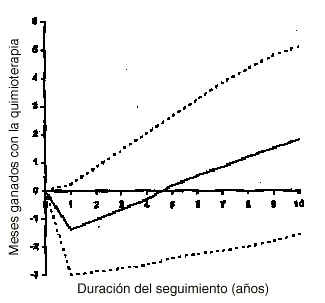
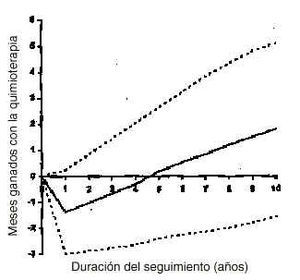
La figura 2 muestra los meses ganados de Q-TWiST con la administración de la quimioterapia adyuvante en función del tiempo de seguimiento. Inicialmente, la función es negativa debido a los efectos tóxicos de la quimioterapia administrada. Conforme avanza el tiempo de seguimiento, mejora la ganancia de Q-TWiST con la quimioterapia adyuvante. No obstante, el incremento de Q-TWiST es escaso, y estadísticamente no significativo.
Figura 2.--Variación del Q-TWiST. Meses de Q-TWiST ganados con la quimioterapia adyuvante respecto a la no administración, según la duración del seguimiento. Las líneas punteadas corresponden a los meses ganados cuando los coeficientes de utilidad varían entre 0 y 1.
DISCUSIÓN
La quimioterapia adyuvante se asocia con la aparición de efectos adversos que deben ser considerados respecto al beneficio que puedan aportar. Por ello, es importante poder disponer de métodos que nos permitan valorar y comparar diferentes alternativas terapéuticas basados en aspectos que reflejen la calidad de vida de los pacientes. El método Q-TWiST integra y cuantifica la calidad de vida y la supervivencia alcanzada, constituyéndose como una herramienta de gran utilidad para la comparación de esquemas quimioterápicos donde las diferencias en la supervivencia no son significativas, pero sí logran mejorar la calidad de vida durante este tiempo.
La administración de quimioterapia adyuvante basada en la doxorrubicina prolonga la supervivencia sin recidivas y muestra una tendencia a mejorar la supervivencia global. No obstante, no se evaluó el efecto sobre la supervivencia de la administración de la doxorrubicina en monoterapia o asociada a otros agentes citotóxicos. No es posible, por tanto, establecer que pauta o esquema quimioterápico es el más aconsejable. El efecto de la quimioterapia adyuvante es menos evidente sobre la supervivencia global que sobre los otros resultados (TWiST, REL y RFS). Esto puede ser atribuido al empleo de «terapias de rescate» durante el tiempo sin recidivas que mejoran la supervivencia (3). Cuando las recidivas son tratadas mediante cirugía local, por ejemplo una toracotomía en pacientes con metástasis pulmonares, se pueden producir diferencias en la incidencia de recidivas entre el grupo de tratamiento y el grupo control que afecten las estimaciones finales obtenidas. Si este factor se tiene en consideración, y está distribuido de forma equivalente entre ambos grupos de pacientes y presenta el mismo grado de efectividad, el impacto sobre la supervivencia será insignificante. No obstante, la utilización de quimioterapia durante el período sin recidivas puede ser más efectiva en los pacientes del grupo control, pues los tumores expuestos a quimioterapia adyuvante pueden ser resistentes al tratamiento, y por ello presentar una supervivencia proporcionalmente mayor. La utilización de dosis altas de quimioterapia para el tratamiento de sarcomas no esta, actualmente, bien establecida. La posible relación dosis-respuesta para la doxorrubicina, epirrubicina e ifosfamida no suele asociarse con respuesta objetivas completas ni en supervivencias más prolongadas (6).
El análisis Q-TWiST se realizó seleccionando de forma arbitraria los coeficientes de utilidad debido a que no fue posible obtener información sobre la valoración de la calidad de vida durante los períodos de TOX y REL a partir de los pacientes. El análisis del umbral de utilidad nos permite evaluar como influyen los coeficientes de utilidad sobre los resultados obtenidos.
Los efectos adversos más frecuentes fueron: leucopenia, alopecia, náuseas y vómitos, originando en algunos casos una reducción de dosis e incumplimiento por parte del paciente. También se observó toxicidad cardíaca, pero no se registró ninguna muerte asociada a esta causa.
En conclusión, la administración de quimioterapia adyuvante en pacientes con sarcoma de tejidos blandos no mejora la supervivencia total de forma significativa. Sin embargo, sí incrementa el tiempo sin recidivas y la supervivencia ajustada a la calidad de vida alcanzada.
BIBLIOGRAFIA
1. Rydholm A. Improvement the management of soft tissue sarcoma. BMJ 1998;317:93-4.
2 Antman KH. Adjuvant therapy of sarcomas of soft tissue. Semin Oncol 1997;24:556-60.
3 Sarcoma Meta-analysis Collaboration. Adjuvant chemotherapy for localised resectable soft-tissue sarcoma of adults: meta-analysis of individual data. Lancet 1997;350:1647-54.
4 Gelber R, Goldhirsch A, Cole B. Parametric extrapolation of survival estimates with applications to quality of life evaluation of treatments. Controll Clin Trials 1993;14:485-99.
5 Gelber R, Goldhirsch A, Cole B, et al. Evaluation of effectiveness: Q-TWiST. Cancer Treat Rev 1993;19 supl.A:73-84.
6 Elias AD. High-dose therapy for adult soft tissue sarcomas: dose-response and survival. Semin Oncol 1998; 25 supl.4:19-23.