Sr. Director:
La agranulocitosis y la neutropenia grave, acompañadas por una infección grave, constituyen la reacción adversa más grave y la principal causa de muerte relacionada con el tratamiento con tiamazol. A pesar de ser un efecto adverso descrito y conocido, consideramos de interés comunicar 4 casos de agranulocitosis en mujeres en tratamiento con tiamazol por hipertiroidismo secundario a enfermedad de Graves-Basedow. Los casos fueron detectados por revisión del diagnóstico de ingreso al servicio de clínica médica desde el 15 de septiembre de 2005 hasta el 28 de abril de 2006 (tabla 1).
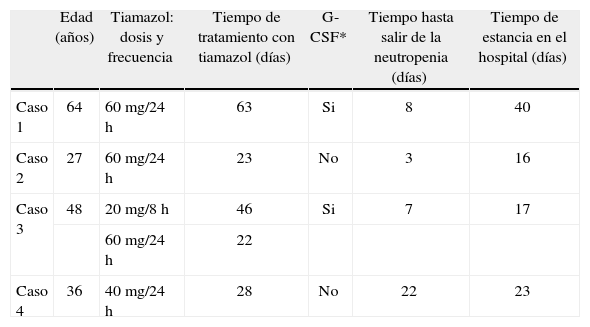
Resumen de las características de los pacientes
| Edad (años) | Tiamazol: dosis y frecuencia | Tiempo de tratamiento con tiamazol (días) | G-CSF* | Tiempo hasta salir de la neutropenia (días) | Tiempo de estancia en el hospital (días) | |
| Caso 1 | 64 | 60 mg/24 h | 63 | Si | 8 | 40 |
| Caso 2 | 27 | 60 mg/24 h | 23 | No | 3 | 16 |
| Caso 3 | 48 | 20 mg/8 h | 46 | Si | 7 | 17 |
| 60 mg/24 h | 22 | |||||
| Caso 4 | 36 | 40 mg/24 h | 28 | No | 22 | 23 |
Mujer de 64 años que consultó por encontrarse febril con escalofríos, rinorrea, odinofagia y mialgia. Se constató por el análisis de laboratorio un recuento de neutrófilos < 500/µl; el cuadro clínico se interpretó como neutropenia febril secundaria a tiamazol. Se suspendió la administración de tiamazol y se ingresó para su tratamiento. Inició tratamiento con ceftriaxona 2 g/12 h y amicacina 1 g/24 h, que continuó durante 5 días. A los 6 días de ingreso presentó un nuevo registro febril, por lo que se cambió a ceftazidima 2 g/8 h, vancomicina 1 g/12 h y metronidazol 500 mg/6 h por vía intravenosa durante 9 días, y se inició fluconazol 100 mg/24 h durante 7 días por lesiones blanquecinas en la boca y factor estimulante de colonias de granulocitos (Filgrastim) 300 µmg/día por vía subcutánea. Al noveno día de ingreso se constató el primer registro fuera de la neutropenia, suspendiéndose el Filgrastim. A los 17 días de ingreso se reinició el tratamiento antibiótico con ceftazidima 1 g/8 h y vancomicina 1 g/12 h por posible neumonía intrahospitalaria, que luego se cambió a imipenem 500 mg/6 h, concluyendo el tratamiento tras la evolución favorable de la paciente. A los 27 días de ingreso recibió 12 mCi 131I y fue dada de alta hospitalaria a los 40 días del ingreso.
Caso 2Mujer de 27 años de edad que consultó por encontrarse febril con odinofagia. Se verificó un recuento de neutrófilos < 500/µl; el cuadro clínico se explicó como neutropenia febril secundaria a tiamazol. Se suspendió la administración de tiamazol y se decidió el ingreso para su tratamiento. En el ingreso tenía fauces congestivas con placas blanquecinas, que se interpretó como foco orofaríngeo. Evolucionó favorablemente con tratamiento antibiótico (ceftriaxona 1 g/12 h durante 11 días), revirtiendo su neutropenia al tercer día de ingreso. A los 10 días del ingreso recibió 8 mCi 131I y 5 días más tarde se decidió el alta hospitalaria.
Caso 3Mujer de 48 años de edad que consultó por encontrarse febril con odinofagia, cefalea y mialgia. Se constató por los análisis de laboratorio un recuento de neutrófilos < 500/µl; el cuadro clínico se interpretó como neutropenia febril secundaria a tiamazol. Se suspendió la administración de tiamazol y se decidió el ingreso para su tratamiento. En el examen físico se observaron fauces congestivas con placas blanquecinas que se interpretaron como foco orofaríngeo y se inició tratamiento antibiótico con amoxicilina-ácido clavulánico 1 g/8 h y ciprofloxacino 750 mg/12 h por vía oral. Se administró factor estimulante de colonias de granulocitos (Filgrastim) 300 µg/día por vía subcutánea durante 6 días y se suspendió al primer registro fuera de neutropenia. Dado que la paciente continuó febril al septimo día de ingreso se cambió a ceftazidima 2 g/8 h y amicacina 1 g/ 24 h por vía intravenosa, y dos días más tarde se agregó ampicilina 2 g/8 h por vía intravenosa. Cuatro días después se cambió a la vía oral con amoxicilina-ácido clavulánico 500 mg/8 h y se le dió el alta hospitalaria con plan de captación de 131I.
Caso 4Mujer de 36 años de edad que consultó en urgencias por encontrarse febril con odinofagia, donde se le indicó tratamiento con penicilina. Tres días más tarde consultó al servicio de endocrinología por continuar febril y se constató por los análisis de laboratorio un recuento de neutrófilos < 500/µl; el cuadro clínico se interpretó como neutropenia febril secundaria a tiamazol. Se suspendió la administración de tiamazol y se decidió el ingreso para su tratamiento. Presentaba fauces congestivas y odinofagia, que se interpretaron como foco orofaríngeo, por lo que se inició tratamiento con amoxicilina-ácido clavulánico 1 g /8 h y ciprofloxacino 750 mg/12 h por vía oral. A los 14 días de tratamiento antibiótico presentó nuevos registros febriles, por lo cual se cambió a ceftazidima 2 g/8 h y amicacina 1 g/24 h, completando tratamiento durante 7 días. A los 23 días de ingreso presentó el primer registro fuera de la neutropenia, por lo cual se decidió su alta en plan de captación de 131I.
DiscusiónLa agranulocitosis (definida como un recuento absoluto de granulocitos < 500/µl) inducida por tiamazol afecta al 0,35% de los pacientes1, en la mayoría de los casos suele aparecer en los primeros 90 días de tratamiento; sin embargo, esta complicación puede ocurrir incluso un año o más después de comenzar la terapia.
Un aspecto que se debe tener en cuenta es el de las dosis de tiamazol; en nuestros pacientes se administraron dosis mayores de 40 mg/día. La agranulocitosis asociada con tiamazol es dependiente de la dosis y la incidencia de agranulocitosis con dosis bajas de tiamazol es 10 veces menor que con dosis altas2.
Durante el curso de esta reacción adversa, las infecciones se complican y dominan el cuadro; las orofaríngeas son las más comunes y los pacientes generalmente presentan fiebre y dolor de garganta3, por lo que se deben emplear antibióticos de amplio espectro y retirar inmediatamente el tiamazol.
Algunos estudios indican que el riesgo de agranulocitosis es mayor en pacientes de más de 40 años de edad1,2 y que estos tienen un riesgo superior de muerte. Sin embargo, sólo dos de nuestros pacientes coincidieron con este factor de riesgo, a diferencia de lo encontrado en otras publicaciones4.
El recuento sistemático de granulocitos en pacientes que reciben fármacos antitiroideos no ha sido considerado coste-efectivo, dado que la neutropenia se instaura muy rápidamente; sólo se recomienda realizar un recuento basal de leucocitos antes de iniciar la terapia con tiamazol.
Algunos autores señalan que la administración de G-CSF puede acortar el tiempo de recuperación y el tiempo de hospitalización en pacientes con agranulocitosis inducida por tiamazol5, aunque en un estudio prospectivo aleatorizado se mostró que no hay diferencias significativas en el tiempo de recuperación entre pacientes no tratados y tratados con G-CSF6. Algunas autoridades recomiendan la utilización de G-CSF para la agranulocitosis inducida por fármacos antitiroideos3,5,7,8 y el servicio de endocrinología de nuestro centro incluye la utilización de G-CSF en el tratamiento de neutropenia asociada con tiamazol. En nuestro caso, dos de las pacientes recibieron G-CSF y en los otros dos casos esto no fue posible dado que no se disponía de este medicamento en el hospital; sin embargo, en una de las pacientes que no recibió G-CSF la neutropenia revirtió y tuvo un tiempo de estancia en el hospital menor que el del paciente que sí recibió.
En conclusión, la agranulocitosis inducida por tiamazol es poco frecuente, pero tiene una alta morbilidad, el diagnóstico temprano muchas veces es difícil por la aparición brusca de la neutropenia que muchas veces antecede al cuadro clínico, y la presencia de fiebre y odinofagia hace sospechar esta complicación, por lo que los pacientes deben ser instruidos para suspender el fármaco y contactar de inmediato con el médico si desarrollan fiebre o dolor de garganta.