Analizar los informes de evaluación publicados en la página de Internet del Grupo de Evaluación de Novedades, Estandarización e Investigación en Selección de Medicamentos (GENESIS) y la variabilidad de sus propuestas sobre incorporación de medicamentos en la Guía Farmacoterapéutica.
MétodosSe analizaron los informes publicados por hospitales en la página web de GENESIS y elaborados de 2004 a 2007. Se recogió el medicamento e indicación, el grupo terapéutico, la publicación en abierto o con clave, el hospital y la fecha de realización. Se elaboró un cuestionario que medía la inclusión en el informe de los 9 apartados recomendados por GENESIS. De aquellos medicamentos con 2 o más informes se analizó si coincidían en la recomendación y la posible causa de discordancia.
ResultadosSe analizaron 416 informes correspondientes a 185 medicamentos-indicaciones diferentes. El 93% incluían 6 o más de los apartados recomendados, número que incrementó con el tiempo. Se incluían con más frecuencia (porcentajes de 2007) las indicaciones aprobadas (92%), el mecanismo de acción (95%) o la bibliografía (86%). Apartados cumplimentados en un porcentaje creciente aunque más bajo son características diferenciales (60%), método de búsqueda bibliográfica (40%) o conclusiones con resumen de eficacia, seguridad y coste (52%); un 73% tenían recomendaciones concretas. En 42 de los 67 medicamentos con más de un informe con recomendación, ésta coincidía.
ConclusionesLa actividad del grupo GENESIS ha contribuido a que los hospitales españoles compartan sus informes de evaluación de medicamentos y a que éstos sean más completos aunque existen aspectos mejorables.
To analyse the assessment reports published on the GENESIS webpage (Group for Innovation, Assessment, Standardisation and Research in the Selection of Drugs) and assess the variability of the group's proposals to include drugs in the Formulary.
MethodWe analysed reports published by hospitals on the GENESIS webpage between 2004 and 2007. Data were collected on drugs and indications, ATC group, open or restricted access publications, hospital, and publication date. We drafted a questionnaire that would measure to what extent to what extent the 9-section model recomended by GENESIS was included in each report. For drugs with two or more reports, we analysed whether the recommendation coincided and the possible cause in the event of conflict.
ResultsWe analysed 416 reports corresponding to 185 different drug indications. 93% included 6 or more of the recommended sections, a number which increased over time. The most frequently included sections were: approved indications (92%), mechanism of action (95%), and references (86%) (percentages from 2007). Sections which had an increasing but lower percentage were: differential characteristics (60%), literature search method (40%) and conclusions with a summary of efficacy, safety and cost data (52%). 73% of which had definite recommendations, which coincided for 42 out of the 67 drugs with more than one recommendation report.
ConclusionsThe work carried out by the GENESIS group has enabled Spanish hospitals to share their drug assessment reports and making them more complete, although there are still some aspects that can be improved.
La evaluación y selección de medicamentos constituye una de las herramientas principales de la política de medicamentos en los centros hospitalarios1. Las novedades terapéuticas de interés son estudiadas por las Comisiones de Farmacia y Terapéutica (CFT)1–4 para determinar si deben incluirse en la Guía Farmacoterapéutica (GFT). Los servicios de farmacia de los hospitales promueven y participan en la implantación y en el desarrollo de los procesos de selección de medicamentos5,6 que, tradicionalmente, se ha venido realizando en cada centro hospitalario de forma independiente, existiendo pocas experiencias de colaboración y coordinación entre centros.
En la actualidad, todos los aspectos vinculados con la información y la toma de decisiones en el sector salud están cada vez más interrelacionados. La necesidad de una mayor coordinación y colaboración entre los hospitales en nuestro ámbito llevó a la creación de un nuevo grupo de trabajo dentro de la Sociedad Española de Farmacia Hospitalaria (SEFH). Se trata del Grupo de Evaluación de Novedades, Estandarización e Investigación en Selección de Medicamentos (GENESIS) que se presentó en el 50° Congreso de la SEFH, realizado en Oviedo el mes de septiembre de 2005.
El grupo GENESIS ha desarrollado una metodología para la redacción de los informes de evaluación de nuevos fármacos, que se concreta en: un modelo de informe de evaluación de un nuevo fármaco, un manual de procedimientos y un programa de ayuda a la redacción del informe de evaluación de un nuevo medicamento, programa MADRE7.
El principal instrumento para la difusión de la metodología y de los informes de evaluación de GENESIS es la página de Internet, http://genesis.sefh.es. La página web permite el acceso a los informes de evaluación redactados por diferentes hospitales españoles desde el año 2004. Estos informes son remitidos por los miembros del grupo de trabajo y/o disponibles en páginas de Internet propias de cada hospital.
El presente proyecto de investigación tiene por objetivo analizar las características de los informes de evaluación publicados en la página de Internet de GENESIS y la variabilidad de las propuestas sobre incorporación de novedades terapéuticas en la Guía Farmacoterapéutica recogidas en los informes, para determinar el grado de seguimiento y la reproducibilidad de la metodología de elaboración de los informes y para detectar posibles oportunidades de mejora.
MétodosSe analizaron los informes publicados en la página web de GENESIS con fecha de realización de enero de 2004 a diciembre de 2007.
Se excluyeron del estudio aquellos informes en cuyo contenido únicamente se describían condiciones de uso anexas al informe principal o que son un complemento del informe inicial, no suponiendo una nueva revisión y evaluación.
De cada uno de los informes se recogieron los siguientes datos: el nombre del medicamento e indicación para la que se evalúa, si se trataba de un informe para una indicación concreta; el grupo terapéutico; la zona de publicación, azul (en abierto) o roja (con clave de acceso para miembros de GENESIS); el hospital que realizaba el informe y la fecha de realización, y si no estaba disponible, la de publicación del informe en la web de GENESIS. La publicación del informe en abierto o con clave de acceso corresponde a la voluntad del hospital autor del informe sin necesidad de justificar el motivo de su decisión.
Con objeto de analizar la adecuación de los informes al estándar metodológico propuesto por el grupo GENESIS, se elaboró un cuestionario que medía la existencia en cada informe de los apartados que define el modelo MADRE7. Para cada pregunta la respuesta podía ser: sí, no, dudoso o parcial, o no aplicable, y se podían añadir comentarios. La versión definitiva del cuestionario se elaboró tras realizar un test piloto con una muestra aleatoria de 30 informes.
Se cumplimentó este cuestionario para cada uno de los informes incluidos en el estudio. La cumplimentación fue repartida entre 13 revisores con unas instrucciones explícitas acerca del procedimiento a seguir y la interpretación de las preguntas. En caso de duda, el cuestionario era revisado por una única persona de referencia. El reparto de los informes entre los investigadores fue por orden alfabético de principio activo con el fin de que revisara la misma persona todos los informes de un mismo principio activo.
Se analizó el grado de cumplimiento de los diferentes apartados de todos los informes en conjunto y por grupos. Se establecieron grupos de acuerdo al año de realización del informe, ya que se consideró que el grado de cumplimiento de los apartados variaría con el tiempo, siendo menor antes de la publicación de las recomendaciones y guías metodológicas del grupo en 2005. También se establecieron grupos según la zona de acceso, roja y azul, y el grupo terapéutico, para analizar si ambos factores tenían alguna influencia en el seguimiento de las recomendaciones.
Con objeto de analizar la variabilidad de las propuestas incluidas en los informes sobre la incorporación o no a la guía farmacoterapéutica del hospital, se estudiaron aquellos medicamentos/indicaciones de los que se disponía de dos o más informes elaborados por diferentes hospitales. Se analizó si coincidían en la recomendación y, en caso de no coincidir, cuál se sospechaba que era la causa de la no coincidencia en la recomendación. En estos informes también se analizó si se citaban unos a otros.
Las variables cualitativas se presentan como número de casos y/o porcentajes, y las variables cuantitativas como media y desviación estándar, o como mediana, percentil 25 y percentil 75, según la distribución normal o no de la variable, utilizando para el análisis estadístico de las diferencias entre grupos χ2, t de Student o U de Mann-Whitney, según correspondiera.
ResultadosSe publicaron 435 informes en el periodo analizado. Se excluyeron del análisis 19 informes: uno por ser un producto sanitario, 6 por no poder acceder al informe, 5 por evaluar conjuntamente un grupo de medicamentos, 5 por ser actualización/complemento de otro informe, y 2 por ser documentos o resúmenes que no eran realmente un informe.
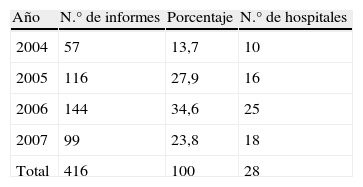
Por lo tanto, se evaluaron finalmente 416 informes correspondientes a 185 medicamentos-indicaciones diferentes. Existía más de un informe de 84 medicamentos-indicaciones diferentes. El reparto por años de los informes se muestra en la tabla 1. Un total de 287 informes (69%) se publicaron en el área azul y el resto en el área roja.
La procedencia de los informes se reparte entre 28 hospitales, de los cuales solo 12 y el grupo responsable de la edición de la Guía Farmacoterapéutica de Referencia de Andalucía enviaron más de 10 informes. El hospital más participativo envió 57 informes.
Los grupos terapéuticos con más informes fueron el L (terapia antineoplásica y agentes inmunosupresores), 25% de los informes, y el N (sistema nervioso) y J (terapia antiinfecciosa [uso sistémico]) con el 16% de los informes cada uno.
El seguimiento de los apartados del programa MADRE de GENESIS se muestra en las tablas 2 y 3. El detalle por apartados y por años se muestra en la tabla 4. En la tabla 5 se recoge el grado de cumplimiento de otros ítems evaluados relacionados con el contenido del informe que no constituyen un apartado o subapartado del programa MADRE en sí mismos.
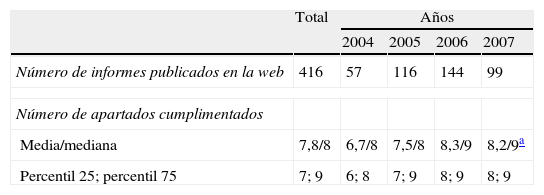
Número de informes publicados en la web de GENESIS y número de apartados cumplimentados en estos informes de los 9 apartados recomendados en el programa MADRE del grupo GENESIS, en total (durante los 4 años) y por años
| Total | Años | ||||
| 2004 | 2005 | 2006 | 2007 | ||
| Número de informes publicados en la web | 416 | 57 | 116 | 144 | 99 |
| Número de apartados cumplimentados | |||||
| Media/mediana | 7,8/8 | 6,7/8 | 7,5/8 | 8,3/9 | 8,2/9a |
| Percentil 25; percentil 75 | 7; 9 | 6; 8 | 7; 9 | 8; 9 | 8; 9 |
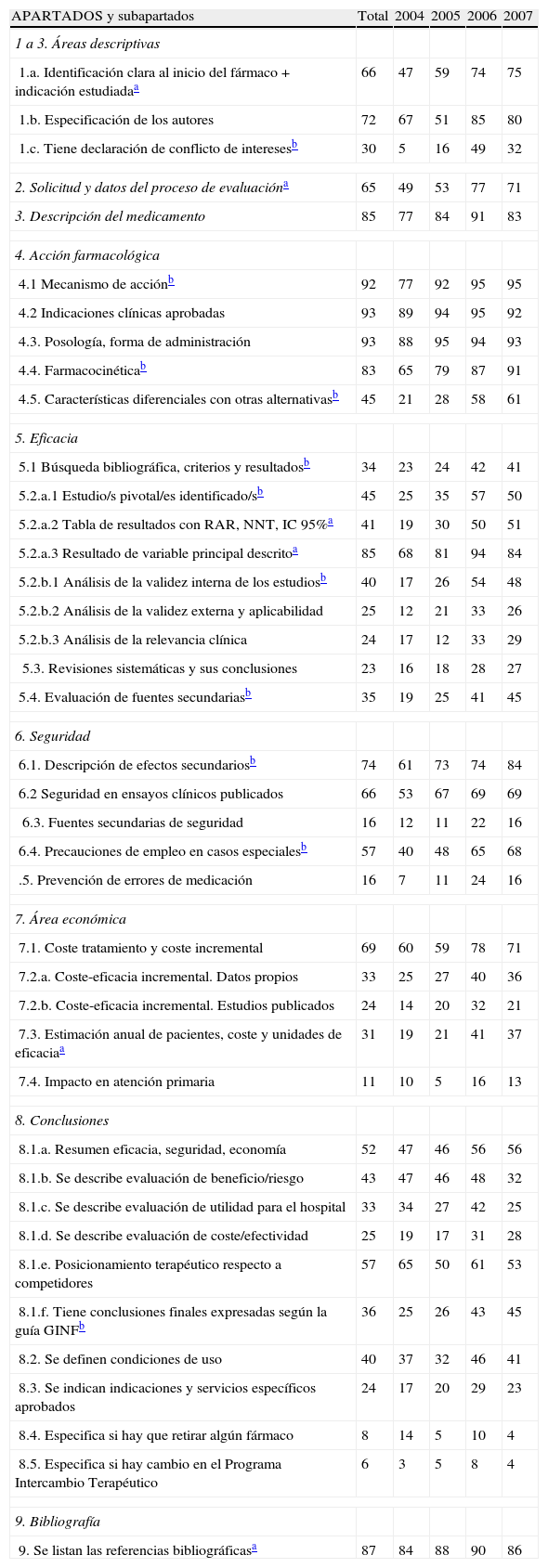
Porcentaje de informes que contienen el subapartado cumplimentado de modo aceptable, no incluidos los dudosos o parciales o no aplicables. Análisis en total (durante los 4 años), por años y significación de la diferencia entre 2007 y 2004
| APARTADOS y subapartados | Total | 2004 | 2005 | 2006 | 2007 |
| 1 a 3. Áreas descriptivas | |||||
| 1.a. Identificación clara al inicio del fármaco + indicación estudiadaa | 66 | 47 | 59 | 74 | 75 |
| 1.b. Especificación de los autores | 72 | 67 | 51 | 85 | 80 |
| 1.c. Tiene declaración de conflicto de interesesb | 30 | 5 | 16 | 49 | 32 |
| 2. Solicitud y datos del proceso de evaluacióna | 65 | 49 | 53 | 77 | 71 |
| 3. Descripción del medicamento | 85 | 77 | 84 | 91 | 83 |
| 4. Acción farmacológica | |||||
| 4.1 Mecanismo de acciónb | 92 | 77 | 92 | 95 | 95 |
| 4.2 Indicaciones clínicas aprobadas | 93 | 89 | 94 | 95 | 92 |
| 4.3. Posología, forma de administración | 93 | 88 | 95 | 94 | 93 |
| 4.4. Farmacocinéticab | 83 | 65 | 79 | 87 | 91 |
| 4.5. Características diferenciales con otras alternativasb | 45 | 21 | 28 | 58 | 61 |
| 5. Eficacia | |||||
| 5.1 Búsqueda bibliográfica, criterios y resultadosb | 34 | 23 | 24 | 42 | 41 |
| 5.2.a.1 Estudio/s pivotal/es identificado/sb | 45 | 25 | 35 | 57 | 50 |
| 5.2.a.2 Tabla de resultados con RAR, NNT, IC 95%a | 41 | 19 | 30 | 50 | 51 |
| 5.2.a.3 Resultado de variable principal descritoa | 85 | 68 | 81 | 94 | 84 |
| 5.2.b.1 Análisis de la validez interna de los estudiosb | 40 | 17 | 26 | 54 | 48 |
| 5.2.b.2 Análisis de la validez externa y aplicabilidad | 25 | 12 | 21 | 33 | 26 |
| 5.2.b.3 Análisis de la relevancia clínica | 24 | 17 | 12 | 33 | 29 |
| 5.3. Revisiones sistemáticas y sus conclusiones | 23 | 16 | 18 | 28 | 27 |
| 5.4. Evaluación de fuentes secundariasb | 35 | 19 | 25 | 41 | 45 |
| 6. Seguridad | |||||
| 6.1. Descripción de efectos secundariosb | 74 | 61 | 73 | 74 | 84 |
| 6.2 Seguridad en ensayos clínicos publicados | 66 | 53 | 67 | 69 | 69 |
| 6.3. Fuentes secundarias de seguridad | 16 | 12 | 11 | 22 | 16 |
| 6.4. Precauciones de empleo en casos especialesb | 57 | 40 | 48 | 65 | 68 |
| .5. Prevención de errores de medicación | 16 | 7 | 11 | 24 | 16 |
| 7. Área económica | |||||
| 7.1. Coste tratamiento y coste incremental | 69 | 60 | 59 | 78 | 71 |
| 7.2.a. Coste-eficacia incremental. Datos propios | 33 | 25 | 27 | 40 | 36 |
| 7.2.b. Coste-eficacia incremental. Estudios publicados | 24 | 14 | 20 | 32 | 21 |
| 7.3. Estimación anual de pacientes, coste y unidades de eficaciaa | 31 | 19 | 21 | 41 | 37 |
| 7.4. Impacto en atención primaria | 11 | 10 | 5 | 16 | 13 |
| 8. Conclusiones | |||||
| 8.1.a. Resumen eficacia, seguridad, economía | 52 | 47 | 46 | 56 | 56 |
| 8.1.b. Se describe evaluación de beneficio/riesgo | 43 | 47 | 46 | 48 | 32 |
| 8.1.c. Se describe evaluación de utilidad para el hospital | 33 | 34 | 27 | 42 | 25 |
| 8.1.d. Se describe evaluación de coste/efectividad | 25 | 19 | 17 | 31 | 28 |
| 8.1.e. Posicionamiento terapéutico respecto a competidores | 57 | 65 | 50 | 61 | 53 |
| 8.1.f. Tiene conclusiones finales expresadas según la guía GINFb | 36 | 25 | 26 | 43 | 45 |
| 8.2. Se definen condiciones de uso | 40 | 37 | 32 | 46 | 41 |
| 8.3. Se indican indicaciones y servicios específicos aprobados | 24 | 17 | 20 | 29 | 23 |
| 8.4. Especifica si hay que retirar algún fármaco | 8 | 14 | 5 | 10 | 4 |
| 8.5. Especifica si hay cambio en el Programa Intercambio Terapéutico | 6 | 3 | 5 | 8 | 4 |
| 9. Bibliografía | |||||
| 9. Se listan las referencias bibliográficasa | 87 | 84 | 88 | 90 | 86 |
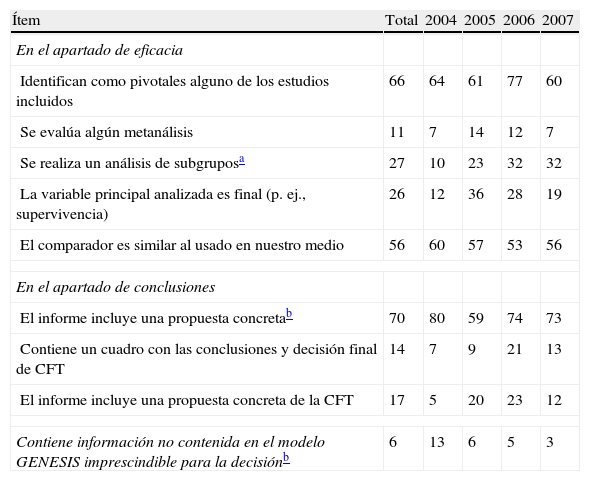
Porcentaje de informes que contienen los ítems cumplimentados de modo aceptable, no incluidos los dudosos o parciales o no aplicables. Análisis en total (durante los 4 años), por años y significación de la diferencia entre 2007 y 2004
| Ítem | Total | 2004 | 2005 | 2006 | 2007 |
| En el apartado de eficacia | |||||
| Identifican como pivotales alguno de los estudios incluidos | 66 | 64 | 61 | 77 | 60 |
| Se evalúa algún metanálisis | 11 | 7 | 14 | 12 | 7 |
| Se realiza un análisis de subgruposa | 27 | 10 | 23 | 32 | 32 |
| La variable principal analizada es final (p. ej., supervivencia) | 26 | 12 | 36 | 28 | 19 |
| El comparador es similar al usado en nuestro medio | 56 | 60 | 57 | 53 | 56 |
| En el apartado de conclusiones | |||||
| El informe incluye una propuesta concretab | 70 | 80 | 59 | 74 | 73 |
| Contiene un cuadro con las conclusiones y decisión final de CFT | 14 | 7 | 9 | 21 | 13 |
| El informe incluye una propuesta concreta de la CFT | 17 | 5 | 20 | 23 | 12 |
| Contiene información no contenida en el modelo GENESIS imprescindible para la decisiónb | 6 | 13 | 6 | 5 | 3 |
CFT: Comisión de Farmacia y Terapéutica.
Únicamente 48 informes (11,5%) citaban los de otros hospitales en la bibliografía.
Respecto a la comparación entre los informes publicados en el área azul o roja, el grado de cumplimiento de los diferentes apartados fue similar, salvo en algunos pocos apartados. Por ejemplo, los informes publicados en el área roja con más frecuencia incluyen autores, conflicto de intereses, descripción de la búsqueda bibliográfica o las referencias; y los informes del área azul con mayor frecuencia incluyen los resultados como reducción absoluta del riesgo (RAR) y número de pacientes que es necesario tratar (NNT) y expresan las conclusiones según la Guía para la valoración de inclusión de nuevos fármacos (GINF).
Respecto a los grupos terapéuticos, solo se analizaron por separado los grupos L, N, J, A y C por tener mayor frecuencia de informes, cumpliéndose en todos ellos aproximadamente el mismo número de apartados recogidos en los informes.
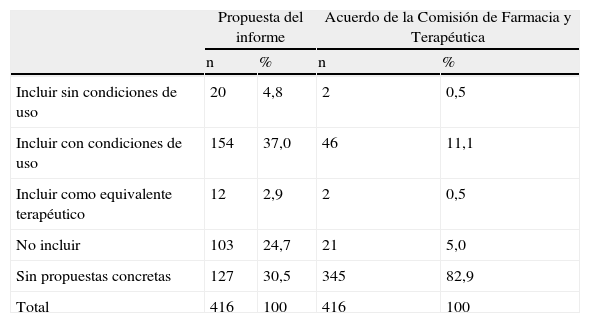
Las propuestas de inclusión o no del medicamento contenidas en el informe y la decisión final tomada por las CFT, recogidas en los informes, se reflejan en la tabla 6. Solo en 71 de los 416 informes (17%) se reflejaban en los mismos la decisión de la comisión, siendo ésta coincidente con la recomendación del informe en 48 casos, en 20 casos el informe no daba una recomendación y en 3 casos no coincidían.
Propuesta del informe y acuerdo de las Comisiones de Farmacia y Terapéutica incluidas en los informes
| Propuesta del informe | Acuerdo de la Comisión de Farmacia y Terapéutica | |||
| n | % | n | % | |
| Incluir sin condiciones de uso | 20 | 4,8 | 2 | 0,5 |
| Incluir con condiciones de uso | 154 | 37,0 | 46 | 11,1 |
| Incluir como equivalente terapéutico | 12 | 2,9 | 2 | 0,5 |
| No incluir | 103 | 24,7 | 21 | 5,0 |
| Sin propuestas concretas | 127 | 30,5 | 345 | 82,9 |
| Total | 416 | 100 | 416 | 100 |
De los 185 medicamentos evaluados, el análisis de la variabilidad en la recomendación solo se pudo realizar con los 84 medicamentos de los cuales había más de un informe. En concreto había 27 medicamentos con 2 informes, 20 con 3 informes, 14 con 4 informes, 10 con 5 informes, 7 con 6 informes y de un medicamento había 8 informes y de otro 11 informes. En 20 (24%) de estos 84 medicamentos/indicaciones con más de un informe, todos los informes coincidían en sus recomendaciones y en 25 medicamentos (30%) las recomendaciones no coincidían entre los informes del mismo medicamento. En 22 casos la coincidencia fue parcial, es decir, los informes con recomendaciones coincidían pero había algunos informes sin recomendaciones concretas, y en 17 casos solo había 2 informes y uno o 2 de ellos no tenía recomendaciones concretas, por lo que no se podía valorar el grado de coincidencia.
Las razones de discordancia entre la recomendación de los diferentes informes de un mismo medicamento en 7 ocasiones, de los 25 casos con discrepancia, no se pudo intuir. En el resto, los revisores de los informes atribuyeron causas muy variadas destacando las que, informalmente, podríamos clasificar como diferencias de criterio o políticas entre hospitales donde se elaboraban los informes, como por ejemplo, diferente interés por individualizar la terapia, diferente grado de ser estrictos, diferente aceptación de uso en condiciones especiales, diferente valoración respecto a la ventaja que supone la vía oral, etc. En 4 ocasiones la discordancia se debió a que en los hospitales atienden a diferente tipo de pacientes o presentan unas sensibilidades a antibióticos diferentes. Solo en dos ocasiones el balance beneficio/riesgo de los autores de los informes era diferente y en una ocasión variaban las condiciones de uso.
DiscusiónLa principal aportación de este trabajo es comunicar la propia existencia de una iniciativa como la del grupo GENESIS, para la que no se ha encontrado otra similar, es decir, una iniciativa para compartir informes de evaluación de nuevos medicamentos de hospitales de un mismo país mediante metodología común y a través de un entorno web.
En general, la cantidad, la adecuación a la metodología propuesta y la homogeneidad de los informes publicados en la web es alta, aunque existen también importantes oportunidades de mejora. El elevado número de informes publicados en la web de GENESIS en este periodo refleja la importante actividad de evaluación de nuevos medicamentos que se genera en los servicios de farmacia de los hospitales españoles y la disposición a compartir esta información. Sin embargo, sería deseable que a los 28 hospitales participantes se sumara alguno más de los 455 hospitales con más de 100 camas existentes en España8.
El grupo GENESIS propuso en 2005 una determinada estructura para los informes de evaluación de nuevos medicamentos conocida como modelo MADRE. Del análisis realizado se puede concluir que la adherencia de los hospitales del grupo a este modelo ha sido muy alta, y también ha crecido con los años en un entorno internacional en el que el uso de un método estandarizado de informes de evaluación de medicamentos no es algo frecuente9.
Sin embargo, sigue habiendo apartados importantes, recomendados, con baja adherencia. Habría que investigar la causa e incidir más en la formación de las personas que elaboran los informes, bien mejorando la información en la web, bien organizando actividades docentes o mediante otras medidas.
Especial interés tiene analizar los apartados de valoración de la eficacia y área económica por ser el núcleo de la evaluación. Destaca, probablemente debido a los esfuerzos docentes en este sentido, que en 2007 la mitad de los informes ya expresaban los resultados de los ensayos analizados en términos de reducción absoluta del riesgo (RAR) y número de pacientes que es necesario tratar (NNT) con sus intervalos de confianza. En cuanto al análisis de subgrupos, aunque es imposible saber en qué proporción del total de informes este análisis fue posible, sí parece que podría haber un gran margen de mejora, en tanto en cuanto la identificación de subpoblaciones tiene unas grandes implicaciones en la relación coste-efectividad y por tanto el posible posicionamiento del fármaco.
Algo parecido ocurre con los estratégicos ítems de análisis de la validez interna, validez externa, relevancia clínica, coste-eficacia incremental e impacto presupuestario. La evaluación crítica de los ensayos clínicos y de la transferencia de sus resultados a la práctica clínica de manera comparada con las alternativas existentes y el análisis farmacoeconómico posterior debería ser el eje central de los informes de evaluación de las CFT hospitalarias, ya que es la principal demanda a la que se enfrentan por parte de clínicos, gestores y pacientes y clave para el posicionamiento de un fármaco según su utilidad terapéutica10,11.
Por lo que se refiere al cumplimiento de algunos aspectos novedosos, éste es aún escaso y por tanto supone oportunidades de mejora, por ejemplo, las consideraciones de seguridad en la prevención de errores de medicación12, y el impacto presupuestario en atención primaria.
Por otro lado, en el análisis de la variable principal analizada y el comparador utilizado resaltan 2 aspectos a los que es necesario enfrentarse en el momento de la selección de los medicamentos. En pocas ocasiones los resultados de eficacia vienen dados por una medida final de eficacia como supervivencia o supervivencia corregida por calidad de vida, que serían las medidas ideales para la toma de la decisión13. Y en casi la mitad de las ocasiones el comparador no corresponde con el utilizado en nuestro entorno, haciendo necesario el uso de estrategias como las comparaciones indirectas. A este respecto, en un estudio reciente publicado14 en el que se analizaban las características de los ensayos clínicos aleatorizados, estudios observacionales o metanálisis de medicamentos publicados de junio de 2008 a septiembre de 2009 en las 6 revistas de medicina general e interna con más impacto, encontraron que solo 145 de los 328 estudios (43%) comparaban 2 o más medicamentos entre sí, y 187 (53%) tenían un comparador no activo.
El objetivo de un informe de evaluación es la ayuda a la toma de decisiones sobre la inclusión de un medicamento en la GFT y sus condiciones. Por ello, los informes deberían contener una propuesta o recomendación, presente en el 70% de los informes. Cuando la propuesta existe para la mayoría de los informes hay un posicionamiento terapéutico.
Respecto a la información disponible sobre la decisión final de la CFT, consta en un una proporción limitada de los informes. Ello puede ser debido, en parte, a que los informes se difunden en la página web, en ocasiones, de forma previa a su evaluación en la comisión, y cuando la decisión se produce, los informes no se actualizan. Convendría mejorar este punto, ya que la decisión final es un dato de interés y el «producto final» del proceso de evaluación.
En cuanto a la diferencia entre los informes publicados en abierto y con clave de acceso, no se encontraron diferencias significativas entre ellos en el grado de cumplimiento de las recomendaciones. Por lo tanto, aunque se desconoce la causa por la que un hospital decide publicar en abierto o no, su calidad no parece ser el motivo de evitar el acceso libre.
Por lo que se refiere a la variabilidad en la recomendación en 42 de los 67 (63%) medicamentos-indicaciones sobre los que había más de un informe con recomendación ésta coincidía. A diferencia de estudios realizados en otros países que muestran una amplia variabilidad en la decisión de incorporación de nuevos medicamentos 6,15–19, en España podría haber más convergencia.
Así Dranove et al15, en una encuesta en que participan 41 organizaciones sanitarias de Estados Unidos, estudian la incorporación de 7 medicamentos en el formulario y encuentran una variabilidad de incorporación de los mismos del 25 al 80%. Shalansky et al6 en un estudio centrado en 6 nuevos medicamentos del área cardiovascular por parte de 164 CFT de hospitales de Canadá, observan que la proporción de incorporaciones era del 9 al 80% según el medicamento. Morgan et al16, en un análisis de los formularios de 9 provincias de Canadá encuentran un rango del 55 al 73% en la incorporación de los 796 medicamentos disponibles y solo un 41% de los mismos se encuentran en todos los formularios.
Se dispone de estudios que analizan las causas de la variabilidad en las decisiones de las CFT4,20–28. Nuestro estudio aporta datos limitados y constata que en los casos en que se presentan discrepancias en las propuestas, parecen predominar las diferencias de criterios y políticas de los centros sobre el resto de factores analizados.
En cuanto a las limitaciones del estudio, podemos destacar tres. El análisis refleja las características de los informes que están voluntariamente publicados en la web pero no tiene por qué ser representativo de los informes totales que se realizan en el país. Por otro lado, existe un cierto grado de subjetividad en las evaluaciones del cumplimiento de apartados, contenido de la información o motivo de la discordancia entre las recomendaciones de varios informes del mismo medicamento, a pesar de que se intentó minimizar por la definición clara de criterios y la posibilidad de revisión por un segundo evaluador. Por último, los informes incluidos en el estudio corresponden a los informes realizados de 2004 a 2007, aunque pudiera haber una mejoría en años posteriores, los aspectos a mejorar y en los que prestar mayor atención pueden aplicarse al momento actual.
De modo general, por tanto, puede decirse que la actividad del grupo GENESIS ha contribuido a que los hospitales españoles compartan sus informes de evaluación de medicamentos y a que éstos sean más completos aunque existen aspectos que se deben mejorar.
FinanciaciónEl trabajo ha sido financiado en parte por la Fundación Española de Farmacia Hospitalaria.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
A los revisores de informes: Beatriz Calderón, Ana Ortega, Montserrat Vilanova, Diana Heredia, Marta Marín, Amaia Egües, María Serrano, Maialen Ortega, Luis Javier Hernández, Paloma Arias, Ana Gascón, Amaia Lizarralde y Ana Juanes.
A los hospitales que han publicado sus informes en la web de GENESIS, siendo los que han enviado mayor número de informes: Hospital Universitario Virgen del Rocío, Hospital Universitario Reina Sofía, Hospital Universitario Son Dureta, Clínica Universidad de Navarra, Hospital General Universitario de Alicante, Hospital Universitario Ramón y Cajal, Hospital General Universitario Gregorio Marañón, Instituto Catalán de Oncología, GFT de Hospitales de Andalucía, Hospital Universitario Vall d’Hebron, Hospital Universitario La Fe, Centro Hospitalario Universitario Juan Canalejo, Hospital Universitario de Bellvitge, Centro Hospitalario La Mancha Centro, Hospital de Galdakao, Hospital Universitario Príncipe de Asturias.
Un resumen del trabajo fue presentado en el 54 Congreso de la Sociedad Española de Farmacia Hospitalaria celebrado en Zaragoza del 23 al 25 de septiembre de 2009.