La cirugía bariátrica es el mejor método para la pérdida de peso y control de comorbilidades asociadas a la obesidad. El bypass y la manga gástrica han demostrado la mayor efectividad; sin embargo, no existen estudios de alto impacto en la población mexicana.
ObjetivoAnalizar la mejora de la diabetes mellitus 2 y la intolerancia a los carbohidratos en pacientes con obesidad sometidos a cirugía bariátrica.
Material y métodosEstudio retrospectivo en el que se analizaron los expedientes de pacientes con diabetes e intolerancia a los carbohidratos asociados a obesidad y que fueron sometidos a cirugía entre 2013-2015. Se realizó un análisis (0, 1, 3, 6, 9 y 12 meses) de los parámetros metabólicos, clínicos, lipídicos y de peso, así como un análisis perioperatorio y de morbimortalidad. Se establecieron cifras de remisión de diabetes.
ResultadosSe analizaron 73 pacientes (46 con diabetes y 27 con intolerancia a los carbohidratos). Sesenta y dos fueron mujeres, con un promedio de edad de 42 años. La glucosa y hemoglobina glucosilada iniciales fueron de 123±34mg/dl y de 6.8±1.6%, y a los 12 meses de 90.1±8mg/dl y de 5.4±0.3%, respectivamente. El 68.7% de los pacientes presentó una remisión completa, el 9.3% una remisión parcial y el 21.8% una mejoría de la diabetes. Durante todo el seguimiento mejoraron significativamente todos los parámetros metabólicos y no metabólicos.
ConclusionesLa cirugía bariátrica mejora eficazmente el estado metabólico de los pacientes con diabetes o con intolerancia a los carbohidratos en el transcurso del primer año, lo que induce a altas tasas de remisión completa. La cirugía incide en una mejoría de la presión arterial, los parámetros lipídicos y los antropométricos.
Bariatric surgery continues to be the best treatment for weight loss and control of obesity related comorbidities. Gastric bypass and sleeve gastrectomy have demonstrated to be the most effective surgeries, but this has not been established in a Mexican (non-American) population.
ObjectiveTo analyse the improvement in type 2 diabetes mellitus and carbohydrate intolerance in obese patients after bariatric surgery.
Material and methodsA retrospective analysis was performed on the data collected prospectively between 2013 and 2015 on every obese patient with diabetes and carbohydrate intolerance submitted for bariatric surgery. Analysis was performed at baseline, and at 1, 3, 6, 9 and 12 months, and included metabolic, clinical, lipid, and anthropometrical parameters. A peri-operative and morbidity and mortality analysis was also performed. Remission rates for patients with diabetes were also established.
ResultsThe analysis included 73 patients, 46 with diabetes and 27 with carbohydrate intolerance. Sixty-two patients were female with a mean age of 42 years. Baseline glucose and glycosylated haemoglobin were 123±34mg/dl and 6.8±1.6%, and at 12 months they were 90.1±8mg/dl and 5.4±0.3%, respectively. Diabetes remission was observed in 68.7% of patients, including 9.3% with partial remission and 21.8% with an improvement. There was also a significant improvement in all metabolic and non-metabolic parameters.
ConclusionsBariatric surgery safely improves the metabolic status of patients with diabetes mellitus or carbohydrate intolerance during the first year, inducing high rates of complete remission. It has also shown a significant improvement on blood pressure, lipid, and anthropometric parameters during the first year of follow-up.
La prevalencia de la obesidad y el sobrepeso ha aumentado de forma progresiva y alarmante en la población mundial, lo que supone un problema grave de salud pública. La relación entre obesidad y diabetes mellitus tipo 2 es bien conocida y afecta al 50-65% de la población mundial, con una proyección de aumento del 1.5 al 2% anual en países de América Latina1,2. En México la prevalencia de sobrepeso u obesidad ha ido en aumento hasta reportarse en el año 2012 un porcentaje de afección del 71.2% para ambos padecimientos. De igual manera la prevalencia de diabetes mellitus tipo 2 continúa en aumento, y ha pasado de un 5.8% en 2000 a un 9.4% en 20123.
El tratamiento de la diabetes mellitus tipo 2 consiste en alcanzar metas glucémicas; es decir, el paciente deberá tener un valor de hemoglobina glucosilada menor a un 7% o igual a un 6.5%, según diferentes autores1,2. Los manejos actuales establecidos por diferentes asociaciones nacionales e internacionales se basan en el manejo médico y en los cambios en el estilo de vida, con un reconocimiento en los últimos años de la cirugía bariátrica como opción terapéutica4. Diversos estudios (aleatorizados, observacionales, metaanálisis y revisiones sistemáticas)5–9 han demostrado que los procedimientos del bypass gástrico y manga gástrica laparoscópicos mejoran significativamente el control glucémico y disminuyen el riesgo cardiovascular de manera superior al tratamiento médico6,10.
Se ha reportado, igualmente, que la prevalencia de diabetes mellitus tipo 2 posterior a cirugía bariátrica permanece estable durante un periodo de 8 años (10.7% inicial y 10.5% final), en contraste con un aumento de la prevalencia, en el mismo periodo para el grupo de manejo médico (7.8% inicial y 24.9% final)11. El impacto de dicha cirugía en la población mexicana no ha sido reportado, ya que únicamente se ha realizado en población hispanoamericana.
ObjetivoEl objetivo de este estudio fue analizar el impacto de la cirugía bariátrica (bypass gástrico y manga gástrica), en pacientes diagnosticados con diabetes mellitus tipo 2 o intolerancia a los carbohidratos, para establecer la remisión o mejoría en nuestra población.
Material y métodosEstudio retrospectivo, observacional y de cohorte, en el que se analizaron los expedientes de todos los pacientes sometidos a cirugía bariátrica, en una sola institución, del 1 de enero de 2013 al 1 de enero de 2015, y que contaban con diagnóstico de diabetes mellitus tipo 2 o intolerancia a los carbohidratos. La recolección de datos fue realizada de manera prospectiva y se excluyeron pacientes que contaran con un expediente incompleto en cualquier tiempo de análisis.
En este estudio se analizó el impacto de la cirugía bariátrica en los parámetros metabólicos: glucosa, hemoglobina glucosilada, péptido-C, insulina y el uso de medicamentos, de forma preoperatoria y al 1, 3, 6, 9, y 12 meses de seguimiento posquirúrgico, para ambos grupos (diabetes mellitus tipo 2 e intolerancia a los carbohidratos). También se analizó el porcentaje de remisión o mejoría en los pacientes con 12 meses de seguimiento. Así mismo, se realizaron los siguientes tipos deanálisis: demográfico, de comorbilidades, perioperatorio y de morbimortalidad temprana (< 30 días). Finalmente, también se reportó la evolución del peso, índice de masa corporal (IMC), porcentaje de exceso de peso perdido (%EPP) y parámetros lipídicos como colesterol total, triglicéridos, lipoproteínas de alta densidad y lipoproteínas de baja densidad.
No se realizó un análisis comparativo entre las cirugías debido al escaso número de pacientes con manga gástrica.
DefinicionesLas definiciones de remisión y mejoría de la diabetes mellitus tipo 2 se basaron en los criterios de la Asociación Americana de Diabetes (American Diabetes Association, ADA) del 2009.
Remisión parcial. Hiperglucemia por debajo del umbral de diabetes mellitus tipo 2 (100-125mg/dl), hemoglobina glucosilada<6.5%, y ausencia tratamiento farmacológico, por lo menos durante un año.
Remisión completa. Glucemia normal (< 100mg/dl), con hemoglobina glucosilada<5.7% y sin tratamiento farmacológico, por lo menos durante un año.
Mejoría. Disminución en el número y/o dosis de los medicamentos (incluida insulina), asociada al control de las cifras de glucosa.
La cirugía bariátrica se realizó en pacientes conforme se establece en las guías internacionales12 y la NOM-008-SSA3-2010: pacientes entre 18 y 60 años de edad, con un IMC>35kg/m2, con alguna comorbilidad asociada, o con un IMC>40kg/m2 sin comorbilidades. Los pacientes son sometidos, previamente, a una evaluación multidisciplinaria que valora: el apego terapéutico, la evaluación psicológica y la pérdida de peso preoperatoria; todo ello para decidir si serán intervenidos quirúrgicamente y qué opción es mejor.
Técnica quirúrgicaEl bypass gástrico por laparoscopía en “Y” de Roux se realizó “simplificado”13, con un asa antecólica y una anastomosis mecánica calibrada a 2cm; el asa biliar y alimentaria midieron 50 y 150cm, respectivamente. Se realizó una división del omento mayor y se cerraron ambos espacios mesentéricos. De forma sistemática se realizó la prueba de azul de metileno y la colocación del drenaje.
La manga gástrica por laparoscopía se realizó a 5-6cm de distancia del píloro, con una calibración de 36Fr. Se usó sobresutura de la línea de grapeo en todos los casos con sutura no absorbible (polipropileno 2-0). De forma sistemática se realizó la prueba de azul de metileno y la colocación del drenaje.
Análisis estadísticoLos resultados se expresaron en media±desviación estándar (DE) o en porcentaje, dependiendo de la variable. Se realizó la prueba de la t de Student tanto para muestras dependientes como independientes, según el caso. Las variables categóricas fueron comparadas con la prueba de χ2 para distribución. Se consideró valor estadísticamente significativo una p<0.05. El análisis estadístico se realizó con NCSS 2007 (NCSS, Kaysville, Utah, Estado Unidos).
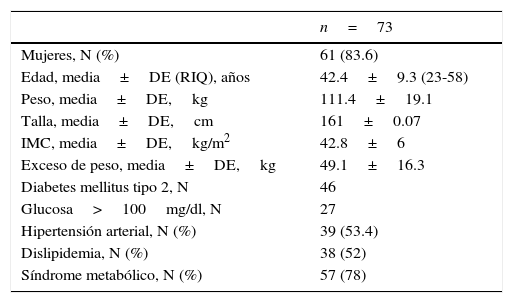
ResultadosDurante el periodo de análisis de 2 años, se realizaron 243 cirugías bariátricas. Se identificó a 46 pacientes con diagnóstico (previo o de novo) de diabetes mellitus tipo 2, y 27 pacientes con intolerancia a los carbohidratos, que representan una prevalencia en nuestra población del 18.9 y 10.6%, respectivamente. Del total de pacientes sometidos a cirugía bariátrica, 61 fueron mujeres (83.6%) y 12 hombres (16.4%), con una mediana de edad de 42 años (rango de 25-48). El peso preoperatorio promedio fue de 111.4±19.1kg/m2 y un IMC de 42.8±6kg/m2. Los parámetros basales analizados se exponen en la tabla 1.
Análisis inicial demográfico, metabólico y de comorbilidades
| n=73 | |
|---|---|
| Mujeres, N (%) | 61 (83.6) |
| Edad, media±DE (RIQ), años | 42.4±9.3 (23-58) |
| Peso, media±DE,kg | 111.4±19.1 |
| Talla, media±DE,cm | 161±0.07 |
| IMC, media±DE,kg/m2 | 42.8±6 |
| Exceso de peso, media±DE,kg | 49.1±16.3 |
| Diabetes mellitus tipo 2, N | 46 |
| Glucosa>100mg/dl, N | 27 |
| Hipertensión arterial, N (%) | 39 (53.4) |
| Dislipidemia, N (%) | 38 (52) |
| Síndrome metabólico, N (%) | 57 (78) |
DE: desviación estándar; IMC: índice de masa corporal; N: número; RIQ: rango intercuartílico.
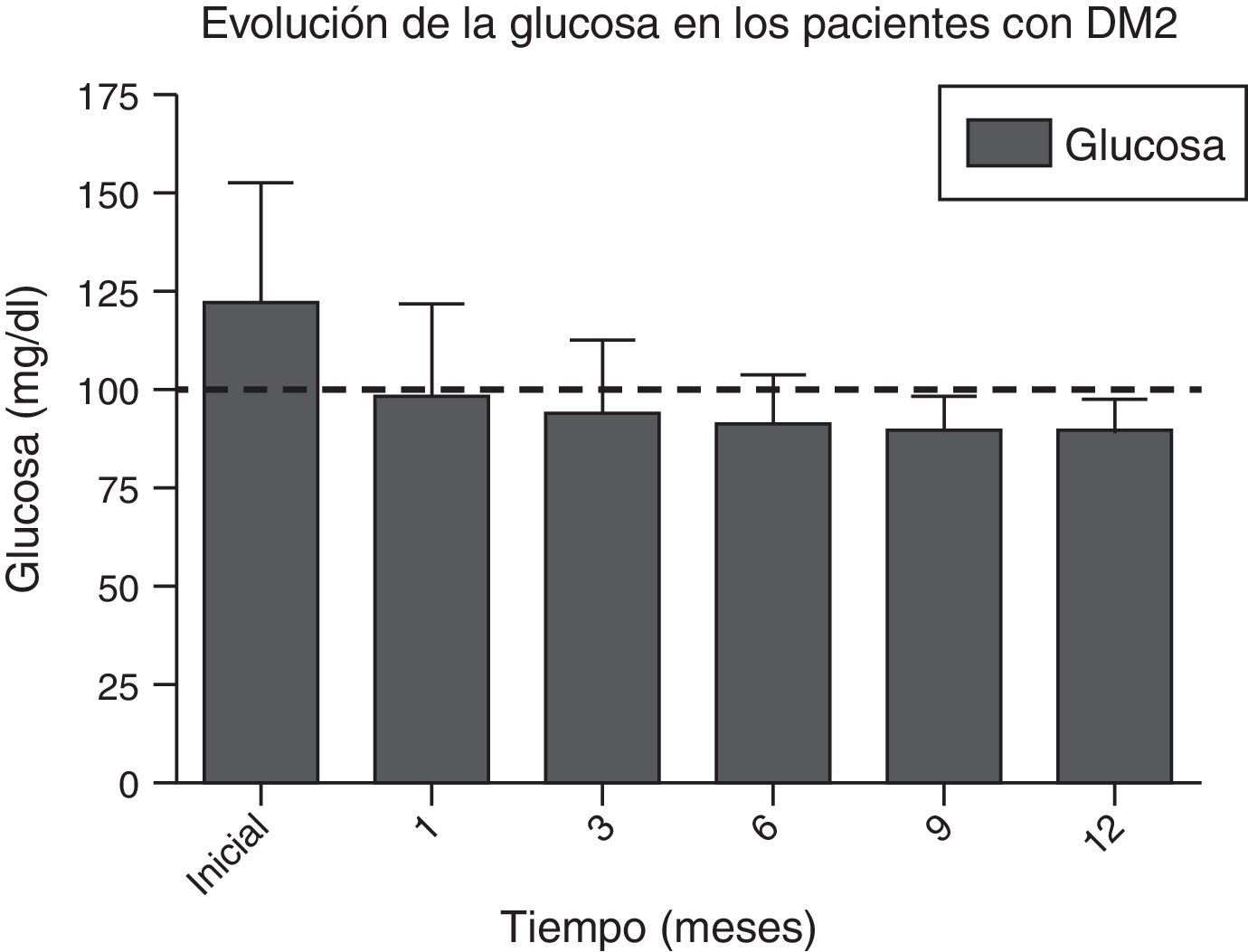
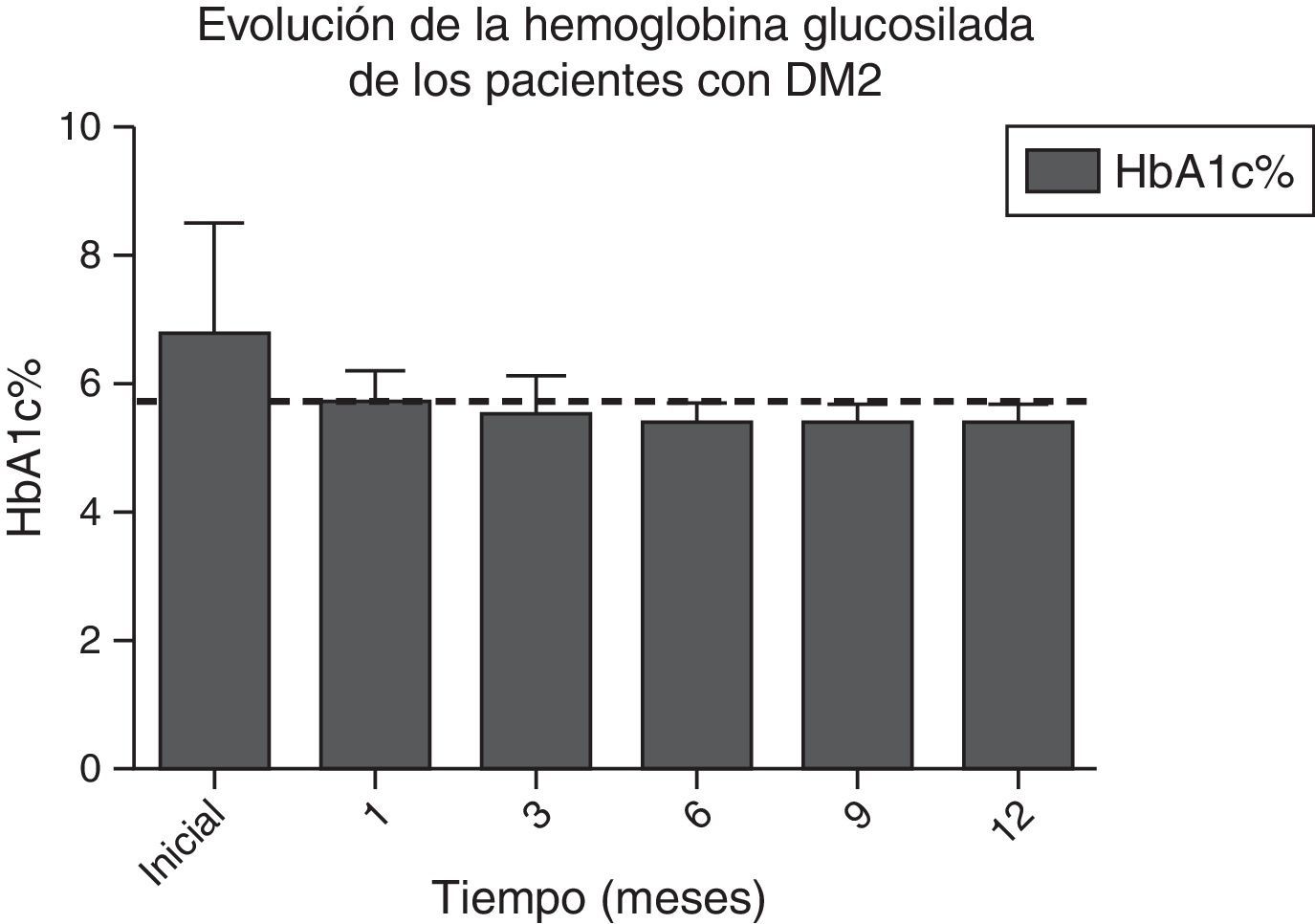
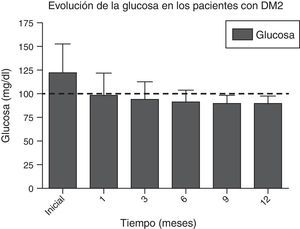
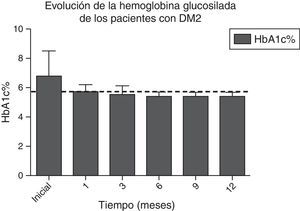
En las figuras 1 y 2 se observa la mejora significativa de los niveles de glucosa central en ayuno y de la hemoglobina glucosilada de todos los pacientes, desde el primer mes posterior a la cirugía, manteniéndose en niveles por debajo de los criterios de la ADA durante todo el seguimiento, en la mayoría de los casos. Las cifras de glucosa promedio en el preoperatorio fueron de 123±34mg/dl; a los 6 meses de 91±11.9mg/dl, y a los 12 meses de 90.1±8mg/dl. La hemoglobina glucosilada inicial promedio fue de 6.8±1.6%; al sexto mes, de 5.5±0.3%, y a los 12 meses de 5.4±0.3%.
Evolución de los niveles de HbA1c% durante todo el seguimiento. La línea punteada indica el límite establecido por la ADA para el diagnóstico de remisión de diabetes mellitus tipo 2.
ADA: American Diabetes Association; DM2: diabetes mellitus tipo 2; HbA1c%: porcentaje de hemoglobina glucosilada.
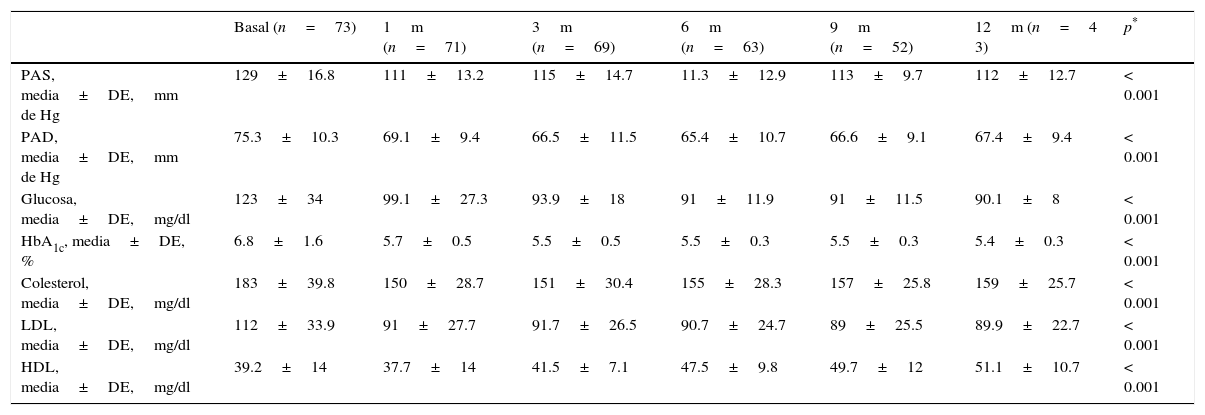
El análisis global de la evolución de los parámetros clínicos y bioquímicos se presenta en la tabla 2, en la que se observa una mejora significativa en todos ellos a los 12 meses.
Evolución clínica y bioquímica de todos los pacientes
| Basal (n=73) | 1m (n=71) | 3m (n=69) | 6m (n=63) | 9m (n=52) | 12m (n=4 3) | p* | |
|---|---|---|---|---|---|---|---|
| PAS, media±DE,mm de Hg | 129±16.8 | 111±13.2 | 115±14.7 | 11.3±12.9 | 113±9.7 | 112±12.7 | < 0.001 |
| PAD, media±DE,mm de Hg | 75.3±10.3 | 69.1±9.4 | 66.5±11.5 | 65.4±10.7 | 66.6±9.1 | 67.4±9.4 | < 0.001 |
| Glucosa, media±DE,mg/dl | 123±34 | 99.1±27.3 | 93.9±18 | 91±11.9 | 91±11.5 | 90.1±8 | < 0.001 |
| HbA1c, media±DE, % | 6.8±1.6 | 5.7±0.5 | 5.5±0.5 | 5.5±0.3 | 5.5±0.3 | 5.4±0.3 | < 0.001 |
| Colesterol, media±DE,mg/dl | 183±39.8 | 150±28.7 | 151±30.4 | 155±28.3 | 157±25.8 | 159±25.7 | < 0.001 |
| LDL, media±DE,mg/dl | 112±33.9 | 91±27.7 | 91.7±26.5 | 90.7±24.7 | 89±25.5 | 89.9±22.7 | < 0.001 |
| HDL, media±DE,mg/dl | 39.2±14 | 37.7±14 | 41.5±7.1 | 47.5±9.8 | 49.7±12 | 51.1±10.7 | < 0.001 |
DE: desviación estándar; HbA1c: hemoglobina glucosilada; HDL: lipoproteínas de alta densidad; LDL: lipoproteínas de baja densidad; PAD: presión arterial diastólica; PAS: presión arterial sistólica.
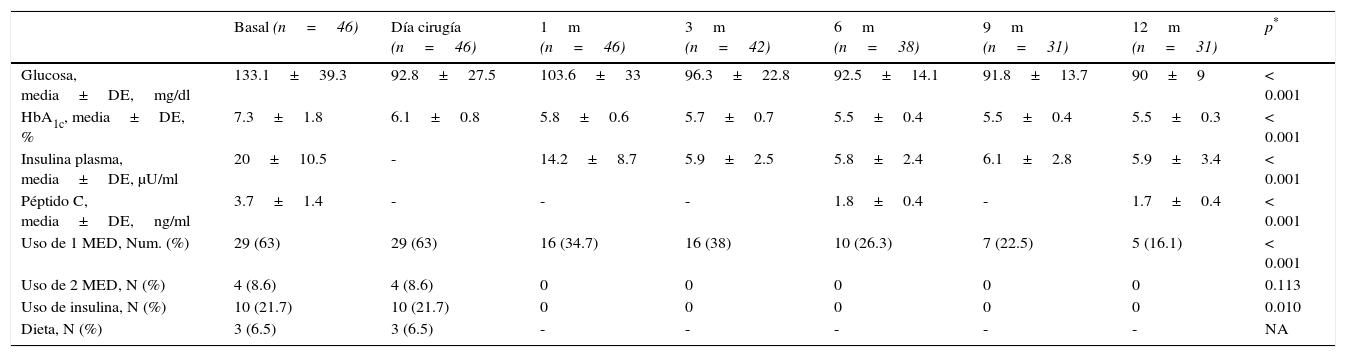
Se realizó un análisis independiente de la evolución de los pacientes con diabetes mellitus tipo 2 e intolerancia a los carbohidratos (tablas 3 y 4). Los pacientes diagnosticados con diabetes mellitus tipo 2 presentaron en un inicio cifras promedio de glucosa de 133.1±39.3mg/dl y de hemoglobina glucosilada de 7.3±1.8%, disminuyendo esta desde los primeros meses postoperatorios de forma significativa, y se mantuvo hasta los 12 meses, registrando valores de glucosa de 90±9mg/dl y de hemoglobina glucosilada de 5.5±0.3%. También, se observó una disminución estadísticamente significativa de los otros parámetros metabólicos analizados (tabla 3). En este grupo en más de la mitad de los pacientes (63%) se utilizó terapéuticamente 1 medicamento hipoglucemiante de forma inicial, a los 6 meses se disminuyó a un 26.3%, y al año solo el 16.1% continuó con el medicamento hipoglucemiante administrado. De igual manera, al 21.7% de los pacientes diabéticos se les administró insulina, la cual se interrumpió desde el primer mes del postoperatorio en todos los casos, persistiendo así durante todo el seguimiento.
Evolución metabólica y de uso de medicamentos de los pacientes con diagnóstico de diabetes mellitus tipo 2
| Basal (n=46) | Día cirugía (n=46) | 1m (n=46) | 3m (n=42) | 6m (n=38) | 9m (n=31) | 12m (n=31) | p* | |
|---|---|---|---|---|---|---|---|---|
| Glucosa, media±DE,mg/dl | 133.1±39.3 | 92.8±27.5 | 103.6±33 | 96.3±22.8 | 92.5±14.1 | 91.8±13.7 | 90±9 | < 0.001 |
| HbA1c, media±DE, % | 7.3±1.8 | 6.1±0.8 | 5.8±0.6 | 5.7±0.7 | 5.5±0.4 | 5.5±0.4 | 5.5±0.3 | < 0.001 |
| Insulina plasma, media±DE, μU/ml | 20±10.5 | - | 14.2±8.7 | 5.9±2.5 | 5.8±2.4 | 6.1±2.8 | 5.9±3.4 | < 0.001 |
| Péptido C, media±DE,ng/ml | 3.7±1.4 | - | - | - | 1.8±0.4 | - | 1.7±0.4 | < 0.001 |
| Uso de 1 MED, Num. (%) | 29 (63) | 29 (63) | 16 (34.7) | 16 (38) | 10 (26.3) | 7 (22.5) | 5 (16.1) | < 0.001 |
| Uso de 2 MED, N (%) | 4 (8.6) | 4 (8.6) | 0 | 0 | 0 | 0 | 0 | 0.113 |
| Uso de insulina, N (%) | 10 (21.7) | 10 (21.7) | 0 | 0 | 0 | 0 | 0 | 0.010 |
| Dieta, N (%) | 3 (6.5) | 3 (6.5) | - | - | - | - | - | NA |
DE: desviación estándar; HbA1c: hemoglobina glucosilada; MED: medicamento; N: número.
Evolución metabólica y de uso de medicamentos de los pacientes con Intolerancia a los HC
| Basal (n=27) | Día cirugía (n=27) | 1m (n=26) | 3m (n=26) | 6m (n=22) | 9m (n=21) | 12m (n=21) | p* | |
|---|---|---|---|---|---|---|---|---|
| Glucosa, media±DE,mg/dl | 106.4±10 | 86.6±9.5 | 91.2±8.5 | 89.9±8 | 88.3±6.6 | 89.9±7.7 | 90.1±6.6 | < 0.001 |
| HbA1c, media±DE, % | 5.8±0.4 | 5.5±0.3 | 5.5±0.3 | 5.3±0.2 | 5.3±0.2 | 5.4±0.1 | 54±0.2 | 0.281 |
| Insulina plasma, media±DE, μU/ml | 24.6±15.3 | - | 11.2±8.2 | 6.3±2.3 | - | 5.9±3.6 | 4.9 ±1.8 | < 0.001 |
| Péptido C, media±DE,ng/ml | 4.5±2 | - | - | - | - | - | 1.6±0.4 | < 0.001 |
| Uso de 1 MED, N (%) | 10 (37) | 10 (37) | 2 (7.6) | 0 | 3 (13.6) | 0 | 1 (4.7) | 0.033 |
| Dieta, N (%) | 17 (62.9) | 17 (62.9) | - | - | - | - | - | NA |
DE: desviación estándar; HbA1c: hemoglobina glucosilada; HC: carbohidratos, MED: medicamento; N: número.
Respecto al grupo de los pacientes con intolerancia a los carbohidratos (tabla 4), se observó una mejora en los valores metabólicos desde el primer mes de la cirugía, que continuó durante todo el seguimiento. A los 12 meses se evidenció un 80.9% de mejoría en los pacientes que completaron dicho seguimiento. Solo 4 pacientes continuaron con tratamiento farmacológico y/o con glucosa>100mg/dl.
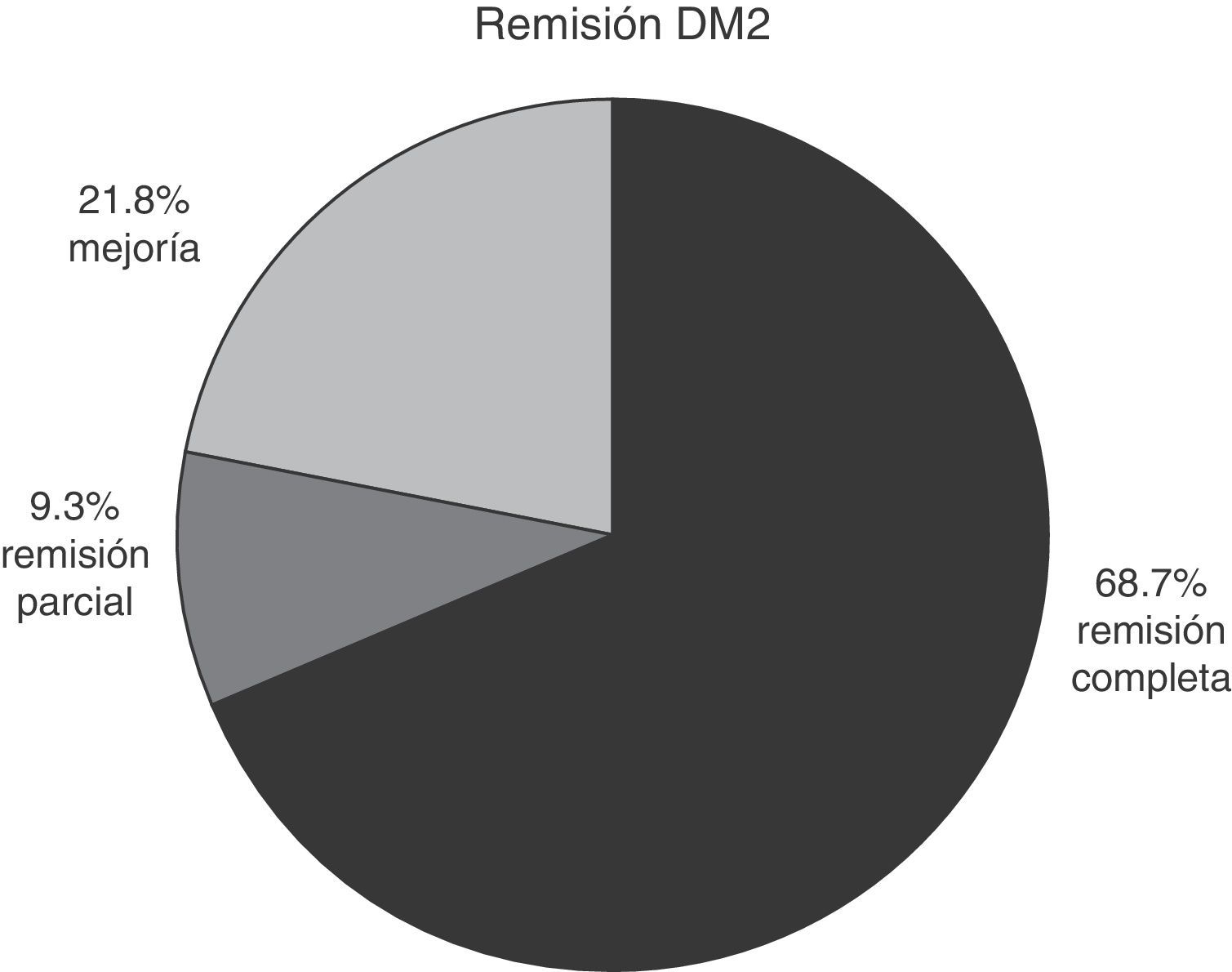
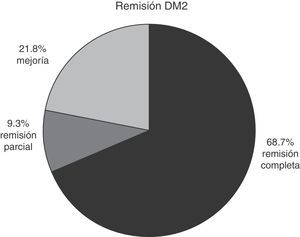
En los pacientes con diabetes mellitus tipo 2 que concluyeron un año completo de seguimiento, y que contaban con expediente completo, se observó remisión completa en el 68.7% de los casos, remisión parcial en el 9.3% y mejoría en el 21.8% (fig. 3).
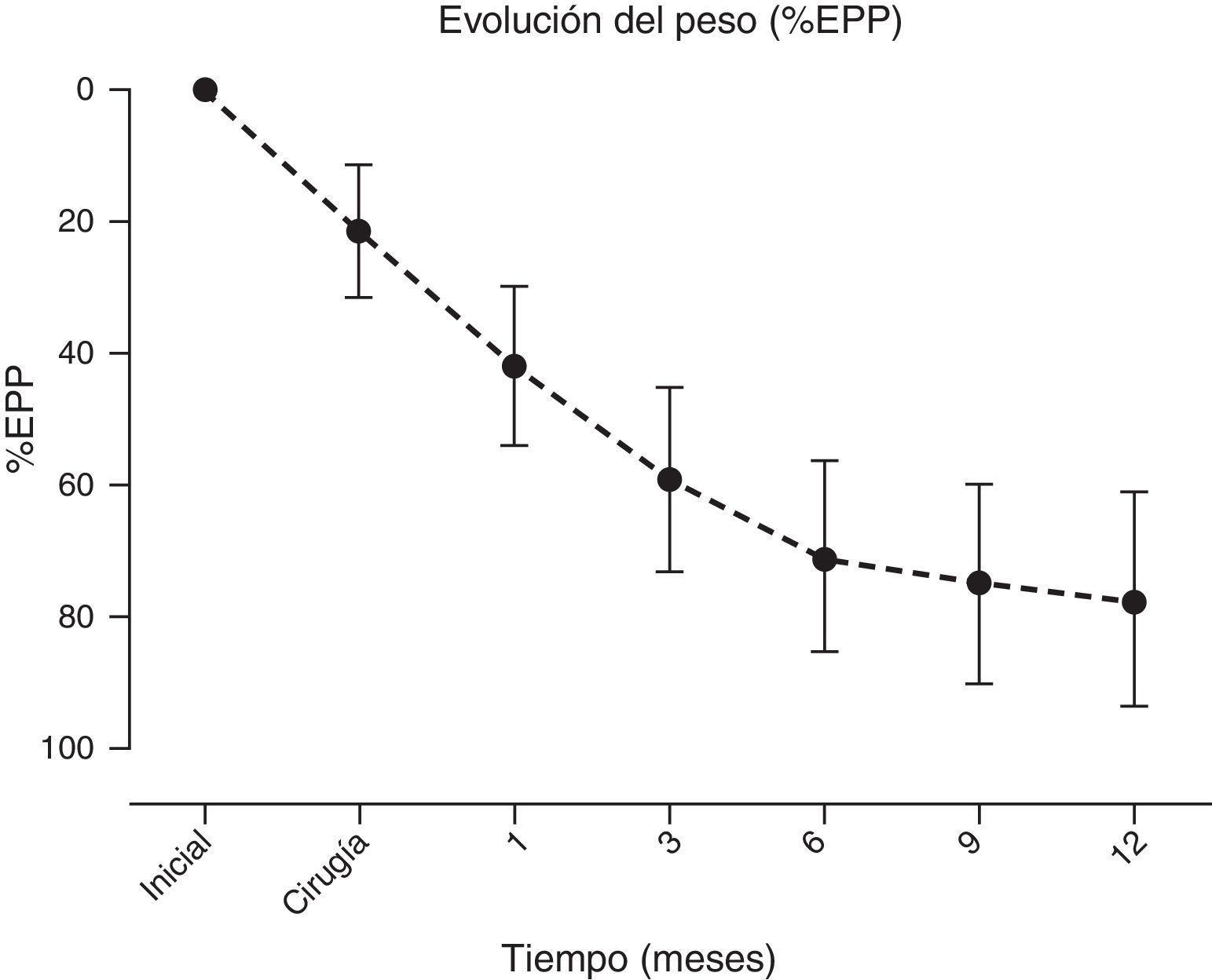
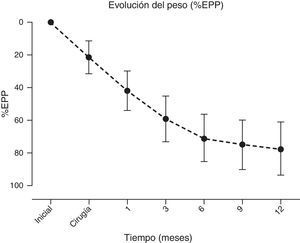
Se puso de manifiesto una pérdida de peso significativa y sostenida de los pacientes a lo largo de todo el seguimiento, alcanzando un %EPP al año de 77.5±16.2 (IMC inicial de 42.8±6kg/m2vs. 12 meses de 28.9±4.3kg/m2, p≤0.001) (fig. 4).
En el análisis de los parámetros bioquímicos correspondientes al perfil lipídico también se observó una mejora significativa y sostenida en cada uno de los pacientes (tabla 3).
El análisis de la evolución de los niveles de albúmina y proteínas como parámetros nutricionales no mostró cambio en la albúmina. Sin embargo, se detectó una disminución significativa en los niveles de proteínas (7.3 vs 7.1 a los 6 meses; p<0.001), dentro del rango normal; por lo tanto, sin significado clínico alguno.
En el análisis perioperatorio y de morbimortalidad se identificaron 70 bypass gástricos (95%) y 3 intervenciones con manga gástrica (5%). El tiempo quirúrgico fue de 167.5±39 minutos, sin conversión a cirugía abierta. Las complicaciones tempranas (<30 días) fueron 10 (13.6%). Del total de complicaciones, 4 fueron menores y 6 mayores. En el caso de las complicaciones mayores se observó: 1 fibrilación auricular paroxística; 1 hernia umbilical incarcerada, que se resolvió con cirugía; 2 estenosis moderadas de la anastomosis gastroyeyunal, que requirieron una dilatación endoscópica cada una; 1 caso de melena con transfusión de dos paquetes globulares, y 1 reintervención laparoscópica por hematoma residual infectado. No se determinó fuga, fístula ni mortalidad. Los días promedio de estancia hospitalaria fueron de 3.1±0.6 días, si se tiene en cuenta que se hospitaliza a los pacientes 1 día antes de su intervención quirúrgica.
DiscusiónEn este estudio retrospectivo, basado en 73 pacientes obesos sometidos a cirugía bariátrica con diagnóstico de diabetes mellitus tipo 2 o intolerancia a los carbohidratos, observamos una mejoría significativa posterior al procedimiento quirúrgico en todos los parámetros metabólicos y no metabólicos analizados. Dicha mejoría fue sostenida durante todo el seguimiento, y se obtuvo una remisión completa en el 68.7% de los casos con diabetes mellitus tipo 2; resultado comparable al de diversos estudios realizados (la mayoría en población no latina)8,9,11.
En la época previa a la cirugía bariátrica, en 1955, Friedmann et al.14 reportaron 3 casos de pacientes diabéticos sometidos a gastrectomía subtotal por ulcera péptica, que mostraron una disminución o eliminación de los requerimientos terapéuticos de insulina para el control de su enfermedad. Años después, con el conocimiento de procedimientos utilizados en pacientes con obesidad mórbida, Poires et al.15 demostraron que la cirugía bariátrica tiene un efecto a largo plazo en la resolución de la diabetes mellitus tipo 2, con la mejoría de las manifestaciones clínicas y de los parámetros de laboratorio en estos pacientes, cifrada en más de un 90%; inclusive observaron que estos pacientes, antes de egresar del hospital, ya tenían un mejor control glucémico que en el preoperatorio. Estos resultados fueron poco aceptados por la comunidad médica debido al carácter retrospectivo y laxo del estudio. No obstante, tras múltiples estudios posteriores, no fue hasta el año 2009 que una revisión sistemática y metaanálisis con 621 estudios demostró el impacto de los procedimientos bariátricos para el manejo de la diabetes mellitus tipo 2, asociada a la obesidad16. En este estudio se reportaron tasas globales de “resolución” del 78%, pero todavía sin tener claro dicho concepto y utilizando la definición previa establecida por la ADA: glucosa en ayuno normal o niveles de hemoglobina glucosilada menores de 6%17.
Después de la modificación de los criterios de remisión en el año 200918, disminuyeron los porcentajes reportados, como lo demostraron Pournaras et al.17 en un estudio realizado en 160 pacientes sometidos a bypass gástrico, en que compararon la antigua y la nueva definición, y mostraron una disminución en las tasas de remisión, de un 57.5 a 40.6% a los 23 meses de seguimiento. La adaptación de dichos criterios por la ADA fue el inicio del reconocimiento formal de la cirugía bariátrica como una opción eficaz en el tratamiento de la diabetes mellitus tipo 2 asociada a la obesidad, e inclusive se incorporó a los algoritmos de manejo por parte de las diversas asociaciones internacionales14,19.
Los resultados a corto plazo de la cirugía (especialmente con bypass gástrico) son superiores a los del tratamiento médico6,10; sin embargo, existe una gran variabilidad en los porcentajes de remisión y mejoría. La diferencia entre estudios (incluidos metaanálisis, revisiones sistémicas y ensayos clínicos aleatorizados) resulta de los criterios de remisión y mejoría utilizados por los autores. Algunos estudios recientes establecieron tasas de remisión a corto plazo que van de un 43.2 hasta un 75%20–22. Aunque casi todas las definiciones actuales concuerdan en la suspensión tratamiento médico y las glucemias<100mg/dl durante el primer año, la discrepancia radica en la cifra de corte de la hemoglobina glucosilada. Las últimas recomendaciones señalan una hemoglobina glucosilada<5.7% como meta del tratamiento20,23; sin embargo, se dispone de escasos estudios basados en esta cifra, ya que generalmente se utiliza el parámetro 6-6.5%21. Es importante mencionar que una hemoglobina glucosilada mayor al 5.7% se asocia a un alto riesgo de diabetes mellitus tipo 2, a enfermedad cardiovascular y a enfermedad micro/macrovascular24; por lo cual consideramos razonable utilizar este parámetro como valor de corte para definir la remisión. En nuestro estudio, la tasa de remisión a 12 meses fue casi del 69%, siendo comparable a los reportes previos de estudios en otras poblaciones25.
Más allá de la simple pérdida de peso como etiología principal de la mejora o control del estado hiperglucémico, existen múltiples razones y teorías de por qué la cirugía bariátrica tiene un impacto tan pronunciado y duradero. Dentro de las causas ya establecidas debe considerarse la regularización de diversas secuencias metabólicas, como el funcionamiento de las células beta y la sensibilidad a la insulina, así como la absorción intestinal de la glucosa, lo cual resulta beneficioso para el control glucémico y potencialmente sinérgico26. También existen cambios significativos en los hábitos alimentarios, que favorecen la elección de alimentos saludables27, asociados con la alteración postoperatoria en el sabor y el olor28, y con las respuestas neurales en los centros de saciedad del cerebro. Los mecanismos neurohormonales también desempeñan un papel importante, en donde están relacionados el péptido similar al glucagón tipo 1 (GLP-1) y péptido tirosina tirosina (PYY), los cuales aumentan su producción posterior a la cirugía de manga gástrica y/o bypass gástrico, principalmente este último procedimiento. Al mismo tiempo, las concentraciones de las hormonas del hambre y la saciedad se modifican, lo que influye en la ingesta de calorías26.
En los resultados a largo plazo, recientemente un estudio reportó la evolución de 78 pacientes sometidos a bypass gástrico, con un seguimiento de 11 años, en el 52.6% de los cuales se observó remisión completa y en el 6.4%, remisión parcial. En dicho estudio la recurrencia global de la enfermedad fue del 15.4%; asimismo, el índice de complicaciones microvasculares fue del 11.5% y del 5% para las complicaciones macrovasculares. En los pacientes en que no se logró una remisión temprana de la diabetes mellitus tipo 2, se manifestó un riesgo 8.8 veces mayor de complicaciones microvasculares, en comparación con los pacientes en remisión. Los autores relacionaron el tiempo de evolución de la diabetes mellitus y de los niveles elevados de hemoglobina glucosilada y de insulina en el periodo preoperatorio con un índice menor de remisión y con un aumento del riesgo de presentar complicaciones vasculares29.
Es necesario realizar estudios aleatorizados y controlados para aspirar a mejores resultados, respecto a ciertos criterios de selección, dado que se ha visto recurrencia o pobre respuesta en relación con los siguientes parámetros: edad avanzada, IMC alto, niveles elevados de hemoglobina glucosilada, número de medicamentos y/o requerimiento de insulina en el periodo preoperatorio30, así como niveles bajos de péptido C31.
Una de las mayores preocupaciones en cuanto a la implementación de dichas intervenciones son las complicaciones quirúrgicas, especialmente a corto plazo (<30 días), con, inclusive, posibles consecuencias fatales en algunos casos. Esta interpretación ha evolucionado en función de la experiencia y con la aparición de la cirugía laparoscópica. La morbilidad asociada a la cirugía bariátrica ha disminuido a tasas globales del 17% (7-23%) y del 21% para bypass gástrico (12-33%)32. Estos resultados se han observado en centros especializados y con flujo alto de pacientes con estas enfermedades, como en nuestra propia clínica, donde el porcentaje de complicaciones tempranas fue del 13.6%.
En síntesis, la cirugía bariátrica es una opción segura y efectiva para el tratamiento de pacientes con diabetes mellitus tipo 2 o intolerancia a los carbohidratos, con obesidad. Las limitaciones de nuestro estudio son el carácter retrospectivo, el escaso tamaño de la muestra y el corto periodo de seguimiento. A pesar de lo anterior, la importancia del análisis radica en que es el primero de su tipo realizado con población mexicana, que tiene un detallado y completo seguimiento, y sobre todo, que implementa una cifra baja de corte para la hemoglobina glucosilada, para definir la remisión.
ConclusiónLa cirugía bariátrica mejora de forma eficaz y segura el estado metabólico de los pacientes diagnosticados con diabetes mellitus tipo 2 y/o intolerancia a los carbohidratos en obesos durante el primer año, lo que lleva a altas tasas de remisión completa. La cirugía bariátrica también tiene un efecto positivo en otros aspectos como la mejoría de la presión arterial sistémica, los parámetros lipídicosy antropométricos, durante el primer año de seguimiento.
Responsabilidades éticasProtección de personas y animalesLos autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses