La endocarditis infecciosa es una enfermedad mortal, que a pesar de las mejoras en su manejo sigue estando asociada a gran mortalidad y complicaciones graves. Se presenta el caso clínico de un hombre de 35 años con cuadro neurológico asociado a masa valvular aórtica con doble lesión valvular. Sospechando endocarditis infecciosa, fue intervenido de sustitución valvular aórtica. El paciente tenía antecedentes de espondiloartropatía tratada con certolizumab y de betatalasemia. Presentó en el postoperatorio un taponamiento cardiaco tardío, complicaciones en la cicatrización de la herida quirúrgica y un bloqueo aurículo-ventricular que requirió de implante de marcapasos. Al cuarto mes postoperatorio fue reintervenido con el hallazgo de un seudoaneurisma subanular, encontrando una desestructuración del anillo aórtico nativo. Se realizó una nueva reintervención pasados 5meses, decidiéndose implante de homoinjerto aórtico en posición subcoronaria. Se realizó un exhaustivo diagnóstico diferencial sin confirmación del agente etiológico hasta la positividad de Tropheryma whipplei en el material quirúrgico de la última cirugía.
Infective endocarditis is a fatal disease, which, despite improvements in its management, is still associated with high mortality and serious complications. A case is presented of a 35 year-old man with neurological symptoms associated with an aortic valve mass with a double valvular lesion. Suspecting infectious endocarditis, aortic valve replacement was performed. The patient had a history of spondyloarthropathy (treated with certolizumab) and beta-thalassaemia. In the postoperative period, he had a late cardiac tamponade, complications in the healing of the surgical wound, and anatrial-ventricular block requiring pacemaker implantation. He was re-intervened in the fourth post-operative month, with the finding of a sub-annular pseudoaneurysm, and a disruption of the native aortic ring. In a further intervention after 5months it was decided to implant an aortic homograft in a sub-coronary position. An exhaustive differential diagnosis was made without confirmation of the aetiological agent until Tropheryma whipplei was found in the surgical material of the last surgery.
La endocarditis infecciosa (EI) es una enfermedad mortal, que a pesar de las mejoras en su manejo sigue estando asociada a gran mortalidad y complicaciones graves. Su manejo requiere de un abordaje multidisciplinar por equipos especializados, idealmente en centros de referencia, debido a sus múltiples formas de presentación dependiendo del curso agudo o subagudo, la cardiopatía subyacente si la hay, el microorganismo implicado, y la presencia de complicaciones. El equipo clínico debe tomar decisiones sobre la indicación de cirugía, el tratamiento antibiótico específico y la duración del tratamiento, algo difícil en ocasiones ante el hallazgo de resultados inconcluyentes en los estudios microbiológicos, que puede obligar a solicitar otras pruebas como serologías, detección de ácidos nucleicos e histopatología1,2.
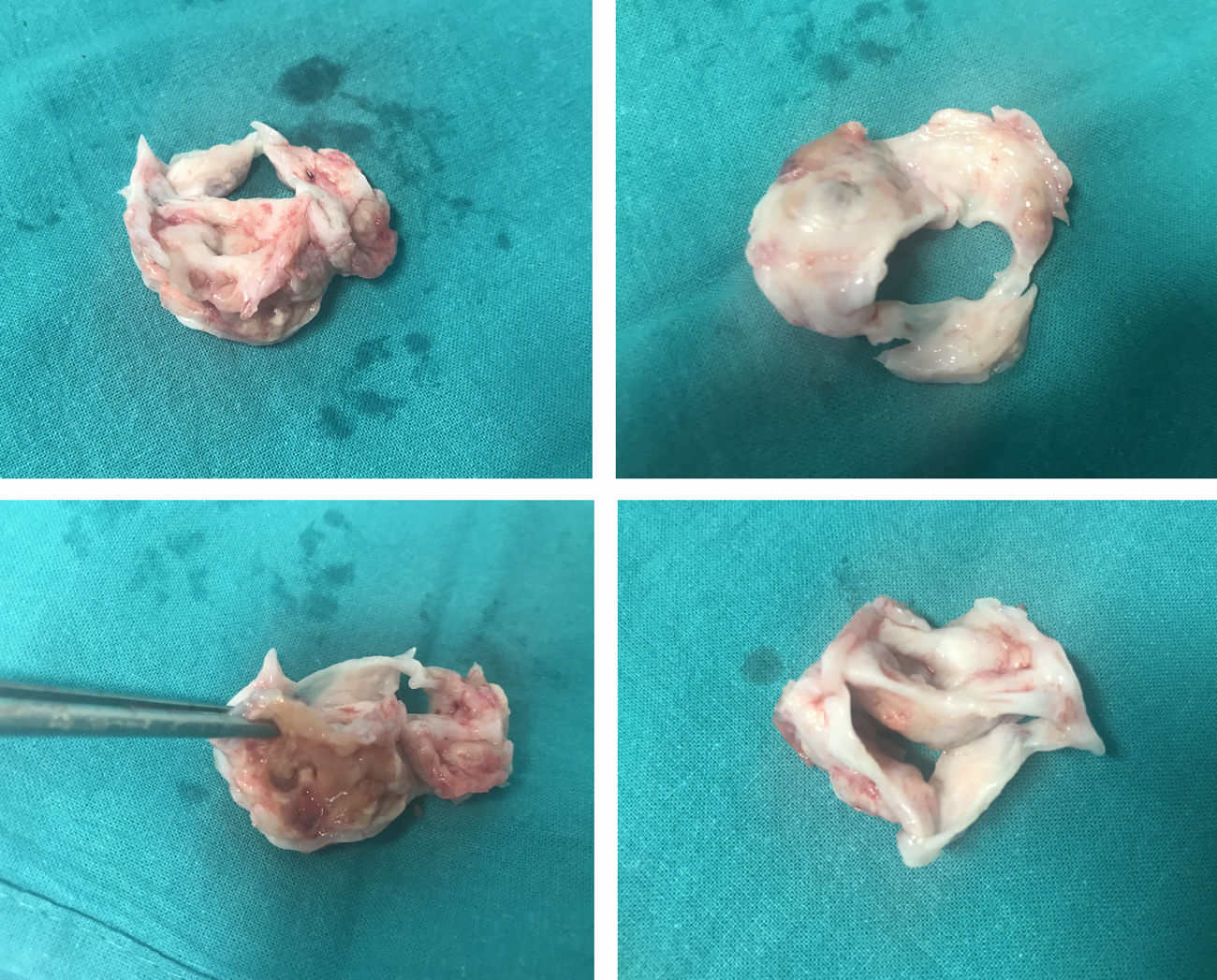
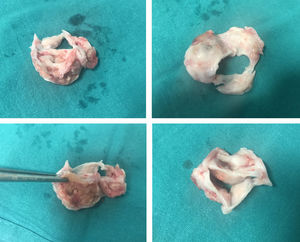
Caso clínicoHombre de 35 años, con antecedentes de hemorragia digestiva alta, betatalasemia y espondiloartropatía, en tratamiento con certolizumab (fármaco antifactor de necrosis tumoral [TNF]), que acudió a Urgencias por cuadrantanopsia homónima izquierda inferior congruente, sin otra clínica. En la tomografía computarizada (TAC) cerebral se objetivó un quiste aracnoideo derecho como hallazgo incidental. Con soplo en la auscultación, se realizó ecocardiografía transtorácica (ETT), diagnóstica de masa sobre el velo coronariano derecho, con superficie de aspecto friable, que generaba una doble lesión aórtica: estenosis moderada e insuficiencia severa. Analíticamente, leucocitosis con neutrofilia. Sospechando EI, fue intervenido de forma urgente con implante de prótesis aórtica mecánica bidisco 24mm. Destacó la presencia de adherencias pericárdicas firmes. La válvula aórtica (fig. 1) era trivalva, displásica, con engrosamiento severo del velo coronariano derecho, de coloración amarillo-parduzca, con material de aspecto necrótico en su interior. El velo coronariano izquierdo presentaba un implante similar en proximidad a la comisura con el velo no coronariano. El velo no coronariano estaba engrosado impresionando de hipoplásico.
Evolución postoperatoria caracterizada por la necesidad de reintervención por taponamiento cardiaco tardío, sin punto sangrante. Persistió la cuadrantanopsia inferior izquierda, con fondo de ojo normal y TAC cerebral con hipodensidad occipital derecha por infarto establecido subagudo en el territorio de la arteria cerebral posterior derecha, sin efecto masa ni transformación hemorrágica. Aunque todos los cultivos microbiológicos fueron negativos, pre, intra y postoperatorios, se mantuvo antibioterapia empírica con vancomicina y gentamicina, que posteriormente se desescaló a ceftriaxona. El paciente no había recibido tratamiento antibiótico previo al diagnóstico que pudiera haber decapitado los hemocultivos. La anatomía patológica mostró polimorfonucleares y agregados de histiocitos rodeando una sustancia amorfa basófila, sin confirmación de material PAS positivo. ETT de control sin alteraciones, procediéndose a alta con seguimiento ambulatorio por complicaciones en la cicatrización de la herida quirúrgica.
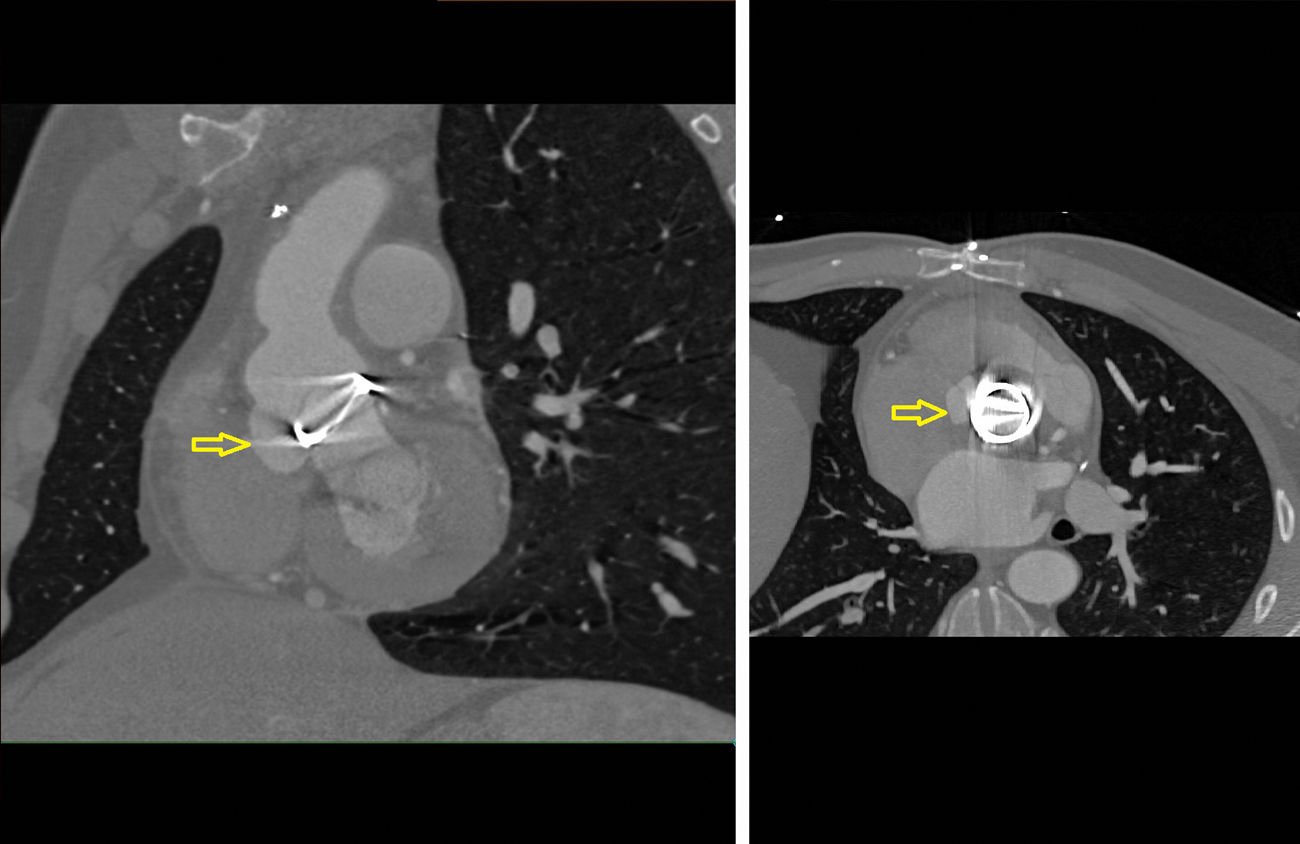
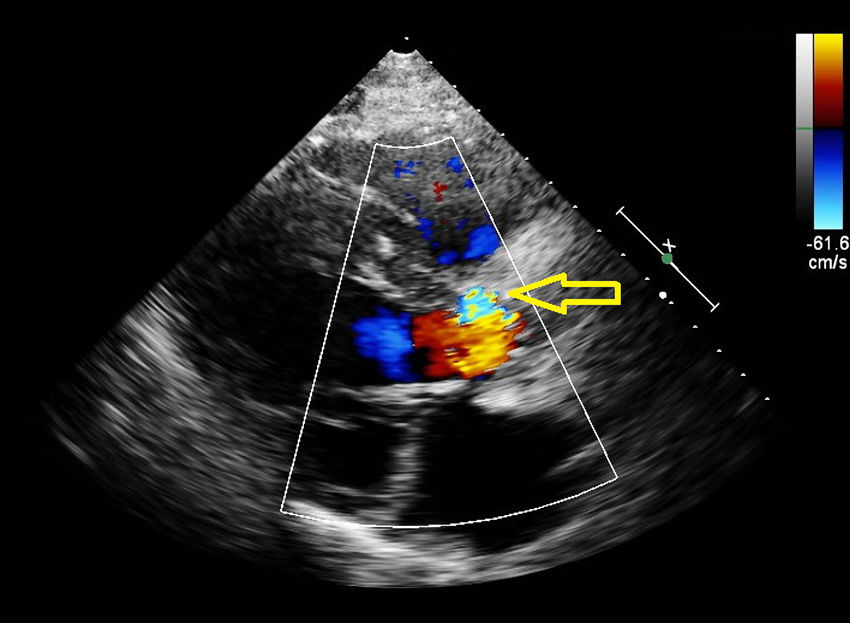
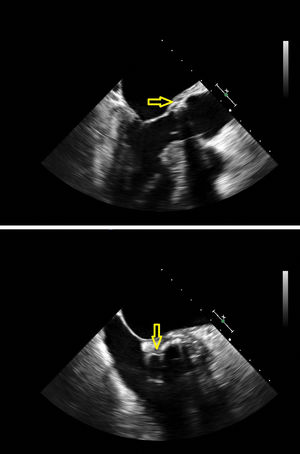
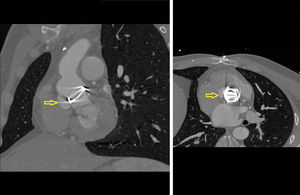
Ingresó nuevamente al cuarto mes postoperatorio por bloqueo aurículo-ventricular completo, requiriéndose implante de marcapasos definitivo. ETT y ecocardiografía transesofágica (ETE) (fig. 2) con masa oscilante en el tracto de salida del ventrículo izquierdo en la vertiente más anterior de la cara ventricular de la prótesis, sin imágenes claras de absceso. Presencia de regurgitación aórtica ligera que no podía definirse correctamente si era intra o periprotésica debido a la sombra acústica de la prótesis. En la TAC torácica (fig. 3), dehiscencia de la prótesis a nivel de la zona entre el seno no coronariano y el coronariano derecho, con dilatación sacular de la aorta. Ante la sospecha de endocarditis protésica precoz con seudoaneurisma, se decidió reintervención. Se encontró una dehiscencia en la zona del seno no coronariano, con disrupción del anillo aórtico nativo y una cavidad seudoaneurismática subanular. Tras explante de la prótesis, todo el anillo nativo se encontraba afectado, con tejido desvitalizado y esfacelos, requiriéndose la transección aórtica completa para un buen abordaje. Se reparó el seudoaneurisma con parche de pericardio, reconstruyendo el anillo nativo en toda su circunferencia con el mismo e implantándose una nueva prótesis mecánica bidisco, de 18mm.
ETE preoperatoria previa segunda cirugía. Arriba, plano de 3cámaras y abajo, plano de corte en eje corto de la válvula aórtica. Se objetiva un seno derecho dilatado con 2imágenes lineales en su interior. Se puede apreciar una masa oscilante en el tracto de salida del ventrículo izquierdo, en la vertiente más anterior de la cara ventricular de la prótesis.
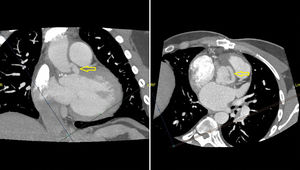
TAC torácica previa segunda cirugía. A la izquierda, corte sagital-oblicuo y a la derecha, corte axial. Se visualiza la prótesis aórtica mecánica bidisco, con un tejido adyacente a las suturas de la prótesis, sospechándose dehiscencia a dicho nivel, con una dilatación sacular de la aorta entre el seno coronario derecho y el no coronario.
Revisión por taponamiento cardiaco tardío, como en la primera intervención, sin objetivar tampoco punto sangrante. Completó nuevo ciclo de antibioterapia empírica con daptomicina y cloxacilina. Se revaloró el caso conjuntamente con Reumatología y Enfermedades Infecciosas. Se había retirado el certolizumab tras la primera intervención como posible causa de alteraciones en la cicatrización e inmunidad. Todos los cultivos microbiológicos, la serología y la detección de ácidos nucleicos solicitados resultaron negativos, al igual que en el primer episodio. La detección de Tropheryma whipplei (T. whipplei) en la muestra quirúrgica, la saliva, las heces y la biopsia duodenal fue negativa. Tampoco se detectó citomegalovirus en biopsia gástrica. Se encontró un tiempo de agregación plaquetaria alargado, sin otras alteraciones en la hemostasia. Ausencia de marcadores de autoinmunidad. La ETT posterior solo detectó unos gradientes de la prótesis moderadamente elevados.
Al quinto mes de la segunda intervención, acudió a Urgencias por disnea progresiva con importante clínica congestiva. ETT con regurgitación aórtica muy severa y reaparición de seudoaneurisma periprotésico extenso que producía cabeceo de la prótesis. Ventrículo izquierdo dilatado, pero con función sistólica aparentemente conservada. Se intervino de forma urgente, realizándose implante de homoinjerto aórtico en posición subcoronaria con cierre del seudoaneurisma con los mismos puntos. Pese a que la ETE intraquirófano mostró una insuficiencia aórtica ligera, la ETT posterior evidenció una insuficiencia probablemente moderada intrahomoinjerto, difícil de cuantificar por ser un jet excéntrico, sin limitación en movilidad de los velos a su apertura. Ventrículo izquierdo dilatado con una depresión moderada-severa de la función. Reproducción de cavidad en la raíz aórtica. Se decidió completar una nueva pauta de antibioterapia empírica y alta con control ambulatorio para repetir pruebas complementarias, a la espera del resultado de cultivos.
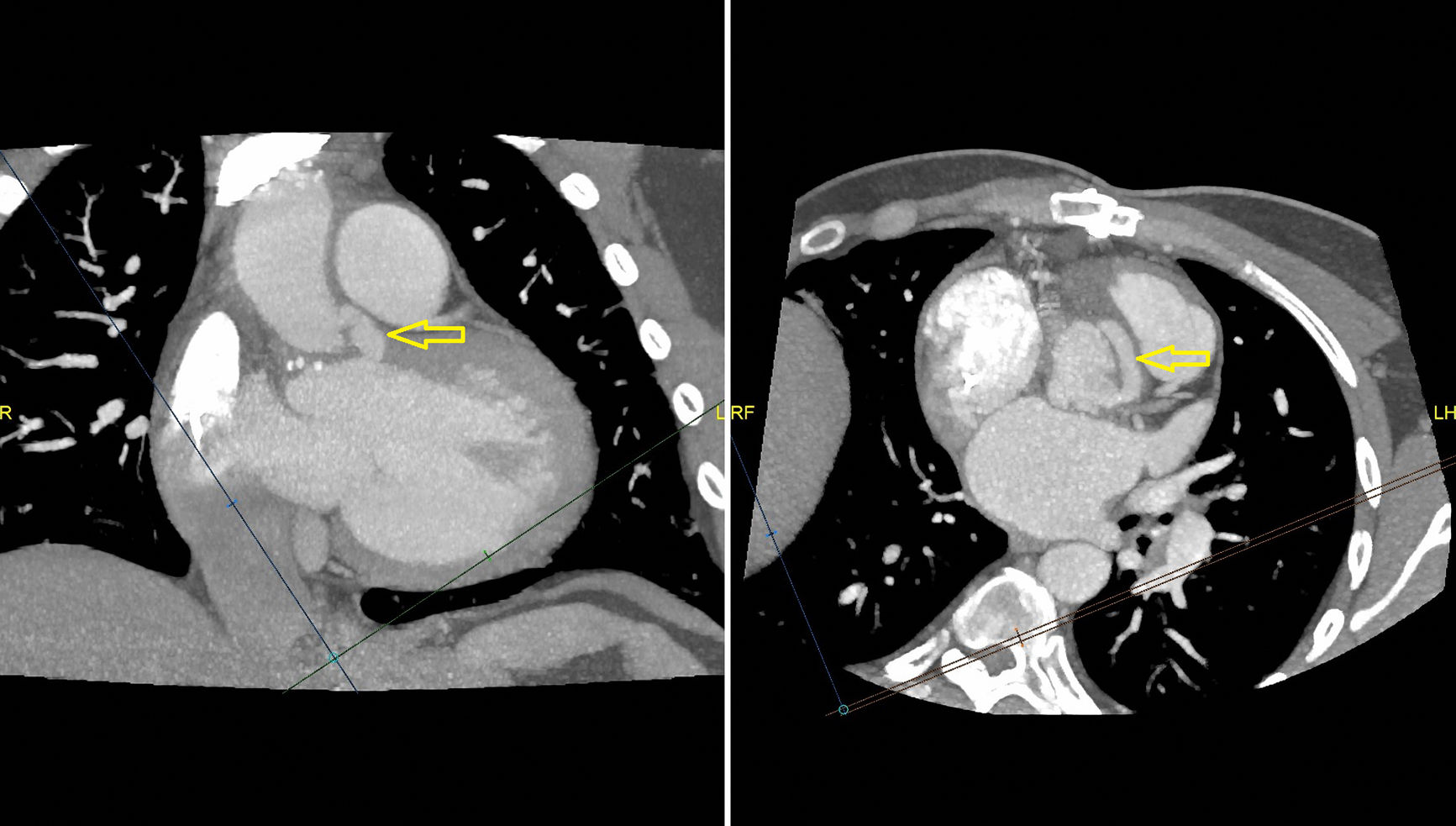
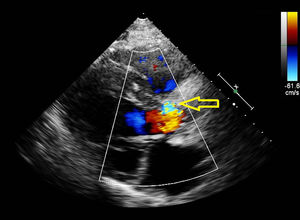
La ETE al mes de la última intervención apreciaba la insuficiencia con jet excéntrico en sentido anterior, al menos moderada. En la raíz aórtica se observaba una cavidad con expansión sistólica compatible con seudoaneurisma, confirmado por TAC torácica. La reacción en cadena de la polimerasa de la muestra quirúrgica de esta última intervención resultó positiva para T. whipplei. Dadas la estabilidad clínica y la complejidad del caso, se decidió iniciar tratamiento para la enfermedad de Whipple con doxiciclina e hidroxicloroquina, y control ambulatorio. En la actualidad, en el sexto mes postoperatorio, se aprecia situación clínica estacionaria, asintomático para disnea u otra sintomatología cardiorrespiratoria. Una nueva ETT (fig. 4) y una nueva TAC (fig. 5) no han mostrado cambios respecto a exploraciones previas, optando por un manejo conservador por el momento dada la complejidad del caso.
La EI es una enfermedad grave, que requiere de rápido manejo basado en diagnóstico de sospecha para un tratamiento médico y quirúrgico óptimo, con decisiones de un equipo multidisciplinar. Con cultivo negativo llega a ocurrir en aproximadamente el 30% de los casos. Puede ser consecuencia de un tratamiento antibiótico previo o debido a hongos y bacterias de cultivo exigente. Destacan microorganismos que requieren para su diagnóstico de serología, como Coxiella burnetii, Bartonella, Aspergillus, Mycoplasma pneumoniae, Brucella y Legionella pneumophila, y microorganismos que requieren de pruebas de reacción en cadena de la polimerasa como T. whipplei, Bartonella y hongos. También, se deben tener en cuenta los diagnósticos de endocarditis no infecciosa y una eventual reacción alérgica a la prótesis en caso de endocarditis protésicas1,2.
Respecto a la enfermedad de Whipple, causada por la bacteria intracelular grampositiva T. whipplei, sus principales manifestaciones clínicas incluyen poliartritis migratoria, pérdida de peso y diarrea, pero puede ser también responsable de cuadros cardiológicos, musculoesqueléticos, genitourinarios y neurológicos. Es una causa infrecuente de EI con cultivo negativo, con pocos casos publicados en la literatura de esta manifestación, y puede dar lugar también a miocarditis y pericarditis, llegando a insuficiencia cardiaca congestiva. El diagnóstico se puede realizar a través la histopatología, demostrando una tinción PAS positiva, pero su confirmación se realizará con la detección del ácido nucleico a través de la reacción en cadena de la polimerasa, que presenta una elevada especificidad, pero baja sensibilidad, pudiendo dar lugar con frecuencia a falsos negativos. En el caso clínico descrito, no se encontró la tinción PAS positiva en la muestra histopatológica. El diagnóstico fue a través de la detección del ácido nucleico. Se recomienda tratamiento con ceftriaxona o penicilina o meropenem por vía intravenosa de inicio, durante 2semanas, para su penetración en el sistema nervioso central. Posteriormente, se debería pasar a tratamiento de mantenimiento, por vía oral, con trimetoprim-sulfametoxazol o doxiciclina e hidroxicloroquina, durante un año3,4.
Debe realizarse diagnóstico diferencial con la endocarditis no infecciosa o de Libman-Sacks. Esta puede ser una manifestación del lupus eritematoso sistémico o de la polimialgia reumática, aunque se ha visto mayor relación con el síndrome antifosfolípido. Suele manifestarse dando lugar a insuficiencia valvular severa asociada con eventos embólicos. En algunos casos cursa con fiebre y mialgias, encontrando una vegetación valvular. Puede elevar marcadores inmunitarios, pero no son específicos, siendo muy difícil su diagnóstico diferencial con la EI5,6. Es menos común la asociación con la espondiloartropatía, como la que presentaba el paciente. No obstante, está descrita la relación de insuficiencia aórtica con bloqueos de la conducción cardiaca debido a fibrosis de la zona de conducción en el septo ventricular en estos pacientes7,8. La endocarditis de Libman-Sacks debe manejarse con anticoagulación y tratamiento de la enfermedad subyacente si la hay1,5,6.
Además, el uso actual de agentes biológicos para el tratamiento de las enfermedades autoinflamatorias, como el certolizumab (anti-TNF) que usaba el paciente, favorece la aparición de infecciones bacterianas y por otros agentes, lo que también debe tenerse en cuenta9. El TNF es una citocina proinflamatoria que produce activación de la producción de óxido nítrico en el endotelio para su vasodilatación y aumento de la permeabilidad, que junto a las inmunoglobulinas y el complemento produce la activación de los linfocitos T y B. De esta forma, su inhibición favorece el riesgo de contraer infecciones poco frecuentes o reactivar una infección latente.
También, hay relación de la betatalasemia con alteraciones de las fibras elásticas, como la piel, los ojos y el tejido vascular, lo que puede dar el llamado seudoxantoma elástico. Y la asociación de la betatalasemia con el riesgo de ictus puede ser un factor confusor en el diagnóstico de EI, lo que también se sospechó en el caso clínico presentado10.
ConclusiónEn conclusión, presentamos el caso de un hombre de 35 años que, con el probable diagnóstico de EI, fue intervenido de sustitución valvular aórtica y posterior manejo con tratamiento antibiótico empírico convencional. Requirió revisión por taponamiento tardío y presentó complicaciones en la cicatrización de las heridas, difícilmente atribuible con certeza a su espondiloartropatía de base, al tratamiento con certolizumab para la misma o a la betatalasemia, al no haber una relación causa-efecto clara. Se reintervino al cuarto mes postoperatorio con la sospecha de recidiva precoz de EI, encontrándose una insuficiencia aórtica periprotésica, un seudoaneurisma infraanular y una disrupción de todo el anillo aórtico nativo. Y requirió nueva reintervención pasados 5 meses con implante de homoinjerto aórtico en posición subcoronaria. Se realizó un exhaustivo diagnóstico diferencial de las posibles causas del cuadro endocardítico, pero no se consiguió confirmación de ninguna de ellas mediante las pruebas disponibles, excepto una positividad para T. whipplei en el material quirúrgico de la última intervención. No obstante, no fue hasta el segundo episodio cuando comenzó a pensarse en la posibilidad de esta etiología y en su búsqueda de forma activa. Es por ello la EI una entidad que requiere de un manejo multidisciplinar altamente especializado, dada la gravedad del proceso y su difícil diagnóstico etiológico sin confirmación en ocasiones, como en el caso presentado. Además, debe realizarse un seguimiento de estos pacientes, encontrándose una tasa de recurrencias del 2-6% que empobrece la supervivencia a largo plazo1. Esta experiencia descrita indica la importancia de ser agresivo, tanto en el tratamiento y la toma de decisiones como en la búsqueda etiológica.
Aprobación del comité éticoAprobado por el Comité de Ética de la Investigación con Medicamentos del Hospital Universitario y Politécnico La Fe.
FinanciaciónSin fuentes de financiación
Conflicto de interesesNo existe conflicto de intereses.