diabetes tipo 2
dipeptidyl peptidase-4 (dipeptidilpeptidasa 4)
glucagon-like peptide-1 (péptido 1 similar al glucagón)
hemoglobina glicosilada
índice de masa corporal
Liraglutide Effect and Action in Diabetes
sulfonilureas
tiazolidindionas.
La diabetes mellitus tipo 2 (DM2) es una enfermedad que comienza con resistencia a la insulina y en la que, en su evolución, se va desarrollando progresivamente una pérdida de función de las células beta. El control metabólico puede verse agravado por diferentes circunstancias, como el sedentarismo, la ganancia de peso, las situaciones de estrés, los fármacos, etc. Todas estas situaciones confieren a la enfermedad cierto grado de predictibilidad. También presenta heterogeneidad, ya que aparece a cualquier edad, con o sin complicaciones crónicas, habitualmente en pacientes obesos pero también en delgados. Además, en su desarrollo están implicados un gran número de genes.
Se han planteado diferentes algoritmos de tratamiento, con tendencia a la uniformidad y sin tener en cuenta aspectos como la edad, el tiempo de evolución, la presencia o no de obesidad, ni, en definitiva, el grado de resistencia a la insulina o de deficiencia de ésta. Por otra parte, sabemos que, según el tipo de fármaco utilizado, podemos encontrarnos con importantes consecuencias, no sólo clínicas, sino también económicas. Por estas razones, la selección de un determinado algoritmo de tratamiento en la diabetes tipo 2 debe basarse en los siguientes puntos: eficacia hipoglucemiante, efectos sobre factores no estrictamente glucémicos (riesgo cardiovascular, peso, sensibilidad a la insulina, mantenimiento de células beta, etc.), seguridad, tolerancia y costes.
La estrategia terapéutica actual1 se fundamenta en la intervención precoz, comenzando con una dieta adecuada, ejercicio físico y evitación del tabaco, junto a la administración de metformina. Si ello no es suficiente, en un plazo máximo de 3 meses se pasa a la segunda etapa, que consiste en añadir sulfonilureas (SU), insulina basal, tiazolidindionas (TZD) o glitazonas, o incretinmiméticos, según las particularidades de cada paciente. Si no se consigue una hemoglobina glicosilada (HbA1c) <7%, se añade un tercer fármaco oral (SU o TZD) o, si el paciente ya estaba con insulina, se intensifica su administración con múltiples dosis de insulina, manteniendo metformina o la TZD2.
Sabemos que los pacientes con diabetes tipo 2, además del defecto de secreción de insulina, no suprimen la secreción de glucagón posprandial. Sólo los fármacos con efecto incretina tienen reconocida acción sobre el glucagón. El efecto incretina viene dado por la acción del péptido 1 similar al glucagón (GLP-1) que, liberado por las células intestinales tras la ingesta, incrementa la secreción de insulina y frena la de glucagón, además de retrasar el vaciamiento gástrico y producir sensación de saciedad. Este péptido tiene una semivida corta (<2 minutos), al ser inactivado por la dipeptidilpeptidasa 4 (DPP-4). Por ello, una de las estrategias utilizadas consiste en el uso de análogos de GLP-1 resistentes a la acción de la DPP-4 y de semivida más prolongada. La segunda estrategia terapéutica consiste en la administración de inhibidores de la DPP-4.
El análogo disponible de GLP-1 actualmente es exenatida, aunque liraglutida ya ha sido aprobado y se comercializará próximamente. Los inhibidores DPP-4 de los que disponemos actualmente son sitagliptina y vildagliptina, aunque se prevee la próxima comercialización de saxagliptina.
Análogos de GLP-1ExenatidaEs un agonista del receptor GLP-1. Se trata de un péptido sintético de 39 aminoácidos que presenta una homología del 53% con el GLP-1 y es resistente a la acción de la DPP-4. Se elimina por filtración glomerular, por lo que su uso está limitado en la insuficiencia renal. Existen ensayos clínicos que han evaluado la terapia adyuvante de exenatida con todos los hipoglucemiantes orales, así como con insulina3. En ellos se demuestra un descenso de la HbA1c de entre el 0,7 y el 1,1%, que el 40% de pacientes consiguen una HbA1c ≤7%, y una pérdida de peso media de 2,1kg, que llega hasta los 5,3kg a los 3 años de seguimiento4. Los efectos secundarios más comunes fueron las náuseas (57%) y los vómitos (17%), que aparecieron sobre todo en las primeras semanas y tendieron a desaparecer posteriormente. En estos estudios se describen también episodios de pancreatitis aguda. También se detectan anticuerpos antiexenatida en el 49% de los pacientes, aunque parecen carecer de influencia en el control glucémico5.
LiraglutidaEs un análogo GLP-1 de larga actividad, con una homología del 97% con el GLP-1 y resistente a la acción de la DPP-4. Los estudios con este fármaco se recogen en el programa LEAD (Liraglutide Effect and Action in Diabetes), que consta de seis ensayos aleatorizados (4.456 pacientes), doble ciego y controlados con placebo. El descenso medio de HbA1c fue del 1,1%, y el 50% de los pacientes consiguieron una HbA1c ≤7% y una pérdida de peso de entre 2,3 y 3,0kg a los 2 años de seguimiento6. Los efectos secundarios más frecuentes fueron las náuseas y los vómitos (40%), que tuvieron una presentación precoz. También se han descrito casos de pancreatitis con este fármaco7. La presencia de anticuerpos antiliraglutida es muy escasa, y no se asocia a pérdida de eficacia3,7. En estudios realizados en roedores se demuestra un incremento de hiperplasia y de tumores de las células parafoliculares con el uso de liraglutida en dosis muy superiores a las utilizadas en humanos. En los estudios controlados se han comprobado discretas elevaciones de la calcitonina en pacientes tratados con liraglutida; sin embargo, estos incrementos siempre estuvieron en el rango de la normalidad, manteniéndose en ese nivel tras más de 2 años de seguimiento8.
Inhibidores de la DPP-4SitagliptinaEs un potente inhibidor que consigue más del 80% de reducción de la actividad de la DPP-4. Su semivida es de 8 a 14 horas. El 80% se excreta inalterado por orina, por lo que no se recomienda su uso en caso de insuficiencia renal moderada o grave y en pacientes en hemodiálisis. En monoterapia o en asociación, se obtienen descensos de HbA1c de entre el 0,3 y el 0,9%3,9. No tiene efectos sobre el peso. Las hipoglucemias son raras y se asocian al tratamiento con SU. Se han descrito nasofaringitis, dermatitis, infecciones urinarias y cefaleas. No se han descrito efectos gastrointestinales de importancia10,11.
VildagliptinaConsigue una inhibición competitiva del 98% de la actividad de la DPP-4 a los 45 minutos y del 60% a las 24 horas. Aproximadamente el 85% de la dosis se elimina por orina y el 15% se recupera en las heces. La excreción renal de vildagliptina inalterada representa un 23% de la dosis administrada por vía oral. Asociada a hipoglucemiantes, obtiene descensos de HbA1c de entre el 0,5 y el 1%. Posee un efecto neutro sobre el peso. Los efectos secundarios son similares a los de sitagliptina11.
SaxagliptinaDe próxima comercialización, es un inhibidor de DPP-4 sumamente potente, selectivo, reversible y competitivo. Su administración inhibe la actividad enzimática de DPP-4 durante un periodo de 24 horas. Se elimina tanto por vía renal como por vía hepática. En estudios realizados asociada a metformina, SU o TZD se consiguen descensos de HbA1c de entre el 0,5 y 0,9%12. No ejerce influencia sobre el peso. Los efectos secundarios descritos son similares a los dos anteriores13.
Respuestas y propuestas al uso de fármacos con efecto incretinaEstos fármacos son una alternativa real para el tratamiento de la DM2. Los análisis disponibles indican que son efectivos en el control de la glucemia y poseen acción favorable o neutra sobre el peso (tabla 1). La baja incidencia de hipoglucemias confiere a este grupo de fármacos un claro valor añadido, aunque el riesgo de esta complicación deberá ser considerado cuando se asocien a secretagogos de insulina.
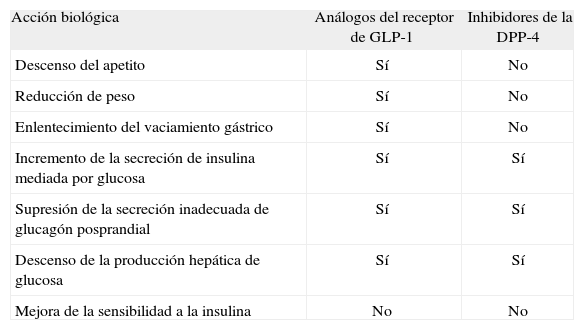
Modos de acción de los análogos del receptor de GLP-1 y de los inhibidores de la DPP-4
| Acción biológica | Análogos del receptor de GLP-1 | Inhibidores de la DPP-4 |
| Descenso del apetito | Sí | No |
| Reducción de peso | Sí | No |
| Enlentecimiento del vaciamiento gástrico | Sí | No |
| Incremento de la secreción de insulina mediada por glucosa | Sí | Sí |
| Supresión de la secreción inadecuada de glucagón posprandial | Sí | Sí |
| Descenso de la producción hepática de glucosa | Sí | Sí |
| Mejora de la sensibilidad a la insulina | No | No |
La acción sobre el control glucémico parece ser más acentuada en el caso de la glucemia posprandial, lo que se considera una ventaja de este tipo de fármacos debido a las limitadas opciones de que disponemos actualmente sobre este aspecto del control de la glucemia. La auténtica eficacia de estos fármacos se consigue más como terapia adyuvante que cuando se utilizan en monoterapia.
Exenatida y liraglutida consiguen una sostenida reducción de la HbA1c, con un número importante de pacientes en rango de control adecuado, además de una significativa pérdida de peso. Sus mayores inconvenientes son sus efectos secundarios y su administración por vía parenteral (subcutánea). El uso de estos fármacos debe ser considerado en los casos siguientes:
- •
Pacientes con un índice de masa corporal (IMC) ≥35kg/m2 con terapia oral (metformina y/o SU) y control metabólico inadecuado, especialmente si presentan problemas psicológicos o problemas asociados a la obesidad.
- •
También estarían indicados con un IMC <35kg/m2 cuando la terapia insulínica no esté aconsejada o se presenten comorbilidades de la obesidad14.
- •
Finalmente, cuando exista un inadecuado control con terapia oral múltiple, el uso de estos análogos constituye una buena alternativa a la terapia insulínica.
Los inhibidores de la DPP-4 tienen la ventaja de su administración oral y sus escasos efectos secundarios. Consiguen un descenso de la HbA1c algo inferior que con los fármacos anteriores. Al igual que con los agonistas del receptor de GLP-1, carecemos de datos definitivos sobre su eficacia y seguridad a largo plazo15.
- •
En pacientes con hiperglucemia moderada, la combinación de metformina con inhibidores de la DPP-4 puede ser una iniciativa adecuada en el tratamiento en pacientes de edad o con tendencia a las hipoglucemias.
- •
En pacientes que no toleran inicialmente la metformina, los inhibidores de la DPP-4 asociados a TZD representan una interesante alternativa, ya que esta asociación mejora considerablemente el control metabólico16.
- •
Si no se consigue un control metabólico adecuado, la asociación con SU también sería una alternativa si no se tolera la metformina, aunque esta asociación parece la menos eficaz4,17.
- •
En cuanto a la utilización de estos fármacos en las fases iniciales de la enfermedad como monoterapia, aunque teóricamente podría ser absolutamente adecuada, carecemos de datos suficientes para generalizar esta práctica.
El Dr. A. Hernández Mijares ha recibido honorarios por charlas y/o consultoría de GSK, Lilly, Novo Nordisk, Pfizer, sanofi-aventis y Solvay. Asimismo, ha participado en ensayos clínicos patrocinados por GSK, Lilly, Novo Nordisk, Pfizer y sanofi-aventis.
En el número de mayo-junio de 2010 de Avances en Diabetología se publicó una versión errónea de este manuscrito. Este documento sustituye al anterior y es el que debe citarse en caso de ser referenciado.