El término enfermedad tromboembólica venosa se refiere a varios procesos patológicos, entre los que destacan la trombosis venosa profunda, el tromboembolismo pulmonar, la hipertensión pulmonar tromboembólica crónica y el síndrome postrombótico. La importancia en nuestro medio reside en que es una patología que precisa un periodo de recuperación largo, de 3 a 6 meses, y que un diagnóstico tardío o no bien realizado puede ocasionar una enfermedad más grave e incluso un desenlace fatal. Es difícil establecer su prevalencia en el ámbito del deporte, aunque de forma empírica parece ser similar a la del individuo que no hace deporte. Sin embargo, el ámbito del deporte y su entorno ofrece condiciones clínicas de riesgo que pueden ser factores que precipiten su presencia, la contusión sobre el lecho vascular, el reposo de los viajes, la deshidratación, la masoterapia mal orientada, ciertas medicaciones o una predisposición genética. La presente guía ofrece una actualización del proceso, se expone la protocolización diagnóstica, las pautas de prevención y de tratamiento estándar y aplicado al deporte, pensando no solo en el deportista sino también en el profesional y en el personal acompañante.
The term venous thromboembolism refers to various pathological processes that include deep vein thrombosis, pulmonary embolism, chronic thromboembolic pulmonary hypertension and the thrombotic syndrome. The importance in sports activities is that it is a pathology that requires a long recovery period varying from 3 to 6 months, and a delayed or unsuccessful diagnosis can lead to a more serious illness and even death. Its prevalence in the field of sport is difficult to establish, but empirically seems to be similar to that of the individual who does not practice sport. However, the field of sport and its environment has other clinical risk conditions to be taken into account. Bruising on the vascular bed, rest, travel, dehydration, misguided massage therapy, certain medications, or a genetic predisposition, may be factors that precipitate their presence. This guide presents an update of the process, as well as the diagnostic protocol, with prevention guidelines and standard treatments and their application in sports, and takes into account not only the sportsman, but also in the professional and accompanying personnel.
El término enfermedad tromboembólica venosa (ETEV) aúna varios procesos patológicos, entre los que destaca la trombosis venosa profunda (TVP), el tromboembolismo pulmonar (TEP), la hipertensión pulmonar tromboembólica crónica y el síndrome postrombótico. La TVP es la presencia de un trombo dentro de una vena, acompañado de una respuesta inflamatoria variable. El TEP supone la generación de un trombo en el interior de una vena y su ulterior embolización en el territorio arterial pulmonar, obstruyéndolo total o parcialmente.
En el deporte, el riesgo intrínseco de padecer una ETEV es similar al del individuo no deportista. Sin embargo, los deportistas se encuentran en condiciones que pueden resultar de la exposición a factores de riesgo no habituales o con una frecuencia diferente, como son traumatismos, viajes, inmovilización, hemoconcentración, y policitemia. La presencia de un trastorno de hipercoagulabilidad genética añade un riesgo adicional1 que puede verse extraordinariamente aumentado en aquellos individuos que utilizan de forma fraudulenta ciertas sustancias dopantes. Por otro lado, la tromboflebitis puede originarse o facilitarse por diversas etiopatogenias, asociadas al traumatismo directo o indirecto, que se acompaña de una inflamación del vaso. La presencia del trombo puede ser previa o consecuencia de esta inflamación, siempre agravando el cuadro clínico.
Incidencia. Las revisiones más actualizadas indican que la incidencia del primer episodio de TVP en la población general es de 1,2/1.000 habitantes/año y afecta a un 3-5% de la población. Es la tercera causa de mortalidad cardiovascular, después del síndrome coronario y el accidente cerebrovascular. La mortalidad de la ETEV es del 14-17% a los 3 meses, y la del TEP, del 25% a la semana. La morbilidad explica la recurrencia de ETEV del 5-7% a los 3 meses; la de TVP del 20% a los 5 años, y la de TEP del 23% a los 5 años; síndrome postrombótico del 17-50% al año y del 23% a los 2 años, hipertensión arterial pulmonar del 1 al 5%2, e incidencia de hemorragias graves del 5%3.
EtiopatogeniaLa ETEV es una enfermedad multifactorial y compleja en la que la interacción de factores genéticos —estimados en un 60%— y ambientales, el uso de anticonceptivos orales, el embarazo, la inmovilización o el cáncer, entre otros, determinan en cada individuo el riesgo de trombosis4. Es importante destacar que los factores genéticos juegan un papel muy importante, y que será la exposición a factores ambientales protrombóticos la que determinará la aparición del episodio.
De estos factores genéticos conocemos las deficiencias de la antitrombina iii, la proteína C y la proteína S (anticoagulantes naturales de la cascada de la coagulación sanguínea), la mutación Factor V Leiden y la mutación G20210A en el gen de la protrombina o F-II. En los últimos años esta lista se ha ampliado, y en la actualidad existe evidencia científica sólida que demuestra la implicación de otras alteraciones genéticas en el riesgo de trombosis5. En función de estas evidencias científicas es imprescindible evaluar la presencia de factores genéticos protrombóticos a la hora de evaluar el riesgo de trombosis de un deportista, especialmente si este presenta historia personal o familiar positiva de enfermedad tromboembólica. La integración de información clínica y genética permite disponer de más información para un diagnóstico, un tratamiento y una prevención más eficaces y personalizados de la enfermedad tromboembólica.
La patogenia, o desarrollo, de la TVP involucra 3 factores que se conocen como tríada de Virchow: daño de la pared venosa, estasis venosa e hipercoagulabilidad. El daño del endotelio provoca que este pierda la capacidad de inhibir la coagulación e iniciar el proceso fibrinolítico. La estasis debida a inmovilización u obstrucción venosa inhibe el clearance y dilución de los factores activados de la coagulación. Por fin, los estados trombofílicos congénitos o adquiridos promueven el proceso trombótico6, 7. Los factores que pueden facilitar la aparición de una TVP de carácter transitorio se muestran en la Tabla 1.
Tabla 1. Factores desencadenantes de enfermedad tromboembólica venosa, transitorios o adquiridos
| Estimación del riesgo | |
| Factores desencadenantes mayores | |
| Inmovilización con yeso | 36,5 |
| Cirugía mayor ortopédica | 16,2 |
| Cirugía general | 9,5 |
| Traumatismo grave | 4,8-8,6 |
| Inmovilización en cama | 5,6 |
| Enfermedad autoinmune (brote) | 3,9-16,4 |
| Embarazo y puerperio | 4,3 |
| Factores desencadenantes menores | |
| Viaje largo de más de 5 h | 2,8 |
| Ingesta de AINE | 2,5 |
| Obesidad | 2,3 |
| Cáncer | 1,8-2,2 |
| Infecciones | 1,7-2,7 |
| Ingreso en hospital | 1,9 |
| Cualquier enfermedad grave | 1,7 |
| Fármacos antipsicóticos | 1,5-1,8 |
| Insuficiencia renal crónica | 1,6-1,9 |
| Raza negra | 1,6 |
| Polución ambiental | 1,5 |
| Tamoxifeno/raloxifeno | 1,5 |
| EPOC | 1,4-1,6 |
| Varices | 1,4 |
| Diabetes mellitus | 1,4 |
| Insuficiencia cardíaca congestiva | 1,4 |
| Anticonceptivos orales | 1,3 |
| Tabaquismo | 1,1-1,5 |
| Terapia hormonal sustitutiva | 1,2 |
La estimación del riesgo se reporta en medidas como hazard ratio, riesgo relativo u odds ratio. Se consideran todas ellas como aproximadamente equivalentes 44 .
El estado de hidratación deficiente favorece cualquiera de los criterios previos 34,45 .
Las TVP de extremidades inferiores se clasifican según su localización en:
DistalesIncluyen: venas gemelares (gastrocnémicas), tronco tibioperoneo (tibiales posteriores y peroneas), tibiales anteriores y venas sóleas.
Son asintomáticas en el 75% de los casos.
Solo un 5% dan lugar a TEP o síndrome posflebítico.
Sin tratamiento, el 20-30% progresan al territorio proximal.
ProximalesIncluyen: vena ilíaca externa, vena ilíaca interna, vena femoral común, vena femoral profunda, vena femoral superficial y vena poplítea.
El 90% de los TEP son causados por émbolos procedentes de TVP proximales.
DiagnósticoSe realiza mediante la evaluación del riesgo, la valoración clínica y las exploraciones complementarias8.
Evaluación del riesgoLa probabilidad de diagnóstico de la TVP se establece según el modelo de Wells para trombosis proximales9, 10, 11 (Tabla 2).
Tabla 2. Probabilidad del diagnóstico de trombosis venosa profunda (TVP). Criterios de Wells
| Parálisis, paresia o reciente inmovilización con férula de los miembros inferiores | +1 |
| Encamamiento > 3 días o cirugía mayor con anestesia general o regional en las últimas 12 semanas | +1 |
| Hinchazón global de la pierna | +1 |
| Aumento del diámetro de la pantorrilla >3 cm unilateral (medido 10 cm por debajo de la protuberancia tibial) | +1 |
| Sensibilidad a la palpación localizada a lo largo del sistema venoso profundo | +1 |
| Edema con fóvea limitado a la pierna sintomática | +1 |
| Venas superficiales colaterales (no varicosas) | +1 |
| Neoplasia activa (en tratamiento < 6 meses) | +1 |
| El diagnóstico alternativo es tanto o más probable que el de TVP | –2 |
Probabilidad clínica alta si ≥ 3, moderada si 1-2, y baja si = 0.
En el deportista activo existe una clasificación de los factores de riesgo que aúna los propios de su actividad con los relacionados con su calidad de individuo físicamente activo (Tabla 3). El estudio del riesgo genético en pacientes y en familiares con riesgo de padecer episodios tromboembólicos se estudia en función de los factores enumerados en la Tabla 45, 12.
Tabla 3. Clasificación de los factores de riesgo para enfermedad tromboembólica venosa (modificado de guía PRETEMED) y su posible aparición en el deportista activo
| Factor | Deporte | Factor | Deporte |
| Constitucional | Circunstancias clínicas agudas | ||
| Embarazo | ACV con paresia de miembro inferior | ||
| Edad | Deshidratación | Sí | |
| Puerperio | IAM | ||
| Estilo de vida | Infección aguda grave | Posible | |
| Encamamiento/inmovilización | Accidental | Insuficiencia cardíaca | |
| Hábito tabáquico | Posible | Traumatismo miembro inferior | Sí |
| Viajes en avión (> 6 h) | Sí | Circunstancias clínicas crónicas | |
| Fármacos e intervenciones | Diabetes mellitus | Posible/PP | |
| Anticonceptivos orales | Femenino | E. Inflamatoria intestinal | Posible/PP |
| Antidepresivos | Posible/PP | EPOC descompensado grave | |
| Antipsicóticos | Hiperhomocisteinemia | ||
| Catéter venoso central | Infección VIH | Posible | |
| Eritropoyetina | Mieloma múltiple | ||
| Inhibidores aromatasa | Posible/PP | Síndrome nefrótico | |
| Marcapasos | Posible/PP | Neoplasias | Posible |
| Tamoxifeno/raloxifeno | Obesidad (IMC > 30) | Posible | |
| Terapia hormonal sustitutiva | Trombofilia a | Posible | |
| TVP previa | Posible | ||
| Vasculitis | Posible/PP |
Posible/PP: indica que es posible su presencia, pero poco probable; Sí: indica que puede presentarse este factor.
a En el 87% de los pacientes con trombosis se identifican factores genéticos de riesgo.
Tabla 4. Indicaciones de la evaluación del riesgo de enfermedad tromboembólica venosa (ETEV) mediante estudio de predisposición genética. Thromboincode®
| Pacientes con patrón de ETEV |
| Pacientes con situación ambiental de riesgo de trombosis |
| Familiares de pacientes con historia familiar de ETEV |
| Patología que sugiere componente hereditario |
| Tromboembolismo venoso idiopático en < 45 años Trombosis venosa recurrente Trombosis venosa en territorios vasculares infrecuentes Púrpura fulminans neonatal Necrosis cutánea inducida por warfarina Pérdida fetal o abortos espontáneos TV en mujeres embarazadas TV en mujeres que toman anticonceptivos Trombosis arterial inexplicada |
Los signos principales de la inflamación son tumor, rubor, calor y dolor. El dolor suele ser el primer síntoma. De inicio insidioso o espontáneo y con sensación de pesadez o tensión en la extremidad, en muchas ocasiones se acompaña de impotencia funcional. La localización es variable, según la zona afectada. En el caso de los miembros inferiores, suele manifestarse en la región gemelar y sobre los trayectos venosos profundos (hueco poplíteo, canal de Hunter, región inguinal). El signo de Homans (la dorsiflexión forzada del pie con la rodilla recta provoca dolor en la pantorrilla y en el hueco poplíteo) solo aparece en un tercio de casos TVP, y más del 50% de pacientes cursan sin este signo, o aparece sin existir proceso5,13.
El edema inicialmente es blando y con fóvea, afectando a los territorios distales a la obstrucción venosa. Al palpar las masas musculares, sobre todo en los gemelos, se observa un endurecimiento característico. Este empastamiento no debe confundirse con el edema de tejido celular subcutáneo típico de otras afectaciones que nada tienen que ver con la patología venosa.
El aumento de la red venosa superficial se va desarrollando de forma paulatina como reflejo de un mecanismo de compensación para facilitar el drenaje venoso, y aunque puede no apreciarse en fases muy iniciales de la trombosis, puede ser un signo claro en trombosis proximales o algo más evolucionadas.
Dado que los síntomas y signos son muy poco específicos, propios de otras afecciones agudas o crónicas como la rotura fibrilar, la celulitis, el linfedema, ciertos procesos neurológicos, etc., debe realizarse una anamnesis y una exploración cuidadosa, acompañándose de otros métodos complementarios para facilitar el diagnóstico.
Exploraciones complementarias1. Ecografía doppler de miembros inferiores. Es la técnica de elección ante la sospecha de TVP proximales, con alta sensibilidad y especificidad en pacientes sintomáticos. Su sensibilidad disminuye en TVP distales y en pacientes asintomáticos, siendo su eficacia subóptima en pacientes con trombosis distales, trombosis pélvicas y trombosis recurrentes.
2. Analítica básica con hemograma, bioquímica y pruebas de coagulación determinando el dímero-D. Respecto a este, se considera normal un valor inferior a 500 mg/ml14. Los estudios acerca de su poder como marcador analítico de la ETEV concluyen que es una prueba de elevada sensibilidad (98-100%) y baja especificidad (35-39%)15. Si esto se combina con el valor predictivo negativo, que puede ser del 98%, hace de esta una prueba útil como diagnóstico de exclusión de TVP, pero no para establecerlo. Por este motivo, es un parámetro que forma parte de los algoritmos diagnósticos utilizados en la actualidad16 pero no tiene ningún valor por sí solo.El dímero-D se genera exclusivamente a partir de la degradación de la fibrina estabilizada, mientras que los productos de degradación del fibrinógeno (PDF) se originan tanto a partir de la degradación del fibrinógeno como de la fibrina no estabilizada; estos últimos originan fragmentos D monoméricos, pero nunca dímero-D17. Por eso, el dímero-D constituye un marcador específico de la actividad fibrinolítica en procesos que producen una excesiva formación de fibrina. Sin embargo, ciertos procesos patológicos que no son de naturaleza trombótica también pueden cursar con una elevación del dímero-D18.Posibles falsos negativos: en los pacientes con trombosis distales o infrapoplíteas tiene un valor predictivo menor, de alrededor del 85%; trombosis de más de una semana de evolución (pueden normalizarse las cifras), anticoagulados, trombosis distales y embolia pulmonar en arterias subsegmentarias. Valores elevados de dímero-D nunca serán suficientes para diagnosticar una ETEV. El valor del dímero-D sirve, además, para determinar la evolución del proceso19, 20.
3. Electrocardiograma y radiografía de tórax.
4. Angiorresonancia nagnética. Constituye un método diagnóstico en la enfermedad tromboembólica, no invasivo, con una sensibilidad y una especificidad comparables a la flebografía en trombosis de venas pélvicas y femorales, ofreciendo la posibilidad de una exploración conjunta de miembros inferiores y sistema respiratorio. Útil en pacientes con férulas, en el embarazo y en alérgicos al contraste iodado que precisan flebografía.
5. Tomografía axial computarizada (TAC). También la TAC con contraste es una prueba que puede ser útil, igualmente, para el diagnóstico de TVP proximales. Esta prueba permite valorar la ubicación de un filtro de vena cava colocado previamente en caso de que fuera preciso. Ante la sospecha de TEP, lo adecuado es realizar inicialmente una angio-TAC pulmonar, que ha demostrado su elevada sensibilidad en el diagnóstico de embolismo pulmonar frente a la angiografía y gammagrafía de ventilación-perfusión.
6. Determinación de la predisposición genética. Su determinación explica un 60% de los casos de ETEV. La presencia de cualquiera de las indicaciones que se presentan en la Tabla 4 justifica la evaluación de la misma.
La accesibilidad a la ecografía en el ámbito del deporte permite acelerar el proceso diagnóstico, por lo que la valoración del riesgo y la ecografía doppler se pueden realizar de una forma rápida ante la sospecha clínica, mientras se solicita y la determinación del dímero-D, que por otra parte puede ser inmediata si se dispone también de la tecnología adecuada. La presencia del dímero-D solo corroborará el diagnóstico previo de la ecografía doppler o nos orientará sobre la evolución del proceso.
Ecografía doppler 21La técnica de imagen por ultrasonidos se ha convertido en la prueba diagnóstica inicial y principal en el diagnóstico de la TVP, gracias a su alta sensibilidad y especificidad, especialmente en el sector venoso proximal. El signo más directo y fiable es la imposibilidad de colapso completo de las paredes venosas cuando se comprimen con la sonda ecográfica en proyección transversal. En ocasiones es posible visualizar directamente la textura del trombo intraluminal y valorar subjetivamente su antigüedad según el grado de ecogenicidad del trombo. A mayor ecogenicidad, mayor antigüedad.
La fiabilidad de la ecografía doppler en el diagnóstico de la TVP cuando se trata de valorar sectores venosos proximales (venas femorales, poplíteas y grandes venas proximales del sóleo y del gastrocnemio) ofrece una elevada sensibilidad (96%) y especificidad (98%). Sin embargo, cuando la TVP se encuentra limitada a las venas del plexo sóleo y gastrocnemio, la sensibilidad disminuye (73%)22. Debido a esta baja sensibilidad en el sector distal, se recomienda repetir la ecografía en una semana, en caso de que esta sea negativa y la sospecha clínica sea elevada23.
En la exploración de segmentos medios y distales del plexo sóleo y gastrocnemio resulta imposible asegurar el colapso completo de la pared de todas y cada una de las venas sóleo-gemelares. Se debe, de forma importante, al pequeño calibre de las venas a este nivel y a su dificultad para apreciar la compresibilidad completa como signo directo de la presencia de un trombo. En estas circunstancias cobra especial relevancia la experiencia del explorador, la optimización de cada equipo de ecografía doppler con flujos lentos, la comparación sistemática con la extremidad contralateral asintomática, las maniobras de aumento eficaz del flujo mediante expresión de la almohadilla plantar con la extremidad declive, la detección de color con independencia del ángulo de exploración de la sonda ecográfica (angio o power-doppler) o la utilización selectiva de ecocontrastes.
Signos indirectos de normalidad son la existencia de flujo espontáneo o la variación del flujo en relación con los movimientos diafragmáticos. Son detectables mediante el modo B color o espectro doppler. Sin embargo, ello solo es posible detectarlo en venas de gran diámetro, como las venas femorales o el eje venoso iliocavo. En los sectores más distales es preciso valorar la permeabilidad de los plexos venosos plantares o sóleo-gemelares mediante compresión manual o con manguito.
Los signos ecográficos que nos ayudarán a diferenciar los cuadros crónicos de los agudos son:
• La vena no se colapsa por completo y su diámetro es normal, a diferencia de lo que ocurre en las TVP agudas, en las que el diámetro está aumentado.
• Las paredes de la vena pueden observarse engrosadas y están mal definidas.
• El material trombótico en el interior de la vena no es ecolúcido ni homogéneo, como ocurre en las TVP agudas.
• Existen con frecuencia, en el entorno de la vena ocluida total o parcialmente, sistemas venosos de suplencia, con desarrollo de circulación venosa colateral que discurre por espacios anatómicos atípicos.
• Existen venas con ocupación parcial de su luz, que demuestran insuficiencia valvular a las maniobras de provocación de reflujo venoso.
• Existe un informe de exploración mediante ecografía doppler del episodio agudo previo que nos permite compararlo con la exploración actual.
El informe de ecografía doppler de una exploración de sospecha de una TVP aguda debe indicar:
• Si la ausencia de colapso de la pared venosa es completa o parcial.
• Si el diámetro de la vena está o no aumentado con respecto a la extremidad contralateral.
• Definir el sector venoso afectado por la trombosis y su extensión proximal y distal.
• Definir las características ecográficas del trombo (ecolúcido o ecogénico).
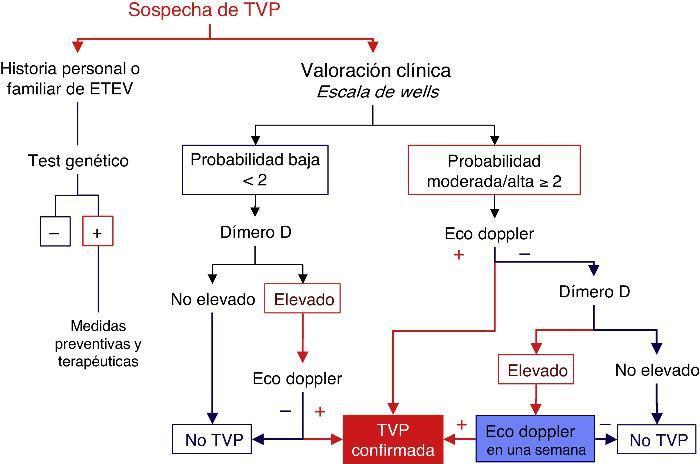
Figura 1. Algoritmo diagnóstico de la TVP en el deportista. La accesibilidad del diagnóstico ecográfico, facilita la aplicación diagnóstica de esta técnica de una forma temprana. El médico del deporte debe familiarizarse con la exploración del territorio vascular para tal fín.
Sin embargo, debe recordarse que los criterios clínicos de estratificación de Wells, unidos a la determinación del dímero-D, permiten una buena eficacia diagnóstica a la TVP de miembros inferiores en los servicios de urgencias. En caso de baja probabilidad clínica con dímero-D negativo, se evita la realización de la ecografía doppler, ya que se asume que será negativa para el diagnóstico de TVP de miembros inferiores24 (Figura 2).
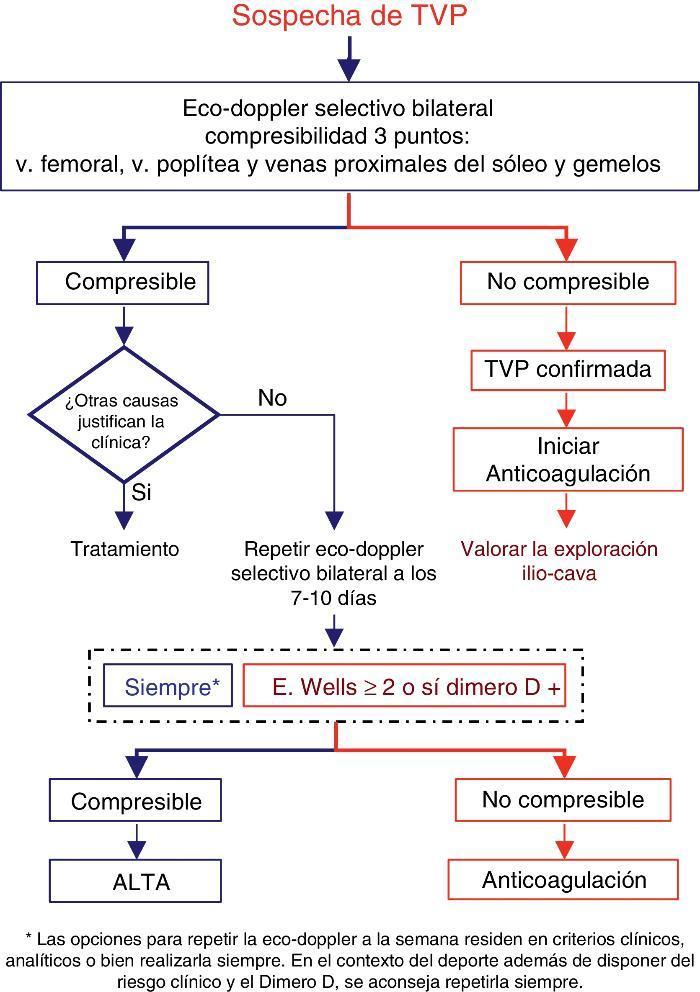
Figura 2. Valoración de la sospecha de TVP en medicina ambulatoria.
ComplicacionesTromboembolismo pulmonarLa mayor complicación es un TEP, y puede ocurrir desde venas importantes, como son las de las piernas, pelvis, abdomen, brazos o cuello. La incidencia anual de TEP es del 0,1%, oscilando entre el 0,01% en adultos jóvenes hasta el 1% en mayores de 60 años, y es causa de una elevada morbimortalidad25, 26. Más de la mitad de tales episodios se originan en la TVP. Por otra parte, nos encontramos ante una situación con elevada mortalidad derivada de una situación de infradiagnóstico. Tan solo uno de cada 3 fallecimientos por embolia pulmonar se diagnostica antes del fallecimiento, y cuando la embolia se produce y se trata adecuadamente, la mortalidad desciende de forma notoria. Debe tenerse en cuenta ante cualquier contusión importante en estas regiones y la aparición de síntomas que orienten el proceso. El TEP puede manifestarse solo con aparición de disnea y/o taquipnea en reposo o a pequeños esfuerzos, a veces además taquicardia, y en casos determinados, con dolor torácico y/o hemoptisis.
Recurrencia de la trombosis venosa profundaLos pacientes que son anticoagulados por un período breve (6 a 12 semanas) por TVP de pantorrilla no complicada tienen un 20% de riesgo de progresión del trombo hacia una TVP proximal. El riesgo de recurrencia es del 8 al 30%, y el de desarrollar síndrome postrombótico, del 1,8 al 20%. La anticoagulación oral a largo plazo supone un riesgo de hemorragia grave de hasta el 5% anual3. Este tipo de anticoagulación para prevenir la recurrencia debe considerarse en pacientes con antecedentes previos de trombosis o con una predisposición congénita o adquirida.
TratamientoEl tratamiento se establece en función de la orientación diagnóstica, y aúna medidas farmacológicas de anticoagulación y medidas generales27.
Trombosis venosa superficial o tromboflebitis• No precisa ingreso hospitalario, aunque sí en casos recidivantes, para descartar síndrome de Trousseau (tromboflebitis migratoria asociada a procesos neoplásicos).
• Heparina de bajo peso molecular (HBPM).
o Sin afectación del cayado de la safena (Clexane 40 mg, Fragmín 5.000 UI, Hibor 3.500 UI, Innohep 4500, todas cada 24 h, con una duración mínima de unos 7-10 días.
o En caso de afectación del cayado de la safena se recomienda anticoagulación 3 meses y cita con el hematólogo.
• Analgesia.
• Reposo relativo.
• Medias de compresión elástica graduada.
• Tratamiento ambulatorio, excepto para las razones expuestas en las Tabla 5, Tabla 6, Tabla 7.
Tabla 5. Criterios de exclusión de tratamiento ambulatorio
Criterios de exclusión Absolutos Falta de colaboración o dificultad para el seguimiento
Intenso dolor
Pacientes con sospecha de enfermedad grave subyacente o neoplasia
Alto riesgo de hemorragia: HTA maligna, úlcera péptica, cirugía reciente, alteraciones de la coagulación, trombocitopenia
Flegmasia cerúlea o alba dolens
Enfermedad grave que requiera ingresoRelativos Pacientes sin diagnóstico claro
Sospecha de embolismo pulmonar
Sospecha de progresión rápida o trombosis de la vena cava inferior
Síndrome posflebítico
Alergia, contraindicación o limitaciones al uso de heparina de bajo peso molecular: trombocitopenia, obesidad mórbida
Recidiva de TEP
Tratamiento fibrinolítico
Pacientes embarazadas
Riesgo de TVP recurrente (TVP previa, embarazo)
TVP bilateralTabla 6. Contraindicaciones de anticoagulación
Absolutas Relativas Hemorragia activa severa Cirugía inminente o reciente Hemorragia intracraneal reciente Traumatismo importante HTA grave no controlable Parto reciente Aneurisma cerebral o aórtico disecante Anemia severa Trastornos de la coagulación no Enfermedad ulcerosa activa corregidos Pericarditis o derrame pericárdico Tabla 7. Criterios para determinar la idoneidad en la selección del tratamiento de descoagulación en el paciente ambulatorio
HBPM NACO Administración Subcutánea Oral Adherencia al tratamiento Adecuada con riesgo Buena Nivel descoagulación Bueno Bueno T.° vida media ½ a 3 h 12 h Duración de la acción Hasta 12 h > 24 h Antídoto Sí (protamina) No Riesgo hemorragia contusión-ciertas actividades deportivas Bajo y controlado con adecuada dosificación Existe. No se aconseja actividad de contacto o riesgo de colisión Posible cirugía menor de UCIA Sí Complicado Contraindicaciones Tabla 8 Interacciones farmacológicas Inhibidores síntesis PG y antiagregantes plaquetarios Tabla 11 • Pautar antagonistas de la vitamina K (AVK) con intervalo terapéutico de índice internacional normalizado (INR) entre 2-3, nuevos anticoagulantes orales (NACO) o HBPM ajustadas al peso del paciente (Tabla 8)28, 29.
Tabla 8. Medidas farmacológicas para la profilaxis de la trombosis venosa profunda en pacientes
Nombre genérico Nombre comercial Dosis/día Contraindicaciones HBPM Bemiparina Hibor® 3.500 U (0,2 ml)/24 h Alergia, trombocitopenia, hemorragias Dalteparina Fragmin®
Boxol®5.000 U/24 h Enoxaparina Clexane®
Decipar®40 mg (0,4 ml)/24 h Nadroparina Fraxiparina® 3.800 U (0,4 ml) < 70 kg
U (0,6 ml) > 70 kgTinzaparina Innohep® 3.500 U (0,35 ml) < 70 kg
U (0,45 ml) > 70 kgInhibidores indirectos del factor Xa Fondaparinux Arixtra® 2,5 mg Alergia, hemorragia activa, endocarditis bacteriana aguda, insuficiencia renal aguda grave NACO Tabla 10 • Media de compresión hasta la raíz del miembro afectado, evitando la excesiva compresión y variándola en función de la evolución del edema del paciente30.
• Analgesia.
• Debe iniciarse cuanto antes la movilización de forma activa de la extremidad afectada. El reposo debe ser relativo desde el primer día de ingreso; aunque no se ha demostrado la necesidad de reposo, se debe individualizar en función del dolor y el edema (determinar días en función del estado del trombo por ecografía doppler por el especialista).
• Cuando se inicia la actividad: a) preservar al individuo de traumatismos directos o indirectos que precisen un nivel de hemostasia dentro de la normalidad; b) evitar ejercicios isométricos de elevada intensidad en la extremidad afectada o que soliciten un aumento de la presión diafragmática importante; c) determinar el grado de actividad en función del proceso de recuperación, determinado por las pruebas complementarias (dímero-D, calidad del trombo) y por el nivel de anticoagulación y asociado a aspectos que caractericen su actividad física habitual. En la Tabla 9 se muestran las recomendaciones estándar en este sentido, hasta alcanzar el alta deportiva31.
Tabla 9. Modelo de referencia hasta el alta deportiva después de iniciada la descoagulación
1.a a 3.a semana Retorno progresivo a la vida cotidiana 4.a semana Iniciar actividades sin carga (p. ej., natación) 5.a semana Iniciar ejercicios sin impacto (cadena cerrada) a ≥ 6.a semana Iniciar los ejercicios con impacto (cadena abierta) b a Bicicleta, ergómetros de gimnasio.
b Carrera, cuerda, juegos.Fuente: modificado de Partsch y Blättler 30 .
En los pacientes con un desencadenante transitorio (Tabla 1) la recurrencia es menor (3%) con respecto a un episodio espontáneo (10%). El tratamiento de 3 meses con AVK, NACO o HBPM disminuye en un 90% el riesgo de recurrencia. En pacientes con factor de riesgo mayor, como cirugía, el riesgo de recurrencia es < 3%, por lo que puede suspenderse a los 3 meses. En los moderados, el riesgo es algo mayor, de un 5%, por lo que se debe considerar mantener el tratamiento hasta los 6 meses, dado que el riesgo de hemorragia es del 2% al año.
Es decir, en el deportista que presenta un proceso de ETEV el tratamiento debe mantenerse al menos 3 meses, y se debe considerar una duración de hasta 6 meses.
PrevenciónCálculo de probabilidad de diagnóstico correcto ( tabla 2 )Pacientes de bajo riesgo: ninguna medida.
Pacientes con riesgo de ETEV: HBPM a dosis profilácticas o inhibidores de la trombina y factor X o AVK.
En los deportistas, la decisión de utilizar HBPM o NACO dependerá de la experiencia del equipo de trabajo y del tipo de deporte practicado. En la Tabla 10 se expresan los conceptos con relación a la posible utilización de uno u otro y la interacción con ciertos tratamientos o nutrientes (Tabla 11).
Tabla 10. Indicaciones de los nuevos anticoagulantes orales (NACO) aprobadas por la Agencia Europea del Medicamento en individuos adultos sin insuficiencia renal ni riesgo hemorrágico
| Dabigatrán Pradaxa® | Rivaroxabán Xarelto® | Apixabán Eliquis® | |
| Profilaxis de tromboembolia venosa en cirugía ortopédica programada | Dosis de inicio de 110 mg y luego 220 mg/24 h | 10 mg/24 h | 2,5 mg/12 h |
| Tratamiento de la trombosis venosa profunda (TVP) y de la embolia pulmonar (EP), y prevención de las recurrencias de la TVP y de la EP en pacientes adultos | 150 mg/12 h | 15 mg/12 h 3 semanas, luego 20 mg/24 h | 5 mg/12 h |
| Prevención del ictus y la embolia sistémica en pacientes con fibrilación auricular | 150 mg/12 h | 20 mg/24 h | 5 mg/12 h |
Fuente: Mateo 28 .
Tabla 11. Interacciones farmacológicas de nuevos anticoagulantes orales aplicable a los 3 en general
| Disminuyen el efecto | Actitud |
| Rifampicina, hierba de san Juan (Hypericum), carbamacepina, fenitoína | No asociar |
| Aumentan el efecto | Actitud |
| Antimicóticos azólicos (ketoconazol, itraconazol, voriconazol, posaconazol) | No asociar |
| Inhibidores de proteasas del VIH (ritonavir y similares) | No asociar |
| Anticoagulantes | No asociar |
| Antibióticos macrólidos (eritromicina, claritromicina) | Precaución |
| AINE | Precaución |
| Ácido acetilsalicílico o clopidogrel | Precaución. Aumenta riesgo de sangrado |
| Quinidina | Precaución |
| Amiodarona | Precaución |
| Verapamilo | Reducir dosis |
Fuente: Mateo 28 .
Por ejemplo, con NACO la actividad deportiva con contrincante o con posibilidades aunque remotas de una contusión desaconsejan la práctica de esa actividad. Con HBPM, una administración nocturna permite un entreno matutino con garantías, así como la administración matutina para un entreno vespertino.
Medidas generales y nivel de evidencia ( tabla 12 )ActividadLa inmovilidad aumenta 10 veces el riesgo de TVP32. Para prevenir la creación del trombo debe estimularse la movilidad de la musculatura de la extremidad inferior. Los ejercicios de piernas reducen la venostasis y deben ser recomendados (Evidencia I y II-1). Para ello es necesario:
• Caminar. Si se está en el avión o en el tren debe caminarse al menos unos 5 min cada hora a lo largo de los pasillos de la cabina o el vagón. Si se va en un automóvil o en autocar es conveniente parar cada hora y aprovechar los descansos para caminar.
• Si se debe estar sentado, hay que procurar activar la musculatura. Flexionar las rodillas, mover los pies, flexiones/extensiones, rotaciones, presionar los pies de forma progresiva contra el suelo, alternando uno y otro y los 2 a la vez.
Tabla 12. Nivel de evidencia considerado para establecer recomendaciones, de acuerdo con la United States Preventive Service Task Force (USPSTF)
| I | Evidencia obtenida de por lo menos un estudio adecuadamente diseñado, aleatorizado y controlado |
| II-1 | Evidencia obtenida de estudios adecuadamente diseñados y controlados, sin aleatorización |
| II-2 | Evidencia obtenida de estudios adecuadamente diseñados, de cohortes o caso-control, preferiblemente de más de un centro o grupo de investigación |
| II-3 | Evidencia obtenida de múltiples series con o sin intervención. Los resultados dramáticos de experimentos no controlados se consideran en este tipo de evidencia |
| III | Opiniones de autoridades respetadas, basadas en experiencia clínica, estudios descriptivos, o comunicaciones de comités de expertos |
La hemoconcentración aumenta la viscosidad de la sangre y reduce el flujo, especialmente en las venas profundas de las piernas de pacientes inmóviles33, 34, debiendo asegurarse una buena hidratación (Evidencia II-3).
Métodos mecánicosLos métodos mecánicos que provocan movilización pasiva de los miembros inferiores imitan las contracciones musculares y aumentan el volumen y la velocidad del flujo venoso35.
• Medias de compresión elástica graduada (8-18 mmHg).
• Compresión neumática intermitente (pre y poscirugía).
• Bombas mecánicas para pies (pre y poscirugía).
Los métodos mecánicos están indicados en los enfermos con riesgo aumentado de sangrado que haga peligrosa la profilaxis farmacológica. Están contraindicados en los pacientes con riesgo de necrosis cutánea isquémica y con neuropatía periférica.
Medias de compresión elástica graduada (MCEG). Un metaanálisis de estudios controlados aleatorizados en prevención de TVP36 encontró que la misma ocurría en el 8,6% de los pacientes tratados contra el 27% de los controles (OR: 0,34; IC 95%: 0,25-0,46)12, por lo que se puede decir que las MCEG son efectivas en la prevención de TVP en pacientes quirúrgicos (Evidencia I) y son preferibles las medias que cubren hasta por encima de la rodilla. La efectividad de las MCEG aumenta significativamente cuando se asocia a profilaxis farmacológica (Evidencia I).
Un estudio observacional multicéntrico encontró que el método combinado es más efectivo que la profilaxis farmacológica aislada37 (Evidencia II).
Compresión neumática intermitente (pre y poscirugía). No se precisan en esta revisión.
Bombas mecánicas para pies (pre y poscirugía). No se precisan en esta revisión.
Prevención de la enfermedad tromboembólica venosa en el deportePaciente. Deportista y personal acompañante con condiciones clínicas de riesgo aplicadas al ámbito del deporte, a las que debería incorporarse, con condición de riesgo, la presencia de factores genéticos (Tabla 13).
Tabla 13. Condiciones clínicas de riesgo de trombosis venosa profunda aplicadas al deporte
| Posibles condiciones presentes | Deportista alto nivel | Acompañante/entorno D×T | Deportista en general |
| Edad mayor de 40 años | No | √ | √ |
| Inmovilización prolongada o parálisis | Viajes/lesión | Viajes | Viajes/lesión |
| Traumatismo sobre la zona vascular | √ | No | √ |
| Enfermedad tromboembólica previa | √ | √ | √ |
| Presencia de factores genéticos | √ | √ | √ |
| Cirugía mayor (abdomen, pelvis, extremidades inferiores) | √ | √ | √ |
| Obesidad | No | √ | √ |
| Venas varicosas | √ | √ | √ |
| Insuficiencia cardíaca congestiva | No | √ | √ |
| Infarto de miocardio | No | √ | No |
| Accidente cerebrovascular | No | No | No |
| Fractura de pelvis, cadera o piernas | √ | √ | √ |
| Catéter venoso femoral | No | No | No |
| Enfermedad intestinal inflamatoria | √ | √ | √ |
| Síndrome nefrótico | No | √ | No |
| Uso de estrógenos | √ | √ | √ |
| Cáncer | No | No | No |
| Anomalías de la hemostasia | √ | √ | √ |
Consideración. El deportista puede sufrir contusiones de importancia, que comprometen el flujo venoso en mayor o menor medida y establecen un proceso inflamatorio del vaso y la consiguiente alteración procoagulante y limitando la anticoagulante. Estas afecciones pueden ser de cierta importancia sobre el tejido musculotendinoso y sobre los vasos sanguíneos de la zona, sobre todo si ocurren en la pierna, el tobillo o el pie, pues precisan en muchas ocasiones de inmovilización y de un cierto reposo. Hasta un 34% de las roturas de tendón de Aquiles cursan con TVP, con independencia de si se operan o no38. En otras, la necesidad de pruebas quirúrgicas, diagnósticas o reparadoras, como por ejemplo en la artroplastia de rodilla, las pautas de profilaxis quirúrgica proporcionan una orientación práctica limitada, pues dependiendo de la serie presentada, la prevalencia muestra un rango muy amplio y no está claro cómo traducir los resultados de los estudios aleatorizados a la práctica clínica, ya que buena parte de los casos de ETEV son por suerte limitados por la profilaxis de rutina cuando la hay, y son TVP distales asintomáticas. Por lo tanto, no hay consenso respecto a la aplicación real de profilaxis farmacológica en estas actuaciones, por lo que a los pacientes sometidos a artroscopia de rodilla se aconseja manejarlos en base a una decisión individual de la evaluación del riesgo de ETEV en lugar de un protocolo general39. Cabe mencionar que en un estudio reciente que valora la incidencia de TVP en sujetos a los que se practica artroscopia para reconstrucción del ligamento cruzado anterior se observa una incidencia de TVP del 12% durante la primera semana, que es superior cuando la cirugía se precisa para reparar otras estructuras en el mismo proceso. En definitiva, aumenta la incidencia alrededor de un 5% por cada 30 min de aplicación del torniquete. Así, pasa de un 5,6% si es < 90 min, del 12,8% si se halla entre 90 y 120 min, y del 17,4% si supera los 120 min40.
También debe considerarse que la práctica deportiva condiciona un cierto grado de deshidratación, con el consiguiente aumento de la viscosidad sanguínea, sobre todo si el sujeto no sabe o no puede hidratarse correctamente, o bien la pérdida de líquidos es muy abundante. Después de la competición no es inhabitual que el viaje deba iniciarse rápidamente. El avión o el automóvil/autocar son vehículos que no permiten la deambulación durante un cierto tiempo. En el territorio nacional los viajes en avión suelen durar menos de 2 h, pero competiciones y compromisos deportivos originan viajes muy superiores en duración y sedentarismo. El avión tiene también el inconveniente, además de la estasis venosa, de ser un medio donde se tiende a la deshidratación, por la humedad del ambiente41, aspecto que debe tenerse en cuenta durante el viaje en los deportistas. En estos aspectos (altura e hidratación), debemos indicar que los deportes realizados en altitud aúnan varios de los factores predisponentes, que aunque se sabe que por sí solos no tienen gran fuerza, se desconoce su sinergia en la creación de un entorno favorable a la presencia de ETEV, hipoxia, deshidratación, hemoconcentración, baja temperatura, ropas ajustadas, disminución de la movilidad, edad, viaje previo de larga duración42. Cualquier proceso sospechoso debe alertar un diagnóstico precoz, y en un sujeto con antecedentes debe valorarse su predisposición genética (Tabla 14).
Tabla 14. Factores fundamentales de riesgo en el deportista y su prevención
| Tabla 14a. Factores de riesgo |
| 1.-Traumatismo sobre la vena (o la arteria): contusión, laceración, elongamiento |
| 2.- Elementos facilitadores relacionados: |
| - Inactividad muscular (lesión, viaje..) |
| - Mala hidratación |
| - Limitación del flujo venoso (compresión, flexión articular), tratamiento procoagulante. |
| - Acción cruenta sobre la vena: física (inyecciones, masajes), química (anabolizantes, antibióticos, antinflamatorios, nutrientes,...) |
| 3.- Infección: streptococo, estafilococo y otros |
| 4.- Predisposición: insuficiencia venosa profunda / varices, trastorno de coagulación, enf. inmunológicas |
| Tabla 14b. Medidas de prevención |
| 1. Evaluación, diagnóstico y tratamiento adecuado |
| Aplicar medidas RICE: compresión, reposo (activo), frío y elevación |
| 2. Movimiento y movilización de la zona |
| 3. Facilitar y asegurar la hidratación |
| 4. Evitar compresión y limitación del flujo de retorno |
| 5. Evitar aumentar el proceso con manipulaciones innecesarias o incorrectas ante la sospecha del proceso |
| 6. Tratar la infección si está indicado |
| 7. Administrar HBPM profiláctica si está indicado. Valoración individual |
Las medidas de prevención son universales, y ante cualquier factor de riesgo deben valorarse todas.
Por último, no debemos olvidar que existen sustancias ergogénicas, como los anabolizantes esteroideos, la hormona de crecimiento, las transfusiones de hemoconcentrados, el uso de eritropoyetina, etc.43 que, con el objeto de preservar la salud del deportista y garantizar una competición limpia, son considerados dopaje y no se espera encontrarlos, pero que desafortunadamente no son infrecuentes en diversos ámbitos del trabajo físico, casi siempre adquiridos de forma ilegal, y que son causantes de un caleidoscopio de patologías serias, donde la ETEV está muy presente. Si estos condicionantes afectan más a individuos predispuestos o asociados a ciertas actividades deberá estudiarse, dado que parece existir una prevalencia alarmante de presentación de la embolia pulmonar en baloncesto46, con probabilidad asociada a idiosincrasias individuales, este suceso no ocurre o lo hace de forma muy diferente y menos llamativa en futbol profesional47. En el primer caso, es posible que las caracteristicas del deporte no sean las que predisponen y facilitan, sino que seleccionan sujetos que disponen de ellas y que también son fruto de una labilidad para presentar ETEV, en las que el entorno del deporte las pone a prueba.
En los viajes de más de menos de 2 h1 hay que tomar la precaución de:
• Caminar. Si se está en el avión o en el tren debe caminarse al menos unos 5 min cada hora a lo largo de los pasillos de la cabina o el vagón. Si se va en un automóvil o autocar es conveniente parar cada hora y aprovechar los descansos para caminar.
• Si se debe estar sentado, hay que procurar activar la musculatura. Flexionar las rodillas, mover los pies, flexiones/extensiones y rotaciones de tobillos, presionar los pies de forma progresiva contra el suelo, alternando uno y otro y los 2 a la vez.
• Evitar ropa que comprima, elásticos fuertes y pliegues en las zonas de flexión (Evidencia III).
• Tomar líquido (no alcohólico) de forma continuada. Hidratarse bien (Evidencia II-3).
En los viajes de más de 2 h, además de lo anterior hay que tomar precaución de:
• Asegurarse caminar cada hora > 5 min (Evidencia II-2).
• Asegurar movimientos de flexión articular de tobillos y rodillas con frecuencia (Evidencia II-2).
• Ocasionalmente, elevar las extremidades (piernas por encima de la cadera) (Evidencia II-2).
Si existe riesgo de trombosis venosa en algún sujeto:
• Usar medias de compresión progresiva (Evidencia II-3).
• Tomar, bajo prescripción facultativa, un anticoagulante.
• HBPM a dosis profilácticas (Evidencia I).
En definitiva, las recomendaciones son hidratarse bien, moverse a menudo, y para los que poseen alguna predisposición, medidas de compresión progresiva e incluso HBPM a dosis profiláctica.
Conflicto de interesesLos autores de este artículo no tienen ningún conflicto de intereses. No tienen ninguna relación contractual con ninguna de las empresas cuyos productos se puedan mencionar en el presente texto/guía, ni ningún interés económico personal al respecto.
1 La toma en consideración de los viajes cercanos a las 2 h es una decisión empírica basada en la máxima duración que pueden tener los viajes en avión en territorio nacional, e incluso continental. La mayor parte de los desplazamientos en autocar pueden superar ese periodo, aunque no siempre lleguen a los límites de la normativa sobre tiempos de conducción y descanso actual, reglamento CE n.° 561/2006: «Tras un periodo de conducción de cuatro horas y media, el conductor hará una pausa ininterrumpida de al menos 45 minutos».
Recibido 15 Junio 2015
Aceptado 10 Septiembre 2015
Autor para correspondencia. franchek.drobnic@fcbarcelona.cat