Resumen. La palabra 'angiosoma' comienza a incluirse en las publicaciones que.se refieren a la revascularización de la isquemia crítica de miembros inferiores. Es un concepto utilizado en cirugía plástica desde hace décadas y recientemente adquirido por cirujanos vasculares, que merece su revisión y actualización. [ANGIOLOGÍA 2009; 61: 247-57]
Summary. The word 'angiosome'is starting to be used in the literature that deals with the revascularisation of critical lower-limb ischaemia. It is a concept that has been used in plástic surgery for decades and has recently been taken up by vascular surgeons, and as a result deserves a review and update. [ANGIOLOGIA 2009; 61: 247-57]
A lo largo de un siglo [1], comienza a definirse el concepto de angiosoma. Manchot, en 1889, describe por primera vez los territorios cutáneos de irrigación arterial. En 1893, Spalteholz divide la circulación de la piel entre vasos directos e indirectos. Salmón, en 1936, diferencia 80 territorios y clasifica la piel, según densidad y tamaño vascular, en zonas hipovasculares (piel fija) e hipervasculares (piel móvil). En 1975, Schafer publica sus estudios sobre la vascularización arterial y venosa de las extremidades inferiores. En 1986, Cormack y Lamberty publican The arterial anatomy of skinflaps.
El sistema arterial aporta una presión constante al lecho capilar y forma una red continua a través de todo el organismo de vasos de pequeño calibre que acaban formando arcadas en su división más distal, y aumentan en número mientras su tamaño disminuye según se acercan al lecho capilar. La situación es reversa en el lado venoso.
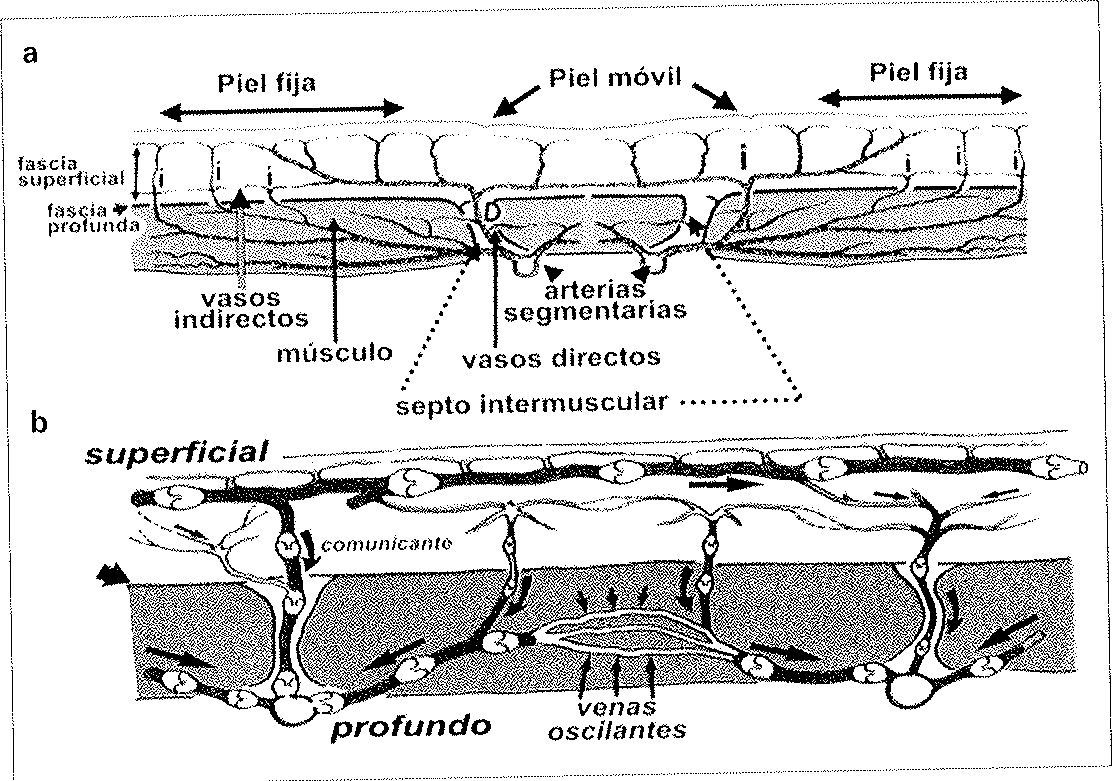
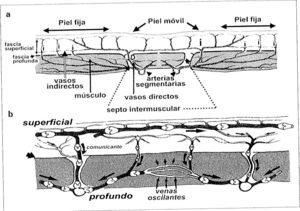
La piel se nutre por 442 ± 121 perforantes (160 fasciocutáneas y 282 musculocutáneas a partir de 120 arterias segmentarias o distributivas. La vascularización de la piel [2] puede dividirse esquemáticamente en (Fig. 1a):
- –
Vasos cutáneos directos septocutcíñeos. El trayecto, tamaño y densidad de las perforantes directas varía según las regiones del organismo. En la cabeza, cuello, torso, brazo y muslo, son largas y poco numerosas. En el antebrazo, pierna y dorso de manos y pies, son más pequeñas, más cortas y más numerosas. En la palma de la mano y la planta del pie, donde la piel es muy fija, la densidad de perforantes es máxima.
- –
Cada territorio está reforzado por vasos cutáneos indirectos musculocutáneos. Pequeños y muy numerosos, proceden de tejidos profundos, fundamentalmente los músculos. Independientemente de su origen, se unirán y formarán una red única con los vasos cutáneos directos.
La fascia profunda en el tronco forma una superficie bien desarrollada. Es elástica y permite el movimiento de tórax y abdomen. En las extremidades es mucho más rígida: la del muslo se continúa con la fascia intercompartimental en la pierna, donde recubre grupos musculares y forma parte del sistema retinacular, de donde nacen fibras musculares y se recubren tendones.
Concepto de angiosomaA partir de los estudios de Manchot y Salmón, Taylor y Palmer desarrollan en 1987 [3, 4] una división anatómica del cuerpo en territorios vasculares tridimensionales (TV3D) que denominan angiosomas. Corresponden a cada TV3D irrigado por una arteria segmentaria o distributiva (source artery). Es un concepto anatómico, no fisiológico.
Estas áreas están limitadas y a la vez unidas a otros angiosomas adyacentes por anastomosis verdaderas (vasos del mismo calibre que las arterias principales, como el arco palmar o plantar) y por 'vasos de choque' (de reducido calibre, conectan angiosomas a través de un mismo músculo, pero no entre músculos distintos), que forman una red continua en cada tejido.
Las venas también forman una red tridimensional bien desarrollada de canales conectados (Fig. 1b) que poseen válvulas para crear flujo unidireccional, pero están interconectadas por venas avalvulares oscilantes que permiten el flujo bidireccional entre territorios venosos adyacentes.
Las zonas de unión entre angiosomas adyacentes tienen lugar en la musculatura profunda. Los músculos proporcionan canales anastomóticos si la arteria y/o vena principal se obstruyen. La mayoría de los tejidos (músculos, nervios, huesos y tendones) están cruzados por dos o más angiosomas.
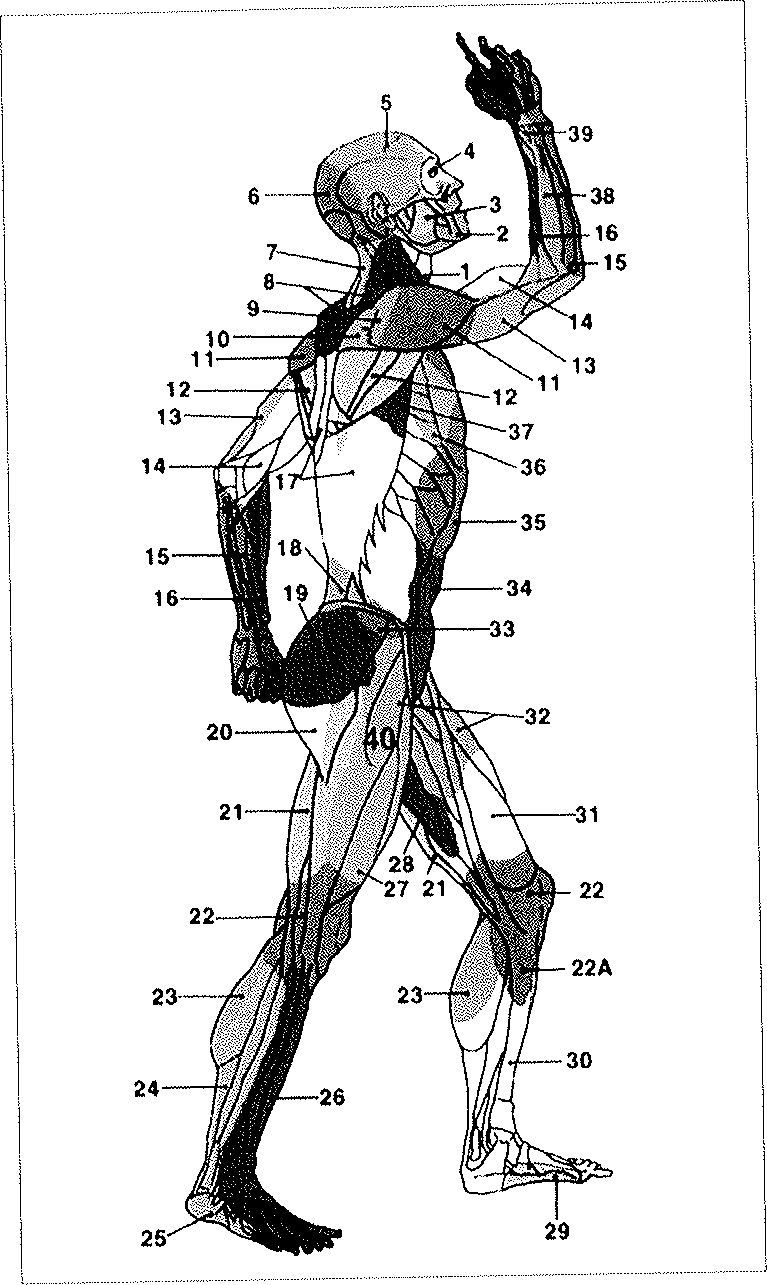
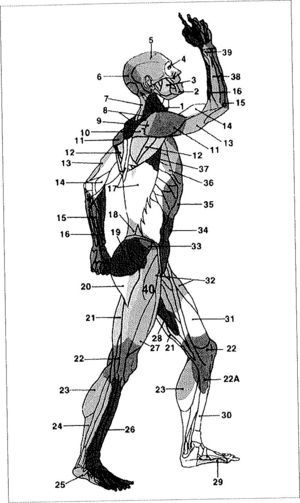
Taylor describió 40 angiosomas para cada hemicuerpo (Fig. 2). Algunos segmentos han podido subdividirse y han revelado que no alcanzan la superficie cutánea, como sucede en la cabeza y el cuello.
Angiosomas según Taylor: (1) tiroideo, (2) facial, (3) maxilar interno, (4) oftálmico (5) temporal superficial, (6) occipital, (7) cervical profundo, (8) cervical transverso (9) acromiotorácico, (10) supraescapular, (11) humeral posterior circunflejo (12) circunflejo escapular, (13) braquial profundo, (14) braquial, (15) ulnar, (16) radial (17) intercostal posterior, (18) lumbar, (19) glúteo superior, (20) glúteo inferior (21) femoral profundo, (22) poplíteo, (22a) genicular descendente o safeno (23) sural (24) peroneo, (25) plantar lateral, (26) tibial anterior, (27) femoral lateral circunflejo, (28) aductor (profundo), (29) medial plantar, (30) tibial posterior (31) femoral superficial, (32) femoral común, (33) circunflejo iliaco profundo, (34) epigástrico inferior profundo, (35) torácico interno, (36) torácico lateral, (37) toracodorsal (38) interóseo posterior, (39) interóseo anterior y (40) pudendo interno.
La teoría del angiosoma explica las variaciones anatómicas que existen entre los vasos de diferentes regiones del cuerpo, y entender los aportes de sangre a la piel y estructuras adyacentes, permite mapear los TV3D para planificar incisiones y colgajos, y proporciona la base para interpretar muchos procesos fisiológicos y patológicos, incluyendo el retardo de la cicatrización o las necrosis de los colgajos.
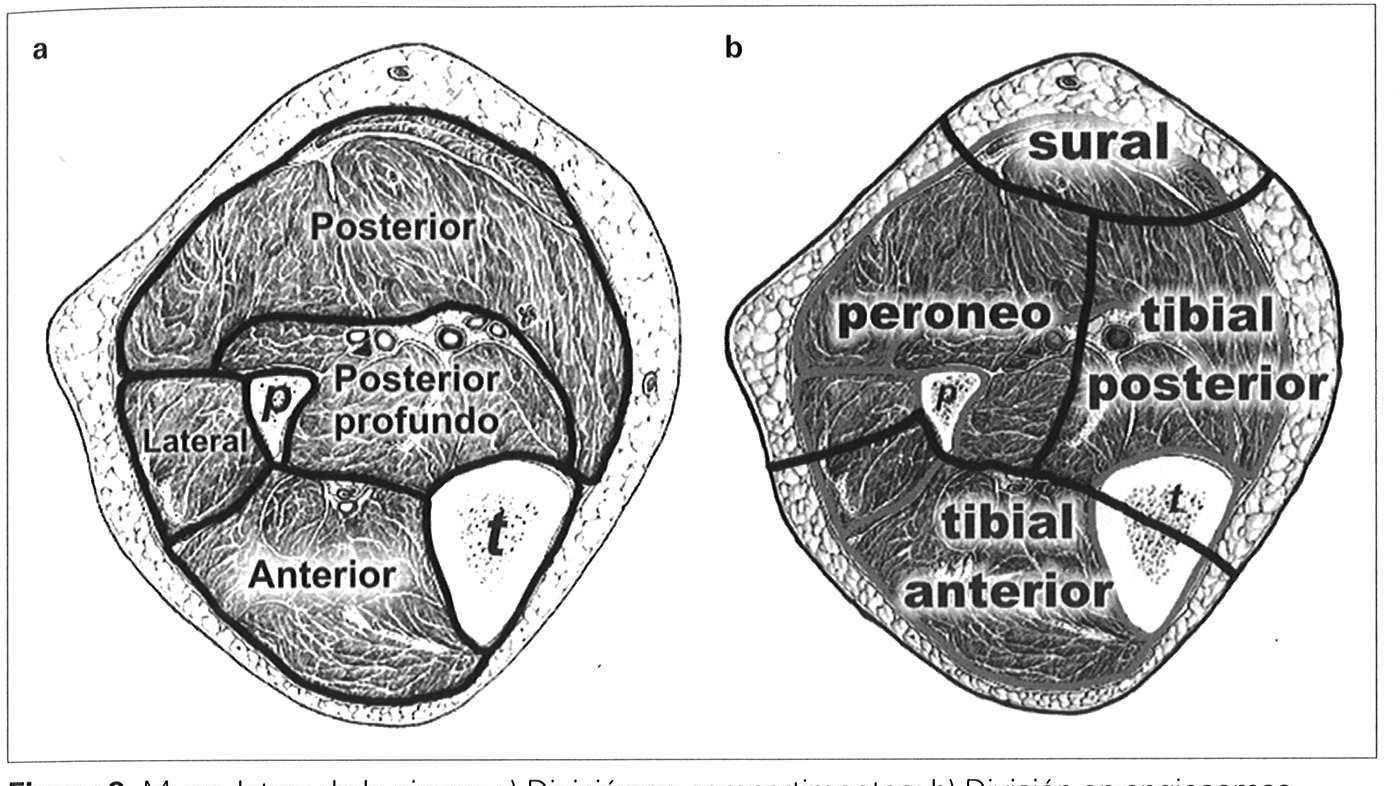
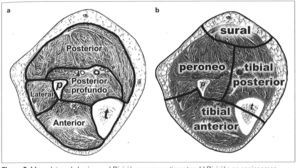
Compartimentos musculares de la piernaLos músculos de la pierna (Fig. 3a) están albergados entre t'ascias superficiales y profundas, acompañados por sus estructuras neurovasculares, formando compartimentos [5]:
- –
Músculos anteriores, nutridos por la tibial anterior. Son muy vulnerables a la isquemia, porque este compartimento de paredes rígidas está atravesado por muy pocas conexiones arteriales. Aloja a los músculos tibial anterior, extensor largo de los dedos, extensor largo del dedo gordo y tercer peroneo.
- –
Músculos laterales, nutridos por la tibial anterior y la peronea, con muchas anastomosis intramusculares. Son el peroneo largo y el peroneo corto.
- –
Musculatura superficial posterior, nutrida por ramas de la poplítea, tibial posterior y peronea. El gastrocnemio recibe ramas directas de la poplítea (surales), separadas para cada gemelo, y tiene muy pocas anastomosis entre ellas y entre el resto de arterias de la pierna. El soleo recibe muchos vasos cortos desde la poplítea, la tibial posterior, la tibial anterior y la peronea. El soleo, donde se anastomosan tres angiosomas, es una esponja vascular virtual, con arterias de diversos calibres y procedencias, que se anastomosan dentro del propio músculo. Es un auténtico shunt vascular vital, un 'corazón periférico', y desempeña un papel fundamental en el retorno venoso.
- –
Musculatura profunda posterior, irrigada por la poplítea por sus ramas geniculares, por la tibial posterior, por la peronea y algo por la tibial anterior. Incluye el flexor largo de los dedos, el flexor largo del dedo gordo y, más profundamente, el músculo tibial posterior.
Los síndromes compartimentales agudos, habituales en la pierna (traumatismo, isquemia prolongada, ejercicio intenso), se producen por aumento de pre sión intersticial intracompartimental por encima de la presión venosa, pero por debajo de la diastólica. Si la presión intersticial no disminuye con una fasciotomía, el resultado es la necrosis en los músculos del compartimento afectado.
De los cuatro compartimentos de la pierna, el tibial anterior es anatómicamente el más sensible a la isquemia, y es uno de los más afectados por el ejercicio crónico, porque el único aporte arterial que recibe procede de la tibial anterior, con un solo drenaje venoso, paralelo al eje arterial.
Las anastomosis entre angiosomas y entre las arterias principales se producen en el interior de los músculos y no entre ellas. Cada TV3D, que incluye piel, músculo, tendón, nervio o hueso, está cruzado por dos o más angiosomas. Es decir, cada TV3D puede recibir aporte vascular de varias arterias principales a través de sus ramas y anastomosis (Tablas I y II). La rodilla está cruzada por pocos músculos, pues en ese nivel son tendones. Los músculos principales que cruzan la rodilla (gastrocnemio y soleo) se nutren más proximalmente, desde la fosa poplítea.
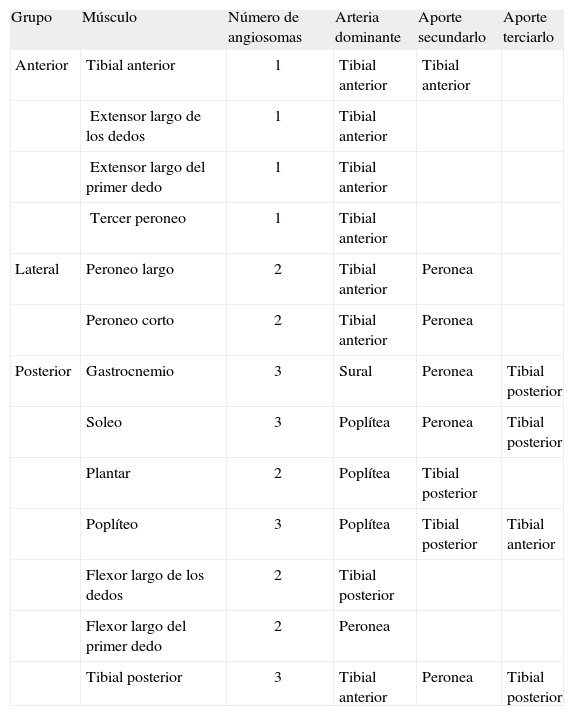
Aporte arterial a los músculos de la pierna.
| Grupo | Músculo | Número de angiosomas | Arteria dominante | Aporte secundarlo | Aporte terciarlo |
| Anterior | Tibial anterior | 1 | Tibial anterior | Tibial anterior | |
| Extensor largo de los dedos | 1 | Tibial anterior | |||
| Extensor largo del primer dedo | 1 | Tibial anterior | |||
| Tercer peroneo | 1 | Tibial anterior | |||
| Lateral | Peroneo largo | 2 | Tibial anterior | Peronea | |
| Peroneo corto | 2 | Tibial anterior | Peronea | ||
| Posterior | Gastrocnemio | 3 | Sural | Peronea | Tibial posterior |
| Soleo | 3 | Poplítea | Peronea | Tibial posterior | |
| Plantar | 2 | Poplítea | Tibial posterior | ||
| Poplíteo | 3 | Poplítea | Tibial posterior | Tibial anterior | |
| Flexor largo de los dedos | 2 | Tibial posterior | |||
| Flexor largo del primer dedo | 2 | Peronea | |||
| Tibial posterior | 3 | Tibial anterior | Peronea | Tibial posterior |
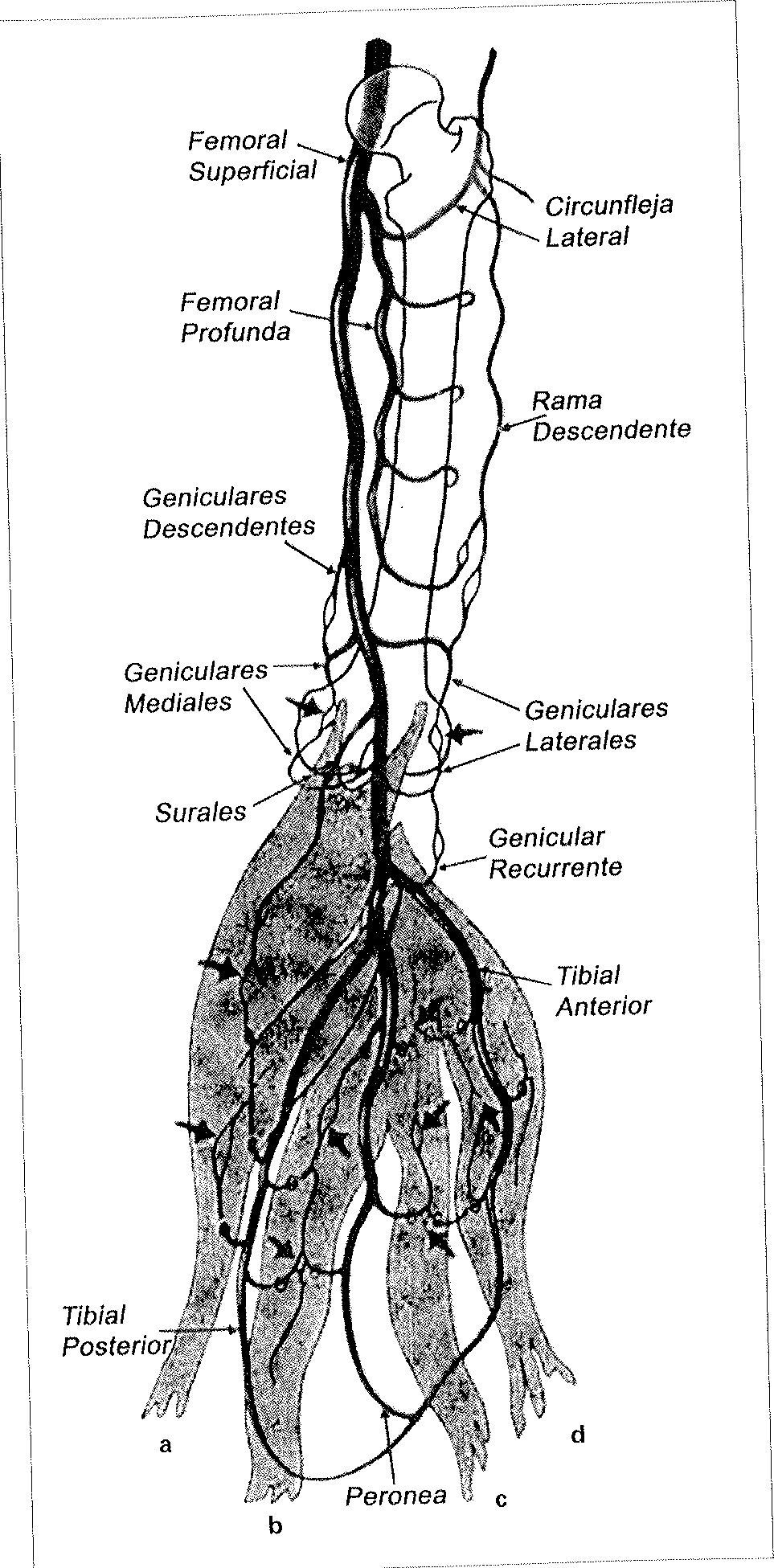
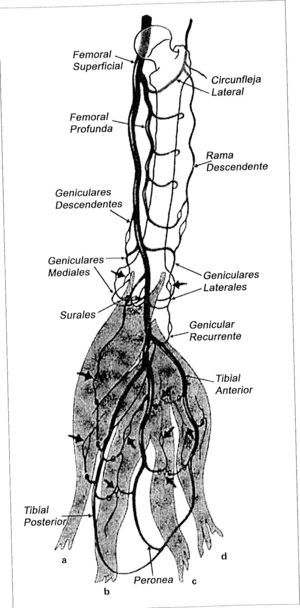
Las principales anastomosis vasculares que cruzan la rodilla son extramusculares, representadas por vasos geniculares (Fig. 4). Este detalle explica la observación de John Hunter y Salmón: la ligadura de la poplítea proximal a las arterias surales tiene un electo deletéreo sobre la vitalidad de la pierna, pero la ligadura de la poplítea distal en la fosa poplítea tiene poco efecto sobre la perfusión de la pierna.
Los compartimentos musculares de la pierna no son equiparables a angiosomas: el aporte de cada arteria se extiende diversamente por la musculatura de la pierna, y los músculos están cruzados por uno, dos o tres angiosomas (Tabla III).
Músculos de la pierna y número de angiosomas de los que dependen.
| Un angiosoma |
| Tibial anterior |
| Extensor largo de los dedos |
| Extensor largo del primer dedo |
| Peroneo medio |
| Dos angiosomas |
| Peroneo largo |
| Peroneo corto |
| Flexor largo de los dedos |
| Flexor largo del primer dedo |
| Tres angiosomas |
| Gastrocnemio |
| Sóleo |
| Poplíteo |
| Tibial posterior |
Taylor y Pan [6] han demostrado que la poplítea, la tibial anterior, la peronea y la tibial posterior, cada una por separado, irrigan el TV3D entre los huesos y la piel. Esta evidencia concuerda con el concepto de angiosomas.
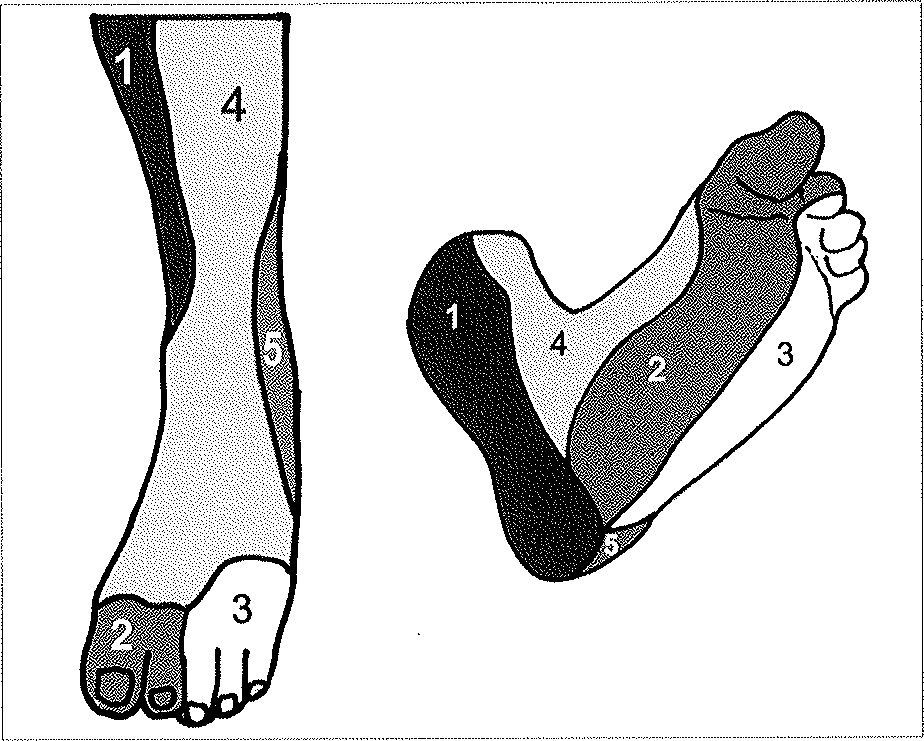
Los angiosomas de la pierna (Fig. 2) son seis: (22) poplíteo (22a) genicular descendente o safeno, (23) sural, (24) peroneo, (26) tibial anteno, y (30) tibial posterior. En el pie se incorporan los angiosomas plantar lateral (25) y plantar medial (29). Descendiendo hacia el tobillo, la pierna queda dividida por tres angiosomas (Fig. 3b):
- –
Tibial posterior. Se extiende desde la mitad de la cara anterior de la pierna hasta la parte media de la pantorrilla. El rafe central a lo largo del tendón de Aquiles demarca su límite lateral, y el borde medial anterior de la tibia demarca su límite anterior.
- –
Tibial anterior. Coincide con el compartimento muscular anterior de la pierna. El peroné actúa como límite lateral y la tibia como frontera medial.
- –
Peroneo. El límite medial es el rafe central del tendón de Aquiles, y su límite lateral es el borde anterior del compartimento lateral.
El pie soporta el peso corporal, mantiene la postura bípeda, el equilibrio y la locomoción. Su vitalidad depende de su sistema arterial, cuyo elemento central es el arco plantar profundo, del que se originan las arterias metatarsianas plantares, fundamentales para la irrigación de los dedos y de la región plantar profunda.
El tobillo y el pie, incluidos los dedos, están compuestos por cinco angiosomas a partir de las arterias principales de la pierna y sus ramas. Como el pie es un órgano terminal, el sistema arterial establece numerosas anastomosis arterioarteriales que permiten rutas alternativas al flujo sanguíneo en condiciones de arteriopatía distal, con frecuentes variaciones anatómicas.
El conocimiento de las fronteras entre angiosomas y sus anastomosis puede ayudar al cirujano vascular a orientar el mejor tratamiento revascularizador directo o endovascular para curar lesiones que se localizan en el órgano distal, o para plantear amputaciones funcionales.
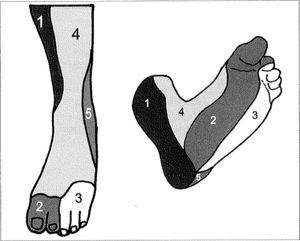
Los angiosomas del pie [7, 8] son continuación natural y final de los de la pierna (Fig. 5):
- –
Angiosomas de la tibial posterior. Son tres, alimentados por las arterias calcánea medial (tobillo y talón medial y plantar), plantar medial (arco plantar medial) y plantar lateral (arco plantar lateral). En el pie, ramas distales de la tibial posterior se anastomosan directamente con ramas distales de la tibial anterior.
- –
Angiosoma de la tibial anterior. Es único y abarca el dorso del pie. En el tobillo sus ramas forman importantes anastomosis con las ramas distales de la peronea y la tibial posterior.
- –
Angiosomas de la peronea. Es único. Tras irrigar la cara posterolateral de la pierna, esta arteria da las ramas perforante anterior (cara anterolateral del tobillo) y calcánea lateral (planta lateral del talón). El talón es una zona privilegiada irrigada por ramas de la peronea y de la tibial posterior. Attinger, en algunas publicaciones, considera dos angiosomas diferentes a partir de estas dos ramas, y divide el pie en seis angiosomas.
Angiosomas del pie.Tres de la tibial posterior: 1) Zona medial y plantar de tobillo y talón; 2) Arco plantar medial, dedos primero y segundo; 3) Arco plantar latera!, dedos tercero, cuarto y quinto. Uno de la tibial anterior: 4) Dorso de pie. Uno de la peronea: 5) Cara anterolateral del tobillo y planta lateral del talón. Dependiendo de la dominancia del sistema plantar o dorsal, los dedos pueden recibir su aporte arterial desde la plantar lateral, plantar medial o pedia.
Dependiendo de la dominancia del sistema plantar o dorsal, los dedos reciben su aporte de la plantar lateral, plantar medial o pedia.
Conexiones arterioarteriales en el tobillo, el talón y el pieEl pie está irrigado por dos sistemas: dorsal y plantar. El dorsal se centra sobre la pedia, continuación de la tibial anterior. Las ramas de la pedia que profundizan forman la principal anastomosis con el sistema plantar. El plantar se forma por la división de la tibial posterior en plantar medial y lateral.
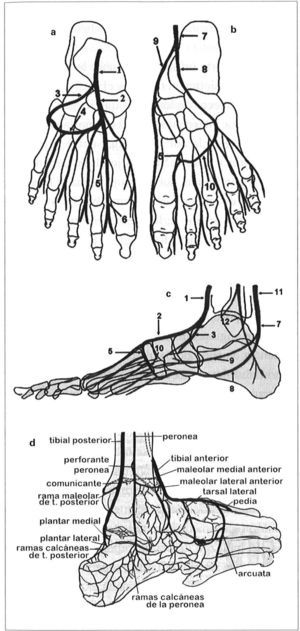
Estas anastomosis complejas (Fig. 6) impiden que el pie se quede sin aporte arterial a pesar de la oclusión de varias arterias. Si se tienen en cuenta, se puede conocer la vascularización de cada zona del pie, qué vías están enfermas y las vías de compensación, si existen; permiten planificar la revascularización a la arteria que esté irrigando predominantemente un angiosoma o tallar los colgajos correctos en caso de amputaciones.
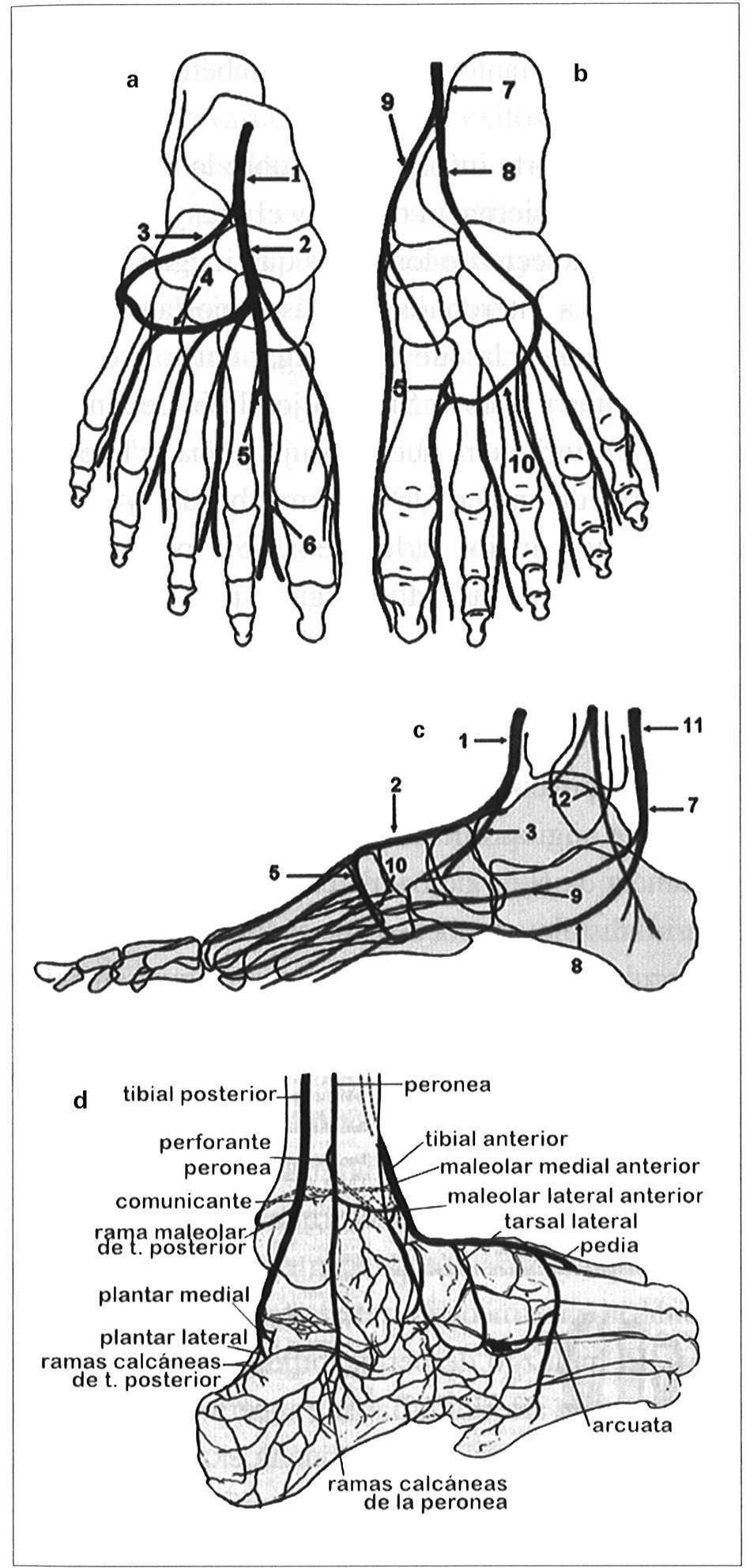
Vascularización arterial del tobillo, el talón y el pie: a) Vista dorsal: tibial anterior (1), da origen a la pedia (2) y tarsal lateral (3). Arteria arcuata (4), se origina en la pedia. Perforante profunda (5), que comunica con la circulación plantar en el primer espacio metatarsal. Dorsal del primer dedo (6), que finaliza la circulación anterior, b) Vista plantar que muestra la circulación posterior: tibial posterior distal o plantar común (7), que da origen a la plantar lateral (8) y la plantar medial (9). Arco plantar (10), anastomosis principal entre circulación anterior y posterior por la perforante plantar profunda (5). c) Vista lateral: tibial anterior (1), pedia (2), tarsal lateral (3) y perforante profunda (5); plantar lateral (8) y medial (9), arco plantar (10).Tibial posterior (11), que se convierte en plantar común. Peronea (12). d) Anastomosis alrededor del tobillo y tarso.
Es importante determinar si el flujo al dorso del pie procede de la tibial anterior, de la tibial posterior o de la peronea; y si el flujo al talón procede directamente de la rama calcánea de la tibial posterior o de la rama calcánea de la peronea, o indirectamente de la tibial anterior a través de las ramas maleolares.
Las anastomosis entre las arterias de la pierna alrededor del tobillo son:
- –
Tibial anterior-peronea. Conectan por la perforante anterior y la maleolar lateral. El flujo de la peronea a este nivel puede ser retrógrado o anterógrado.
- –
Peronea-tibial posterior. Comparten de una a tres comunicaciones transversas en el tejido laxo que rodea el tendón de Aquiles.
- –
Tibial anterior-tibial posterior. Comunican directamente a través de la pedia con las plantares. En situaciones de arteriopatía grave, la interrupción de estas conexiones puede provocar isquemia del compartimento tibial anterior y necrosis tisular. Cuando estas conexiones se interrumpen por el decúbito supino prolongado, se favorece la aparición de las úlceras de talón. También tienen importancia crítica para el aporte a la superficie plantar y dorsal del pie, si existe una obstrucción de alguna de las dos arterias principales, pues, si se interrumpe esta conexión durante una intervención o amputación, se puede provocar gangrena de la porción del pie que dependa de un flujo retrógrado.
El talón recibe flujo a partir de la rama calcánea de la tibial posterior y de la rama calcánea de la peronea. No hay conexiones anatómicas entre estas arterias, y casi siempre una predomina sobre la otra. En el pie, las conexiones son múltiples entre la circulación dorsal y la plantar.
La interconexión final está formada por un delicado plexo subdérmico arteriolar, que une la pedia con las plantares lateral y medial, y arropa circunferencialmente a toda la planta del pie. Este plexo de arterias de fino calibre desempeña un papel importante al permitir la recuperación de esta zona de los traumatismos diarios al caminar o si hay una alteración del aporte arterial.
Angiosomas y angiologíaLas anastomosis entre las arterias del pie pueden explorarse mediante Doppler de ultrasonidos (DU) para conocer qué arterias son dominantes y evaluar la calidad de flujo que llega a los cinco angiosomas, o si las interconexiones llevan flujo anterógrado o retrógrado en función del lugar donde se provoca la obstrucción arterial por la arteriopatía distal.
Más allá del valor de las técnicas de imagen modernas (dúplex, angiotomografía computanzada, angiorresonancia magnética), la permeabilidad de arterias muy distales que no se visualizan en la angiografía puede valorarse con DU, como ya se destacó hace un cuarto de siglo [9], aportando información sobre la etiología, los requisitos terapéuticos y las posibilidades de curación de las lesiones isquémicas de la pierna y el pie, tanto en pacientes diabéticos como no diabéticos.
El DU aporta información sobre la distribución arterial de la pierna, el tobillo y el pie, y la permeabilidad y trayecto de los vasos que irrigan cada angiosoma. La interconexión más importante que se debe evaluar es la que tiene lugar entre la circulación plantar y dorsal. Si el flujo al pie depende de una sola arteria, entonces el flujo global a la planta o al dorso dependerá de la permeabilidad y calidad de las interconexiones, lo que tiene importancia capital a la hora de tallar los colgajos para las amputaciones, para predecir la curación de las lesiones o para saber si los antibióticos van a llegar al lugar de la infección.
El estudio con DU debe ser suplementario a la exploración angiográfica, sobre todo en diabéticos. La presencia de flujo de buena calidad es frecuente en arterias distales y debe tenerse en cuenta para indicar revascularización endovascular o quirúrgica distal, y puede ayudar al cirujano a elegir el vaso más apropiado que asegure que el angiosoma amenazado va a recibir flujo directo, si es posible.
La no visualización de arterias que están permeables a nivel distal es un hecho habitual en arteriografías preoperatorias que pueden estar mal seriadas, o cuando la enfermedad arterial afecta a múltiples niveles. El hallazgo de permeabilidad distal se puede demostrar en arteriografías intraoperatorias, pero ya se puede vaticinar con una buena exploración con DU [10, 11]. Los hallazgos angiográficos por sí solos no deberían ser, por tanto, los decisivos en salvamentos de la extremidad o para determinar la posibilidad de revascularización.
Informaciones clave para planificar una revascularización distal, como la permeabilidad de los arcos arteriales del pie, la presencia y calidad de los trayectos colaterales, y la decisión sobre qué vaso es el más adecuado, también se pueden tomar basándose en estudios con angiorresonancia magnética [12].
Angiosomas y revascularizaciónA pesar de revascularizaciones exitosas, un porcentaje de lesiones distales del pie no se consigue curar. Incluso, pacientes con pulsos distales tras revascularización precisan amputación mayor, sobre todo cuando las lesiones afectan al talón.
Cuando un angiosoma se revasculariza indirectamente y va a recibir sangre a través de vasos retrógrados o colaterales, las posibilidades de curación de una lesión se rebajan en un 50%, y aumentan en cuatro veces las posibilidades de amputación mayor [13], por mala revascularización del área afectada o porque las conexiones entre los vasos revascularizados y las arterias segmentarias que nutren esa porción de tejido o angiosoma están obstruidas o enfermas.
Si no se puede recanalizar la arteria que nutre el angiosoma afectado, la revascularización podría no recuperar el tejido isquémico, a menos que se demuestren conexiones entre la arteria revascularizada y la arteria que nutre ese angiosoma: una revascularización satisfactoria es más compleja que restaurar sólo la circulación de una arteria específica [14-16],
El éxito técnico inicial y la duración de la angioplastia infrapoplitea (AIP) es limitado cuando se compara con la cirugía de revascularización distal, pero el beneficio clínico es aceptable, ya que las tasas de salvamento de extremidad son equivalentes a las de la cirugía [17].
La AIP puede ser una indicación primaria para pacientes con isquemia crítica. La tasa de reestenosis, reintervención o amputación es mayor en pacientes que no son candidatos a revascularización quirúrgica; sin embargo, intentar una AIP puede estar indicado como alternativa a la amputación primaria. Y aunque la reestenosis, la reintervención o la amputación son más probables después de una AIP, pueden obtenerse excelentes tasas de salvamento de la extremidad con un adecuado seguimiento de los pacientes, nuevas AIP o revascularización sin son necesarias [18].
Desde que se ha dado importancia al conocimiento de que la perfusión del pie tiene una distribución segmentaria repartida en angiosomas, distintos grupos destacan la preferencia y necesidad de recanalizar la arteria distal que alimenta directamente la parte del pie en donde se asienta la lesión isquémica [19,20], Esto no es siempre posible o práctico, y aunque en la mayoría de pacientes diabéticos la arteria habitualmente menos lesionada es la peronea, revascularizarla sola puede ser insuficiente [21].
Esto nos obliga a reflexionar sobre una mejor selección de pacientes para revascularización quirúrgica y endovascular, y valorar la perfusión de la piel y el flujo arterial al pie para identificar qué arteria distal o qué casos se beneficiarían mejor de un procedimiento más directo sobre determinados territorios arteriales.
Estas premisas adquieren importancia capital en pacientes diabéticos con isquemia crítica, ya que la AIP es efectiva para la curación de las úlceras isquémicas. La recurrencia clínica después de una revascularización exitosa es infrecuente, y el procedimiento endovascular puede repetirse varias veces. En estos pacientes diabéticos que se benefician de la recanalización distal, la amputación por encima del tobillo es muy rara. Por eso, merece la pena destacar de nuevo que la AIP debe tenerse en cuenta como primera indicación de revascularización en pacientes diabéticos con isquemia crítica [22, 23],
La AIP puede realizarse incluso en lesiones largas o a múltiples niveles, o en arterias calcificadas, para obtener un flujo directo al pie a través de un vaso tibial o peroneo. Paradójicamente, las características de la arteriopatía diabética distal permiten conseguir resultados angiográficos iniciales muy buenos, al igual que en la grave arteriopatía distal de la que son víctimas las arterias en la insuficiencia renal crónica terminal [24].
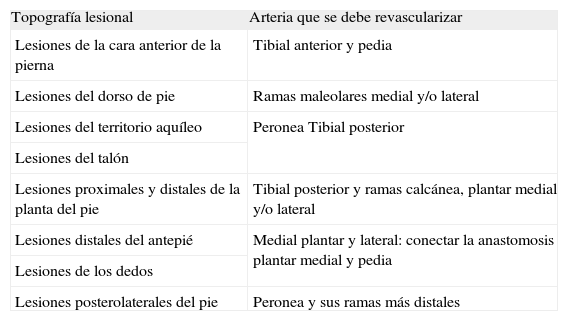
No obstante, es necesario destacar que un flujo directo a las arterias del pie no siempre se consigue usando técnicas endovasculares, a pesar de que se han mejorado mucho los materiales y dispositivos que usamos. Como a este nivel son frecuentes las anomalías o variables anatómicas, el tratamiento debería ir orientado, siempre, a recanalizar el vaso dominante donde se asiente la lesión [25] (Tabla IV).
Topografía lesional y arteria que se debe revascularizar.
| Topografía lesional | Arteria que se debe revascularizar |
| Lesiones de la cara anterior de la pierna | Tibial anterior y pedia |
| Lesiones del dorso de pie | Ramas maleolares medial y/o lateral |
| Lesiones del territorio aquíleo | Peronea Tibial posterior |
| Lesiones del talón | |
| Lesiones proximales y distales de la planta del pie | Tibial posterior y ramas calcánea, plantar medial y/o lateral |
| Lesiones distales del antepié | Medial plantar y lateral: conectar la anastomosis plantar medial y pedia |
| Lesiones de los dedos | |
| Lesiones posterolaterales del pie | Peronea y sus ramas más distales |
En lesiones de antepié y dedos, se debe procurar conectar las anastomosis entre las arterias plantar medial y pedia, basándose en la prevalencia angiográfica del flujo arterial hacia el dorso o la planta del pie.