El número de personas con inmunodepresión está aumentando considerablemente debido a su mayor supervivencia y al empleo de nuevas terapias inmunosupresoras en diversas patologías crónicas. Se trata de un grupo heterogéneo de pacientes en los que la vacunación como arma preventiva supone uno de los pilares básicos de su bienestar, por su elevado riesgo a padecer infecciones. Este consenso, elaborado conjuntamente entre la Sociedad Española de Infectología Pediátrica (SEIP) y el Comité Asesor de Vacunas de la Asociación Española de Pediatría (CAV-AEP), aporta unas directrices para programar un calendario adaptado a cada paciente en situaciones especiales que incluye recomendaciones generales, vacunación en pacientes con trasplante de médula y trasplante de órgano sólido, vacunación en niños con errores innatos de la inmunidad, vacunación en el paciente oncológico, vacunación en pacientes con enfermedades crónicas o sistémicas y vacunación en niños viajeros inmunodeprimidos.
The number of people with immunosuppression is increasing considerably due to their greater survival and the use of new immunosuppressive treatments for various chronic diseases. This is a heterogeneous group of patients in whom vaccination as a preventive measure is one of the basic pillars of their wellbeing, given their increased risk of contracting infections. This consensus, developed jointly by the Sociedad Española de Infectología Pediátrica (Spanish Society of Pediatric Infectious Diseases) and the Advisory Committee on Vaccines of the Asociación Española de Pediatría (Spanish Association of Paediatrics), provides guidelines for the development of a personalised vaccination schedule for patients in special situations, including general recommendations and specific recommendations for vaccination of bone marrow and solid organ transplant recipients, children with inborn errors of immunity, oncologic patients, patients with chronic or systemic diseases and immunosuppressed travellers.
En las últimas décadas, el número de personas con inmunodepresión está aumentando debido a su mayor supervivencia y al empleo de nuevas terapias inmunosupresoras en diversas patologías crónicas. Se trata de un grupo heterogéneo de pacientes en los que la inmunodepresión puede ser consecuencia de un error innato de la inmunidad, o ser secundaria a una enfermedad o tratamiento inmunosupresor.
En función de la causa responsable (tabla 1), la evolución de la enfermedad de base y los tratamientos aplicados, el grado de inmunosupresión puede ser leve, moderado o grave; además, puede ser estable, variable o incluso reversible en el tiempo1–3.
Clasificación de las inmunodeficiencias en función del grado de inmunodepresión
| Inmunodeficiencia de alto gradoa |
| • Errores innatos de la inmunidad con afectación de linfocitos B y T• Tratamiento quimioterápico y radioterápico recibido en los 6 meses previos• Receptores de TPH• Receptores de terapia CAR-T• Trasplante de órgano sólido• Fallo renal crónico. Tratamiento sustitutivo (hemodiálisis y diálisis peritoneal)• Infección por VIH con T-CD4<200 células/mm3 en ≥14 años o T-CD4<15% en <13 años de edad• Tratamiento con: azatioprina >3mg/kg/día, 6-mercaptopurina >1,5mg/kg/día, metotrexato >0,4mg/kg/semana o ≥15mg/m2/semana o ≥25mg/semana, leflunomida ≥0,5mg/kg/día o >20mg/semana, ciclosporina >2,5mg/kg/día, micofenolato mofetil ≥30mg/kg/día o >1000mg/día, ciclofosfamida oral >2mg/kg/día, tacrolimus >1,5mg/día• Corticoterapiab: tratamiento sistémico con prednisona (o dosis equivalente): ≥2mg/kg/día durante ≥14 días; ≥1mg/kg/día durante ≥28 días; ≥20mg/día en mayores de 10kg durante ≥14 días. Metilprednisolona intravenosa, bolo ≥500mg• Anticuerpos monoclonales inmunosupresores (ACMIs)c y otros fármacos biológicos: anti-TNFα infliximab, adalimumab, certolizumab, etanercept y golimumab), antilinfocitos B (rituximab), antilinfocitos T (alemtuzumab), inhibidores de IL-6R (sarilumab, tocilizumab), IL-17A (secukinumab), IL-12/23 (ustekinumab), IL-23 (guselkumab), IL-1 (canakinumab), IL-1R (anakinra), IL-4/13 (dupilumab), IL-5 (mepolizumab) y anti-factor estimulador de linfocitos B (BLyS, belimumab). Inhibidores de la familia de la Janus kinasa (JAK)• Terapias combinadas con independencia de la dosis |
| Inmunodeficiencia de bajo grado |
| • VIH asintomático y T-CD4≥200 células/mm3 en ≥14 años, o T-CD4≥15% en <13 años• Corticoterapia ≥14 días de una dosis diaria inferior a la que ocasiona inmunosupresión de alto nivel, o quienes reciben terapia de corticoides a días alternos• Metotrexato a dosis de ≤0,4mg/kg/semana o <15mg/m2/semana, azatioprina a dosis de ≤3mg/kg/día o 6-mercaptopurina a dosis de ≤1,5mg/kg/día |
En las situaciones asociadas a inmunodeficiencia de alto grado las vacunas atenuadas están contraindicadas.
Corticoterapia: tratamientos de <2 semanas (salvo bolo), las dosis más bajas, el tratamiento sustitutivo a dosis fisiológicas, los tratamientos tópicos, intraarticulares o en aerosol no contraindican la administración de vacunas atenuadas. Tras un tratamiento inmunodepresor de alto grado la administración de vacunas atenuadas debe retrasarse un mes y 3 meses después de un bolo.
ACMIs: aplicar las vacunas antes de iniciar el tratamiento: las inactivadas 2 semanas y las atenuadas 4 semanas (6 semanas para el alemtuzumab). Durante el tratamiento, si es preciso aplicar vacunas inactivadas hay que procurar vacunar unos días antes de la siguiente administración del fármaco, las atenuadas están contraindicadas, aunque en algún caso se pueden considerar en pacientes estables con tratamiento inmunosupresor de mantenimiento (Apartado 5). Tras final del tratamiento, los tiempos recomendados son de 5 veces la semivida plasmática, lo que equivale a esperar 3-6 meses antes de la vacunación tras el tratamiento con anti-TNFα o anti-interleucina, y 12 meses tras ACMIs dirigidos a receptores de linfocitos B.
Esta población presenta mayor riesgo de enfermedades inmunoprevenibles que pueden desestabilizar la patología de base y presentar un curso más grave. Por este motivo, es prioritario optimizar su vacunación4. Durante la inmunosupresión, la respuesta a las vacunas es subóptima, por ello, la vacunación se debe realizar precozmente, preferentemente en el momento del diagnóstico para conseguir la mejor respuesta posible y teniendo en consideración que no se debe posponer el tratamiento necesario. Sin embargo, la desinformación, los temores en relación con la seguridad o el curso de la enfermedad de base, con frecuencia, condicionan la infravacunación o el retraso de la inmunización de estos niños5.
Este documento, fruto de la revisión crítica de información científica relevante obtenida a partir de una revisión no sistemática de la literatura y consensos de expertos, aporta unas directrices para programar un calendario adaptado a cada paciente. Se divide en 6 apartados: a) recomendaciones generales; b) vacunación en pacientes con trasplante de progenitores hematopoyéticos (TPH) y trasplante de órgano sólido (TOS); c) vacunación en niños con errores innatos de la inmunidad (EII); d) vacunación en el paciente oncológico; e) vacunación en pacientes con enfermedades crónicas o sistémicas, y f) vacunación en niños viajeros inmunodeprimidos.
Recomendaciones generales de vacunación en niños y adolescentes inmunodeprimidosSalvo las excepciones que se plantean en cada situación de riesgo, deben recibir todas las vacunas del calendario junto a las recomendadas en el grupo al que pertenecen. En todos los grupos está especialmente indicada la vacunación antigripal anual, antineumocócica y frente al SARS-CoV-2 con la pauta vigente para grupos de riesgo en cada momento.
Las vacunas inactivadas no plantean problemas de seguridad, aunque la respuesta inmune no es óptima y pueden necesitar dosis adicionales de primovacunación y/o aplicar refuerzos.
Las vacunas vivas atenuadas (triple vírica, varicela, rotavirus, gripe atenuada, tifoidea oral, fiebre amarilla, Bacilo de Calmette-Guérin [BCG] y vacuna polio oral [VPO]) están contraindicadas en las situaciones de inmunosupresión de alto grado (tabla 1) por el riesgo de replicación y desarrollo de enfermedad por cepas vacunales. Existen nuevos datos que muestran como pueden ser seguras e inmunogénicas, si los parámetros de inmunidad humoral y celular están dentro de unos rangos determinados, pero son necesarios más estudios que avalen esta recomendación6.
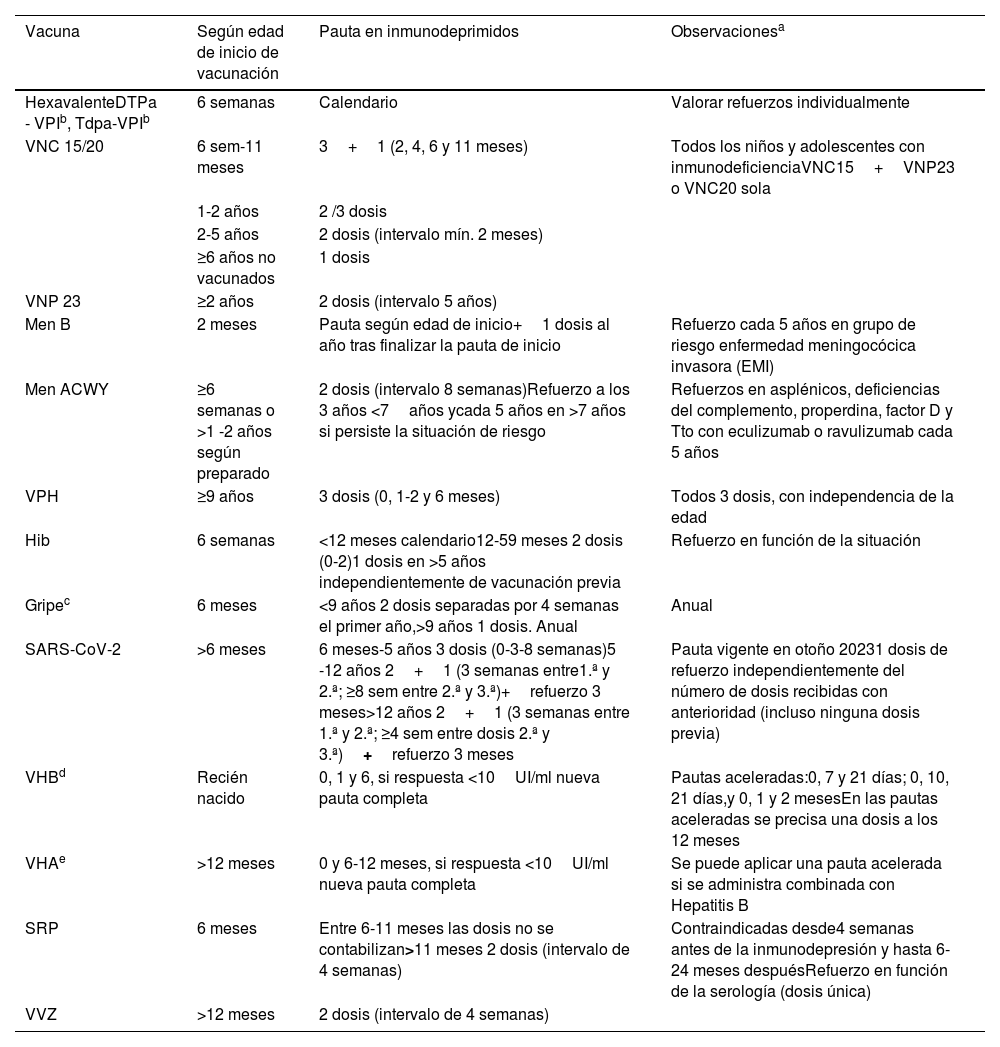
En caso de inmunodepresión programada, es recomendable administrar todas las vacunas indicadas aplicando esquemas acelerados antes de su inicio, las vacunas atenuadas, al menos 4 semanas antes y las inactivadas 2 semanas antes. Tras finalizar el tratamiento, el intervalo recomendado varía ente 3 meses y 2 años en función de la situación y del tipo de vacuna. En la tabla 2 se resumen las recomendaciones generales de vacunación en inmunodeprimidos7.
Recomendaciones generales de vacunación en inmunodeprimidos
| Vacuna | Según edad de inicio de vacunación | Pauta en inmunodeprimidos | Observacionesa |
|---|---|---|---|
| HexavalenteDTPa - VPIb, Tdpa-VPIb | 6 semanas | Calendario | Valorar refuerzos individualmente |
| VNC 15/20 | 6 sem-11 meses | 3+1 (2, 4, 6 y 11 meses) | Todos los niños y adolescentes con inmunodeficienciaVNC15+VNP23 o VNC20 sola |
| 1-2 años | 2 /3 dosis | ||
| 2-5 años | 2 dosis (intervalo mín. 2 meses) | ||
| ≥6 años no vacunados | 1 dosis | ||
| VNP 23 | ≥2 años | 2 dosis (intervalo 5 años) | |
| Men B | 2 meses | Pauta según edad de inicio+1 dosis al año tras finalizar la pauta de inicio | Refuerzo cada 5 años en grupo de riesgo enfermedad meningocócica invasora (EMI) |
| Men ACWY | ≥6 semanas o >1 -2 años según preparado | 2 dosis (intervalo 8 semanas)Refuerzo a los 3 años <7años ycada 5 años en >7 años si persiste la situación de riesgo | Refuerzos en asplénicos, deficiencias del complemento, properdina, factor D y Tto con eculizumab o ravulizumab cada 5 años |
| VPH | ≥9 años | 3 dosis (0, 1-2 y 6 meses) | Todos 3 dosis, con independencia de la edad |
| Hib | 6 semanas | <12 meses calendario12-59 meses 2 dosis (0-2)1 dosis en >5 años independientemente de vacunación previa | Refuerzo en función de la situación |
| Gripec | 6 meses | <9 años 2 dosis separadas por 4 semanas el primer año,>9 años 1 dosis. Anual | Anual |
| SARS-CoV-2 | >6 meses | 6 meses-5 años 3 dosis (0-3-8 semanas)5 -12 años 2+1 (3 semanas entre1.ª y 2.ª; ≥8 sem entre 2.ª y 3.ª)+refuerzo 3 meses>12 años 2+1 (3 semanas entre 1.ª y 2.ª; ≥4 sem entre dosis 2.ª y 3.ª)+refuerzo 3 meses | Pauta vigente en otoño 20231 dosis de refuerzo independientemente del número de dosis recibidas con anterioridad (incluso ninguna dosis previa) |
| VHBd | Recién nacido | 0, 1 y 6, si respuesta <10UI/ml nueva pauta completa | Pautas aceleradas:0, 7 y 21 días; 0, 10, 21 días,y 0, 1 y 2 mesesEn las pautas aceleradas se precisa una dosis a los 12 meses |
| VHAe | >12 meses | 0 y 6-12 meses, si respuesta <10UI/ml nueva pauta completa | Se puede aplicar una pauta acelerada si se administra combinada con Hepatitis B |
| SRP | 6 meses | Entre 6-11 meses las dosis no se contabilizan>11 meses 2 dosis (intervalo de 4 semanas) | Contraindicadas desde4 semanas antes de la inmunodepresión y hasta 6-24 meses despuésRefuerzo en función de la serología (dosis única) |
| VVZ | >12 meses | 2 dosis (intervalo de 4 semanas) |
DTPa: vacuna difteria-tétanos-tosferina de carga estándar; Hib: vacuna Haemophilus influenzae tipo b; Men B: vacuna meningococo B; MenACWY: vacuna meningococo ACWY; SRP: triple vírica (sarampión-rubeola-parotiditis); Tdpa: vacuna difteria-tétanos-tosferina de baja carga; VHA: virus hepatitis A; VHB: virus hepatitis B; VNC: vacuna neumocócica conjugada; VNC15: vacuna neumocócica conjugada 15-valente; VNC20: vacuna neumocócica conjugada 20-valente; VNP23: vacuna neumocócica polisacárida 23-valente; VPH: vacuna papiloma humano; VPI: vacuna polio inactivada; VVZ: vacuna varicela-zóster.
Las vacunas inactivadas se deben aplicar, al menos, 2 semanas antes del comienzo de la inmunodepresión y entre 3-6 meses tras el fin. Las vacunas atenuadas se deben aplicar, al menos, 4 semanas antes del comienzo de la inmunodepresión y entre 3-24 meses tras el fin y están contraindicadas durante la inmunodepresión. Aparte de las dosis adicionales recomendadas en inmunodeprimidos, los refuerzos necesarios varían en función del grupo de riesgo.
DTPa: de alta carga, algunos autores la recomiendan con independencia de la edad en situaciones de inmunodepresión, como el TPH. Las vacunas hexavalentes están autorizadas en calendarios de rescate tras inmunodepresión con independencia de la edad.
Gripe: valorar dosis adicional en situaciones en las que la cepa circulante sea muy diferente a las de las temporadas anteriores, independientemente de la situación vacunal previa. La vacuna antigripal intranasal con virus atenuados está contraindicada.
VHB: en caso de no respondedores (anti-HBs ≤10mUI/ml), revacunar con 3 dosis (pauta 0, 1 y 6 meses). En >15 años valorar utilizar la vacuna adyuvada o de alta carga. Si tras revacunar persiste con anti-HBs ≤10mUI/ml se considera no respondedor, y se debe administrar inmunoglobulina específica en caso de exposición.
VHA: revacunar con 2 dosis, si IgG<10mUI/ml después de la serie de vacunación primaria frente al VHA. La serología debe realizarse 1-2 meses después y si no es adecuada (<10mUI/ml), no se recomienda la vacunación adicional y se debe aconsejar sobre cómo prevenir la infección, incluida la necesidad de inmunoglobulina polivalente después de una exposición.
Las personas vacunadas sin respetar los intervalos recomendados, o durante el propio tratamiento, deben considerarse como posibles no respondedoras y evaluar si precisan un refuerzo; si se dispone de pruebas serológicas con correlato de protección, se recomienda su realización un mes tras la última dosis para guiar la revacunación y considerar la inmunoprofilaxis pasiva y/o quimioprofilaxis ante una exposición de riesgo.
Los convivientes y cuidadores deben tener actualizado su calendario de vacunación, haciendo especial énfasis en la vacunación frente a triple vírica, varicela, gripe y covid. Están contraindicadas las vacunas orales frente a la polio y Salmonella typhi Ty21. La vacuna antigripal intranasal atenuada se puede utilizar en los contactos, salvo en el caso de TPH en los 2 meses previos, enfermedad injerto contra huésped (EICH) o inmunodeficiencia combinada grave (IDCG).
Como precaución, tras la vacunación de un conviviente frente al rotavirus se debe evitar cualquier contacto con las heces del lactante en las 4 semanas siguientes a la vacunación; y si tras la vacunación frente a la varicela aparece un exantema, se debe evitar el contacto con las lesiones.
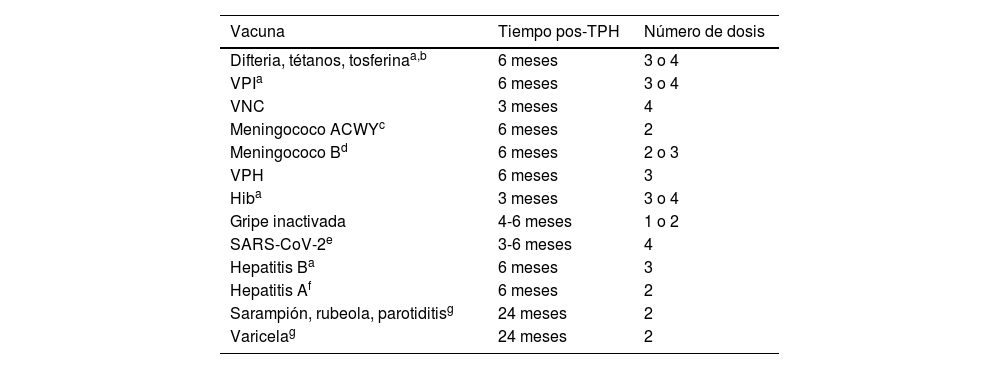
Vacunación en niños con trasplante de progenitores hematopoyéticos y trasplante de órgano sólidoTrasplante hematopoyético (tabla 3)8–12Los niños que reciben un TPH sufren una inmunosupresión que depende de la enfermedad de base y del tipo de trasplante, siendo más acusada y duradera en el alotrasplante. Las alteraciones inmunitarias disminuyen la respuesta a vacunas, por lo que es necesario esperar un tiempo tras el TPH para adaptar el calendario, que debe incluir una vacunación completa.
Tipo de vacunas, tiempo para iniciar la vacunación tras el TPH y número de dosis necesarias
| Vacuna | Tiempo pos-TPH | Número de dosis |
|---|---|---|
| Difteria, tétanos, tosferinaa,b | 6 meses | 3 o 4 |
| VPIa | 6 meses | 3 o 4 |
| VNC | 3 meses | 4 |
| Meningococo ACWYc | 6 meses | 2 |
| Meningococo Bd | 6 meses | 2 o 3 |
| VPH | 6 meses | 3 |
| Hiba | 3 meses | 3 o 4 |
| Gripe inactivada | 4-6 meses | 1 o 2 |
| SARS-CoV-2e | 3-6 meses | 4 |
| Hepatitis Ba | 6 meses | 3 |
| Hepatitis Af | 6 meses | 2 |
| Sarampión, rubeola, parotiditisg | 24 meses | 2 |
| Varicelag | 24 meses | 2 |
Hib: vacuna Haemophilus influenzae tipo b; VNC: vacuna neumocócica conjugada; VPH: vacuna papiloma humano; VPI: vacuna polio inactivada.
La vacunación frente al neumococo debe iniciarse a partir de los 3 meses del TPH con vacunas conjugadas, aplicando 3 dosis separadas por un intervalo mínimo de un mes y una cuarta dosis 6 meses tras la última dosis. Posteriormente, a partir de 6 meses del TPH se aplicarán el resto de vacunas conjugadas, incluidas vacuna difteria-tétanos-tosferina de baja carga (Tdpa), vacuna polio inactivada (VPI), vacuna hepatitis b (VHB), vacuna Haemophilus influenzae tipo b (Hib), meningococo B/ACWY y antigripal. La vacuna antigripal, durante la epidemia, puede administrarse a los 4 meses del TPH y si el paciente tiene enfermedad injerto contra huésped (EICH) se puede administrar un refuerzo a las 4-8 semanas. Se recomienda vacuna virus del papiloma humano nonavalente (VPH9) (3 dosis) a partir de los 9 años.
Las vacunas triple vírica y varicela pueden administrarse a partir de los 24 meses (2 dosis separadas por un mes) siempre que el niño no tenga EICH, no reciba tratamiento inmunosupresor, no haya recibido inmunoglobulina sustitutiva en los últimos meses y los linfocitos T CD4 sean superiores a 200/mm3.
Trasplante de órgano sólido8,9,11,12Es primordial intentar llegar al TOS con el calendario vacunal lo más optimizado posible, incluso utilizando calendario acelerado. Tras el TOS, el niño estará inmunodeprimido y la respuesta a las vacunas inactivadas no será óptima y las atenuadas estarán contraindicadas.
La vacunación pre-TOS debe finalizar, al menos, 4 semanas antes en el caso de vacunas vivas y 2 semanas para las inactivadas. La vacunación podrá reanudarse 6 meses tras el trasplante.
PretrasplanteLas vacunas triple vírica y varicela pueden adelantarse y administrarse desde los 6 meses de edad. Las vacunas frente a hepatitis B y A están indicadas, y se recomienda determinar la inmunidad posvacunación (tabla 2, notas c y d). Es primordial asegurar una correcta inmunización frente al neumococo. Está indicada la vacunación frente al VPH9 con 3 dosis independientemente de la edad.
Postrasplante (tabla 4)Las vacunas de microorganismos vivos (triple vírica, varicela, rotavirus, fiebre amarilla, fiebre tifoidea oral) están contraindicadas. En el caso de las vacunas inactivadas, aunque el calendario esté completo, se recomienda refuerzo frente a VPI, DTPa/Tdpa, neumococo y SARS-CoV-2. La vacuna antigripal se recomienda a partir del mes postrasplante. Vacuna antineumocócica con la mayor valencia disponible. Se recomienda realizar serologías de VHB y virus hepatitis A (VHA) posvacunales tras la vacunación pos-TOS (tabla 2), y cada 2 años, y administrar una dosis de refuerzo en caso de que las serologías sean negativas.
Tipo de vacunas, número de dosis necesarias e intervalos en función de vacunación completa o incompleta pretrasplante de órgano sólido
| Vacunación pre-TOS | ||||
|---|---|---|---|---|
| Vacunación completa pre-TOSa | Vacunación incompleta pre-TOS | No vacunación pre-TOS | ||
| Dosis recibidas | Dosis a recibir | Dosis a recibir | Dosis a recibir | |
| Hepatitis B | 3 (0-1-6 meses) | En función de serología:- si anti-HBs negativos pos-TOS pauta completa- si anti-HBs ≥10UI/L no precisa | Completar pauta de vacunación | 3 dosis (0-1-6 meses) |
| Hepatitis A | 2 (0-6 meses) | En función de serología:- si IgG VHA positiva, no precisa- si IgG VHA negativa, pauta completa | 2 dosis (0-6 meses) | |
| VPI | 4 | 1 | Completar pauta de vacunación | <24 meses: 3 dosis (0-2-8 meses) y continuar pauta vacunal según calendario24 meses-6 años: 4 dosis (0-2-8-14 meses) y continuar pauta vacunal según calendario7-18 años: 3 dosis (0-2-8 meses) |
| DTPa/Tdpa (según edad) | ≥4 | 1 (cada 10 años administrar 1 dosis de Tdpa) | Completar pauta de vacunación | <24 meses: 3 dosis (0-2-8 meses)2-5 años: 3 dosis (0-2-8 meses)6-11 años: 4 dosis (0-2-8-14 meses)12-18 años: 5 dosis Tdpa (0-2-8-14-20 meses) |
| Hib | 3 | 0 | Completar pauta de vacunación | 3 dosis si es menor de 5 años (0-2-8 meses) |
| Meningococo Bb | 2/3 | 0 | Completar pauta de vacunación | <2 años: 3 dosis (0-2-6)2-18 años: 2 dosis (0-2 meses) |
| Meningococo Cc | 3 | 0 | Si tiene 1 dosis previa de MenC (pre-TOS), dos dosis Men ACWY | Se vacuna con MenACWY, 2 dosis (0-2 meses) |
| Meningococo ACWYc | 2 | 0 | 2 dosis (0-2 meses) | |
| Neumococo conjugada 7V | 4 | 1 dosis de VNC15+2 dosis VPN23 (a los 2 meses de la última VNC15, a partir de los 2 años de edad, y a los 5 años de la primera VPN23) o 1 dosis de VNC20 | Completar la pauta con VNC15 y posteriormente, 2 dosis VPN23 (a los 2 meses de la última VNC13, a partir de los 2 años de edad, y a los 5 años de la primera VPN23) o completar la pauta con VNC20 | 0 |
| Neumococo conjugada 13V (Prevenar13, VNC13) o 15V (VNC15) | 3 | <24 meses: 3 dosis VNC15/20 (0-2-4 meses)24 meses-6 años: 2 dosis VNC15/20 (0-2 meses)7-18 años: 1 dosis VNC15+2 dosis VPN23: a los 2 meses de la última VNC15 y 5 años después o bien 1 dosis de VNC20 | ||
| Neumococo polisacárido 23V (VPN23) | 0 | |||
| VPHd | 2/3 (según la vacuna administrada y la edad de inicio de la vacunación) | 1 (si previamente ha recibido 2 dosis) | Completar pauta de vacunación | 3 dosis (0-2-6 meses) |
| Gripe epidémica | Anual | Anual | Anual | Anual |
| Triple vírica | 2 | Contraindicada | Contraindicada | Contraindicada |
| Varicela | 2 | Contraindicada | Contraindicada | Contraindicada |
DTPa: vacuna difteria-tétanos-tosferina carga estándar; Hib: vacuna Haemophilus influenzae tipo b; MenACWY: meningococo ACWY; Tdpa: vacuna difteria-tétanos-tosferina baja carga; VHA: virus hepatitis A; VNC: vacuna neumocócica conjugada; VNC20: vacuna neumocócica conjugada 20-valente; VPH: vacuna papiloma humano; VPI: vacuna polio inactivada; VPN23: vacuna neumocócica polisacárida 23-valente; 7V: 7-valente; 13V: 13-valente; 15V: 15-valente.
Pauta vacunal que debe haber recibido según el calendario de primovacunación infantil actualmente recomendado.
La vacunación frente al meningococo B se considera completa con pauta de 3 dosis si se ha iniciado antes de los 24 meses, siempre que la última dosis se haya administrado después de los 12 meses, y con 2 dosis si se ha iniciado después de los 24 meses.
Los errores innatos de la inmunidad (EII) son un grupo heterogéneo de enfermedades asociadas a un número creciente de mutaciones genéticas13,14 con riesgo variable de infección, por lo que la vacunación debe individualizarse. A efectos prácticos, se clasifican en 3 grupos: defectos de la inmunidad adaptativa, trastornos de la inmunidad innata y trastornos inmunitarios con fenotipo característicos o inmunodeficiencias sindrómicas15.
Los EII tienen un riesgo aumentado de infecciones inmunoprevenibles y una respuesta inmune de menor intensidad y duración. Aun así, hay evidencia del efecto protector de las vacunas reduciendo complicaciones y mortalidad15 y por ello precisan habitualmente refuerzos.
Las vacunas atenuadas (víricas y bacterianas) conllevan riesgo de diseminación en pacientes con defectos de inmunidad celular15,16, y aunque ante una sospecha de EII no se debe retrasar la vacunación, las vacunas vivas están contraindicadas hasta conocer el grado de inmunosupresión16.
Las vacunas inactivadas o de subunidades son seguras y pueden ser efectivas. En EII que requieran terapia sustitutiva con inmunoglobulinas no se deben administrar vacunas de virus atenuados por la interferencia en los 3-11 meses siguientes.
Con estas consideraciones los niños con EII, en general, requieren un calendario ampliado17,18 especialmente frente a bacterias encapsuladas: neumococo, meningococo (B/ACWY) y Hib, a partir de los 6 meses precisan vacunación anual antigripal con vacunas inactivadas tetravalentes y vacunación frente a covid-19 según las recomendaciones vigentes18. Además, es fundamental fomentar vacunación de convivientes y en la población general19.
En la tabla 5 se expone una aproximación al esquema de vacunación de los EII más frecuentes.
Vacunación en errores innatos de la inmunidad más frecuentes
| Error innato de la inmunidad | Vacunas contraindicadas o que no se deberían administrar | Vacunas indicadas | Observaciones |
|---|---|---|---|
| Inmunodeficiencias celulares | Todas las vacunas vivas atenuadas | Deben recibir vacunación ampliada frente a bacterias encapsuladas (neumococo, meningococo ([B/ACWY] y Hib), así como frente a SARS-COV-2 y antigripal inactivada anual | La mayoría de guías recomiendan todas las vacunas inactivadas del calendario, mientras que otras no lo recomiendan (con la excepción de vacuna antigripal) si el paciente recibe tratamiento con gammaglobulinas |
| Deficiencias mayores de anticuerpos (deficiencias puras de células B): agammaglobulinemia ligada al X, inmunodeficiencia común variable, síndrome de PI3K-delta activada (APDS) | Todas las vacunas vivas | Deben recibir vacunación ampliada frente a bacterias encapsuladas (meningococo y neumococoa), así como frente a SARS-COV-2 y antigripal inactivada anualOtras vacunas inactivadas del calendario | La vacunación frente al rotavirus puede administrarseLa vacuna triple vírica y la de la varicela no serían necesarias si el paciente recibe inmunoglobulinas, ya que éstas aportan inmunidad pasiva frente a estas infecciones y pueden interferir la respuesta vacunal |
| Deficiencias menores de anticuerpos: déficit de IgA, déficit de subclases de IgG | Vacuna antipoliomielítica oral | Todas las vacunas del calendario, incluidas triple vírica y varicelaVacunación antigripal anual | Si el paciente tiene síntomas respiratorios frecuentes, recomendación de vacuna antineumocócica conjugada (15 o 20): |
| Inmunodeficiencias de células T combinadas o sindrómicas: síndrome de Di George, ataxia-telangiectasia, síndrome de Wiskott-Aldrich, síndrome de HiperIgE, síndrome de hiperIgM, candidiasis mucocutánea crónica | Deben recibir vacunación ampliada frente a bacterias encapsuladas (neumococo, meningococo ([B/ACWY] y Hib), así como frente a SARS-COV-2 y antigripal inactivada anual | Pueden recibir vacunas de virus vivos atenuados si tienen CD4 ≥500céls/mm3 (>1000 si 1-6 años; 1500 si <1 año) y CD8 ≥200céls/mm3 | |
| Deficiencias del complemento: deficiencias de factores tardíos del complemento, de properdina o de factor D | No hay vacunas contraindicadas | Todas las vacunas del calendario, incluidas triple vírica y varicelaDeben recibir vacunación ampliada frente a bacterias encapsuladas: (neumococo, meningococo (B/ACWY-considerar revacunar cada 3-5 años- y Hib), así como frente a SARS-COV-2 y antigripal anual inactivada | Se recomienda vacunación con una dosis de Hib en mayores de 5 años no inmunizadosConsiderar otras medidas como profilaxis antibiótica |
| Deficiencias del sistema fagocítico: enfermedad granulomatosa crónica –EGC, defectos de moléculas de adhesión –LAD, S. de Chediak-Higashi, neutropenia congénita | Vacunas bacterianas vivas (BCG y la vacuna oral atenuada frente a la fiebre tifoidea). Las vacunas de virus vivos están contraindicadas en LAD y S. de Chediak-Higashi, pero no en la EGC ni en la neutropenia congénita | Todas las vacunas del calendario, con la excepción de la triple vírica y la vacuna frente a la varicela en LAD y S. de Chediak-Higashi, donde están contraindicadas. La vacunación antigripal es prioritaria, ya que la gripe predispone a infecciones por S. aureus | La vacunación antineumocócica debe hacerse con VCN15+VNP23 o VNC20 exclusivamente |
| Defectos de inmunidad innata: (alteraciones del eje IL-12/interferón gamma) | Todas las vacunas vivas atenuadas, tanto bacterianas (BCG y vacuna oral atenuada de F. tifoidea) como las víricas (triple vírica y varicela) | Todas las vacunas del calendario, excepto las vacunas vivas atenuadas | La vacunación antineumocócica debe hacerse con VCN15+VNP23 o VNC20 exclusivamente |
| Defectos de inmunidad innata: (deficiencia de IRAK4 y MyD88) | Ninguna | Todas las vacunas. Deben recibir vacunación antineumocócica con VCN15+VNP23 o VNC20 exclusivamente, así como vacunación frente a SARS-COV-2 y antigripal inactivada anual |
Hib: Haemophilus influenzae tipo b; VNC15: vacuna neumocócica conjugada 15-valente; VNC20: vacuna neumocócica conjugada 20-valente; VPN23: vacuna neumocócica polisacárida 23-valente.
Pauta de vacunación ampliada frente a bacterias encapsuladas: H. influenzae tipo b, neumococo y frente a todos los serogrupos de meningococo (B/ACWY). Cuando se comience la inmunización en los primeros meses de vida se requiere vacunación antineumocócica conjugada siempre con pautas 3+1, complementando con VPN23 en mayores de 2 años, si se emplea VNC15, y con un intervalo mínimo de 8 semanas desde la última dosis o bien administrando VNC2017.
La inmunosupresión de los niños oncológicos se extiende hasta meses después de finalizado el tratamiento, y repercute sobre la inmunogenicidad de las vacunas administradas antes, durante, o poco después de finalizar la quimioterapia8,20,21. Además, en algunas situaciones se produce asplenia anatómica o funcional (radioterapia en abdomen, EICH). Los datos sobre vacunación en los nuevos tratamientos de inmunoterapia son insuficientes20,21.
Principios generales de vacunación en los niños que reciben quimioterapiaAntes de la quimioterapiaSe recomienda si es posible actualizar el calendario vacunal antes de iniciar el tratamiento, con un intervalo de 2 semanas para vacunas inactivadas y 4 para atenuadas8.
Durante la quimioterapiaLas vacunas del calendario vacunal no se deben administrar durante la quimioterapia intensiva. Las vacunas inactivadas tienen escasa inmunogenicidad (deberían considerarse no válidas), y las atenuadas están contraindicadas.
En los niños con leucemia linfoblástica en tratamiento de mantenimiento se recomienda vacunación antigripal anual en mayores de 6 meses. Las guías de la European Conference on Infections in Leukaemia recomiendan también una dosis de refuerzo de VNC21, aunque la respuesta inmune puede ser subóptima y es necesario administrar otra dosis una vez finalizado el tratamiento22,23.
Tras la quimioterapiaNo es necesario volver a administrar las vacunas previamente recibidas. En los niños con vacunación completa, se recomienda administrar una dosis de recuerdo de las vacunas recibidas, y posteriormente continuar el calendario según la edad8,21. En el caso de que el calendario de vacunación fuera incompleto previo a la administración de la quimioterapia, se procederá a adecuar su calendario vacunal en primer lugar. Para ello, el número de dosis de cada vacuna, así como la edad mínima para administración de cada vacuna y sus intervalos de separación mínimos se pueden consultar en las tablas del Comité Asesor de Vacunas de la Asociación Española de Pediatría (CAV-AEP)24.
Las vacunas inactivadas se administran entre los 3 y los 6 meses (preferentemente 6) después de finalizar la quimioterapia, mientras que la administración de vacunas atenuadas se demora hasta pasados los 6-12 meses (preferentemente 12). En regímenes terapéuticos que incluyen anticuerpos anti-B se recomienda esperar 6-12 meses para administrar cualquier vacuna8,21. Datos recientes muestran que los niños con leucemia linfoblástica podrían recibir la vacuna conjugada frente al neumococo justo al finalizar el tratamiento, ya que la respuesta es similar a los que se vacunan a los 6 meses22. Se podría valorar adelantar esta vacuna especialmente en niños que no se han vacunado durante la quimioterapia de mantenimiento.
Recomendaciones específicas de vacunación en los pacientes oncológicos- -
Neumococo: pauta secuencial VNC15+VNP23, o bien VNC20 exclusivamente8.
- -
Gripe: vacuna inactivada anual, al menos, en las 3 temporadas siguientes al fin de la quimioterapia8.
- -
SARS-CoV-2: pauta según edad y tipo de vacuna18.
- -
VPH9: recomendada a partir de los 9 años18.
- -
No se recomienda el uso de vacunas atenuadas en pacientes tratados con inhibidores de la tirosina cinasa o ruxolitinib19.
Las primeras recomendaciones EULAR (European Alliance of Associations for Rheumatology) se desarrollaron en 2011 y muchas de ellas se extrapolaron de adultos dada la baja calidad de los estudios publicados en niños. Desde entonces, la evidencia sobre seguridad e inmunogenicidad en vacunas se ha duplicado.
Recomendaciones generales- -
Si es posible, las vacunas deben ser administradas 2-4 semanas antes de iniciar el tratamiento inmunosupresor (especialmente si el tratamiento reduce las células B), pero nunca un tratamiento necesario debe ser pospuesto. No obstante, el intervalo puede variar según el tipo de fármaco (ver tabla 14.3 del CAV-AEP https://vacunasaep.org/documentos/manual/cap-14#7).
- -
Es aconsejable realizar la vacunación durante la fase inactiva/remisión de la enfermedad, teniendo en cuenta que no debe retrasarse por miedo a desencadenar un brote ya que no se ha demostrado este hecho.
- -
Todos los pacientes inmunodeprimidos deben adherirse al calendario vacunal y las normas de vacunación de los viajeros, excepto para vacunas vivas atenuadas.
- -
Las vacunas inactivadas pueden ser administradas en pacientes que reciben corticoides o tratamiento con FAME (fármacos antirreumáticos modificadores de la enfermedad).
- -
Las vacunas de virus vivos atenuados están contraindicadas en pacientes con tratamiento inmunosupresor de alto grado (tabla 1); como excepción, el refuerzo de triple vírica (sarampión-rubeola-parotiditis) (TV) y la vacunación frente a varicela se pueden valorar individualmente en condiciones específicas.
- -
Vacunación antitetánica según recomendaciones generales y en caso de indicación de administrar toxoide tetánico, la inmunización pasiva se recomienda en pacientes que han recibido en los últimos 6 meses tratamiento que reduce las células B.
- -
La vacuna VPH9 debe ser considerada en pacientes con LES o enfermedad inflamatoria intestinal no vacunados (3 dosis si tratamiento inmunosupresor).
- -
El refuerzo de TV podría ser considerado individualmente y tras valoración por parte de su médico especialista en pacientes tratados con dosis inmunomoduladoras de MTX (grado de recomendación A) o dosis bajas de corticoides, anti-TNFα, anti-IL-1 y anti-IL-6 (grado de recomendación C).
- -
La vacuna frente a varicela podría ser considerada individualmente y tras valoración por parte de su médico especialista en pacientes naive que reciben dosis inmunomoduladoras de MTX (grado de recomendación A) o dosis bajas de corticoides, anti-TNFα, anti IL-1 y anti-IL-6 (grado de recomendación D).
- -
La vacunación frente a fiebre amarilla debe ser evitada en todos los pacientes que reciben tratamiento inmunosupresor (grado de recomendación D).
- -
Es recomendable la vacunación frente a hepatitis A en los pacientes que reciben algún inmunosupresor hepatotóxico (MTX o tocilizumab).
Es primordial la vacunación frente a hepatitis B, con monitorización de la respuesta vacunal. Además, está indicada la vacunación frente a la hepatitis A con pauta estándar, o alternativamente con la vacuna combinada (A+B) si se precisa un refuerzo frente a VHB. Sin inmunosupresión se recomienda la vacunación frente a sarampión y varicela lo antes posible tras el diagnóstico.
Enfermedades cardiacas y respiratorias25,26Se incluyen niños con cardiopatías congénitas (cianosantes, que asocian insuficiencia cardiaca o alteración hemodinámica), hipertensión pulmonar, displasia broncopulmonar, fibrosis quística, bronquiectasias y el asma moderado-grave. La vacunación frente a varicela se recomienda según pauta de calendario, teniendo en cuenta que, en aquellos tratados con salicilatos, es aconsejable suspender el tratamiento durante 6 semanas tras administrar la vacuna (si no es posible, debe vacunarse ya que no se ha descrito S. de Reye con virus vacunal).
Enfermedades neurológicas25,26En niños con epilepsia no se contraindica ninguna vacuna. De hecho, el empleo de vacuna antitosferina acelular ha disminuido significativamente la incidencia de convulsiones febriles asociadas a DTPa. El empleo de fármacos hepatotóxicos como el ácido valproico conlleva la recomendación de vacunación frente a hepatitis A.
Sin embargo, en presencia de una enfermedad neurológica evolutiva, inestable o no filiada, es recomendable retrasar las vacunas que pudieran desestabilizar la enfermedad (tosferina). En caso de enfermedad neurológica inflamatoria autoinmune en la que haya sospecha razonada de relación con alguna vacuna, se debería prescindir de administrar nuevas dosis.
Enfermedades genéticas (S. Down)25,26En los niños con S. de Down se recomienda la vacunación antigripal anual, la vacunación antineumocócica ([VNC15+VNP23] o bien VNC20 exclusivamente); y frente a hepatitis A.
En el resto de enfermedades genéticas, sólo se harán recomendaciones específicas en caso de alteraciones inmunitarias crónicas asociadas.
Hemoglobinopatías25,26En hemoglobinopatías con hipoesplenia funcional, es imprescindible la vacunación antineumocócica (VNC15+VNP23 o VNC20), frente a Hib, meningococo (Men ACWY+refuerzo a los 5 años y Men B con refuerzo 1 año tras finalizar la pauta y posteriormente cada 5 años), así como hepatitis (A y B) dado el riesgo de hepatopatía. Hay que tener en cuenta los intervalos recomendados (6-7 meses) entre las transfusiones de hemoderivados y la administración de vacunas atenuadas. En nuestro país, siempre que no exista un brote de sarampión, rubeola o parotiditis, no está indicado modificar el calendario de vacunación si el paciente va a recibir hidroxiurea en el primer año de vida.
Los pacientes con betatalasemia minor o rasgo falciforme deben recibir las mismas vacunaciones que la población general.
Implante coclear25,26Dado el riesgo de padecer meningitis y otitis media, está especialmente recomendada la vacunación antineumocócica (VNC15+VNP23 o VNC20), así como Hib y antigripal anual.
En la tabla 6 se expone una aproximación al esquema de vacunación de las enfermedades crónicas.
Vacunas especialmente recomendadas en enfermedades crónicas
| Vacuna | Enfermedades cardiacas y respiratoriasa | Enfermedad renal | Hepatopatía | Enfermedades neurológicas |
|---|---|---|---|---|
| Tdpa | ||||
| Neumococob | ||||
| VVZ | ||||
| VHBc | ||||
| VHAd | ||||
| Influenza | ||||
| SARS-CoV-2 |
Tdpa: difteria-tétanos-tosferina carga estándar; VHA: vacuna frente a virus hepatitis A; VHB: vacuna frente a virus hepatitis B; VPH: vacuna frente a virus del papiloma humano; VVZ: vacuna varicela zóster.
Se incluyen niños con cardiopatías congénitas cianosantes, cardiopatías que cursan con insuficiencia cardiaca o alteración hemodinámica, hipertensión pulmonar, displasia broncopulmonar, fibrosis quística, bronquiectasias y el asma con alto riesgo de exacerbaciones.
Vacuna conjugada VNC20 o VNC15 seguida de una dosis de VPN23 y un recuerdo a los 5 años en niños >2 años de alto riesgo, como asplenia, implante coclear, pérdida de líquido cefalorraquídeo, cardiopatía, diabetes, hepatopatía, enfermedad pulmonar crónica y pacientes con tratamiento inmunosupresor.
Antes de iniciar el viaje, el niño inmunodeprimido deberá tener actualizado su calendario vacunal; siendo un buen momento para administrar, incluso adelantar, dosis pendientes, si su situación inmunitaria lo permite32–39. El consejo individualizado debe hacerse con suficiente antelación para que las vacunas administradas sean efectivas. Por ello, se recomienda que acuda a la consulta entre 4 y 6 semanas antes de iniciar el viaje. Y si puede evitarse, el niño menor de 2 años no debería viajar.
Vacunas específicas del viajero32–39Vacunas sistemáticas o universalesRecomendadas en el calendario oficial, para todos los niños de su edad. Si su calendario de vacunación no está completo, se administrarán antes del viaje las dosis que falten. Si el niño fuese a viajar a un país donde es endémica una enfermedad de la que aún no ha sido vacunado, como sarampión o varicela, se adelantará la vacuna, siempre que sea posible.
Vacunas específicas del viajero (tabla 7)- •
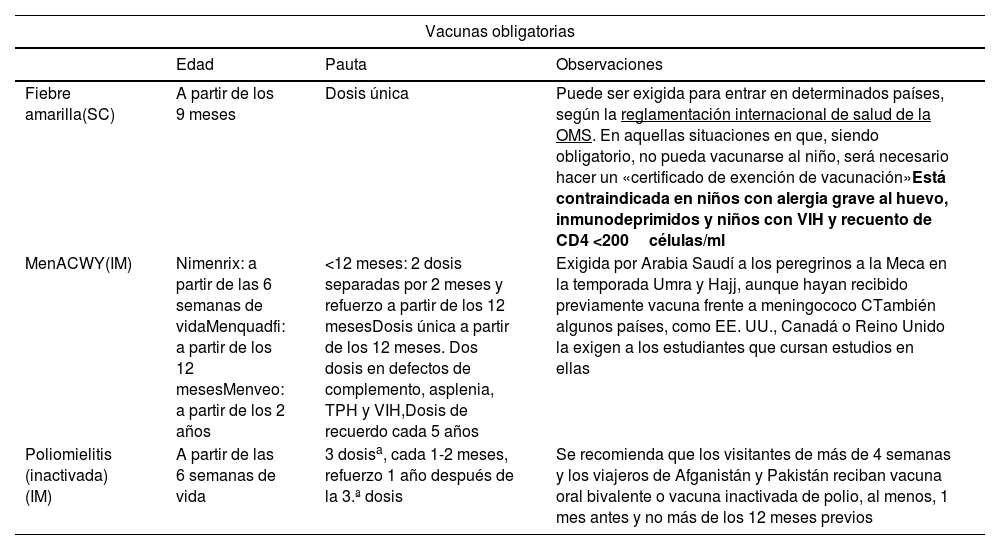
Obligatorias: dependen del país a visitar, tipo de viaje y edad. Son aquellas exigidas por las autoridades para entrar en un país: fiebre amarilla, antimeningocócicas y antipoliomielítica. Las autoridades de los países con requerimientos específicos solicitarán a los viajeros un Certificado Internacional de Vacunación donde figuren las vacunas correctamente registradas.
Tabla 7.Vacunas específicas del viajero: obligatorias y recomendadas según el viaje
Vacunas obligatorias Edad Pauta Observaciones Fiebre amarilla(SC) A partir de los 9 meses Dosis única Puede ser exigida para entrar en determinados países, según la reglamentación internacional de salud de la OMS. En aquellas situaciones en que, siendo obligatorio, no pueda vacunarse al niño, será necesario hacer un «certificado de exención de vacunación»Está contraindicada en niños con alergia grave al huevo, inmunodeprimidos y niños con VIH y recuento de CD4 <200células/ml MenACWY(IM) Nimenrix: a partir de las 6 semanas de vidaMenquadfi: a partir de los 12 mesesMenveo: a partir de los 2 años <12 meses: 2 dosis separadas por 2 meses y refuerzo a partir de los 12 mesesDosis única a partir de los 12 meses. Dos dosis en defectos de complemento, asplenia, TPH y VIH,Dosis de recuerdo cada 5 años Exigida por Arabia Saudí a los peregrinos a la Meca en la temporada Umra y Hajj, aunque hayan recibido previamente vacuna frente a meningococo CTambién algunos países, como EE. UU., Canadá o Reino Unido la exigen a los estudiantes que cursan estudios en ellas Poliomielitis (inactivada)(IM) A partir de las 6 semanas de vida 3 dosisa, cada 1-2 meses, refuerzo 1 año después de la 3.ª dosis Se recomienda que los visitantes de más de 4 semanas y los viajeros de Afganistán y Pakistán reciban vacuna oral bivalente o vacuna inactivada de polio, al menos, 1 mes antes y no más de los 12 meses previos Vacunas recomendadas Cólera(VO) A partir de los 2 años Inactivada. 2-3 dosis2-6 años: 3 dosis. Recuerdo a los 6 meses>6 años: 2 dosis. Recuerdo a los 2 añosAtenuada. 1 dosis2-6 años: 1 dosis de 50ml>6 años: 1 dosis de 100ml Se indica, de forma excepcional, en los viajeros a zonas epidémicas o de elevada endemicidad como son: Benín, Burundi, Camerún, República Democrática del Congo, Etiopía, Kenia, Malawi, Mozambique, Nigeria, Somalia, Sudán, Uganda, Bangladesh, India, Yemen, Haití y Filipinas Encefalitis centroeuropea(IM) A partir de los 12 meses 3 dosis (0, 1-3 meses y 6-15 meses). Recuerdo cada 5 añosPauta acelerada: 0, 7, 21 días, o bien 0, 14 díasRecuerdo 12-18 meses Viajeros a zonas de riesgo con estancias superiores a 3-4 semanas en áreas boscosas de Rusia y del centro y noreste de Europa (especialmente Lituania, República Checa, Alemania y Suecia) Encefalitis japonesa (IM) A partir de los 2 meses de edad 2 dosis en los días 0 y 28 Viajeros que van a pasar mucho tiempo al aire libre (campistas, senderistas) en zonas rurales con transmisión endémica, durante la estación de las lluvias, principalmente en Japón, el Sudeste Asiático y el Oeste del Pacífico Fiebre tifoideaA) IMB) VO A) A partir de los 2 años de edadB) A partir de los 6 años (en ficha técnica 3 años) A) Dosis única. Recuerdo cada 2-3 añosB) 3 dosis. 3 cápsulas, tomadas en días alternos, en ayunasRevacunar cada 1-3 años si persiste riesgo Viaje a zonas del norte y oeste de África, sur de Asia, Indonesia y Perú Hepatitis A(IM) A partir de 12 mesesSi hay riesgo, a partir de los 6 meses se puede aplicar, pero nose contabiliza como dosis válida 2 dosis: 0 y 6-12 meses Rabia(IM e ID) No aplicar a menores de 1 año de forma preventiva, pero sí, si hay riesgo por mordedura De 2 a 6 dosisPauta preexposición:ID: 02, 72 y 282b, 4 o 6 dosisIM: 0, 7 y 28b días, 2 o 3 dosisRecuerdo en 2-5 añosPauta postexposición:(+gammaglobulina antirrábica)ID: 0, 3 y 7 en 2 lugares, 6 dosisIM: 0, 3, 7 y 21, 4 dosisIM: 0 en 2 lugares, 7 y 21, 4 dosis Niños viajeros con estancia prolongada en zonas endémicas, especialmente con destino a áreas endémicas remotas o incursiones en cuevas, con difícil acceso a la administración de gammaglobulina Dengue(SC) A partir de los 4 años de edad 2 dosis: 0 y 3 meses Contraindicada en anafilaxia a algún componente, inmunodeficiencias, embarazadas y mujeres lactantes Tuberculosis(ID) Desde recién nacido Dosis única: 0,1ml en >1 año y 0,05ml en <1 año Puede plantearse en personas no vacunadas previamente y Mantoux negativas, según el destino y la naturaleza del viaje. Contraindicada en <2 años en un hogar en el que se sospeche o se haya confirmado un caso de tuberculosis activa, seropositivos VIH, bebés nacidos de una madre que haya recibido terapia biológica inmunosupresora durante el embarazo y a quienes estén recibiendo o hayan recibido en los últimos 6 meses terapias que impacten en la inmunidad (quimioterapia, radioterapia o terapia biológica) SC: subcutánea; ID: intradérmica; IM: intramuscular; VO: oral.
- •
Recomendadas según el viaje: se recomiendan según el destino, dependiendo de la evaluación del riesgo del niño y del tipo de viaje.
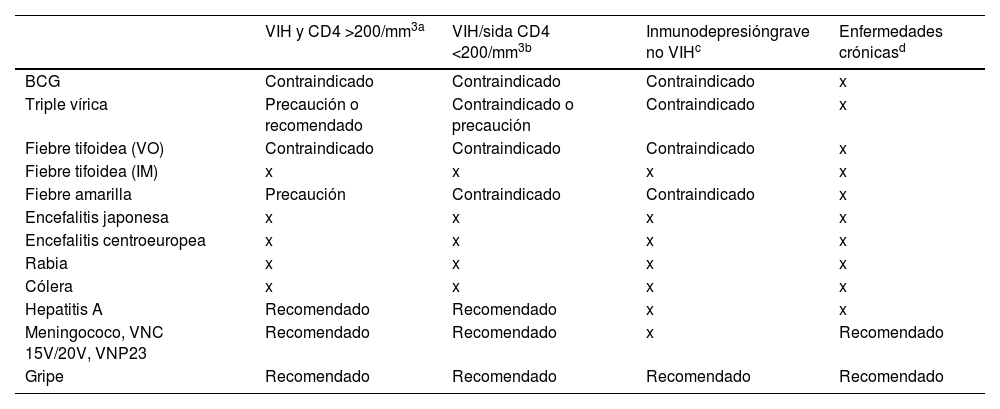
Las recomendaciones específicas de vacunación en el niño viajero inmunodeprimido se detallan en la tabla 8.
Recomendaciones específicas de vacunación en el niño viajero inmunodeprimido
| VIH y CD4 >200/mm3a | VIH/sida CD4 <200/mm3b | Inmunodepresióngrave no VIHc | Enfermedades crónicasd | |
|---|---|---|---|---|
| BCG | Contraindicado | Contraindicado | Contraindicado | x |
| Triple vírica | Precaución o recomendado | Contraindicado o precaución | Contraindicado | x |
| Fiebre tifoidea (VO) | Contraindicado | Contraindicado | Contraindicado | x |
| Fiebre tifoidea (IM) | x | x | x | x |
| Fiebre amarilla | Precaución | Contraindicado | Contraindicado | x |
| Encefalitis japonesa | x | x | x | x |
| Encefalitis centroeuropea | x | x | x | x |
| Rabia | x | x | x | x |
| Cólera | x | x | x | x |
| Hepatitis A | Recomendado | Recomendado | x | x |
| Meningococo, VNC 15V/20V, VNP23 | Recomendado | Recomendado | x | Recomendado |
| Gripe | Recomendado | Recomendado | Recomendado | Recomendado |
BCG: Bacilo de Calmette-Guérin; IM: intramuscular; VNC: vacuna neumocócica conjugada; VO: oral; VPN: vacuna neumocócica polisacárida 23-valente; X: indicada vacunación igual que en niños sanos; 15V: 15-valente; 20V: 20-valente.
X: indicada vacunación igual que en niños sanos.
VIH y CD4 >200/mm3. No deben recibir vacunas vivas atenuadas, salvo la triple vírica y varicela, si los CD4 son >200. La respuesta a vacunas inactivadas puede ser subóptima. Se recomienda posponer el viaje y, por tanto, la vacunación, al menos, 3 meses tras la reconstitución inmunitaria. A pesar de tasas de seroconversión y títulos de Ac menores que en niños sanos, responden con Ac protectores frente a la mayoría de las vacunas estudiadas.
VIH/sida CD4 <200/mm3. Imprescindible conocer el valor de linfocitos CD4 en niños VIH antes del viaje. Si el recuento de CD4 <200/mm3 y están sin tratamiento antirretroviral, deben retrasar el viaje hasta iniciar terapia antirretroviral y conseguir la reconstitución inmunitaria.
Inmunodepresión grave no VIH. Incluye: leucemia o linfoma activo, carcinoma generalizado, anemia aplásica, EICH, errores innatos de la inmunidad, tratamiento con radioterapia o muy reciente, TOS o TPH en los 2 primeros años postrasplante y trasplantados hace >2 años, pero con tratamiento inmunosupresor.
Enfermedades crónicas asociadas con un déficit inmunitario limitado. Incluye: asplenia, enfermedad renal o hepática crónica, diabetes o déficit de complemento. Los pacientes asplénicos tienen mayor susceptibilidad a patógenos encapsulados bacterianos y aunque la respuesta vacunal puede ser subóptima, debemos asegurarnos de que está correctamente vacunado frente a meningococo (ABCWY), neumococo y Hib.
La presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
Conflicto de intereses (últimos 5 años)Irene Rivero Calle ha colaborado en actividades docentes subvencionadas por GlaxoSmithKline, MSD, Pfizer y Sanofi Pasteur, como investigadora en ensayos clínicos de vacunas de Abbot, AstraZeneca, Enanta, Gilead, GlaxoSmithKline, HIPPRA, Janssen, Medimmune, Merck, Moderna, MSD, Novavax, Pfizer, Reviral, Roche, Sanofi y Seqirus; y como consultora en Advisory Board de GlaxoSmithKline, MSD, Pfizer y Sanofi.
Teresa del Rosal ha recibido honorarios por conferencias y becas de investigación de MSD, ayuda económica para asistir a actividades docentes de Pfizer y ha participado como investigadora en ensayos clínicos de GSK, Janssen y MSD, recibiendo la institución honorarios por ello.
Elisa Garrote ha colaborado en actividades docentes subvencionadas por GlaxoSmithKline, MSD, Pfizer y Sanofi como investigadora en ensayos clínicos de vacunas de GlaxoSmithKline, y como consultora en Advisory Board de GlaxoSmithKline y MSD.
Esmeralda Núñez ha colaborado en actividades docentes subvencionadas por Pfizer.
María Luisa Navarro ha colaborado en actividades docentes subvencionadas por Gilead, GlaxoSmithKline, Janssen, MSD, Pfizer y ViiV, como consultor en Advisory Board para Abbott, AstraZeneca, Novartis, Pfizer y ViiV y en ensayos clínicos promovidos por GlaxoSmithKline, Pfizer, Roche, MSD, Sanofi, Pfizer.
José Tomas ha recibido honorarios por conferencias de Gilead, GSK, ViiF y Pfizer. Ha recibido becas/ayudas para asistencia a cursos de formación de Biomerieux, Gilead y Pfizer. Ha recibido honorarios por consultorías para Pfizer, GSK y ViiF. Ha participado como investigador principal del centro en ensayos clínicos de Pfizer, GSK y Janssen recibiendo su institución honorarios por ello.
Cristina Calvo ha recibido honorarios por conferencias de MSD y Pfizer. Ha recibido becas/ayudas de investigación de MSD y BioMerieux. Ha recibido honorarios por consultorías para Sanofi. Ha participado como investigador en ensayos clínicos de Abbott, MSD, Pfizer, Janssen, GSK y Allergan recibiendo su institución honorarios por ello.
Francisco Álvarez García ha recibido ayuda económica para asistir a actividades docentes nacionales. He participado en actividades docentes subvencionadas por Alter, AstraZeneca, GSK, Pfizer, MSD y Sanofi. Consultor en Advisory Board de GSK, Pfizer, MSD y Sanofi.
Francisco José Álvarez García (FJAG), Antonio Iofrío de Arce (AIA), Javier Álvarez Aldeán (JAA), María Garcés-Sánchez (MGS), Elisa Garrote Llanos (EGL), Abián Montesdeoca Melián (AMM), Marisa Navarro Gómez (MLNG), Valentín Pineda Solas (VPS), Irene Rivero Calle (IRC), Jesús Ruiz-Contreras (JRC) y Pepe Serrano Marchuet (PSM).