Aunque el tratamiento endoluminal agresivo para la patología oclusiva de la arteria femoral superficial (AFS) es habitual, no están claras las implicaciones de la nefropatía crónica (NC) en los desenlaces a largo plazo en esta población. Examinamos las consecuencias del tratamiento endovascular de la AFS en pacientes sin y con diversos estadios de NC. Se examinó una base de datos de pacientes sometidos a tratamiento endovascular de la AFS entre 1986 y 2007, y se definieron dos grupos: tasa de filtración glomerular estimada (TFGe)≤60 y>60ml/min/1,73cm2. Se efectuó un análisis por intención de tratar. Los resultados se estandarizaron según los criterios del TransAtlantic Inter-Society Consensus (TASC-II) y la Society for Vascular Surgery. Para evaluar las variables tiempodependientes se efectuaron análisis de Kaplan-Meier. También se efectuaron análisis de factor utilizando un modelo de riesgos proporcionales de Cox para las variables tiempodependientes. Los datos se presentan como medias ± desviación estándar cuando es apropiado. Se trataron 525 extremidades en 535 pacientes (68% de hombres, edad media 66±14 años) que se sometieron a tratamiento endovascular por claudicación o isquemia crítica crónica de la extremidad (51%). Los pacientes del grupo con TFGe≤60 eran de mayor edad y experimentaban con una frecuencia significativamente mayor coronariopatía, insuficiencia cardíaca congestiva, diabetes mellitus, e hiperlipemia. La distribución de las lesiones TASC II fue equivalente (37% de lesiones TASC II C y D) pero el runoff tibial fue significativamente peor en dicho grupo. Además, en este grupo se efectuaron un mayor número de intervenciones de flujo eferente y aferente. En pacientes con claudicación, no se detectaron diferencias en la permeabilidad o salvamento de la extremidad entre aquellos con TFGe≤60 y>60. En pacientes con isquemia crítica de la extremidad, no hubo diferencias de permeabilidad entre ambos grupos. Las tasas de salvamento de la extremidad fueron peores en pacientes con TFGe≤60. Al respecto, seis factores se asociaron significativamente con su disminución: presencia de pérdida de tejido en el momento de la presentación (riesgo relativo [RR]=6,45, p=0,003), runoff tibial de 0 o 1 vaso (RR=2,56, p<0,01), progresión de la enfermedad distal observada en el seguimiento (RR=4,62, p<0,01), embolización accidental en la intervención inicial (RR=2,70, p<0,05), diabetes mellitus (RR=3,71, p<0,01) y antecedentes de insuficiencia cardíaca congestiva (RR=2,42, p<0,01). Los factores destacados no asociados significativamente incluyeron la calcificación de la lesión (p=0,64), una clasificación de la lesión como TASC C o D (p=0,99), la oclusión aguda en la intervención inicial (p=0,40) y la implantación adyuvante de un stent (p=0,67). La NC no influye en la permeabilidad en las intervenciones de la AFS. En pacientes con isquemia crítica la tasa de salvamento de la extremidad es significativamente peor cuando la TFGe es≤60ml/min/1,73cm2.
En Estados Unidos los pacientes con nefropatía crónica (NC) representan un problema sustancial de salud pública y que va en aumento. La prevalencia estimada de los estadios 1-4 de la enfermedad ha aumentado desde el 10,0% en el período 1988-1994 hasta el 13,1% en el período 1999-20041. De acuerdo con el Annual Data Report del US Renal Data System de 2007, en 2004, 472.099 pacientes adicionales se sometieron a diálisis2 (alrededor del 0,2% de la población estadounidense), con una tasa de crecimiento anual de algo menos del 3% desde 2001. La NC es un factor de riesgo reconocido de desarrollo de enfermedad cardiovascular3, presentando los pacientes más probabilidades de fallecer de ella que de insuficiencia renal4. También es bien conocido que los pacientes con NC (tasa de filtración glomerular [TFG]≤60ml/min/1,73cm2) corren un mayor riesgo específico de arteriopatía periférica (AP) con una odds ratio ajustada de 2,5 de prevalencia de disminución del índice tobillo-brazo en función de los datos del National Health and Nutrition Examination Survey 1999-20005. Utilizando los datos del estudio Atherosclerosis Risk in Communities, se identificó a los pacientes con NC (TFG≤60ml/min/1,73cm2) como portadores de un riesgo relativo (RR) de AP incidente de 1,59 después de un ajuste para los factores demográficos y de riesgo cardiovascular6. En pacientes con insuficiencia renal no se dispone de una serie a gran escala sobre desenlaces endovasculares del tratamiento de la isquemia crítica de la extremidad7 (ICE).
Aunque es evidente que los pacientes con nefropatía corren mayor riesgo de desarrollar arteriopatía de la extremidad inferior, no se ha definido claramente su influencia en los resultados después de una intervención quirúrgica. En numerosas series quirúrgicas retrospectivas se ha identificado sistemáticamente la insuficiencia renal terminal como un factor de riesgo sustancial de mayor mortalidad y pérdida de la extremidad tras bypass quirúrgico8-16. En comparación, apenas se han publicado datos sobe el resultado de pacientes con nefropatía avanzada después de revascularización endoluminal. El objetivo del presente estudio fue definir los desenlaces relacionados con la permeabilidad y salvamento de la extremidad para las intervenciones endoluminales de la arteria femoral superficial (AFS) a través de un espectro de nefropatía, definido por la TFG estimada (TFGe).
MétodosDiseño del estudioSe examinó una base de datos de pacientes sometidos a angioplastia transluminal percutánea (ATP) y/o implantación de un stent de la AFS entre 1986 y 2007. Preoperatoriamente se clasificó a los pacientes según unos valores de la TFGe≤60 o>60ml/min/1,73cm2. Se efectuó un análisis por intención de tratar. Los resultados se estandarizaron según los criterios del TransAtlantic Inter-Society Consensus17 (TASC-II) y la Society for Vascular Surgery18 (SVS). Para evaluar las variables tiempodependientes se efectuaron análisis de Kaplan-Meier. También se efectuaron análisis de factor utilizando un modelo de riesgos proporcionales de Cox para las variables tiempodependientes.
MetodologíaPara cada paciente identificado, se registraron la demografía, los síntomas, procesos comórbidos, y factores de riesgo de aterosclerosis. Se animó a todos aquellos con claudicación a efectuar ejercicio todos los días, y sus médicos de cabecera identificaron y corrigieron sus factores de riesgo. Se ofreció intervención endoluminal a los que desarrollaron pérdida de tejido o síntomas de deterioro durante el tratamiento. Los pacientes con isquemia crítica fueron tratados en la misma hospitalización. La preferencia del médico responsable individual dictó el tratamiento para cada paciente y no estuvo regulado por las guías de la unidad. Todos los pacientes recibieron 81 o 325mg/día de aspirina como fármaco de protección cardiovascular general. Inicialmente se efectuaron estudios no cruentos; sin embargo, en pacientes con signos o síntomas sustanciales de estenosis/oclusión grave en función de estos exámenes iniciales se practicaron angiografías. Se revisaron éstas y los informes angiográficos clasificando las lesiones con el sistema TASC-II, y se puntuó el drenaje distal o runoff preoperatorio. Se practicó angioplastia con la administración de heparina sistémica (40-60 unidades/kg) y, para evaluar el resultado técnico después del procedimiento, se efectuó una angiografía. Los stents se utilizaron (a discreción del cirujano vascular) para disecciones limitantes del flujo (grado C o mayores), flaps intimales, oclusiones agudas o resultados técnicos desfavorables (estenosis residual≥50%). No se efectuaron procedimientos o intervenciones que potencialmente pusieran en riesgo el vaso de salida distal. Los pacientes en los que la intervención endoluminal fue satisfactoria recibieron 75mg de clopidogrel. Mientras el paciente recibía este tratamiento, se mantuvo la administración de aspirina en dosis de 81mg/día. Aquellos ya tratados con clopidogrel antes de la intervención continuaron con el tratamiento después de ella. Los pacientes se sometieron a un eco-Doppler sistemático a 1, 3 y 6 meses después del procedimiento y, acto seguido, cada 6 meses. Durante el seguimiento, sólo se efectuaron angiografías si los estudios no cruentos sugirieron reestenosis/oclusión y el paciente se encontraba sintomático.
DefinicionesLa coronariopatía se definió como antecedentes de angina de pecho, infarto de miocardio, insuficiencia cardíaca congestiva o revascularización coronaria previa. La enfermedad vascular cerebral se definió como antecedentes de ictus, episodio isquémico transitorio o revascularización de la arteria carótida. Para definir las categorías de las lesiones se usó la clasificación TASC-II de gravedad de la patología para las lesiones femorales. La TFG se estimó a partir de la ecuación abreviada desarrollada con los datos del estudio Modification of Diet in Renal Disease19,20 del siguiente modo: TFGe 186,3 ∗ (creatinina sérica)−1,154 ∗ edad−0,203 ∗ 0,742 (en pacientes de sexo femenino) ∗ 1,212 (si el individuo es afroamericano). La muerte dentro de los 30 días postprocedimiento se consideró mortalidad relacionada con el mismo. Una complicación mayor se definió como cualquier acontecimiento, con independencia de su grado, no observado habitualmente después del tratamiento endoluminal que requirió una intervención terapéutica o una nueva hospitalización al cabo de 30 días del procedimiento. El runoff en los vasos tibiales se determinó por el número de vasos permeables presentes con un máximo de 3 (puntuado como 0, 1, 2 o 3) y mediante un sistema de puntuación de la SVS modificado21.
Análisis estadísticoLa serie de datos se documentó en función de los resultados de la TFG≤60 o>60ml/min/1,73cm2. Los valores determinados se documentan como porcentajes o medias ± desviación estándar (DE). Las tasas de permeabilidad y de salvamento de la extremidad se calcularon utilizando el análisis de Kaplan-Meier y se documentaron usando los criterios actuales de la SVS18. En los análisis de Kaplan-Meier se documentaron los errores estándar. Se efectuaron análisis de riesgos proporcionales de Cox para identificar los factores asociados con los desenlaces. Los análisis se efectuaron utilizando el programa JMP, versión 7.0.1 (SAS Institute, Cary, Estados Unidos).
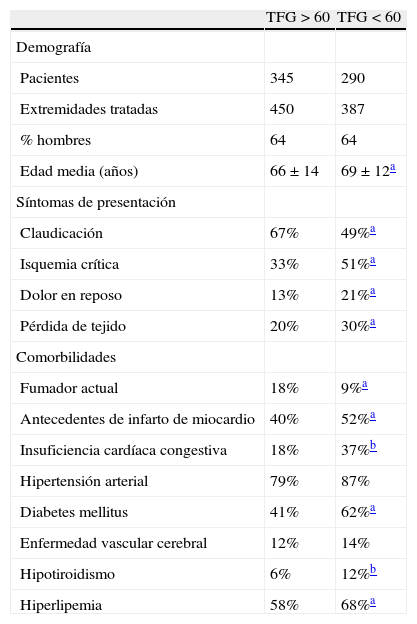
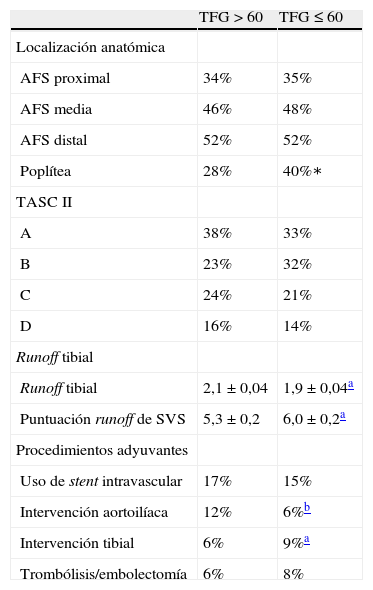
ResultadosPoblación de pacientesDurante el período de estudio 837 extremidades en 635 pacientes se sometieron a tratamiento endoluminal de la AFS (tabla I). Los pacientes con TFGe≤60 eran de mayor edad y presentaban con una significativa mayor frecuencia coronariopatía, insuficiencia cardíaca congestiva, diabetes mellitus, hipotiroidismo e hiperlipemia. De este grupo, un 51% presentaban ICE (tabla I). La distribución de las lesiones TASC II fue equivalente pero el runoff tibial fue peor en el grupo con TFGe≤60ml/min/1,73cm2 (tabla II). Además, en este grupo se efectuaron un mayor número de intervenciones concomitantes tanto sobre flujo aferente como eferente (inflow y outflow).
Características y presentación de los pacientes
| TFG>60 | TFG<60 | |
| Demografía | ||
| Pacientes | 345 | 290 |
| Extremidades tratadas | 450 | 387 |
| % hombres | 64 | 64 |
| Edad media (años) | 66±14 | 69±12a |
| Síntomas de presentación | ||
| Claudicación | 67% | 49%a |
| Isquemia crítica | 33% | 51%a |
| Dolor en reposo | 13% | 21%a |
| Pérdida de tejido | 20% | 30%a |
| Comorbilidades | ||
| Fumador actual | 18% | 9%a |
| Antecedentes de infarto de miocardio | 40% | 52%a |
| Insuficiencia cardíaca congestiva | 18% | 37%b |
| Hipertensión arterial | 79% | 87% |
| Diabetes mellitus | 41% | 62%a |
| Enfermedad vascular cerebral | 12% | 14% |
| Hipotiroidismo | 6% | 12%b |
| Hiperlipemia | 58% | 68%a |
Localización de la enfermedad, categoría TAS, runoff tibial y procedimientos adyuvantes
| TFG>60 | TFG≤60 | |
| Localización anatómica | ||
| AFS proximal | 34% | 35% |
| AFS media | 46% | 48% |
| AFS distal | 52% | 52% |
| Poplítea | 28% | 40%∗ |
| TASC II | ||
| A | 38% | 33% |
| B | 23% | 32% |
| C | 24% | 21% |
| D | 16% | 14% |
| Runoff tibial | ||
| Runoff tibial | 2,1±0,04 | 1,9±0,04a |
| Puntuación runoff de SVS | 5,3±0,2 | 6,0±0,2a |
| Procedimientos adyuvantes | ||
| Uso de stent intravascular | 17% | 15% |
| Intervención aortoilíaca | 12% | 6%b |
| Intervención tibial | 6% | 9%a |
| Trombólisis/embolectomía | 6% | 8% |
AFS: arteria femoral superficial; SVS: Society for Vascular Surgery; TASC: TransAtlantic Inter-Society Consensus.
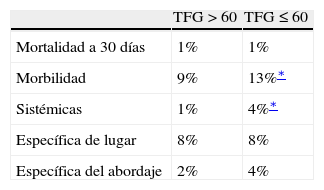
La mortalidad fue equivalente en ambos grupos. Sin embargo, en pacientes con TFGe<30ml/min/1,73cm2 o sometidos a hemodiálisis la tasa de mortalidad fue del 2%. Hubo un aumento significativo de la mortalidad (sistémica y relacionada con el acceso vascular) en el grupo≤60 comparado con el otro grupo (tabla III).
La eficacia hemodinámica fue mejor en el grupo TFGe≤60 comparado con el otro grupo (54% frente a 46%, p<0,05). La mayoría de los pacientes de ambos grupos refirieron una mejora o resolución equivalente de los síntomas (83% para el grupo TFGe<60 frente al 86% para el deTFGe>60). Hubo un reducido número de casos en los que se produjo trombosis in situ o embolización distal (tabla III). En estos casos, se requirió trombólisis y embolectomía. No se objetivaron diferencias entre ambos grupos.
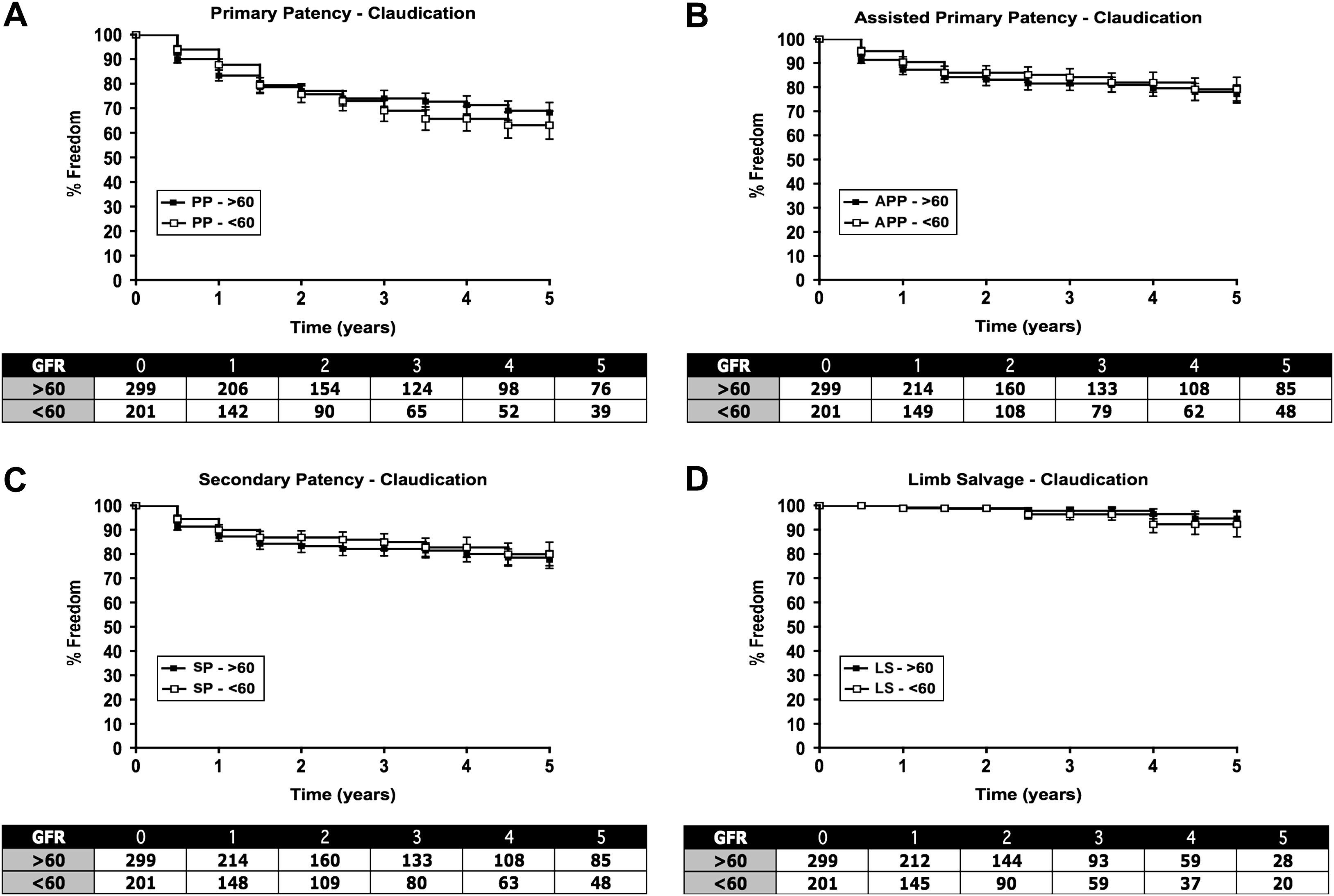
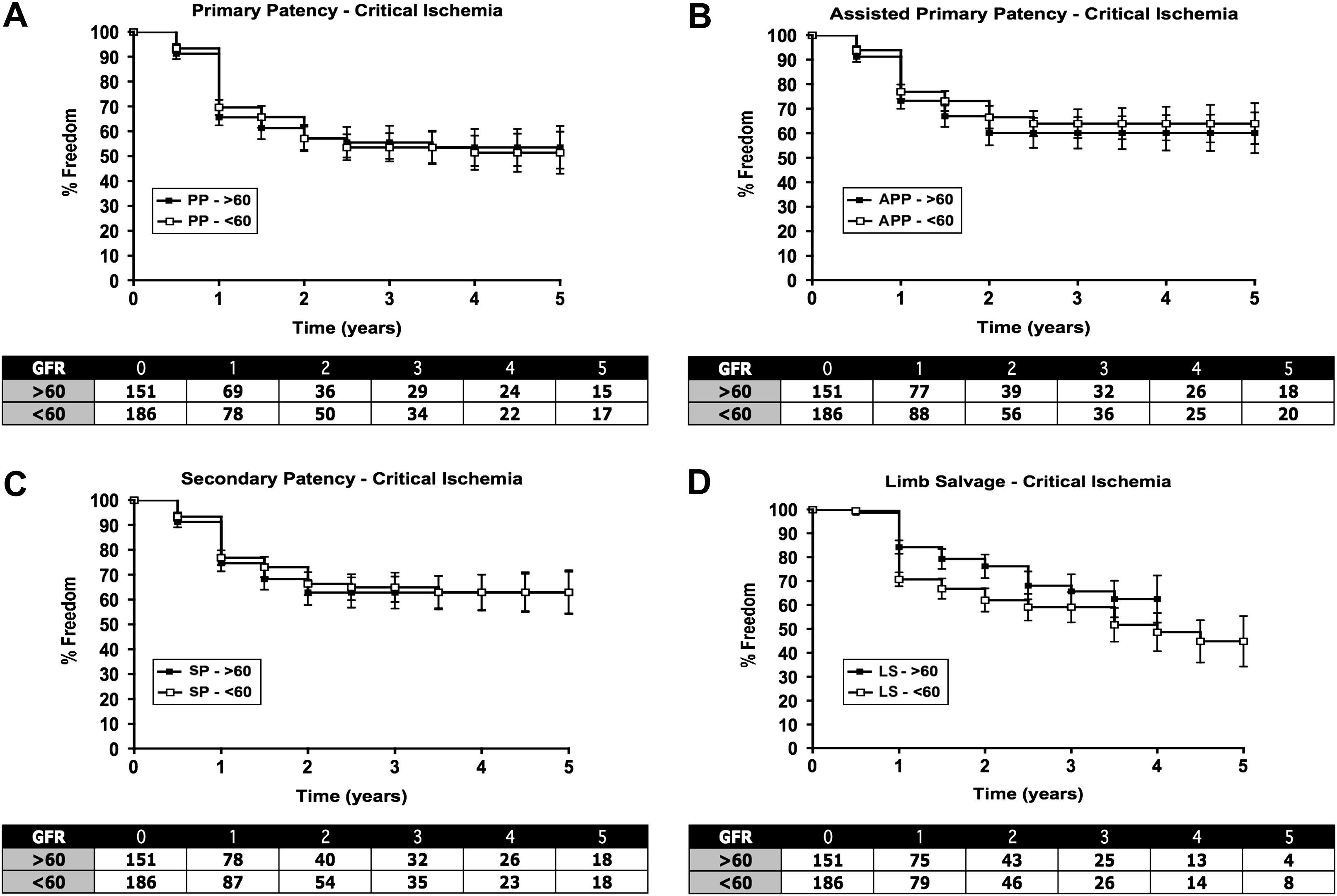
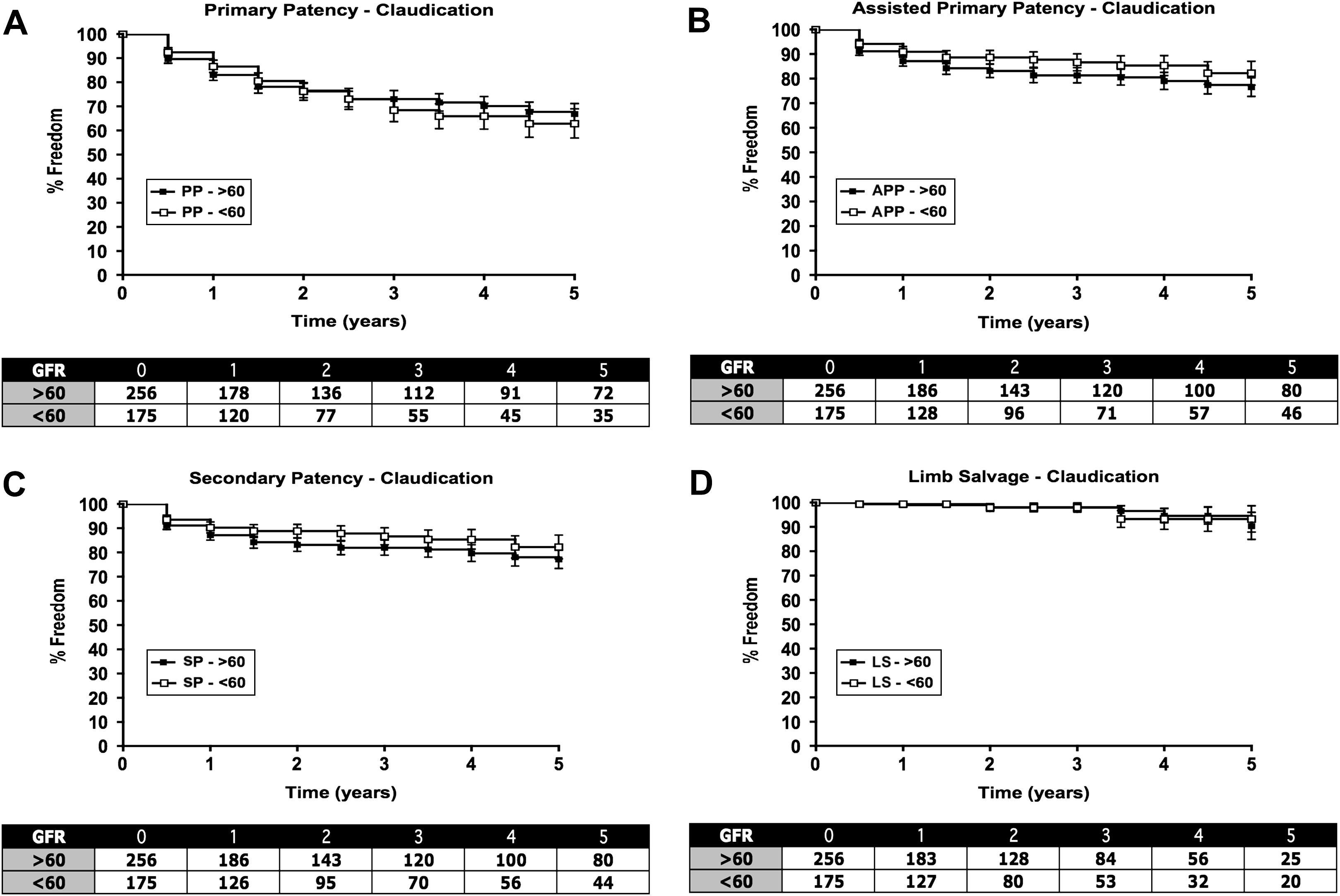
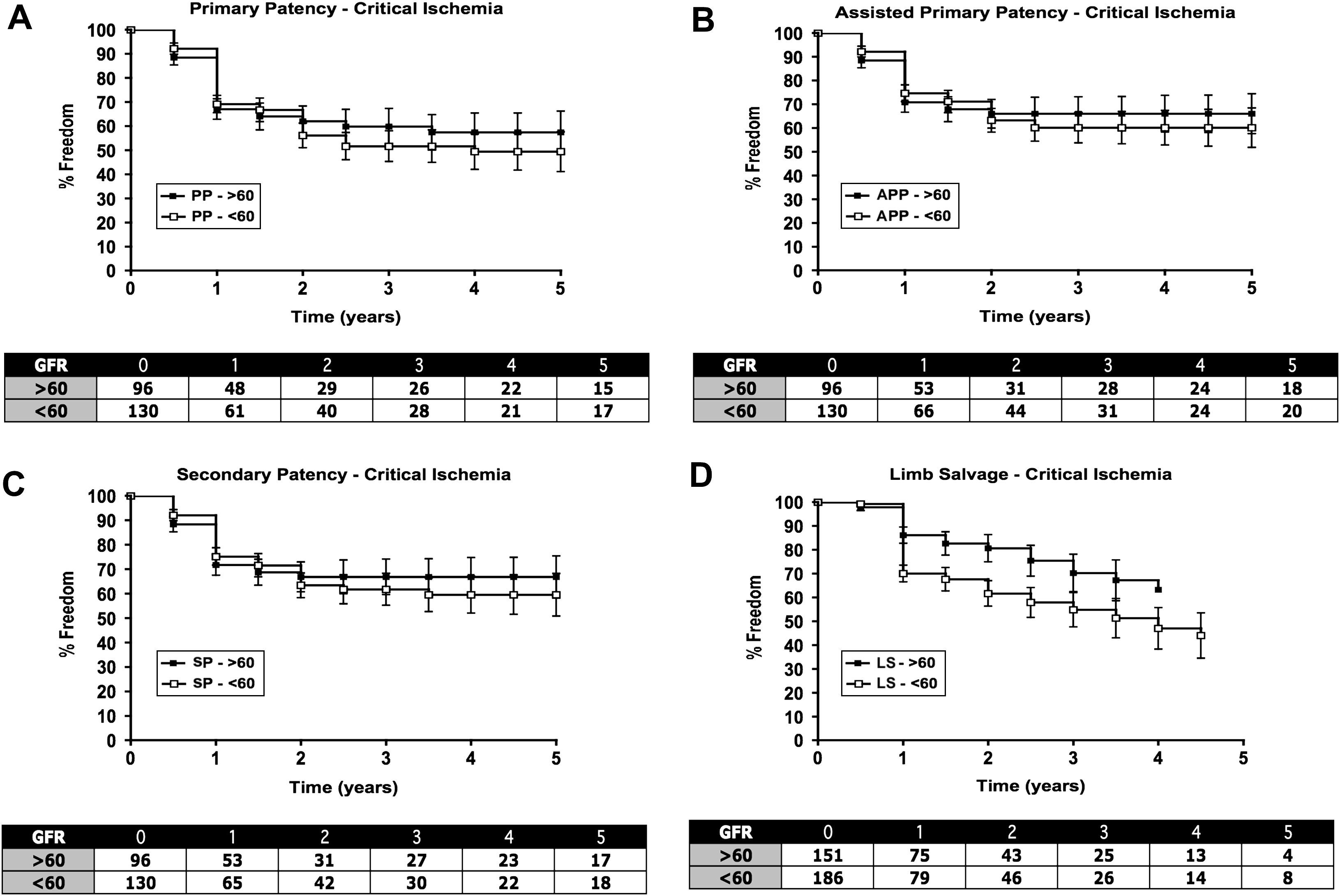
Desenlaces a más largo plazoEn pacientes con claudicación, no se detectaron diferencias en la permeabilidad o salvamento de la extremidad entre aquellos con TFGe>60 y≤60mg/min/1,73cm2, con tasas de permeabilidad acumulada a los 5 años del 78±4% y 79±5% respectivamente y una tasa de salvamento de la extremidad a los 5 años del 95±3% y 92±5% respectivamente (fig. 1). En pacientes con ICE, no hubo diferencias en la tasa de permeabilidad entre ambos grupos, siendo la tasa de permeabilidad acumulada a los 5 años de 63±8% y 63±9% respectivamente (figs. 2A a 2C). La tasa de salvamento de la extremidad fue peor en pacientes con TFGe≤60 comparado con>60, siendo, respectivamente, de 48±8% y de 62±9% (fig. 2D). En ambos grupos se efectuó un notable número de intervenciones sobre el flujo aferente y eferente (inflow y outflow). Por esta razón, examinamos a los pacientes de la cohorte sometidos exclusivamente a intervenciones de la AFS (figs. 3 y 4). En este subgrupo, al igual que en toda la población, se identificaron diferencias significativas entre el grupo claudicación e isquemia crítica por lo que respecta a la permeabilidad (tasa de permeabilidad acumulada a los 5 años: claudicación, 77±4% y 82±5%, e ICE, 67±9% y 60±9% para el grupo TFGe>60 y≤60, respectivamente) y tasas de salvamento de la extremidad (tasa de salvamento a los 5 años: claudicación, 90±6% y 93±5%, e ICE, 67±9% y 47±9% para el grupo TFGe>60 y≤60, respectivamente). Cuando este subgrupo se separó por síntomas (claudicación e isquemia crítica) y TFGe (≤ 60 y>60ml/min/1,73cm2), la TFGe no predijo una diferencia de la permeabilidad (figs. 3 y 4). Sin embargo, aunque la tasa de salvamento de la extremidad fue equivalente en el grupo claudicación entre ambos subgrupos de TFG, fue marcadamente diferente en el grupo de isquemia crítica entre subgrupos de TFGe≤60 y>60 (p<0,01).
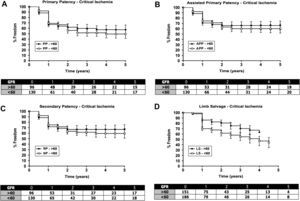
Todos los pacientes con claudicación. Análisis de la tabla de vida de todos los pacientes (intervenciones en la arteria femoral superficial [AFS] e intervenciones adyuvantes) que presentaron claudicación agrupados por una tasa de filtración glomerular estimada (TFGe)≤60 y>60ml/min/1,73cm2. Los datos son la media y el error estándar de la media y en la tabla se muestra el número en riesgo. A: permeabilidad primaria, B: permeabilidad primaria asistida, C: permeabilidad secundaria, D: salvamento de la extremidad. % Freedom: porcentaje libre de; APP: permeabilidad primaria asistida; Assisted Primary Patency - Claudication: permeabilidad primaria asistida, claudicación; Limb Salvage - Claudication: salvamento de la extremidad, claudicación; LS: salvamento extremidad; PP: permeabilidad primaria; Primary Patency - Claudication: permeabilidad primaria, claudicación; Secondary Patency - Claudication: permeabilidad secundaria, claudicación; SP: permeabilidad secundaria; TFG: tasa de filtración glomerular; Time (years): tiempo (años).
Todos los pacientes con isquemia crítica de la extremidad. Análisis de la tabla de vida de todos los pacientes (intervenciones de la arteria femoral superficial [AFS] e intervenciones adyuvantes) que presentaron ICE agrupados por una tasa de filtración glomerular estimada (TFGe)≤60 y>60ml/min/1,73cm2. Los datos son la media y el error estándar de la media y en la tabla se muestra el número en riesgo. A: permeabilidad primaria, B: permeabilidad primaria asistida, C: permeabilidad secundaria, D: salvamento de la extremidad. % Freedom: porcentaje libre de; APP: permeabilidad primaria asistida; Assisted Primary Patency - Critical Ischemia: permeabilidad secundaria, isquemia crítica; GFR: tasa de filtración glomerular; Limb Salvage - Critical Ischemia: salvamento de la extremidad, isquemia crítica; LS: salvamento de la extremidad; PP: permeabilidad primaria; Primary Patency - Critical Ischemia: permeabilidad primaria, isquemia crítica; Secondary Patency - Critical Ischemia: permeabilidad secundaria, isquemia crítica; SP: permeabilidad secundaria; Time (years): tiempo (años).
Sólo intervenciones de arteria femoral superficial (AFS). Pacientes con claudicación. Análisis de la tabla de vida de todos los pacientes (intervenciones sólo de la AFS) que presentaron claudicación agrupados por una tasa de filtración glomerular estimada (TFGe)≤60 y>60ml/min/1,73cm2. Los datos son la media y el error estándar de la media y en la tabla se muestran el número en riesgo. A: permeabilidad primaria, B: permeabilidad primaria asistida, C: permeabilidad secundaria, D: salvamento de la extremidad. % Freedom: porcentaje libre de; APP: permeabilidad primaria asistida; Assisted Primary Patency - Claudication: permeabilidad primaria asistida, claudicación; GFR: tasa de filtración glomerular; Limb Salvage - Claudication: salvamento extremidad, claudicación; LS: salvamento extremidad; PP: permeabilidad primaria; Primary Patency - Claudication: permeabilidad primaria, claudicación; Secondary Patency - Claudication: permeabilidad secundaria, claudicación; SP: permeabilidad secundaria.
Sólo intervenciones de arteria femoral superficial (AFS). Pacientes con isquemia crítica de la extremidad (ICE). Análisis de la tabla de vida de todos los pacientes (intervenciones sólo de la AFS) que presentaron ICE agrupados por una tasa de filtración glomerular estimada (TFGe)≤60 y>60ml/min/1,73cm2. Los datos son la media y el error estándar de la media y en la tabla se muestran el número en riesgo. A: permeabilidad primaria, B: permeabilidad primaria asistida, C: permeabilidad secundaria, D: salvamento de la extremidad. % Freedom: porcentaje libre de; APP: permeabilidad primaria asistida; Assisted Primary Patency - Critical Ischemia: permeabilidad primaria asistida, isquemia crítica; GFR: tasa de filtración glomerular; Limb Salvage - Critical Ischemia: salvamento extremidad, isquemia crítica; LS: salvamento extremidad; PP: permeabilidad primaria; Primary Patency - Critical Ischemia: permeabilidad primaria, isquemia crítica; Secondary Patency - Critical Ischemia: permeabilidad secundaria, isquemia crítica; SP: permeabilidad secundaria; Time (years): tiempo (años).
Se efectuó un análisis de riesgos proporcionales de Cox para investigar la influencia de los factores pre y perioperatorios relacionados con los desenlaces de la permeabilidad al igual que el salvamento de la extremidad entre los grupos claudicación e isquemia crítica subdivididos por la TFGe. Ningún proceso comórbido afectó a la permeabilidad primaria. La calcificación de las lesiones (RR=2,62, p<0,01), clasificación de la lesión TASC C o D (RR=2,44, p<0,01), oclusión aguda en la intervención inicial (RR=3,81, p<0,01), y pérdida de tejido en el momento de la presentación (RR=7,38, p=0,02) se asociaron significativamente con disminuciones de la permeabilidad primaria. Los factores asociados significativamente con una disminución de la permeabilidad primaria asistida y secundaria también incluyeron la calcificación (RR=6,31, p<0,01), las lesiones TASC C o D (RR=4,20, p<0,01), la oclusión aguda en la intervención inicial (RR=4,37, p<0,01), y la pérdida de tejido en el momento de la presentación (RR=7,43, p<0,01). El runoff de 0 o 1 y una puntuación SVS modificada>8 también se asociaron con una disminución de la tasa de permeabilidad primaria asistida y secundaria (RR=3,72, p<0,05). El uso de stents no fue significativo. Con respecto al salvamento de la extremidad, seis factores se asociaron significativamente con una disminución de las tasas: presencia de pérdida de tejido en el momento de la presentación (RR=6,45, p<0,003), runoff tibial de 0 o 1 vaso (RR=2,56, p<0,01), progresión de la enfermedad distal observada en el seguimiento (RR=4,62, p<0,01), embolización en la intervención inicial (RR=2,70, p<0,05), diabetes mellitus (RR=3,71, p<0,01), y antecedentes de insuficiencia cardíaca congestiva (RR=2,42, p<0,01). Los factores destacados no asociados significativamente incluyeron la calcificación de la lesión (p=0,64), clasificación C o D de la lesión TASC (p=0,99), oclusión aguda en la intervención inicial (p=0,40) e implantación adyuvante de un stent (p=0,67).
DiscusiónEl presente estudio demuestra que la NC apenas parece influir en las intervenciones de la AFS en pacientes que se presentan con claudicación, en parte porque aquellos con un deterioro renal mínimo presentan claudicación mientras que aquellos con un deterioro renal más grave presentan isquemia crítica. A pesar del elevado número de pacientes sometidos a procedimientos adyuvantes en el flujo de entrada y de salida (inflow y outflow), la permeabilidad de las intervenciones de la AFS siguió dependiendo de los síntomas de presentación, con independencia de los valores de la TFGe. En comparación, en la isquemia crítica de la extremidad el deterioro renal influye significativamente en el salvamento de la extremidad.
Como han observado otros investigadores14,22,23, encontramos que entre los que experimentaban ICE predominaban pacientes con nefropatía avanzada. Estos resultados son cualitativamente similares a los de otros estudios publicados sobre bypass infrainguinal en pacientes con grados variables de disfunción renal22-25. Dado el perfil de tolerancia demostrado en otras poblaciones de pacientes, algunos autores han sugerido26 que esta intervención en pacientes con disfunción renal avanzada podría mitigar parte del riesgo de mortalidad perioperatoria inherente al bypass infrainguinal. Aunque en la presente serie no incluimos una cohorte sometida a cirugía abierta, en pacientes tratados con técnicas endoluminales encontramos una mortalidad periprocedimiento reducida, siendo la tasa de mortalidad a 30 días del 1% en pacientes con valores bajos de la TFGe; en aquellos con valores<30 o sometidos a hemodiálisis, la tasa de mortalidad fue del 2%. Estos resultados son mejores que los descritos por Graziani et al26, que documentaron una tasa de mortalidad a 30 días del 8% entre 107 pacientes sometidos a diálisis después de ATP para isquemia, y los datos del National Surgical Quality Improvement Program de los Veterans Affairs documentados por O'Hare et al22, que demostraron una tasa de mortalidad a 30 días del 10% tanto para pacientes dependientes de diálisis como para aquellos con TFG<30ml/min que no requerían diálisis. En otro estudio publicado, que comparó la angioplastia y el bypass, los investigadores demostraron que, comparados con los pacientes sometidos a angioplastia, en los tratados con bypass el riesgo de mortalidad por cualquier causa, mortalidad cardíaca y de causa infecciosa fue mayor27. Por lo tanto, estos datos sugieren una ventaja inmediata de la intervención endoluminal para pacientes con deterioro renal. Sin embargo, observamos una tasa de morbilidad del 10% en pacientes con deterioro avanzado que pareció determinada por las complicaciones sistémicas y del lugar de acceso vascular.
En un estudio de 2004, efectuado en 800 pacientes sometidos a un procedimiento de revascularización inicial mediante bypass quirúrgico o angioplastia, la incidencia global de amputación ulterior fue de 16,3/100 años-persona, de 22,6 para el bypass y de 5,7 para la angioplastia. Después de un ajuste para las características del paciente, el riesgo de amputación fue mayor entre pacientes sometidos a bypass comparado con angioplastia27 (cociente de riesgo [CR]=4,00, intervalo de confianza del 95% 2,46-6,57).
En las publicaciones previas sobre bypass se han demostrado mayores tasas de salvamento de la extremidad al año para pacientes con nefropatía crónica en estadio 4 de la clasificación de la National Kidney Foundation23 (88%) que para aquellos dependientes de diálisis23,28 (71-78%). De forma parecida, Graziani et al26 describieron una tasa de salvamento de la extremidad al año del 86% después de ATP. En los resultados del presente estudio una posible variable de confusión es la mayor tasa de diabetes mellitus (85-87% de pacientes ICE con TFGe≤60ml/min/1,73cm2) en comparación con la tasa descrita en los estudios mencionados previamente23,26 (53-59%). La diabetes influye significativamente en estas tasas después de tratamiento endoluminal para ICE29,30. Variables de confusión adicionales pueden incluir diferentes tasas de ulceración, gangrena e infección activa de los tejidos (que no se definieron específicamente en el presente estudio) y del runoff tibial, que se han asociado con peores desenlaces22-24. Además, hemos demostrado que el runoff influirá sustancialmente en los resultados de la intervención en la ICE21. Cuando examinamos la tasa de salvamento de la extremidad en función de los subgrupos con TFGe≤60 y>60ml/min/1,73cm2, encontramos que el primero se asoció con una tasa más baja de salvamento de la extremidad, con independencia de que examináramos toda la cohorte o el subgrupo donde sólo se efectuó la intervención sobre la AFS. Estos datos sugieren que, mientras la tasa de salvamento es reducida en la ICE, un valor de TFGe≤60 tiene además una repercusión en el resultado, pero estos esfuerzos se acompañan de una menor tasa perioperatoria de mortalidad.
En un metaanálisis reciente se describieron tasas de permeabilidad primaria y secundaria al año del 75 y 81%, respectivamente, para pacientes con insuficiencia renal terminal sometidos a bypass infrainguinal28. En el presente estudio, la tasa de permeabilidad primaria al año fue del 86% para pacientes con claudicación y del 69% para la ICE en pacientes con TFGe≤60. La tasa de permeabilidad secundaria al año fue del 90% para la claudicación y del 75% para la ICE en pacientes con estos valores de TFGe. Las permeabilidades en ambas situaciones fueron similares en el subgrupo con TFGe>60. A los 5 años, en el caso del subgrupo TFGe≤60, en pacientes con claudicación se detectaron tasas de permeabilidad primaria y secundaria del 63% y 82%, respectivamente. Para la ICE, las tasas de permeabilidad primaria y secundaria fueron del 49 y 59%, respectivamente. En pacientes con TFG>60 las tasas a los 5 años fueron equivalentes en el grupo con claudicación e ICE. Si sólo se analiza a los pacientes sometidos a intervención de AFS, las conclusiones extraídas son similares. Es decir, parece ser que los valores de la TFGe no influyeron en la permeabilidad anatómica de las intervenciones en la arteria y que nuestros resultados acumulativos deparan la misma permeabilidad que la descrita para el bypass en esta población, con una morbilidad menor.
Es preciso destacar que los datos descritos en este estudio representan un análisis retrospectivo de pacientes no seleccionados y no aleatorizados. Por consiguiente, es posible, por no decir previsible, la presencia de un sesgo de selección. En la práctica clínica, con frecuencia, los pacientes son derivados/considerados para una intervención endoluminal debido a su constelación de comorbilidades. Esto puede dar lugar a una intervención en los más problemáticos con una patología vascular sistémica más compleja, lo que se traducirá en peores desenlaces como consecuencia de esta población exclusiva de pacientes. Al contrario, algunos no son considerados para una intervención endoluminal porque se cree que su patología vascular difusa y complicada contraindica este tratamiento. Esto, a su vez, puede dar lugar a la migración externa de estos pacientes complicados, lo que inflará artificialmente los resultados. Lamentablemente en la actualidad no podemos definir la contribución relativa de cualquiera de ambos fenómenos partiendo de los datos disponibles.
ConclusiónEn general, los pacientes que se presentan para una intervención de la AFS con claudicación experimentan un deterioro renal mínimo, mientras que aquellos con isquemia crítica presentan con más probabilidad un deterioro renal de mayor gravedad. La nefropatía crónica no parece influir en la tasa de permeabilidad de las intervenciones de la AFS. El salvamento de la extremidad en pacientes con isquemia crítica es significativamente más desfavorable cuando la TFGe es≤60ml/min/1,73cm2. Los factores asociados significativamente con una tasa desfavorable de salvamento de la extremidad en este grupo fueron la presencia de pérdida de tejido en la presentación, un runoff tibial desfavorable, la progresión de la enfermedad distal, la embolización en la intervención inicial, diabetes mellitus y los antecedentes de insuficiencia cardíaca congestiva.
Presentado en parte en la reunión de invierno de la Peripheral Vascular Surgery Society Winter Meeting, Park City, UT, EE. UU., 27-29 de enero de 2006.




![Todos los pacientes con claudicación. Análisis de la tabla de vida de todos los pacientes (intervenciones en la arteria femoral superficial [AFS] e intervenciones adyuvantes) que presentaron claudicación agrupados por una tasa de filtración glomerular estimada (TFGe)≤60 y>60ml/min/1,73cm2. Los datos son la media y el error estándar de la media y en la tabla se muestra el número en riesgo. A: permeabilidad primaria, B: permeabilidad primaria asistida, C: permeabilidad secundaria, D: salvamento de la extremidad. % Freedom: porcentaje libre de; APP: permeabilidad primaria asistida; Assisted Primary Patency - Claudication: permeabilidad primaria asistida, claudicación; Limb Salvage - Claudication: salvamento de la extremidad, claudicación; LS: salvamento extremidad; PP: permeabilidad primaria; Primary Patency - Claudication: permeabilidad primaria, claudicación; Secondary Patency - Claudication: permeabilidad secundaria, claudicación; SP: permeabilidad secundaria; TFG: tasa de filtración glomerular; Time (years): tiempo (años). Todos los pacientes con claudicación. Análisis de la tabla de vida de todos los pacientes (intervenciones en la arteria femoral superficial [AFS] e intervenciones adyuvantes) que presentaron claudicación agrupados por una tasa de filtración glomerular estimada (TFGe)≤60 y>60ml/min/1,73cm2. Los datos son la media y el error estándar de la media y en la tabla se muestra el número en riesgo. A: permeabilidad primaria, B: permeabilidad primaria asistida, C: permeabilidad secundaria, D: salvamento de la extremidad. % Freedom: porcentaje libre de; APP: permeabilidad primaria asistida; Assisted Primary Patency - Claudication: permeabilidad primaria asistida, claudicación; Limb Salvage - Claudication: salvamento de la extremidad, claudicación; LS: salvamento extremidad; PP: permeabilidad primaria; Primary Patency - Claudication: permeabilidad primaria, claudicación; Secondary Patency - Claudication: permeabilidad secundaria, claudicación; SP: permeabilidad secundaria; TFG: tasa de filtración glomerular; Time (years): tiempo (años).](https://static.elsevier.es/multimedia/11302542/0000002300000005/v2_201308271555/S1130254209002440/v2_201308271555/es/main.assets/thumbnail/gr1.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)
![Todos los pacientes con isquemia crítica de la extremidad. Análisis de la tabla de vida de todos los pacientes (intervenciones de la arteria femoral superficial [AFS] e intervenciones adyuvantes) que presentaron ICE agrupados por una tasa de filtración glomerular estimada (TFGe)≤60 y>60ml/min/1,73cm2. Los datos son la media y el error estándar de la media y en la tabla se muestra el número en riesgo. A: permeabilidad primaria, B: permeabilidad primaria asistida, C: permeabilidad secundaria, D: salvamento de la extremidad. % Freedom: porcentaje libre de; APP: permeabilidad primaria asistida; Assisted Primary Patency - Critical Ischemia: permeabilidad secundaria, isquemia crítica; GFR: tasa de filtración glomerular; Limb Salvage - Critical Ischemia: salvamento de la extremidad, isquemia crítica; LS: salvamento de la extremidad; PP: permeabilidad primaria; Primary Patency - Critical Ischemia: permeabilidad primaria, isquemia crítica; Secondary Patency - Critical Ischemia: permeabilidad secundaria, isquemia crítica; SP: permeabilidad secundaria; Time (years): tiempo (años). Todos los pacientes con isquemia crítica de la extremidad. Análisis de la tabla de vida de todos los pacientes (intervenciones de la arteria femoral superficial [AFS] e intervenciones adyuvantes) que presentaron ICE agrupados por una tasa de filtración glomerular estimada (TFGe)≤60 y>60ml/min/1,73cm2. Los datos son la media y el error estándar de la media y en la tabla se muestra el número en riesgo. A: permeabilidad primaria, B: permeabilidad primaria asistida, C: permeabilidad secundaria, D: salvamento de la extremidad. % Freedom: porcentaje libre de; APP: permeabilidad primaria asistida; Assisted Primary Patency - Critical Ischemia: permeabilidad secundaria, isquemia crítica; GFR: tasa de filtración glomerular; Limb Salvage - Critical Ischemia: salvamento de la extremidad, isquemia crítica; LS: salvamento de la extremidad; PP: permeabilidad primaria; Primary Patency - Critical Ischemia: permeabilidad primaria, isquemia crítica; Secondary Patency - Critical Ischemia: permeabilidad secundaria, isquemia crítica; SP: permeabilidad secundaria; Time (years): tiempo (años).](https://static.elsevier.es/multimedia/11302542/0000002300000005/v2_201308271555/S1130254209002440/v2_201308271555/es/main.assets/thumbnail/gr2.jpeg?xkr=ue/ImdikoIMrsJoerZ+w96p5LBcBpyJTqfwgorxm+Ow=)