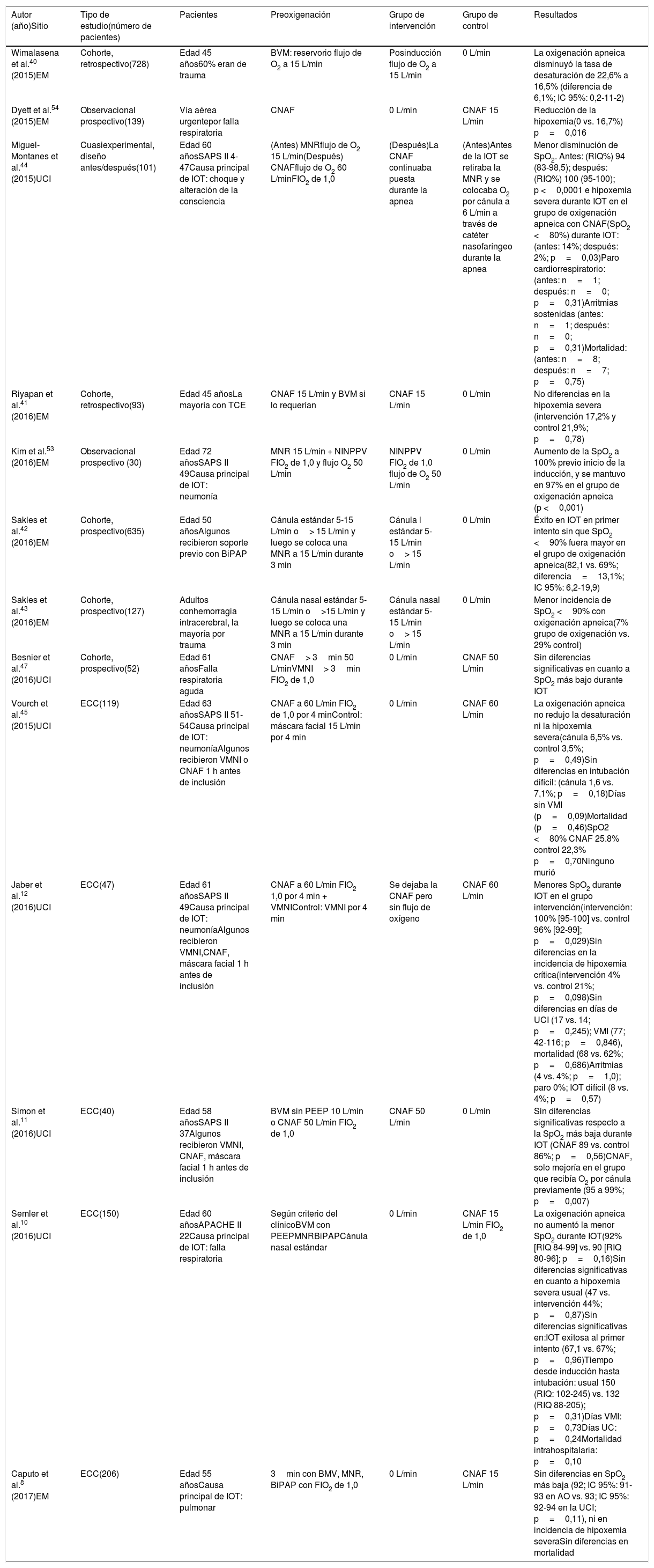
Los pacientes críticamente enfermos sufren desaturación arterial e hipoxemia durante la intubación orotraqueal más rápidamente que los pacientes sanos, lo que los pone en riesgo de inestabilidad hemodinámica y de muerte. La oxigenación apneica mejora la saturación de oxígeno y prolonga la duración de la apnea segura en anestesia; sin embargo, existe controversia sobre su efectividad en el paciente críticamente enfermo. Se realizó una revisión no sistemática de la literatura incluida en las bases de datos PubMed, EBSCO, Medline, SciELO y Scopus. Aunque desde la fisiología respiratoria esta intervención parezca una alternativa para reducir los episodios de hipoxemia grave durante la intubación, pocos estudios clínicos la respaldan. Su uso no resulta en menores tasas de desaturación crítica, de éxito de la intubación sin hipoxemia, eventos adversos, días de hospitalización ni de mortalidad. A la luz de la evidencia actual, no hay información suficiente para recomendar la oxigenación apneica durante la intubación en el paciente crítico.
Critically ill patients suffer arterial desaturation more rapidly than healthy patients during intubation and the resulting hypoxaemia has been shown to put patients at risk of haemodynamic instability and death. Apnoeic oxygenation improves oxygen saturation and prolongs the duration of safe apnoea in anaesthesia. There is controversy around its usefulness and efficiency in critically ill patients. A non-structured search was carried out in PubMed, EBSCO, Medline, SciELO, and Scopus databases. Although this intervention can be seen as an alternative method to reduce episodes of severe hypoxaemia during intubation, few clinical studies support its routine use. Apnoeic oxygenation did not lead to any differences in desaturation rates, intubation success without hypoxaemia, adverse events, days of hospital admission, and mortality. Apnoeic oxygenation in the critically ill patient did not prevent oxygen desaturation. Its routine use cannot be recommended.
Artículo
Socios de la Asociación de Medicina Crítica y Cuidado Intensivo
Para acceder a la revista
Es necesario que lo haga desde la zona privada de la web de la AMCI, clique aquí
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora