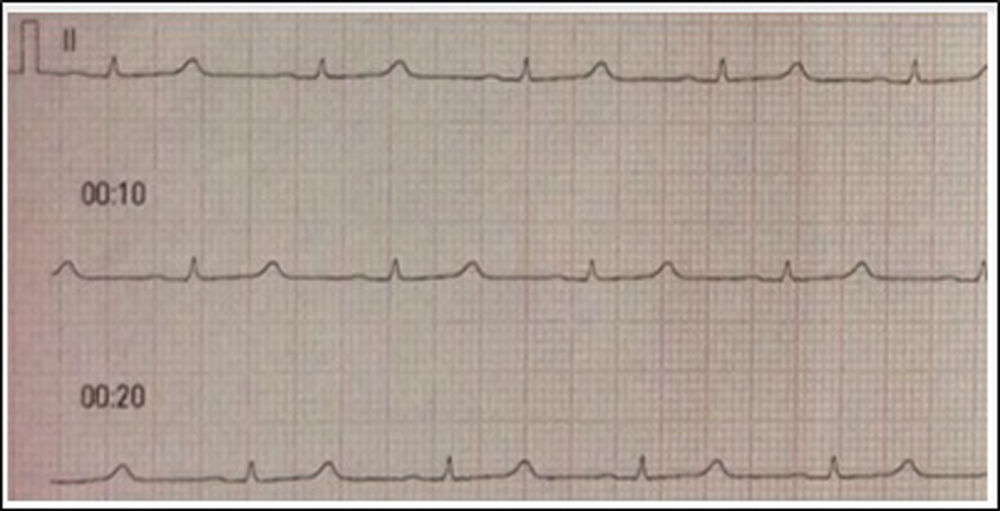
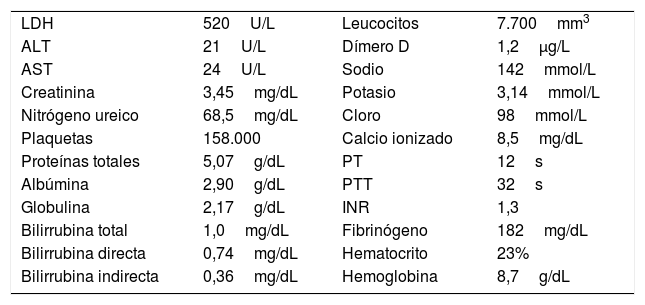
El magnesio es un ion importante en el organismo dadas las implicaciones que tiene en diversos procesos metabólicos, especialmente a nivel del sistema nervioso central y el beneficio en mejorar el flujo sanguíneo en caso de resistencia placentaria. Se ha propuesto como el agente de elección en el manejo de trastornos hipertensivos del embarazo en los que adicionalmente se busca generar efecto protector neurológico. A pesar de no ser común la toxicidad en el manejo de estas entidades, se expone a continuación un caso clínico que se manifiesta por deterioro progresivo de la función renal hasta requerir terapia de soporte, lo que hace necesario tener una adecuada vigilancia clínica durante su administración.
Magnesium is an ion with great importance in the organism, given the involvement it has in various metabolic processes, especially at the level of the central nervous system and a certain benefit in improving blood flow in case of placental resistance. It has been proposed as the agent of choice in the management of hypertension disorders during pregnancy in which an additional neurological protective effect is sought. Although the rates of complications in the management of these diseases are low, a clinical case is presented of a patient with progressive acute renal failure who required support therapy. Close monitoring was necessary during its administration.
Artículo
Socios de la Asociación de Medicina Crítica y Cuidado Intensivo
Para acceder a la revista
Es necesario que lo haga desde la zona privada de la web de la AMCI, clique aquí
Comprando el artículo el PDF del mismo podrá ser descargado
Precio 19,34 €
Comprar ahora