Una nueva pandemia fue declarada por la Organización Mundial de la Salud por el virus SARS-CoV-2 recientemente. Este virus se caracteriza por ser altamente transmisible, letal y afectar a todos los grupos etarios. Esta declaración permitió la activación en todos los países de mecanismos de urgencia para atender esta crisis de salud pública que ha expuesto las debilidades de los sistemas de salud y el déficit de camas de cuidado intensivo adulto (UCIA) y pediátrico (UCIP). Colombia tiene un número reducido de camas de UCIP con respecto a otros países de medianos y bajos ingresos. Por esta razón, debemos optimizar los recursos, anticiparse a los casos graves y conocer el comportamiento de la enfermedad por el virus del SARS-CoV-2 (llamada COVID-19) en pediatría, especialmente en las formas severas de presentación en niños.
La severidad y grado de afectación por el virus en todos los países ha sido muy similar con una mayor gravedad y frecuencia de infección en la población adulta, particularmente en personas mayores de 60 años y con comorbilidades (obesidad, hipertensión, diabetes, entre otros). No obstante, también se ha registrado en la población pediátrica casos graves que requieren intervenciones avanzadas en terapia intensiva, incluyendo una forma de presentación con gran respuesta inflamatoria en niños denominada síndrome inflamatorio multisistémico (MIS-C por sus siglas en inglés).
La Asociación Colombiana de Medicina crítica y Cuidados Intensivos (AMCI) convocó un equipo multidisciplinario de expertos en medicina crítica pediátrica para establecer una declaratoria de consenso de buena práctica clínica para la atención de niños con COVID-19 grave que requieran atención en cuidado intermedio o cuidado intensivo pediátrico.
El objetivo de esta declaración de consenso es facilitar y estandarizar la toma de decisiones en los aspectos más relevantes en la atención y realizar un abordaje integral del paciente pediátrico basado en la mejor evidencia disponible y opinión de expertos en cuidado intensivo pediátrico de al menos 10 años de experiencia de trabajo en el área. Adicionalmente, se buscó involucrar a aquellos intensivistas pediatras que deben hacer atención directa de los niños con COVID-19, pertenecen a hospitales de referencia o universitarios y tienen demostrada trayectoria en investigación y docencia en cuidado crítico pediátrico. Esta declaración de consenso se buscará actualizar con la frecuencia que sea necesaria de acuerdo con el cambio de la mejor evidencia disponible, que les permita a los médicos que atienden niños críticos con COVID-19 realizar una atención integral y adecuada acorde con la mejor literatura disponible.
A new pandemic was recently declared by the World Health Organisation due to the SARS-CoV-2 virus. This virus is characterised by being highly transmissible, lethal, and affecting all age groups. This declaration led to the activation, in all countries, of emergency mechanisms to deal with this public health crisis that has exposed the weaknesses of the health systems and the deficit of beds in adult intensive care (UCIA) and paediatric intensive care units (PICU). Colombia has a reduced number of PICU beds compared to other low- and middle-income countries. For this reason, we must optimise resources, anticipate severe cases, and understand the behaviour of the disease caused by the SARS-CoV-2 virus (called COVID-19) in paediatrics, especially in severe forms of presentation in children.
The severity and degree of involvement by the virus in all countries has been very similar, with a greater severity and frequency of infection in the adult population, particularly in people over 60 years of age, and with comorbidities (obesity, hypertension, diabetes, among others). However, severe cases requiring advanced interventions in intensive care have also been reported in the paediatric population, including a form of presentation with a large inflammatory response in children, called multi-systemic inflammatory syndrome (MIS-C).
The Colombian Association of Critical Medicine and Intensive Care (AMCI) convened a multidisciplinary team of experts in paediatric critical medicine to establish a consensus statement of good clinical practice for the care of children with severe COVID-19 requiring care in intermediate care or paediatric intensive care.
The objective of this consensus statement is to facilitate and standardise decision making in the most relevant aspects of care and to carry out a comprehensive approach to the paediatric patient based on the best available evidence and the opinion of experts in paediatric intensive care with at least 10 years of work experience in the area. Additionally, it was sought to involve those Paediatric Intensivists who have to directly care for children with COVID-19, and belong to reference or university hospitals and have a proven track record in research and teaching in paediatric critical care. This consensus statement will seek to update, as often as necessary, according to the change in the best available evidence, which will enable physicians who care for critical children with COVID-19 to provide comprehensive and adequate care according to the best available literature.
La infección por el virus del coronavirus grave del síndrome respiratorio agudo 2 (severe acute respiratory syndrome coronavirus2 [SARS-CoV-2]) es la última pandemia declarada por la Organización Mundial de la Salud (OMS,) que ha afectado a la mayoría de los países en el mundo. Se reconoció por primera vez en diciembre del 2019 en Wuhan, China. En ese país, en la primera fase llegó a afectar más de 80.000 personas y se ha diseminado por todo el mundo afectando a millones de personas. La OMS recomienda implementar estrategias de detección temprana de la infección, fomentar las medidas de aislamiento de los casos confirmados y fortalecer los sistemas de salud para una atención rápida y oportuna de los casos más graves. A medida que esta infección evoluciona, 245 países en el mundo han reportado casos positivos, con tasas de mortalidad que oscilan entre el 4 y el 11%, particularmente en la población adulta. En niños, el curso clínico de la enfermedad suele ser menos grave. En una revisión sistemática de la COVID-19 en 7.780 niños publicada recientemente, incluyendo 131 estudios en más de 26 países, se describe que la enfermedad, en el 80% de los casos, suele cursar sin síntomas o síntomas leves en pediatría. En el 20% restante ocurren casos de moderados a graves, requiriendo hospitalización en terapia intensiva entre el 5 y el 10% de los casos y con una mortalidad en niños que puede oscilar entre el 1 y el 3% de todos los casos.
Para el desarrollo de este consenso, la AMCI, en su capítulo de pediatría, ha convocado a un grupo de trabajo conformado por intensivistas pediatras, epidemiólogos y bioeticistas para el desarrollo de tópicos relevantes de la enfermedad en pacientes con sospecha o infección confirmada por COVID-19. El grupo desarrollador (anexo 1) buscó involucrar especialistas en Cuidado Intensivo Pediátrico con amplia experiencia y trayectoria en el área e investigación y que adicionalmente realicen atención directa de pacientes con COVID-19 en hospitales de referencia o universitarios. Consideramos que el intensivista pediatra, al pertenecer al grupo de especialistas de primera línea en la atención de estos pacientes, puede compartir su experiencia en aquellos tópicos pediátricos en los que la evidencia no existe o está en construcción. El objetivo de esta declaración de consenso es generar sugerencias de manejo del niño crítico con COVID-19 basado en la mejor evidencia científica disponible, recopilada y analizada por expertos en medicina crítica pediátrica. Las sugerencias de este capítulo pediátrico de la AMCI se formulan en calidad de expertos por las razones expuestas, como puntos de buena práctica y deben ser actualizadas en la medida que se publique literatura de buena calidad que generen un cambio importante en la práctica clínica de la atención de niños críticos con infección por SARS-CoV-2.
MetodologíaSe desarrolló un consenso mediante técnica formal basado específicamente en la estrategia Delphi modificada. El grupo desarrollador seleccionó 6 tópicos de relevancia para que fuera revisado por los expertos en Cuidado Intensivo Pediátrico. Se establecieron preguntas con la estrategia PICOT acerca de los temas más relevantes en el ámbito de la atención en cuidado intensivo y de parte del equipo desarrollador se les pidió a los expertos que revisaran el tema con la mejor evidencia disponible y generaran sugerencias de manejo en cada tópico. Estas revisiones se basaron en la literatura más recientes de la COVID-19, que incluyó búsquedas no sistemáticas, literatura sugerida por expertos en cuidado intensivo adulto, pediátrico y otras disciplinas, así como estrategia de bola de nieve. Se complemento con el anexo 2 de las estrategias sugeridas por la AMCI de prevención de infecciones intrahospitalarias por COVID-19.
Considerando la multidimensionalidad del espectro de la enfermedad COVID-19 y la escasa información de alta calidad metodológica, se prefirió la metodología de consenso para establecer acuerdo entre expertos en medicina crítica pediátrica del país y emitir un juicio responsable, como sugerencias de buena práctica clínica, para no forzar decisiones rígidas a los usuarios del consenso.
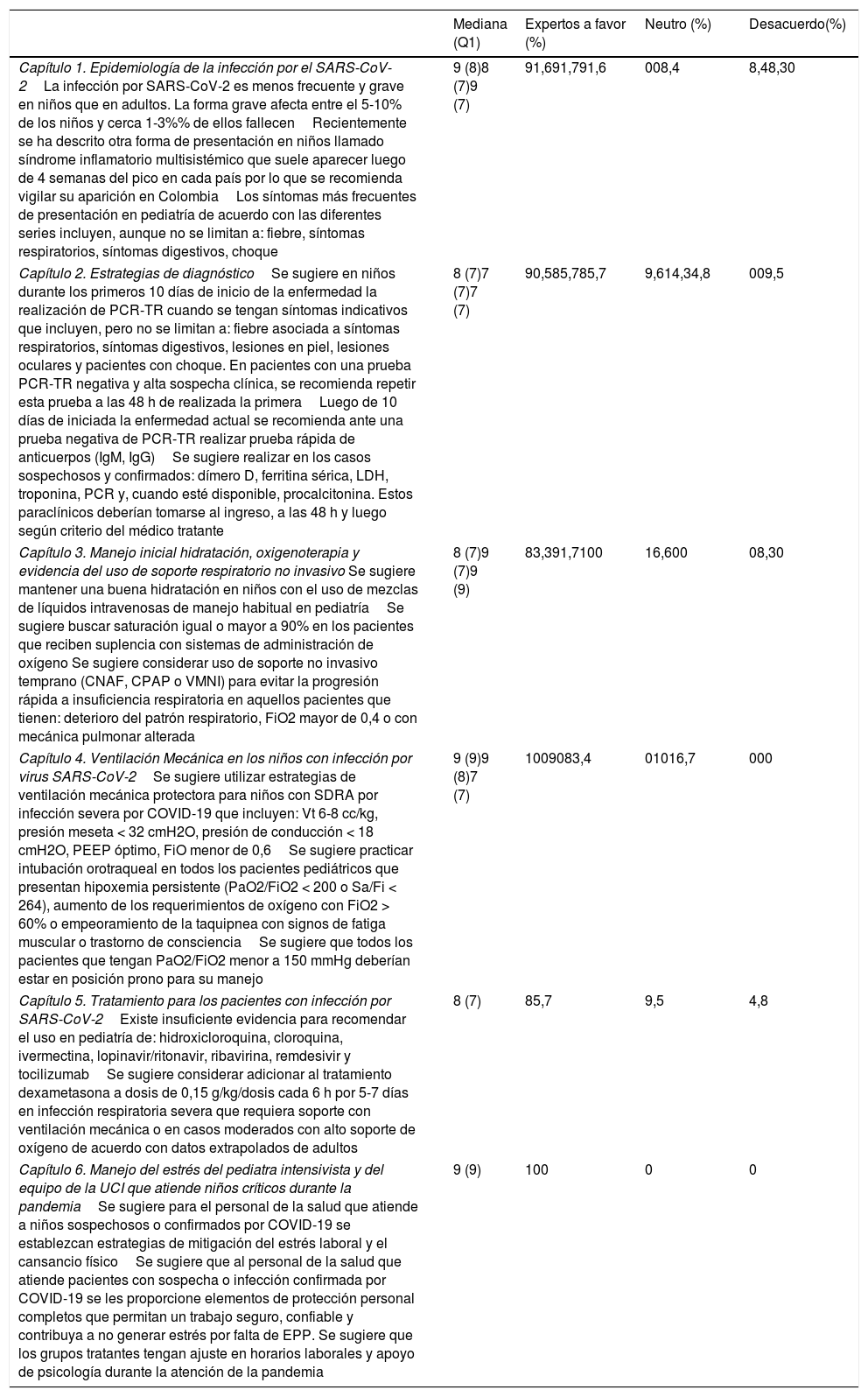
Se pidió a cada persona o grupo seleccionada por tópico específico que realizara la revisión de la literatura y emitiera recomendaciones que luego fueron sometidas con el método Delphi modificado a consenso entre todos los participantes. Cada tema fue enviado por vía electrónica a los expertos, respetando la disposición de la cuarentena nacional como medida de control de la enfermedad. Los capítulos fueron calificados en una escala ordinal de aceptación y el asesor metodológico se aseguró de revisar estas votaciones y clasificarlas. Se utilizó la escala de Likert (1-3 desacuerdo total, 4-6 acuerdo relativo, 7-9 acuerdo total), considerando que la mediana estaba incluida dentro del rango. En caso de no existir un mínimo de un 80% de acuerdo en la primera votación electrónica, se estableció un mecanismo de retroalimentación, con el cual se ajustó el texto en su versión final. En la primera ronda de preguntas se alcanzó el valor mínimo planteado en 9 de las 11 preguntas, por lo que se hizo una segunda ronda de preguntas en aquellos ítems en los que no se obtuvo consenso en la ronda precedente. Se realizó una reunión con los expertos participantes de manera virtual, el día 3 de julio del 2020, en la que se realizó votación de la pregunta que no superó el umbral de consenso y se llegó a un acuerdo. Se definió consenso en las recomendaciones si se cumplía por lo menos uno de 2criterios: que se alcanzara al menos el 80% de las respuestas de los panelistas en la región de acuerdo o desacuerdo, o que el análisis estadístico de las respuestas revelara que la mediana de las calificaciones (el valor que divide al 50% por arriba y por abajo las respuestas) y el cuartil 1 (Q1: el valor por encima del cual están el 75% de los datos) se encontraban en la región de acuerdo. En el documento final se incluyeron sugerencias adicionales por el grupo desarrollador, calificadas como buena práctica clínica, relacionadas con algunos temas de vital importancia no escogidos en la fase inicial de preguntas. En la tabla 1 se presenta el resumen de las sugerencias.
Resumen de las sugerencias
| Mediana (Q1) | Expertos a favor (%) | Neutro (%) | Desacuerdo(%) | |
|---|---|---|---|---|
| Capítulo 1. Epidemiología de la infección por el SARS-CoV-2La infección por SARS-CoV-2 es menos frecuente y grave en niños que en adultos. La forma grave afecta entre el 5-10% de los niños y cerca 1-3%% de ellos fallecenRecientemente se ha descrito otra forma de presentación en niños llamado síndrome inflamatorio multisistémico que suele aparecer luego de 4 semanas del pico en cada país por lo que se recomienda vigilar su aparición en ColombiaLos síntomas más frecuentes de presentación en pediatría de acuerdo con las diferentes series incluyen, aunque no se limitan a: fiebre, síntomas respiratorios, síntomas digestivos, choque | 9 (8)8 (7)9 (7) | 91,691,791,6 | 008,4 | 8,48,30 |
| Capítulo 2. Estrategias de diagnósticoSe sugiere en niños durante los primeros 10 días de inicio de la enfermedad la realización de PCR-TR cuando se tengan síntomas indicativos que incluyen, pero no se limitan a: fiebre asociada a síntomas respiratorios, síntomas digestivos, lesiones en piel, lesiones oculares y pacientes con choque. En pacientes con una prueba PCR-TR negativa y alta sospecha clínica, se recomienda repetir esta prueba a las 48 h de realizada la primeraLuego de 10 días de iniciada la enfermedad actual se recomienda ante una prueba negativa de PCR-TR realizar prueba rápida de anticuerpos (IgM, IgG)Se sugiere realizar en los casos sospechosos y confirmados: dímero D, ferritina sérica, LDH, troponina, PCR y, cuando esté disponible, procalcitonina. Estos paraclínicos deberían tomarse al ingreso, a las 48 h y luego según criterio del médico tratante | 8 (7)7 (7)7 (7) | 90,585,785,7 | 9,614,34,8 | 009,5 |
| Capítulo 3. Manejo inicial hidratación, oxigenoterapia y evidencia del uso de soporte respiratorio no invasivo Se sugiere mantener una buena hidratación en niños con el uso de mezclas de líquidos intravenosas de manejo habitual en pediatríaSe sugiere buscar saturación igual o mayor a 90% en los pacientes que reciben suplencia con sistemas de administración de oxígeno Se sugiere considerar uso de soporte no invasivo temprano (CNAF, CPAP o VMNI) para evitar la progresión rápida a insuficiencia respiratoria en aquellos pacientes que tienen: deterioro del patrón respiratorio, FiO2 mayor de 0,4 o con mecánica pulmonar alterada | 8 (7)9 (7)9 (9) | 83,391,7100 | 16,600 | 08,30 |
| Capítulo 4. Ventilación Mecánica en los niños con infección por virus SARS-CoV-2Se sugiere utilizar estrategias de ventilación mecánica protectora para niños con SDRA por infección severa por COVID-19 que incluyen: Vt 6-8 cc/kg, presión meseta < 32 cmH2O, presión de conducción < 18 cmH2O, PEEP óptimo, FiO menor de 0,6Se sugiere practicar intubación orotraqueal en todos los pacientes pediátricos que presentan hipoxemia persistente (PaO2/FiO2 < 200 o Sa/Fi < 264), aumento de los requerimientos de oxígeno con FiO2 > 60% o empeoramiento de la taquipnea con signos de fatiga muscular o trastorno de conscienciaSe sugiere que todos los pacientes que tengan PaO2/FiO2 menor a 150 mmHg deberían estar en posición prono para su manejo | 9 (9)9 (8)7 (7) | 1009083,4 | 01016,7 | 000 |
| Capítulo 5. Tratamiento para los pacientes con infección por SARS-CoV-2Existe insuficiente evidencia para recomendar el uso en pediatría de: hidroxicloroquina, cloroquina, ivermectina, lopinavir/ritonavir, ribavirina, remdesivir y tocilizumabSe sugiere considerar adicionar al tratamiento dexametasona a dosis de 0,15 g/kg/dosis cada 6 h por 5-7 días en infección respiratoria severa que requiera soporte con ventilación mecánica o en casos moderados con alto soporte de oxígeno de acuerdo con datos extrapolados de adultos | 8 (7) | 85,7 | 9,5 | 4,8 |
| Capítulo 6. Manejo del estrés del pediatra intensivista y del equipo de la UCI que atiende niños críticos durante la pandemiaSe sugiere para el personal de la salud que atiende a niños sospechosos o confirmados por COVID-19 se establezcan estrategias de mitigación del estrés laboral y el cansancio físicoSe sugiere que al personal de la salud que atiende pacientes con sospecha o infección confirmada por COVID-19 se les proporcione elementos de protección personal completos que permitan un trabajo seguro, confiable y contribuya a no generar estrés por falta de EPP. Se sugiere que los grupos tratantes tengan ajuste en horarios laborales y apoyo de psicología durante la atención de la pandemia | 9 (9) | 100 | 0 | 0 |
- 1.
Considerar que la infección por el SARS-CoV-2 es menos frecuente y grave en niños que en adultos. La forma grave afecta entre el 5-10% de los niños y cerca del 1-3%% de ellos fallecen.
- 2.
Recientemente se ha descrito otra forma de presentación en niños llamado síndrome inflamatorio multisistémico (MIS-C) que suele aparecer luego de 4 semanas del pico en cada país, por lo que se recomienda vigilar su aparición en Colombia.
- 3.
Los síntomas más frecuentes de presentación en pediatría, de acuerdo con las diferentes series, incluyen aunque no se limitan a: fiebre, síntomas respiratorios, síntomas digestivos, choque.
El coronavirus es uno de los principales patógenos que afectan al sistema respiratorio humano. Los brotes anteriores de coronavirus incluyen el síndrome respiratorio agudo grave (SARS-CoV) en el 2003 y el síndrome respiratorio de Oriente Medio (MERS-CoV) en el 2012, que representaron una verdadera amenaza para la salud pública de la población afectada1.
A finales de diciembre del 2019, en la ciudad de Wuhan, provincia de Hubei, China, 5 pacientes fueron hospitalizados con un diagnóstico inicial de neumonía de etiología desconocida; evolucionaron a síndrome de dificultad respiratoria aguda y uno de estos pacientes murió2. Estos pacientes estaban vinculados epidemiológicamente a un mercado mayorista de mariscos y animales húmedos.
China había reorganizado su plan de salud a raíz de la epidemia de MERS en 2012, estableció un nuevo servicio basado en la web para alarmar rápidamente en caso de una enfermedad emergente de origen desconocido a través de un sistema de vigilancia común, lo que permitió la caracterización del brote y el 30 de enero del 2020 la OMS emitió una alerta mundial de salud pública sobre la aparición de una nueva enfermedad viral epidémica3.
El agente etiológico de la COVID-19ha sido confirmado como un nuevo coronavirus, ahora conocido como SARS-CoV-2. El análisis del genoma viral ha revelado que el nuevo coronavirus está filogenéticamente cerca del SARS-CoV, el agente causal del brote viral en 2003.
En las primeras etapas de la propagación global de la COVID-19, los casos identificados fuera de China fueron en su mayoría viajeros que se infectaron en ese país y luego viajaron a zonas cercanas con un número de casos de infección relativa 10 veces mayor que para el SARS-CoV o MERS-CoV.
Este nuevo SARS-CoV-2 ha causado una de las peores pandemias de la humanidad (245 países con casos confirmados). Las formas graves representan el 14% de los casos notificados y se estima que el número reproductivo básico de esta infección es de 2,2 (IC del 95%, 1,43,9).
Los pacientes pediátricos menores de 18 años han representado un número mucho menor de los casos confirmados en las series descritas4. En Italia, los casos de COVID-19 en la cohorte pediátrica (0-18 años) representan solo el 1,2%3. En Corea, los niños menores de 19 años fueron el 4,8%.
En Colombia, hasta el 26 de junio se han reportado 7.380 casos confirmados en menores de 18 años, que representan el 8,7% de los casos totales del país.
En un estudio que describe la presentación de la enfermedad entre los niños en China se incluyeron series de casos nacionales de 2.135 pacientes pediátricos con COVID-19 reportados al Centro Chino para el Control y la Prevención de Enfermedades desde el 16 de enero del 2020 hasta el 8 de febrero del 2020, y estos resultados sugieren que los niños pequeños, en particular los lactantes, eran los más vulnerables. Las proporciones de casos graves y críticos fueron del 10,6, el 7,3, el 4,2, el 4,1 y el 3,0% para los grupos de edad menores de 1 año, de 1 a 5 años, 6 a 10 años, de 11 a 15 años, y 16 años, respectivamente. No se observó ninguna diferencia significativa de sexo en este estudio5.
La evidencia sugiere que, en comparación con pacientes adultos, las manifestaciones clínicas de la COVID-19 en pacientes pediátricos son menos graves, observándose hasta ahora que más del 90% de todos los pacientes tienen casos asintomáticos, leves o moderados y la población menor de un año es la que ha registrado la mayor probabilidad de desarrollar enfermedad severa.
Los síntomas más comunes son fiebre, fatiga y tos, y en menor frecuencia congestión y secreción nasal, expectoración, diarrea, dolor de cabeza. La disnea, la cianosis y otros síntomas pueden ocurrir a medida que la afección progresa, generalmente después de una semana de la enfermedad, acompañada de síntomas tóxicos sistémicos. Algunos niños pueden progresar rápidamente hasta insuficiencia respiratoria que no puede ser corregida con oxígeno convencional (catéter nasal, máscara). Los casos graves pueden llevar a choque y disfunción multiorgánica. trastornos de la coagulación, daño miocárdico con insuficiencia cardíaca en casos graves, disfunción gastrointestinal, nivel elevado de enzimas hepáticas, ferritina y rabdomiólisis6.
Otra forma de presentación en niños es el llamado MIS-C, que suele aparecer luego de 4 semanas del pico en cada país y en el que los pacientes tienen manifestaciones como lesiones en la piel, lesiones oculares e inicio con estado de choque. No se conoce la etiología, pero fue inicialmente descrito en algunos países europeos y posteriormente en EE. UU. El curso clínico suele ser adecuado con una mortalidad reportada que oscila entre el 1-2% de los casos afectados6.
Capítulo 2. Estrategias de diagnósticoSe sugiere- 1.
Se sugiere en niños, durante los primeros 10 días de inicio de la enfermedad, la realización de PCR-TR cuando se tengan síntomas indicativos que incluyen pero no se limitan a: fiebre asociada a síntomas respiratorios, síntomas digestivos, lesiones en piel, lesiones oculares y pacientes con choque.
- 2.
Luego de 10 días de iniciada la enfermedad actual, se sugiere ante una prueba negativa de PCR-TR realizar prueba rápida de anticuerpos (IgM, IgG).
- 3.
En pacientes con una prueba PCR-TR negativa y alta sospecha clínica, se sugiere repetir esta prueba a las 48 h de realizada la primera.
- 4.
Se sugiere realizar, en los casos sospechosos y confirmados, dímero D, ferritina sérica, LDH, troponina, PCR y, cuando esté disponible, procalcitonina. Estos paraclínicos deberían tomarse al ingreso, a las 48h y luego según criterio del médico tratante.
En Colombia, el 6 de marzo del 2020 se confirmó el primer caso de SARS-CoV-2 y para el 25 de junio ya se habían diagnosticado 84.442 casos y 2.811 muertes7. En los primeros días de la epidemia, los pacientes pediátricos eran poco comunes; sin embargo, a medida que más porcentaje de la población se ha contagiado los casos pediátricos han aumentado.
El diagnóstico de SARS-CoV-2 se basa en la prueba de detección de ácidos nucleicos por PCR; este tipo de pruebas es el recomendado por la OMS por tener alta sensibilidad y especificidad8. Sin embargo, aun en nuestro país, la capacidad técnica para la realización de dichas pruebas es insuficiente, lo que impide el manejo adecuado de las medidas de salud pública.
En Colombia, la circular externa 19 del Ministerio de Salud, publicada el 25 de marzo del 2020 autoriza, en el momento de su disponibilidad, el uso de pruebas rápidas con base en identificación de anticuerpos como pruebas de detección para lograr optimizar los recursos, definir el cerco epidemiológico, la toma de decisiones de aislamiento y la realización de pruebas confirmatorias. A la fecha, 7 kits de pruebas rápidas han sido aprobados por el INVIMA para el diagnóstico de infección por SARS-CoV-2 (tabla 2).
Pruebas rápidas que han sido aprobados por el INVIMA para el diagnóstico de infección por SARS-CoV-2 al 17 de abril del 2020
| Nombre | Registro sanitario | Marca |
|---|---|---|
| COVID-19 IgG/IgM rapid test cassette | INVIMA 2020rd-0006129 | Lumira S.A.S. |
| COVID-19 IgG/IgM cassette (lineal) | INVIMA 2020rd-0006125 | Labtronics S.A.S. |
| Standard q COVID-19 IgG/IgM duo | INVIMA 2020rd-0006126 | Annar Diagnóstica Import S.A.S. |
| Basepoint COVID-19 IgG/IgM rapid test device venous whole blood/fingerstick whole blood/serum/plasma | INVIMA 2020rd-0006128 | Alere Colombia S.A. |
| SARS-COV-2 antibody test (lateral flow method) | INVIMA 2020rd-0006124 | Lumira S.A.S |
| SARS-COV-2 IgG/IgM antibody rapid test | INVIMA 2020rd-0006119 | Labtronics S.A.S. |
| Amp rapid test SARS- COV-2 IgG/IgM | INVIMA 2020rd-0006117 | Biometrika Laboratorio S.A.S. |
Las pruebas rápidas se basan en la detección de anticuerpos tipo IgM e IgG por técnicas de inmunocromatografía, inmunoanálisis, quimioluminiscencia y orocoloidal que, en general, tienen un buen valor predictivo positivo dado la prevalencia actual de la enfermedad, por lo que permiten indicar si una persona ha estado expuesta al SARS-CoV-29-11. Estas pruebas tienen la ventaja de tener un tiempo de ejecución corto y requerir un equipamiento mínimo, por lo que permiten realizarse fuera de un laboratorio10.
La principal utilidad de aplicación de estas pruebas es para el cribado de poblaciones que hayan estado expuestas a personas con SARS-CoV-2 confirmado8, o para casos asintomáticos o con síntomas leves de más de 10 días de evolución12,13, permitiendo la evaluación retrospectiva de la extensión del brote. El ministerio, en el lineamiento para el uso de pruebas diagnósticas de laboratorio durante la pandemia del SARS-CoV-2, propone el uso de estas para realizar estudios de vigilancia epidemiológica o para inferir la seroprevalencia en un sitio o área determinada, incluyendo cribado a los trabajadores de la salud que se encuentran en los servicios de urgencias, hospitalización y UCI con pabellones de pacientes con COVID-1914.
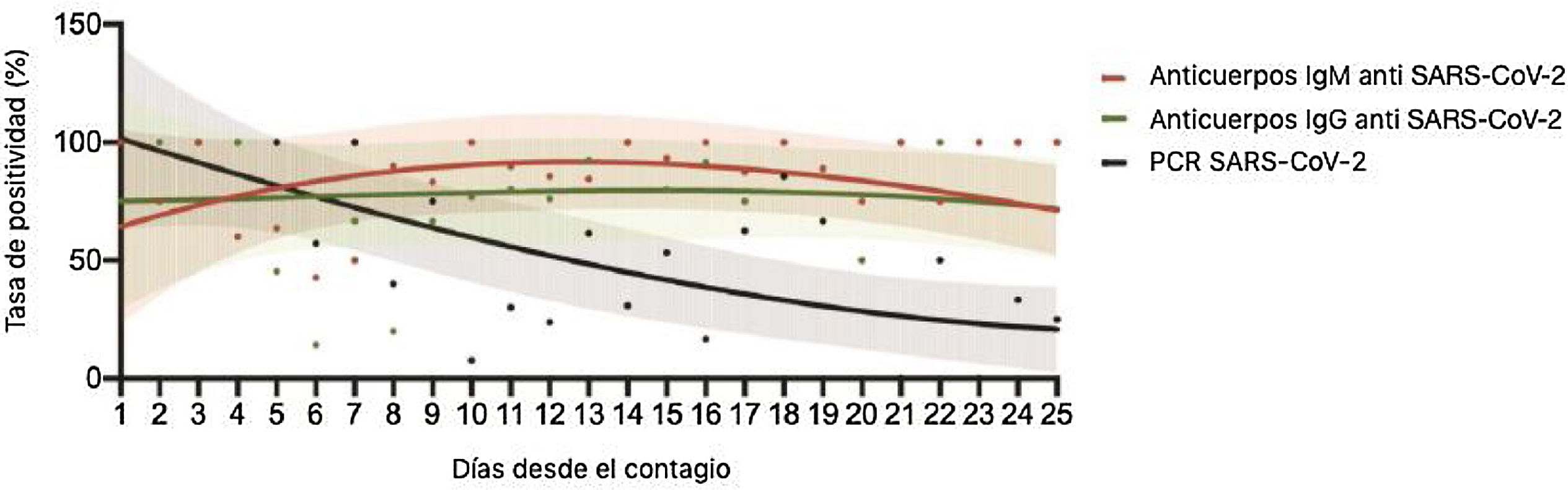
Se ha visto que, pasados los primeros días de la infección, la positividad de las pruebas moleculares por PCR comienza a disminuir12,15. En estos casos, el uso de las pruebas serológicas aumenta la tasa de detección de la infección por SARS-CoV-2 (fig. 1).
Curva ajustada de detección positiva por PCR y ELISA IgG e IgM en diferentes días después del inicio de los síntomas.
Tomado y modificado de Guo et al.15.
En el estudio de Zhao et al., que incluyó a 173 pacientes positivos para SARS-CoV-2, la detección por PCR se disminuyó al 66,7% luego de una semana de evolución y la seroconversión fue del 93,1% para IgM y del 64,7% para IgG12. En el estudio de Guo et al., los anticuerpos IgM tuvieron su mayor positividad entre los días 8-14 y los IgG entre los días 8 y 21; la detección de SARS-CoV-2 por PCR fue del 51,9% que se aumentó al 98,6% cuando se combinó con la detección de anticuerpos IgM específicos, incluso la positividad de la IgM en dicho estudio fue del 75,6% en los pacientes con SARS-CoV-2 confirmados (62/82 pacientes) y del 93,1% en los SARS-CoV-2 posibles (54/58 pacientes)15, siendo así una ayuda útil para la búsqueda epidemiológica de sitios de transmisión de la infección por SARS-CoV-2; sin embargo, hay que tener en cuenta que previamente se ha reportado reactividad cruzada entre distintos coronavirus16, lo que pudiera también presentarse con el nuevo coronavirus SARS-CoV-215.
Aunque el surgimiento de estas pruebas ha sido acelerado y no han habido suficientes estudios para la estandarización de los mismos, dada la utilidad clínica potencial de las pruebas rápidas, se recomienda entonces el uso de pruebas rápidas de detección de anticuerpos (altamente sensibles) en combinación con pruebas de identificación molecular PCR (altamente específicas) para mejorar el cribado de SARS-CoV-2 y el seguimiento epidemiológico de la seroconversión en poblaciones de interés, en el caso de UCIP, pacientes sospechosos con prueba de PCR para SARS-CoV-2 negativa o pacientes con otras enfermedades a quienes no se les conozca el estatus de infección y sean asintomáticos respiratorios para guiar estrategias de aislamiento y estudio de convivientes, siempre y cuando los estudios con los que se desarrollaron dichas pruebas estén disponibles para el personal sanitario y en estos se evidencie que se trata de pruebas con buen rendimiento diagnóstico.
Adicionalmente, en los pacientes sospechosos o confirmados que suelen cursar con tormenta de citocinas, se recomienda realizar estudios que evalúen el estado inflamatorio del paciente17. En este sentido, se ha encontrado que los pacientes que tienen infección por SARS-CoV-2 tienen elevada proteína C reactiva como manifestación de activación de inmunidad innata. Esta proteína se produce a nivel hepático y en adipocitos por estímulo de interleucina (IL)-1 y 6, y factor de necrosis tumoral alfa. Igualmente, se ha encontrado elevada la ferritina sérica como manifestación de inflamación sistémica y muerte celular regulada con patrón piroptosis. Los estudios han encontrado que niveles mayores de 500 mg/dl se asocian a peores desenlaces. En este sentido, la elevación del dímero D sugiere un estado procoagulante y antifibrinolítico, y en los pacientes con peores desenlaces se ha encontrado elevado en niños.
Capítulo 3. Manejo inicial: hidratación, oxigenoterapia y evidencia del uso de cánula de alto flujoSe sugiere- 1.
Mantener una buena hidratación en niños con el uso de mezclas de líquidos intravenosas de manejo habitual en pediatría.
- 2.
Se sugiere buscar saturación igual o mayor al 90% en los pacientes que reciben suplencia con sistemas de administración de oxígeno.
- 3.
Se sugiere considerar uso de soporte no invasivo temprano (CNAF, CPAP o ventilación mecánica no invasiva [VMNI]) para evitar la progresión rápida a insuficiencia respiratoria en aquellos pacientes que tienen: deterioro del patrón respiratorio, FiO2 mayor a 0,4 o con mecánica pulmonar alterada.
El paciente pediátrico que ingresa en la Unidad de Cuidado Intensivo es aquel en el cual los cuidados generales y el oxígeno suplementario a bajo flujo (CN convencional) ha fracasado y presenta signos diversos: 1) a nivel respiratorio, aumento del trabajo de este y agudización de la hipoxemia; 2) a nivel cardiovascular, signos de alteración en la perfusión, y 3) compromiso multiorgánico o evidencia de factores bioquímicos de riesgo. Se inicia con una valoración detallada por sistemas, y se debe clasificar su estado hemodinámico, de hidratación, trabajo respiratorio, SatO2, FiO2, Sa/Fi, que está recibiendo a su ingreso, para determinar las primeras medidas terapéuticas18. Aunque, como es bien sabido, una gran proporción de los menores de edad infectados por el virus cursan de manera asintomática, el porcentaje que manifiesta sintomatología presenta varios factores que pueden llevar a la deshidratación y al compromiso hemodinámico. Entre estos factores se encuentran el aumento del trabajo respiratorio, la disminución de la aceptación de la vía oral, las manifestaciones gastrointestinales, tales como diarrea, y compromiso de la resistencia vascular periférica y de la función miocárdica. Por lo tanto, una adecuada valoración del estado de hidratación y perfusión del paciente permitirá un manejo ajustado a las necesidades del menor. Se debe calcular el déficit de deshidratación y definir su reposición de manera lenta con los líquidos recomendados para su grupo etario.
En esta condición patológica, se considera un manejo conservador de los fluidos, teniendo como premisa evitar la sobrecarga hídrica, que podría empeorar la hipoxemia propia de la enfermedad. Los líquidos por vía intravenosa recomendables para tal fin son los de características isotónicas. En caso de requerir reanimación hídrica, se preferirán los líquidos balanceados con su respectiva administración cautelosa. Para definir el volumen de los líquidos de mantenimiento o basales se recomienda el entre el 80 y el 100% de los calculados por la fórmula de Holliday-Segar si no hay signos de choque. El tipo de líquidos intravenosos a usar para los aportes basales será acorde con el grupo etario y la concentración sérica de cloro en los casos en que esté disponible sus niveles séricos.
Cuando consideramos el manejo del componente respiratorio propiamente dicho, debemos tener en cuenta el grado de dificultad respiratoria, la SatO2, la FiO2 con el que ingresa y la Sa/Fi calculada. De igual manera, su estado hemodinámico y neurológico, la presencia marcada o no de componente hipercápnico y el compromiso multiorgánico. De estar presentes un síndrome de dificultad respiratoria severo, inestabilidad hemodinámica, estado neurológico alterado, falla respiratoria de componente hipercápnico marcado o predominante y disfunción orgánica múltiple, se debe considerar la intubación orotraqueal sin retrasos. Si el paciente cumple criterios para síndrome de dificultad respiratoria leve a moderado, se propone optar por CNAF/CPAP19 como una medida que intente evitar la intubación y aprovechar sus beneficios sobre las características de la mecánica respiratoria de los niños: O2 entregado húmedo y caliente, FiO2 programable, satisfaciendo la demanda inspiratoria del paciente, mejorando la oxigenación, disminuyendo el drive respiratorio, un lavado de CO2, favoreciendo la función mucociliar, efecto de presión dinámica constante en la vía aérea y es una interfase mucho más cómoda. De tal manera que podría llegar a disminuir el trabajo respiratorio, la asincronía toracoabdominal y el estado clínico del paciente. Requiere monitorización estrecha; se plantea una primera reevaluación a los 20 min. Es recomendable colocar una mascarilla quirúrgica a los niños que se les coloca CNAF o CPAP con el ánimo de limitar la difusión de aerosoles, especialmente si no se cuenta con unidades o cubículos con presión negativa20. Podría considerarse una adecuada respuesta el tener: una disminución del trabajo respiratorio, lograr SatO2 > 93%, mejoría de la Sa/Fi, la frecuencia respiratoria, la frecuencia cardíaca, persistencia de estabilidad hemodinámica y neurológica. Si este tipo de respuesta está presente, se debe continuar con esta estrategia y revaloraciones cada 30min y de no ser adecuada alguna de ellas, pasar de inmediato a intubación orotraqueal.
Si la primera revaloración a los 20min de inicio el manejo con CNAF/CPAP no fue adecuada, especialmente en términos de mejoría de la hipoxemia y el trabajo respiratorio, pero persiste con estabilidad hemodinámica y neurológica, se debe adicionar la posición prona; si no se logra por poca aceptación del paciente no debe retrasarse la intubación orotraqueal. Si el paciente tolera y colabora en esta posición, se realiza revaloración a los 20min; de tener adecuada respuesta, se debe continuar con las revaluaciones constantes cada 30min y de no tener adecuada respuesta, realizar intubación orotraqueal de inmediato21-26.
Es importante tener en cuenta que para lograr con seguridad esta estrategia de manejo se debe contar con entrenamiento del personal y experiencia, y con el EPP completo para protección de aerosoles, y se debe tener activado el equipo de vía aérea difícil de respaldo desde el inicio. Se sugiere buscar minimizar los aerosoles con la colocación de una mascarilla al paciente, verificar la colocación adecuada de los vástagos en las narinas, bajar el flujo apenas sea posible y ventilación natural del área (apertura de ventanas) en caso de no contar con un área de presión negativa. Todas estas recomendaciones son vitales, ya que la seguridad del personal sanitario debe ser una prioridad.
Capítulo 4. Ventilación mecánica en los niños con infección por virus SARS-CoV-2Se sugiere- 1.
Se sugiere utilizar estrategias de ventilación mecánica protectora para niños con SDRA por infección severa por COVID-19 que incluyen: Vt 6-8 cc/kg, presión meseta < 32cmH2O, presión de conducción < 18cmH2O, PEEP óptima y FiO2 menor de 0,6.
- 2.
Se sugiere practicar intubación orotraqueal en todos los pacientes pediátricos que presentan hipoxemia persistente (PaO2/FiO2 < 200 o Sa/Fi < 264), aumento de los requerimientos de oxígeno con FiO2 > 60% o empeoramiento de la taquipnea con signos de fatiga muscular o trastorno de consciencia.
- 3.
Se sugiere que todos los pacientes que tengan PaO2/FiO2 menor de 150mmHg deberían estar en posición prono para su manejo.
Usualmente, la hipoxemia por COVID-19 se asocia a aumento del gradiente alvéolo-arterial de oxígeno (DA-a)O2 por aumento del shunt intrapulmonar o por un desbalance ventilación-perfusión (por aumento de la ventilación de espacio muerto). No obstante, en niños es frecuente este aumento de la (DA-a)O2 por trastornos de difusión similar a otras infecciones virales. En caso de que exista mejoría de la PaO2 con aumento de la FiO2, posiblemente la causa de la hipoxemia es un desbalance ventilación-perfusión. Pero en caso de no mejorar, con este aumento de la FiO2 es posible que el paciente curse con aumento del shunt intrapulmonar. También el encontrar una relación EtCO2/PaCO2 menor de 1 sugiere la presencia de aumento del shunt intrapulmonar o del espacio muerto27,28.
El uso de la ventilación mecánica invasiva temprana se ha propuesto para disminuir el trabajo respiratorio, favorecer el desempeño cardiovascular y optimizar la entrega tisular de oxígeno en pacientes con falla respiratoria secundaria a la infección por COVID-1929,30. No se recomienda el uso de la VMNI en los niños con sospecha de infección por COVID-19. Además de las dificultades tradicionales por un mal sello, claustrofobia y mal acople observados en pediatría, se ha demostrado que es gran generadora de aerosoles y favorece la contaminación de los equipos médicos31.
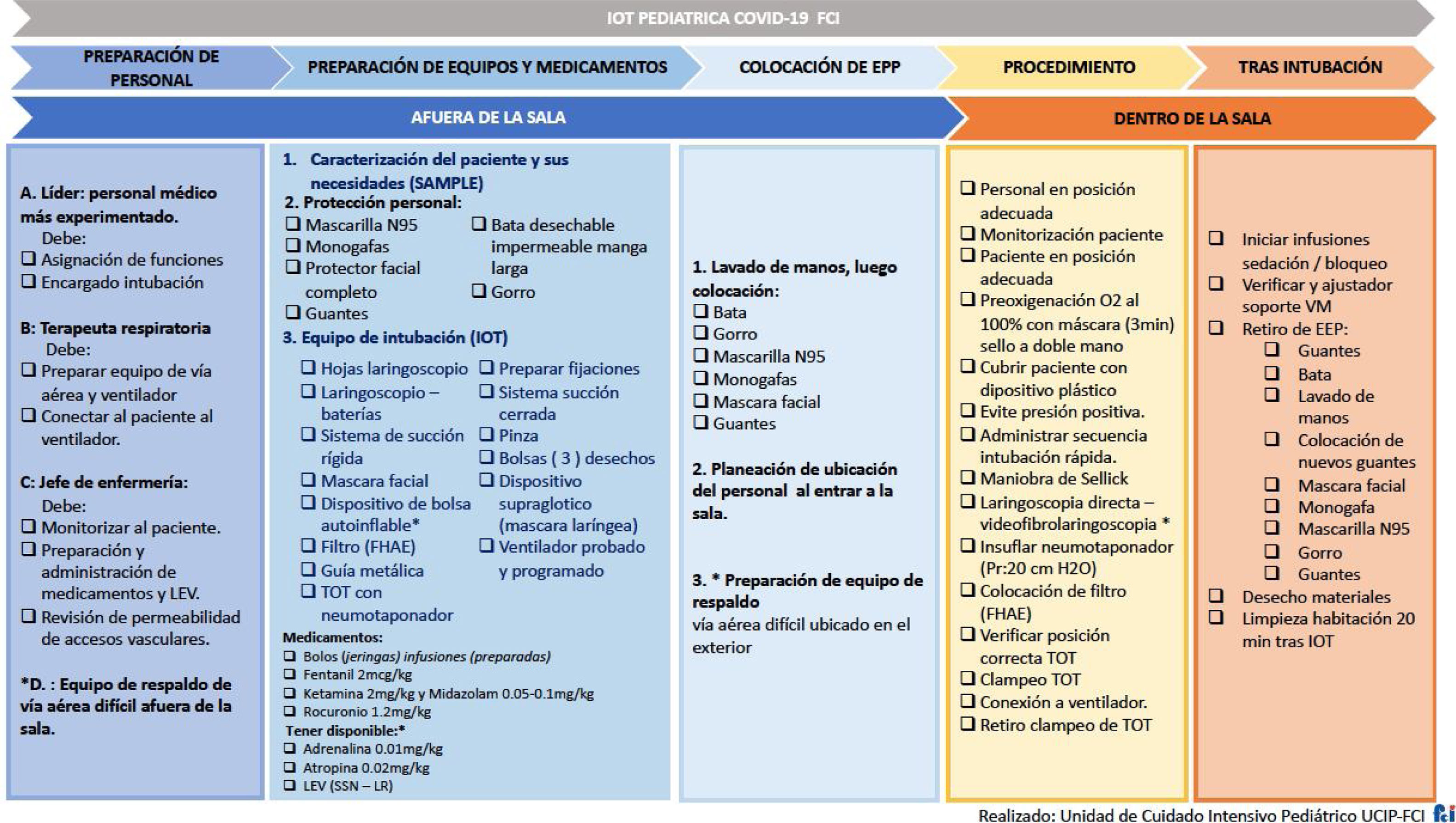
La intubación orotraqueal debe ser llevada a cabo de forma segura, contando con los EPP adecuados para el personal de salud y preparando el equipo de vía aérea y medicamentos con antelación como se describe en la figura 2. La hipoxemia persistente (PaO2/FiO2 < 200 o Sa/Fi < 264), aumento de los requerimientos de oxígeno o empeoramiento de la taquipnea son indicaciones para considerar el inicio de la ventilación mecánica invasiva en pacientes que reciben CNAF. Es muy importante no atrasar el inicio de la ventilación mecánica, pero siempre tomando la decisión de practicar intubación basada en el juicio clínico y apoyado en las ayudas paraclínicas. No obstante, debe considerarse que el paciente que tiene distrés respiratorio progresivo, asociado a trastorno de consciencia, cursa con falla respiratoria y requiere manejo avanzado de la vía aérea32.
Una vez se intuba al paciente, se debe iniciar ventilación mecánica protectora, que involucra estrategias encaminadas a disminuir la lesión pulmonar inducida por la ventilación mecánica. No debemos olvidar que la ventilación mecánica es una medida de soporte. No tiene efectos curativos en sí misma. Así como puede salvar la vida del paciente, puede llegar a lesionar el pulmón de manera importante y aumentar la mortalidad. En la tabla 3 se resumen los parámetros recomendados para iniciar la ventilación mecánica en todos los grupos etarios. Es importante resaltar que, dada la alta transmisibilidad del virus, deben instalarse filtros inspiratorios para evitar la propagación de aerosoles. Este sistema de humidificación pasiva son los de elección en la neumonía que lleva a falla respiratoria por COVID-19. No obstante, con frecuencia estos niños son hipersecretantes y requiere cambiarse a un sistema de humidificación activa. No debe olvidarse siempre usar sistemas de succión cerrado. Lo importante es mantener al paciente siempre conectado al ventilador mecánico y por ningún motivo debe desconectarse.
Estrategias de ventilación mecánica de inicio en niños con SDRA por infección por COVID-19
| Modo ventilatorio | Volumen control o modo volumen controlado regulado por presión |
| Volumen corriente | 5 a 8 ml/kgVigilar presión meseta: si > 32 cmH2O, disminuir volumen corriente |
| Frecuencia respiratoria | Niños de 1 m a 2 años: 22 a 30 rpmNiños de 2 a 4 años: 18 a 24 rpmNiños mayores de 8 años 14 a 20 rpm |
| Relación inspiración espiración (rel. I:E) | 1:2 |
| Presión al final de la espiración | Óptimo de acuerdo con el pacienteInicial: 5 a 8 cmH2OTitular de acuerdo con la oxigenaciónRadiografía de tórax y gases arterialesAumentar de a 2 cmH2O |
| Fracción inspirada de O2 | Iniciar 100% y disminuir rápidamente menos del 60% en las primeras 2-6 h |
| Alarmas | 10% por encima y por debajo parámetrosPresión meseta < 32 cmH2O, driving pressure < 15 cmH2O |
En caso de que el paciente presente paro cardiorrespiratorio, recientemente la American Heart Asssociation (AHA)generó algunas recomendaciones. Debe cambiarse a un modo controlado (si no está en el previamente, preferiblemente presión control), aumentar la FiO2 al 100%, programar la frecuencia respiratoria en niños a 30/min, la sensibilidad debe estar apagada y se debe garantizar que el paciente recibe un volumen corriente de 6-8ml/kg. Debe continuarse con RCP de alta calidad habitual. En otras palabras, el paciente no se desconecta del ventilador. No se da ventilación con bolsa autoinflable. Si el paciente está en posición prona intubado, no debe cambiarse de posición. Aunque la evidencia está en construcción, la AHA recomienda hacer compresiones torácicas a nivel de T7-T10 como parte de la RCP de alta calidad33,34.
La posición de prono es parte fundamental del tratamiento de pacientes con SDRA moderado a severo. Debe iniciarse a todos los pacientes con una PaO2/FiO2 menor de 150mmHg por periodos de 12-16 h cada día. Con esta posición se logra mejorar la redistribución del flujo sanguíneo, optimizar la relación ventilación perfusión y la apertura de zonas del pulmón que se encuentran colapsadas por la gravedad.
Recientemente, se ha propuesto identificar 2fenotipos de SDRA por COVID-19. El tipo 1, asociado a distensibilidad pulmonar normal, hipoxemia con poca ocupación alveolar y pobre respuesta a niveles altos de PEEP35,36. Se sugiere como posible causa alteración del mecanismo de vasoconstricción pulmonar hipóxica y alteración de la regulación vascular. El tipo 2, en cambio, se caracteriza por baja distensibilidad, hipoxemia con gran ocupación alveolar y necesidad de altos niveles de PEEP. La causa de la hipoxemia es más asociada al aumento del shunt intrapulmonar. Esta propuesta de clasificación fisiopatológica la han planteado médicos de adultos, pero no tenemos evidencia de esta diferenciación tan clara en niños. Es más frecuente que en pediatría observemos que en las infecciones virales habituales (p. ej., infección por vrus respiratorio sincitial) se tenga diferentes patrones obstructivos o restrictivos, que en oportunidades son mixtos, que exigen estrategias de ventilación mecánica específicas y para cada paciente sin una clara diferenciación en estos 2tipos descritos en adultos.
Capítulo 5. Tratamiento para los pacientes con infección por SARS-CoV-2Se sugiere- 1.
Existe insuficiente evidencia para recomendar el uso en pediatría de: hidroxicloroquina (HCQ), cloroquina (CQ), ivermectina, lopinavir/ritonavir, ribavirina, remdesivir y tocilizumab.
- 2.
Se sugiere considerar adicionar al tratamiento dexametasona a dosis de 0,15 mg/kg/dosis cada 6h por 5-7 días en infección respiratoria severa que requiera soporte con ventilación mecánica o en casos moderados con alto soporte de oxígeno de acuerdo con datos extrapolados de adultos.
Hasta la fecha no existe evidencia sólida que avale el uso de alguna terapia específica para el manejo de la infección por SARS-CoV-2 en Pediatría ni evidencia indirecta de la población de adultos37. Organismos como la IDSA recomiendan su uso solo en el contexto de estudios clínicos con una estructura metodológica adecuada. A continuación, se describen las moléculas más estudiadas38.
Cloroquina (CQ)/hidroxicloroquina (HCQ)Han mostrado actividad in vitro para SARS-CoV-2, evitando la entrada viral a las células del huésped por inhibición de la glucosilación de receptores del huésped, alterando el proceso proteolítico, generando acidificación endosomal; presenta efecto inmunomodulador por medio de la atenuación de producción de citocinas e inhibición de la autofagia y actividad lisosomal en el huésped39,40. Un ensayo clínico realizado en China con más de 100 pacientes adultos con COVID encontró mejoría radiológica y disminución de la progresión de la enfermedad con el uso de CQ; sin embargo, el diseño y los datos de los desenlaces no han sido evaluados por pares, lo que limita validar dichas recomendaciones41. Otros 2estudios, realizados en Francia y China, mostraron resultados contradictorios. El primero, de Gautret et al., abierto, no aleatorizado, evidenció mejoría de la eliminación viral al sexto día y los autores reportaron una mejor respuesta en los pacientes con terapia combinada con azitromicina42. El segundo estudio, de Chen et al.43, prospectivo aleatorizado, no mostró diferencia significativa en la eliminación viral a la semana entre el grupo intervenido y el que recibió cuidado estándar. Estos 2estudios son muy limitados por el tamaño de sus muestras, no mayores a 36 casos en el más grande, y no reportaron desenlaces en seguridad. Mahévas et al. describieron a 181 adultos con neumonía por SARS-CoV-2 en un estudio comparativo, de 2grupos, uno con régimen de HCQ, el cual no mostró mejores desenlaces que el grupo de régimen estándar. Estudios observacionales y ensayos abiertos con la combinación HCQ/CQ + azitromicina han reportado mayor eliminación viral, pero no generan una recomendación por las limitaciones metodológicas y los pequeños números de casos44.
Están descritos efectos adversos hasta en el 10% de los pacientes que usan CQ/HCQ, tales como: prolongación del intervalo QT, hipoglucemia, efectos neuropsiquiátricos y retinopatía45. Con esta información no puede realizarse una recomendación para su uso en población pediátrica a la luz de la evidencia actual. Algunas guías y consensos han sugerido, bajo criterios específicos, dosis en niños para infección por SARS-CoV-2 de CQ 5mg/kg cada 12 h por 2 dosis, seguido de 5mg/ kg cada 24 h por 5-7 días e HCQ 8mg/kg/dosis por vía oral, cada 12 h (dosis máxima: 400mg) por 2dosis, seguido de 4mg/kg/dosis (dosis máxima 200mg) cada 12 h por 5-7 días, sin que se tenga evidencia clara de la indicación, momentos de uso en la enfermedad y efectividad.
Lopinavir/ritonavirMedicamento inhibidor de proteasa, que inhibe la proteinasa principal del CoV, interrumpiendo su replicación. Un ensayo clínico aleatorizado y 2estudios de casos evaluaron el tratamiento combinado de lopinavir/ritonavir para pacientes hospitalizados por infección por SARS-CoV-2. Cao et al. aleatorizaron a 199 pacientes con enfermedad severa por COVID-19; 99 pacientes en manejo estándar + lopinavir/ritonavir y 100 en manejo estándar. No hubo diferencias en la mejoría clínica, en eliminación viral y en mortalidad. Se describieron importantes efectos secundarios, sobre todo a nivel gastrointestinal46. Con esta información no puede realizarse una recomendación para su uso en población pediátrica a la luz de la evidencia actual.
RibavirinaAnálogo de la guanina, que inhibe el ARN viral dependiente del ARN polimerasa. In vitro ha mostrado requerir de dosis muy altas para inhibir la replicación viral de SARS-CoV-2. Las dosis alta generan toxicidad hematológica, con presencia de anemia hemolítica en más del 60% cuando se usó en ensayos clínicos para SARS. Eficacia no concluyente para otros coronavirus y esto limita su uso para la COVID-1947,48.
Con esta información no puede realizarse una recomendación para su uso en población pediátrica a la luz de la evidencia actual.
RemdesivirProfármaco que inhibe el ARN polimerasa viral y, por lo tanto, evita que el virus se multiplique por la replicación en las células infectadas. Promisorio potencial terapéutico para COVID-19 in vitro. Grein et al. describen una serie de casos de uso compasivo con remdesivir en pacientes con casos severos de SAR-CoV-2; sin embargo, la no existencia de grupo control y la financiación del estudio por la industria farmacéutica limitan emitir una recomendación al respecto49.
Con esta información no puede realizarse una recomendación para su uso en población pediátrica a la luz de la evidencia actual.
TocilizumabAnticuerpo monoclonal que se une específicamente a los receptores de IL-6, inhibiendo la señalización de la IL-6 mediada a través de estos receptores, atenuando la desregulación presentada por las citocinas inflamatorias. Xu et al. describieron a 21 pacientes adultos con infección por SARS-CoV-2 en protocolo par aplicación de tocilizumab. El grupo intervenido presentó mejoría en su función respiratoria, disminución de síntomas, sobre todo fiebre, y egresos más temprano, sin embargo, no hubo grupo control, lo que limita la interpretación de un efecto específico atribuible al medicamento37,50.
Con esta información no puede realizarse una recomendación para su uso en población pediátrica a la luz de la evidencia actual.
IvermectinaAntiparasitario que in vitro ha demostrado tener actividad inhibiendo la replicación viral de SARS-CoV-248 y ausencia de material viral luego de 48 h de la terapia51. En un estudio observacional en diferentes países, se indicó a 52 pacientes en ventilación mecánica por SARS-CoV-2 ivermectina 150 μg/kg, con disminución de la severidad de la enfermedad, estancia y mortalidad. Sin embargo, no hubo grupo control, ni revisión por pares, limitando una recomendación sobre su uso52.
Con esta información no puede realizarse una recomendación para su uso en población pediátrica a la luz de la evidencia actual.
Recientemente, existe una publicación de reporte preliminar de un gran ensayo clínico controlado denominado RECOVERY53, que evaluó el papel de la dexametasona como medicamento coadyuvante en la infección respiratoria severa por SARS-CoV-2 en pacientes adultos. Encontró que en los casos severos tiene un NNT de 8 para reducir mortalidad en pacientes que requieren soporte con ventilación mecánica y un NNT de 25 para modificar curso clínico en pacientes que requieren oxigenoterapia, pero no tienen soporte ventilatorio. Esta experiencia extrapolada de los adultos a dosis utilizada de 6 mg/día es equivalente a 0,15 mg/kg/dosis cada 6 h por 5 a 7 días en Pediatría. No existe suficiente evidencia para recomendarlo en los casos leves y no se conoce el efecto en estos pacientes. Tampoco se conoce si otros esteroides con potencia diferente (metilprednisolona, prednisona, etc.) tienen los mismos efectos biológicos que la dexametasona.
Capítulo 6. ¿Cómo manejar el estrés del pediatra intensivista y del equipo de la UCI que atiende niños críticos durante la pandemia?Se sugiere- 1.
Se sugiere para el personal de la salud que atiende a niños sospechosos o confirmados por COVID-19 que se establezcan estrategias de mitigación del estrés laboral y el cansancio físico.
- 2.
Se sugiere que al personal de la salud que atiende a pacientes con sospecha o infección confirmada por COVID-19 se le proporcione elementos de protección personal completos que permitan un trabajo seguro, confiable y contribuya a no generar stress por falta de EPP.
- 3.
Se sugiere que los grupos tratantes tengan ajuste en horarios laborales, apoyo de psicología durante la atención de la pandemia.
La pandemia que estamos sufriendo es una situación completamente nueva para todos los individuos vivos del planeta. Hasta hace pocas semanas, ningún médico podía imaginar que en pleno siglo xxi, cuando la medicina ha alcanzado avances extraordinarios para prevenir y tratar enfermedades, cuando tenemos cada vez más tecnología para apoyar la función de órganos y lograr que la esperanza de vida sea cada vez mayor; un virus emergente iba a golpearnos de tal forma que todas las certezas previas empiezan a tambalear, o como lo dijo algún filósofo del siglo xix: «Todo lo sólido se desvanece en el aire».
Cuando un paradigma tambalea, la seguridad y la confianza también lo hacen. Descubrimos de un momento a otro que, a pesar de lo que ha logrado la medicina actual, somos seres mortales, estamos tratados mediante los caprichos de la naturaleza, no lo sabemos ni lo podemos todo. Nos enfrentamos a la probabilidad de que lo que hacíamos como una rutina, lo que era parte de nuestra cotidianidad, de pronto se convierte en un trabajo riesgoso, que puede afectar de formas insólitas a nuestras vidas y las de nuestras familias; que podemos enfermar gravemente o morir en pocos días, por practicar el oficio que conocemos y amamos, o peor aún, tenemos el temor de ser fuentes de contagio para nuestros seres queridos.
Los pediatras que deciden especializarse en cuidado intensivo saben que van trabajar en un entorno con múltiples fuentes de estrés. En primer lugar, la responsabilidad sobre la vida de niños críticamente enfermos; en segundo lugar, la demanda de los padres, que en esta era de la información interfieren en las decisiones; por otro, la dinámica de sistema de salud que exige el cumplimiento de trámites para desplegar el arsenal terapéutico, las largas jornadas de trabajo con una carga al límite en muchas ocasiones, etc. Como si esto fuera poco, muchas veces los intensivistas en algunas regiones tienen contratos de trabajo a término fijo, mal remunerados, donde cada cual debe encargarse de su seguridad social, riesgos laborales, etc.
Estudios realizados antes de esta pandemia muestran que entre los médicos existen altos niveles de estrés y de síntomas depresivos54. Un estudio colombiano hecho entre anestesiólogos determinó que cerca del 20% de los profesionales entrevistados tienen signos y síntomas de desgaste profesional o burnout55. Los estudios realizados específicamente en Unidades de Cuidado Intensivo demuestran que los intensivistas están tratados mediante altos niveles de estrés no solo por el ambiente físico en el que se practica la disciplina (espacios cerrados y ruidosos), sino por la exigencia diaria física, intelectual y emocional que se les exige al enfrentarse diariamente a pacientes críticos; esto produce en algunos profesionales irritabilidad, hostilidad, falta de concentración y respuestas físicas como cefalea, insomnio, dolor de espalda y trastornos digestivos56.
Algunos colegas que ya han vivido la pandemia y lidiado con ella, describen el fenómeno como un «tsunami», un fenómeno en el cual, como factor de estrés agregado, debido al uso de elementos de protección personal que cubren no solo nuestro cuerpo, nuestras manos, sino nuestra cara, el trato cercano, personal y directo tanto con el paciente y su familia, como con los compañeros de trabajo, se ha perdido. Se extraña el sosiego, una risa, un roce57.
Es indudable que la pandemia ha empeorado el estrés de los profesionales de la salud al agregar a las dificultades diarias el temor por la salud y la vida. ¿Qué hacer en estos momentos de incertidumbre? ¿Qué estrategias seguir para reducir y manejar este estrés?
- –
Cambio en los horarios de trabajo que permitan estar más tiempo en casa. Algunos médicos de grupos COVID en España han definido jornadas de 24 h continuas con periodos de descanso de 48 h, para disminuir la exposición al virus y aumentar el tiempo de descanso.
- –
Contar con todos los elementos de protección necesarios para la atención de pacientes sospechosos o confirmados de COVID-19, hacer talleres sobre su uso correcto. Cuando el personal del turno sabe hacer las cosas bien, aumentan la tranquilidad y la confianza.
- –
Programas de apoyo institucional al personal de mayor riesgo que incluyan manejo de angustia emocional y de habilidades de comunicación.
- –
Técnicas de relajación como yoga, masajes o tiempo libre programado durante el cual se haga ejercicio físico dirigido en forma virtual.
- –
Canal institucional de noticias veraces, tanto de la institución como del país, que mantenga informado al equipo.
- –
Estrategias para limitar el tiempo destinado a revisar noticias en las redes sociales. Muchas de las noticias falsas o de los mensajes que angustian al personal vienen por esos medios.
- –
Enseñanza sobre atención de final de vida y de cuidados paliativos. Cuando un equipo tiene claro que la muerte no es siempre un desenlace no deseado, disminuye el nivel de estrés.
- –
Disponibilidad de apoyo con psicología o psiquiatría de forma grupal o individual por canales digitales.
- –
Mensajes institucionales donde se manifieste el respaldo total al personal de salud.
- –
Como mensaje final, a modo personal y subjetivo, estamos convencidos de que la mejor manera para que nuestro equipo esté más tranquilo es que perciban en nosotros, en nuestro lenguaje preverbal, la seguridad que sentimos: estamos haciendo las cosas bien, en la medida de nuestras posibilidades. Para afrontar nuestro propio estrés, no creemos que haya mejor remedio que recordar día a día que hacemos lo que hacemos por verdadera vocación, con amor y determinación de servicio.