A vitamina D é única entre as vitaminas, pois funciona como uma hormona e pode ser sintetizada na pele a partir da exposição à luz solar. Além dos seus efeitos no metabolismo fosfocálcico, evidências recentes correlacionam níveis insuficientes de vitamina D com um risco aumentado de desenvolvimento de outras patologias não ósseas. O nível sérico de 25-hidroxivitamina D (25(OH)D) é o melhor indicador do conteúdo corporal de vitamina D ao refletir a vitamina obtida a partir da ingestão alimentar e da exposição à luz solar, bem como a conversão de vitamina D a partir dos depósitos adiposos no fígado. Os níveis de 25(OH)D constituem um espectro contínuo de suficiência de vitamina D. Apesar de controverso, parece existir um «consenso» de que os valores plasmáticos de 25(OH)D inferiores a 30-32ng/ml indicam um défice relativo de vitamina D. A vitamina D usada para fins de substituição ocorre em 2 formas principais: o colecalciferol (vitamina D3) e o ergocalciferol (vitamina D2). Estas 2 vitaminas são equivalentes; ambas aumentam os níveis séricos de 25(OH)D de forma semelhante, sugerindo uma absorção equivalente. As últimas orientações da Endocrine Society sugerem o rastreio do défice de vitamina D apenas em indivíduos em risco e não na população em geral. Nestes doentes, recomenda-se a medição da 25(OH)D sérica circulante, por um método analítico fiável. O défice de vitamina D é definido por um valor de 25(OH)D inferior a 20ng/ml (50nmol/l). Em indivíduos em risco recomenda-se a ingestão de vitamina D na dieta, de acordo com a idade e situações especiais (gravidez, amamentação, obesidade e toma concomitante de fármacos). Para o tratamento e prevenção do défice de vitamina D sugere-se a utilização de qualquer das isoformas (vitamina D2 ou vitamina D3), em dose dependente do grupo etário e das necessidades específicas. Para obtenção dos benefícios não calcémicos da vitamina D, a Endocrine Society recomenda a suplementação com vitamina D para prevenção de quedas. No entanto, não se recomenda a suplementação além das necessidades diárias recomendadas, com o objetivo de prevenir a doença ou morte cardiovascular ou aumentar a qualidade de vida.
Vitamin D is unique among vitamins, as it acts as a hormone and may be synthesized in the skin from exposure to sunlight. In addition to its effects on phosphorus-calcium metabolism, recent evidence correlates insufficient levels of vitamin D with an increased risk of developing other diseases, not bone related. Serum levels of 25-hydroxyvitamin D (25(OH)D) is the best indicator of vitamin D body content, as it reflects the vitamin obtained from dietary intake and exposure to sunlight, as well as the conversion of vitamin D from fatty deposits in liver. 25(OH)D levels form a continuous spectrum of vitamin D sufficiency. Although controversial, there appears to be a “consensus” that plasma levels of 25(OH)D below 30-32 ng/ml indicates a relative deficiency of vitamin D. Vitamin D used for replacement occurs in two major forms: cholecalciferol (vitamin D3) and ergocalciferol (vitamin D2). Both vitamins are equivalent, both increase serum levels of 25 (OH) D similarly, suggesting an equivalent absorption. The latest Endocrine Society guidelines suggest screening for vitamin D deficiency only in individuals at risk and not in the general population. In these patients, it is recommended the measurement of 25(OH)D circulating in serum, by a reliable analytical method. The vitamin D deficiency is defined by a value of 25 (OH) D less than 20ng/ml (50nmol/l). In individuals at risk, it is recommended the intake of dietary vitamin D, according to the age and special medical conditions (pregnancy, breastfeeding, obesity and concomitant intake of drugs). For treatment and prevention of vitamin D deficiency it is suggested the use of any of the isoforms (vitamin D2 or vitamin D3) in an age-dependent and individual dose. To obtain the non-calcemic benefits of vitamin D, the Endocrine Society recommends vitamin D supplementation to prevent its decrease. However, supplementation beyond the recommended daily dose is not recommended for the purpose of preventing cardiovascular death or increase quality of life.
O papel da vitamina D na regulação do metabolismo fosfocálcico, assegurando, entre outras funções, uma mineralização óssea normal, é há muito conhecido. Evidências recentes correlacionam níveis insuficientes de vitamina D com um risco aumentado de desenvolvimento de outras patologias não ósseas: doenças cardiovasculares, hipertensão, neoplasias, diabetes, esclerose múltipla, demência, artrite reumatóide, doenças infeciosas. Os diferentes efeitos da vitamina D são mediados por vários recetores em diferentes localizações, que regulam mais de 200 genes. Além dos recetores presentes no intestino e no osso, recetores de vitamina D foram identificados no cérebro, próstata, mama, cólon, células do sistema imunitário, do músculo liso vascular e em miócitos cardíacos1,2. Valores plasmáticos suficientes de vitamina D são, portanto, fundamentais para manter uma boa saúde em geral.
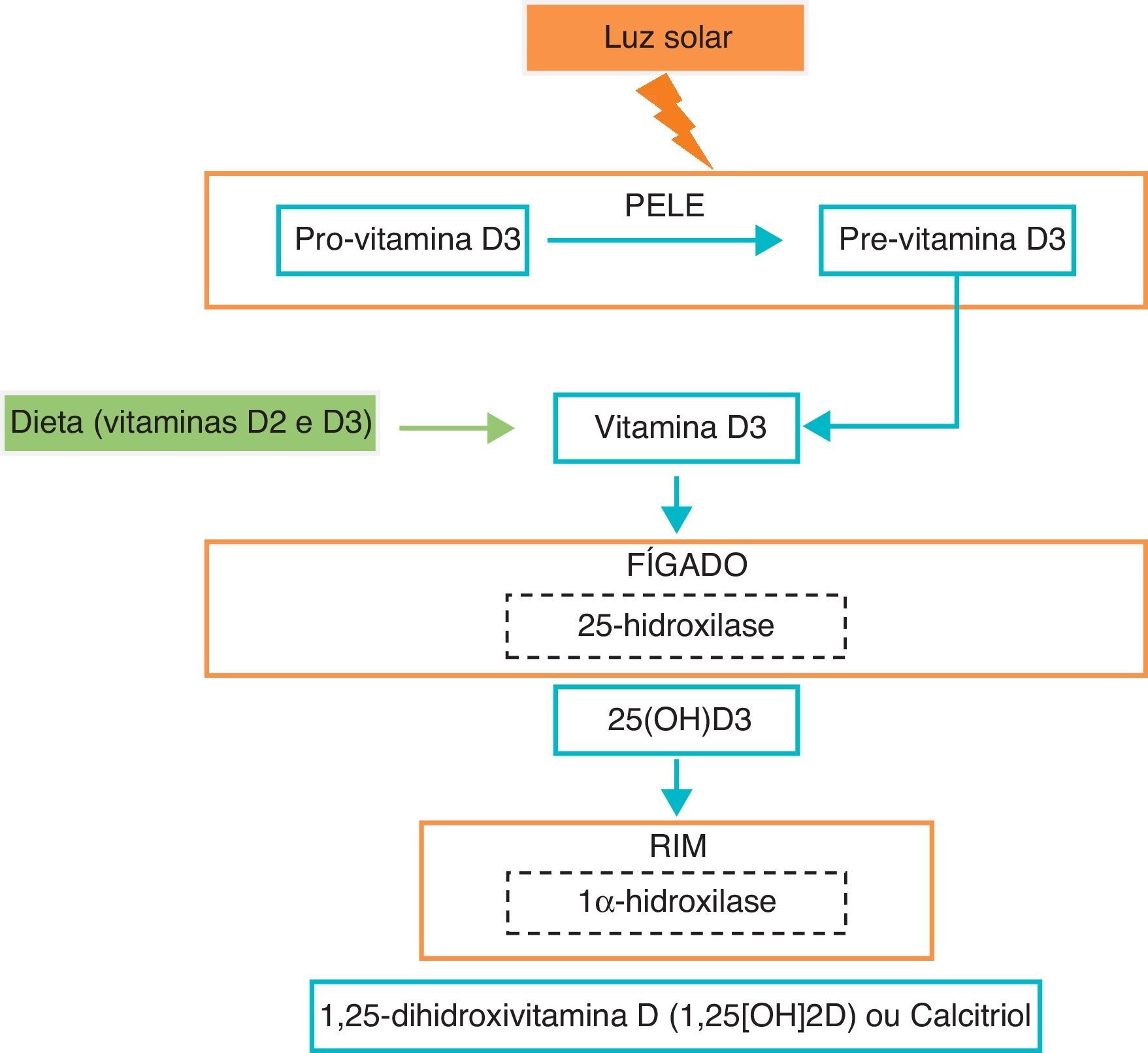
Metabolismo da vitamina DA vitamina D é única entre as vitaminas, pois funciona como uma hormona e pode ser sintetizada na pele a partir da exposição à luz solar (radiação ultravioleta na faixa de 290-315nm) (fig. 1). Uma parte da vitamina D vem ainda de fontes alimentares (entre 100-200UI por dia)3.
Existem várias formas químicas da vitamina D. As 2 formas principais são a vitamina D2 (ou ergocalciferol) e a vitamina D3 (ou colecalciferol). A vitamina D2 é obtida da irradiação ultravioleta do ergosterol (esterol da membrana de fungos e invertebrados) e é encontrada naturalmente em leveduras e cogumelos expostos à luz solar. A vitamina D3 é obtida da irradiação ultravioleta do percursor do colesterol - 7-dihidrocolesterol (naturalmente presente na pele de animais ou no leite) - sendo sintetizada na pele e encontrada naturalmente nos peixes gordos como o salmão, a cavala e o arenque4.
As condições ambientais, hormonais, genéticas e nutricionais influenciam os níveis plasmáticos de vitamina D5.
A síntese de vitamina D através da pele é bastante variável, dependendo da pigmentação, latitude, estação do ano, vestuário, idade, uso de protetor solar e condições meteorológicas locais. Os níveis de vitamina D são consideravelmente mais baixos na raça negra do que na raça branca, devido à maior pigmentação da pele. Nas latitudes nórdicas, estes níveis reduzem cerca de 20% desde o final do verão até meados do inverno, no entanto, 30 minutos de exposição corporal ao sol durante o verão rapidamente originam vitamina D suficiente4,5.
Os níveis de vitamina D podem ainda variar de acordo com fatores hormonais, genéticos e nutricionais. Por exemplo, o Índice de Massa Corporal (IMC) correlaciona-se de forma indireta com os valores séricos de vitamina D, que são menores em obesos. Esta diferença pode ser parcialmente explicada pela diminuição da atividade física e exposição solar em obesos5.
A vitamina D (D2, D3 ou ambas) ingerida é incorporada em quilomicrons, que são absorvidos no sistema linfático e entram na circulação venosa.
A vitamina D que vem da pele ou da dieta é biologicamente inerte e requer uma primeira hidroxilação no fígado, pela 25-hidroxilase, a 25-hidroxivitamina D (25(OH)D, forma parcialmente hidrossolúvel com uma semivida curta, que circula ligada às proteínas de ligação). Esta requer mais uma hidroxilação a nível renal, pela 1α-hidroxilase (CYP27B1), para formar a 1,25-dihidroxivitamina D (1,25[OH]2D), a forma biologicamente ativa da vitamina D. Esta forma circula em concentrações inferiores às da 25(OH)D, mas tem uma afinidade muito maior para o recetor e é biologicamente mais potente5.
Vários tecidos e células possuem atividade 1α-hidroxilase. A produção local de 1,25(OH)2D pode ser responsável pela regulação de mais de 200 genes, que podem justificar muitos dos benefícios pleiotrópicos na saúde que estão associados à vitamina D3.
A forma ativa interage com o recetor nuclear da vitamina D presente na maioria dos tecidos e células do organismo. No intestino delgado, a 1,25(OH)2D estimula a absorção intestinal do cálcio. Sem vitamina D, apenas 10-15% do cálcio da dieta e cerca de 60% do fósforo são absorvidos. A suficiência de vitamina D aumenta a absorção de cálcio e fósforo em 30-40% e em 80%, respetivamente. No osteoblasto, a 1,25(OH)2D interage com o recetor da vitamina D, induzindo os monócitos imaturos a tornarem-se osteoclastos maduros, que dissolvem a matriz e mobilizam cálcio e outros minerais do esqueleto. No rim, a 1,25(OH)2D estimula a reabsorção de cálcio do filtrado glomerular.
A 1,25(OH)2D tem ainda um amplo espectro de outras ações biológicas, incluindo a inibição da proliferação celular e a indução da diferenciação terminal, a inibição da angiogénese, a estimulação da produção de insulina, a inibição da produção de renina e a estimulação da produção de catelicidina dos macrófagos3.
Além disto, a 1,25(OH)2D estimula a sua própria destruição através do aumento da expressão da 24-hidroxilase (CYP24R), que metaboliza a 25(OH)D e a 1,25(OH)2D em formas hidrossolúveis inativas.
Efeitos pleiotrópicos da vitamina DUm número crescente de estudos associa a insuficiência de vitamina D com um maior risco de desenvolver diversas patologias. Um estudo prospetivo que acompanhou, durante 5 anos, 1.739 participantes sem doença cardiovascular prévia mostrou que os indivíduos com hipertensão arterial (HTA) e níveis de 25(OH)D <15ng/mL apresentaram um risco 2 vezes superior de eventos cardiovasculares em comparação com aqueles com níveis superiores a 15ng/mL2. Uma análise de 454 indivíduos, sem doença cardiovascular diagnosticada previamente e que desenvolveram enfarte de miocárdio (EAM) ou doença coronária durante 10 anos de seguimento, assim como de 900 indivíduos no grupo de controlo, indicou que o risco de EAM duplicou nos indivíduos com níveis de 25(OH)D <15ng/mL, em comparação com aqueles com níveis >30ng/mL6. Um estudo de seguimento de 7 anos de 3.258 indivíduos que tinham sido encaminhados para angiografia coronária mostrou que a diminuição dos níveis de 25(OH)D (7,6ng/mL vs. 13,3ng/mL vs. 18,9ng/mL vs. 28,4ng/mL) estava associada a um risco crescente de mortalidade global e mortalidade cardiovascular7.
A análise conjunta de 2 estudos com 880 casos de cancro da mama e 880 casos controlo demonstrou que mulheres com níveis séricos de 25(OH)D de cerca de 52ng/mL tiveram um risco 50% inferior de desenvolver cancro da mama em comparação com aquelas com níveis <13ng/mL8. Uma análise de 1.394 mulheres na pós-menopausa com cancro da mama e 1.365 casos controlo sugeriu que a concentração sérica de 25(OH)D está inversamente associada, de forma significativa, com o risco de cancro da mama, especialmente em níveis <20ng/mL9. Um ensaio de 4 anos, incluindo 1.085 mulheres saudáveis, ingerindo suplementos de placebo, cálcio ou cálcio+vitamina D mostrou que a suplementação com vitamina D reduzia em 77% o risco relativo de desenvolver cancro10.
Uma metaanálise de 8 estudos prospetivos, que incluiu 1.822 doentes com cancro do cólon e 868 com cancro retal, mostrou uma associação inversa entre os níveis circulantes de 25(OH)D e o cancro colorretal, com uma associação mais significativa nos doentes com cancro retal11.
O risco de esclerose múltipla numa população branca de 148 doentes e 296 casos controlo demonstrou ser 51% inferior para os indivíduos com níveis de 25(OH)D >40ng/mL, comparativamente com níveis <30ng/mL12. Um estudo incluindo 103 doentes e 110 controlos mostrou que, para cada aumento sérico de 4ng/mL nos níveis de 25(OH)D, a probabilidade de desenvolver esclerose múltipla em mulheres reduz 19%13. Numa população de 206 doentes com poliartrite inflamatória inicial, uma relação inversa entre os níveis de 25(OH)D e a avaliação do Disease Activity Score (DAS) foi encontrada: a cada aumento de 10ng/mL de 25(OH)D foi associada uma diminuição de 0,3 no DAS14.
Num estudo de coorte com 10.366 crianças, a suplementação de vitamina D com doses diárias de 2.000UI foi associada a uma redução de 78% no risco de desenvolver diabetes tipo 1, comparativamente com doses mais baixas15. Uma metaanálise de 4 estudos com um total de 1.429 casos e 5.026 controlos demonstrou que crianças que receberam suplementos de vitamina D tiveram uma redução de 29% no risco de desenvolver diabetes tipo 1, em comparação com as crianças sem suplemento16. Um seguimento de 10 anos de 524 adultos não diabéticos demonstrou uma associação inversa entre os níveis basais de 25(OH)D e o desenvolvimento futuro de anomalias da glicémia e insulinorresistência17. Outros estudos mais recentes têm corroborado estes resultados, demonstrando um papel importante da vitamina D no desenvolvimento de anomalias metabólicas, obesidade e diabetes18,19.
Doseamento de vitamina DA forma ativa da vitamina D, a 1,25(OH)2D, não fornece informação fidedigna sobre o conteúdo corporal de vitamina D, dado que, na presença de défice desta vitamina, há elevação da paratormona (PTH), o que irá aumentar a atividade renal da 1α-hidroxilase, promovendo a conversão da 25(OH)D em 1,25(OH)2D. Como a primeira existe em maior concentração que a segunda, com o aumento da conversão, a 1,25(OH)2D pode ser normal mesmo em situação de défice de vitamina D20.
O nível sérico de 25(OH)D é o melhor indicador do conteúdo corporal de vitamina D ao refletir a vitamina obtida a partir da ingestão alimentar e da exposição à luz solar, bem como a conversão de vitamina D a partir dos depósitos adiposos no fígado21.
Embora existam vários métodos de dosear a 25(OH)D (por radioimunoensaio, ensaios enzimáticos e cromatografia líquida com espectrometria de massa), a precisão e exatidão destes testes continua problemática22. Esta avaliação laboratorial demonstrou alguns problemas ao longo do tempo, com uma variabilidade marcada de métodos e resultados entre diferentes laboratórios. Apesar da melhoria dos ensaios da 25(OH)D, a variabilidade dos resultados laboratoriais está sempre presente. A imprecisão analítica de qualquer método quantitativo resulta das limitações do próprio método, humanas e instrumentais, que dificultam a aplicação de limites diagnósticos rígidos20.
A avaliação exata do conteúdo corporal baseia-se na medição do nível total de 25(OH)D (25-hidroxivitamina D2(25(OH)D2)+25-hidroxivitamina D3 (25(OH)D3)). Alguns imunoensaios são equipotentes na medição de 25(OH)D2 e 25(OH)D3, enquanto outros detetam preferencialmente uma das formas. Assim, alguns imunoensaios podem levar a erros de interpretação e classificação clínica22.
Métodos antigos de doseamento dependiam da ligação competitiva às proteínas ou de imunoensaios para medição da 25(OH)D e incluíam uma etapa de extração de solvente para remover os esteróis das proteínas de ligação. Esta etapa de extração de solvente procurou-se substituir com agentes bloqueadores. Na prática clínica, o sucesso desta abordagem «block and displace» é limitado, conduzindo a resultados erroneamente elevados de 25(OH)D, com elevada imprecisão.
Para resolver os problemas decorrentes dos métodos de imunoensaio desenvolveram-se técnicas de medição de 25(OH)D baseadas em espectrometria de massa. Tais métodos normalmente envolvem tratamento prévio da amostra para separar a 25(OH)D da sua proteína de ligação, seguido por cromatografia líquida e quantificação, utilizando espectrometria de massa. Embora estes métodos permitam a medição simultânea da 25(OH)D2 e da 25(OH)D3, a harmonização do método é limitada e não há nenhuma preparação de referência ou calibrador consensual para a 25(OH)D23.
Desde 1985 existem ensaios que medem com precisão os níveis totais de 25(OH)D, graças a anticorpos que são coespecíficos para a 25(OH)D2 e a 25(OH)D3. O ensaio de RIA 125I 25(OH)D definiu o padrão para o diagnóstico clínico da deficiência nutricional de vitamina D e tem sido utilizado na maioria dos estudos correlacionando-o com o risco de desenvolver várias doenças24.
À medida que procuramos compreender os recentes papéis da vitamina D na saúde e na doença, a importância da sua medição exata torna-se essencial. É necessária melhor concordância entre os métodos, tanto para permitir a comparação mais significativa entre os estudos de investigação como para facilitar um acordo sobre os objetivos mínimos adequados a uma terapêutica de substituição ideal com vitamina D23.
Défice de vitamina DDefinição e epidemiologiaO valor limiar e até a nomenclatura utilizada para descrever o défice de vitamina D é controversa, sendo usadas várias denominações por diferentes autores (insuficiência, deficiência, hipovitaminose). Além disto, a variabilidade dos métodos laboratoriais e a ausência de valores de referência globalmente aceites, dificulta ainda mais esta classificação.
Os níveis plasmáticos de 25(OH)D constituem um espectro contínuo de suficiência de vitamina D. Apesar da controvérsia, parece existir um «consenso» de que os valores plasmáticos de 25(OH)D inferiores a 30-32ng/ml indicam um défice relativo de vitamina D. Este valor de corte foi sugerido com base no papel da vitamina D na absorção de cálcio e fósforo. Assim, uma deficiência de vitamina D menos grave causa malabsorção de cálcio, conduzindo a hiperparatiroidismo secundário, com resultante aumento do turnover ósseo e consequente perda de massa óssea. A relação da 25(OH)D com a PTH é inversa e em vários estudos encontra-se um ponto de inflexão perto dos 20-30ng/mL. A malabsorção do cálcio não ocorre até valores graves de deficiência de vitamina D, devido à resposta da PTH, com consequente manutenção dos níveis de 1,25(OH)2D25.
Foi recentemente sugerido que o ponto no qual deixa de ocorrer produção hepática de 25(OH)D, por saturação da 25-hidroxilase, pode ser usado para definir o limite inferior da suficiência de vitamina D. Provavelmente, o valor «ótimo» de 25(OH)D é confundido pelos diferentes níveis desta vitamina, nos diferentes tecidos-alvo, necessários à sua ação biológica26.
Além disso, é possível que o valor de 25(OH)D para um ótimo funcionamento fisiológico possa diferir entre diferentes indivíduos. Alguns dados sugerem ainda variações na degradação da vitamina D por prováveis diferenças na capacidade da 24-hidroxilase, dependentes da raça.
No entanto, existe uma concordância de opiniões que estabelece como baixo um valor de 25(OH)D inferior a 30-32ng/mL27,28.
Existem 2 razões para a definição do limite inferior do intervalo normal de 25(OH)D ser 30ng/ml, apesar de recentemente serem questionáveis5. Primeiro, está demonstrado que é abaixo deste valor que os níveis de PTH se elevam; segundo, a absorção ativa de cálcio é a ideal quando o nível de 25(OH)D é 30ng/ml29.
Os níveis séricos ideais de 25(OH)D são aqueles para os quais a absorção de cálcio está otimizada, os níveis de PTH reduzidos e o maior beneficio para o osso e função muscular são obtidos, sendo atualmente recomendado que sejam superiores a 30ng/ml (75nmol/l)3.
Quando este limiar é aplicado, a prevalência de défice de vitamina D torna-se muito elevada (52-77%)30–32. Um limiar menos restrito (défice <20ng/mL) identifica défice de vitamina D em 18-36% da população33.
Apesar da diferença nos métodos de doseamento, no limiar da normalidade e nas populações estudadas a prevalência do défice de vitamina D além de elevada, tem apresentado uma tendência crescente20.
CausasAs fontes alimentares de vitamina D (D2 ou D3) são escassas e de conteúdo não significativo na maioria dos casos. As principais são os óleos de peixe e os produtos alimentares enriquecidos, como os produtos lácteos e pão20,34. Além do défice dietético, outras condições podem originar valores séricos de vitamina D abaixo do desejável, incluindo falta de exposição solar (um fator de proteção solar de 30 reduz a síntese de vitamina D na pele em 95%3), malabsorção (doença inflamatória intestinal, doença celíaca, cirurgia gástrica, doença biliar ou polipose intestinal), uso de anticonvulsivantes (p. ex. fenobarbital, fenitoína) ou glicocorticóides a longo prazo.
Lucas et al.35 avaliaram os valores de ingestão de cálcio e de vitamina D numa amostra constituída por 1.456 mulheres adultas, não especificamente sofrendo de osteoporose (idades compreendidas entre os 18-92 anos; média+desvio padrão de 52,5±14,9 anos), e representativa da população feminina residente na cidade do Porto. Neste estudo foi observada uma ingestão de cálcio inferior à recomendada em 58,1% das mulheres com idades superiores a 70 anos; para a vitamina D a proporção de mulheres com aporte insuficiente foi bastante maior variando entre 70,5% na população com idade inferior a 30 anos e 96% entre os 60-69 anos de idade.
TratamentoA vitamina D usada para fins de substituição ocorre em 2 formas principais: o colecalciferol (vitamina D3, a forma animal natural) e o ergocalciferol (vitamina D2, derivado das plantas).
Em Portugal existem no mercado vários suplementos vitamínicos contendo a vitamina D, a maioria em associação com outros elementos. Nestes suplementos, a vitamina D é disponibilizada sob a forma de D2 ou D3. Estudos sugerem que estas 2 vitaminas são equivalentes; ambas aumentam os níveis séricos de 25(OH)D de forma semelhante, sugerindo uma absorção equivalente. Foi demonstrado, no entanto, que, apesar dos aumentos dos níveis séricos de 25(OH)D serem semelhantes após 3 dias nos doentes tratados com vitamina D3, os níveis séricos de 25(OH)D continuam a aumentar atingindo valores máximos após 14 dias. Nos doentes tratados com vitamina D2 os níveis séricos de 25(OH)D caem rapidamente; ao 14.° dia estes valores são idênticos aos observados antes do tratamento36,37.
Embora as vitaminas D3 e D2 sejam estruturalmente semelhantes, as diferenças entre elas são suficientes para causar uma resposta variável nos imunoensaios usados para medir as formas hidroxiladas dessas preparações.
Em Portugal, a Direção Geral de Saúde (DGS) publicou em abril de 2008 uma Circular Informativa aconselhando 700-800UI/dia de vitamina D nas pessoas com idade >65 anos com osteoporose38. Segundo dados da The Food and Nutrition Board of the National Academy of Sciences of USA39 a dose tóxica da vitamina D situa-se acima das 2.000UI/dia. Para além disso, não foi observada toxicidade com o uso continuado da vitamina D3 em doses até 10.000UI/dia, numa população adulta saudável40. Também o uso de doses elevadas (100.000UI de vitamina D3, de 4 em 4 meses) se revelou seguro numa população adulta e saudável com idade superior a 65 anos41.
Fármacos disponíveis no mercado portuguêsNo mercado português estão disponíveis 5 formas ativas para suplementação de vitamina D, cada uma com indicações específicas (tabela 1).
Fármacos disponíveis no mercado português,
| Princípio ativo | Colecalciferol | Calcifediol | Calcitriol | Alfacalcidol | Paricalcitol |
| Nome comercial | Vigantol® | Dedrogyl® | Rocaltrol® | Etalpha® | Zemplar® |
| Forma farmacêutica | Sol. Oral 10ml | Sol. Oral 10ml | Cápsulas | Sol. Oral 10mlCápsulas | CápsulasSol. Injetável 1 ml |
| Dose e composição | 0,5mg/ml(1 ml=30 gotas=20.000 UI vit. D3) | 0,15mg/ml(1 ml=30 gotas) | 0,25μg | 2μg/ml (sol. Oral)0,25μg, 0,5μg ou 1μg (cápsulas) | 1μg ou 2μg (Cápsulas)5μg/ml (Sol. Injetável) |
| Indicações | Carência de vitamina D; osteodistrofia renal; hipoparatiroidismo; raquitismo | Prevenção e tratamento do hiperparatiroidismo associado à insuficiência renal crónica | |||
| Reações adversas | Hipervitaminose (anorexia, cansaço, cefaleias, náuseas e vómitos, diarreia, perda de peso, poliúria, sede, suores, vertigens, aumento das concentrações de cálcio e fosfatos no sangue e urina) | ||||
| Contraindicações e precauções | Hipersensibilidade às vitaminas do grupo D, hipercalcemia, hipercalciúria e calcificação metastática. Monitorizar o cálcio sérico, especialmente em doentes a tomar digitálicos ou insuficientes renais. Gravidez e aleitamento | Hipersensibilidade às vitaminas do grupo D, hipercalcemia. Monitorizar a paratormona,o cálcio e fósforo séricos. Gravidez e aleitamento | |||
| Interações | Digitálicos, tiazidas, anticonvulsivantes e antiácidos | Digitálicos, cetoconazol, colestiramina e antiácidos | |||
| Posologia | Ajuste individual da dose diária, dependendo da calcémiaA ingestão total de cálcio não deve exceder os 800 mg/diaDose inicial recomendada variável, dependendo da situação clínica e do grupo etário, com ajuste periódico após monitorização da calcémia | Dose muito variável, dependendo das concentrações da paratormona, do cálcio e fósforo séricos, da situação clínica e do grupo etário, com ajustes periódicos após a sua monitorização | |||
| Notas | O tratamento é limitado a 7 dias, salvo casos excepcionais | O seu uso requer cuidados especiais, incluindo a avaliação periódica do cálcio plasmático e o controlo adequado da ingestão de cálcio | A solução injectável só deverá ser administrada após sessõesde hemodiálise | A via de administração habitual do medicamento é intravenosa através do acesso vascular durante a hemodiálise | |
Fonte: adaptado de Prontuário Terapêutico, Infarmed, edição 2011
O rastreio de défice de vitamina D faz-se através do doseamento da 25(OH)D. Apenas devem ser rastreadas as populações em risco, nomeadamente idosos, institucionalizados, grávidas e mulheres pós-menopausa (maior risco de fraturas), não sendo custoefetivo rastrear a população em geral.
Recomendações atuaisAs últimas orientações da Endocrine Society3, publicadas em 2011, sugerem o rastreio do défice de vitamina D apenas em indivíduos em risco e não na população em geral. Nestes doentes, recomenda-se a medição da 25(OH)D sérica circulante por um método analítico fiável. O défice de vitamina D é definido por um valor de 25(OH)D inferior a 20ng/ml (50nmol/l).
O doseamento de 1,25(OH)2D sérica não se recomenda para avaliação rotineira de défice de vitamina D. O seu doseamento é importante apenas na monitorização de certas patologias, como as doenças congénitas e adquiridas do metabolismo da vitamina D e fosfato.
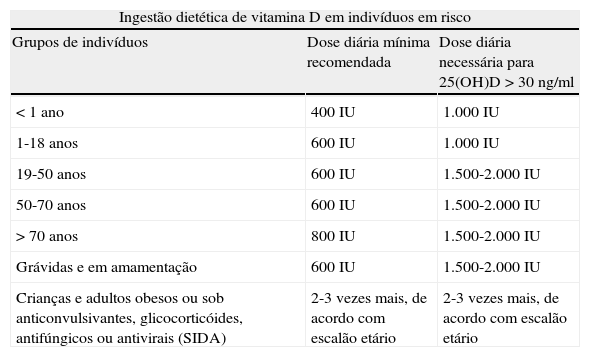
Em indivíduos em risco recomenda-se a ingestão de vitamina D na dieta (tabela 2). As crianças entre 0-1 anos necessitam, no mínimo, de 400IU/dia (1IU=25ng) de vitamina D. As crianças com um ano ou mais (até 18 anos) necessitam de, no mínimo, 600IU/dia para maximizar o desenvolvimento ósseo. No entanto, para manter os níveis séricos de 25(OH)D persistentemente acima de 30ng/ml (75nmol/L) pode ser necessária uma quantidade mínima de 1.000IU/dia de vitamina D. Os adultos entre os 19-50 anos necessitam de, no mínimo, 600IU/dia de vitamina D para otimizar a função muscular e óssea. Para manter valores de vitamina D persistentemente acima de 30ng/ml, pode ser necessário 1.500-2.000IU/dia de vitamina D. Todos os adultos com 50-70 anos necessitam de, pelo menos, 600IU/dia. Com mais de 70 anos as necessidades de vitamina D sobem para 800IU/dia. Para manter os níveis acima de 30ng/ml podem ser necessários suplementos de vitamina D até 1.500-2.000IU/dia.
Indicações da Endocrine Society para a ingestão de vitamina D em indivíduos em risco
| Ingestão dietética de vitamina D em indivíduos em risco | ||
| Grupos de indivíduos | Dose diária mínima recomendada | Dose diária necessária para 25(OH)D >30ng/ml |
| <1 ano | 400IU | 1.000IU |
| 1-18 anos | 600IU | 1.000IU |
| 19-50 anos | 600IU | 1.500-2.000IU |
| 50-70 anos | 600IU | 1.500-2.000IU |
| > 70 anos | 800IU | 1.500-2.000IU |
| Grávidas e em amamentação | 600IU | 1.500-2.000IU |
| Crianças e adultos obesos ou sob anticonvulsivantes, glicocorticóides, antifúngicos ou antivirais (SIDA) | 2-3 vezes mais, de acordo com escalão etário | 2-3 vezes mais, de acordo com escalão etário |
Mulheres grávidas e a amamentar necessitam, no mínimo, de 600IU/dia de vitamina D, com necessidade de 1.500-2.000IU/dia para manter níveis séricos de 25(OH)D acima de 30ng/ml.
Crianças e adultos obesos e aqueles sob medicação anticonvulsivante, glicocorticóides, antifúngicos (p. ex. cetoconazol) e antirretrovirais devem receber, no mínimo, 2-3 vezes mais vitamina D que o seu grupo etário, de forma a satisfazer as necessidades corporais de vitamina D.
O limite superior tolerável de manutenção de vitamina D (UL), que não deve ser excedido sem supervisão médica, deve ser de 1.000IU/dia em crianças até aos 6 meses, 1.500IU/dia em crianças dos 6 meses ao 1 ano de idade, 2.500IU/dia em crianças entre os 1-3 anos, 3.000IU/dia dos 4-8 anos e 4.000IU/dia para todos os indivíduos acima dos 8 anos de idade.
No entanto, valores mais elevados, de cerca de 2.000IU/dia em crianças dos 0-1 anos, 4.000IU/dia dos 1-18 anos e 10.000IU/dia para indivíduos a partir dos 19 anos, podem ser necessários para corrigir o défice de vitamina D.
A Endocrine Society sugere a utilização de qualquer das isoformas (vitamina D2 ou vitamina D3) para o tratamento e prevenção do défice de vitamina D.
Em crianças dos 0-1 anos de idade, com défice de vitamina D, sugere-se tratamento com 2.000IU/dia de vitamina D2 ou vitamina D3 ou com 50.000IU semanais, durante 6 semanas, de forma a atingir um nível sérico de 25(OH)D acima de 30ng/ml, seguida de terapêutica de manutenção de 400-1.000IU/dia. Crianças dos 1-18 anos de idade, com défice de vitamina D, devem ser tratadas com 2.000IU/dia de vitamina D2 ou vitamina D3 por um período mínimo de 6 semanas, ou com 50.000IU de vitamina D2 uma vez por semana, durante pelo menos 6 semanas, para atingir um nível sérico de 25(OH)D acima de 30ng/ml, seguida de terapêutica de manutenção com 600-1.000IU/dia.
Sugere-se que todos os adultos com défice de vitamina D sejam tratados com 50.000IU de vitamina D2 ou D3, uma vez por semana, durante 8 semanas, ou o seu equivalente de 6.000IU/dia de vitamina D2 ou vitamina D3, para atingir um nível sérico de 25(OH)D acima de 30ng/ml, seguida de terapêutica de manutenção com 1.500-2.000IU/dia.
Em doentes obesos, doentes com síndromes de malabsorção e doentes sob medicação que afeta o metabolismo da vitamina D, sugere-se uma dose mais elevada (2-3 vezes maior; no mínimo 6.000-10.000IU/dia) de vitamina D para corrigir o défice de vitamina D e manter um nível sérico de 25(OH)D acima de 30ng/ml, seguida de terapêutica de manutenção com 3.000-6.000IU/dia.
Em doentes com produção extrarrenal de 1,25(OH)2D sugere-se monitorização seriada dos níveis séricos de cálcio e 25(OH)D durante o tratamento com vitamina D para prevenir a hipercalcémia.
Em doentes com hiperparatiroidismo primário e défice de vitamina D sugere-se tratamento com vitamina D, de acordo com as necessidades, monitorizando os níveis séricos de cálcio.
Para obtenção dos benefícios não calcémicos da vitamina D, a Endocrine Society recomenda a suplementação com vitamina D para prevenção de quedas. No entanto, não se recomenda a suplementação além das necessidades diárias recomendadas, com o objetivo de prevenir a doença ou morte cardiovascular ou aumentar a qualidade de vida.
Experiência de um laboratório central (laboratório de hormonologia do Centro Hospitalar e Universitário de Coimbra)O método de ensaio laboratorial utilizado (Liaison 25 OH Vitamin D Total®) utiliza tecnologia de imunoensaio quimioluminescente (CLIA) para a determinação quantitativa de 25(OH)D e outros metabolitos hidroxilados da vitamina D no soro humano, plasma-EDTA ou plasma com lítio-heparina, a usar na avaliação da quantidade de vitamina D.
Este é um imunoensaio quimioluminescente competitivo (CLIA) direto, que determina a quantidade de 25(OH)D total no soro ou plasma. Durante a primeira incubação, a 25(OH)D é dissociada da sua proteína de ligação e liga-se ao anticorpo específico na fase sólida. Ao fim de 10 minutos é adicionado o marcador vitamina D ligado a um derivado de isoluminol. Após uma segunda incubação de 10 minutos, o material não ligado é removido com um ciclo de lavagem. Subsequentemente, os reagentes iniciadores são então adicionados e inicia-se uma reação quimioluminescente rápida. O sinal de luz é medido por um fotomultiplicador como unidades de luz relativas (RLU), sendo inversamente proporcional à concentração de 25(OH)D nos calibradores, nos controlos ou nas amostras.
Os valores séricos ou plasmáticos de 25(OH)D medidos encontram-se entre 4,0-150ng/ml. A concentração de 25(OH)D é apresentada em ng/ml. Para converter os resultados para unidades SI utiliza-se o seguinte cálculo: ng/mlx2,5=nmol/l.
É importante que cada laboratório estabeleça o seu próprio intervalo de referência, representativo da sua população típica.
A especificidade de deteção das diferentes formas da vitamina D é a seguinte: 25(OH)D2 - 104%; 25(OH)D3 - 100%, vitamina D2 - <1%, vitamina D3 - <1%, 1,25(OH)2 vitamina D2 - 40%, 1,25(OH)2 vitamina D3 - 17%, 3-epi-25-OH vitamina D3 - <1%.
O resultado do imunoensaio não sofre alterações com a hemólise (até 200mg/dl de hemoglobina), lipémia (até 549mg/dl de triglicéridos), bilirrubinémia (até 20mg/dl bilirrubina) ou colesterolémia (até 259mg/dl colesterol). No entanto, pode ser afetado por oscilações de temperatura, pelo que o ambiente laboratorial deve ser controlado. A contaminação bacteriana das amostras ou ciclos repetidos de congelação-descongelação podem ainda afetar os resultados do teste. Deve ainda ter-se em conta que o anticorpo utilizado neste ensaio revela reatividade cruzada com muitos metabolitos dihidroxilados da vitamina D; nos humanos, estes compostos estão presentes naturalmente em concentrações picomolares.
Os resultados dos ensaios devem ser usados em conjunto com outros dados clínicos e laboratoriais para ajudar o clínico a tomar decisões individuais de gestão dos pacientes numa população adulta.
Pode usar-se soro humano, plasma EDTA, plasma com lítio-heparina ou tubos SST. Recomenda-se o uso de amostras em jejum, mas não é necessário. O sangue deve ser recolhido assepticamente por punção venosa, deve permitir-se que coagule e o soro deve ser separado do coágulo logo que possível. Os espécimes podem ser armazenados em frascos de vidro ou de plástico. Não são necessários aditivos ou conservantes para manter a integridade da amostra. As amostras com partículas, turvação, lipémia ou restos de eritrócitos podem precisar de clarificação por filtração ou centrifugação antes de testar.
Evitar testar tanto amostras puramente hemolisadas ou lipémicas, como amostras que contenham partículas ou que apresentem contaminação microbiana óbvia. Se o ensaio for efetuado no prazo de 120 horas após a recolha da amostra, as amostras devem ser mantidas a 2-8°C; caso contrário, devem ser conservadas congeladas (a -20°C ou a uma temperatura inferior). Se as amostras forem armazenadas congeladas, misturar bem as amostras descongeladas antes de testar. Evitar os ciclos repetidos de congelação-descongelação. Verificar a presença de bolhas de ar e, se necessário, remover as mesmas antes de realizar o ensaio. O volume mínimo necessário é de 250ul de amostra para o primeiro teste e 25ul mais para cada teste adicional.
Resultados no tempo de estágioNo período de 1/09/2010 a 31/12/2010, foi determinada a 25(OH)D, no laboratório dos HUC em 2.071 pacientes, 61,3% do sexo feminino e 38,7% do sexo masculino, com uma média de idades de 54,0 anos.
Os pedidos de doseamentos efetuados tiveram origem, na sua maioria, em doentes acompanhados nos serviços de medicina interna (38,2%) e de endocrinologia (21,3%).
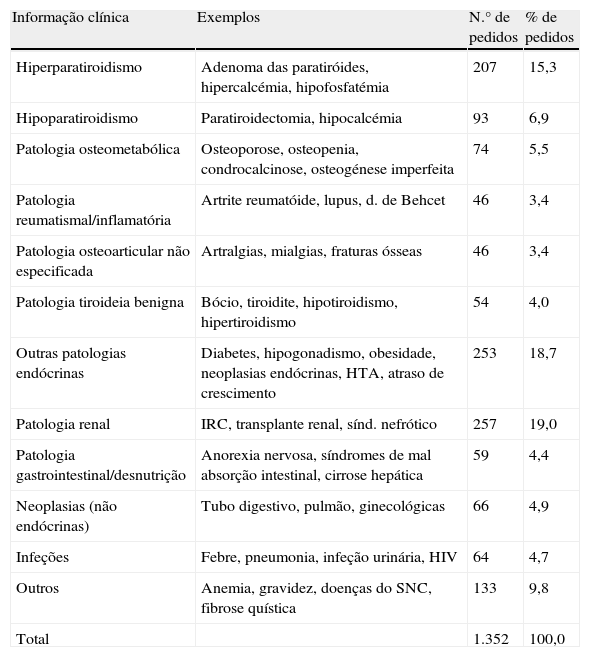
A informação clínica foi associada aos pedidos em apenas 65,3% dos casos (1.352 pedidos). Nestes, as informações foram variadas, sendo a maioria por insuficiência renal crónica, sem menção de alteração do metabolismo fosfocálcico. As patologias endócrinas mais frequentemente enumeradas foram o hiperparatiroidismo (207 casos; 15,3% do total), o hipoparatiroidismo (93 pedidos; 6,9% do total) e a diabetes mellitus (76 casos; 5,6% do total). A informação clínica dos pedidos efetuados apresenta-se na tabela 3.
Resultados dos pedidos de doseamento de 25-OHD no tempo de estágio
| Informação clínica | Exemplos | N.° de pedidos | % de pedidos |
| Hiperparatiroidismo | Adenoma das paratiróides, hipercalcémia, hipofosfatémia | 207 | 15,3 |
| Hipoparatiroidismo | Paratiroidectomia, hipocalcémia | 93 | 6,9 |
| Patologia osteometabólica | Osteoporose, osteopenia, condrocalcinose, osteogénese imperfeita | 74 | 5,5 |
| Patologia reumatismal/inflamatória | Artrite reumatóide, lupus, d. de Behcet | 46 | 3,4 |
| Patologia osteoarticular não especificada | Artralgias, mialgias, fraturas ósseas | 46 | 3,4 |
| Patologia tiroideia benigna | Bócio, tiroidite, hipotiroidismo, hipertiroidismo | 54 | 4,0 |
| Outras patologias endócrinas | Diabetes, hipogonadismo, obesidade, neoplasias endócrinas, HTA, atraso de crescimento | 253 | 18,7 |
| Patologia renal | IRC, transplante renal, sínd. nefrótico | 257 | 19,0 |
| Patologia gastrointestinal/desnutrição | Anorexia nervosa, síndromes de mal absorção intestinal, cirrose hepática | 59 | 4,4 |
| Neoplasias (não endócrinas) | Tubo digestivo, pulmão, ginecológicas | 66 | 4,9 |
| Infeções | Febre, pneumonia, infeção urinária, HIV | 64 | 4,7 |
| Outros | Anemia, gravidez, doenças do SNC, fibrose quística | 133 | 9,8 |
| Total | 1.352 | 100,0 |
Os resultados obtidos mostraram valores de 25(OH)D inferiores a 30ng/mL em 88,1% dos doentes avaliados, sendo que 65% do total de doentes apresentava valores inferiores a 20ng/mL (média 11,3ng/mL).
Esta elevada prevalência de défice de vitamina D está em concordância com os doseamentos de PTH efetuados nos mesmos doentes. O doseamento conjunto de PTH foi realizado apenas em 1.069 pacientes (51,6% do total). Os resultados mostram valores elevados em 55,3% dos doentes avaliados, com uma média de valores de 221,3pg/mL.
Em conclusão, verificou-se que a falta de correlação clínica, dada pela informação associada aos pedidos de 25(OH)D, é muito frequente, dificultando a interpretação dos resultados analíticos.
A maioria dos doseamentos efetuados mostrou uma elevada prevalência de défice de vitamina D (25(OH)D <30ng/mL em 88,1% dos doentes avaliados), o que se pode explicar pelo contexto de internamento e doença ativa nestes doentes.
Conflito de interessesOs autores declaram não haver conflito de interesses.