Apresentar um novo instrumento de classificação de risco pediátrico, o CLARIPED, e descrever as etapas de seu desenvolvimento.
MétodosEtapas do desenvolvimento: (i) primeira rodada de discussão entre especialistas, primeiro protótipo; (ii) pré‐teste de confiabilidade, 36 casos hipotéticos; (iii) segunda rodada de discussão para ajustes; (iv) treinamento da equipe; (v) pré‐teste com pacientes em tempo real; (vi) terceira rodada de discussão para novos ajustes; (vii) pré‐teste final de validade (20% dos atendimentos de cinco dias).
ResultadosO CLARIPED apresenta cinco categorias de urgência: Vermelha (emergência), Laranja (muito urgente), Amarela (urgente), Verde (pouco urgente) e Azul (sem urgência). A primeira etapa da classificação inclui a aferição de quatro sinais vitais (escore Vipe); a segunda etapa consiste na avaliação de discriminadores de urgência. Cada etapa resulta na atribuição de uma cor, seleciona‐se a de maior urgência para a classificação final. Cada cor corresponde a um tempo máximo de espera pelo atendimento médico e ao encaminhamento à área física mais adequada à condição clínica do paciente. A concordância interobservador foi substancial (kappa=0,79) e o pré‐teste final, com 82 atendimentos, evidenciou boa correlação entre a proporção de pacientes em cada categoria de urgência e o número de recursos usados (p<0,001).
ConclusõesO CLARIPED é um instrumento para classificação de risco simples, objetivo e de fácil uso, cujos pré‐testes sugerem boa confiabilidade e validade. Estudos em maior escala sobre sua validade e confiabilidade em diferentes contextos de saúde estão em curso e podem contribuir para a adoção de um sistema de classificação de risco pediátrico em âmbito nacional.
To present a new pediatric risk classification tool, CLARIPED, and describe its development steps.
MethodsDevelopment steps: (i) first round of discussion among experts, first prototype; (ii) pre‐test of reliability, 36 hypothetical cases; (iii) second round of discussion to perform adjustments; (iv) team training; (v) pre‐test with patients in real time; (vi) third round of discussion to perform new adjustments; (vii) final pre‐test of validity (20% of medical treatments in five days).
ResultsCLARIPED features five urgency categories: Red (Emergency), Orange (very urgent), Yellow (urgent), Green (little urgent) and Blue (not urgent). The first classification step includes the measurement of four vital signs (Vipe score); the second step consists in the urgency discrimination assessment. Each step results in assigning a color, selecting the most urgent one for the final classification. Each color corresponds to a maximum waiting time for medical care and referral to the most appropriate physical area for the patient's clinical condition. The interobserver agreement was substantial (kappa=0.79) and the final pre‐test, with 82 medical treatments, showed good correlation between the proportion of patients in each urgency category and the number of used resources (p<0.001).
ConclusionsCLARIPED is an objective and easy‐to‐use tool for simple risk classification, of which pre‐tests suggest good reliability and validity. Larger‐scale studies on its validity and reliability in different health contexts are ongoing and can contribute to the implementation of a nationwide pediatric risk classification system.
Um grande desafio na área da saúde, nas duas últimas décadas, tem sido encontrar soluções para a superlotação crescente nos serviços hospitalares de emergência. Uma das estratégias adotadas em vários países para lidar com o problema foi a implantação de sistemas de triagem, que consistem em classificar o grau de urgência de cada paciente, logo após a sua chegada ao setor de emergência, definindo uma fila de espera baseada no risco clínico, e não na ordem de chegada, para aguardar a avaliação médica e o tratamento.
Os instrumentos para triagem em serviços de emergência mais usados no mundo têm cinco níveis de urgência. São eles: a Escala Australiana de Triagem (ATS); a Escala Canadense de Triagem e Acuidade (CTAS); o Sistema de Triagem de Manchester (MTS) e o Índice de Gravidade na Emergência (ESI).1,2
No Brasil, o sistema de classificação de risco desenvolvido pelo Ministério da Saúde no programa Qualisus tem somente quatro categorias de urgência, não contempla as particularidades da faixa etária pediátrica e não tem alcançado adesão nacional expressiva.3,4 Por outro lado, os desenvolvidos na Europa, América do Norte e Austrália são complexos e tornam sua adoção em ampla escala problemática num contexto de saúde heterogêneo como o brasileiro. Além disso, as versões pediátricas desses modelos carecem de muitas especificidades para essa faixa etária e de literatura suficiente sobre sua validade e confiabilidade.
O objetivo deste estudo é apresentar um novo instrumento de classificação de risco para emergências pediátricas, o CLARIPED, e descrever as etapas de seu desenvolvimento. Estima‐se dessa forma chegar a uma ferramenta, confiável e válida, que apresente uma melhor adequação ao contexto de saúde brasileiro.
MétodoO desenvolvimento do CLARIPED se deu em sete etapas: (i) reuniões de especialistas para discussão do novo instrumento até a proposta de um protótipo (primeiro semestre de 2013); (ii) primeiro pré‐teste, com a aplicação do protótipo em 36 casos hipotéticos, submetidos a nove profissionais do serviço de emergência, após treinamento de três horas (agosto de 2013) e avaliação da concordância entre eles (estatística kappa); (iii) nova rodada de discussões a partir dos resultados do primeiro pré‐teste, que originou modificações no protótipo; (iv) novo treinamento dos profissionais da triagem, com supervisão e discussão de casos reais por um especialista (setembro de 2013); (v) segundo pré‐teste, feito em tempo real com a participação de toda a equipe de triagem, com o uso do segundo protótipo, após assinatura de Termo de Consentimento Livre e Esclarecido pelos responsáveis (outubro e novembro de 2013); (vi) nova rodada de discussões e apresentação da versão final a partir da incorporação das modificações propostas; (vii) estudo pré‐teste final de validade, com o objetivo de avaliar a associação entre as categorias de urgência e um desfecho proxy de urgência (número de recursos usados); para isso, aplicou‐se retrospectivamente a versão final do CLARIPED em uma amostra sistemática de 20% dos atendimentos feitos em cinco dias de dezembro de 2013; os níveis de urgência obtidos foram comparados com o número de recursos diagnósticos e/ou terapêuticos usados; os dados de triagem e de evolução foram obtidos por meio da revisão de prontuários. O estudo foi aprovado pelo Comitê de Ética em Pesquisa do Instituto D’Or de Pesquisa e Ensino (IDOR), sob o número 209.075/2013.
ResultadosUm grupo de especialistas (três médicos e duas enfermeiras) com ampla experiência em emergências pediátricas foi constituído com o objetivo de escolher e testar um instrumento de classificação de risco para o serviço de emergência pediátrica. Após ampla revisão de literatura, concluiu‐se que os quatro sistemas de triagem idealizados na América do Norte (CTAS e ESI), no Reino Unido (MTS) e na Austrália (ATS) não eram adequados para o nosso país por serem extensos, complexos ou carentes de especificidades para a pediatria. A Escala Sul Africana de Triagem (SATS),5 apesar de mais simples e adaptável ao contexto de saúde brasileiro, só apresentava quatro níveis de urgência, estratificação insuficiente de faixas etárias pediátricas, além de poucos estudos sobre seu uso em crianças. Decidiu‐se, então, pelo desenvolvimento de um novo sistema de triagem específico para emergências pediátricas.
O sistema CLARIPEDO CLARIPED é composto de cinco categorias de urgência: Vermelha (risco iminente de vida), Laranja (muito urgente), Amarela (urgente), Verde (pouco urgente) e Azul (sem urgência). A cada categoria atribui‐se um tempo máximo de espera para a avaliação médica e o encaminhamento para uma área de atendimento adequada ao nível de urgência do paciente, do seguinte modo: vermelho, atendimento imediato, sala de estabilização; laranja, atendimento em até 10 minutos, sala de observação; amarelo, até 30 minutos, sala de espera; verde, até 90 minutos, sala de espera; e azul, até 180 minutos, sala de espera. A classificação de risco deve se iniciar em no máximo 10 minutos após a chegada e registro do paciente, deve ser feita por um enfermeiro e ter duração de 2‐5 minutos.
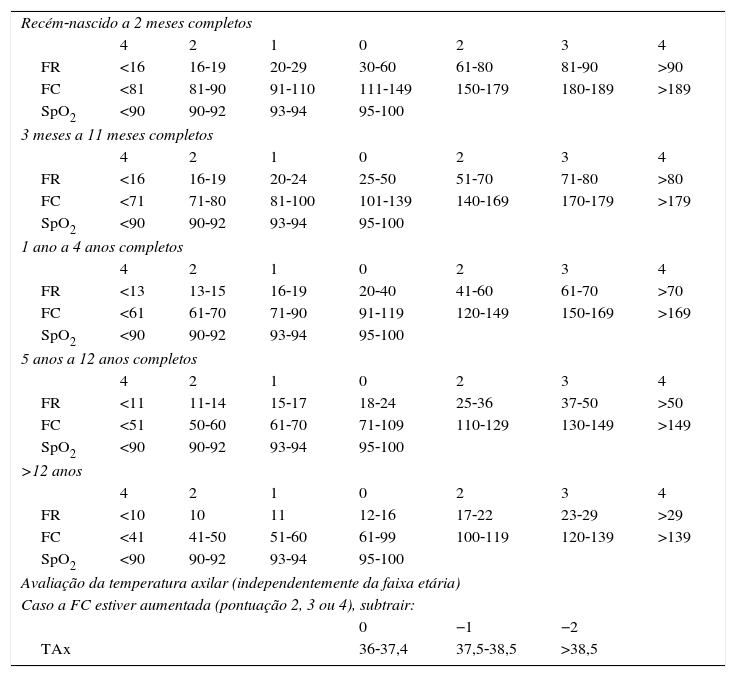
A primeira etapa se inicia com seis perguntas: motivo da consulta, alergia a medicações, se usa assistência pediátrica regular, morbidades associadas, medicações em uso e último peso aferido. Segue‐se a avaliação de quatro sinais vitais: frequência respiratória (FR), frequência cardíaca (FC), saturação de oxigênio (SpO2) e temperatura cutânea (Temp). A cada sinal vital aferido atribui‐se uma pontuação, que irá compor um escore (escore Vipe), que pode variar entre 0 e 12 e consiste na soma dos pontos dos três primeiros parâmetros, subtraídos da pontuação da temperatura em caso de FC aumentada (FR+FC+SpO2‐Temp, se FC aumentada). O escore Vipe deve, então, ser associado a uma das cinco cores: escore 0=Azul; 1 a 2=Verde; 3 a 5=Amarelo; 6 a 9=Laranja e ≥10=Vermelho (tabela 1).
Cálculo do escore Vipe (sinais vitais em pediatria)
| Recém‐nascido a 2 meses completos | |||||||
| 4 | 2 | 1 | 0 | 2 | 3 | 4 | |
| FR | <16 | 16‐19 | 20‐29 | 30‐60 | 61‐80 | 81‐90 | >90 |
| FC | <81 | 81‐90 | 91‐110 | 111‐149 | 150‐179 | 180‐189 | >189 |
| SpO2 | <90 | 90‐92 | 93‐94 | 95‐100 | |||
| 3 meses a 11 meses completos | |||||||
| 4 | 2 | 1 | 0 | 2 | 3 | 4 | |
| FR | <16 | 16‐19 | 20‐24 | 25‐50 | 51‐70 | 71‐80 | >80 |
| FC | <71 | 71‐80 | 81‐100 | 101‐139 | 140‐169 | 170‐179 | >179 |
| SpO2 | <90 | 90‐92 | 93‐94 | 95‐100 | |||
| 1 ano a 4 anos completos | |||||||
| 4 | 2 | 1 | 0 | 2 | 3 | 4 | |
| FR | <13 | 13‐15 | 16‐19 | 20‐40 | 41‐60 | 61‐70 | >70 |
| FC | <61 | 61‐70 | 71‐90 | 91‐119 | 120‐149 | 150‐169 | >169 |
| SpO2 | <90 | 90‐92 | 93‐94 | 95‐100 | |||
| 5 anos a 12 anos completos | |||||||
| 4 | 2 | 1 | 0 | 2 | 3 | 4 | |
| FR | <11 | 11‐14 | 15‐17 | 18‐24 | 25‐36 | 37‐50 | >50 |
| FC | <51 | 50‐60 | 61‐70 | 71‐109 | 110‐129 | 130‐149 | >149 |
| SpO2 | <90 | 90‐92 | 93‐94 | 95‐100 | |||
| >12 anos | |||||||
| 4 | 2 | 1 | 0 | 2 | 3 | 4 | |
| FR | <10 | 10 | 11 | 12‐16 | 17‐22 | 23‐29 | >29 |
| FC | <41 | 41‐50 | 51‐60 | 61‐99 | 100‐119 | 120‐139 | >139 |
| SpO2 | <90 | 90‐92 | 93‐94 | 95‐100 | |||
| Avaliação da temperatura axilar (independentemente da faixa etária) | |||||||
| Caso a FC estiver aumentada (pontuação 2, 3 ou 4), subtrair: | |||||||
| 0 | −1 | −2 | |||||
| TAx | 36‐37,4 | 37,5‐38,5 | >38,5 | ||||
Escore Vipe, 0 a 12, representa a soma dos pontos atribuídos a cada sinal vital. Entretanto, caso a frequência cardíaca esteja aumentada (pontuação 2, 3 ou 4), deve‐se subtrair da pontuação final ‐1, se a temperatura axilar estiver entre 37,5‐38,5°C e ‐2 se a temperatura axilar estiver >38,5°C.
Classificação da urgência: Azul (0), Verde (1‐2), Amarelo (3‐5), Laranja (6‐9) e Vermelho (≥10).
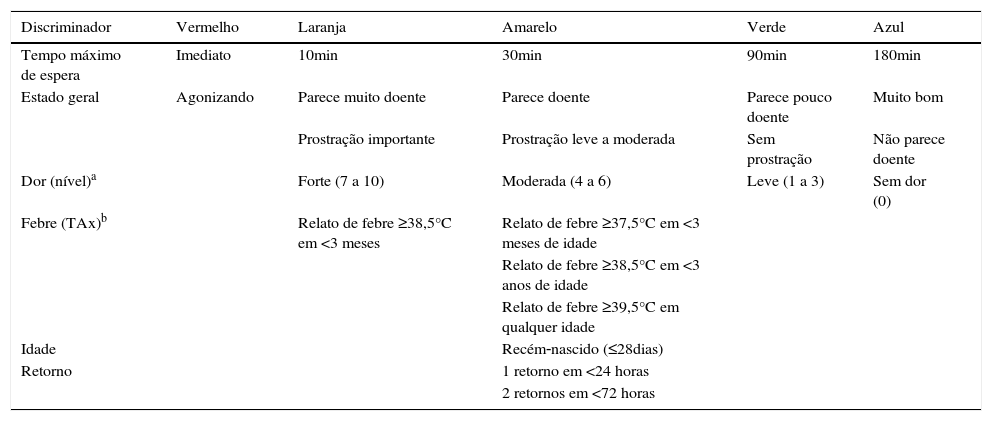
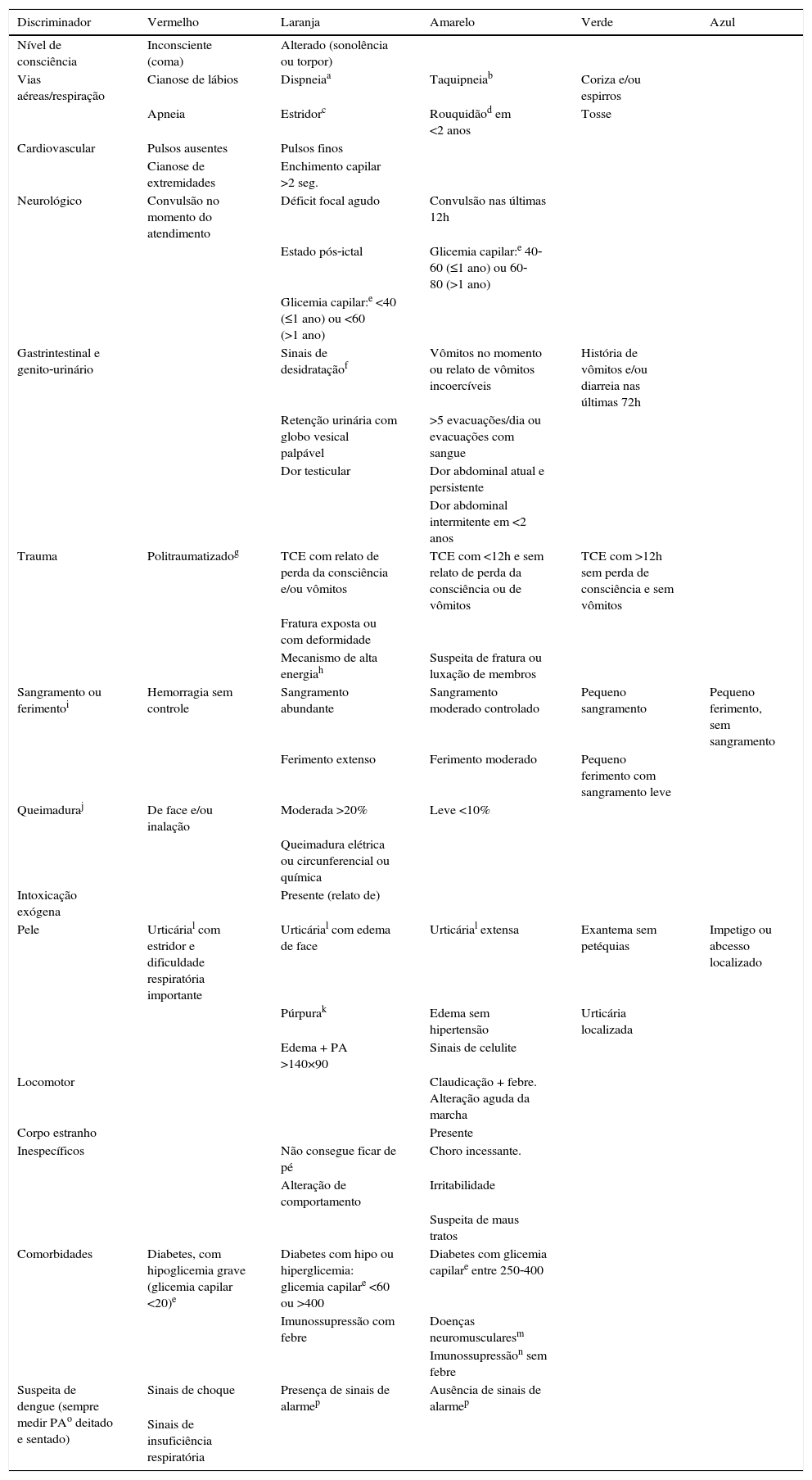
A segunda etapa consiste na consulta a tabelas de discriminadores, subdivididos por tipos ou sistemas de acometimento (linhas) e por categorias de urgência (colunas). A avaliação de cinco discriminadores gerais (dor, estado geral, relato de febre, idade e retorno) é obrigatória em todos os pacientes (tabela 2). Os demais discriminadores são avaliados de acordo com a queixa do paciente (tabela 3). Não é necessário consultar todas as linhas e colunas da segunda tabela, somente as linhas pertinentes aos motivos de consulta e as colunas das categorias de urgência mais elevadas do que a atribuída pelo Escore Vipe. Se estiver presente um discriminador que corresponde a um nível de urgência mais elevado do que o atribuído pelo Escore Vipe, o nível de maior urgência determinará a classificação final. Não se pode rebaixar a urgência dada pelo Escore Vipe, somente elevá‐la a partir da avaliação dos discriminadores.
Discriminadores CLARIPED gerais e obrigatórios
| Discriminador | Vermelho | Laranja | Amarelo | Verde | Azul |
|---|---|---|---|---|---|
| Tempo máximo de espera | Imediato | 10min | 30min | 90min | 180min |
| Estado geral | Agonizando | Parece muito doente | Parece doente | Parece pouco doente | Muito bom |
| Prostração importante | Prostração leve a moderada | Sem prostração | Não parece doente | ||
| Dor (nível)a | Forte (7 a 10) | Moderada (4 a 6) | Leve (1 a 3) | Sem dor (0) | |
| Febre (TAx)b | Relato de febre ≥38,5°C em <3 meses | Relato de febre ≥37,5°C em <3 meses de idade | |||
| Relato de febre ≥38,5°C em <3 anos de idade | |||||
| Relato de febre ≥39,5°C em qualquer idade | |||||
| Idade | Recém‐nascido (≤28dias) | ||||
| Retorno | 1 retorno em <24 horas | ||||
| 2 retornos em <72 horas |
Discriminadores CLARIPED de acordo com o motivo da consulta
| Discriminador | Vermelho | Laranja | Amarelo | Verde | Azul |
|---|---|---|---|---|---|
| Nível de consciência | Inconsciente (coma) | Alterado (sonolência ou torpor) | |||
| Vias aéreas/respiração | Cianose de lábios | Dispneiaa | Taquipneiab | Coriza e/ou espirros | |
| Apneia | Estridorc | Rouquidãod em <2 anos | Tosse | ||
| Cardiovascular | Pulsos ausentes | Pulsos finos | |||
| Cianose de extremidades | Enchimento capilar >2 seg. | ||||
| Neurológico | Convulsão no momento do atendimento | Déficit focal agudo | Convulsão nas últimas 12h | ||
| Estado pós‐ictal | Glicemia capilar:e 40‐60 (≤1 ano) ou 60‐80 (>1 ano) | ||||
| Glicemia capilar:e <40 (≤1 ano) ou <60 (>1 ano) | |||||
| Gastrintestinal e genito‐urinário | Sinais de desidrataçãof | Vômitos no momento ou relato de vômitos incoercíveis | História de vômitos e/ou diarreia nas últimas 72h | ||
| Retenção urinária com globo vesical palpável | >5 evacuações/dia ou evacuações com sangue | ||||
| Dor testicular | Dor abdominal atual e persistente | ||||
| Dor abdominal intermitente em <2 anos | |||||
| Trauma | Politraumatizadog | TCE com relato de perda da consciência e/ou vômitos | TCE com <12h e sem relato de perda da consciência ou de vômitos | TCE com >12h sem perda de consciência e sem vômitos | |
| Fratura exposta ou com deformidade | |||||
| Mecanismo de alta energiah | Suspeita de fratura ou luxação de membros | ||||
| Sangramento ou ferimentoi | Hemorragia sem controle | Sangramento abundante | Sangramento moderado controlado | Pequeno sangramento | Pequeno ferimento, sem sangramento |
| Ferimento extenso | Ferimento moderado | Pequeno ferimento com sangramento leve | |||
| Queimaduraj | De face e/ou inalação | Moderada >20% | Leve <10% | ||
| Queimadura elétrica ou circunferencial ou química | |||||
| Intoxicação exógena | Presente (relato de) | ||||
| Pele | Urticárial com estridor e dificuldade respiratória importante | Urticárial com edema de face | Urticárial extensa | Exantema sem petéquias | Impetigo ou abcesso localizado |
| Púrpurak | Edema sem hipertensão | Urticária localizada | |||
| Edema + PA >140×90 | Sinais de celulite | ||||
| Locomotor | Claudicação + febre. Alteração aguda da marcha | ||||
| Corpo estranho | Presente | ||||
| Inespecíficos | Não consegue ficar de pé | Choro incessante. | |||
| Alteração de comportamento | Irritabilidade | ||||
| Suspeita de maus tratos | |||||
| Comorbidades | Diabetes, com hipoglicemia grave (glicemia capilar <20)e | Diabetes com hipo ou hiperglicemia: glicemia capilare <60 ou >400 | Diabetes com glicemia capilare entre 250‐400 | ||
| Imunossupressão com febre | Doenças neuromuscularesm | ||||
| Imunossupressãon sem febre | |||||
| Suspeita de dengue (sempre medir PAo deitado e sentado) | Sinais de choque | Presença de sinais de alarmep | Ausência de sinais de alarmep | ||
| Sinais de insuficiência respiratória |
Glicemia capilar (mg/dL): fazer o teste em todo paciente com alteração do nível de consciência, convulsão recente ou atual, prostração importante ou história prévia de diabete.
Sinais de desidratação: boca seca, olhos fundos, sem urinar nas últimas 12 horas, turgor de pele diminuído.
Mecanismo de alta energia (na falta de informação considerar qualquer acidente de trânsito como mecanismo de alta energia): a) acidente com veículo a motor: >60Km/h (colisão com cinto); >40Km/h (colisão sem cinto); >30Km/h (moto) e >10Km/h (atropelamento); b) queda de mais de um metro de altura.
Ferimento: a) pequeno: escoriações e contusões sem necessidade de sutura; b) moderado: pequenas feridas corto‐contusas com necessidade de sutura, mas com sangramento controlado; c) extenso: feridas corto‐contusas extensas com necessidade de sutura, com sangramento abundante e mantido.
Urticária: diferente de outros exantemas; placas hiperemiadas e elevadas, em geral muito pruriginosas, mas nem sempre.
Imunossupressão: pós‐quimioterapia, síndrome nefrótica em atividade, uso crônico de corticosteroide.
Na presença de discriminadores evidentes de emergência ou muita urgência, como convulsões, nível de consciência comprometido, apneia, cianose e outros, o paciente é enviado para abordagem médica rápida ou imediata, antes de qualquer procedimento administrativo. O processo de classificação de risco, então, é feito retrospectivamente.
Estudos pré‐testeOs cenários clínicos hipotéticos, idealizados pelos especialistas para treinamento, tinham a seguinte distribuição de urgências: Vermelho 11%, Laranja 42%, Amarelo 31%, Verde 8% e Azul 8%. O kappa geral para múltiplos observadores resultante do primeiro pré‐teste com 36 cenários clínicos hipotéticos foi 0,79 e o kappa para cada categoria de urgência foi 0,93 (Vermelho); 0,82 (Laranja); 0,73 (Amarelo); 0,65 (Verde) e 0,93 (Azul), com desvio‐padrão de 0,03 e p<0,001, o que demonstrou uma substancial confiabilidade do instrumento.
O segundo pré‐teste, feito com pacientes em tempo real, determinou modificações em relação aos limites e à pontuação dos parâmetros fisiológicos e em relação a alguns discriminadores (recém‐nascido, retorno com menos de 24 horas, relato de febre, dor abdominal e traumatismo crânio encefálico).
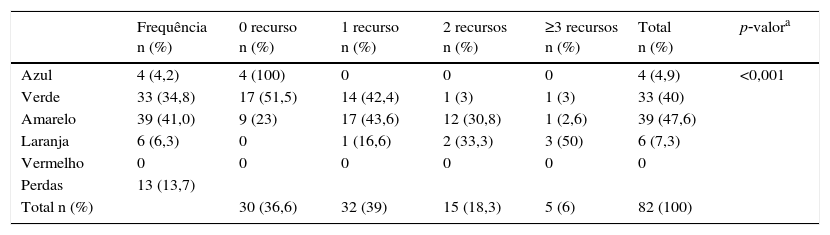
O pré‐teste final de validade, com amostra retrospectiva de atendimentos, incluiu a análise de 82 prontuários de uma amostra sistemática de 95 atendimentos, correspondentes a 20% da população atendida nos primeiros cinco dias de dezembro de 2013. O objetivo foi avaliar a distribuição das categorias de urgência e sua associação com um desfecho proxy de urgência, como número de recursos diagnósticos e terapêuticos usados. A distribuição de urgências foi: Azul (4,2%); Verde (34,7%); Amarelo (41%); Laranja (6,3%) e Vermelho (0%). Nenhum dos atendimentos classificados como Azul usou algum recurso diagnóstico e/ou terapêutico no setor da emergência; um terço dos Verdes usou um recurso; metade dos Amarelos usou um recurso e 20% usaram dois ou mais recursos; mais de 80% dos Laranjas usaram dois ou mais recursos (tabela 4; p<0,001).
Pré‐teste de validade piloto: uso de recursos de tratamento de acordo com o nível de classificação de risco
| Frequência n (%) | 0 recurso n (%) | 1 recurso n (%) | 2 recursos n (%) | ≥3 recursos n (%) | Total n (%) | p‐valora | |
|---|---|---|---|---|---|---|---|
| Azul | 4 (4,2) | 4 (100) | 0 | 0 | 0 | 4 (4,9) | <0,001 |
| Verde | 33 (34,8) | 17 (51,5) | 14 (42,4) | 1 (3) | 1 (3) | 33 (40) | |
| Amarelo | 39 (41,0) | 9 (23) | 17 (43,6) | 12 (30,8) | 1 (2,6) | 39 (47,6) | |
| Laranja | 6 (6,3) | 0 | 1 (16,6) | 2 (33,3) | 3 (50) | 6 (7,3) | |
| Vermelho | 0 | 0 | 0 | 0 | 0 | 0 | |
| Perdas | 13 (13,7) | ||||||
| Total n (%) | 30 (36,6) | 32 (39) | 15 (18,3) | 5 (6) | 82 (100) |
A proposta de desenvolver um instrumento simples, objetivo e de fácil uso para classificação de risco em emergências pediátricas, adequado a um contexto de saúde brasileiro, resultou no CLARIPED. A magnitude continental e a heterogeneidade do país tornam difíceis a adoção de um sistema de classificação de risco em âmbito nacional. A opção de desenvolver um novo instrumento, em detrimento do uso de outros sistemas de triagem mais estudados, justifica‐se. Os sistemas mais usados no mundo foram desenvolvidos em países da América do Norte,6,7 Europa8 e Austrália.9 O contexto de saúde desses países é bastante diverso do de países da América Latina, tanto em termos de epidemiologia dos eventos de saúde quanto da formação, disponibilidade e habilidade dos recursos humanos. O SATS, um sistema de triagem simplificado, desenvolvido num país africano com muitas semelhanças socioeconômicas e demográficas com o Brasil, poderia ser um instrumento mais adequado. Desenvolvido e implantado na Cidade do Cabo em 2006, com a denominação de Cape Town Score (CTS), foi posteriormente adotado em todo o país como South African Triage Scale (SATS).10–12 O CLARIPED manteve a logística do processo de triagem em duas etapas, preconizadas pelo SATS, aferição de parâmetros fisiológicos, seguida de avaliação da presença de discriminadores, mas várias modificações foram necessárias e estão discriminadas a seguir.
Embora o SATS apresente cinco cores, a rigor ele só tem quatro níveis de urgência, uma vez que o nível Azul não se refere a pacientes sem urgência, e sim a pacientes que chegam sem vida ao setor. No contexto de saúde brasileiro, o afluxo de pacientes ambulatoriais aos serviços de emergência é grande.3,4 Justifica‐se, assim, a existência de um nível para pacientes não urgentes, à semelhança de outros sistemas, como MTS,8 ESI‐4,6 PaedCTAS7 e ATS.9 Os instrumentos de triagem com cinco categorias de urgência demonstraram maior confiabilidade e validade do que instrumentos com menos categorias.13
No CLARIPED, optou‐se pela estratificação em cinco faixas etárias, em vez de três, como no SATS. Essa opção está de acordo com tabelas de sinais vitais recomendadas em livros textos de pediatria14,15 e com outros instrumentos de triagem, que usam quatro ou mais faixas.6,7 Entretanto, há uma carência de estudos que validem a estratificação de faixas etárias para sinais vitais em pediatria. O Escore Pediátrico de Sinais de Alerta à Beira do Leito (Bedside Pediatric Early Warning System Score – Bedside PEWS Score), um instrumento desenvolvido para detectar precocemente a deterioração clínica de crianças internadas, foi derivado de métodos estatísticos e recentemente validado.16 A estratificação em cinco faixas etárias do CLARIPED baseou‐se nesse instrumento.
Embora ainda não haja um consenso internacional sobre os parâmetros a serem incluídos em um instrumento de triagem, há evidências de que os sinais vitais devem ser parte integrante de um processo de classificação de risco seguro, particularmente em crianças.5,17,18 Entretanto, a aferição de sinais vitais pode ser extremamente difícil no âmbito da emergência, principalmente nas crianças pequenas ou pouco cooperativas. Selecionar os parâmetros mais objetivos, que representem uma contribuição eficaz para a discriminação de urgências, é de importância fundamental para atingir as metas de tempo e aprimoramento do processo. No SATS, a primeira etapa inclui a avaliação de sete parâmetros: FR, FC, pressão arterial sistólica (PAS), Temp, nível de consciência, mobilidade e presença de trauma. A versão pediátrica revisada do SATS excluiu a aferição da PAS. O PaedCTAS7 recomenda a aferição da FC, FR e SpO2 como modificadores de primeira ordem, enquanto o ESI‐46 preconiza a medida dos mesmos três sinais vitais somente em determinadas circunstâncias. O ATS19 deixa a critério do profissional da triagem a necessidade de aferir sinais vitais. No CLARIPED, os quatro sinais vitais selecionados e a pontuação atribuída a cada um basearam‐se em estudos sobre o desenvolvimento de dois instrumentos que usaram métodos estatísticos para avaliar a capacidade de alguns parâmetros fisiológicos para prever desfechos evolutivos: o Bedside Pews16 e o Pediatric Emergency Assessment Tool (PEAT),20 um modelo multivariado para predizer três níveis de cuidados requeridos por pacientes pediátricos no serviço de emergência.
A inclusão da SpO2 no escore Vipe baseou‐se não só no uso em outros instrumentos já validados, como o ESI‐4,6 o PaedCTAS7 e o Bedside Pews Score,16 como também em evidências de que pacientes com SpO2 baixa usualmente não apresentam aumento de frequência respiratória e que sua aferição pode gerar mudanças significativas no tratamento de uma parcela de pacientes atendidos em serviços de emergência pediátrica.21,22
A exclusão da pressão arterial do Escore Vipe baseou‐se na evidência de que o benefício de sua aferição obrigatória em pacientes pediátricos no serviço de emergência é limitado.23 Por um lado, a hipotensão é um sinal de choque tardio em crianças. Por outro lado, a triagem de crianças com hipertensão arterial no serviço de emergência pode resultar em elevada prevalência de falsos positivos.24 Outros instrumentos de triagem, como o MTS,8 o Paed CTAS,7 o ESI‐46 e o ATS,19 não incluem a medida obrigatória da pressão arterial, mas apenas a avaliação inicial da presença de choque a partir de sinais clínicos evidentes, como diminuição da amplitude dos pulsos, enchimento capilar retardado, sudorese e palidez.
A correção da FC pela intensidade da febre é um aspecto único do CLARIPED e baseou‐se no fato de que a taquicardia é um dos parâmetros da síndrome da resposta inflamatória sistêmica (SRIS) e da sepse.25 Estudo recente propõe correção semelhante na avaliação de crianças com infecção aguda.26 Nenhum outro sistema de triagem considera essa correção. A valorização da intensidade da febre, por outro lado, é considerada na etapa dos discriminadores, de acordo com a idade e segue as recomendações do Colégio Americano de Médicos de Emergência.27 Entretanto, diferentemente de outros sistemas de triagem, no CLARIPED leva‐se em conta não só a febre atual, mas o relato de febre nas últimas 24 horas.
No CLARIPED, a avaliação do nível de consciência e da presença de trauma foi deslocada para a etapa dos discriminadores. Em vez de considerar o comprometimento do nível de consciência em quatro categorias (alerta, resposta à dor, resposta à voz e não responsivo), como preconizado no SATS,11 o CLARIPED considera que a presença de qualquer comprometimento da consciência coloca o paciente no nível Laranja (muito urgente). Essa estratégia já é usada no MTS,8 no ESI‐4,6 no PaedCTAS7 e no ATS.19
No CLARIPED o trauma é avaliado não só quanto à sua presença ou ausência, como preconizado no SATS, mas de acordo com aspectos sobre o mecanismo, a extensão, a localização e a presença de sintomas. A valorização do mecanismo e da intensidade do trauma também é usada em outros instrumentos. O PaedCTAS7 e o ATS19 valorizam a presença de um mecanismo de alta energia, independentemente de sintomas clínicos, para classificar o paciente em categorias de maior urgência. No MTS8 existe um fluxograma específico para grandes traumas, em que o paciente é classificado no nível um, dois ou no mínimo três de urgência, em função das manifestações clínicas.
Finalmente, a tabela de discriminadores usada na segunda etapa do CLARIPED difere muito da usada no SATS, em termos de conteúdo e organização. Assim como no PaedCTAS,7 os discriminadores são agrupados por sistemas orgânicos. O instrumento canadense, entretanto, é muito mais extenso e complexo, abrange 167 queixas agrupadas em 17 sistemas orgânicos.
Estudo recente sobre o SATS5 demonstrou que a combinação das duas etapas, avaliação de parâmetros fisiológicos e avaliação de discriminadores clínicos na triagem de crianças, aumentou significativamente a sensibilidade (91%), em comparação com o uso de cada etapa isoladamente (57,1% e 75,6%, respectivamente). No CLARIPED, considera‐se que o cálculo do Escore Vipe tem um peso menor na sensibilidade do instrumento, embora essa hipótese ainda não tenha sido testada.
O pré‐teste final de validade com uma amostra de 82 atendimentos encontrou distribuição de urgências semelhante à de outros estudos.28–30 A associação entre os cinco níveis de urgência e o número de recursos usados sugerem uma boa validade do instrumento.
Algumas limitações podem ser apontadas no desenvolvimento do modelo CLARIPED. A primeira se refere à metodologia para obter consenso sobre as modificações propostas e sobre a escolha e organização dos discriminadores. Uma metodologia Delphi, que garantisse anonimato entre os especialistas participantes, interação com feedback controlado e tratamento estatístico das respostas às sucessivas rodadas de interação, seria o método de eleição para minimizar vieses e ruídos e assegurar a prevalência da opinião da maioria. Por outro lado, o desenvolvimento do instrumento em várias etapas garantiu a sistematização do processo e uma ampla participação dos profissionais do setor de emergência no desenvolvimento e amadurecimento do instrumento até sua última versão. A segunda limitação refere‐se ao uso do CLARIPED em outros contextos de saúde. Pode‐se alegar que as especificidades do contexto no qual o CLARIPED foi idealizado limita a sua aplicação em outros locais. Discriminadores mais específicos relacionados a emergências oftalmológicas ou psiquiátricas, por exemplo, estão ausentes no CLARIPED. Entretanto, a busca pela simplicidade, objetividade e facilidade de treinamento do instrumento pode tornar viável a sua adaptação e disseminação em outras regiões brasileiras menos desenvolvidas por meio da inclusão de discriminadores mais abrangentes e/ou específicos para determinados contextos. A preocupação de refinar a discriminação entre as urgências intermediárias (Amarelo [urgente] vs. Verde [pouco urgente]) também torna a ferramenta teoricamente aplicável a serviços de pronto atendimento. Entretanto, o instrumento não se presta para triagem de eventos críticos em massa em ambientes externos. Instrumentos específicos com foco em triagem de pacientes graves em ambiente extra‐hospitalar são necessários para essa finalidade.
Pode‐se concluir que o desenvolvimento do CLARIPED para classificação de risco em emergências pediátricas resultou em um instrumento simples, objetivo e de fácil uso, cujos pré‐testes sugerem boa confiabilidade e validade. Estudos em maior escala sobre sua validade, confiabilidade e aplicação em diferentes contextos de saúde encontram‐se em curso e podem contribuir para a adoção de um sistema de classificação de risco pediátrico em âmbito nacional.
FinanciamentoCNPq (Conselho Nacional de Desenvolvimento Científico e Tecnológico, processo n° 448855/2014‐3). Faperj (Fundação Carlos Chagas Filho de Amparo à Pesquisa do Estado do Rio de Janeiro, processo n° E‐26/010.000196/2015).
Conflitos de interesseOs autores declaram não haver conflitos de interesse.