¿ Introducción
En abril de 2009 se identificaron por primera vez infecciones en seres humanos causadas por un virus nuevo al cual se le dio el nombre de: influenza tipo A (H1N1).1,2 Se observó que los grupos etarios más afectados correspondían a adultos de entre los 20 y 49 años de edad, representando 32% del total de la población afectada por este nuevo virus, según datos de la Secretaria de Salud hasta el mes de septiembre. Esto representa que las mujeres en edad reproductiva son un grupo de alto riesgo tanto para ellas como para el feto.3 Existe incertidumbre mundial en cuanto al abordaje clínico y terapéutico de los recién nacidos cuyas madres tuvieron contacto con este virus.
¿ Antecedentes
En 1918 y hasta 1920, ocurrió una pandemia denominada como influenza española que causó entre 50 y 100 millones de muertes, enfermando a una tercera parte de la población mundial, hoy se sabe que en aquel entonces el virus causal fue un subtipo H1N1. En 1957 ocurrió otra epidemia menos catastrófica conocida como influenza asiática. Sin embargo, en las epidemias de 1918 y 1957 se estima que el porcentaje de mortalidad en mujeres embarazadas fue de 27% y 20% respectivamente. Otras epidemias ocurrieron en 1968 (Hong Kong) y en 1977 en Rusia.4,5
Sin embargo, las últimas pandemias de que se tiene reporte han sido causadas por virus recombinantes y se ha demostrado que han evolucionado en hospederos como caballos, gaviotas, pájaros norteamericanos, aves euroasiáticas, en cerdos y en humanos.1,3,6,7
Durante el mes de marzo y abril de 2009, se identificaron casos en nuestro país y en Estados Unidos de un virus nuevo tipo A, hasta entonces no tipificable, conocido más tarde a nivel mundial con el nombre científico de H1N1. Como resultado de la recombinación genética de los virus de la influenza humana, porcina y aviaria.5,8 Para junio de ese mismo año, se consideró una pandemia, demostrando así la rápida difusión de esta enfermedad.9
Agente etiológico: El virus de la influenza humana pertenece a la familia de los ortomixovirus; consta de los subtipos A, B, C y de los Thogavirus. En los seres humanos sólo los virus de la influenza A y B son de interés epidemiológico. Los principales factores determinantes antigénicos de los virus de la influenza A y B son la hemaglutinina (H o HA) y neuraminidasa (N o NA) glucoproteínas transmembrana. Basado en la antigenicidad de las glucoproteínas el virus de la influenza A se subdividen en dieciséis subtipos de H (H1 a H16) y nueve para N (N1 a N9), todas antigénicamente distintas.2,8,10
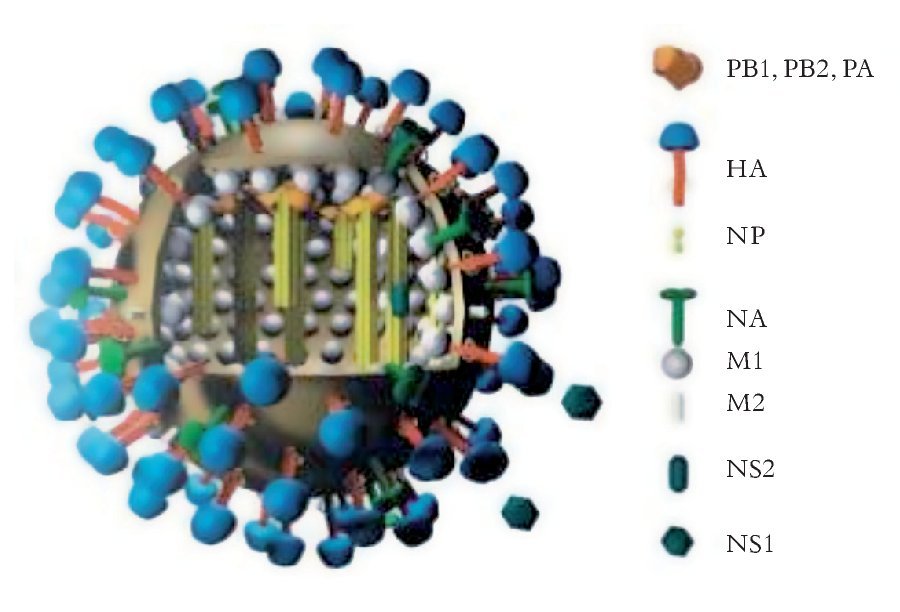
Tanto el virus A como el B consta de ocho diferentes segmentos genómicos cubiertos por una proteína de nucleocápside, juntos constituyen una ribonucleoprotéina cada segmento codifica para una proteína funcionalmente importante, la estructura consta de tres polimerasas (PA, PB1 y PB2), una hemaglutinina (HA) una proteína de nucleocapside (NP), una neuraminidasa (NA o N), una proteína de matriz (M) a la cual se le atribuye el mantenimiento del pH ácido del endosoma y una última no estructural (NS) cuya función aún no es definida (Figura 1).
¿ Figura 1. Nótense los ocho diferentes segmentos genómicos.
La hemaglutinina juega un papel primordial en la unión a los receptores celulares, en tanto que la neuraminidasa tiene un rol crucial en la liberación de las células infectadas así como en la replicación viral.2 ,8,10
El virus de la influenza humana consta de una sola cadena de ARN con apariencia pleomorfica teniendo un diámetro promedio de 120 nm, y las proyecciones de la hemaglutinina y de la neuraminidasa cubren la partícula.
Por lo tanto, cuando un virus originado en una especie animal contamina a otra especie diferente, el hospedero sufre una rápida evolución y puede inducir alrededor de 256 diferentes combinaciones de ácidos nucleícos por el entrecruzamiento de los ocho diferentes segmentos genómicos del virus.2,7,8,10
El virus nuevo de influenza tipo A H1N1 causal de la pandemia actual, es una recombinación de los virus de la influenza humana, porcina y aviaria.7,8
Dos cualidades son importantes a considerar en el origen de la pandemia causada por el virus de la influenza humana; la primera es la capacidad de salir y circular en los reservorios como las aves y los cerdos, ya sea por contacto directo o por redistribución génica, para posteriormente diseminarse en los humanos en intervalos regulares de tiempo. El segundo; es la manera rápida y el cambio antigénico impredecible, lo cual le impide ser blanco inmunológico una vez que el virus se ha establecido en un ser humano.2,7,8,10,11
Grupos vulnerables: Con la información disponible hasta el momento, es difícil establecer quienes están en riesgo alto de contraer la infección por el virus nuevo de la influenza Tipo A H1N1 o quienes podrían desarrollar complicaciones secundarias a esta viremia. Hasta el momento la evidencia muestra que el riesgo de infección por el virus nuevo de la influenza A H1N1 es el mismo en las personas susceptibles de infección por influenza o gripe estacional.10
A medida de que se disponga de más datos epidemiológicos y clínicos se podrá establecer grupos específicos de riesgo.
Este artículo se enfoca principalmente a dos poblaciones de riesgo, de interés para los médicos neonatólogos, la mujer embarazada y sus recién nacidos.
¿ Patogénesis en grupos vulnerables
En las pandemias de 1918 y 1957 se observó que la neumonía se presentó en 50% de las mujeres embarazadas, con 50% de mortalidad y en la mitad de los casos el embarazo se interrumpió por aborto espontáneo o por el parto.11,12
Los mecanismos por los cuales ocurrió la pandemia de 1918 fueron la transmisión directa y la reagrupación de los virus aviar y humano, se cree que la epidemia actual incluso podría ser un remante genético de la ocurrida en 1918.3,4
En los periodos interpandémicos se encontró que las embarazadas poseen un riesgo mayor de sufrir complicaciones durante el segundo y tercer trimestre.3,4
El riesgo de complicaciones es alto en los niños menores de seis meses con cualquier tipo de influenza estacional, por lo cual se ha considerado a los recién nacidos como una población en riesgo ante este nuevo virus H1N1, y con los datos de las pandemias se ha especulado cual es el efecto en los fetos y recién nacidos de mujeres que presentan la enfermedad. La evidencia hasta el momento es menos consistente, aun cuando ya se han descrito efectos teratógenos.12-16
Transmisión: Continúa siendo objeto de estudio la pandemia del pasado mes de abril. La evidencia hasta el momento marca que el principal mecanismo de trasmisión del virus nuevo de influenza es a través de partículas grandes provenientes de las secreciones del tracto respiratorio, lo que requiere de un contacto cercano entre las personas, dado que las gotitas no permaneces suspendidas en el aire y sólo pueden viajar menos de 1.80 metros.1,2,6,10
El contacto a través de superficies contaminadas también es posible, aunque aún es incierta la forma en cómo estos modos de transmisión influyen en las características epidemiológicas del brote. También se desconoce el riesgo de infección por secreciones provenientes del aparato ocular, conjuntival o gastrointestinal; por lo tanto, se recomienda que las secreciones y líquidos corporales de pacientes infectados con el virus nuevo de influenza se manejen con precaución ya que pueden ser potencialmente infectantes.
Transmisión trans-placentaria: Los últimos reportes han demostrado que las mujeres embarazadas e infectadas con el virus H1N1, al igual que las infectadas con influenza aviar H5N1, pueden tener transmisión trans-placentaria.4, 9,10,17,18
No se ha podido demostrar hasta el momento que los recién nacidos cuyas madres se infectaron con el nuevo virus de la influenza hayan tenido mayor riesgo de; peso bajo al nacer, anomalías congénitas o calificaciones bajas de Apgar, comparados con madres no infectadas.6,16,19
Hipertermia materna: La hipertermia materna ha sido ampliamente estudiada en el modelo animal, y se demostró sus efectos teratogénicos, que ocurren con cifras alrededor de los 38.9°C, ocasionando malformaciones del tubo neural, defectos oculares, paladar, hipoplasia maxilar, agenesia renal y en extremidades.9,12,13,14,20
En humanos los estudios epidemiológicos sugieren la asociación con defectos en el tubo neural y aborto espontáneo, incluso algunos estudios retrospectivos realizados en 1991 encontraron malformaciones cardiovasculares asociadas a fiebre materna.9,12,20,21
De acuerdo con esto, la fiebre es el síntoma más frecuente y orientador al diagnóstico de la nueva influenza H1N1. La fiebre materna parece ser el principal riesgo de teratogenicidad en el feto asociada al virus, aún más que por algún mecanismo del propio virus.20,22-24
La presencia de fiebre materna, ha mostrado ser un factor de riesgo para la aparición de convulsiones en el recién nacido, encefalopatía parálisis cerebral e incluso muerte en el neonato, por lo cual se recomienda el tratamiento eficaz y oportuno de la fiebre materna en la toda mujer embarazada. El acetaminofén es la primera elección.20,22-24
Otros estudios han asociado la presencia de influenza estacional con leucemia en la infancia, esquizofrenia y Parkinson; sin embargo no hay evidencia suficiente para sustentar tales hallazgos.25-28
¿ Manifestaciones clínicas
El CDC de Atlanta de los Estados Unidos de Norteamérica, reporta que en la mujer embarazada los signos y síntomas más comúnmente encontrados son; fiebre (97%), tos (94%), rinorrea (54%), cefalea (47%), disnea (41%), mialgias (35%), vómitos (18%), diarrea (12%) y conjuntivitis (9%). En algunos países se han definido criterios de gravedad en base a alteraciones hemodinámicas y ventilatorias; hipotensión arterial, taquipnea, cianosis, e hipoxemia, y ante la presencia de estas manifestaciones recomiendan la hospitalización de los pacientes.
La mayoría de los estudios coinciden en el periodo de incubación del virus nuevo de la influenza H1N1; el cual es de uno a cuatro días,29 y las manifestaciones clínicas son en general muy similares a las del virus de influenza estacional. Se ha encontrado de manera constante la presencia de fiebre y tos (Tabla 1).
¿ Diagnóstico
Se confirma el caso sospechoso ante la presencia del virus nuevo tipo A H1N1 mediante reacción en cadena de polimerasa (PCR), prueba con especificidad de 99% y con resultado en 24 a 48 horas. Cultivo del virus nuevo es el estándar de oro, requiere de tres a 10 días para tener el resultado.
También se utilizan pruebas de inmunofluorescencia directa para determinación de antígenos, con resultados en seis a ocho horas y ofrecen una sensibilidad de 70% a 95% y una especificidad mayor de 90%, lo que las hace más recomendables que las pruebas rápidas o inmunoenzimáticas, en estas últimas el resultado se obtiene entre 15 a 30 minutos, con sensibilidad de 59% a 93% y especificidad de 76% a 100%.30-33
¿ Directrices para el tratamiento
Actualmente sólo se recomiendan dos antivirales para el tratamiento y prevención del virus nuevo de influenza A H1N1, los cuales son inhibidores de la neuraminidasa (Tabla 2).34
Oseltamivir se hidroliza en el hígado a su metabolito activo; oseltamivir carboxilato, con vida media de seis a 12 horas. Biodisponibilidad 2%.
Zanamivir inhalado, biodisponibilidad de 10% a 20%. Sin embargo, al no pasar por plasma su excreción es 90% sin cambios a través de la orina, con vida media de 2.5 a cinco horas, debido a su excreción sin cambios y su baja disponibilidad en sangre, se cree que puede ser la mejor opción y que los efectos teratogénicos serían bajos. Sin embargo, dada la escaza información hasta el momento no es posible sustentar la seguridad de ninguno de los dos antivirales e incluso hasta la fecha la FDA las cataloga como medicamentos clase C, lo cual significa que no se han realizado estudios clínicos para tal evaluación, por lo cual la única evidencia sobre seguridad proviene de estudios de laboratorio o modelo animal.
La OMS y la CDC recomiendan actualmente, que en el caso de la mujer embarazada y con infección por el virus nuevo de influenza H1N1, se utilice el oseltamivir o zanamivir.19,35-38
En nuestro país se considera como droga de elección el oseltamivir con dosis de 75 mg cada 12 horas durante cinco días, pero siempre y cuando se confirme caso H1N1 y se esté dentro de las 48 horas del inicio de los síntomas.
Para la embarazada con infección por el virus nuevo de influenza A H1N1 existe poca información con el uso de antivirales, pero actualmente se recomienda el oseltamivir en casos confirmados, aun cuando hayan pasado más de 48 horas de haber iniciado con sintomatología, independientemente de la etapa de gestación. Las complicaciones respiratorias durante el embarazo debido a influenza pueden ser más graves en el último trimestre. En el primer trimestre de la gestación se recomienda el uso de zanamivir a dosis de dos inhalaciones cada 12 horas durante cinco días, y está contraindicado en pacientes con historia de asma, y se debe disminuir la dosis a 5 mg en las mujeres con insuficiencia renal.
No debemos de perder de vista los efectos colaterales o indeseables de los antivirales, existe la información al respecto, se mencionan efectos de tipo neuropsiquiátrico.
Lactancia materna: Se recomienda continuar con la lactancia materna39 por el efecto protector humoral y celular conferido por la leche humana. Debido a que los dos antivirales se excretan en cantidades mínimas de su metabolito activo de 38.2 ng/ml durante un tratamiento de 75 mg por cinco días. El oseltamivir se excreta en a razón de 0.012 mg/kg, la dosis pediátrica es de 2 mg a 4 mg/kg/día. El zanamivir se reporta en concentraciones de 0.075 mg/día, lo cual es también mucho menor que la dosis pediátrica recomendada de 10 mg/día.
Quimioprofilaxis: En el caso de pacientes embarazadas que tuvieron contacto con un caso confirmado está recomendada la profilaxis con oseltamivir a la dosis de 75 mg día por 10 días o con zanamivir 5 mg cada 12 horas durante cinco días.
El CDC considera al zanamivir como el antiviral de elección para quimioprofilaxis debido a la baja biodisponibilidad; sin embargo, es muy importante señalar que las recomendaciones aún pueden modificarse en tanto se disponga de mayor evidencia.
No se dispone de datos científicos hasta el momento de un potencial riesgo teratogénico por el uso de los antivirales durante la gestación.19,35-38
¿ Manejo en el recién nacido
Con los estudios que existen hasta el momento, se recomienda el tratamiento con oseltamivir 12 mg cada 12 horas por cinco días. Aunque existen cuatro casos publicados de H1N1 en el recién nacido, y se ha demostrado su paso trans-placentario, no hay suficiente evidencia sobre la adquisición in útero, ya que no se ha comprobado como en el caso de influenza aviar H5N1 el hallazgo de la secuencia genómica en células citotrofoblásticas de la placenta, así como en el pulmón células mononucleares circulantes o macrófagos del feto. Sin embargo, hay que considerar esta etiología dentro de las neumonías congénitas en todo recién nacido cuya madre presente un cuadro clínico compatible con influenza para iniciar el tratamiento antiviral en forma precoz.10,19,35-37
¿ Vacuna trivalente en la mujer embarazada
La aplicación de la vacuna trivalente durante el embarazo si ha demostrado disminuir las complicaciones a nivel respiratorio, ya que se ha encontrado reduce el número de ingresos a la unidad de cuidados intensivos de adultos, por lo cual su administración en centros de primer nivel de atención, es una medida útil y ampliamente recomendable como pilar en la prevención de esta enfermedad en la mujer embarazada, pues se han demostrado títulos protectores de anticuerpos IgG contra Influenza A (H1N1 y H3N2), en los recién nacidos desde el momento del parto hasta por lo menos las 20 semanas de edad posnatal.9,40,41
Correspondencia: Dr. Luis Paulino Islas Domínguez.
Dr. Balmis N° 148
Colonia Doctores, Delegación Cuauhtémoc. C. P. 06726.
Teléfono: 2789 2000, ext. 1489.
Correo electrónico: lu-islas@hotmail.com.