¿ Tejido adiposo (funciones y estructura)
El tejido adiposo es un órgano endocrino con múltiples funciones, las cuales ejerce a través de una gran variedad de hormonas y citocinas denominadas adipocinas que sirven de mediadores entre el tejido adiposo y los órganos adyacentes y a distancia como el endotelio, hígado, músculo, páncreas, glándulas suprarrenales y sistema nervioso. Dentro de sus funciones mantiene el balance energético a largo plazo, participa en la termorregulación, en el metabolismo de los lípidos y de la glucosa, además de modular la función hormonal y la reproducción. También participa en la regulación de la presión arterial, en la coagulación sanguínea y en condiciones de alteración funcional contribuye a la inflamación sub-clínica crónica y al estrés oxidativo crónico asociados a la obesidad.1,2
En los mamíferos, el tejido adiposo de acuerdo al aspecto y características de las células grasas que lo forman se ha divido en blanco y pardo.3
El tejido pardo con un alto contenido de mitocondrias tiene como principal función la termorregulación, en cambio el tejido blanco sirve como reservorio energético y es utilizado en situaciones de desbalance energético. Esta última función del tejido adiposo era la única reconocida hasta el descubrimiento de las adipocinas y la clasificación del tejido adiposo como órgano endócrino.3
El tejido adiposo está compuesto por: adipocitos (50%), pre-adipocitos, células del sistema inmune, del sistema nervioso, matriz extracelular y vasos sanguíneos (en conjunto el restante 50%),4,5 es esencial para la vida y en extremos de abundancia (obesidad) o falta del mismo (lipodistrofia) se provocan alteraciones metabólicas significativas (resistencia a la insulina, diabetes y dislipidemia) y se incrementa el riesgo de mortalidad;5 de esta manera se vuelve relevante el estudio de sus funciones y de la alteración de las mismas como posible mecanismo responsable de las complicaciones cardiovasculares asociadas a la obesidad.
¿ Obesidad y alteración funcional del tejido adiposo
La obesidad se caracteriza por el exceso de tejido adiposo corporal, tiene una alta prevalencia mundial y nacional (aproximadamente 500 millones de personas con obesidad en el mundo y sobre 30% de la población adulta mexicana). Esta condición incrementa el riesgo de mortalidad por enfermedad cardiovascular, genera pérdida en la calidad y expectativa de vida en quien la padece y elevados gastos en salud pública. Además, el riesgo de presentar hipertensión arterial, diabetes mellitus tipo 2 (DM2), algunos tipos de cáncer, apnea del sueño, dislipidemias, osteoartritis, eventos vasculares cerebrales, colelitiasis, entre otras enfermedades, está elevado en individuos con obesidad comparados con sujetos con índice de masa corporal (IMC) normal.6-9
A pesar del aumento en la prevalencia de la obesidad y sus repercusiones, no se conocen con precisión los mecanismos moleculares mediante los cuales la obesidad desencadena el daño cardiovascular en los individuos que la padecen. Sin embargo, el papel de los adipocitos es primordial en este fenómeno.5,9 Las funciones del tejido adiposo se modifican a medida que los adipocitos aumentan de tamaño en relación directa con el grado de obesidad. En sujetos con peso normal, los adipocitos pequeños participan en la homeostasis metabólica principalmente en el balance energético, en el metabolismo de los lípidos, en la termorregulación y en la función hormonal. Sin embargo, en la obesidad cuando el tejido adiposo se hipertrofia y predomina su acúmulo central o visceral en el organismo, esta hipertrofia está asociada a dislipidemia, resistencia a la insulina, hipertensión arterial, aterogénesis y síndrome metabólico, condicionando un incremento en la morbi-mortalidad de los individuos obesos con dichas características.9-13
La alteración funcional de los adipocitos representa un factor crítico en los individuos con exceso de tejido adiposo para la aparición de las comorbilidades de la obesidad antes mencionadas.5,9,14 Los mecanismos fisiopatológicos necesarios para que se presente dicha alteración son complejos e interactúan tanto factores genéticos como ambientales. Sin embargo, tres eventos comunes son relevantes: 1. ¿Cómo se almacena el tejido adiposo? (hipertrofia vs. hiperplasia), 2. ¿Dónde se almacena el tejido adiposo? (subcutáneo vs. visceral) y 3. La comunicación de los adipocitos con diversos órganos a distancia.5
El aumento del tejido adiposo per se no es suficiente para alterar la función metabólica del individuo; es necesario que éste se deposite visceralmente y que su incremento se lleve a cabo principalmente por hipertrofia. De manera que la distribución del tejido adiposo (subcutáneo vs. visceral) y la forma de incrementar dichos depósitos (hipertrofia vs. hiperplasia) son más importantes que la cantidad total de grasa que tenga un individuo para determinar su riesgo cardiovascular.9,5,11,12
1. ¿Cómo se almacena el tejido adiposo (hipertrofia vs. hiperplasia)?
En periodos de sobre alimentación el adipocito del humano adulto puede presentar la capacidad tanto de aumentar el tamaño de las células adiposas existentes (hipertrofia), como la de generar nuevos adipocitos maduros a partir de pre-adipocitos (hiperplasia), con el fin de almacenar el exceso de energía en forma de triglicéridos. Este último proceso, denominado adipogénesis, consta de dos etapas: I. Proliferación: que consiste en la creación de nuevos adipocitos a partir de pre-adipocitos y II. Diferenciación: que consiste en la madurez de los nuevos adipocitos, los cuales presentan la capacidad de secretar adipocinas y la capacidad de lipogénesis.5 Inicialmente existe una hipertrofia del adipocito para almacenar el exceso de energía, esto sirve de estímulo para iniciar la adipogénesis y la hiperplasia para mantener la función normal del tejido adiposo. El aumento en el número de nuevos adipocitos funcionales pequeños (hiperplasia), incrementa la capacidad del tejido adiposo para almacenar el excedente energético y mantener un estado metabólico estable.5 Sin embargo, si el depósito energético se genera mediante la hipertrofia de los adipocitos existentes, el crecimiento excesivo del tejido adiposo, aunado al balance energético positivo permanente, trae como consecuencia una sobrecarga metabólica de los mecanismos intracelulares (oxidación de sustratos energéticos y síntesis de proteínas) y extracelulares del adipocito (expansión de matriz extracelular y angiogénesis), volviéndolos incapaces de cumplir con las demandas metabólicas, lo que provoca alteraciones funciones tales como:5,9,14
1. Deficiencias en la producción energética y en la síntesis de proteínas, induciendo la activación de una respuesta inflamatoria intracelular, mediante vías de señalización como el factor nuclear NFkB y la sobreproducción de especies reactivas por activación de enzimas como la NADPH oxidasa, causando un estado de estrés oxidativo e inflamación.5,9,14
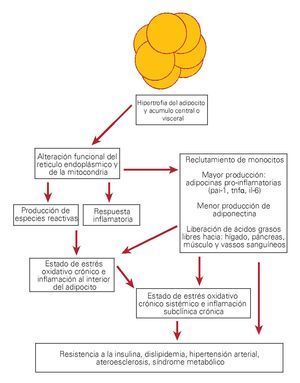
2. Pérdida en la regulación de la síntesis de adipocinas, incrementando las citocinas proinflamatorias tales como: factor de necrosis tumoral alfa (TNFα), interleucina 6 (IL-6), el inhibidor del activador del plasminógeno 1 (PAI-1), la proteína quimioatrayente de monocitos 1 (MCP-1); además disminución de adiponectina (adipocina anti-inflamatoria y anti-aterogénica) y reclutamiento de células inflamatorias al interior del tejido adiposo, lo que incrementa la secreción de citocinas proinflamatorias y la generación de especies reactivas.9,13,14 Estos eventos contribuyen al estado de estrés oxidativo e inflamación subclínica crónica que está presente en el paciente con obesidad (Figura 1).
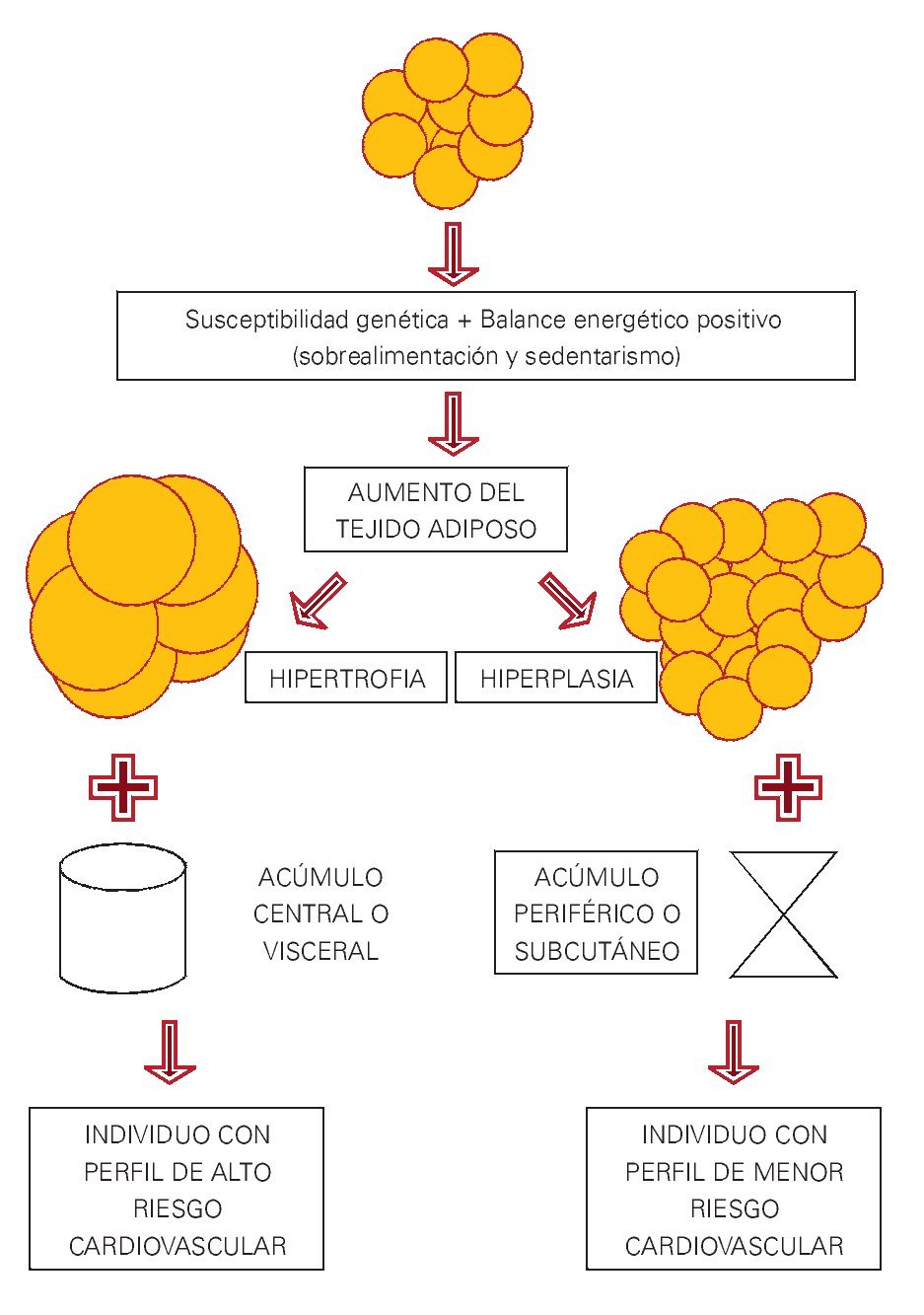
¿ Figura 1. Esquema general de las consecuencias de la forma y el sitio de almacén del incremento del tejido adiposo.
Cualquier fenómeno que afecte la proliferación o diferenciación e impida la hiperplasia, genera hipertrofia como mecanismo de almacén del exceso de energía. Un ejemplo es el efecto de los glucocorticoides que estimulan la diferenciación de los adipocitos existentes en especial del tejido adiposo visceral y disminuyen la proliferación del tejido adiposo subcutáneo, estos cambios están asociados con hipertrofia y disfunción de los adipocitos, hipertensión, dislipidemia y DM2, encontrados comúnmente en la hipercortisolemia.5 También la hipertrofia de los adipocitos está asociada a la DM2, a la resistencia muscular a la insulina, al aumento de los factores inflamatorios en sangre y disminución de factores anti-inflamatorios, además los pacientes con DM2 tienen adipocitos de mayor tamaño comparados con sujetos con igual índice de masa corporal, pero sin diabetes.5,9,14-17
2. ¿Dónde se almacena la grasa? (subcutánea vs. visceral)
La distribución del tejido adiposo es un factor reconocido de incremento en el riesgo cardiovascular. Individuos con distribución central o visceral de la obesidad presentan mayor riesgo de mortalidad general, mayor riesgo de padecer enfermedad arterial coronaria, DM2, hipertensión y dislipidemia comparados con aquellos con distribución periférica o subcutánea de la obesidad. En pacientes con cantidades similares de tejido adiposo corporal total (medidas mediante el índice de masa corporal o porcentaje de grasa), la diferencia en las alteraciones metabólicas la establece la cantidad de tejido adiposo visceral de cada individuo (a mayor cantidad de grasa visceral, mayor alteración metabólica).13,18-20 Aún en sujetos con índice de masa corporal dentro de rangos saludables, el poseer una circunferencia de cintura mayor de 88 cm en mujeres o 102 cm en hombres, representa un riesgo mayor de mortalidad comparados con individuos con IMC normal y circunferencia de cintura normal.21
También se han encontrado en pacientes con diabetes una menor cantidad de adipocitos subcutáneos comparados con sujetos con similar IMC pero sin diabetes.20 Estos datos resaltan la importancia del sitio de distribución y la alteración funcional del tejido adiposo en el incremento el riesgo cardiovascular asociado a la obesidad (Figura 2).
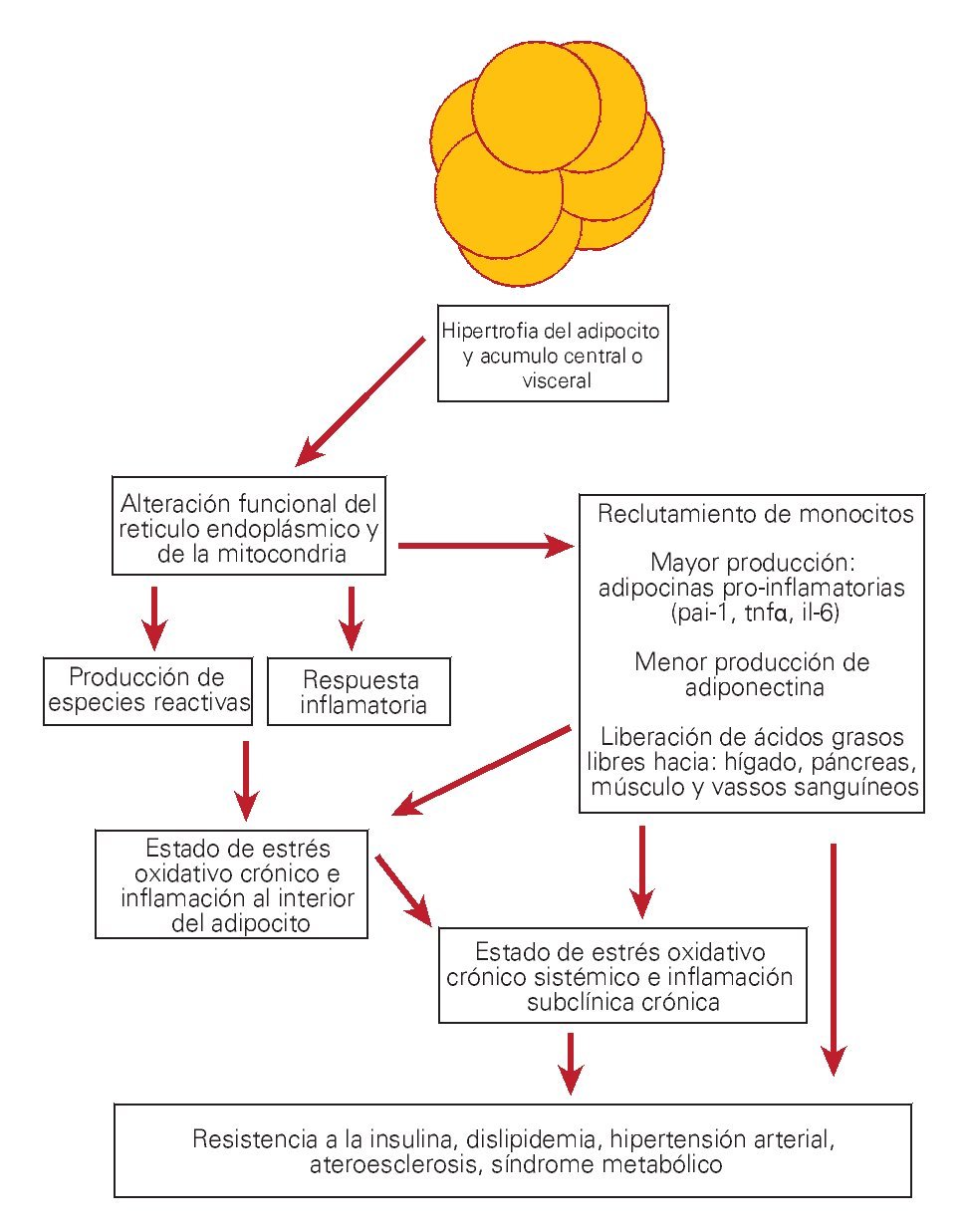
¿ Figura 2. Esquema de la alteración funcional del adipocito hipertrófico.
Las diferencias en la función y actividad metabólica de ambos sitios de depósito de tejido adiposo explican parte del incremento del riesgo cardiovascular antes mencionado. El tejido adiposo subcutáneo es un sitio de depósito fisiológico para el excedente energético en ambientes de balance positivo de energía. Al compararlo con el tejido adiposo visceral el tejido adiposo subcutáneo, presenta mayor capacidad para absorber ácidos grasos libres y triglicéridos, es más sensible a la insulina y contiene adipocitos con mayor capacidad de diferenciación. Algunos autores consideran que el incremento patológico del tejido adiposo visceral funciona como un sitio ectópico de almacén de grasa corporal, tal como sucede con el músculo y el hígado, agregándolo al fenómeno de lipotoxicidad. Además, existe evidencia de que los depósitos de grasa visceral aumenten a consecuencia de rebasar el umbral de almacenamiento de energía del tejido adiposo subcutáneo.9,5,13
En el tejido adiposo visceral existe mayor actividad lipolítica, mayor producción y expresión genética de interleucina 6 (IL-6), angiotensinógeno, TNF-a, adiponectina y factor quimiotáctico de monocitos, así como mayor número de receptores a glucocorticoides y andrógenos, mayor acceso a la circulación portal, además de menor capacidad de almacén de ácidos grasos libres postprandiales, menor capacidad de diferenciación de pre-adipocitos con células con mayor predisposición a hipertrofia y menor producción de leptina. Por lo tanto, el tejido adiposo visceral contiene adipocitos con menor sensibilidad a la insulina, con mayor liberación de ácidos grasos a la circulación, mayor producción de citocinas pro-inflamatorias y radicales libres los cuales pasan directamente hacia el hígado con las consecuencias metabólicas que de ahí se derivan.2,5,9-11,13
Los factores de riesgo cardiovascular asociados al acúmulo de grasa visceral son: hiperinsulinemia y resistencia a la insulina, microalbuminuria, ateroesclerosis prematura, partículas de LDL con mayor susceptibilidad a oxidación, disminución y alteración funcional de las partículas de HDL, aumento en la concentración de triglicéridos, de fibrinógeno, de la producción del inhibidor del activador del plasminógeno, de la proteína C reactiva, de TNFα, IL-6, de la viscosidad sanguínea e hipertrofia ventricular cardiaca5,10-12,22,23 Lo anterior contribuye a la aparición del síndrome metabólico con un estado proinflamatorio, pro-aterogénico y pro-trombótico a consecuencia del incremento del tejido adiposo visceral y remarca la importancia de la obesidad central o visceral como eje del síndrome metabólico.
3. Comunicación del tejido adiposo con otros órganos a distancia
Un tercer evento de importancia mediante la cual el tejido adiposo con alteraciones funcionales (especialmente el visceral) genera finalmente el daño cardiovascular asociado se debe a tres vías de comunicación con órganos adyacentes y a distancia:5,9,12
1. Liberación de ácidos grasos libres y adipocinas hacia el hígado y otros órganos con la consecuente hiperglucemia, dislipidemia y resistencia a la insulina.
2. La producción de adipocinas y el estado de estrés oxidativo crónico e inflamación subclínica crónica.
3. Acumulación ectópica de lípidos en diversos órganos (lipotoxicidad) con la consecuente disfunción orgánica, entrando en juego la susceptibilidad genética de dichos órganos (tejido adiposo adyacente, sistema nervioso, hígado, músculo, páncreas, corazón y vasos sanguíneos).
El acúmulo excesivo de grasa corporal, principalmente en la región abdominal, se ha asociado con un estado de estrés oxidativo (sobreproducción de especies reactivas y disminución de las defensas antioxidantes) e inflamación subclínica crónica. En general a mayor nivel de índice de masa corporal (IMC) y circunferencia de cintura (CC) mayor es el nivel de marcadores inflamatorios y de estrés oxidativo tanto en hombres como en mujeres.24-26
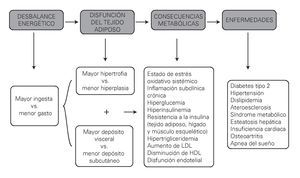
La combinación de estos tres fenómenos (acúmulo visceral, hipertrofia y comunicación del tejido adiposo con otros órganos) conlleva a las múltiples comorbilidades de la obesidad abdominal (Figura 3).
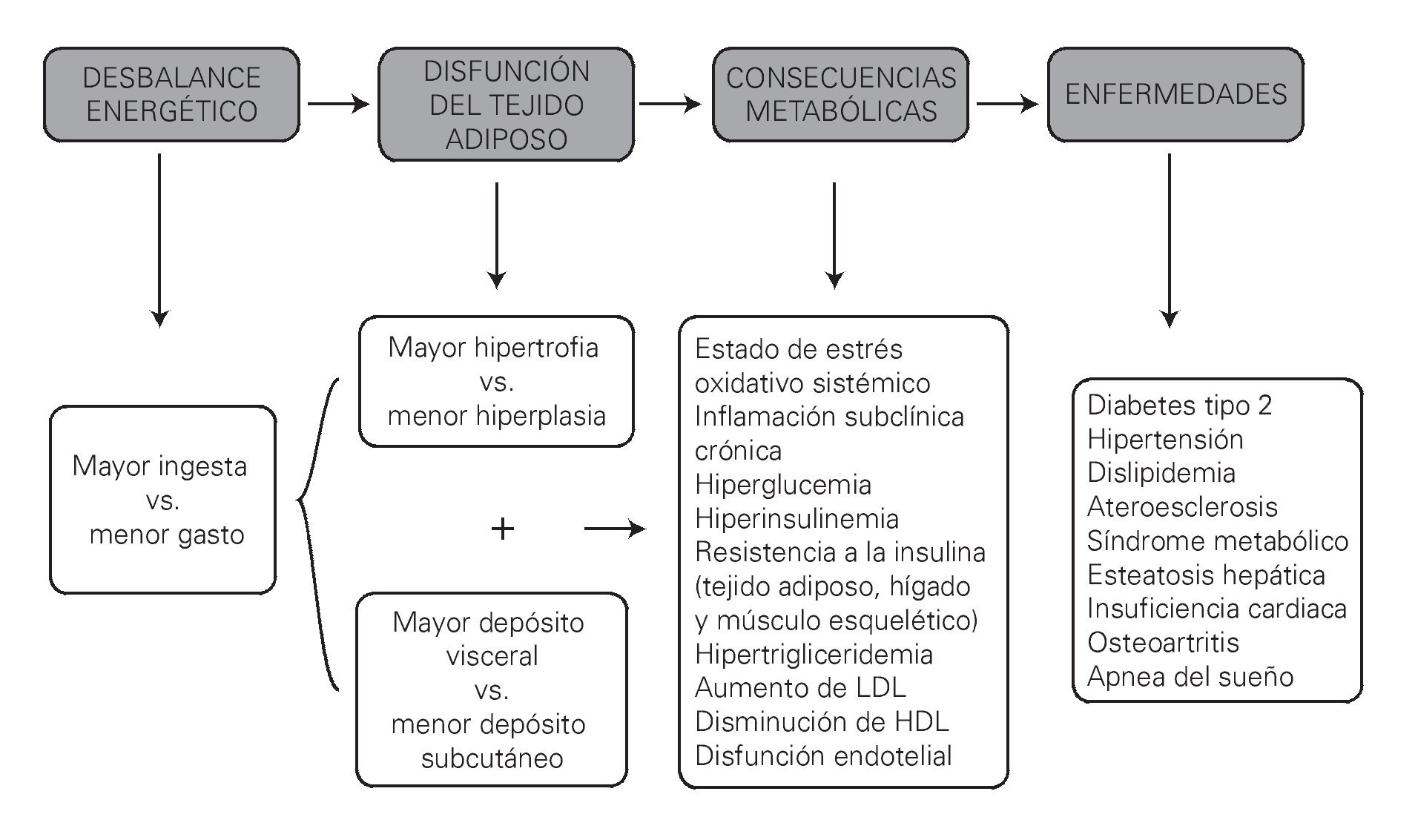
¿ Figura 3. Mecanismos de disfunción del tejido adiposo y su repercusión metabólica (3° cuadro gris; las consecuencias metabólicas).
Resistencia a la insulina y diabetes mellitus tipo 2: La activación de factores nucleares que desencadenan inflamación, la producción excesiva de radicales libres, la falla en la capacidad de oxidación mitocondrial y de la producción de ATP, así como el daño al retículo endoplásmico intracelular en el adipocito, hígado, músculo y páncreas, provocado tanto por los niveles circulantes plasmáticos de ácidos grasos como por las citocinas derivadas del tejido adiposo y el acúmulo ectópico de lípidos en dichos órganos, condicionan alteraciones en la señalización de la insulina y la consecuente resistencia a su acción.27,28
Debido al incremento en la producción de glucosa por el hígado, el páncreas inicialmente se estimula ante la hiperglucemia para secretar mayores cantidades de insulina (generando hiperinsulinemia); sin embargo, a largo plazo (en individuos susceptibles) este estado de estrés oxidativo crónico e inflamación provoca deficiencia en la producción de insulina en las células pancreáticas con apoptosis de las mismas condicionando la aparición de DM2.27,28 Las sustancias derivadas del adipocito que han sido asociadas a la resistencia a la insulina y a la diabetes son: TNF-α, PAI-1, Proteína de unión del retinol 4 (RBP-4), adiponectina, resistina, ácidos grasos libres, IL-6, el número de macrófagos dentro del tejido adiposo y los niveles de cortisol.27
La obesidad está claramente asociada a la DM2, hasta 90% de los pacientes con este padecimiento presentan al menos sobrepeso. Al comparar individuos con obesidad con aquellos con IMC normal el riesgo para presentar diabetes es 12.4 veces más alto en mujeres y 6.7 veces más alto en hombres. De igual forma la diabetes se asocia a una elevación de marcadores sanguíneos de estrés oxidativo e inflamación comparados con sujetos con IMC normal.29-31
Disfunción y daño del endotelio vascular: El riesgo de enfermedad arterial coronaria se eleva tres veces en mujeres con obesidad comparadas con mujeres que presentan un IMC normal.30 La obesidad se acompaña de disminución en la capacidad de vasodilatación, ateroesclerosis, alteraciones en la coagulación sanguínea e hipertensión arterial. Los posibles mecanismos son: sobreproducción de factores inflamatorios y disminución de adiponectina (anti-inflamatorio), disminución en la biodisponibilidad de óxido nítrico y producción de peroxinitritos y la consiguiente reducción en la respuesta de vasodilatación del músculo liso vascular, oxidación de LDL, estimulación la síntesis y depósito de colágeno, engrosamiento de la pared vascular, vasoconstricción y estado protrombótico.32-35
Las partículas pequeñas y densas de LDL actúan como estímulo aterogénico al oxidarse, penetrar el endotelio vascular y provocar disminución en la producción del óxido nítrico, quimiotaxis de monocitos y su transformación macrófagos en el endotelio vascular, formación de células espumosas, incremento de la respuesta inflamatoria y de la producción de especies reactivas, proliferación de células musculares lisas y agregación plaquetaria en el endotelio. Todos estos fenómenos participan en el proceso de aterogénesis.29,34 Aunado a esto la acción de la insulina (en estados de hiperinsulinemia) puede funcionar como factor de crecimiento tisular, pro-trombótico y proaterogénico al activar vías de señalización intracelular que participan en la respuesta vascular, migración de monocitos, macrófagos y células musculares lisas, producción de endotelina-1 e inhibidor del activador del plasminógeno 1.36
Hipertensión arterial: La participación del tejido adiposo se da a distintos niveles, secreta angiotiensinógeno e incrementa la función del sistema renina angiotensina aldosterona (con aumento del volumen plasmático e incremento de la resistencias vasculares), el estado de estrés oxidativo y la inflamación subclínica crónica provocan disminución de la biodisponibilidad de óxido nítrico e incremento de los peroxinitritos y la consiguiente vasoconstricción periférica, además de la activación del sistema nervioso simpático. La IL-6 y moléculas de adhesión celular se han asociado a los niveles de presión arterial sistólica y diastólica. Comparados con sujetos con IMC normal los individuos con obesidad presentan niveles mayores de renina, de angiotensinógeno, de enzima convertidora de angiotensina, de aldosterona, mayor actividad del sistema nervioso simpático y menores niveles de adiponectina, cuya concentración en sangre se asocia inversamente con la posibilidad de padecer hipertensión arterial. Otros factores de la obesidad asociados a la hipertensión arterial son: el aumento del gasto cardiaco, de la presión intratorácica, el daño renal (glomerulopatía), el aumento en los ácidos grasos libres circulantes los cuales están asociados a un incremento de actividad del sistema nervioso simpático, así como a la producción excesiva de especies reactivas que llevan a la disfunción endotelial.37-39
La hipertensión es seis veces más frecuente en individuos con obesidad comparados con individuos con IMC normal. Hasta 79% en hombres y 65% mujeres de la hipertensión arterial puede atribuirse a la obesidad. El riesgo de presentar hipertensión arterial se incrementa a medida que el IMC aumenta; de 15% para hombres con IMC ≤25 kg/m2 hasta 38% para individuos con IMC >30 kg/m2 y en mujeres el riesgo se incrementa de 15% para personas con IMC <25 hasta 42% para mujeres con un IMC >30. Por cada 10 kg de ganancia de peso la presión arterial sistólica aumenta 3 mmHg y la presión arterial diastólica 2.3 mmHg. Esto se traduce en un incremento en el riesgo de 12% para enfermedad arterial coronaria y de 24% para evento vascular cerebral.29,37 La apnea obstructiva del sueño (AOS) puede también asociarse a la hipertensión arterial (hasta 60% de los pacientes hipertensos padecen AOS), estos pacientes presentan incrementos en la actividad del sistema nervioso simpático, del sistema renina angiotensina aldosterona y disminución del control barorreceptor de la presión arterial.37-39
Dislipidemia: Las características de la dislipidemia asociada a la obesidad central son: hipertrigliceridemia, incremento en las lipoproteínas de baja densidad (LDL) y descenso de los niveles de lipoproteínas de alta densidad (HDL). A nivel hepático el estado de estrés oxidativo, la inflamación subclínica crónica y el flujo de ácidos grasos provenientes del tejido adiposo visceral produce incremento en la síntesis triglicéridos y de las lipoproteínas de muy baja densidad que lo transportan (VLDL). Existe además una disminución en la depuración de las VLDL y una alteración en la conformación de las lipoproteínas de alta densidad, con mayor susceptibilidad a su depuración por acción de la lipasa hepática (sobre-expresadas en estados resistencia a la insulina hepática) y el consiguiente descenso en niveles sanguíneo. Además las LDL son más densas, pequeñas y con mayor susceptibilidad de oxidarse.32,40,41
¿ Conclusiones
La complejidad de la función del tejido adiposo, de los mecanismos que controlan la adipogénesis en condiciones de sobrealimentación, la secreción de adipocinas, la interacción de las mismas con otros órganos, la participación de factores genéticos y ambientales que modifican la susceptibilidad del tejido adiposo y de diversos órganos para su alteración funcional, aún representan campos de intensa investigación para explicar la diversidad de patologías que pueden presentarse en individuos con obesidad. Desde individuos con IMC elevado sin aparente repercusión metabólica hasta individuos con IMC normal con trastornos severos del metabolismo, la disfunción del adipocito representa un fenómeno determinante, el predominio de la hipertrofia vs. la hiperplasia, el acúmulo primordial en la zona central del cuerpo (área visceral vs. subcutánea, tronco vs. extremidades inferiores), el flujo de ácidos grasos y adipocinas del tejido adiposo visceral al hígado y la acumulación ectópica de dichos ácidos grasos en diversos órganos (músculo, corazón, páncreas, vasos sanguíneos e hígado) y la consiguiente disfunción de dichos órganos, son fenómenos que interactúan y dan luz a la explicación de los distintos escenarios presentes en la obesidad y sus repercusiones como la resistencia a la insulina, la DM2, la disfunción endotelial y el síndrome metabólico.
A pesar de la importancia de todos estos descubrimientos en la fisiopatología de la enfermedad, aún queda largo camino por recorrer, sobre todo en términos de traducir dichos descubrimientos a la práctica clínica, en donde intervienen otros factores al menos de igual importancia como la adherencia al tratamiento, las barreras socioculturales, los aspectos psicológicos asociados a la obesidad y al cambio de estilo de vida necesario para combatir enfermedades crónico-degenerativas. La prevalencia de la obesidad y sus repercusiones siguen en aumento y los tratamientos no parecen ser efectivos a largo plazo. Sin embargo, los avances en la fisiología y fisiopatología del tejido adiposo abren nuevas expectativas en la comprensión del fenómeno de la obesidad y sus repercusiones sobre la salud, así como nuevas estrategias terapéuticas. Muchos de los efectos benéficos de la actividad física y de la alimentación balanceada en el tratamiento de la obesidad ahora se sabe se deben al contrarrestar algunas de las consecuencias de la alteración funcional del tejido adiposo, en particular a la inflamación subclínica crónica y el estado de estrés oxidativo, ya sea al disminuir la cantidad de tejido adiposo visceral y por lo tanto la secreción de dichas adipocinas, así como en mejorar los sistemas antioxidantes endógenos, incrementar la biodisponibilidad del oxido nítrico, mejorar el perfil de lípidos, incrementar la sensibilidad a la insulina, disminuir la producción de especies reactivas, etc. Los avances en la fisiopatología de la alteración funcional del tejido adiposo, pueden llevar a la comprensión y el diagnóstico temprano en fases preclínicas y de esta manera establecer tratamientos que eviten la evolución crónica hacia enfermedades antes mencionadas.
Correspondencia: José Rolando Flores Lázaro.
Universidad Nacional Autónoma de México.
Teléfono: 5622 0540.
Correo electrónico:rolomd2000@yahoo.com.mx