A estenose grave do terço proximal da artéria descendente anterior (ADA) é classificada como lesão de alto risco, visto que pode comprometer grande parte do miocárdio ventricular esquerdo. Os stents farmacológicos (SF) de segunda geração têm demonstrado maior eficácia e segurança quando comparados aos não farmacológicos ou aos de primeira geração. São escassos os relatos na literatura do emprego desses dispositivos para o tratamento de lesões isoladas do terço proximal da ADA.
MétodosEstudo observacional e prospectivo, que incluiu pacientes uniarteriais, portadores de lesão de novo no terço proximal da ADA, tratados eletivamente com SF de segunda geração. Avaliamos os desfechos clínicos hospitalares e tardios.
ResultadosForam incluídos 70 pacientes, sendo a maioria do sexo masculino (70%), com média de idades de 65,4 ± 11,2 anos e com alta prevalência de diabetes (37%). O quadro clínico mais frequente foi angina estável (57,1%) e metade das lesões era do tipo B2 ou C. Foram tratadas 70 lesões com 71 stents, com sucesso angiográfico de 100%. O desfecho primário composto por óbito cardíaco, infarto não fatal ou revascularização do vaso alvo no seguimento clínico de 2,5 anos ocorreu em 3% dos pacientes. A mortalidade cardíaca foi de 1,5%, e a revascularização da lesão alvo foi necessária em apenas 1,5% dos pacientes.
ConclusõesEm pacientes uniarteriais com lesões de novo da ADA proximal, o tratamento eletivo com SF de segunda geração parece ser uma opção segura, com baixas taxas de eventos cardíacos adversos ou necessidade de nova revascularização.
Severe stenosis of the proximal left anterior descending artery (LAD) is classified as a high‐risk lesion, as it may affect a large part of the left ventricular myocardium. Second‐generation drug‐eluting stents (DES) have been shown to be more effective and safer when compared to bare‐metal or first‐generation ones. There are few reports in the literature on the use of these devices for the treatment of isolated lesions in the proximal LAD.
MethodsObservational and prospective study, which included single‐vessel patients with de novo lesions in the proximal LAD, electively treated with second‐generation DES. In‐hospital and late clinical outcomes were evaluated.
ResultsSeventy patients were included, most of them males (70%), with a mean age of 65.4 ± 11.2 years and a high prevalence of diabetes (37%). The most common clinical presentation was stable angina (57.1%) and half of the lesions were type B2 or C. A total of 70 lesions were treated with 71 stents, with 100% angiographic success. The primary endpoint, consisting of cardiac death, nonfatal infarction, or target‐vessel revascularization during the 2.5‐year clinical follow‐up, occurred in 3% of the patients. Cardiac death was 1.5%, and target‐lesion revascularization was required in only 1.5% of the patients.
ConclusionsElective treatment with second‐generation DES seems to be a safe option in single‐vessel patients with de novo lesions in the proximal LAD, with low rates of adverse cardiac events or need for additional revascularization procedure.
A estenose significativa da porção proximal da artéria descendente anterior (ADA) é classificada como lesão de alto risco, visto que pode comprometer grande parte do miocárdio ventricular esquerdo, tendo um prognóstico habitualmente mais desfavorável do que qualquer outro território acometido pela doença arterial coronariana.1
A cirurgia de revascularização miocárdica (CRM) com utilização da artéria torácica interna esquerda para o tratamento de lesões proximais da ADA tem demonstrado excelentes resultados, com evolução clínica favorável e elevada taxa de permeabilidade a longo prazo.2–5 Uma potencial vantagem da CRM é a proteção de um amplo território arterial, comparado ao tratamento apenas focal obtido da intervenção coronária percutânea (ICP), com benefício nos casos de futura progressão da doença arterial coronariana.6
Metanálises de estudos randomizados e registros7,8 de pacientes portadores de lesões isoladas da ADA não relataram diferenças significativas na taxa de mortalidade, infarto agudo do miocárdio (IAM) ou acidente vascular encefálico entre o tratamento cirúrgico com a utilização da artéria torácica interna esquerda e a ICP. Entretanto, a recorrência de angina e a necessidade de uma nova revascularização foram, respectivamente, três e cinco vezes maiores com o tratamento percutâneo em um seguimento clínico de até 5 anos. É importante salientar que a maioria destes estudos utilizou stents não farmacológicos, sendo que está bem estabelecida a maior eficácia dos stents farmacológicos (SF) na redução da revascularização do vaso alvo (RVA).9
Os stents mais atuais, chamados de segunda geração, têm demonstrado maior eficácia e, principalmente, segurança no tratamento da doença arterial coronariana,10–13 sendo escassos os relatos na literatura do emprego destes dispositivos para o tratamento de lesões isoladas do terço proximal da ADA.
MétodosEstudo observacional e prospectivo, realizado no período de julho de 2007 a janeiro de 2015, no Complexo Hospitalar da Real e Benemérita Sociedade Portuguesa de Beneficência de São Paulo, em São Paulo (SP), utilizando o banco de dados do Registro SAFIRA (Seguranc¿A e eFIcácia dos stents farmacolo¿gicos em uma populac¿a¿o do mundo ReAl). Os pacientes foram incluídos após o esclarecimento, a leitura e a assinatura do Termo de Consentimento Livre e Esclarecido.
Foram selecionados pacientes uniarteriais portadores de lesão de novo no terço proximal da ADA, com indicação de revascularização percutânea eletiva, tratados com SF de segunda geração. Foram excluídos pacientes com síndrome coronária aguda com elevação do segmento ST, síndrome coronariana aguda sem elevação do segmento ST associada à angina refratária, instabilidade elétrica ou instabilidade hemodinâmica.14 Outros critérios incluíram CRM ou ICP prévia, contraindicação ao uso dos antiplaquetários ou dos anticoagulantes previstos pelo protocolo medicamentoso.
As ICP foram realizadas de acordo com as técnicas habituais e conforme orientações das diretrizes vigentes.14 A avaliação da lesão foi realizada por análise angiográfica quantitativa, após administração de nitrato intracoronário. As lesões foram classificadas de acordo com a definição do American College of Cardiology/American Heart Association (A, B1, B2 e C).15 Pré e pós‐dilatação foram utilizadas a critério do operador. Todos os pacientes receberam heparina não fracionada no início do procedimento (70 a 100 U/kg), sendo doses adicionais administradas, se necessário, para manter um tempo de coagulação ativado entre 250 e 350 segundos. Dupla terapia antiplaquetária foi utilizada em todos os pacientes, com a administração de ácido acetilsalicílico, 100 a 200mg ao dia, associado a um inibidor P2Y12 (clopidogrel, prasugrel ou ticagrelor). Após o procedimento, o ácido acetilsalicílico foi mantido indefinidamente na dose de 100mg por dia. O inibidor P2Y12 de escolha foi recomendado por um período mínimo de 1 ano.
Foi definida como desfecho primário a taxa de eventos cardíacos adversos maiores (ECAM), composta por óbito cardíaco, IAM não fatal e RVA guiada por isquemia no seguimento clínico. Todos os óbitos foram considerados cardíacos, a não ser que uma causa não cardíaca pudesse ser claramente estabelecida. IAM foi caracterizado como elevação do marcador sorológico da lesão miocárdica isoenzima MB da creatina quinase (CK‐MB) acima de três vezes o valor de referência, com ou sem alterações eletrocardiográficas.
Os desfechos secundários incluíram a taxa de sucesso angiográfico (definido por estenose residual < 20% com fluxo final Thrombolysis In Myocardial Infarction ‐ TIMI III, na ausência de trombos e dissecção) e taxa de sucesso clínico (definido por sucesso angiográfico associado à ausência de ECAM) na fase hospitalar. Outros desfechos secundários foram a trombose definitiva ou provável do stent, definida de acordo com a classificação da Academic Research Consortium;16 o sangramento maior, avaliado pelo critério TIMI (definido por sangramento intracraniano, evidência clínica de sangramento associado à queda ≥ 5g/dL ou sangramento fatal);17 a revascularização da lesão alvo e a mortalidade por todas as causas.
Os pacientes foram seguidos após a alta hospitalar por contato telefônico, por consulta médica ou por informações obtidas pelo médico assistente, sendo estas avaliações efetuadas com 1, 6 e 12 meses e, a partir deste momento, anualmente.
Análise estatísticaAs variáveis categóricas foram expressas em frequência absoluta e porcentuais, e as contínuas como média e desvio padrão. A curva de sobrevida livre de eventos foi estimada pelo método Kaplan‐Meier. A análise dos dados estatísticos foi realizada pelo programa STATA 14 (STATA Corp, College Station, EUA).
ResultadosForam incluídos 70 pacientes uniarteriais com lesão de novo no terço proximal da ADA submetidos à ICP eletiva com implante de SF de segunda geração no período de junho de 2009 a outubro de 2015.
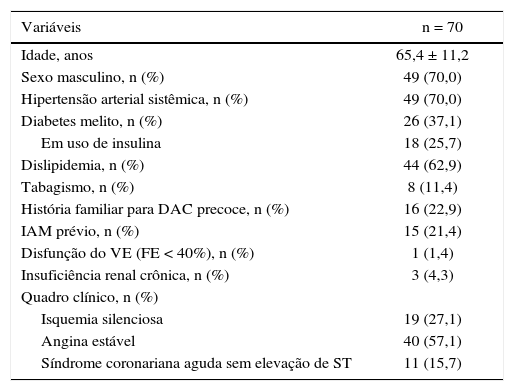
A maior parte dos pacientes era do sexo masculino (70%) e com média de idades de 65,4 ± 11,2 anos e mais de um terço (37,1%) era diabético (tabela 1). Uma minoria (1,4%) apresentava disfunção ventricular modera ou importante, e o quadro clínico de apresentação mais frequente foi angina estável (57,1%).
Características clínicas
| Variáveis | n = 70 |
|---|---|
| Idade, anos | 65,4 ± 11,2 |
| Sexo masculino, n (%) | 49 (70,0) |
| Hipertensão arterial sistêmica, n (%) | 49 (70,0) |
| Diabetes melito, n (%) | 26 (37,1) |
| Em uso de insulina | 18 (25,7) |
| Dislipidemia, n (%) | 44 (62,9) |
| Tabagismo, n (%) | 8 (11,4) |
| História familiar para DAC precoce, n (%) | 16 (22,9) |
| IAM prévio, n (%) | 15 (21,4) |
| Disfunção do VE (FE < 40%), n (%) | 1 (1,4) |
| Insuficiência renal crônica, n (%) | 3 (4,3) |
| Quadro clínico, n (%) | |
| Isquemia silenciosa | 19 (27,1) |
| Angina estável | 40 (57,1) |
| Síndrome coronariana aguda sem elevação de ST | 11 (15,7) |
DAC: doença arterial coronariana; IAM; infarto agudo do miocárdio; VE: ventrículo esquerdo; FE: fração de ejeção.
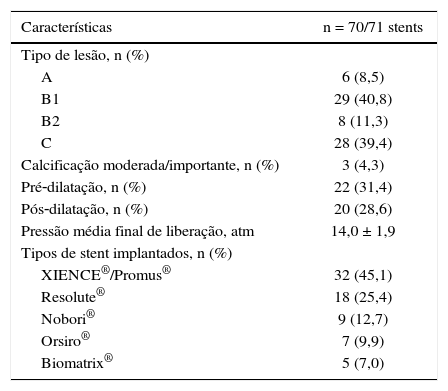
As lesões de maior complexidade tipo B2 e C estavam presentes em metade dos casos. A via de acesso mais utilizada foi a radial (74,3%), seguida da via femoral (24,3%), e stents com polímeros biocompatíveis foram utilizados em cerca de 20% dos casos (tabela 2).
Características angiográficas e do procedimento
| Características | n = 70/71 stents |
|---|---|
| Tipo de lesão, n (%) | |
| A | 6 (8,5) |
| B1 | 29 (40,8) |
| B2 | 8 (11,3) |
| C | 28 (39,4) |
| Calcificação moderada/importante, n (%) | 3 (4,3) |
| Pré‐dilatação, n (%) | 22 (31,4) |
| Pós‐dilatação, n (%) | 20 (28,6) |
| Pressão média final de liberação, atm | 14,0 ± 1,9 |
| Tipos de stent implantados, n (%) | |
| XIENCE®/Promus® | 32 (45,1) |
| Resolute® | 18 (25,4) |
| Nobori® | 9 (12,7) |
| Orsiro® | 7 (9,9) |
| Biomatrix® | 5 (7,0) |
Os sucessos angiográfico e clínico do procedimento foram de 100 e 95,7%, respectivamente. O desfecho combinado de óbito, IAM não fatal e revascularização de urgência ocorreu em três pacientes (4,3%), todos às custas de IAM sem supradesnivelamento de ST periprocedimento. Não ocorreu óbito ou necessidade de revascularização de urgência durante a internação hospitalar. Não houve caso de sangramento maior.
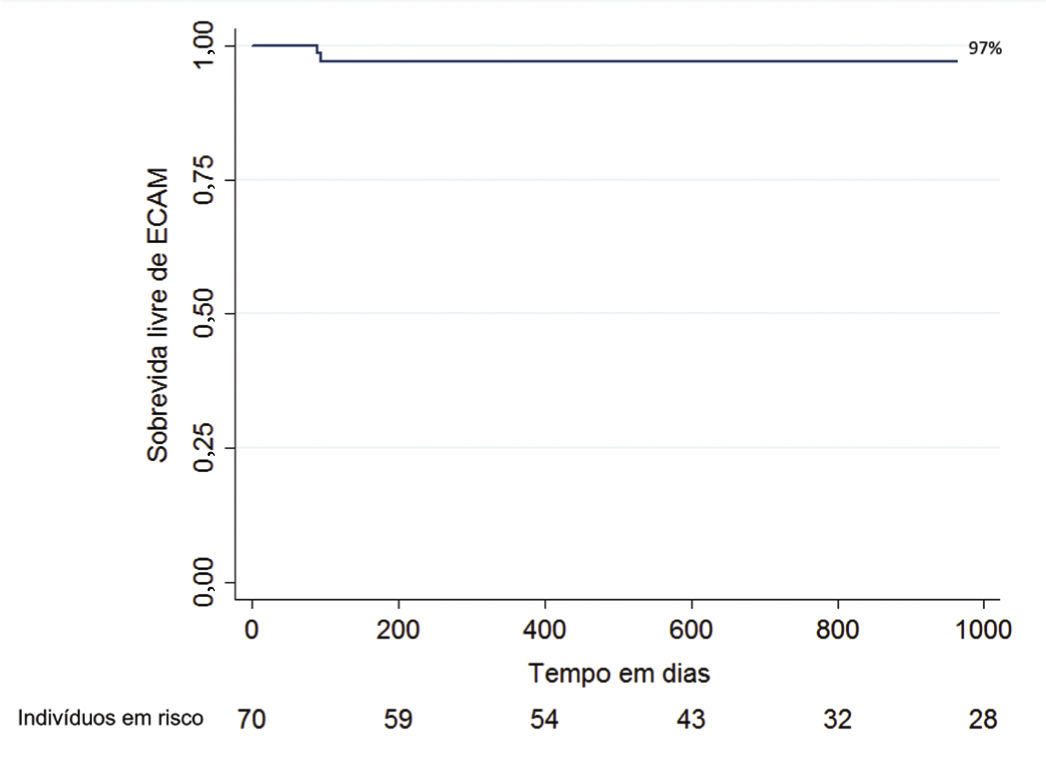
O seguimento clínico foi realizado em 68 pacientes (97,1%) durante um período médio de 2,5 ± 1,8 anos. O desfecho primário combinado de óbito cardíaco, IAM não fatal ou RVA guiada por isquemia no seguimento clínico incidiu em dois pacientes (3,0%). Ocorreram dois óbitos, sendo um de origem não cardíaca (choque séptico), e outro no pós‐operatório imediato de cirurgia para troca valvar aórtica. Não ocorreu IAM não fatal no seguimento, e a necessidade de revascularização da lesão alvo foi necessária em apenas um paciente (1,5%). Não ocorreram casos de trombose do stent definitiva ou provável. A probabilidade livre de ECAM de acordo com a curva de Kaplan‐Meier foi de 97% (fig. 1).
DiscussãoNo presente estudo, pacientes estáveis, portadores de lesão isolada, proximal, de novo da ADA submetidos à ICP com SF de segunda geração tiveram baixa taxa de ECAM (3,0%), mortalidade cardíaca (1,5%) e RVA (1,5%) em um seguimento clínico de 2,5 anos.
O uso dos SF reduziu substancialmente a necessidade de revascularização repetida, comparado aos stents convencionais. No entanto, à medida que os dados de seguimento clínico tornaram‐se disponíveis, surgiu a preocupação em relação à segurança destes dispositivos, devido a um aumento da incidência de trombose muito tardia.18
Os SF de segunda geração foram projetados para superar as questões de segurança a longo prazo, empregando novos revestimentos com polímeros mais biocompatíveis, drogas antiproliferativas menos tóxicas e hastes metálicas ultrafinas. Comparado aos SF de primeira geração, esta tecnologia proporcionou redução significativa na taxa de revascularização repetida,19,20 além de melhor segurança, com diminuição das taxas de trombose de stent, IAM e mortalidade.21–23
Um dos primeiros trabalhos que comparou o tratamento cirúrgico ao tratamento percutâneo para lesões proximais da ADA em pacientes estáveis foi o estudo MASS (The Medicine, Angioplasty or Surgery Study),24 no qual foi reportada taxa similar de morte e IAM da angioplastia com o balão comparada ao tratamento cirúrgico. Houve, porém, maior necessidade de nova revascularização e angina no grupo angioplastia em um seguimento clínico de até 5 anos.
Duas metanálises compararam o tratamento percutâneo com stents ao tratamento cirúrgico, com uso da artéria torácica interna esquerda, em pacientes com lesão proximal da ADA. Em ambas, não houve diferença em mortalidade, IAM ou AVC em um seguimento de até 5 anos. Porém, ocorreu um aumento significativo da taxa de nova revascularização no grupo ICP. Vale ressaltar que a maioria dos estudos utilizou stents não farmacológicos e apenas um estudo incluído utilizou SF de primeira geração.7,8
Alguns registros e estudos randomizados compararam a CRM com ICP utilizando SF de primeira geração para tratamento de lesões da porção proximal da ADA. Assim como com os stents não farmacológicos, não houve diferença entre os grupos na incidência de ECAM, porém ainda houve maior necessidade de nova revascularização no grupo SF.25,26 Até onde sabemos, não há nenhum estudo comparando CRM vs. ICP utilizando apenas stents farmacológicos de segunda geração neste grupo de pacientes.
Nosso estudo mostrou um ótimo resultado a curto e médio prazos com baixas taxas de RVA (1,5%) e mortalidade cardíaca (1,5%). Estes resultados são comparáveis aos dados previamente publicados sobre a revascularização cirúrgica utilizando a artéria torácica interna esquerda, com taxas relatadas de mortalidade entre zero e 5,4%, e necessidade de nova revascularização em até 3 anos de zero a 4,0%.7,8,24
Atualmente, a indicação da ICP para o tratamento das lesões proximais da ADA chega a ser até sete vezes mais frequente do que a indicação da CRM.26 Este dado possivelmente justifica o desinteresse em realizar novos estudos randomizados nesta população.
O presente estudo utilizou os stents mais modernos, incluindo stents com polímeros biocompatíveis, e avaliou uma população de mundo real, demonstrando a eficácia e a segurança destes dispositivos para o tratamento de lesões complexas em pacientes com indicação eletiva de revascularização. Nossos resultados estão de acordo com as recomendações da diretriz europeia de revascularização miocárdica,14 que classifica como classe IA (tratamento é útil e eficaz com evidência suficiente provinda de múltiplos estudos randomizados ou metanálises) tanto a CRM quanto a ICP para o tratamento de lesões da ADA proximal com anatomia favorável.
Vale ressaltar a baixa prevalência de disfunção ventricular esquerda na população do estudo e a não inclusão de pacientes com indicação de estratificação invasiva de urgência, sendo, portanto, nossos dados não aplicáveis para estes grupos de pacientes.
Limitações do estudoForam limitações da presente análise sua natureza observacional, unicêntrica, o tamanho limitado da amostra e a ausência de grupo cirúrgico para comparação. Outra possível limitação foi a ausência de seguimento clínico mais prolongado, apesar de estudos randomizados prévios com stents não farmacológicos não terem encontrado diferenças relevantes a longo prazo nos desfechos duros.27
ConclusõesEm pacientes uniarteriais com indicação eletiva de revascularização de lesões de novo da artéria descendente anterior proximal, o tratamento com stents farmacológicos de segunda geração parece ser uma opção segura, com baixas taxas de eventos cardíacos adversos e necessidade de nova revascularização. Nossos achados são similares aos dados históricos publicados previamente obtidos com o tratamento cirúrgico com utilização da artéria torácica interna esquerda. Estudos randomizados são necessários para confirmação destes achados.
Fonte de financiamentoNão há.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.
A revisão por pares é de responsabilidade da Sociedade Brasileira de Hemodinâmica e Cardiologia Intervencionista.