Apesar de a alta hospitalar no mesmo dia (AHMD) após intervenção coronária percutânea (ICP) eletiva não complicada ser adotada mundialmente, ela permanece pouco estudada em nosso meio. Objetivamos, assim, avaliar nossa experiência inicial com a AHMD após ICP eletiva, em relação à sua segurança e aos preditores de sucesso.
MétodosForam incluídos 161 pacientes consecutivos para AHMD, de único centro, selecionados em ambulatório especializado. Para a identificação dos fatores associados ao sucesso da AHMD, foram ajustados modelos de regressão logística simples e múltipla.
ResultadosA AHMD foi realizada com sucesso em 114 pacientes (70,8%), tendo os 47 pacientes restantes permanecido internados (45 com alta na manhã seguinte e 2 pacientes após 2 dias). Nenhum paciente com AHMD apresentou evento cardíaco adverso maior ou complicação vascular importante aos 30 dias e no seguimento mediano de 12 meses. No grupo internação, ocorreu apenas um caso de infarto agudo do miocárdio por oclusão de ramo lateral e dois hematomas > 5cm relacionados ao sítio de punção. Os preditores de sucesso da AHMD foram: via de acesso radial (OR = 5,92; IC95% 1,73‐20,21; p = 0,005), presença de lesões tipo A/B1 (OR = 14,09; IC95% 1,70‐116,49; p = 0,01) e volume de contraste (OR = 0,76; IC95% 0,65‐0,88; p < 0,001).
ConclusõesA AHMD foi segura e pôde ser realizada com sucesso na maioria dos pacientes selecionados para ICP eletiva, sendo seus preditores de sucesso o acesso radial, as lesões menos complexas e um volume menor de contraste.
Although same‐day discharge (SDD) after elective uncomplicated percutaneous coronary intervention (PCI) be adopted worldwide, it remains poorly studied in our country. We aim to evaluate our initial experience with SDD after elective PCI, regarding its safety and predictors of success.
MethodsA hundred and sixty‐one single‐center consecutive patients, selected in a specialized outpatient clinic, were included for SDD. To identify the factors associated with SDD, single and multiple logistic regression models were adjusted.
ResultsSDD was successfully performed in 114 patients (70.8%) and the remaining 47 patients remained hospitalized (45 with discharge in the following morning and 2 patients after 2 days). No patient with SDD presented major adverse cardiac events or major vascular complications at 30 days or at a median follow‐up of 12 months. In the inpatient group, there was only one case of acute myocardial infarction due to a lateral branch occlusion and two patients with > 5cm hematoma related to the access site. The SDD predictors were radial access route (OR = 5.92; 95%CI 1.73‐20.21; p = 0.005), presence of type A/B1 lesions (OR = 14.09; 95%CI 1.70‐116.49%; p = 0.01) and contrast volume (OR = 0.76; 95%CI 0.65‐0.88; p < 0.001).
ConclusionsSDD was safe and could be successfully performed in most patients selected for elective PCI, and its predictors were the radial access, less complex coronary lesions and a and lower contrast volume.
Desde que foi realizada pela primeira vez, há mais de três décadas, a intervenção coronária percutânea (ICP) tornou‐se o método mais utilizado de revascularização coronária em todo o mundo. O aperfeiçoamento das técnicas, aliado ao avanço tecnológico dos materiais dedicados e à eficácia da medicação adjunta, melhorou substancialmente a segurança e o sucesso do procedimento, reduzindo complicações e propiciando um menor tempo de internação hospitalar.1–5
Esses avanços tecnológicos, entretanto, permitiram o aumento crescente do número de ICPs, bem como propiciaram incrementos nos custos, impondo políticas de gerenciamento hospitalar voltadas para uma logística de contenção de gastos e que preservasse eficácia clínica, segurança e satisfação dos pacientes submetidos ao procedimento.6–9 Nesse sentido, estudos anteriores demonstraram significativa redução de custos relacionados à ICP, com a inclusão de pacientes eletivos selecionados e de baixo risco de complicações em programa de alta hospitalar no mesmo dia (AHMD).10 O conceito da AHMD foi avaliado em diversos estudos, os quais foram agrupados em recente metanálise, que confirmou a segurança e a eficácia da AHMD em comparação à observação hospitalar noturna para ICPs eletivas não complicadas.11,12
A AHMD nas ICPs não complicadas, embora bem estabelecida na prática da Cardiologia Intervencionista mundial,11 permanece pouco estudada e difundida em nosso meio.13 Além disso, há poucos dados na literatura a respeito dos preditores de sucesso na implementação de tal prática. Assim, os objetivos do presente estudo foram avaliar nossa experiência inicial com a AHMD após ICP eletiva, em relação à sua segurança e aos preditores de sucesso.
MétodosPopulação do estudoPacientes consecutivos, encaminhados para realização de angioplastia eletiva entre março de 2013 e novembro de 2014 (n = 459), de um único centro, foram avaliados ambulatorialmente, por um cardiologista intervencionista de nosso serviço (F.C.) antes da ICP, com o intuito de selecionar candidatos à AHMD. O estudo foi aprovado pelo Comitê de Ética em Pesquisa de nosso serviço e todos os pacientes assinaram um Termo de Consentimento para os procedimentos.
Com base nos critérios de apropriabilidade para a realização de ICP14 e em estudos prévios de AHMD,2,7,11,12,15,16 os seguintes critérios foram aplicados, com a intenção de selecionar pacientes elegíveis para o estudo: (1) presença de angina estável, angina em crescendo ou pacientes assintomáticos com teste funcional positivo para isquemia; (2) angioplastia eletiva de um ou dois vasos; (3) ausência de comorbidades clínicas significativas que justificassem necessidade de maior tempo de internação hospitalar para preparo do procedimento e cuidados pós‐angioplastia, como insuficiência cardíaca e fração de ejeção < 35%, doença renal crônica (clearance de creatinina < 60mL/minuto), diátese hemorrágica ou coagulopatias conhecidas, doença pulmonar obstrutiva crônica sintomática, alergia ao contraste, fragilidade e/ou idade > 80 anos; (4) anatomia coronária de baixa ou intermediária complexidade (escore SYNTAX < 33) que não envolvesse o tronco da coronária esquerda ou lesões em bifurcações planejadas para serem tratadas com dois stents; (5) possibilidade de realização do procedimento pela via radial, ou pela via femoral, preferencialmente com introdutor 5 F.
Após a realização do procedimento foram considerados os seguintes critérios para AHMD: ausência de complicações durante a ICP; ausência de dor precordial prolongada durante o procedimento ou dor precordial no período de repouso pós‐ICP; ausência de elevação de marcadores de necrose miocárdica 6 horas após o procedimento ou nova alteração eletrocardiográfica sugestiva de isquemia; ausência de complicações vasculares ou hematomas > 5cm relacionados ao sítio de punção; ICPs deveriam ser realizadas preferencialmente no período da manhã, em função do tempo de repouso, por conta do acesso vascular.
ProcedimentoPara os pacientes elegíveis para AHMD, a antiagregação plaquetária utilizada foi clopidogrel em dose de ataque de 300mg, administrado 24 horas antes do procedimento (com dose suplementar de 300mg imediatamente após a ICP), seguido de 75mg/dia por pelo menos 30 dias para stents convencionais ou 1 ano para stents farmacológicos. Para os pacientes que já faziam uso prévio do clopidogrel, foi administrada dose suplementar de 300mg ao término do procedimento. Para aqueles que utilizavam ticagrelor ou prasugrel, foram administrados 90 e 10mg, respectivamente, ao final do procedimento. Além disso, os pacientes receberam prescrição para utilizar aspirina (100mg/dia) indefinidamente. A via de acesso preferencial foi a radial, sendo a femoral uma alternativa diante da impossibilidade ou falha da via radial. Após obtenção do acesso vascular (5 ou 6 F), foi administrada heparina não fracionada na dose de 100 UI/kg. Inibidores da glicoproteína IIb/IIIa não foram utilizados. O procedimento seguiu a técnica atualmente estabelecida, sempre que possível utilizando o implante de stent direto. Após a ICP, os introdutores foram imediatamente retirados. Para a via femoral, foi administrada dose de protamina (1mL de Protamina 1000® para neutralizar 1.000 UI de heparina) e foi retirado o introdutor com compressão manual por 15 a 30 minutos, tendo sido feitos, em seguida, curativo compressivo e repouso do membro por, no mínimo, 4 horas. No caso da via radial, foi utilizada pulseira hemostática (TR Band®, Terumo Medical Co., Elkton, Estados Unidos) e foi realizado repouso do membro por 2 horas. O controle pós‐procedimento foi feito com eletrocardiograma (comparado com eletrocardiograma prévio à ICP), sinais vitais e exame físico da via de acesso. Foi realizada dosagem de troponina de alta sensibilidade 6 horas após o procedimento em todos os pacientes elegíveis para AHMD. Os pacientes que permaneceram assintomáticos, sem alterações eletrocardiográficas ou aumento significante de troponina, e sem complicações no local da punção, receberam alta, com orientações sobre a medicação, períodos adicionais de repouso, possíveis complicações e retorno ambulatorial para reavaliação. No caso de quaisquer sinais ou sintomas relacionados ao procedimento, eles foram orientados a procurar o serviço de emergência de nosso hospital.
Coleta e análise de dadosA coleta de dados do estudo foi realizada por enfermeiras e médicos treinados durante a internação índice, seguindo o preenchimento de formulários previamente padronizados. A coleta incluiu características clínicas, resultados de exames laboratoriais, dados do procedimento invasivo e evolução clínica até a alta hospitalar. Após a alta, o seguimento clínico dos pacientes foi realizado com retorno ambulatorial em até 30 dias do procedimento e, após esse período, por contato telefônico e revisão dos registros hospitalares.
Todas as angiografias foram analisadas pelo Serviço de Hemodinâmica e Cardiologia Intervencionista do hospital onde o estudo foi realizado, com o intuito de determinar o sucesso do procedimento, medidas e características do vaso e eventos adversos angiográficos (F.C. e H.B.R.). A aquisição de imagens foi realizada usando‐se duas ou mais projeções angiográficas da estenose após a administração de nitrato. Essas projeções foram repetidas no momento da angiografia de seguimento nos casos em que esta foi necessária. As características morfológicas qualitativas foram avaliadas utilizando‐se critérios padronizados.17,18
Desfechos e definiçõesO desfecho primário de segurança do estudo foi a ocorrência de eventos cardíacos adversos maiores combinados (óbito, infarto agudo do miocárdio ‐ IAM) e reintervenção, bem como a taxa de trombose de stent, reinternação e complicações vasculares aos 30 dias. Também foram avaliados tais desfechos no seguimento tardio de 12 meses, bem como os preditores de sucesso da AHMD, baseando‐se nas características clínicas e angiográficas e nos desfechos intra‐hospitalares.
Os óbitos incluíram causas cardíacas e não cardíacas. O diagnóstico de IAM com supradesnivelamento do segmento ST, angina estável e angina instável seguiram critérios descritos previamente.17,18 Foi considerada elevação significante da troponina o aumento de marcadores > 5 vezes o limite superior da normalidade (LSN da troponina de 0,01μg/L).19 O sucesso angiográfico foi definido por redução da lesão‐alvo < 30%, com manutenção ou restabelecimento do fluxo anterógrado normal (Thrombolysis in Myocardial Infarction ‐ TIMI 3). A revascularização da lesão‐alvo foi definida como nova intervenção, cirúrgica ou percutânea, em lesões com obstrução > 50% dentro do stent previamente implantado ou no segmento que incluísse os 5mm proximais e/ou os 5mm distais ao stent. Trombose intra‐stent foi definida segundo a classificação do Academic Research Consortium.20
Complicações intraprocedimento incluíram dor torácica prolongada, instabilidade hemodinâmica, oclusão transitória do vaso, fenômenos de no‐reflow e slow‐flow, oclusão de ramo lateral > 1,5mm e resultado angiográfico subótimo. As lesões foram classificadas em tipos A, B1, B2 e C, segundo o American College of Cardiology/American Heart Association (ACC/AHA).21 Complicações vasculares compreendiam sangramento maior pela classificação TIMI (hemorragia intracraniana ou queda > 5mg/dL da hemoglobina ou 15% do hematócrito), hematoma importante no local da punção > 5cm, pseudoaneurisma, fístulas ou trombose com necessidade de intervenção cirúrgica.15
Análise estatísticaAs variáveis categóricas foram apresentadas como frequências e porcentagens, e comparadas com o teste qui quadrado. As variáveis contínuas foram descritas como médias e desvios padrão, ou mediana e intervalo interquartil (percentis 25 e 75), sendo comparadas com o teste de t de Student ou a Análise de Variância (ANOVA). Modelos univariados e multivariados, utilizando a regressão logística binária, foram utilizados para identificar os preditores de sucesso da AHMD, apresentando as variáveis um valor de p < 0,05 incluídas no modelo multivariado. Todos os testes foram bicaudais e um valor de p < 0,05 foi considerado significativo. As análises foram realizadas com a utilização do programa Statistical Package for the Social Science (SPSS), versão 20.0 (SPSS Inc., Chicago, Estados Unidos).
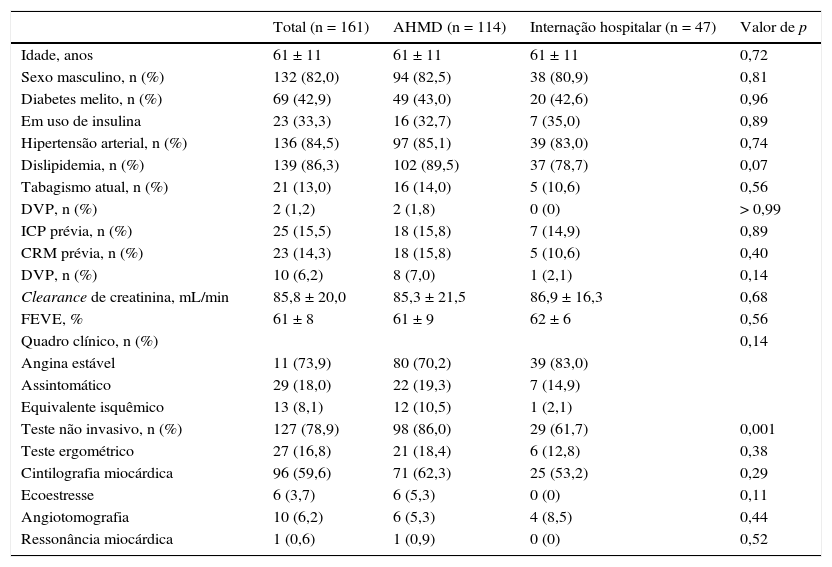
ResultadosNo período do estudo, 161 pacientes foram selecionados para AHMD, tendo essa estratégia sido adotada com sucesso em 114 pacientes (70,8%); os 47 pacientes restantes (29,2%) permaneceram internados (45 com alta na manhã seguinte e 2 pacientes após dois dias). As características clínicas da população global do estudo, bem como em relação aos grupos AHMD e internação, estão apresentadas na tabela 1. Ambos os grupos foram bastante semelhantes, sendo a maioria dos pacientes do sexo masculino, com média de idade de 61 ± 11 anos e alta prevalência de diabéticos (42,9%). A maioria dos pacientes apresentou‐se com angina estável (73,9%) e tinha fração de ejeção do ventrículo esquerdo preservada (61% ± 8%).
Características clínicas basais
| Total (n = 161) | AHMD (n = 114) | Internação hospitalar (n = 47) | Valor de p | |
|---|---|---|---|---|
| Idade, anos | 61 ± 11 | 61 ± 11 | 61 ± 11 | 0,72 |
| Sexo masculino, n (%) | 132 (82,0) | 94 (82,5) | 38 (80,9) | 0,81 |
| Diabetes melito, n (%) | 69 (42,9) | 49 (43,0) | 20 (42,6) | 0,96 |
| Em uso de insulina | 23 (33,3) | 16 (32,7) | 7 (35,0) | 0,89 |
| Hipertensão arterial, n (%) | 136 (84,5) | 97 (85,1) | 39 (83,0) | 0,74 |
| Dislipidemia, n (%) | 139 (86,3) | 102 (89,5) | 37 (78,7) | 0,07 |
| Tabagismo atual, n (%) | 21 (13,0) | 16 (14,0) | 5 (10,6) | 0,56 |
| DVP, n (%) | 2 (1,2) | 2 (1,8) | 0 (0) | > 0,99 |
| ICP prévia, n (%) | 25 (15,5) | 18 (15,8) | 7 (14,9) | 0,89 |
| CRM prévia, n (%) | 23 (14,3) | 18 (15,8) | 5 (10,6) | 0,40 |
| DVP, n (%) | 10 (6,2) | 8 (7,0) | 1 (2,1) | 0,14 |
| Clearance de creatinina, mL/min | 85,8 ± 20,0 | 85,3 ± 21,5 | 86,9 ± 16,3 | 0,68 |
| FEVE, % | 61 ± 8 | 61 ± 9 | 62 ± 6 | 0,56 |
| Quadro clínico, n (%) | 0,14 | |||
| Angina estável | 11 (73,9) | 80 (70,2) | 39 (83,0) | |
| Assintomático | 29 (18,0) | 22 (19,3) | 7 (14,9) | |
| Equivalente isquêmico | 13 (8,1) | 12 (10,5) | 1 (2,1) | |
| Teste não invasivo, n (%) | 127 (78,9) | 98 (86,0) | 29 (61,7) | 0,001 |
| Teste ergométrico | 27 (16,8) | 21 (18,4) | 6 (12,8) | 0,38 |
| Cintilografia miocárdica | 96 (59,6) | 71 (62,3) | 25 (53,2) | 0,29 |
| Ecoestresse | 6 (3,7) | 6 (5,3) | 0 (0) | 0,11 |
| Angiotomografia | 10 (6,2) | 6 (5,3) | 4 (8,5) | 0,44 |
| Ressonância miocárdica | 1 (0,6) | 1 (0,9) | 0 (0) | 0,52 |
AHMD: alta hospitalar no mesmo dia; ICP: intervenção coronária percutânea; CRM: cirurgia de revascularização miocárdica; FEVE: fração de ejeção do ventrículo esquerdo; DVP: doença vascular periférica.
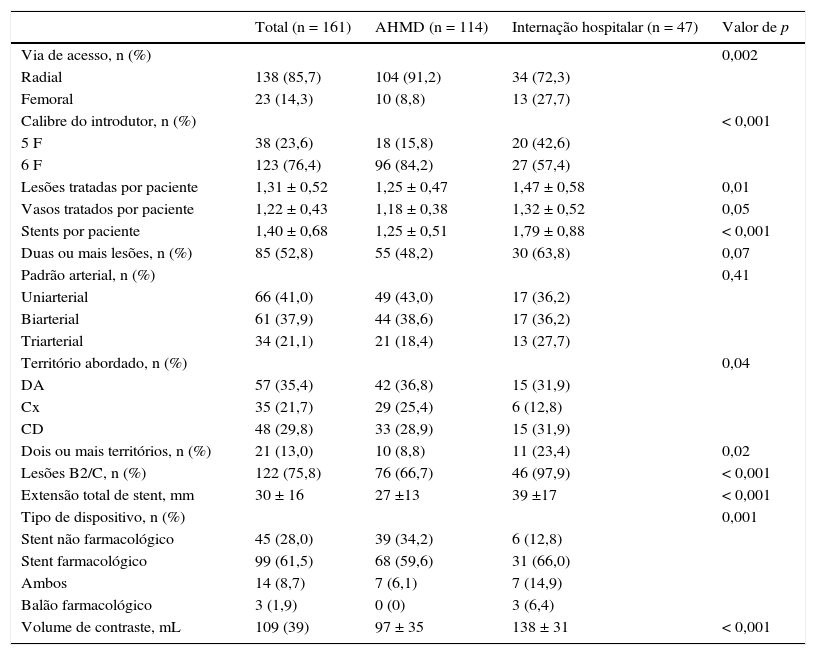
As características angiográficas são apresentadas na tabela 2. Houve um maior uso do acesso radial e introdutor 6 F no grupo AHMD (91,2% vs. 72,3%; p = 0,002; e 84,2% vs. 57,4%; p < 0,001, respectivamente). Apesar do padrão arterial semelhante entre ambos os grupos, a complexidade das intervenções foi menor no grupo AHMD em relação ao grupo internação. Isso ficou demonstrado pelo menor número de lesões tratadas por paciente (1,25 ± 0,47 vs. 1,47 ± 0,58; p = 0,01), a menor complexidade das lesões (lesões tipo B2/C 66,7% vs. 97,9%; p < 0,001) e o menor número de stents/paciente (1,25 ± 0,51 vs. 1,79 ± 0,88; p < 0,001).
Características angiográficas
| Total (n = 161) | AHMD (n = 114) | Internação hospitalar (n = 47) | Valor de p | |
|---|---|---|---|---|
| Via de acesso, n (%) | 0,002 | |||
| Radial | 138 (85,7) | 104 (91,2) | 34 (72,3) | |
| Femoral | 23 (14,3) | 10 (8,8) | 13 (27,7) | |
| Calibre do introdutor, n (%) | < 0,001 | |||
| 5 F | 38 (23,6) | 18 (15,8) | 20 (42,6) | |
| 6 F | 123 (76,4) | 96 (84,2) | 27 (57,4) | |
| Lesões tratadas por paciente | 1,31 ± 0,52 | 1,25 ± 0,47 | 1,47 ± 0,58 | 0,01 |
| Vasos tratados por paciente | 1,22 ± 0,43 | 1,18 ± 0,38 | 1,32 ± 0,52 | 0,05 |
| Stents por paciente | 1,40 ± 0,68 | 1,25 ± 0,51 | 1,79 ± 0,88 | < 0,001 |
| Duas ou mais lesões, n (%) | 85 (52,8) | 55 (48,2) | 30 (63,8) | 0,07 |
| Padrão arterial, n (%) | 0,41 | |||
| Uniarterial | 66 (41,0) | 49 (43,0) | 17 (36,2) | |
| Biarterial | 61 (37,9) | 44 (38,6) | 17 (36,2) | |
| Triarterial | 34 (21,1) | 21 (18,4) | 13 (27,7) | |
| Território abordado, n (%) | 0,04 | |||
| DA | 57 (35,4) | 42 (36,8) | 15 (31,9) | |
| Cx | 35 (21,7) | 29 (25,4) | 6 (12,8) | |
| CD | 48 (29,8) | 33 (28,9) | 15 (31,9) | |
| Dois ou mais territórios, n (%) | 21 (13,0) | 10 (8,8) | 11 (23,4) | 0,02 |
| Lesões B2/C, n (%) | 122 (75,8) | 76 (66,7) | 46 (97,9) | < 0,001 |
| Extensão total de stent, mm | 30 ± 16 | 27 ±13 | 39 ±17 | < 0,001 |
| Tipo de dispositivo, n (%) | 0,001 | |||
| Stent não farmacológico | 45 (28,0) | 39 (34,2) | 6 (12,8) | |
| Stent farmacológico | 99 (61,5) | 68 (59,6) | 31 (66,0) | |
| Ambos | 14 (8,7) | 7 (6,1) | 7 (14,9) | |
| Balão farmacológico | 3 (1,9) | 0 (0) | 3 (6,4) | |
| Volume de contraste, mL | 109 (39) | 97 ± 35 | 138 ± 31 | < 0,001 |
AHMD: alta hospitalar no mesmo dia; DA: descendente anterior; Cx: circunflexa; CD: coronária direita.
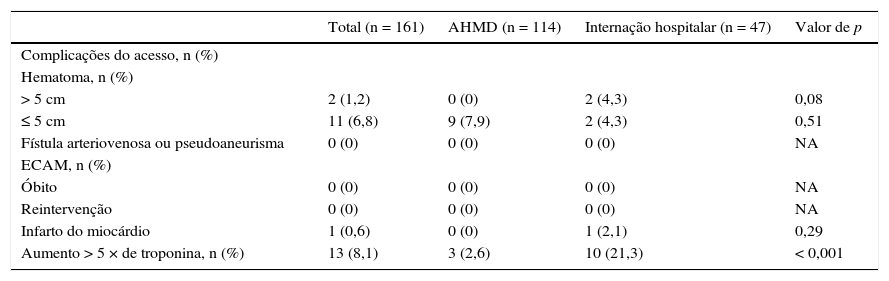
Os desfechos hospitalares são apresentados na tabela 3. Com respeito às complicações da via de acesso, observamos hematomas > 5 cm em 2 pacientes do grupo internação nas primeiras 12 horas após a intervenção e 11 pacientes com hematoma pequenos (≤ 5 cm), sendo 9 no grupo AHMD e 2 no grupo internação (p = 0,51). Não houve caso de pseudoaneurisma e nem fístula arteriovenosa em nenhum dos grupos. O aumento da troponina > 5 vezes o LSN, apesar de ser critério de exclusão para AHMD, ocorreu em 2,6% dos casos desse grupo. Com respeito às complicações cardíacas adversas maiores, observamos apenas um caso de IAM no grupo internação, em decorrência do fechamento de ramo lateral associado a dor torácica, alteração eletrocardiográfica e elevação de marcadores de necrose miocárdica. Não houve óbitos e nem reintervenções em ambos os grupos até um seguimento mediano de 12 meses (6,2 a 28,7 meses).
Desfechos hospitalares
| Total (n = 161) | AHMD (n = 114) | Internação hospitalar (n = 47) | Valor de p | |
|---|---|---|---|---|
| Complicações do acesso, n (%) | ||||
| Hematoma, n (%) | ||||
| > 5 cm | 2 (1,2) | 0 (0) | 2 (4,3) | 0,08 |
| ≤ 5 cm | 11 (6,8) | 9 (7,9) | 2 (4,3) | 0,51 |
| Fístula arteriovenosa ou pseudoaneurisma | 0 (0) | 0 (0) | 0 (0) | NA |
| ECAM, n (%) | ||||
| Óbito | 0 (0) | 0 (0) | 0 (0) | NA |
| Reintervenção | 0 (0) | 0 (0) | 0 (0) | NA |
| Infarto do miocárdio | 1 (0,6) | 0 (0) | 1 (2,1) | 0,29 |
| Aumento > 5 × de troponina, n (%) | 13 (8,1) | 3 (2,6) | 10 (21,3) | < 0,001 |
AHMD: alta hospitalar no mesmo dia; ECAM: eventos cardíacos adversos maiores; NA: não aplicável.
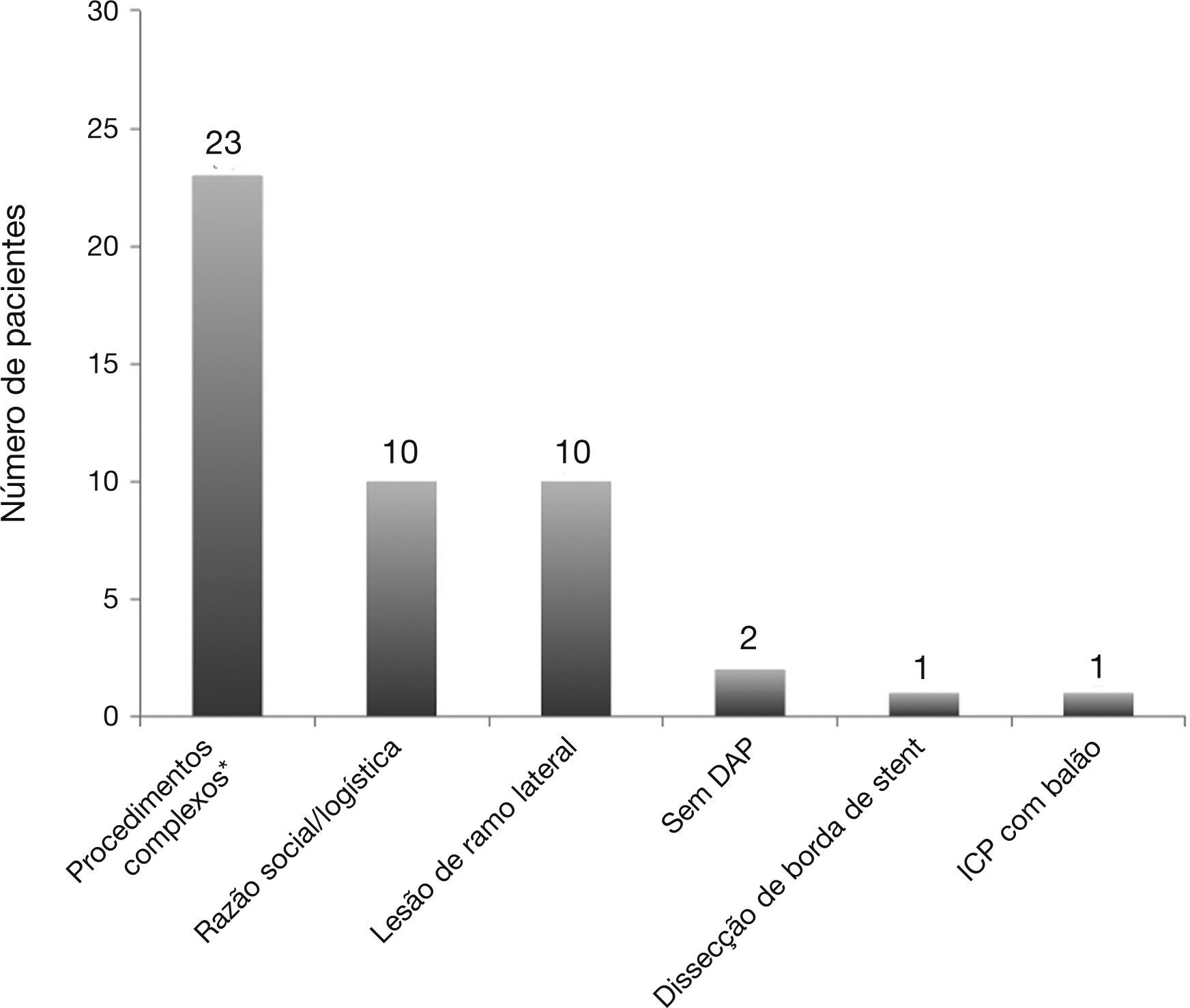
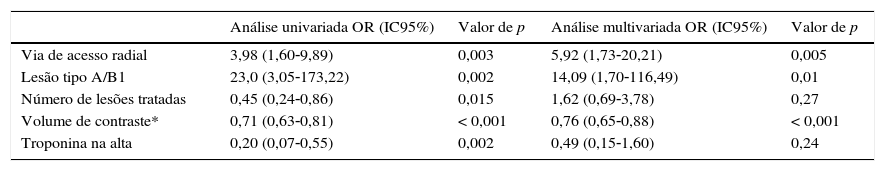
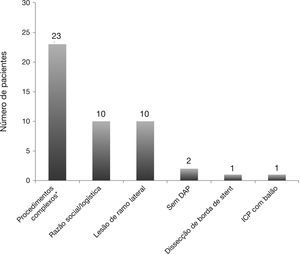
As principais razões para a falha da AHMD nessa população são demonstradas na figura 1. Os preditores independentes de sucesso da AHMD pela análise multivariada são apresentados na tabela 4. O uso do acesso radial (Odds Ratio ‐ OR: 5,920; intervalo de confiança de 95% ‐ IC95%: 1,73‐20,21; p = 0,005), a presença de lesões tipo A/B1 (OR: 14,09; IC95% 1,70‐116,49; p = 0,01) e o volume de contraste (OR: 0,76; IC95%: 0,65‐0,88; p < 0,001) foram fatores relacionados ao sucesso da AHMD.
Preditores de sucesso da alta hospitalar no mesmo dia
| Análise univariada OR (IC95%) | Valor de p | Análise multivariada OR (IC95%) | Valor de p | |
|---|---|---|---|---|
| Via de acesso radial | 3,98 (1,60‐9,89) | 0,003 | 5,92 (1,73‐20,21) | 0,005 |
| Lesão tipo A/B1 | 23,0 (3,05‐173,22) | 0,002 | 14,09 (1,70‐116,49) | 0,01 |
| Número de lesões tratadas | 0,45 (0,24‐0,86) | 0,015 | 1,62 (0,69‐3,78) | 0,27 |
| Volume de contraste* | 0,71 (0,63‐0,81) | < 0,001 | 0,76 (0,65‐0,88) | < 0,001 |
| Troponina na alta | 0,20 (0,07‐0,55) | 0,002 | 0,49 (0,15‐1,60) | 0,24 |
OR: Odds Ratio; IC95%: intervalo de confiança de 95%.
* A cada incremento de 10mL de volume de contraste.
O presente estudo teve como objetivo avaliar nossa experiência inicial com a AHMD após ICP eletiva, no que diz respeito à sua segurança, bem como os preditores de sucesso. Em população consecutiva de 161 pacientes selecionados de nosso ambulatório pré‐ICP, a AHMD foi aplicada com sucesso em grande parte dos pacientes (71%), sendo que, em ambos os grupos (AHMD e internação), a taxa de eventos cardíacos adversos maiores foi baixa, e nenhum evento ocorreu nos pacientes do grupo AHMD. Foram seus preditores de sucesso: o uso do acesso radial, a menor complexidade angiográfica das lesões e o menor volume de contraste utilizado.
Desde os primeiros relatos de sucesso há quase duas décadas,22 a prática da AHMD enfrentou uma série de barreiras para que pudesse ser implementada como estratégia viável em pacientes eletivos submetidos à ICP. As preocupações abrangiam desde questões de segurança médico‐legais, preferência e satisfação dos pacientes, além de análise de custos.23–27 Mesmo assim, diversos estudos ao longo dos últimos anos avaliaram a prática da AHMD com resultados bastante interessantes. Tais resultados foram agrupados em importante metanálise por Abdelaal et al.,11 envolvendo cinco estudos randomizados e oito observacionais, com um total de 111.830 pacientes incluídos. Apesar de diferentes métodos de adoção da prática de AHMD entre os estudos avaliados, foi evidenciada uma ampla aplicabilidade da AHMD, com baixas taxas de eventos adversos cardiovasculares, internações repetidas e complicações globais, confirmando‐a como alternativa viável em ICPs eletivas não complicadas.
Em nosso meio, a experiência com tal prática é pequena.13 No presente estudo, que avaliou pacientes consecutivos selecionados para AHMD, esta foi possível em 71%, sendo que 29% acabaram internados para alta no dia seguinte. Isto é um pouco superior ao observado na literatura, que gira em torno de 10 a 20%.15 Se fizermos uma análise dos principais motivos que levaram os pacientes a não terem AHMD, o acesso vascular (femoral) e a complexidade dos procedimentos foram os mais importantes. Grande parte dos estudos de AHMD analisou a segurança e a eficácia dessa estratégia utilizando o acesso radial como forma de minimizar eventuais complicações do acesso vascular. Em nosso estudo, 85,7% dos pacientes utilizaram a via radial e 14,3%, a femoral, sendo que o uso do acesso femoral aumentou em seis vezes a chance de internação, apesar de, na maioria das vezes, ter sido utilizado introdutor menos calibroso (5 F). Por conta do tempo de repouso menor e dos claros benefícios em relação à redução de complicações vasculares, o acesso preferencial na adoção da prática de AHMD deve ser o radial.11,16,28 No entanto, a abordagem femoral ainda é muito utilizada globalmente, principalmente em países da Europa, Estados Unidos e em grande parte do Brasil. Assim, a alta precoce com a abordagem femoral já foi descrita com segurança em alguns estudos e também poder ser utilizada.12,29
Nosso estudo evidenciou grande segurança em relação aos desfechos hospitalares, após 30 dias do procedimento e no seguimento tardio, conforme já demonstrado na literatura.11,16,30,31 Houve apenas dois casos de complicações vasculares maiores (hematoma > 5cm no sítio do acesso vascular) observados dentro das 6 horas após ICP e apenas um caso de IAM sintomático por fechamento do ramo lateral durante o procedimento. Não tivemos caso de óbito ou reintervenção na mediana de seguimento de 12 meses. Além disso, entre os pacientes com aumento significativo de troponina (8,1%), não foi observada qualquer implicação clínica relacionada à elevação isolada desses marcadores, sendo que três desses pacientes foram de AHMD e dez deles ficaram internados para observação no período noturno. Heyde et al.,12 em estudo randomizado prévio, também observaram baixa taxa de eventos clínicos adversos, sendo que nenhum deles ocorreu entre as 6 e 24 horas pós‐procedimento, validando a confiança do monitoramento da AHMD apenas nas primeiras 6 horas. Em nosso meio, Trindade et al.,13 avaliando retrospectivamente 69 pacientes incluídos em protocolo de AHMD, também demonstraram sua segurança após observação média de 6,8 horas, sendo que, em seguimento de 30 dias, nenhum evento clínico foi identificado.
A construção de um programa bem‐sucedido de AHMD exige a escolha e a implicação em uma equipe multidisciplinar, bem como de todos os profissionais de saúde envolvidos no atendimento ao paciente. A seleção desses pacientes envolve uma reeducação institucional naturalmente voltada para um programa bem estabelecido de triagem pré‐procedimento, estreitando as relações médico‐paciente‐familiares, com planejamento de contingência para as prováveis emergências e acompanhamento minucioso em curto e longo prazos após o procedimento. Foi pensando nessa estratégia que implementamos, em nosso hospital, o ambulatório de avaliação pré‐angioplastia, para que um cardiologista intervencionista pudesse selecionar os candidatos ideais para a implementação do projeto de AHMD. Na literatura, tal seleção de pacientes mostrou‐se capaz de reduzir as complicações pós‐ICP, como eventos isquêmicos (fechamento abrupto de vasos principais e ramos secundários e dissecções de bordas), infartos periprocedimento e trombose aguda de stent, bem como redução de sangramentos e complicações vasculares.28,32
LimitaçõesTratou‐se de estudo unicêntrico com amostra pequena e de pacientes selecionados, de tal forma que potenciais vieses de seleção podem ter influenciado nos resultados, e sua generalização para outros centros com características distintas pode não ser possível. No presente estudo, o grau de satisfação não foi avaliado e isso deve ser objeto de futuros estudos. Os custos hospitalares, bem como sua potencial redução com a prática da AHMD, não foram especificamente avaliados, e isso deve ser considerado em estudos futuros.
ConclusõesEm pacientes selecionados ambulatorialmente de baixo risco para intervenção coronária percutânea, a estratégia de alta hospitalar no mesmo dia foi alcançada na maioria dos casos e mostrou‐se segura em nosso meio, com respeito às taxas de eventos cardíacos adversos maiores e às complicações vasculares. Foram preditores de sucesso: uso da via de acesso radial e menor complexidade angiográfica das lesões ‐ ressaltando que a via de acesso radial deve ser preferida e que a seleção de pacientes é fundamental. O crescente número de procedimentos eletivos de intervenção coronária percutânea e os gastos envolvidos com essa expansão ao longo dos anos fazem da alta hospitalar no mesmo dia uma estratégia logística substancial para a redução de custos hospitalares. Nesse sentido, os resultados do presente estudo, em congruência com os diversos estudos na literatura, ressaltam que a prática da alta hospitalar no mesmo dia deve ser estimulada para pacientes de baixo risco submetidos à intervenção coronária percutânea eletiva em nosso meio.
Fonte de financiamentoNão há.
Conflitos de interesseOs autores declaram não haver conflitos de interesse.