Los test cognitivos breves (TCB) pueden ayudar a detectar el deterioro cognitivo (DC) en el ámbito asistencial. Se han desarrollado y/o validado varios TCB en nuestro país, pero no existen recomendaciones específicas para su uso.
DesarrolloRevisión de estudios sobre el rendimiento diagnóstico en la detección del DC llevados a cabo en España con TCB que requieran menos de 20min y recomendaciones de uso consensuadas por expertos, sobre la base de las características de los TCB y de los estudios disponibles.
ConclusiónEl Fototest, el Memory Impairment Screen (MIS) y el Mini-Mental State Examination (MMSE) son las opciones más recomendables para el primer nivel asistencial, pudiendo añadirse otros test (Test del Reloj [TR] y test de fluidez verbal [TFV]) en caso de resultado negativo y queja o sospecha persistente (aproximación escalonada). En el segundo nivel asistencial es conveniente una evaluación sistemática de las distintas áreas cognitivas, que puede llevarse a cabo con instrumentos como el Montreal Cognitive Assessment, el MMSE, el Rowland Universal Dementia Assessment o el Addenbrooke's Cognitive Examination, o bien mediante el uso escalonado o combinado de herramientas más simples (TR, TFV, Fototest, MIS, Test de Alteración de la Memoria y Eurotest). El uso asociado de cuestionarios cumplimentados por un informador (CCI) aporta valor añadido a los TCB en la detección del DC.
La elección de los instrumentos vendrá condicionada por las características del paciente, la experiencia del clínico y el tiempo disponible. Los TCB y los CCI deben reforzar —pero nunca suplantar— el juicio clínico, la comunicación con el paciente y el diálogo interprofesional.
Brief cognitive tests (BCT) may help detect cognitive impairment (CI) in the clinical setting. Several BCT have been developed and/or validated in our country, but we lack specific recommendations for use.
DevelopmentReview of studies on the diagnostic accuracy of BCT for CI, using studies conducted in Spain with BCT which take less than 20min. We provide recommendations of use based on expert consensus and established on the basis of BCT characteristics and study results.
ConclusionThe Fototest, the Memory Impairment Screen (MIS) and the Mini-Mental State Examination (MMSE) are the preferred options in primary care; other BCT (Clock Drawing Test [CDT], test of verbal fluency [TVF]) may also be administered in cases of negative results with persistent suspected CI or concern (stepwise approach). In the specialised care setting, a systematic assessment of the different cognitive domains should be conducted using the Montreal Cognitive Assessment, the MMSE, the Rowland Universal Dementia Assessment, the Addenbrooke's Cognitive Examination, or by means of a stepwise or combined approach involving more simple tests (CDT, TVF, Fototest, MIS, Memory Alteration Test, Eurotest). Associating an informant questionnaire (IQ) with the BCT is superior to the BCT alone for the detection of CI.
The choice of instruments will depend on the patient's characteristics, the clinician's experience, and available time. The BCT and IQ must reinforce — but never substitute — clinical judgment, patient-doctor communication, and inter-professional dialogue.
El envejecimiento de la población ha incrementado la prevalencia del deterioro cognitivo (DC) y de la demencia asociados a procesos neurodegenerativos, vasculares, médicos de otra índole o psiquiátricos, muchos de los cuales son modificables1,2. La existencia de tratamientos farmacológicos y no farmacológicos, tanto preventivos como paliativos, que reducen significativamente la carga personal, familiar y social del DC obliga a su diagnóstico temprano, tal y como han recomendado los profesionales, gobiernos y colectivos implicados3–6.
La demencia, en la mayoría de los casos, está precedida por una situación de disfunción cognitiva objetivable denominada DC ligero o alteración cognitiva leve (ACL)7–9. Esta entidad sindrómica, aunque etiológicamente heterogénea, comporta un riesgo elevado de desarrollo de demencia10 y ofrece un espacio muy atractivo para evaluar las posibles intervenciones preventivas2. En la práctica clínica habitual, los pacientes acuden a la consulta en distintas fases del DC y la separación entre la ACL y la demencia no es nítida. Parece, por tanto, oportuno dirigir los esfuerzos diagnósticos a la detección de todo el espectro del DC, tanto en sus formas incipientes (ACL) como en las más avanzadas (demencia).
En un reciente estudio poblacional realizado en mayores de 65años en nuestro país, se obtuvo una prevalencia de casos con DC del 20%11; a pesar de la elevada prevalencia, muchos de los casos están probablemente sin diagnosticar12 o sin registrar adecuadamente13, algo que contrasta con la elevada frecuencia de quejas de pérdida de memoria reportadas en las consultas médicas14. Las razones de este infradiagnóstico pueden ser: la falta de accesibilidad o de tiempo en las consultas médicas, la escasa formación, confianza o seguridad diagnóstica de los profesionales, la falta de herramientas de detección eficientes o el uso inadecuado de las mismas15.
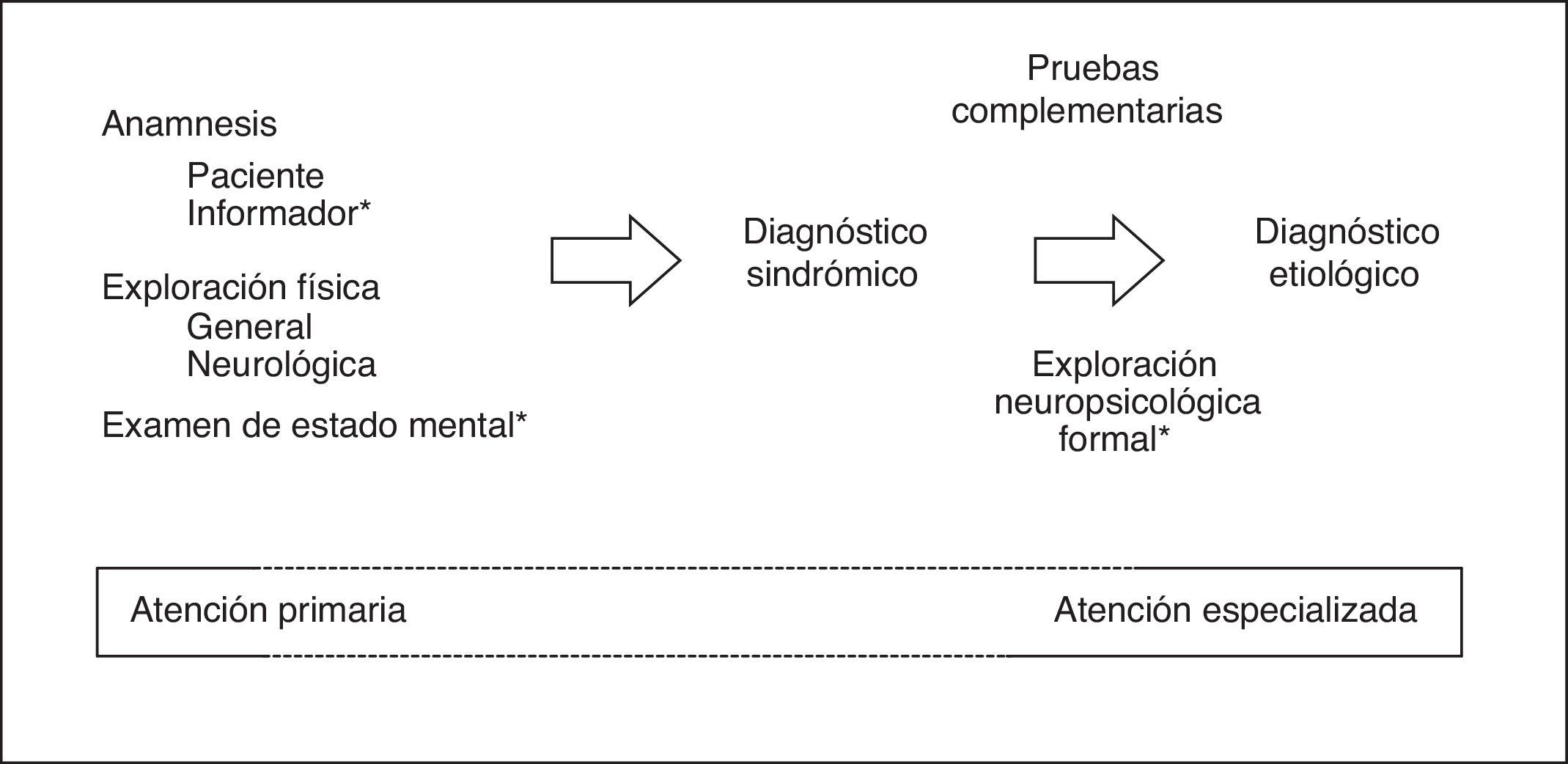
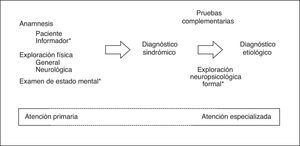
Ante una sospecha de DC es fundamental descartar, en primer lugar, un síndrome confusional o un síndrome focal agudo o subagudo (menos de 3meses de evolución), cuadros sustancialmente distintos del DC (de naturaleza crónica) que requieren un manejo urgente (generalmente hospitalario)9 y que han de ser evaluados con herramientas específicas16. Por definición, el DC ha de detectarse y diagnosticarse mediante pruebas que pongan en juego las capacidades cognitivas del paciente, dentro del marco tradicional pero insustituible del método clínico17, en el que cobran especial relevancia la información aportada por una persona allegada al paciente (tanto en lo que respecta a las capacidades cognitivas como al desempeño en las actividades habituales) y el examen del estado mental (EEM)18 (fig. 1).
Existen excelentes revisiones acerca del valor de los test cognitivos breves (TCB) en la detección de la demencia, algunas de ellas realizadas en nuestro país19–21, pero la utilidad de los TCB en la detección del DC ha sido mucho menos abordada21. El objetivo de este artículo es revisar la utilidad de los TCB y ofrecer orientaciones para su uso racional en una primera aproximación al paciente con queja o sospecha de DC, desde el ámbito asistencial. Se espera poder contribuir así a un diagnóstico más eficiente y preciso y a una actuación terapéutica temprana que evite o retrase la aparición de la demencia y reduzca su elevado coste personal, familiar y social.
DesarrolloMétodoEn esta revisión de expertos se evalúan las principales características de los TCB y se ofrecen orientaciones para su utilización en la práctica clínica. Se entiende por TCB aquel cuyo tiempo medio de administración es inferior a 20min. Para establecer las orientaciones de uso se distinguen los 2 principales niveles asistenciales en los que se articulan los sistemas sanitarios: el primer nivel o atención primaria (AP) y el segundo nivel o atención especializada (AE). Habitualmente, el primer contacto del paciente con el sistema sanitario ocurre en el primer nivel, que presta atención ambulatoria en el centro de salud y en el domicilio y que realiza además actividades de prevención y de detección precoz. El segundo nivel cubre la asistencia de los pacientes derivados tanto del primero como del segundo nivel mediante consultas, unidades de hospitalización, servicios de hospitalización a domicilio y urgencias hospitalarias. Los sistemas sanitarios interactúan, además, con otros dispositivos sociosanitarios que proveen otros servicios asistenciales o que cubren necesidades concretas (hospitales de media estancia, centros de día, residencias, etc.). La definición de cada nivel asistencial, adaptada a los objetivos de esta revisión, se muestra en la tabla 1.
Definición de los niveles asistenciales aplicada en esta revisión
| Primer nivel asistencial (AP) | Segundo nivel asistencial (AE) | |
|---|---|---|
| Definición | Ámbito de actuación médica, público o privado, en el que el paciente o un informador acuden por iniciativa propia | El paciente acude remitido por otro profesional, de cualquier ámbito o nivel asistencial, por sospecha de deterioro cognitivo |
| Profesionales implicados | Médicos en general, médicos de familia, profesionales de enfermería | Neurólogos, psicólogos, geriatras, psiquiatras, internistas |
La AP es el ámbito más próximo y accesible, y sus profesionales poseen una perspectiva longitudinal del paciente que es fundamental para la detección del DC, especialmente en los pacientes con un elevado nivel educativo o intelectual previo y cuando no se dispone de un informador. Los profesionales de la AE no suelen tener conocimiento previo del paciente, pero sí más experiencia y medios en relación con tareas menos frecuentes. La AP es, por tanto, el lugar adecuado para la detección y el manejo inicial del DC, mientras que la AE lo es para la confirmación diagnóstica, para el establecimiento de la etiología y para el inicio del tratamiento específico.
En esta revisión no se valora la detección sistemática del DC en la población, cuya oportunidad no está clara5 y cuya metodología sigue siendo incierta22. Tampoco se evalúan los test cognitivos realizados telefónicamente o a través de Internet, ni los test cognitivos autocumplimentados o administrados por un cuidador; estas pueden ser opciones útiles para pacientes que se encuentran en zonas aisladas, que presentan problemas de movilidad u otros problemas de salud o que están poco motivados para acudir a la consulta, pero la experiencia es todavía limitada23–25.
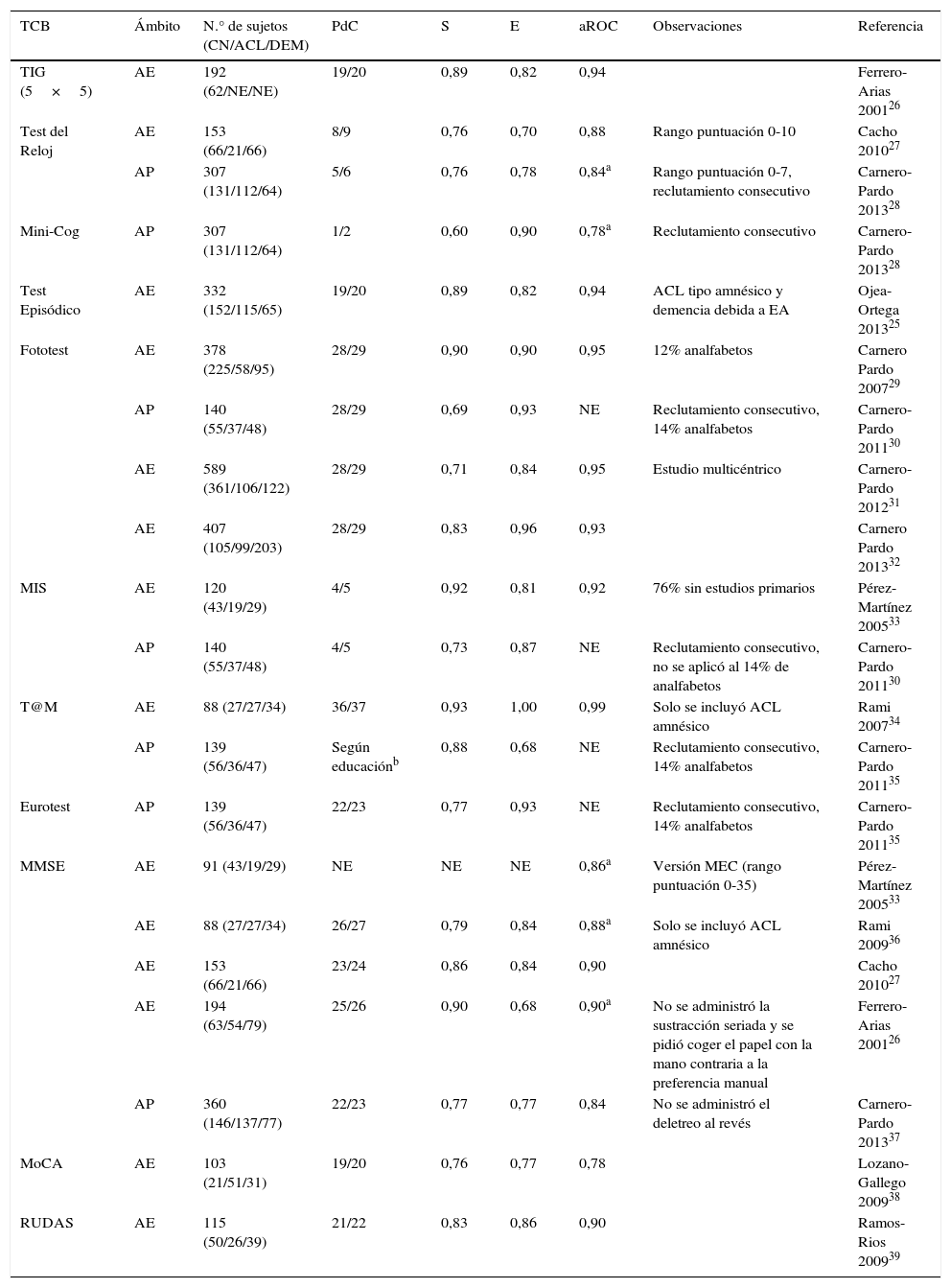
Se describen brevemente los TCB con estudios de validación para la detección del DC realizados en nuestro país y se ofrecen orientaciones para su utilización. El orden de presentación viene dado por el tiempo de administración y solo se reseñan los datos esenciales. El lector podrá encontrar más detalles acerca de las características de cada test, de su modo de administración y de su rendimiento diagnóstico en la tabla 2, en los estudios de validación referidos en esa tabla25–39 y en una reciente monografía específica40. Para facilitar la comparación entre los distintos TCB, solo se describen los parámetros de exactitud diagnóstica (sensibilidad, especificidad y área bajo la curva ROC [aROC]) correspondientes al punto de corte que maximiza la suma de la sensibilidad y la especificidad.
Estudios de validación de los TCB para la detección del DC realizados en España
| TCB | Ámbito | N.° de sujetos (CN/ACL/DEM) | PdC | S | E | aROC | Observaciones | Referencia |
|---|---|---|---|---|---|---|---|---|
| TIG (5×5) | AE | 192 (62/NE/NE) | 19/20 | 0,89 | 0,82 | 0,94 | Ferrero-Arias 200126 | |
| Test del Reloj | AE | 153 (66/21/66) | 8/9 | 0,76 | 0,70 | 0,88 | Rango puntuación 0-10 | Cacho 201027 |
| AP | 307 (131/112/64) | 5/6 | 0,76 | 0,78 | 0,84a | Rango puntuación 0-7, reclutamiento consecutivo | Carnero-Pardo 201328 | |
| Mini-Cog | AP | 307 (131/112/64) | 1/2 | 0,60 | 0,90 | 0,78a | Reclutamiento consecutivo | Carnero-Pardo 201328 |
| Test Episódico | AE | 332 (152/115/65) | 19/20 | 0,89 | 0,82 | 0,94 | ACL tipo amnésico y demencia debida a EA | Ojea-Ortega 201325 |
| Fototest | AE | 378 (225/58/95) | 28/29 | 0,90 | 0,90 | 0,95 | 12% analfabetos | Carnero Pardo 200729 |
| AP | 140 (55/37/48) | 28/29 | 0,69 | 0,93 | NE | Reclutamiento consecutivo, 14% analfabetos | Carnero-Pardo 201130 | |
| AE | 589 (361/106/122) | 28/29 | 0,71 | 0,84 | 0,95 | Estudio multicéntrico | Carnero-Pardo 201231 | |
| AE | 407 (105/99/203) | 28/29 | 0,83 | 0,96 | 0,93 | Carnero Pardo 201332 | ||
| MIS | AE | 120 (43/19/29) | 4/5 | 0,92 | 0,81 | 0,92 | 76% sin estudios primarios | Pérez-Martínez 200533 |
| AP | 140 (55/37/48) | 4/5 | 0,73 | 0,87 | NE | Reclutamiento consecutivo, no se aplicó al 14% de analfabetos | Carnero-Pardo 201130 | |
| T@M | AE | 88 (27/27/34) | 36/37 | 0,93 | 1,00 | 0,99 | Solo se incluyó ACL amnésico | Rami 200734 |
| AP | 139 (56/36/47) | Según educaciónb | 0,88 | 0,68 | NE | Reclutamiento consecutivo, 14% analfabetos | Carnero-Pardo 201135 | |
| Eurotest | AP | 139 (56/36/47) | 22/23 | 0,77 | 0,93 | NE | Reclutamiento consecutivo, 14% analfabetos | Carnero-Pardo 201135 |
| MMSE | AE | 91 (43/19/29) | NE | NE | NE | 0,86a | Versión MEC (rango puntuación 0-35) | Pérez-Martínez 200533 |
| AE | 88 (27/27/34) | 26/27 | 0,79 | 0,84 | 0,88a | Solo se incluyó ACL amnésico | Rami 200936 | |
| AE | 153 (66/21/66) | 23/24 | 0,86 | 0,84 | 0,90 | Cacho 201027 | ||
| AE | 194 (63/54/79) | 25/26 | 0,90 | 0,68 | 0,90a | No se administró la sustracción seriada y se pidió coger el papel con la mano contraria a la preferencia manual | Ferrero-Arias 200126 | |
| AP | 360 (146/137/77) | 22/23 | 0,77 | 0,77 | 0,84 | No se administró el deletreo al revés | Carnero-Pardo 201337 | |
| MoCA | AE | 103 (21/51/31) | 19/20 | 0,76 | 0,77 | 0,78 | Lozano-Gallego 200938 | |
| RUDAS | AE | 115 (50/26/39) | 21/22 | 0,83 | 0,86 | 0,90 | Ramos-Rios 200939 |
ACE-III: Addenbrooke's Cognitive Examination (3.ª versión); ACL: alteración cognitiva leve; AE: atención especializada; AP: atención primaria; aROC: área bajo la curva ROC; CN: cognitivamente normales; DC: deterioro cognitivo; DEM: demencia; E: especificidad; EA: enfermedad de Alzheimer; MEC: Mini-Examen Cognoscitivo; MIS: Memory Impairment Screen; MMSE: Mini-Mental State Examination; MoCA: Montreal Cognitive Assessment; NE: no especificado; PdC: punto de corte; RUDAS: Rowland Universal Demencia Assessment; S: sensibilidad; T@M: Test de Alteración de Memoria; TCB: test cognitivos breves; TIG: Test de Información General; TF: Test de las Fotos.
El Test de Evocación de Animales en un minuto es la prueba más breve estudiada para la detección de la demencia41. Su limitación a la evaluación de las capacidades lingüísticas y ejecutivas desaconseja este tipo de test como primera opción para la detección del DC. Los test de fluidez verbal (TFV) ofrecen datos cualitativos y cuantitativos de gran utilidad, en el contexto de una evaluación más amplia. La prueba de evocación de animales y la prueba de evocación de palabras que empiezan por la letra «p» en un minuto son las más aconsejables, por ser complementarias y por haber sido muy bien estudiadas en nuestro país42,43. Existen algunas variaciones, como el Set-Test de Isaacs44 y el Test de Información General o Test 5×526, que alargan y complican la aplicación sin mejorar la utilidad diagnóstica, por lo que no suponen una alternativa recomendable.
El Test del Reloj (TR) evalúa el área o capacidad visuoespacial (AV) y las funciones ejecutivas (FE)45. A pesar de la ventaja de su sencillez y brevedad, el TR no resulta suficiente para la detección del DC27, ni siquiera en el ámbito de la AP28 (tabla 2). Sin embargo, el TR es muy sensible al daño cortical parietal derecho y resulta de gran ayuda como complemento de otros test breves, especialmente cuando no se detecta un rendimiento anómalo en pruebas de memoria (de hecho, el TR ha sido incluido con éxito en varios test más amplios, como más adelante se verá). Como contrapartida, su dependencia de un mínimo de habilidades gráficas hace del TR una herramienta poco apropiada en pacientes analfabetos o con poca destreza grafomotora. Hay diferentes propuestas de puntuación; las más sencillas son más adecuadas para la detección del DC, mientras que las más elaboradas pueden ser más útiles para el control evolutivo o el análisis del caso46,47.
El Mini-Cog incluye las áreas que más frecuentemente se ven alteradas al inicio del DC. Une para ello una prueba de aprendizaje de 3 palabras similar a la del test Mini-Mental de Folstein (memoria episódica [ME]) y el TR (AV, FE). Su puntuación tiene un rango estrecho (0-5: un punto por cada palabra recordada y 2 puntos adicionales de valoración cualitativa si el reloj tiene todos los números, en el orden correcto y las agujas señalan la hora requerida) con poca sensibilidad para la detección del DC28 (tabla 2) y para el control evolutivo. Con todo, el Mini-Cog puede servir para sustentar el diagnóstico de demencia, especialmente en los casos relativamente claros desde la anamnesis.
El Test Episódico ha sido recientemente creado y validado en una muestra de pacientes con ACL de tipo amnésico y enfermedad de Alzheimer (EA)25 (tabla 2). Es un test «amigable», que no precisa de lápiz ni papel (presumiblemente poco influido por la educación) y que evalúa exclusivamente la ME a través de preguntas relacionadas con el pasado reciente. Su principal inconveniente es la necesaria presencia de un informador allegado que corrobore la veracidad de las respuestas.
El Fototest o Test de las Fotos consta de una tarea de denominación visuoverbal de 6 fotos de objetos (lenguaje), una tarea de fluidez verbal (lenguaje, FE) y una tarea de ME mediante el recuerdo libre y facilitado de las imágenes previamente denominadas. Junto con el test Mini-Mental de Folstein (MMSE), el Fototest es el TCB más estudiado para la detección del DC en nuestro país. Es un instrumento bien aceptado que ha demostrado una utilidad satisfactoria para el DC, tanto en la AP como en la AE, con un punto de corte estable (28/29)29,31,32,35. El Fototest ha demostrado, además, una relación coste-efectividad en la AP superior a la del MMSE30, con la ventaja adicional de contar con versiones paralelas equivalentes que pueden ser muy útiles para disminuir el efecto de la práctica en el caso de aplicaciones repetidas (AP, seguimiento)48 (tabla 2).
El Memory Impairment Screen (MIS) evalúa el aprendizaje verbal (ME) a través de la lectura y posterior recuerdo libre y facilitado de 4 palabras. Existen varios estudios de validación realizados en nuestro país que han mostrado resultados aceptables para el DC30,33 (tabla 2) y buenos para la demencia30,33,49, especialmente si es debida a EA50. El MIS presenta, además, una buena correlación con las medidas de volumetría hipocámpica y entorrinal51, datos que apoyan su validez para la detección temprana de la EA.
El Test de Alteración de la Memoria (T@M) incluye ítems relacionados con la ME (recuerdo libre y facilitado, orientación temporal) y, en menor proporción, ítems de información general (memoria remota/semántica [MS]). Estas características, junto a su amplio rango de puntuación (0-50), le convierten en una herramienta especialmente adecuada para la detección y el seguimiento de las primeras fases clínicas de la EA típica34,36 (tabla 2). El T@M distingue las quejas subjetivas de memoria y la ACL y ha sido, además, validado mediante marcadores bioquímicos y de neuroimagen52. Aunque también se ha demostrado su utilidad en la AP35, parece más adecuado y realista reservar este test para la AE.
El Eurotest es una original propuesta de evaluación cognitiva breve que utiliza las monedas en curso y que se desarrolla en 3 partes: conocimiento de las monedas en uso (MS), operaciones con unas monedas (cálculo) y recuerdo de las monedas utilizadas (ME). El Eurotest, que permite en cierta medida hacer una evaluación funcional de la capacidad de manejar el dinero, ha obtenido resultados aceptables para la detección del DC35 (tabla 2) y buenos para la demencia53,54. Se trata de un instrumento muy ecológico y aplicable a analfabetos, cuyo uso se ha extendido a varios sistemas monetarios, incluido el chino.
El MMSE, con sus innumerables adaptaciones y traducciones55–59, es el TCB más utilizado en el mundo, tanto en el ámbito de la AP como en el de la AE. La virtud de la universalidad, que permite la comparación y el seguimiento de sujetos de distintas procedencias, tiene como contrapartida una estandarización y fiabilidad cuestionables, derivadas principalmente de la existencia de múltiples versiones y de la ausencia de instrucciones precisas de puntuación60. Otras limitaciones del MMSE son la escasa representación de las FE, que le resta sensibilidad para la detección de la ACL y de la demencia frontotemporal y las restricciones al uso libre derivadas de su reciente copyright61. Tradicionalmente estudiado para la detección de la demencia55,59,62,63, la mayor parte de la información relativa a la utilidad del MMSE en la detección del DC procede de estudios de validación de otros instrumentos que incluyeron el MMSE como test de comparación. En estos estudios, la utilidad del MMSE fue, en general, inferior a la de los test con los que se comparaba27,30,33,36 (tabla 2). En el único estudio específico de evaluación del MMSE en el DC, el mejor rendimiento se obtuvo con un punto de corte (PdC) inferior al habitualmente empleado (22/23) y, en contra de la práctica habitual, el ajuste por edad y educación no mejoró la capacidad discriminativa28. Con todo, el MMSE permite obtener perfiles o rasgos cualitativos que ofrecen confianza al clínico tanto en el diagnóstico como en el seguimiento, especialmente en los pacientes con EA típica; sirvan como ejemplo la alteración selectiva de los ítems de la ME (recuerdo diferido, día del mes) en la EA prodrómica, la transformación de los pentágonos en cuadriláteros en la EA con demencia ligera y la pérdida de la orientación con respecto al mes y de la denominación del bolígrafo en la EA moderada.
El Montreal Cognitive Assessment (MoCA) aporta un diseño ecléctico y equilibrado para la detección de la ACL de cualquier etiología. Incluye ítems de atención, recuerdo libre (lista de 5 palabras), FE (Test del Trazo, semejanzas), cálculo, AV (copia de un cubo, TR), orientación y lenguaje. Los primeros estudios de validación, realizados en Canadá, fueron prometedores64, pero en un estudio realizado en nuestro país la eficacia para la detección de la ACL no fue tan alta (el 69% de los sujetos fueron clasificados correctamente, frente al 90% en el estudio original)38 (tabla 2). El MoCA está muy influido por el nivel cultural, como ya se constató en las validaciones realizadas en otros países.
El Rowland Universal Dementia Assessment (RUDAS) fue desarrollado en Australia con vistas a una aplicación multicultural y en analfabetos. Evalúa la identificación de partes del cuerpo, la ME, la praxis visuoconstructiva (dibujo de un cubo) y el razonamiento. En España se ha realizado un estudio preliminar, con buenos resultados, para la detección del DC39 (tabla 2).
Existen 2 TCB que han sido validados en el ámbito poblacional, por lo que no cumplen los criterios de inclusión de esta revisión, pero que se mencionarán aquí por su posible utilidad en la AP.
El Abbreviated Mental Test (AMT) de Hodkinson evalúa la orientación, la atención y la memoria. Consta de 10ítems, su aplicación es sencilla (con la excepción del ítem de reconocimiento de 2 personas) y está poco influido por el nivel educativo. Un PdC7/8 mostró un buen rendimiento para la detección de la ACL65 y de la demencia66. El AMT se usa muy poco en España, tal vez por su escasa difusión y disponibilidad.
La Prueba Cognitiva de Leganés (PCL) fue diseñada para evaluar las capacidades cognitivas de ancianos con bajo nivel educativo67; mostró valores excelentes para la detección de la demencia (PdC22/23) y buenos para el DC (PdC26/27)68. Dado que contiene en su mayoría ítems relacionados con la ME, la PCL puede ser útil para la detección y el seguimiento de la EA típica cuando la edad avanzada, el bajo nivel educativo u otras circunstancias desaconsejen la administración de test más complejos.
Existen otros TCB de uso habitual en nuestro país, pero que no han sido evaluados específicamente para el DC, aunque sí para la demencia, y que se reseñan a continuación:
El cuestionario de Pfeiffer (Short Portable Mental Status Questionnaire [SPMSQ]) es similar al AMT, con algo más de peso para la MS y con la diferencia de que se puntúan los errores, en vez de los aciertos. El SPMSQ tiene un rendimiento bueno para la detección de la demencia en la AP69 y en la AE (PdC2/3)70 y excelente en el ámbito geriátrico (PdC4/5)71.
El Test de los Siete Minutos (T7M), que requiere un tiempo de administración algo mayor que el que su nombre indica, presenta algunas características (prueba de aprendizaje de 16 figuras, laborioso sistema de puntuación) que dificultan su uso en una primera aproximación al DC en el ámbito médico asistencial. No obstante, puede ser una herramienta útil, a medio camino entre el EEM y la exploración neuropsicológica formal (fig. 1), para evaluar áreas cognitivas habitualmente afectadas en la EA. El T7M consigue un rendimiento excelente para la detección de la demencia (PdC20/21)70,72, pero su utilidad en la ACL ha sido cuestionada en un estudio argentino73.
El Addenbrooke's Cognitive Examination (ACE) se desarrolló a partir del MMSE, al que se añadieron elementos frontales/ejecutivos y visuoespaciales. Ha alcanzado ya una tercera versión (ACE-III), que ha demostrado un rendimiento bueno para la demencia74, llegando a ser excelente en los sujetos con más de 9años de escolaridad (PdC73/74). El ACE puede ser, además, útil para distinguir los principales tipos etiológicos de demencia75. Recientemente se ha validado una versión abreviada (M-ACE) que podría tener más capacidad discriminativa que la versión original76.
Límites de los test cognitivos breves: nuevas vías de actuación e investigaciónSin cuestionar su utilidad y oportunidad, el rendimiento diagnóstico de los TCB dista de ser plenamente satisfactorio, en especial en lo que respecta a la detección del DC. A mayor representación y extensión de las áreas cognitivas, el test pierde eficiencia y aplicabilidad y la cuestión deviene circular (la herramienta de detección y el «patrón de oro» se identifican). Una posible salida es la utilización de tareas exigentes, que pongan en juego habilidades cognitivas diversas, incluida la velocidad de procesamiento (tareas de atención dividida, fluidez de figuras, etc.)77, pero es probable que, a mayor complejidad y dificultad de la tarea, la influencia de factores no patológicos (envejecimiento, estrés, etc.) sea también mayor, restando especificidad. La utilización de cuestionarios de quejas cognitivas o metacognición podría ser otra opción, pero no ha resultado útil debido a la influencia de la topografía lesional, de la comorbilidad psiquiátrica y de los factores psicológicos y sociales78.
Los cuestionarios del informador son instrumentos en general sencillos y cómodos de administrar que ofrecen una perspectiva (longitudinal y del informador) complementaria a la de los test cognitivos79. El Informant Questionnaire on Cognitive Decline in the Elderly (IQCODE) o Test del Informador es el cuestionario más estudiado en nuestro país. Tanto su versión completa (26ítems) como su versión abreviada (17ítems) han mostrado un buen rendimiento en la detección de la demencia80–82, alcanzándose un aROC de 0,91 en uno de los estudios82. Además, este cuestionario no se ve influido por la edad, el sexo, la salud mental o el nivel intelectual previo62. En otro estudio, el rendimiento del IQCODE para la detección del DC fue menor (aROC0,75), pero aportó un valor añadido al test MMSE (aROC0,86, frente a 0,82 con el MMSE solo)83. El Functional Activities Questionnaire (FAQ) posee 11ítems y ha dado también buenos resultados en la detección de la demencia (aROC0,91), aunque inferiores en el DC (aROC0,77). Al igual que el IQCODE, el FAQ mejoró el rendimiento del MMSE en la detección de la demencia (aROC0,95, frente a 0,91 con el MMSE solo)83. El Ascertain Dementia-8 (AD 8) es una propuesta ultrabreve, ideada para la AP. Consta de 8ítems que se responden al modo «sí o no» y tiene un buen rendimiento para el diagnóstico de DC (aROC0,90). Además, su uso asociado a un TCB (Fototest) aporta valor añadido (aROC Fototest 0,93, aROC Fototest más AD8, 0,96)32.
Otros marcadores complementarios para la detección del DC podrían extraerse de la exploración física (alteraciones motoras, signos frontales, etc.) o de muestras biológicas accesibles (saliva, sangre, etc.). Pero estas líneas de investigación, especialmente interesantes para el diagnóstico etiológico, no han dado todavía frutos de utilidad práctica84,85.
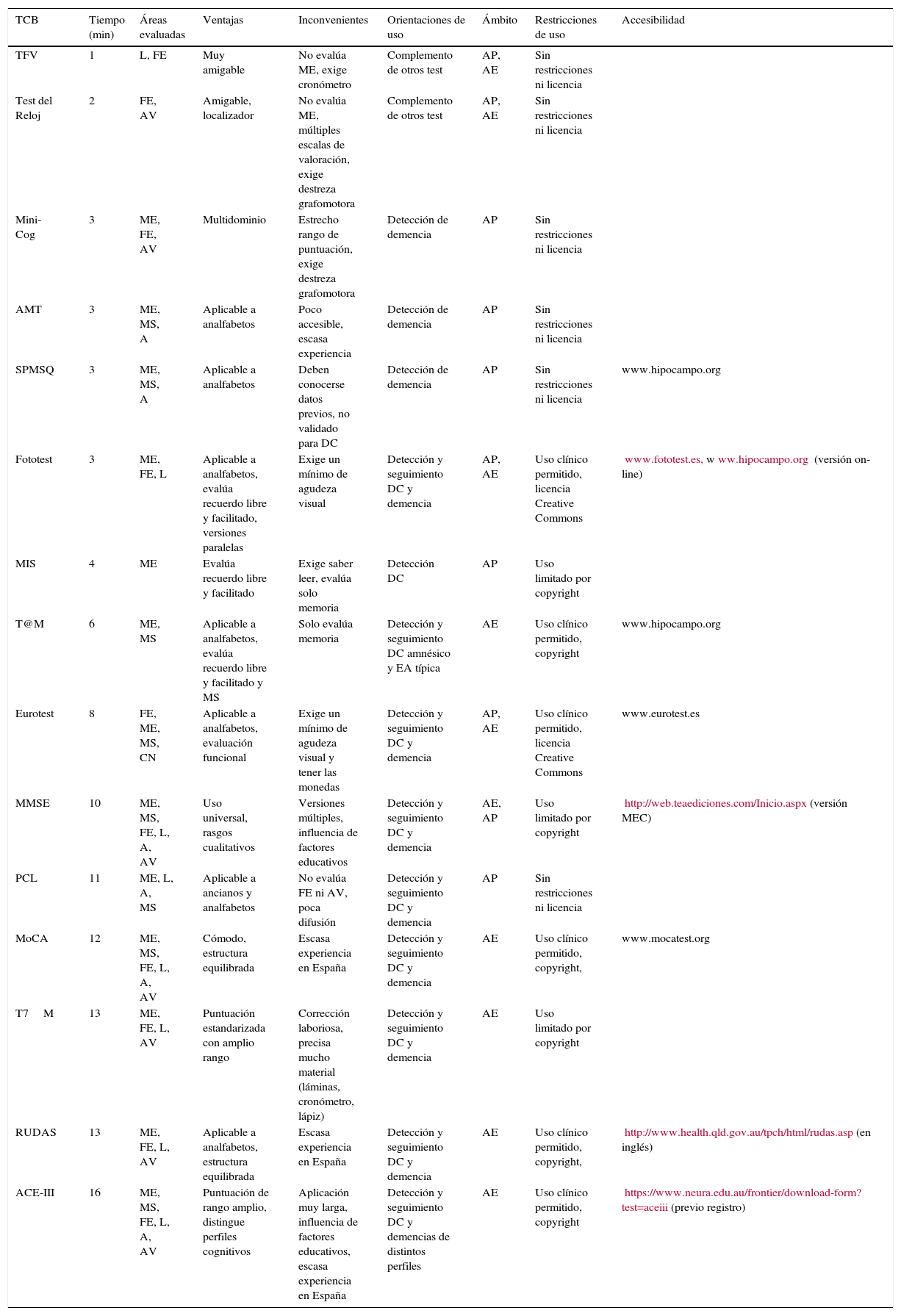
ConclusionesUna primera aproximación al paciente con queja o sospecha de DC debería incluir el examen de, al menos, las áreas más frecuentemente alteradas (ME y FE). En el primer nivel asistencial se recomienda la utilización de algún TCB que dé soporte objetivo a la sospecha clínica y propicie una derivación eficiente al segundo nivel, para la realización del diagnóstico preciso. El Fototest y el MIS han sido suficientemente estudiados y son las opciones más recomendables para la AP, pudiendo añadirse otros test (TR, TFV) sobre todo en caso de resultado negativo y queja o sospecha persistente (aproximación escalonada). El Eurotest y el MMSE pueden ser también alternativas válidas en la AP, en función de las circunstancias particulares (el Eurotest en analfabetos y el MMSE si hay mayor disponibilidad de tiempo) (tabla 3). Tanto en la AP como en la AE, debe quedar claro el rendimiento del paciente en su entorno social cotidiano (manejo del dinero, medicación, etc.); si este está afecto, el paciente debe ser sospechoso de demencia y no de ACL.
Test cognitivos breves: características generales y orientaciones de uso
| TCB | Tiempo (min) | Áreas evaluadas | Ventajas | Inconvenientes | Orientaciones de uso | Ámbito | Restricciones de uso | Accesibilidad |
|---|---|---|---|---|---|---|---|---|
| TFV | 1 | L, FE | Muy amigable | No evalúa ME, exige cronómetro | Complemento de otros test | AP, AE | Sin restricciones ni licencia | |
| Test del Reloj | 2 | FE, AV | Amigable, localizador | No evalúa ME, múltiples escalas de valoración, exige destreza grafomotora | Complemento de otros test | AP, AE | Sin restricciones ni licencia | |
| Mini-Cog | 3 | ME, FE, AV | Multidominio | Estrecho rango de puntuación, exige destreza grafomotora | Detección de demencia | AP | Sin restricciones ni licencia | |
| AMT | 3 | ME, MS, A | Aplicable a analfabetos | Poco accesible, escasa experiencia | Detección de demencia | AP | Sin restricciones ni licencia | |
| SPMSQ | 3 | ME, MS, A | Aplicable a analfabetos | Deben conocerse datos previos, no validado para DC | Detección de demencia | AP | Sin restricciones ni licencia | www.hipocampo.org |
| Fototest | 3 | ME, FE, L | Aplicable a analfabetos, evalúa recuerdo libre y facilitado, versiones paralelas | Exige un mínimo de agudeza visual | Detección y seguimiento DC y demencia | AP, AE | Uso clínico permitido, licencia Creative Commons | www.fototest.es,www.hipocampo.org (versión on-line) |
| MIS | 4 | ME | Evalúa recuerdo libre y facilitado | Exige saber leer, evalúa solo memoria | Detección DC | AP | Uso limitado por copyright | |
| T@M | 6 | ME, MS | Aplicable a analfabetos, evalúa recuerdo libre y facilitado y MS | Solo evalúa memoria | Detección y seguimiento DC amnésico y EA típica | AE | Uso clínico permitido, copyright | www.hipocampo.org |
| Eurotest | 8 | FE, ME, MS, CN | Aplicable a analfabetos, evaluación funcional | Exige un mínimo de agudeza visual y tener las monedas | Detección y seguimiento DC y demencia | AP, AE | Uso clínico permitido, licencia Creative Commons | www.eurotest.es |
| MMSE | 10 | ME, MS, FE, L, A, AV | Uso universal, rasgos cualitativos | Versiones múltiples, influencia de factores educativos | Detección y seguimiento DC y demencia | AE, AP | Uso limitado por copyright | http://web.teaediciones.com/Inicio.aspx(versión MEC) |
| PCL | 11 | ME, L, A, MS | Aplicable a ancianos y analfabetos | No evalúa FE ni AV, poca difusión | Detección y seguimiento DC y demencia | AP | Sin restricciones ni licencia | |
| MoCA | 12 | ME, MS, FE, L, A, AV | Cómodo, estructura equilibrada | Escasa experiencia en España | Detección y seguimiento DC y demencia | AE | Uso clínico permitido, copyright, | www.mocatest.org |
| T7M | 13 | ME, FE, L, AV | Puntuación estandarizada con amplio rango | Corrección laboriosa, precisa mucho material (láminas, cronómetro, lápiz) | Detección y seguimiento DC y demencia | AE | Uso limitado por copyright | |
| RUDAS | 13 | ME, FE, L, AV | Aplicable a analfabetos, estructura equilibrada | Escasa experiencia en España | Detección y seguimiento DC y demencia | AE | Uso clínico permitido, copyright, | http://www.health.qld.gov.au/tpch/html/rudas.asp(en inglés) |
| ACE-III | 16 | ME, MS, FE, L, A, AV | Puntuación de rango amplio, distingue perfiles cognitivos | Aplicación muy larga, influencia de factores educativos, escasa experiencia en España | Detección y seguimiento DC y demencias de distintos perfiles | AE | Uso clínico permitido, copyright | https://www.neura.edu.au/frontier/download-form?test=aceiii(previo registro) |
A: atención; ACE-III: Addenbrooke's Cognitive Examination (3.ª versión); AE: atención especializada; AMT: Abbreviated Mental Test; AP: atención primaria; AV: área visuoespacial; CN: capacidades numéricas; DC: deterioro cognitivo; DLFT: degeneración lobular frontotemporal; EA: enfermedad de Alzheimer; FE: funciones frontales/ejecutivas; L: lenguaje; ME: memoria episódica; MEC: Mini-Examen Cognoscitivo; min: minutos; MIS: Memory Impairment Screen; MMSE: Mini-Mental State Examination; MoCA: Montreal Cognitive Assessment; MS: memoria remota/semántica; PCL: Prueba Cognitiva de Leganés; RUDAS: Rowland Universal Dementia Assessment; SPMSQ: Short Portable Mental Status Questionnaire; T@M: Test de Alteración de Memoria; TFV: test de fluidez verbal (animales, palabras por p); T7M: Test de los Siete Minutos.
Una evaluación sistemática de las principales áreas cognitivas (atención, lenguaje, ME, FE, AV) es obligada en la AE, por lo que lo ideal sería llevar a cabo una exploración neuropsicológica formal (fig. 1); por este motivo, los instrumentos teóricamente más aconsejables en este ámbito son los que permiten la evaluación de un mayor número de dominios cognitivos, como el MoCA, el MMSE, el RUDAS o el ACE-III, cuya selección estaría en función de las características del paciente (MoCA si el paciente parece próximo a la normalidad, MMSE si se sospecha un DC avanzado, RUDAS si es analfabeto, ACE-III si se plantea la duda entre EA y degeneración lobular frontotemporal), de la experiencia del clínico y del tiempo disponible (el ACE-III requiere más de 15min). Sin embargo, queda por demostrar —sea por la ausencia de estudios específicos (ACE-III), porque los resultados disponibles son discretos o negativos (MMSE, MoCA)30,38 o por la presencia de otros inconvenientes, como la no gratuidad (MMSE)60,61— si el uso de estos instrumentos es más eficiente que el uso de otros test cognitivos más breves y simples, ya sea de forma aislada (MIS33, T@M36 y Fototest30), combinada (FVS, TR y MMSE)27,28 o escalonada (Fototest y Eurotest)86, especialmente en situaciones de poca disponibilidad de tiempo.
En un país desarrollado, con recursos sanitarios y sociales suficientes, deben evitarse los falsos negativos, ya que las posibles actuaciones son muchas y eficaces (promoción de hábitos saludables, control de factores de riesgo vascular, asesoramiento, investigación, etc.), no son arriesgadas ni costosas y todas ellas pueden ser abordadas o encauzadas desde la AP. Es lícito utilizar puntos de corte distintos de los recomendados, con el fin de elevar la sensibilidad y propiciar una detección temprana, especialmente en los casos de queja o sospecha persistente o en sujetos con un elevado nivel intelectual previo. En cualquier caso, los puntos de corte serán siempre orientativos o sustentadores, pero nunca determinantes del diagnóstico de DC, al que se llegará aplicando el juicio clínico, tras haber considerado toda la información disponible (fig. 1).
Los cuestionarios del informador presentan un rendimiento para el diagnóstico de demencia similar o incluso superior al de los TCB, probablemente debido a la menor especificidad de los test cognitivos, fruto de la escasa escolarización de buena parte de los ancianos de nuestro país. Aun así, debe realizarse siempre que sea posible un EEM, dado que la diana ha de ser el DC (ACL o demencia) y que la percepción del informador puede estar distorsionada por aspectos primariamente no cognitivos (salud física, déficit sensorial, etc.), puede no ser válida o incluso puede ser interesada. Los cuestionarios del informador ofrecen valor añadido en la detección del DC mediante el uso asociado con un TCB, uso que ha de seguir investigándose. El trabajo riguroso, constante e imaginativo de los investigadores de nuestro país ha cristalizado en una oferta variada y complementaria de TCB, muchos de ellos de diseño propio y todos ellos útiles para mejorar la confianza y la precisión del clínico en su primera aproximación al paciente con queja o sospecha de DC. Con el fin de facilitar y rentabilizar su uso, los TCB recomendados, junto con sus instrucciones y puntos de corte, deberían estar accesibles, a ser posible, en la historia clínica informatizada de la AP y de la AE. El potencial de los TCB merece más investigación, especialmente en lo que respecta al diagnóstico etiológico (p.e., el Eurotest podría ayudar en la detección del DC de causa diferente de la EA típica)87 y a su utilidad en el control evolutivo. En el ámbito asistencial, los test y cuestionarios deben reforzar —pero nunca suplantar— el juicio clínico, la comunicación profunda con el paciente y sus allegados, la coordinación entre los distintos niveles asistenciales y el diálogo interprofesional.
Conflictos de interesesC. Carnero-Pardo es el creador del Fototest y del Eurotest. Los demás autores declaran no tener ningún conflicto de intereses.