Introducción
La vejiga hiperactiva tiene un efecto negativo importante sobre la calidad de vida, reflejándose en aislamiento social, depresión y pérdida de la autoestima,1 60% de las mujeres adultas con urgencia evitan alejarse de sus hogares.2,3 La urgencia urinaria se define como la imperiosa necesidad de micción, no diferible, siendo un síntoma característico de diversas entidades clínicas del tracto urinario inferior, tales como vejiga hiperactiva e incontinencia urinaria de urgencia.4,5 Hasta ahora los anti-muscarínicos son la primera línea de tratamiento para la urgencia-frecuencia no siempre son efectivos y se han asociado con efectos adversos que limitan su uso.6 Su eficacia sin embargo es limitada por su efecto anti-colinérgico sobre receptores muscarínicos fuera de la vejiga.7
Debido a que las terapias intravesicales reducen la incidencia de los efectos sistémicos secundarios, la ruta intravesical ha permitido el uso de agentes muy tóxicos.8
Hasta el momento, a pesar de que la atropina es un fármaco barato y de fácil disponibilidad, no ha sido establecida su instilación intravesical como tratamiento de la vejiga hiperactiva.9,10 El dimetilsulfóxido fue aprobado por la FDA en 1978 como solución al 50% aplicado en la cistitis intersticial,11 al disminuir el dolor y la restauración de la función normal de la vejiga por períodos que duran por lo menos tres meses con reducción significativa en frecuencia y nicturia, sin embargo ha sido utilizado para vejiga hiperactiva con buenos resultados y aun no ha sido aprobado para esta patología.12,13 Aunque se ha probado su seguridad y eficacia en la cistitis intersticial, su uso puede causar irritación o dolor vesical en 48% de pacientes después de la primera instilación causando desapego al tratamiento.14
El objetivo del estudio es comparar los resultados clínicos posterior a la aplicación intravesical de sulfato de atropina vs. dimetilsulfóxido, en dosis de una instilación semanal por diez ocasiones en el tratamiento de la vejiga hiperactiva, se valoró la mejoría de las variables clínicas:
Nicturia.
Capacidad vesical.
Frecuencia urinaria.
Urgencia urinaria.
Calidad de vida.
Métodos
Diseño del estudio: Longitudinal, prospectivo, experimental, comparativo, con asignación al azar y piloto para las variables frecuencia urinaria y urgencia urinaria.
Tamaño de la muestra: se calculó con base a los resultados reportados en la bibliografía para cada uno de los factores en estudio, buscando lograr un cambio de 40% en la capacidad vesical y considerando un nivel de error alfa de 5% y error beta de 20%, se encontró que con siete pacientes por grupo y un total de 14 pacientes se lograría demostrar una diferencia.15
Se llevó a cabo la asignación al azar de los pacientes para asignación a los grupos 1 y 2, mediante un programa desarrollado por los autores cegado para el paciente. Uno de los autores administró la solución y los datos fueron recabados al menos por otro de los autores y un ayudante. Se llevaron a cabo las comparaciones de los valores promedio mediante pruebas de distribución T para datos paramétricos; en el caso de datos no paramétricos o comparación de porcentajes se utilizó pruebas de distribución de Ji cuadrada.16,17 Se utilizó el paquete estadístico STATA, C-10 con licencia: Licencia: INTERMED-08-191-0531-ECE-247. La significancia alfa se tomó en 0.05 y la potencia beta en 0.80; Dado que todas las hipótesis son de mejoría de valores con la administración de atropina, se tomaron las pruebas estadísticas en una sola dirección.16,17
Los 14 pacientes femeninos incluidas tenían el diagnóstico de urgencia urinaria confirmado mediante estudio de urodinamia. El centro de reclutamiento fue la consulta de Ginecología y Obstetricia del Hospital Universitario Dr. José Eleuterio González, UANL, de enero 2006 a julio 2008. Posterior a la firma del consentimiento informado, se procedió al tratamiento. En el grupo 1, previa asepsia, antisepsia y vaciamiento vesical, por vía intravesical se instilaron 6 mg de sulfato de atropina diluidos en 20 mL de solución fisiológica, además se evitó el vaciamiento vesical por 2 horas como mínimo posterior a la administración del medicamento, se interrogó en relación a efectos colaterales. En el segundo grupo se aplicó DMSO al 50% (25 mL al 100% vía intravesical diluidos en 25 mL de solución fisiológica). Se evitó el vaciamiento vesical por 25 minutos, y se interrogó sobre dolor vesical. Al egreso se administró en forma profiláctica el antibiótico fosfomicina 1 g vía oral dosis única. A todas las pacientes se les citó en forma semanal, para la aplicación del tratamiento hasta completar 10 dosis. Se otorgó un diario miccional semanal, que permitió el llenado individual personal en el hogar, con el fin de valorar urgencia urinaria, frecuencia urinaria, nicturia, previamente y al término de las 10 instilaciones intravesicales. Con la finalidad de valorar la efectividad del tratamiento, previo y al término del tratamiento también se realizó una cistometría. Se aplicaron los cuestionarios OAB-q, validados por la ICS en 2004,16 previo y a los 30 días de la última instilación, para evaluar si se mantuvieron los cambios observados.
Se realizó el análisis estadístico de las siguientes variables: urgencia urinaria, frecuencia urinaria (ocho micciones o más), nicturia, capacidad vesical, calidad de vida valorada por el instrumento OAB-q SF.18 Esta última es una versión corta que consiste en una escala de síntomas de seis puntos y una escala de calidad de vida de 13 puntos. Esta encuesta ha sido incluida en la Consulta Internacional sobre la Incontinencia para evaluar el impacto del síndrome de vejiga hiperactiva sobre las vidas de los pacientes. El desarrollo y la validación de la OAB-q SF se desarrolló en la reunión 2004 de la Sociedad de Continencia Internacional y la Sociedad Internacional de Uroginecología. En la presente investigación se incluyó a pacientes con un puntaje entre 35 y 108, que corresponde a una mala calidad de vida.
Resultados
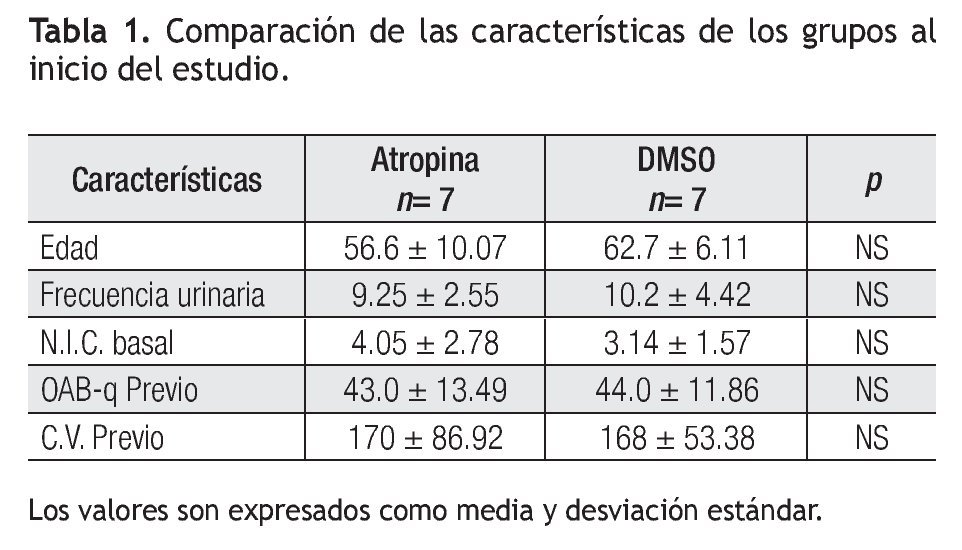
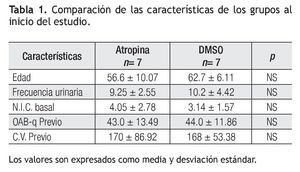
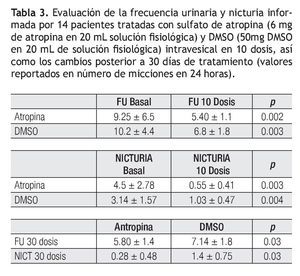
Se incluyó un total de 14 pacientes divididas en el grupo 1 tratado con sulfato de atropina (n = 7) y el grupo 2 tratado con DMSO (n = 7). Los resultados se muestran en la Tabla 1, 2, 3. Al valorar urgencia urinaria en el grupo 1, 86% (n = 6) no refirieron urgencia posterior a tratamiento, mientras que 14% (n = 1) continuaron con el síntoma. En el grupo 2, el 86% (n = 6) no refirieron urgencia posterior a tratamiento, y 14% (n = 1) continuaron con el síntoma. No hubo diferencia estadística significativa entre los dos grupos.
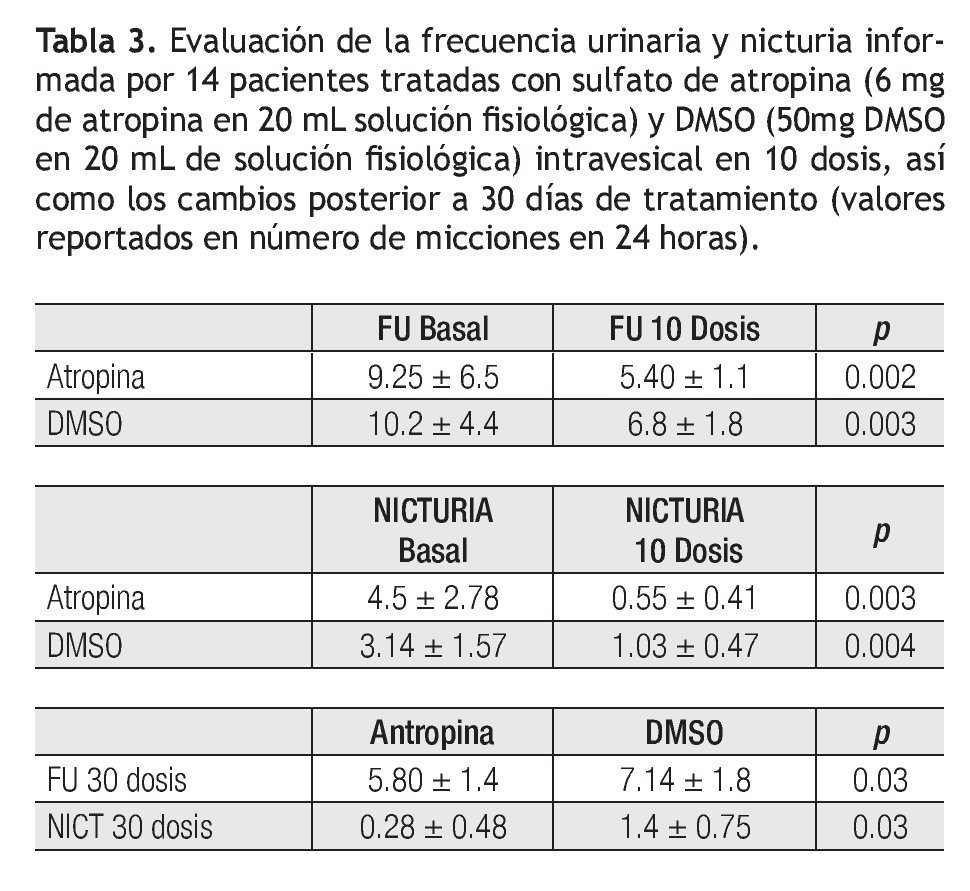
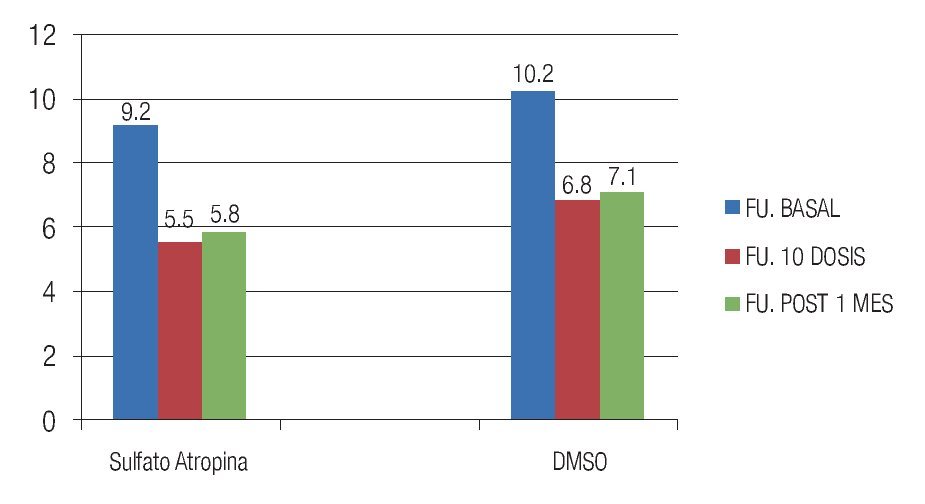
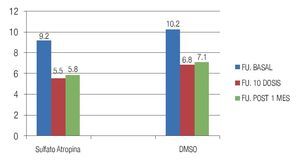
En el grupo 1 la FU basal media fue 9.25 ± 6.5 vs. la FU posterior al tratamiento la media fue de 5.4 ± 1.1 (p = 0.002). En el grupo 2 la FU basal media fue 10.2 ± 4.42 y la posterior fue de 6.8 ± 1.8, siendo esta diferencia significativa (p = 0.03) (Figura 1). Al comparar la FU posterior a 10 dosis intravesicales en ambos grupos se detectó diferencia estadísticamente significativa (p = 0.03). Al comparar la FU en ambos grupos después de 30 días de terminado el tratamiento, en el grupo 1 la FU media fue 5.8 ± 1.4, en el grupo 2 la FU media fue 7.14 ± 1.8 (p = 0.03), concluyendo que se mantienen los cambios observados durante 30 días en ambos grupos (Figura 1).
Figura 1. Comparación de la frecuencia urinaria después de 10 dosis intravesicales y cambios observados durante 30 días después de terminado el tratamiento.
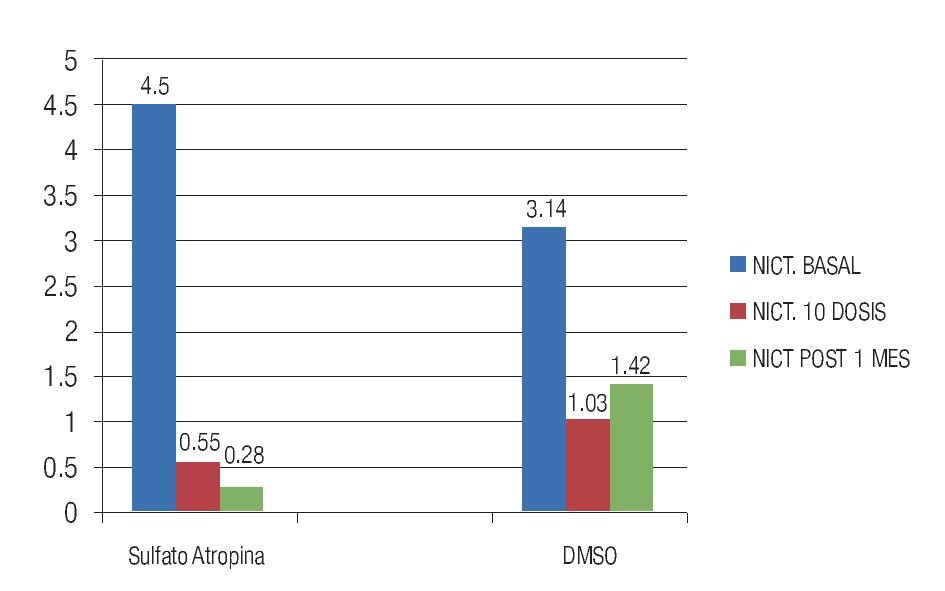
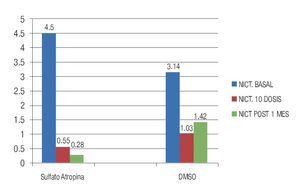
Al analizar el síntoma de nicturia en el grupo 1, la media basal fue 4.5 ± 2.78 y posterior al tratamiento de 0.55 ± 0.41 (p = 0.003). En el grupo 2 la nicturia basal media fue 3.14 ± 1.57 y posterior al tratamiento fue de 1.03 ± 0.47 (p = 0.004). Al comparar la nicturia posterior a 10 dosis intravesicales en ambos grupos, ésta fue estadísticamente significativa, (p = 0.044) (Figura 2). Al comparar la nicturia en ambos grupos después de 30 días de terminado el tratamiento, en el grupo 1 la NICT media fue 0.28 ± 0.48, en el grupo 2 la NICT media de 1.4 ± 0.77, significante en forma estadística (p = 0.03), observamos que los cambios en la nicturia se mantuvieron 30 días después de 10 dosis intravesicales bajo los dos tratamientos (Figura 2).
Figura 2. Comparación de la nicturia después de 10 dosis intravesicales entre ambos grupos y cambios observados durante 30 días después de terminado el tratamiento.
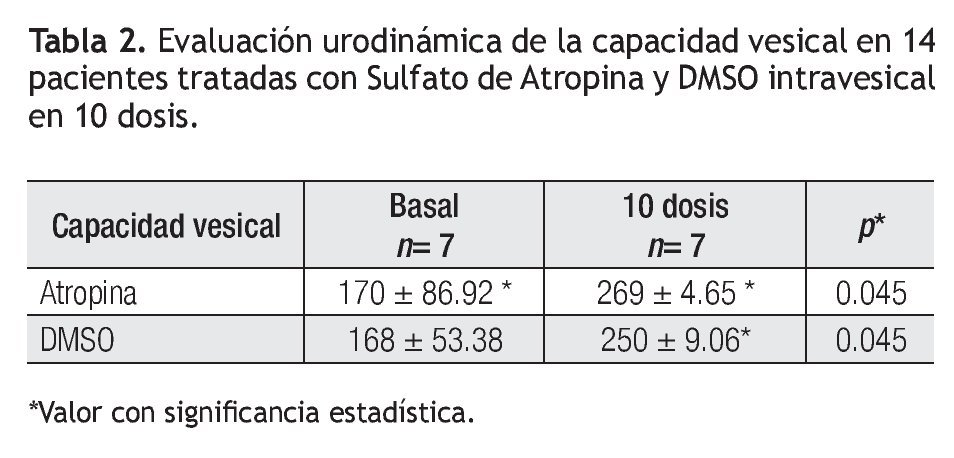
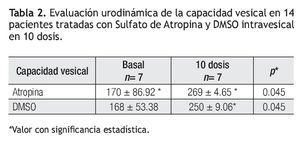
La capacidad vesical (CV) fue valorada previa al tratamiento con una media de 170 mL ± 86.92 mL en el Grupo 1 vs. 168.4 mL ± 53.38 mL en el Grupo 2. Después de siete días, de las 10 dosis se revaloró la capacidad vesical con una media de 269 mL ± 4.65 mL para el grupo 1 vs. 250 mL ± 9.06 mL para el grupo 2 respectivamente. Al comparar el incremento promedio observado en ambos grupos se observo una diferencia significativa: p = 0.045, (Tabla 1).
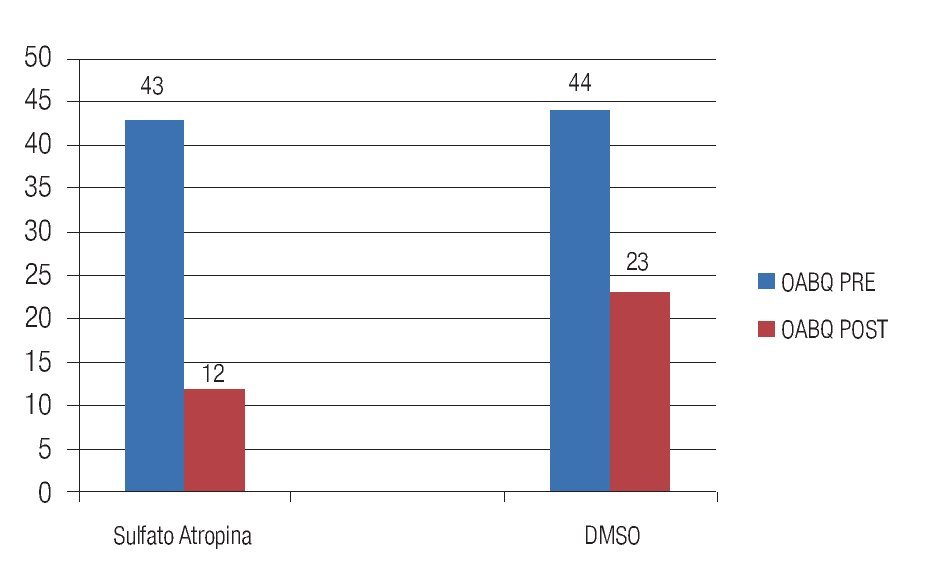
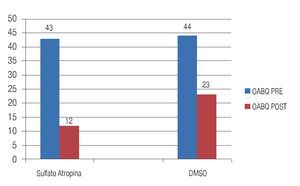
En la valoración de calidad de vida usando el cuestionario de vejiga hiperactiva OAB-q SF, el puntaje promedio oscilo entre 33 a 108 puntos en ambos grupos, en el grupo 1 la media de 43.7 puntos y en el Grupo 2 una media de 44 puntos. Después de siete días del tratamiento se repitió esta encuesta, obteniéndose un puntaje promedio de 0 a 35 puntos en ambos grupos con una media de 12 puntos en el grupo 1 y una media de 23.7 puntos en el grupo 2.
Al comparar ambas medias mediante la prueba de t de Student se obtuvo: p = 0.18; no significativo (Figura 3).
Figura 3. Valoración de la incontinencia y calidad de vida: cuestionario OAB-q.
Discusión
El presente estudio se considera piloto debido a que los estudios realizados con sulfato de atropina demostraron la seguridad y no ha sido establecida la dosis respuesta optima, hasta la fecha el DMSO está aprobado por la FDA para el tratamiento de cistitis intersticial y no de vejiga hiperactiva sin embargo por sus propiedades farmacológicas ha sido utilizado de forma experimental.
En nuestra experiencia ambos tratamientos intravesicales inducen beneficios clínicos, 86% de mejoría en la urgencia urinaria y un aumento en la capacidad vesical fue observado en ambos grupos siendo mayor y en forma significativa en el grupo con sulfato de atropina.
En el caso del presente trabajo, se formulo la teoría de que al aumentar la capacidad vesical se reduciría la urgencia urinaria, frecuencia urinaria y nicturia. Dicha teoría fue aceptada en ambos grupos lo cual fue comprobado a través de estudios urodinámicos; al comparar ambos grupos se encontró un mayor aumento en la capacidad vesical en el grupo de sulfato de atropina (99 mL) vs. el grupo con DMSO (85 mL), diferencia estadísticamente significativa, p = 0.045.
La encuesta de calidad de vida OAB realizada previo y posterior a 30 días del término de tratamiento, determinó una mejoría en la calidad de vida con una disminución en la urgencia miccional, frecuencia y nicturia sin embargo, no se obtuvo una diferencia importante para calificar al grupo 1 como mejor respuesta vs. el grupo 2.
Conclusión
A través de los resultados de este estudio podemos concluir que y demostrar por una parte la seguridad del uso en instilaciones intravesicales de atropina en las dosis utilizadas en este estudio y una casi nula presencia de efectos colaterales indeseables con su uso, además de una notable mejoría clínica en relación a las variables de nicturia, capacidad vesical, urgencia, frecuencia urinaria y calidad de vida mediante su uso (Sulfato de Atropina 6 mg de sulfato de atropina diluidos en 20 mL de solución fisiológica), estos resultados son equiparables y en algunos aspectos superiores a los resultados obtenidos empleando dimetilsulfóxido al 50% (25 mL al 100% vía intravesical diluidos en 25 mL de solución fisiológica), sin los efectos colaterales indeseables de este último reportados en la literatura. También en comparación con el costo de otros tratamientos ya sea intravesicales o administrados vía oral el costo promedio del uso de sulfato de atropina es mucho menor, permitiendo un mayor apego del paciente al tratamiento; Es necesario posteriores estudios con un mayor número de pacientes comparándolo con otros anticolinérgicos para el impacto real en el uso de atropina intravesical en el tratamiento de urgencia urinaria.
Correspondencia: Dr. Marcelo Jr. Luna Rivera,
Avenida Francisco I. Madero y Avenida Gonzalitos s/n colonia Mitras Centro, CP 64460. Monterrey, Nuevo León, México. Teléfono (+52 81) 8346 3443.
Correo electrónico:dr@marceloluna.com
Recibido: Enero 2010.
Aceptado: Julio 2010