El uso de prótesis esofágicas para el manejo endoscópico de fístulas y perforaciones se ha convertido en un procedimiento habitual. Una de sus limitaciones es su alta tasa de migración. Para resolver esta situación, se ha propuesto el uso de prótesis cubiertas de doble malla.
ObjetivosAnalizar nuestra experiencia práctica en el empleo de prótesis esofágicas cubiertas de doble malla (PECDM) (modelo Niti S™ DOUBLE™ Esophageal Metal Stent) en pacientes con fístula o perforación esofágica.
Material y métodosEstudio retrospectivo, descriptivo y unicéntrico, donde se incluyen pacientes con diagnóstico de fístula o perforación esofágica, desde noviembre 2010 hasta octubre 2018. Como objetivo primario, se evaluará su eficacia en términos de éxito técnico. Como objetivo secundario, se analizará su perfil de seguridad.
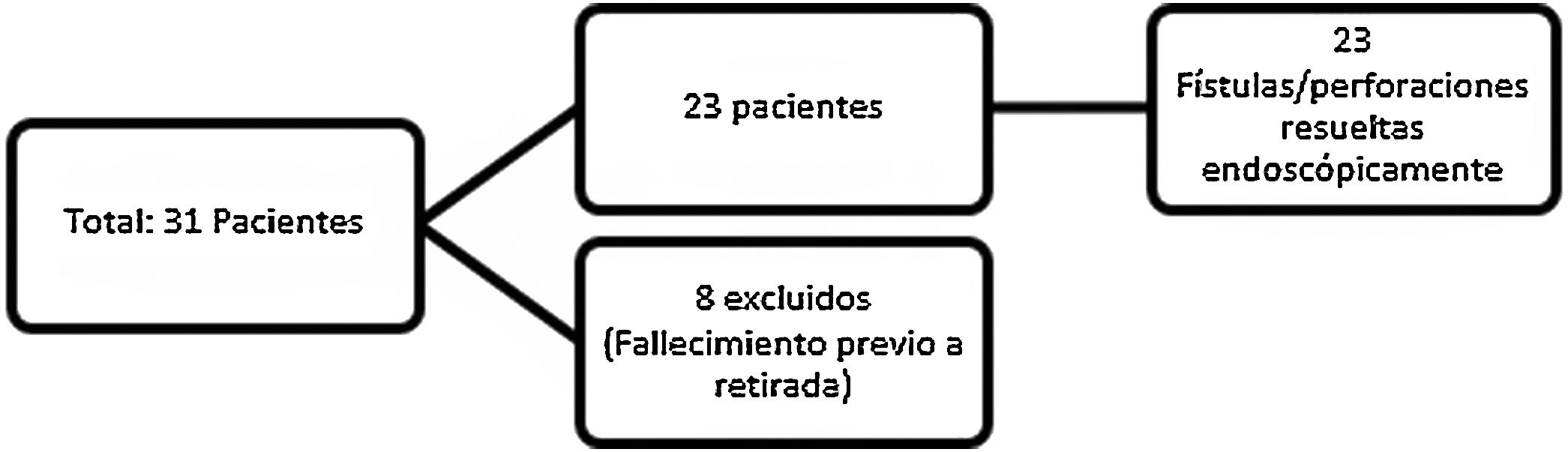
ResultadosSe incluyeron inicialmente un total de 31 pacientes, siendo 8 de ellos excluidos por fallecimiento por causas ajenas a la técnica. Se detectó un éxito técnico del 100%, con un éxito primario del 75% tras la recolocación de la prótesis. Entre sus complicaciones, la migración ocurrió en un 21,7% de los pacientes (n=5), resolviéndose vía endoscópica en el 100% de los casos.
ConclusionesSegún nuestros hallazgos, las PECDM suponen una alternativa en el tratamiento de fístulas y perforaciones esofágicas, con una alta tasa de éxito en la resolución de fístulas y baja de complicaciones, en contraste con lo expuesto en las series publicadas. En todos los casos, la migración de la prótesis se resolvió mediante recolocación endoscópica, sin requerir nueva prótesis ni cirugía.
The use of esophageal stents for the endoscopic management of esophageal leaks and perforations has become a usual procedure. One of its limitations is its high migration rate. To solve this incovenience, the double-layered covered esophageal stents have become an option.
ObjectivesTo analyse our daily practice according to the usage of double-layered covered esophageal metal stents (DLCEMS) (Niti S™ DOUBLE™ Esophageal Metal Stent Model) among patients diagnosed of esophageal leak or perforation.
MethodsRetrospective, descriptive and unicentric study, with inclusion of patients diagnosed of esophageal leak or perforation, from November 2010 until October 2018. The main aim is to evaluate the efficacy of DLCEMS, in terms of primary success and technical success. The secondary aim is to evaluate their (the DLCEMS) safety profile.
ResultsThirty-one patients were firstly included. Among those, 8 were excluded due to mortality not related to the procedure. Following stent placement, technical success was reached in 100% of the cases, and primary success, in 75% (n=17). Among the complications, stent migration was present in 21.7% of the patients (n=5), in whom the incident was solved by endoscopic means.
ConclusionsAccording to our findings, DLCEMS represent an alternative for esophageal leak and perforation management, with a high success rate in leak and perforation resolutions and low complication rate, in contrast to the published data. The whole number of migrations were corrected by endoscopic replacement, without the need of a new stent or surgery.
La gran mayoría de las fístulas y perforaciones esofágicas son resultado de intervenciones quirúrgicas de enfermedad esofagogástrica, de etiología tanto benigna como maligna. Se ha descrito una prevalencia de hasta el 4-27% en pacientes tras gastrectomía radical, y en el 5-18% de pacientes tras esofaguectomía1–3. Estas complicaciones implican altas tasas de morbilidad, con un aumento de la estancia hospitalaria, ingresos en unidades de cuidados intensivos, y una mortalidad de entre un 12 y un 50% de los pacientes4–6.
El manejo endoscópico de estas lesiones supuso hace años un gran avance en el pronóstico de estos pacientes, tanto en términos de éxito terapéutico como de supervivencia. El uso de prótesis o stents esofágicos implicó una menor dificultad técnica, con una morbimortalidad significativamente inferior que las técnicas quirúrgicas7,8.
Característicamente, se han empleado prótesis metálicas autoexpandibles cubiertas, que obtienen tasas de eficacia, definida como cierre completo de la lesión, del 60-90%3,9. Su principal inconveniente es el alto porcentaje de migración, que oscila entre el 13 y el 50% según las distintas series5,10. Esto es causa de una parte importante de los fracasos terapéuticos y de un sobrecoste importante. Posteriormente, se desarrollaron las prótesis plásticas con el objetivo de facilitar su retirada, observando igualmente altas tasas de migración11, así como las prótesis biodegradables, si bien por el momento no disponemos de estudios y resultados suficientes que avalen su empleo en la práctica diaria12. Por este motivo, se ha extendido el uso de prótesis esofágicas parcialmente cubiertas, las cuales consiguen un porcentaje de migración inferior a expensas de incrementar notablemente la dificultad técnica de retirada13. Esto es debido al crecimiento intraluminal de la mucosa en los extremos descubiertos de la prótesis que comporta a su vez un aumento en la incidencia de disfagia tras la extracción3,7.
Como alternativa, y con el objetivo de combinar los beneficios de las anteriores, se desarrollaron las prótesis esofágicas metálicas cubiertas autoexpandibles de doble malla (PECDM). Estas se componen de una malla externa de nitinol, aleación de níquel y titanio, que permite una adherencia a los tejidos circundantes, así como de una cubierta interna de poliuretano que sella la fístula y permite su retirada14.
Las PECDM surgen hace más de 10 años con vistas a implementar los resultados en el tratamiento paliativo de la disfagia por neoplasias esofagogástricas a costa de disminuir la incidencia de migración y de obstrucción por crecimiento tumoral. Esta hipótesis se ha confirmado a posteriori en varios estudios14–16. A la vista de estos resultados, hemos extrapolado el uso de las prótesis metálicas autoexpandibles a la enfermedad benigna.
Hoy en día, no disponemos de estudios que valoren el éxito técnico y terapéutico en estos pacientes, limitándose a casos aislados10. Sin embargo, los datos actualmente disponibles en enfermedad maligna demuestran una eficacia similar respecto a las prótesis parcialmente cubiertas, con una incidencia de migración significativamente inferior que podría mejorar sustancialmente los resultados en estos pacientes14–16.
Las PECDM (modelo Niti S™ DOUBLE™ Esophageal Metal Stent) disponen de un mecanismo de recolocación y retirada, y la malla externa descubierta en su zona central disminuye la tasa de migración. Además, al estar el cuerpo de la prótesis totalmente cubierto, evita el crecimiento de tejido a través de los orificios de la malla lo que evita su obstrucción. Por ello, con este estudio planteamos evaluar la eficacia de estas prótesis en fístulas y perforaciones esofágicas, y las complicaciones asociadas a su uso.
ObjetivosNuestro objetivo principal consiste en evaluar la eficacia (éxito técnico) de PECDM (modelo Niti S™ DOUBLE™ Esophageal Metal Stent) en el tratamiento de las fístulas esofágicas o esofagogástricas no neoplásicas.
Como objetivos secundarios, analizar su perfil de seguridad en nuestra práctica clínica, basado en la presencia de complicaciones posteriores, y especialmente, en la tasa de migración de la prótesis.
Material y métodosSe trata de un estudio observacional, retrospectivo y unicéntrico tras nuestra experiencia en el empleo de PECDM (modelo Niti S™ DOUBLE™ Esophageal Metal Stent) desde octubre 2010 hasta noviembre 2018.
Se incluyeron pacientes portadores de PECDM (modelo Niti S™ DOUBLE™ Esophageal Metal Stent) tras diagnóstico endoscópico o radiológico de perforación o fístula esofágica o gastroesofágica de origen multifactorial, siendo excluidas únicamente aquellas de origen neoplásico.
Los procedimientos fueron realizados, bajo sedación profunda, por 3 endoscopistas expertos, considerando urgentes aquellos realizados en menos de 24h tras el diagnóstico de la lesión. La colocación de las prótesis fue guiada por endoscopia y fluoroscopia, con liberación de las mismas en paralelo al endoscopio.
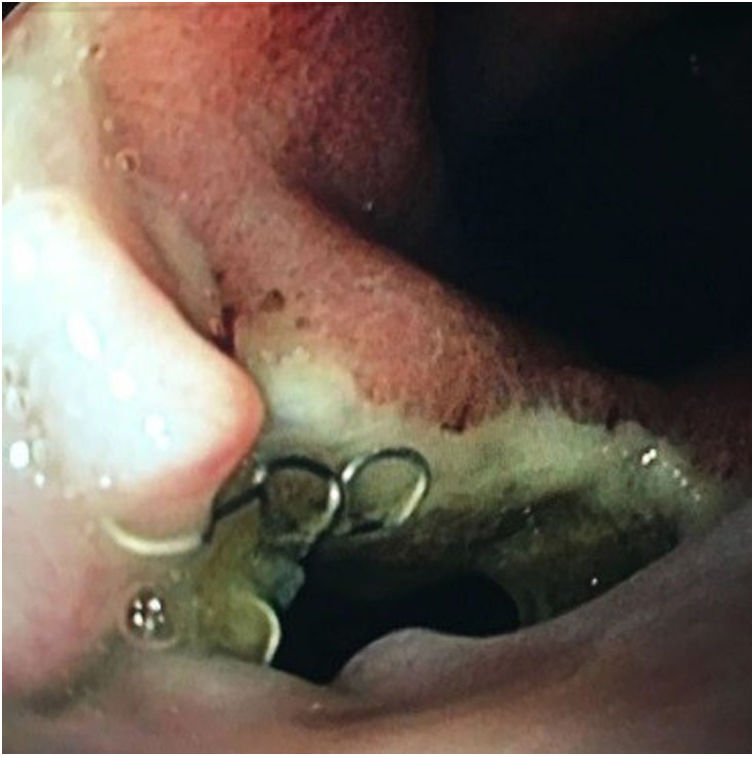
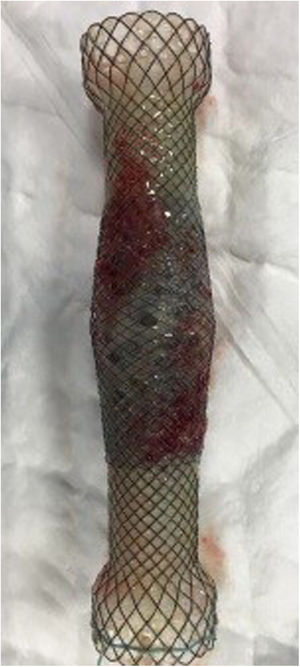
El modelo concreto de PECDM utilizado se compone de 2 capas de malla de nitinol, una interior, completamente cubierta de silicona, y una exterior totalmente descubierta. Dispone de un lazo en su extremo proximal, para facilitar su recolocación o retirada. Asimismo, presenta cuatro radiomarcadores opacos en cada extremo, y 2 en el centro, para facilitar su colocación por fluoroscopia (fig. 1). El sistema de liberación es de apertura distal.
Se analizaron las variables edad, sexo, características (longitud, diámetro) e indicación de colocación de la prótesis, resultado obtenido expresado en éxito técnico, tiempo hasta su retirada, así como complicaciones derivadas de la técnica.
Definimos éxito técnico como el cierre completo de la fístula o perforación, comprobado vía endoscópica, en el momento de su retirada; siendo primario si no ha precisado la colocación de una nueva prótesis, o bien fue solventada con su recolocación, y secundario si fue precisa una segunda prótesis, o un método endoscópico diferente, para conseguir su cierre.
Respecto a las complicaciones, se definió migración como el desplazamiento de la prótesis de su lugar de inserción, siendo parcial si la prótesis pudo ser recolocada endoscópicamente, y completa, si fue preciso colocar una nueva.
Las variables categóricas se presentaron en forma de frecuencias y porcentajes; y las variables continuas, como media y desviación estándar, siendo analizados con el programa SPSS® versión 21.
El protocolo fue aprobado por parte del Comité de Ética del Instituto Aragonés de Ciencias de la Salud.
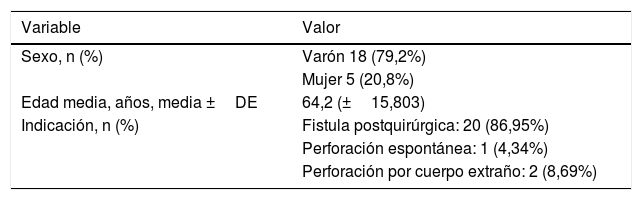
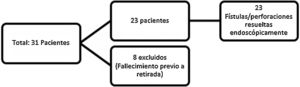
ResultadosSe analizó una muestra inicial de 31 pacientes. Se excluyeron posteriormente 8 pacientes por ausencia de seguimiento por fallecimiento. En todos los casos, el fallecimiento se produjo por causas ajenas a la técnica (fig. 2). De la muestra final, la edad media fue de 64,2 años, siendo el 79,2% varones (n=18). La indicación de la colocación de la PECDM fue fístula esofágica o esofagogástrica postquirúrgica en el 86,95% de ellos (n=20), y perforación esofágica por cuerpo extraño en el 8,69% (n=2), y espontánea (síndrome de Boerhaave) en el 4,34% restante (n=1) (tablas 1 y 2). Se colocaron con carácter urgente en un 47,82% de los casos (n=11).
Indicaciones y características de las prótesis empleadas
| Edad (años) | Sexo | Indicación | Distancia de ADS (cm) | Longitud (cm) | Diámetro (mm) | Timing de colocación | Tiempo Dx-colocación (días) |
|---|---|---|---|---|---|---|---|
| 47 | V | Fístula postquirúrgica | 12 | 18 | Programada | 7 | |
| 66 | M | Fístula postquirúrgica | 12 | 20 | Programada | ||
| 67 | V | Fístula postquirúrgica | 35 | 15 | 20 | Urgente | 1 |
| 34 | M | Fístula postquirúrgica | 40 | 12 | 20 | Programada | 32 |
| 67 | V | Perforación | 40 | 10 | 20 | Programada | 33 |
| 46 | V | Fístula postquirúrgica | 20 | 10 | 20 | Urgente | 1 |
| 69 | M | Fístula postquirúrgica | 35 | 12 | 20 | Programada | 2 |
| 81 | V | Fístula postquirúrgica | 33 | 12 | 20 | Urgente | 1 |
| 76 | V | Perforación | 32-35 | 15 | 20 | Urgente | <1 |
| 61 | V | Fístula postquirúrgica | 19 | 10 | 20 | Programada | 3 |
| 70 | M | Fístula postquirúrgica | 24 | 12 | 20 | Urgente | <1 |
| 73 | V | Fístula postquirúrgica | 28 | 10 | 18 | Urgente | Durante endoscopia diagnóstica |
| 53 | V | Fístula postquirúrgica | 29 | 12 | 20 | Programada | 3 |
| 21 | V | Fístula postquirúrgica | 40 | 15 | Programada | 31 | |
| 50 | V | Fístula postquirúrgica | 29 | 10 | 20 | Programada | 8 |
| 50 | V | Fístula postquirúrgica | 12 | 18 | Programada | ||
| 42 | V | Fístula postquirúrgica | 20 | 10 | 20 | Urgente | Durante endoscopia diagnóstica |
| 68 | V | Fístula postquirúrgica | 30 | 10 | 20 | Urgente | 1 |
| 79 | V | Perforación | 27 | 12 | 20 | Programada | 3 |
| 66 | V | Fístula postquirúrgica | 23 | 12 | 20 | Urgente | 1 |
| 75 | V | Fístula postquirúrgica | 22 | 10 | 22 | Urgente | 1 |
| 47 | M | Fístula postquirúrgica | 35 | 10 | 20 | Programada | 2 |
| 78 | V | Fístula postquirúrgica | 28 | 10 | 20 | Urgente | 1 |
ADS: arcada dental superior; M: mujer; Tiempo Dx-colocación: tiempo entre diagnóstico y colocación (casilla en blanco: datos no disponibles); V: varón.
El éxito técnico o cierre de la fístula, se produjo en el 100% de los pacientes, con un éxito primario del 62,5% (n=15), y alcanzando el 75% (n=18) tras la recolocación endoscópica de la prótesis. En el resto de los pacientes (n=5) persistió la fístula tras la retirada del stent, por lo que fue precisa una segunda PECDM (n=4), así como la colocación de un hemoclip (n=1). El tiempo medio de permanencia de la prótesis (stenting time) fue de 42,8 días (DE: ±21,363) (tabla 3).
Resultados tras la colocación de PECDM
| Variable | Valor |
|---|---|
| Éxito técnico, n (%) | 23 (100%) |
| Éxito primario, n (%) | 18 (75%) |
| Complicaciones, n (%) | 6 (29,1%) |
| Migración | 5 (83,3%) |
| Intolerancia | 1 (16,7%) |
| Tiempo medio hasta retirada: días (±DE) | 42,8 (±21,363) |
DE: desviación estándar; PECDM: prótesis esofágicas cubiertas de doble malla.
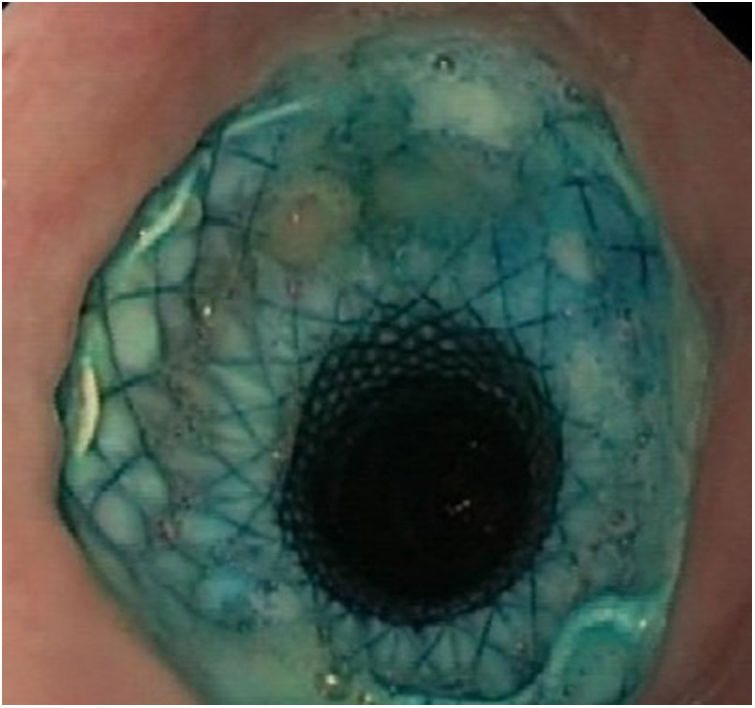
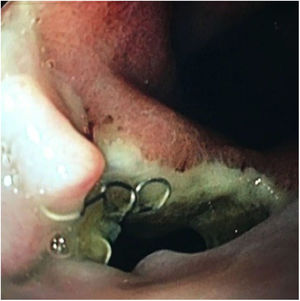
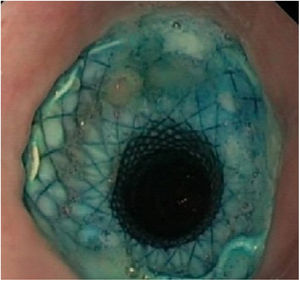
Respecto a su perfil de seguridad, se registraron complicaciones en el 29,1% de los pacientes (n=6). En el 21,7% (n=5) se objetivó migración de la prótesis: en 3 casos fue parcial y en 2 casos completa. En todos los casos se resolvió la fístula vía endoscópica: tras la recolocación de la prótesis migrada, o tras la inserción de un nuevo stent (figs. 3 y 4). Por otra parte, en un paciente fue preciso retirar la prótesis a las 2 semanas por intolerancia a la misma (dolor torácico persistente), si bien a pesar de su precoz retirada, la fístula ya se había cerrado.
En ningún caso se objetivó disfunción de prótesis por crecimiento tisular intra o peri-protésico, ni se registró ningún fallecimiento en relación con la técnica.
DiscusiónEl manejo de las fístulas esofágicas supone un reto para los facultativos, siendo frecuentemente resultado de una compleja intervención quirúrgica previa, y agravado por un paciente frágil con importante comorbilidad asociada.
De acuerdo con la última guía clínica sobre el manejo de prótesis en enfermedad esofágica benigna y maligna de la Sociedad Europea de Endoscopia Gastrointestinal (European Society of Gastrointestinal Endoscopy [ESGE]), el uso de prótesis esofágicas cubiertas es una opción terapéutica eficaz en el manejo de fístulas y perforaciones esofágicas13. Su duración todavía no está bien definida, si bien en la mayoría de estudios su retirada se realiza entre la sexta y octava semana17,18, siguiendo la misma línea que en nuestro centro.
Las PECDM han surgido con el objetivo de resolver las complicaciones más frecuentes derivadas del uso de prótesis en enfermedad esofágica: la migración y la re-estenosis por crecimiento tisular intra o peri-protésico. Inicialmente pensadas para su empleo en estenosis malignas, su mecanismo de recolocación posibilita la retirada de las mismas con facilidad, lo que las hace aptas para el tratamiento de enfermedad esofágica benigna.
En varios estudios, se ha descrito una tasa de complicaciones asociadas a la colocación de prótesis totalmente cubiertas del 34%4,14. La más frecuente es su migración, que, según un metaanálisis publicado recientemente, puede alcanzar hasta un 23% de los casos (IC 95%: 19-28%)19. En nuestra serie, el uso de las PECDM demostró una baja tasa de migración (21,73% del total, 3 parcial: 13% y 2 completa: 8,69%), encontrándose por debajo de la media de lo publicado hasta la fecha, y teniendo en cuenta, además, que no se trata de una PECDM diseñada específicamente para el cierre de fístulas postquirúrgicas.
No obstante, en otro estudio publicado recientemente, se describe una tasa de migración del 38,2% (13/34 stents), con un 53,8% (7/13 stents) de migración parcial, concluyendo que el éxito técnico y clínico del uso de prótesis esofágicas autoexpandibles cubiertas es muy alto, e incluso parece independiente de que exista migración o no de las prótesis20.
En nuestra serie, 3 de las 5 migraciones ocurridas (60%) fueron parciales, corrigiéndose mediante la recolocación endoscópica del stent, sin incidencias. No se registró ningún caso de crecimiento tisular intra o peri-protésico que ocasionase disfunción de la PECDM. Finalmente, se consiguió un éxito técnico con una o dos prótesis en el 95,6% (n=22) de los pacientes (una única prótesis en el 75% de los casos), alcanzando la resolución endoscópica de la fístula en el 100% (en un caso fue preciso la colocación de un hemoclip). Ningún caso requirió reintervención quirúrgica, y todas las complicaciones se solventaron mediante endoscopia.
No obstante, nuestro estudio presenta una serie de limitaciones. En primer lugar, su carácter retrospectivo. En segundo lugar, el pequeño tamaño muestral disponible, si bien el empleo de las PECDM en la patología benigna esofágica no resulta tan habitual en la práctica diaria, siendo nuestra serie la más extensa publicada hasta la fecha con este tipo de prótesis.
En un futuro, las prótesis biodegradables, al no requerir retirada ni recolocación en caso de migración, podrían suponer una alternativa, si bien todavía no disponemos de suficientes estudios que avalen su uso, e incluso se han descrito casos de disfagia y estenosis por reactividad mucosa12,21,22.
ConclusionesLas PECDM suponen un tratamiento mínimamente invasivo, eficaz y seguro en el manejo de fístulas y perforaciones esofágicas, con un alto porcentaje de éxitos y bajo de complicaciones, contrastado con lo expuesto en las series publicadas. En nuestra serie, destaca una tasa de migración completa similar o inferior a lo expuesto en estudios previos14, todas ellas resueltas vía endoscópica sin requerir cirugía, con ausencia de disfunción protésica secundaria a crecimiento tisular.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.