Evaluar la relación coste-efectividad del cribado universal para la enfermedad tiroidea en mujeres embarazadas frente al cribado selectivo y no realizar cribado.
MetodologíaModelo analítico de decisión para embarazo y periodo posparto que compara los años de vida ajustados por la calidad (AVAC) obtenidos gracias a la realización de un cribado universal frente al cribado de alto riesgo y no realizar cribado. Se consideraron las probabilidades de los ensayos aleatorios controlados para los resultados obstétricos adversos. Se utilizó un modelo de Markov para valorar el período de vida tras el primer año después del parto y considerar la posible progresión a hipotiroidismo clínico. Los principales supuestos del modelo, así como el uso de recursos fueron evaluados por expertos clínicos. Se consideraron únicamente los costes sanitarios directos.
ResultadosRealizar un cribado universal produce 0,011 AVAC más que el cribado selectivo y 0,014 AVAC más que la alternativa de no realizar cribado. Los costes totales directos por paciente fueron de 5.786€ para el cribado universal, 5.791€ para cribado por riesgo y de 5.781€ sin cribado. El paso del cribado selectivo por riesgo al cribado universal puede ahorrar 2.653.854€ al sistema sanitario español.
ConclusionesEl cribado universal de enfermedad tiroidea durante el primer trimestre de gestación es una estrategia dominante frente al cribado selectivo y coste-efectiva con respecto al no cribado (ratio coste-efectividad incremental de 374€ por AVAC), que permite además diagnosticar y tratar casos de hipotiroidismo clínico y subclínico que podrían no ser detectados al cribar solo mujeres con alto riesgo.
To assess the cost-effectiveness of universal screening for thyroid disease in pregnant women in Spain as compared to high risk screening and no screening.
MethodologyA decision-analytic model comparing the incremental cost per quality-adjusted life year (QALY) of universal screening versus high risk screening and versus no screening. was used for the pregnancy and postpartum period. Probabilities from randomized controlled trials were considered for adverse obstetrical outcomes. A Markov model was used to assess the lifetime period after the first postpartum year and account for development of overt hypothyroidism. The main assumptions in the model and use of resources were assessed by local clinical experts. The analysis considered direct healthcare costs only.
ResultsUniversal screening gained .011 QALYs over high risk screening and .014 QALYS over no screening. Total direct costs per patient were €5,786 for universal screening, €5,791 for high risk screening, and €5,781 for no screening. Universal screening was dominant compared to risk-based screening and a very cost-effective alternative as compared to no screening. Use of universal screening instead of high risk screening would result in €2,653,854 annual savings for the Spanish National Health System.
ConclusionsUniversal screening for thyroid disease in pregnant women in the first trimester is dominant in Spain as compared to risk-based screening, and is cost-effective as compared to no screening (incremental cost-effectiveness ratio of €374 per QALY). Moreover, it allows diagnosing and treating cases of clinical and subclinical hypothyroidism that may not be detected when only high-risk women are screened.
Durante el embarazo la prevalencia del hipotiroidismo clínico (HC) oscila entre el 0,3-0,5% y la de hipotiroidismo subclínico (HS) entre el 2-3%1,2. Estos trastornos subclínicos de la función tiroidea constituyen las anomalías funcionales más comunes en las mujeres gestantes con enfermedades tiroideas.
El hipotiroidismo durante el embarazo suele ser asintomático. En los casos más graves tanto el HS como el HC pueden producir algunos signos y síntomas tales como una ganancia de peso inapropiada, intolerancia al frío, astenia y sequedad de piel3. El HS y HC en el embarazo pueden causar resultados obstétricos adversos como el desprendimiento prematuro de la placenta y el parto pretérmino, siendo más frecuente el ingreso en cuidados intensivos neonatales1,4,5. Por otro lado, las gestantes con anticuerpos antiperoxidasa (antiTPO) positivos tienen concentraciones de tirotropina (TSH) significativamente más altas que las mujeres con antiTPO negativos5, habiéndose observado una elevación del porcentaje de pérdidas fetales en estas pacientes3,5–7.
El diagnóstico de HC y HS durante el embarazo requiere conocer los cambios específicos que se producen en la función tiroidea durante cada trimestre8. Desde que se identificó al HC/HS como causa de morbilidad materno-fetal, se ha establecido un debate sobre la conveniencia de realizar un cribado universal de la función tiroidea durante el embarazo o, simplemente, un cribado selectivo en función de factores de riesgos (mujeres con antecedentes de historia familiar de enfermedades tiroideas, diabetes tipo 1, desorden de tiroides, parto prematuro, terapia de irradiación sobre cabeza o cuello, entre otros). El cribado selectivo por factores de riesgo ha sido el método preferido debido a su aplicabilidad y a la falta de estudios que demostraran la superioridad del cribado universal frente al cribado por riesgos. Trabajos recientes han mostrado que el cribado solo de mujeres consideradas como de alto riesgo no identificaría el 30-50% de mujeres con HC o HS que podrían beneficiarse del tratamiento9,10.
Actualmente en España se realiza la prueba de cribado a aquellas mujeres que presentan alto riesgo de HC. Así pues, no existe un programa poblacional de cribado para la disfunción tiroidea, sino que solo existen unas recomendaciones del Grupo de Trabajo de Trastornos por Deficiencia de Yodo y Disfunción Tiroidea de la Sociedad Española de Endocrinología y Nutrición y de la Sociedad Española de Ginecología y Obstetricia11.
Recientemente, en un análisis coste-efectividad en Estados Unidos, se ha demostrado que el cribado universal para enfermedad tiroidea autoinmune de las mujeres en el primer trimestre del embarazo es coste-efectivo, tanto si se compara con el escenario de gestantes sin cribado como con el cribado selectivo en las mujeres de alto riesgo12. El objetivo de nuestro estudio fue evaluar la relación coste-efectividad del cribado universal del HS y HC durante el embarazo como alternativa al cribado por riesgo o la no utilización del cribado en España.
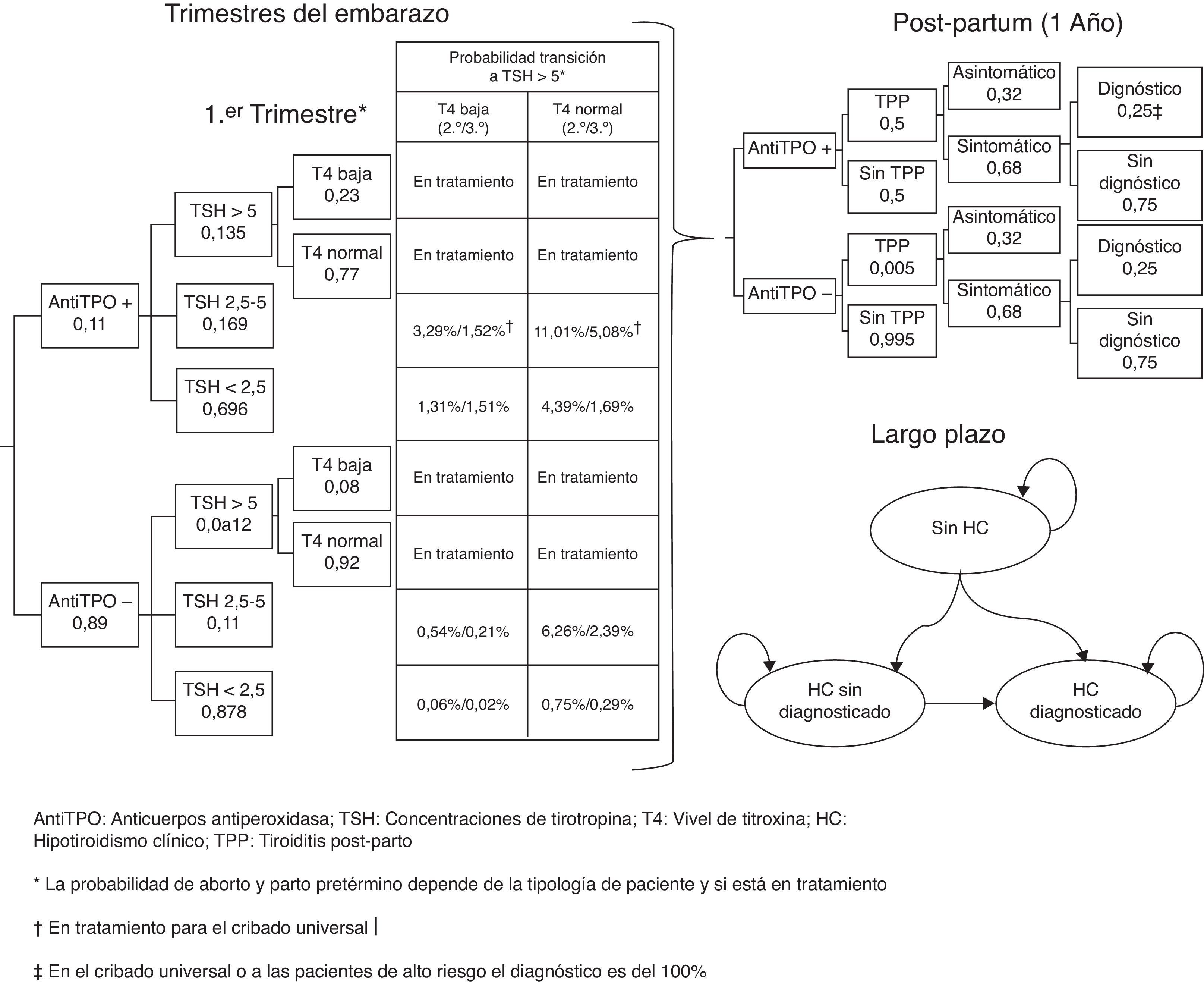
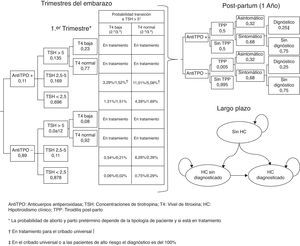
Materiales y métodosSe ha desarrollado un modelo de decisión a corto plazo (tiempo de embarazo y año postembarazo) y un modelo de Markov de ciclos anuales a largo plazo para evaluar los beneficios clínicos y económicos de las estrategias de cribado del HC y HS durante el embarazo (fig. 1). En el modelo se ha asumido una cohorte hipotética de mujeres embarazadas de 31,46 años (media de edad de las mujeres embarazas en España)13, de las cuales un 20% pertenece a alguno de los grupos denominados de alto riesgo12.
El indicador de coste-efectividad utilizado en el estudio es el coste por año de vida ajustado por calidad (AVAC). Adicionalmente se analizó el coste por aborto evitado y el coste por parto pretérmino evitado.
Las 3 estrategias de cribado consideradas fueron:
- 1)
Cribado universal: se realiza la determinación de niveles de anticuerpos antiTPO y de la TSH a todas las mujeres embarazadas. Si la TSH es >5mIU/l se determinan los niveles de T4 para diferenciar entre HC y HS, previamente a la derivación al endocrinólogo. La administración de levotiroxina en las mujeres embarazadas se realiza a partir de TSH>5mIU/l o con TSH entre 2,5-5mIU/l con anticuerpos antiTPO positivos. A las mujeres se les realizan todas las determinaciones durante el primer trimestre del embarazo y, con posterioridad, tan solo se les realiza la determinación de TSH y T4 en cada trimestre durante la gestación.
- 2)
Cribado selectivo basado en factores de riesgo: se realizan las mismas determinaciones que en el cribado universal, pero solo a las mujeres clasificadas de alto riesgo. Al resto de embarazadas no se les realiza ninguna determinación adicional. El tratamiento con levotiroxina únicamente se administra a mujeres embarazadas con TSH>5mIU/l.
- 3)
Sin cribado: no se realizan de forma sistemática las determinaciones de TSH, T4, ni la de anticuerpos antiTPO.
El análisis se ha realizado desde la perspectiva del sistema sanitario, descontando al 3% los costes y efectos, tal como recomiendan las guías españolas de evaluación económica14. Se han tenido en cuenta los costes médicos, las probabilidades y las utilidades relacionadas con el tratamiento y las posibles secuelas durante toda la vida de las mujeres.
Modelo de decisiónEl árbol de decisión comienza con una clasificación de las mujeres embarazadas según el nivel TSH, anticuerpos antiTPO y T4. Dependiendo del cribado el médico podrá clasificar a la mujer embarazada durante el primer trimestre como HC, HS o anticuerpos antiTPO+, o no hará ninguna determinación analítica hasta observar alguno de los síntomas característico del HC o del HS que sugiera realizar el cribado a partir del segundo trimestre (fig. 1). A lo largo de los trimestres del embarazo la mujer puede continuar con la evolución de su embarazo, tener un aborto a lo largo del primer y segundo trimestre o un parto prematuro en el tercer trimestre. En el transcurso del embarazo se ha previsto que las pacientes con HC y HS sean tratadas con levotiroxina y que el resto de las embarazadas puedan incrementar sus niveles de TSH>5mIU/l a lo largo del segundo y tercer trimestre.
A partir del parto a término o del parto pretérmino se evalúa a lo largo del siguiente año la posibilidad de que la mujer sufra de tiroiditis posparto (TPP) en función de si tiene positividad o no para anticuerpos antiTPO (fig. 1). Se ha tenido en consideración el cribado para valorar con qué probabilidad las pacientes con TPP sintomática serían diagnosticadas.
Pasado el aborto o el año tras el parto se inicia el modelo de Markov considerando a todas las mujeres en el estado de no tener HC, exceptuando aquellas que evolucionan a tener HC permanente tras padecer una TPP o aquellas con HC detectado en el embarazo (fig. 1). A lo largo del tiempo las mujeres pueden padecer HC (no diagnosticado, diagnosticado y cumpliendo el tratamiento farmacológico y diagnosticado pero sin cumplir el tratamiento farmacológico) o fallecer por cualquier causa. Se ha incorporado en el modelo la probabilidad de eventos cardiovasculares y su mortalidad asociada en función del tipo de paciente.
ProbabilidadesLas probabilidades para el árbol de decisión y las transiciones de los estados del modelo de Markov se han obtenido principalmente de Dosiou et al.12. Se asoció una probabilidad de anticuerpos antiTPO positivos en las mujeres del 11,16% (10% bajo riego y 15,8% alto riesgo). En función de si las mujeres tuviesen anticuerpos antiTPO positivos o negativos se diferenció el nivel de TSH, de tal forma que la probabilidad de TSH<2,5mIU/l fue del 69,6% para las positivas y del 87,8% para las negativas, la probabilidad de TSH entre 2,5 y 5mIU/l fue del 16,9% para las positivas y del 11% para las negativas; y la probabilidad de TSH>5mIU/l fue del 13,5% para las positivas y del 1,2% para las negativas12.
A partir del segundo trimestre las mujeres sin tratamiento con levotiroxina pueden progresar a TSH>5mIU/l, de tal forma que la progresión en el segundo trimestre ha sido en un 14,3% con anticuerpos antiTPO positivos y TSH entre 2,5 y 5mIU/l, en un 6,80% con anticuerpos antiTPO negativos y TSH entre 2,5 y 5 mIU/l, en un 5,70% con anticuerpos antiTPO positivos y TSH<2,5mIU/l y en un 0,81% con anticuerpos antiTPO negativos y TSH<2,5mIU/l12. En el tercer trimestre la progresión ha sido en 6,60% con anticuerpos antiTPO positivos y TSH entre 2,5 y 5mIU/l, en un 2,60% con anticuerpos antiTPO negativos y TSH entre 2,5 y 5mIU/l; en un 2,20% con anticuerpos antiTPO positivos y TSH<2,5mIU/l y en un 0,31% con anticuerpos antiTPO negativos y TSH<2,5mIU/l12. Se ha asumido que la proporción de pacientes con incremento de la TSH y con T4 baja es del 23% para las mujeres con anticuerpos antiTPO positivos y del 8% para las mujeres con antiTPO negativos. Así, el modelo asume que el 100% de las mujeres embarazadas con HC o HS reciben tratamiento, exceptuando las que no han sido cribadas o las del subgrupo de pacientes de bajo riesgo condicionado a que solo el 28% de las mujeres con HS son diagnosticadas y tratadas. El modelo asume el cumplimiento del tratamiento con levotiroxina siempre en la fase de embarazo y del 90% en el tratamiento a largo plazo.
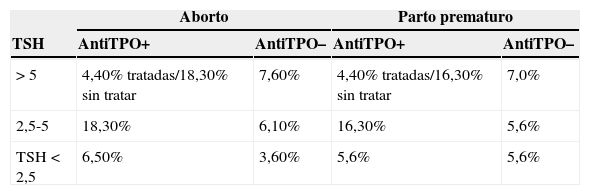
La probabilidad de aborto espontáneo o de parto prematuro proviene del estudio de Negro et al.15, donde se analiza el tratamiento de la disfunción tiroidea en 4.562 mujeres según se hubiera realizado o no el cribado universal (tabla 1). Para ajustar los datos a la población española se ha tenido en cuenta que el 85% de los abortos se producen en el primer trimestre16.
Probabilidad de aborto/parto prematuro del árbol de decisión y probabilidades del modelo de Markov
| Aborto | Parto prematuro | |||
|---|---|---|---|---|
| TSH | AntiTPO+ | AntiTPO– | AntiTPO+ | AntiTPO– |
| >5 | 4,40% tratadas/18,30% sin tratar | 7,60% | 4,40% tratadas/16,30% sin tratar | 7,0% |
| 2,5-5 | 18,30% | 6,10% | 16,30% | 5,6% |
| TSH<2,5 | 6,50% | 3,60% | 5,6% | 5,6% |
| Probabilidades de transición anuales del modelo de Markov | ||||
|---|---|---|---|---|
| TSH>5 y antiTPO+ | TSH>5 y antiTPO– | TSH<5 y antiTPO+ | TSH<5 y antiTPO– | |
| De sin evento a | ||||
| HC no diagnosticado | 0,00% | 0,00% | 1,58% | 0,23% |
| HC cumplidor | 3,87% | 2,34% | 0,47% | 0,07% |
| HC no cumplidor | 0,43% | 0,26% | 0,05% | 0,01% |
| De HC no diagnosticado a | ||||
| HC cumplidor | 45,00% | 45,00% | 45,00% | 45,00% |
| HC no cumplidor | 5,00% | 5,00% | 5,00% | 5,00% |
| De HC no cumplidor | ||||
| HC cumplidor | 50,00% | 50,00% | 50,00% | 50,00% |
| Hazard ratio cardiovasculara | ||||
|---|---|---|---|---|
| Sin evento | HC desconocido | HC no cumplidor | HC cumplidor | |
| Eventos | ||||
| 18-49 | 1 | 4,01 | 2,12 | 1 |
| 50-64 | 1 | 3,10 | 1,64 | 1 |
| 65-79 | 1 | 3,29 | 1,74 | 1 |
| 80+ | 1 | 3,57 | 1,89 | 1 |
| Mortalidad | ||||
| 18-49 | 1 | 4,81 | 3,31 | 1 |
| 50-64 | 1 | 2,93 | 2,02 | 1 |
| 65-79 | 1 | 2,98 | 2,05 | 1 |
| 80+ | 1 | 2,28 | 1,57 | 1 |
Se ha aplicado que tras el embarazo las mujeres con anticuerpos antiTPO positivos tienen una probabilidad entre el 40% y el 60% de presentar TPP17 y de un 0,5% en las mujeres con anticuerpos antiTPO negativos12. Este TPP será sintomático en el 68% de los casos y será diagnosticado totalmente en el cribado universal o en los pacientes de alto riesgo12. En cambio, para aquellas sin cribado o del subgrupo de pacientes de bajo riesgo sin cribado se ha considerado que las pacientes con TTP sintomático serán solo diagnosticadas en el 25% de los casos12.
Aunque es conocido que alrededor del 10-20% de las mujeres que están eutiroideas después de una fase inicial de hipotiroidismo por TPP desarrollarán hipotiroidismo permanente en los 3-10 años siguientes17, no se ha incluido este efecto por estar indivisiblemente unido con la probabilidad de transición a HC del modelo de Markov. Las probabilidades de transición entre estados de salud en función de la TSH y de los anticuerpos antiTPO provienen del estudio de Dosiou et al.12. La probabilidad de morir por cualquier causa provenía de datos españoles ajustando por edad y sexo18. Basándonos en el estudio de Rodondi et al.19, donde se identifica un mayor riesgo de eventos cardiovasculares en función de la TSH, del sexo y la edad, se han estimado las hazard ratios específicas para los pacientes con HC no diagnosticado, con HC diagnosticado sin cumplimiento de tratamiento y con HC diagnosticado con cumplimiento de tratamiento (tabla 1). La aplicación de estas hazard ratios a la probabilidad de tener eventos cardiovasculares en España20 nos permitió estimar los eventos cardiovasculares de la cohorte de mujeres ajustada por edad. Con el mismo procedimiento se incorporó también la mortalidad cardiovascular21.
Uso de recursos y costesEn el periodo del embarazo se asoció el consumo habitual de una embarazada con respecto a las visitas al ginecólogo y las pruebas diagnósticas. Se tuvo en cuenta las pruebas diagnósticas (TSH, T4 y anticuerpos antiTPO) en los 3 trimestres, así como la visita al endocrinólogo y el tratamiento con levotiroxina (primer trimestre 50mcg, segundo y tercer trimestre 75mcg) en función de la tipología de paciente y el cribado.
Para las mujeres con parto pretérmino se ha asociado el uso de recursos derivado de que el neonato tiene un peso inferior de 1.500g y genera necesidades específicas (incubadora, intervención quirúrgica, cuidados intensivos, etc.). En ese sentido el uso de recursos y la proporción de cada tipo de casos se basa en los grupos relacionados de diagnóstico del código 602 al 608 del conjunto mínimo básico de datos del Ministerio de Sanidad20.
En el periodo posparto se han identificado las visitas al endocrinólogo, los test diagnósticos en función de los anticuerpos antiTPO y, en el caso necesario, el tratamiento con levotiroxina a dosis de 50mcg/día a partir de la primera visita del endocrinólogo. En el caso de identificar la TPP en la mujer entonces se hace un seguimiento más intensivo (hasta 4 veces) y se administra el tratamiento aproximadamente durante 4 meses.
Asimismo en el periodo de seguimiento a largo plazo las mujeres diagnosticadas de HS por cribado universal no son tratadas después del primer año posparto y solo incurren en coste las mujeres diagnosticadas de HC (2 visitas de atención primaria, una visita de endocrinólogo, 1,4 determinaciones de TSH y 1,4 determinaciones de T4). Se asume que las mujeres con HC diagnosticada, pero con falta de cumplimiento de tratamiento, consumen el 80% del tratamiento farmacológico (levotiroxina 100mcg/día).
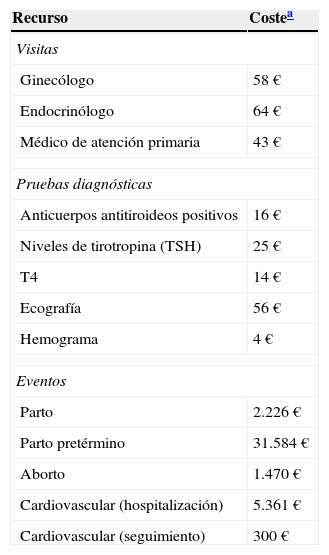
Los costes del uso de recursos se han obtenido de la base de datos de costes españoles eSalud22 y los costes farmacológicos según el PVL, principalmente el tratamiento con levotiroxina se ha obtenido de la bases de datos de medicamentos BotPLUS23 (tabla 2).
Costes unitarios
| Recurso | Costea |
|---|---|
| Visitas | |
| Ginecólogo | 58€ |
| Endocrinólogo | 64€ |
| Médico de atención primaria | 43€ |
| Pruebas diagnósticas | |
| Anticuerpos antitiroideos positivos | 16€ |
| Niveles de tirotropina (TSH) | 25€ |
| T4 | 14€ |
| Ecografía | 56€ |
| Hemograma | 4€ |
| Eventos | |
| Parto | 2.226€ |
| Parto pretérmino | 31.584€ |
| Aborto | 1.470€ |
| Cardiovascular (hospitalización) | 5.361€ |
| Cardiovascular (seguimiento) | 300€ |
Costes medios en euros de 2012 obtenidos a partir de la base de datos eSalud. Fuente: Gisbert y Brosa22.
Adicionalmente se ha estimado el impacto económico de la incorporación de la estrategia más coste-efectiva en el sistema nacional de salud a partir de la estimación de mujeres embarazadas para España multiplicado por la diferencia de costes con la estrategia actual de cribado por riesgo. La estimación de las mujeres embarazadas se realizó en función de la tasa de fecundidad por edad y periodo de 12 meses13 multiplicado por las mujeres en España18.
UtilidadesPara llevar a cabo la transformación de los años de vida a AVAC se han asociado valores de utilidad para cada estado de salud según la media del indicador EQ-5D. Los valores del EQ-5D constituyen un indicador numérico que representa el valor que la sociedad concede al estado de salud actual, que toma valores de 1 cuando representa la mejor salud posible y 0 cuando representa la muerte. Se ha asignado una utilidad máxima (valor de 1) a las mujeres eutiroideas, a las pacientes con HC, HS o TPP asintomático o sintomático pero tratado. Se ha estimado que las utilidades de las pacientes con HC sin tratar, o que incumplen el tratamiento es de 0,7085, con HS sintomático sin tratar es de 0,9 y con TPP sintomático sin tratar es de 0,8112. Asimismo para el aborto espontáneo se ha aplicado una utilidad de 0,9 y para el parto prematuro de 0,9112. La utilidad asociada a las enfermedades cardiovasculares se estimó en 0,379 a partir de un estudio de calidad de vida español en pacientes con insuficiencia cardiaca24.
Análisis de sensibilidadSe ha llevado a cabo una batería de análisis de sensibilidad modificando, principalmente, la probabilidad de anticuerpos antiTPO positivos (10-30% alto riesgo/5-15% bajo riesgo), la proporción de mujeres de alto riesgo (10-30%), la proporción de pacientes con TPP (40-60%), las utilidades asociadas, la probabilidad de diagnosticar de HC a mujeres que han sido cribadas pero con valores de TSH<5 (100%), la probabilidad de diagnosticar de HC a mujeres que no han sido cribadas pero con valores de TSH>5 (25%) y la edad de gestación (18-45 años).
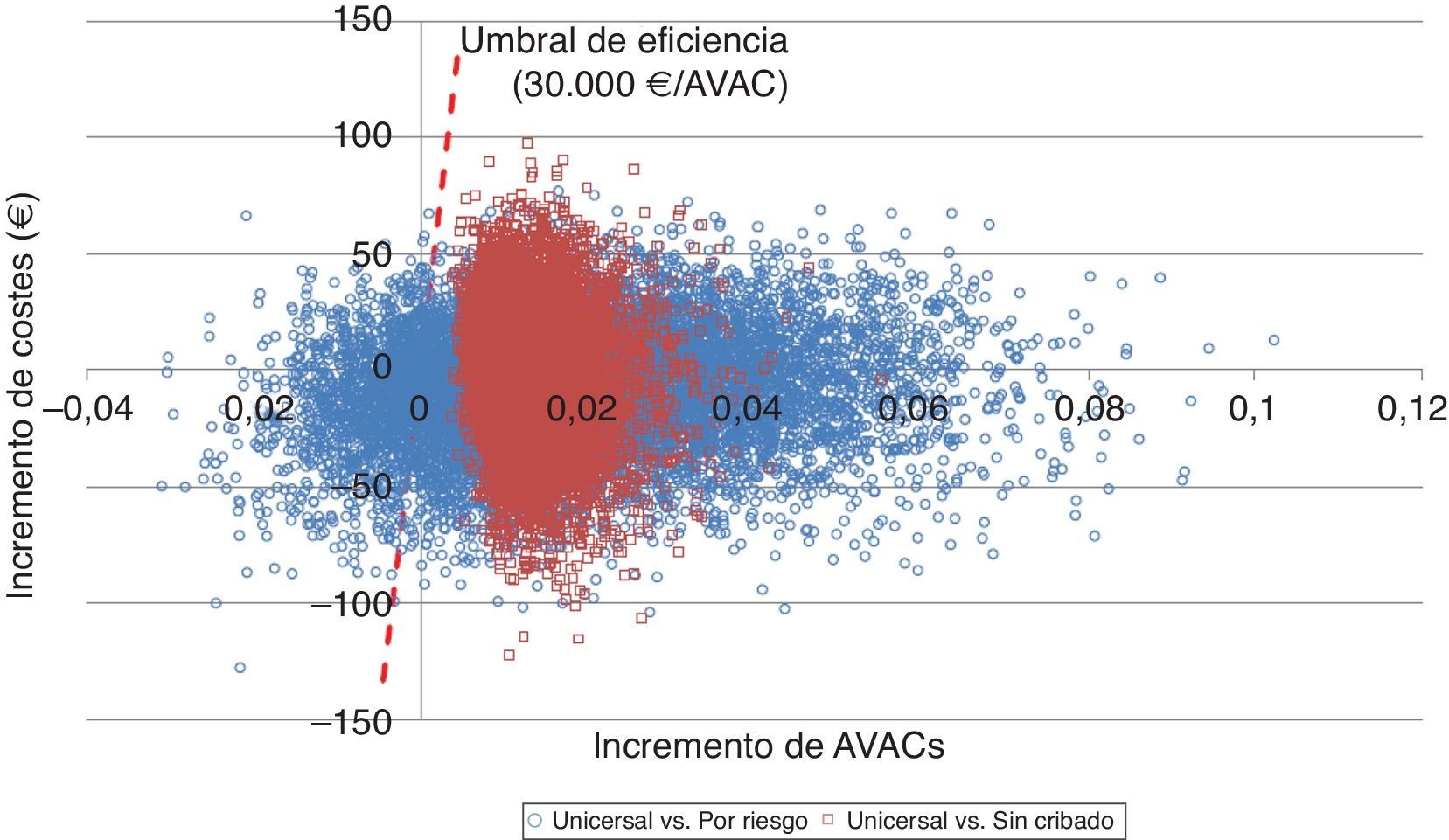
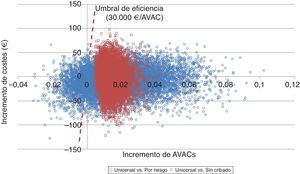
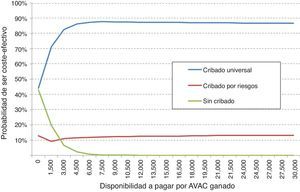
Adicionalmente, se realizó el análisis de sensibilidad probabilístico mediante la simulación de Monte Carlo de segundo orden. Este análisis permite valorar la influencia de la incertidumbre sobre los parámetros y la robustez de los resultados. Se simularon 10.000 veces los resultados del caso base del modelo sobre una cohorte hipotética, con el fin de observar la probabilidad con la que los resultados se mantienen estables ante la variación multivariante y simultánea de los principales parámetros incluidos. Los resultados del análisis de sensibilidad probabilístico se expresaron mediante el plano de coste-efectividad, en el cual se representan como puntos cada simulación, en el eje de abscisas los AVAC incrementales y en el de ordenadas los costes incrementales del cribado universal respecto el cribado por riesgo o el no cribado. Se ha incluido el umbral español de disponibilidad a pagar normalmente utilizado (30.000€/AVAC ganado) para designar la opción coste-efectiva25. La variación de las variables fue realizada asignando una distribución triangular para las probabilidades y la edad, una distribución log-normal para las hazard ratios, una distribución gamma para las desutilidades y los costes. Adicionalmente, se muestra la probabilidad de que las alternativas sean coste-efectivas en función de un abanico de disponibilidades a pagar por incrementos en AVAC mediante la curva de aceptabilidad a pagar.
ResultadosLa probabilidad de que una mujer embarazada aborte espontáneamente fue del 4,12% para el cribado universal, del 4,52% para el cribado por riesgo y del 4,57% para la opción sin cribar. Asimismo, los partos pretérmino se observaron en mayor medida en la opción sin cribado (5,65%) y en el cribado por riesgos (5,63%). Por tanto, el cribado universal evita entre 0,4% y 0,46% de abortos; y entre 0,22% y 0,24% de partos pretérmino.
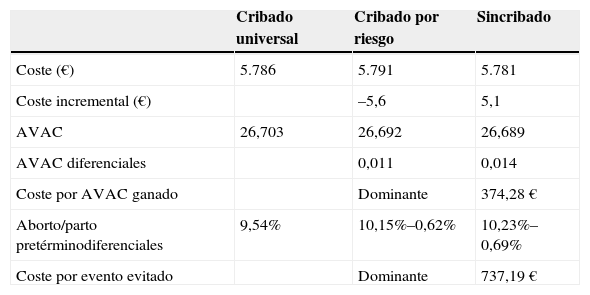
Los costes totales directos por paciente fueron 5.786€ para el cribado universal, 5.791€ para el cribado por riesgo y 5.781€ para el escenario de no cribado. Si focalizamos en el cribado por riesgo, se observó que las mujeres de grupo de alto riesgo alcanzaron el coste medio más elevado (5.923€) y las del grupo de bajo riesgo alcanzaron el más bajo (5.758€). El cribado universal incrementó en 4,02 días (0,011 AVAC) el tiempo de vida ajustado por calidad respecto del cribado por riesgos, siendo por tanto una alternativa dominante al mostrar mejor la efectividad y el menor coste. Respecto del escenario de no cribado el cribado universal incrementó en 4,99 días (0,014 AVAC) el tiempo de vida ajustado por calidad, obteniendo una ratio coste-efectividad incremental de 374€ por AVAC. Al focalizar en la comparación entre el cribado por riesgos respecto del escenario de no cribado, se observó un incremento de 0,97 días (0,003 AVAC) el tiempo de vida ajustado por calidad, obteniendo una ratio coste-efectividad incremental de 4.020€ por AVAC (tabla 3).
Análisis coste-efectividad
| Cribado universal | Cribado por riesgo | Sincribado | |
|---|---|---|---|
| Coste (€) | 5.786 | 5.791 | 5.781 |
| Coste incremental (€) | –5,6 | 5,1 | |
| AVAC | 26,703 | 26,692 | 26,689 |
| AVAC diferenciales | 0,011 | 0,014 | |
| Coste por AVAC ganado | Dominante | 374,28€ | |
| Aborto/parto pretérminodiferenciales | 9,54% | 10,15%–0,62% | 10,23%–0,69% |
| Coste por evento evitado | Dominante | 737,19€ |
AVAC: años de vida ajustados por calidad.
Por tanto, teniendo en cuenta el número de embarazos en España (477.132) y el ahorro de 5,56€ por paciente entre realizar el cribado universal y el cribado por riesgo, el sistema sanitario español se podría ahorrar aproximadamente 2.653.854€.
Análisis de sensibilidadLas variables que más influenciaron el resultado fueron la probabilidad de anticuerpos antiTPO positivos en las mujeres de bajo riesgo y alto riesgo, de tal forma que si dicha probabilidad disminuye considerablemente (5% y 10%, respectivamente) la ratio coste-efectividad incremental del cribado universal respecto del cribado por riesgo es como máximo de 3.062€ por AVAC ganado, y respecto al escenario sin cribado es como máximo 3.735€ por AVAC ganado, que están muy por debajo del umbral de eficiencia (30.000€/AVAC ganado). Respecto a la edad de gestación se observó que a medida que aumentaba la edad se incrementan los AVAC a favor del cribado universal; en cambio, el coste diferencial respecto al cribado por riesgos disminuía de 5,92€ a 4,90€ cuando respecto al no cribado aumentaba de 4,74€ a 5,76€. Cabe destacar que estas variaciones en las variables no modificaron en ningún caso las conclusiones.
El análisis de sensibilidad probabilístico mostró que la realización del cribado universal es una opción más efectiva y menos costosa en el 50% de las simulaciones respecto del cribado por riesgo, y además en el 36% muestra valores del ratio coste-efectividad incremental por debajo del umbral español. Respecto a la comparación entre cribado universal y no realizar el cribado se muestra la dominancia del cribado en el 48% y es coste-efectivo en el 52% de los casos (fig. 2).
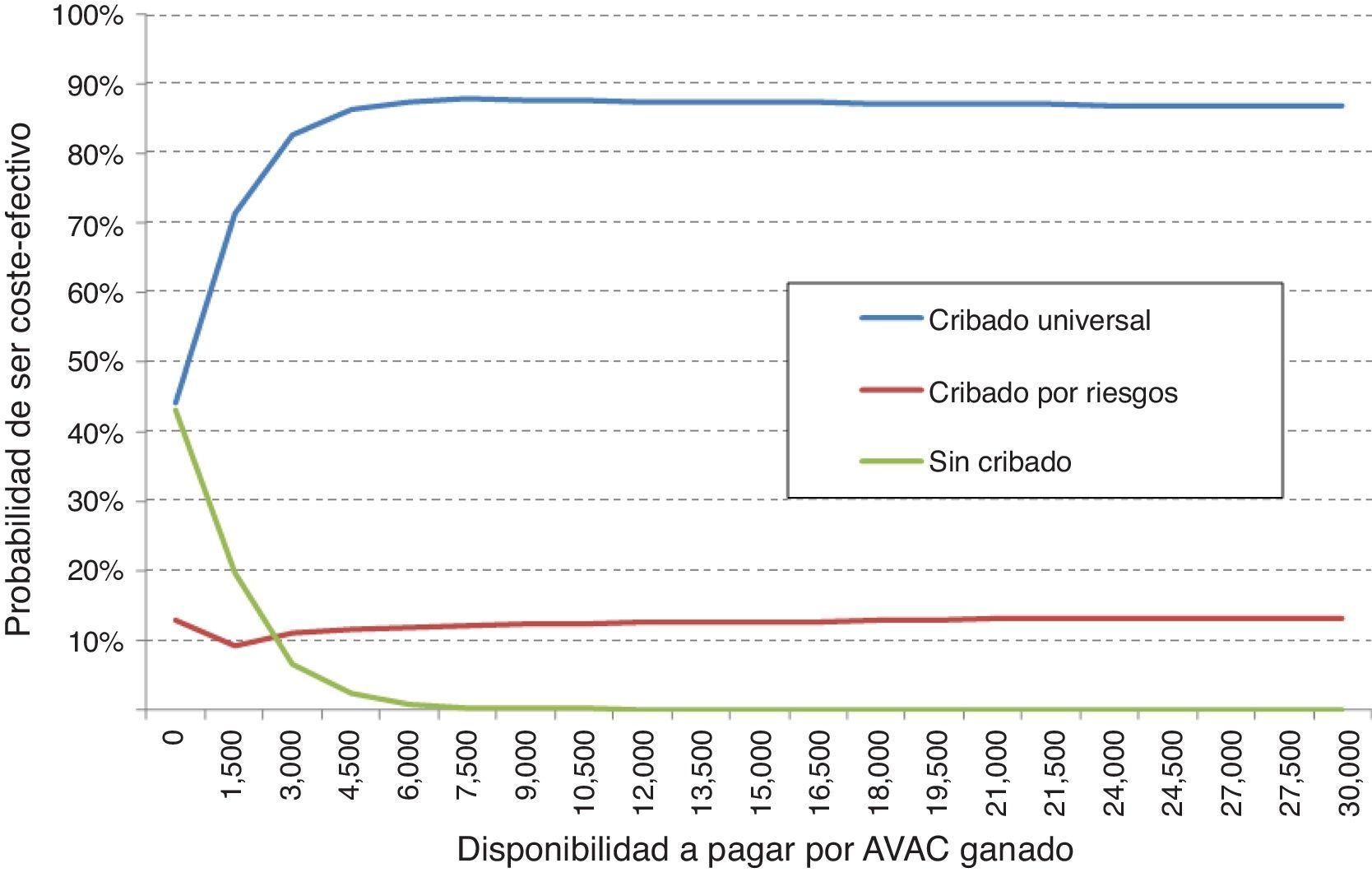
Al valorar en conjunto el beneficio neto sanitario del cribado universal, el cribado por riesgo y la no realización del cribado, se observa que la opción más coste-efectiva fue, para cualquier disponibilidad a pagar, el cribado universal. Por tanto, con el umbral español normalmente utilizado (30.000€/AVAC ganado), la opción de elección debe ser el cribado universal. De este modo, el análisis de sensibilidad probabilístico confirma los resultados obtenidos en el análisis determinístico (fig. 3).
DiscusiónEl presente estudio, a partir de la metodología antes descrita, ha puesto de manifiesto que el cribado universal del hipotiroidismo en mujeres embarazadas es coste-efectivo comparado en España con el cribado por riesgos, y que la estrategia de no cribar no representa una alternativa válida. Este mismo efecto se había podido observar en 2 análisis coste-efectividad anteriores llevados a cabo en Estados Unidos que mostraban que el cribado universal en mujeres embarazadas es coste-efectivo comparado con la estrategia de no cribado26,27. Por otro lado, nuestros resultados están en línea con los observados en otro estudio llevado a cabo en Estados Unidos que compara el cribado universal en mujeres embarazadas con respecto al cribado por riesgos, mostrando un coste muy similar y aportando un mayor número de AVAC ganados12. Hay que tener en cuenta que en el ámbito nacional este es el primer estudio coste-efectividad que evalúa en un modelo de decisión a largo plazo la idoneidad del cribado universal por su balance beneficios-riesgos. Además, de este estudio se desprende que la aplicación del cribado universal en lugar del cribado por riesgo puede suponer un ahorro de de 2,6 millones de euros al Sistema Nacional de Salud.
Un punto fuerte del presente estudio es haber usado datos de ensayos clínicos aleatorizados de las tasas de efectos adversos obstétricos y haber incluido los eventos cardiovasculares relacionados con el HC sin tratar. Hay que tener en cuenta que en un estudio reciente que se valoraba la carga de la enfermedad del HS para España, se observó que el HS supone la pérdida de más de 30.000 años de vida ajustados por discapacidad, que equivale a un coste de casi 67 millones de euros por los eventos cardiovasculares que produce28. Además, cuando hubo que hacer supuestos se fue muy conservador y posiblemente se esté subestimando el beneficio del cribado universal. Cabe destacar que se han excluido del modelo otros potenciales beneficios del cribado universal de gran trascendencia, como pueden ser la mejoría del cociente intelectual del neonato8.
El presente análisis tiene diversas limitaciones. En primer lugar, cabe recordar que se trata de un modelo teórico complejo que intenta a su vez representar una simulación simplificada de la realidad. Dada la complejidad de la realidad, su simulación teórica no está exenta de incertidumbre, y con el objetivo de minimizarla se llevaron a cabo diversos análisis de sensibilidad.
Otras limitaciones del actual estudio incluyen el hecho de que ciertas probabilidades fueron estimadas cuando había escasez de datos. Se intentó minimizar los efectos de la incertidumbre introducida considerando las asunciones más conservadoras en el modelo y analizándolo en profundidad en el análisis de sensibilidad, de tal modo que se puede observar que el análisis de sensibilidad nos permite ser más robustos en nuestras conclusiones al reafirmar los resultados obtenidos, pero para un abanico de tipologías de mujeres mucho más amplio que el caso base.
También hay que resaltar que el modelo obtiene las probabilidades de efectos adversos obstétricos con levotiroxina de 2 ensayos clínicos aleatorios del sur de Italia, donde la deficiencia de yodo es leve. Así pues, se debe realizar con cautela cualquier extrapolación de los resultados a otras zonas geográficas con diferentes niveles de nutrición de yodo, o donde las pruebas de detección precoz se realicen en edades gestacionales más avanzadas.
ConclusionesEl cribado universal de la HC y HS en las mujeres embarazadas en comparación con el cribado por riesgo es una estrategia más efectiva y menos costosa en España. Asimismo, el cribado universal es altamente coste-efectivo en comparación con la estrategia de no llevar a cabo el cribado. Por tanto, los resultados obtenidos en nuestro estudio apoyan la conveniencia de la realización del cribado universal en la población gestante de nuestro país.
FinanciaciónEste estudio ha sido financiado por Merck S.L.
Conflicto de interesesLos autores declaran la independencia del órgano promotor y financiador en el análisis de resultados y la elaboración de las conclusiones. Los doctores S. Donnay, J. Álvarez y J.A. Balsa no recibieron honorarios por la redacción de este manuscrito. F. Pérez-Alcántara y C. Crespo trabajan en una consultora independiente que recibió financiación por parte de Merck S.L. C. Polanco es empleado de Merck S.L.