El procedimiento de punción-aspiración con aguja fina ecoguiada de nódulos tiroideos con examen citológico in situ del material extraído puede reducir el número de citologías obtenidas de categoría BethesdaI. El objetivo del estudio ha sido evaluar nuestra experiencia del segundo año en dicha técnica para analizar la eficacia diagnóstica, la prevalencia y los factores predictores de los resultados de categoría BethesdaI.
Pacientes y métodoEstudio retrospectivo sobre 279 nódulos en 233 pacientes. La punción-aspiración se realizó según los criterios de 2015 de la American Thyroid Association. Una muestra de cada punción se fijó al aire y se procesó in situ mediante tinción con Diff-Quik y examen microscópico para valorar su idoneidad; en caso contrario, se repitió la punción hasta un total de 5veces. La eficacia diagnóstica se valoró en base a la sensibilidad y a la especificidad sobre las categorías citológicas BethesdaII y BethesdaVI.
ResultadosLa sensibilidad y la especificidad diagnóstica fueron del 100% en ambos casos. Obtuvimos un 5,4% de resultados de categoría BethesdaI y las variables independientemente asociadas fueron la edad (incremento del 4,7% por cada año de vida) y el volumen del nódulo (incremento del 2,3% por cada 1ml de volumen).
ConclusionesLa punción-aspiración ecoguiada con aguja fina y examen citológico in situ del material extraído permite obtener una elevada eficacia diagnóstica y demuestra ser un procedimiento de gran validez por conseguir una tasa muy baja de resultados citológicos de categoría BethesdaI, cuyo riesgo ha sido superior en sujetos de mayor edad y en nódulos de mayor tamaño.
Ultrasound-guided fine needle aspiration of thyroid nodules with on-site cytological examination may decrease the number of Bethesda categoryI cytologies. The study objective was to evaluate our second-year experience with this procedure to analyze diagnostic efficacy, prevalence, and factors predicting for Bethesda categoryI results.
Patients and methodA retrospective study was conducted of 279 nodules from 233 patients. Ultrasound -guided fine needle aspiration was performed according to the 2015 criteria of the American Thyroid Association. A specimen of each aspiration was air-fixed on site before Diff-Quik staining and microscopic examination to assess its suitability; otherwise, nodule aspiration was repeated up to 5times. Diagnostic efficacy was assessed based on sensitivity and specificity on the cytological categories BethesdaII and BethesdaVI.
ResultsDiagnostic sensitivity and specificity were both 100%, 5.4% Bethesda categoryI results were obtained, and variables independently associated were age (4.7% increase per year of life) and nodule volume (2.3% increase per each 1mL of volume).
ConclusionsUltrasound-guided fine needle aspiration of thyroid nodules with on-site cytological examination allows for a high diagnostic efficacy and has been shown to be a highly relevant procedure because it has a very low rate of cytological results of Bethesda categoryI, whose risk has been higher in older subjects and with larger nodules.
El principal objetivo ante un paciente con bocio nodular es reconocer la posible malignidad de dicha patología. Aunque esta probabilidad es baja (5-15%), la alta prevalencia de bocio nodular en la población (5-68% según se detecte por palpación o ecografía) da lugar a un número elevado de pacientes con cáncer de tiroides1,2. Para identificar la benignidad o malignidad de un nódulo tiroideo se dispone de tres abordajes: la valoración endocrinológica, el examen ecográfico y, especialmente relevante, el estudio citológico a partir de la punción-aspiración con aguja fina1-3. Con estos procedimientos se ha conseguido seleccionar los nódulos malignos para su tratamiento quirúrgico y, por otra parte, evitar cirugías innecesarias y sus posibles secuelas en el caso de nódulos benignos4.
En los últimos años se ha adoptado la clasificación de Bethesda para el diagnóstico citológico de los nódulos tiroideos. En ciertas ocasiones se obtiene un resultado de categoría BethesdaI (muestra no apta para diagnóstico citológico). El panel de expertos de Bethesda ha recomendado que los procedimientos empleados para conseguir el diagnóstico citológico de un nódulo tiroideo no ofrezcan más del 10% de resultados de categoría BethesdaI5,6. Este porcentaje guarda una estrecha relación con las características ecográficas e histopatológicas del nódulo, y con la calidad del procedimiento de citología realizado2,5,7-12, por lo cual es recomendable que cada centro recopile, analice y valore los resultados citológicos y anatomopatológicos de los pacientes con bocio nodular. Ante un resultado citológico de categoría BethesdaI se recomienda repetir la citología de forma ecoguiada y, si es posible, con examen citológico in situ del material extraído, o bien realizar una biopsia con aguja gruesa1,2,5,6,13-15. Aunque en la mayoría de centros se ha incorporado la ecografía a dicho procedimiento2, no ha ocurrido lo mismo en cuanto a la valoración citológica in situ del material extraído, aduciendo falta de recursos humanos y un elevado coste en algunas circunstancias10,16-18.
Por otra parte, algunos estudios han focalizado sus objetivos en encontrar signos ecográficos o características citológicas asociados a la posible malignidad de los nódulos con resultados citológicos de categoría BethesdaI11,19. Sin embargo, han sido escasos los estudios que han hallado algún marcador clínico predictor de un resultado citológico de categoría BethesdaI7,20,21.
El objetivo del presente estudio ha sido evaluar los resultados durante el segundo año de nuestra experiencia en la punción-aspiración con aguja fina ecoguiada de nódulos tiroideos con examen citológico in situ del material extraído. Se presentan los resultados citológicos del total de los nódulos y del examen histopatológico en los casos intervenidos quirúrgicamente, con énfasis en el análisis de la eficacia diagnóstica, la prevalencia y los factores predictores de los resultados obtenidos de categoría BethesdaI.
Material y métodosSe trata de un estudio retrospectivo, en un entorno hospitalario, descriptivo de la práctica clínica habitual, que incluye a los pacientes atendidos durante el segundo año (de mayo de 2017 hasta mayo de 2018, ambos incluidos) en la consulta de punción-aspiración de nódulos tiroideos. Se han excluido los pacientes con antecedente de tiroidectomía por cáncer de tiroides y las citologías ganglionares cervicales. Este tiempo se divide en dos períodos consecutivos de 6meses para comprobar si se ha superado el período de aprendizaje. El estudio ha sido revisado y aprobado por el Comité Ético de Investigación Clínica de la Fundació Asistencial Mútua de Terrassa. Se obtuvo el consentimiento informado de todos los pacientes.
Se han incluido 233 pacientes y se han abordado 279 nódulos. La variable principal es el resultado del examen citológico siguiendo la clasificación de Bethesda5,6. Las variables secundarias son: edad, sexo, tipo de bocio (uni o multinodular en la ecografía), ecogenicidad de la porción sólida del nódulo (muy hipoecoico si es más hipoecoico que los músculos pretiroideos, hipoecoico, isoecoico o hiperecoico en relación al parénquima tiroideo adyacente), presencia de microcalcificaciones en el nódulo (no, sí o dudosas), naturaleza del nódulo (sólido, mixto sólido-quístico o predominantemente quístico si dicho componente es superior al 50%), medidas de los diámetros del nódulo en altura, anchura, longitud y sus derivadas (diámetro en altura superior o no al diámetro en anchura, diámetro mayor, diámetro mayor superior a 4cm, diámetro mayor inferior a 1cm, volumen calculado con la fórmula del elipsoide: altura(mm)*anchura(mm)*longitud(mm)*0,525/1.000), patrón de vascularización del nódulo (periférica o central), valores hormonales plasmáticos de tirotropina y tiroxina libre de los pacientes que no recibían tratamiento sustitutivo tiroideo ni antitiroideo, anticuerpos antitiroideos en plasma (positividad para anticuerpos antitiroperoxidasa y/o antitiroglobulina), número de punciones en cada nódulo (número de pases) y resultado histopatológico si el paciente fue intervenido quirúrgicamente. Se consideró hipertiroidismo si el valor de la TSH fue inferior a 0,1mUI/ml e hipotiroidismo si fue superior a 4,5mUI/ml.
La punción-aspiración se llevó a cabo sobre el nódulo tiroideo único, y en los casos de bocio multinodular, sobre el nódulo dominante por su mayor tamaño y/o el/los nódulo/s con caracteres ecográficos de sospecha de malignidad, de acuerdo con los criterios de la American Thyroid Association 20151. El procedimiento de punción-aspiración ecoguiada se ha realizado por un único médico endocrinólogo (L.G.P.). Para el examen ecográfico se utilizó una sonda lineal de 6-11MHz en un ecógrafo Esaote modelo MyLab Seven U185F1 2015. Para la punción se usaron agujas de tamaño 23 o 25G acopladas a una jeringa de 10ml, sin anestesia y sin guía de biopsia. Dos citotécnicos (M.L.S. y X.M.) participaron en el procesamiento de la muestra extraída, que se repartió en pares de laminillas que se deslizaban una sobre la otra para que las extensiones acabaran conteniendo similar material. Una de las laminillas fue fijada al aire y se procesó in situ mediante tinción con Diff-Quik, seguido de examen al microscopio para valorar si se cumplía el criterio de material adecuado para diagnóstico citológico por contener al menos 6grupos de 10células foliculares5. En caso contrario se repitió la punción del nódulo hasta un total de 5veces. El material de la otra laminilla se fijó en alcohol de 96° y se remitió al laboratorio de anatomía patológica para completar el estudio tras la tinción de Papanicolaou. Cuando fue posible se realizaron preparaciones del citobloque procedente de la muestra obtenida.
Cuando se obtuvo un resultado de categoría BethesdaI o BethesdaIII quedó a criterio del paciente y de su médico responsable la decisión de repetir la citología en 2-3meses, el seguimiento clínico y ecográfico o bien la exéresis quirúrgica de la lesión. Los pacientes con bocio multinodular compresivo y todos aquellos en los que se obtuvo una citología sospechosa de neoplasia folicular (BethesdaIV), sospechosa de malignidad (BethesdaV), maligna (BethesdaVI) o benigna (BethesdaII) pero con hallazgos ecográficos altamente sospechosos de malignidad, fueron remitidos a cirugía1.
En el análisis estadístico se han descrito las medias ±desviación estándar de las variables continuas, así como el número de casos (n) y el porcentaje (%) de las variables cualitativas. La eficacia diagnóstica del método se ha evaluado en base al cálculo de la sensibilidad y especificidad de los resultados anatomopatológicos obtenidos en los pacientes con las categorías BethesdaII y BethesdaVI. La relación entre variables cualitativas se ha explorado mediante la prueba de chi cuadrado o el test exacto de Fisher cuando procedió, y las diferencias en las variables cuantitativas respecto a variables cualitativas de dos grupos mediante la prueba t de Student. Para analizar factores predictores de un resultado citológico de categoría BethesdaI se agruparon los casos en una variable dependiente binaria (sí/no) y se aplicó un modelo de regresión logística por pasos. Se consideró estadísticamente significativa una p<0,05.
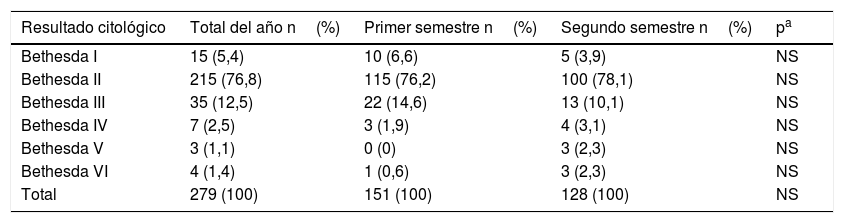
ResultadosEntre los meses de mayo de 2017 y mayo de 2018 se han realizado 279 citologías mediante punción-aspiración con aguja fina con control ecográfico y examen citológico in situ del material extraído de nódulos de tiroides provenientes de 233 pacientes. El resultado y la distribución durante el primero y el segundo semestre del año se muestran en la tabla 1; no se encontraron diferencias estadísticamente significativas en los resultados entre ambos períodos. El porcentaje de resultados de categoría BethesdaI fue del 5,4%. En 112 nódulos (40,1%) se obtuvo una muestra apta para diagnóstico citológico con el primer pase. Únicamente se repitió la citología de 10 nódulos que tuvieron un resultado inicial de categoría BethesdaIII, obteniendo en 7 casos una citología de categoría BethesdaII, y un caso en cada una de las categorías BethesdaIII, BethesdaIV y BethesdaVI.
Resultados de las 279 citologías efectuadas mediante punción-aspiración con aguja fina con control ecográfico y examen citológico in situ del material extraído, desglosados en cada semestre del segundo año de nuestra experiencia
| Resultado citológico | Total del año n(%) | Primer semestre n(%) | Segundo semestre n(%) | pa |
|---|---|---|---|---|
| Bethesda I | 15 (5,4) | 10 (6,6) | 5 (3,9) | NS |
| Bethesda II | 215 (76,8) | 115 (76,2) | 100 (78,1) | NS |
| Bethesda III | 35 (12,5) | 22 (14,6) | 13 (10,1) | NS |
| Bethesda IV | 7 (2,5) | 3 (1,9) | 4 (3,1) | NS |
| Bethesda V | 3 (1,1) | 0 (0) | 3 (2,3) | NS |
| Bethesda VI | 4 (1,4) | 1 (0,6) | 3 (2,3) | NS |
| Total | 279 (100) | 151 (100) | 128 (100) | NS |
NS: no significativo.
Los resultados anatomopatológicos de los pacientes intervenidos, según la citología previa, se muestran en la tabla 2. Al no haber ningún caso de falso negativo ni falso positivo en las categorías BethesdaII y BethesdaVI, la sensibilidad y la especificidad diagnóstica fue del 100% en ambos casos.
Diagnóstico anatomopatológico en los pacientes intervenidos según el resultado citológico previo
| Resultado anatomopatológico | ||||||
|---|---|---|---|---|---|---|
| Resultado citológico | Total, n | Intervenidos, n | Hiperplasia, n | Adenoma, n | NIFTP, n | Carcinomaa, n |
| Bethesda I | 15 | 1 | 1 | − | − | − |
| Bethesda II | 215 | 8 | 8 | − | − | − |
| Bethesda III | 35 | 14 | 7 | 2 | 1 | 4 |
| Bethesda IV | 7 | 7 | 1 | 5 | − | 1 |
| Bethesda V | 3 | 3 | − | − | − | 3 |
| Bethesda VI | 4 | 4 | − | − | − | 4 |
| Total | 279 | 37 | 17 | 7 | 1 | 12 |
NIFTP: neoplasia folicular tiroidea no invasiva con hallazgos nucleares de tipo papilar.
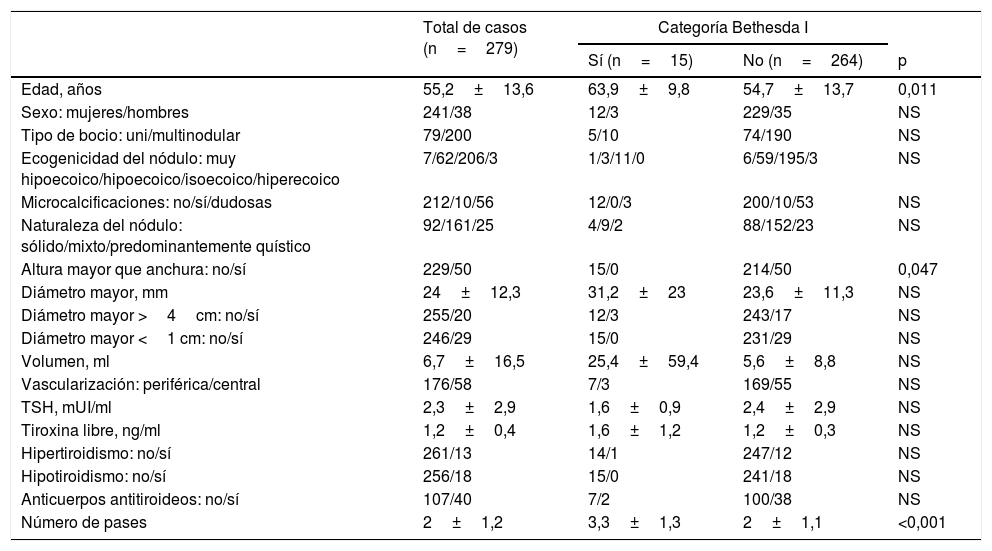
El estudio univariante de las variables predictoras de un resultado citológico de categoría BethesdaI se muestra en la tabla 3. La recopilación retrospectiva ha motivado la ausencia de algunos datos en algunas variables de algunos pacientes: disponemos del resultado de los anticuerpos antitiroideos en el 52,7% de los pacientes, de la tiroxina libre plasmática en el 77,4% y del tipo de vascularización del nódulo en el 83,9%.
Resultados de las variables estudiadas en el total de los pacientes y su comparación entre los pacientes con nódulos con citología de categoría BethesdaI y el resto de categorías citológicas de Bethesda
| Total de casos (n=279) | Categoría Bethesda I | |||
|---|---|---|---|---|
| Sí (n=15) | No (n=264) | p | ||
| Edad, años | 55,2±13,6 | 63,9±9,8 | 54,7±13,7 | 0,011 |
| Sexo: mujeres/hombres | 241/38 | 12/3 | 229/35 | NS |
| Tipo de bocio: uni/multinodular | 79/200 | 5/10 | 74/190 | NS |
| Ecogenicidad del nódulo: muy hipoecoico/hipoecoico/isoecoico/hiperecoico | 7/62/206/3 | 1/3/11/0 | 6/59/195/3 | NS |
| Microcalcificaciones: no/sí/dudosas | 212/10/56 | 12/0/3 | 200/10/53 | NS |
| Naturaleza del nódulo: sólido/mixto/predominantemente quístico | 92/161/25 | 4/9/2 | 88/152/23 | NS |
| Altura mayor que anchura: no/sí | 229/50 | 15/0 | 214/50 | 0,047 |
| Diámetro mayor, mm | 24±12,3 | 31,2±23 | 23,6±11,3 | NS |
| Diámetro mayor >4cm: no/sí | 255/20 | 12/3 | 243/17 | NS |
| Diámetro mayor <1 cm: no/sí | 246/29 | 15/0 | 231/29 | NS |
| Volumen, ml | 6,7±16,5 | 25,4±59,4 | 5,6±8,8 | NS |
| Vascularización: periférica/central | 176/58 | 7/3 | 169/55 | NS |
| TSH, mUI/ml | 2,3±2,9 | 1,6±0,9 | 2,4±2,9 | NS |
| Tiroxina libre, ng/ml | 1,2±0,4 | 1,6±1,2 | 1,2±0,3 | NS |
| Hipertiroidismo: no/sí | 261/13 | 14/1 | 247/12 | NS |
| Hipotiroidismo: no/sí | 256/18 | 15/0 | 241/18 | NS |
| Anticuerpos antitiroideos: no/sí | 107/40 | 7/2 | 100/38 | NS |
| Número de pases | 2±1,2 | 3,3±1,3 | 2±1,1 | <0,001 |
NS: no significativo.
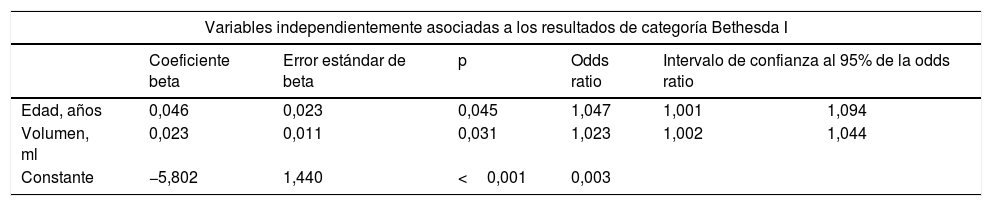
En el estudio multivariante de regresión logística binaria las variables independientemente asociadas a un resultado de categoría BethesdaI fueron la edad y el volumen del nódulo (tabla 4).
Resultados de la regresión logística binaria aplicada a la predicción de resultados citológicos de categoría Bethesda I en nódulos tiroideos
| Variables independientemente asociadas a los resultados de categoría Bethesda I | ||||||
|---|---|---|---|---|---|---|
| Coeficiente beta | Error estándar de beta | p | Odds ratio | Intervalo de confianza al 95% de la odds ratio | ||
| Edad, años | 0,046 | 0,023 | 0,045 | 1,047 | 1,001 | 1,094 |
| Volumen, ml | 0,023 | 0,011 | 0,031 | 1,023 | 1,002 | 1,044 |
| Constante | −5,802 | 1,440 | <0,001 | 0,003 | ||
Durante el segundo año de nuestra experiencia en la punción-aspiración con aguja fina ecoguiada de nódulos tiroideos con valoración citológica in situ del material extraído hemos abordado 279 nódulos, con una sensibilidad y una especificidad diagnósticas del 100%, y un 5,4% de resultados citológicos de categoría BethesdaI, lo cual demuestra una elevada eficacia diagnóstica y una gran validez del procedimiento. La edad (incremento del 4,7% por cada año de vida) y el volumen del nódulo (incremento del 2,3% por cada 1ml de volumen) fueron predictores de los resultados obtenidos de categoría BethesdaI.
Las categorías de diagnóstico citológico BethesdaII y BethesdaVI se consideran definitivas porque son el máximo exponente de las lesiones benignas y malignas, respectivamente; el resto de categorías citológicas de Bethesda representan grados intermedios de malignidad22. Según el consenso de Bethesda, es asumible una tasa de resultados falsos negativos de entre el 0 y el 3% en la categoría BethesdaII (lesión benigna) y de falsos positivos de entre el 1 y el 3% en la categoría BethesdaVI (lesión maligna)5,6. En nuestra serie, el método de diagnóstico citológico mediante punción-aspiración con aguja fina ecoguiada y examen citológico in situ del material extraído nos ha ofrecido muy buenos resultados en cuanto a sensibilidad y especificidad diagnósticas valoradas en las categorías definitivas de Bethesda, al constatar que entre los pacientes intervenidos no hubo ningún caso de falso negativo (todos los que tenían un resultado citológico de categoría BethesdaII fueron nódulos benignos en el examen anatomopatológico) ni tampoco ningún resultado falso positivo (todos los que tenían un resultado citológico de categoría BethesdaVI fueron nódulos malignos en el examen anatomopatológico). No obstante, estos resultados deberán contrastarse en el futuro con una mayor casuística de pacientes intervenidos.
Las cifras reportadas de casos de nódulos tiroideos con un diagnóstico citológico de categoría BethesdaI oscilan entre el 0,6 y el 47%, si bien en la mayoría de las series este porcentaje se encuentra entre el 8 y el 20%1,2,11, y en las series de nuestro entorno entre el 2,3 y el 27,2%23-27. En nuestro centro, la tasa de resultados BethesdaI previa a la técnica ecoguiada con valoración in situ del material extraído fue del 19,8%28. Las consecuencias de obtener un resultado citológico de categoría BethesdaI incluyen repetir la citología, ansiedad para el paciente y, en ocasiones, llevar a cabo intervenciones quirúrgicas innecesarias14,17,26.
La obtención de material adecuado para diagnóstico citológico en la punción-aspiración de los nódulos tiroideos está relacionada con la experiencia previa en dicho procedimiento, con la técnica utilizada y con las características del nódulo que se punciona1,8,14-17,19,23. En los últimos años se ha ido implementando la técnica de punción ecoguiada por sus mejores resultados, y debido a la mayor disponibilidad de ecógrafos, ha sido incorporada a las consultas de los servicios clínicos de endocrinología y cirugía de cabeza y cuello, agilizando de este modo el diagnóstico10,13. Paralelamente se ha considerado necesario obtener medidas de calidad para asegurar que el procedimiento se realiza adecuadamente. Algunos estudios han considerado como medida de calidad el análisis de la curva de aprendizaje de dicha técnica a partir del número de resultados de muestras inadecuadas (categoría BethesdaI) obtenidas en el tiempo10,12. Para los autores más exigentes, el aprendizaje se consigue cuando se llega a obtener un 90-95% de muestras adecuadas10, mientras que otros consideran que idealmente las unidades experimentadas (las que practican más de 100 punciones/año) deben tener una cifra inferior al 10-15% de resultados de categoría BethesdaI2,5,6,9,11. En nuestra serie, el 5,4% obtenido en el segundo año de su implementación es un resultado que avala una adecuada calidad del procedimiento de citología mediante punción-aspiración con aguja fina ecoguiada y valoración citológica in situ del material extraído, y el hecho de no encontrar diferencias significativas entre el primero y el segundo semestre nos indica que se ha conseguido la estabilidad en la curva de aprendizaje.
La American Thyroid Association1 recomienda, después obtener un diagnóstico citológico de categoría BethesdaI, repetir la citología con control ecográfico y, si es posible, con examen citológico in situ del material extraído, por su mejor rendimiento diagnóstico13,14. La valoración citológica in situ del material extraído en la punción de nódulos tiroideos por un citotécnico o un patólogo para confirmar una muestra de calidad no siempre es posible, por lo que en muchos centros no se lleva a cabo16,17; por otra parte, ha sido controvertida su relación coste-efectividad17,18. Cuando no se efectúa la valoración citológica in situ, no hay un criterio claro para definir el número de pases que hay que efectuar sobre el nódulo para conseguir una muestra adecuada. Algunos estudios han focalizado su objetivo en buscar alternativas para obtener resultados comparables al método de valoración citológica in situ del material extraído. En uno de ellos, realizar 4pases en cada nódulo redujo el número de resultados de categoría BethesdaI al 11%16, y en otro estudio, con 3pases en cada nódulo se consiguió un 13,7% de resultados de categoría BethesdaI17. Ambas situaciones pueden ser excesivas para muchos pacientes, pues en nuestra serie el número promedio de pases resultó ser de2 con un 5,4% de resultados de categoría BethesdaI, dato similar al de la serie de Castells et al.26 (5,3%) con una metodología similar. Por otra parte, el no conocer inmediatamente después de la punción si el material es adecuado no favorece que el operador valore el rendimiento de variantes técnicas como el calibre de la aguja, la técnica de aspiración, etc., ni que pueda reconocer la utilidad de los cambios efectuados en el siguiente pase después de uno infructuoso. Además, la valoración in situ del material permite una aproximación diagnóstica en tiempo real.
Respecto a los posibles factores predictores de un diagnóstico citológico de categoría BethesdaI, los más citados se refieren a las características del nódulo. Es bien conocido que aquellos nódulos con un tamaño pequeño (menor de 10mm), un gran componente quístico, necrótico, fibroso o una gran vascularización hacen que sea más frecuente el resultado de muestra no adecuada para diagnóstico citológico7-9,19,23,29. Sin embargo, pocos han sido los estudios dirigidos a encontrar factores clínicos, distintos de los puramente ecográficos o intrínsecos a la técnica de punción-aspiración, que puedan ser predictores de resultados citológicos de categoría BethesdaI en los nódulos tiroideos. Moon et al.20 y Alexander et al.7 no encontraron variables clínicas predictoras. Baier et al.21 comunicaron que la edad superior a 75años duplicaba significativamente el riesgo de obtener un resultado de categoría BethesdaI y lo interpretaron en relación con la rigidez cervical que dificultaba la posición de trabajo. En nuestra serie, el tamaño pequeño del nódulo, el componente quístico o el patrón de vascularización no han sido factores predictores de un resultado de categoría BethesdaI, probablemente porque la técnica ecoguiada con valoración citológica in situ del material extraído ha podido obviar las dificultades que entrañan estos condicionantes. Sin embargo, la mayor edad del paciente y el mayor volumen del nódulo han estado independientemente asociados a este resultado. Puesto que la prevalencia de bocio aumenta con la edad30 y el paso de los años se acompaña de un incremento gradual en el tamaño de los nódulos31, nuestra interpretación es que la mayor edad del paciente y también el mayor volumen del nódulo representan una mayor antigüedad de la lesión, y este hecho ha favorecido el desarrollo de fenómenos hemorrágicos y necróticos que finalmente han conducido a la fibrosis del nódulo, lo cual es un factor reconocido para la obtención de muestras inadecuadas para el diagnóstico citológico8.
El estudio tiene algunas limitaciones. El carácter retrospectivo ha motivado la ausencia de algunos datos en algunas variables de algunos pacientes, lo cual puede haber reducido la capacidad de encontrar diferencias estadísticamente significativas. No se recogieron las características de los tratamientos tiroideos, ni los antecedentes de radioterapia cervical. Tampoco se evaluó la variabilidad interobservador en los hallazgos ecográficos ni en el diagnóstico citológico. El número de pacientes intervenidos fue escaso por tratarse de un período temporal de un año.
En conclusión, la punción-aspiración con aguja fina ecoguiada de nódulos de tiroides con valoración citológica in situ del material extraído es un procedimiento que permite obtener una elevada eficacia diagnóstica y demuestra una gran calidad al conseguir una tasa muy baja de resultados obtenidos de categoría BethesdaI, por lo cual se convierte en una alternativa a otras técnicas cuando sus resultados no son satisfactorios. El inconveniente a superar consiste en la obtención de muestras adecuadas para diagnóstico citológico en los sujetos de mayor edad y en los nódulos de mayor volumen.
FinanciaciónLa presente investigación no ha recibido ayudas específicas provenientes de agencias del sector público, sector comercial o entidades sin ánimo de lucro.
AutoríaCada autor ha contribuido materialmente en la investigación y en la preparación del artículo. En concreto: concepción y diseño del estudio, adquisición y análisis de datos, interpretación de resultados, escritura del borrador y aprobación de la versión final.
Conflicto de interesesNinguno.